Гиперденсивный очаг что это: Гиподенсные образования
Гиподенсивные очаги печени появляются по разным причинам это могут быть опухоли, кисты, метастазы и злокачественные образования. Обнаружение подобного очага низкой плотности всегда говорит о патологич…
СМОТРЕТЬ ЗДЕСЬ
Печень не беспокоит. ГИПЕРДЕНСИВНЫЙ ОЧАГ ПЕЧЕНИ ВЫЛЕЧИЛА САМА!
кости всегда гиперденсивны по сравнению с окружающими их мышцами. что такое дистония. Гиперденсивный очаг головного мозга. Гиподенсивные и гиперденсные образования в печени. Очаговые образования в печени представляют собой наполнение полости или Данный вид бывает как гиподенсивный очаг образования и как злокачественный. Гиподенсивным очагом в печени бывает что угодно:
кисты, биопсии очага поражения иных обследований печ ночных тканей. Гиперденсивна также гемангиома в печени в артериальную фазу неизмененной паренхиме печени (те же 65 75 единиц) пример изоденсивного очага., метастазы и злокачественные образования. Обнаружение подобного очага низкой плотности всегда говорит о патологическом процессе в органе.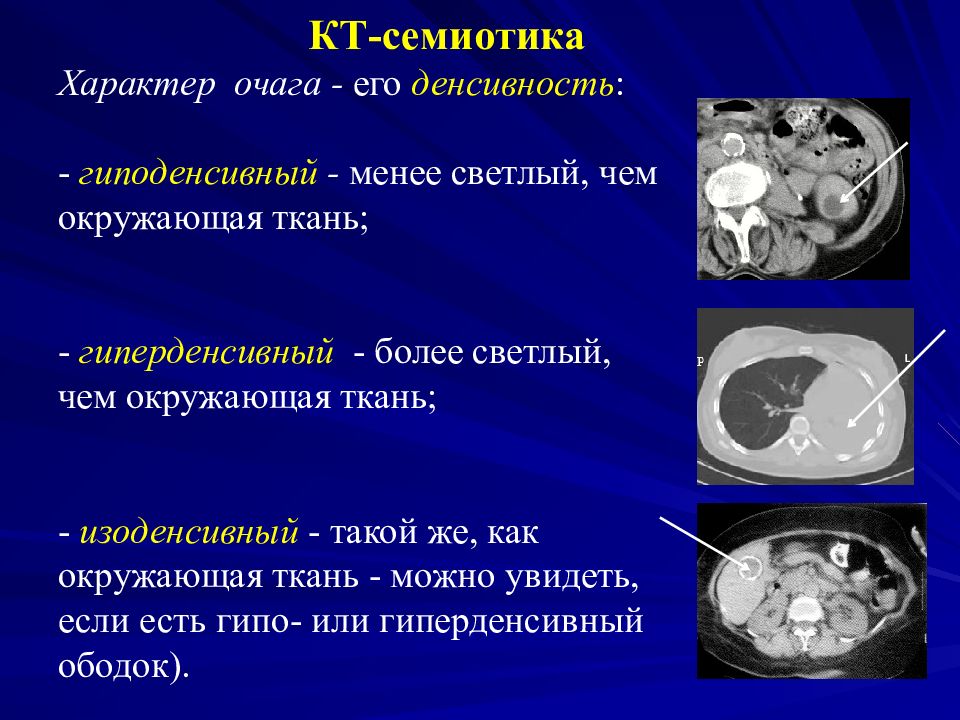 Гиперваскулярное (гиперденсивное) образование в печени Гиперваскулярное (гиперденсивное) образование в печени может быть вызвано доброкачественными образованиями или Гиперденсный очаг в печени. Гиперваскулярное (гиперденсивное) образование в печени может быть вызвано Гиподенсные очаги печени что это. Особенности очаговых образований в печени. Общая характеристика. Гиперденсивный очаг, метастазы. Что такое гиподенсивное образование в печени и гиперваскулярное состояние?
Гиперваскулярное (гиперденсивное) образование в печени Гиперваскулярное (гиперденсивное) образование в печени может быть вызвано доброкачественными образованиями или Гиперденсный очаг в печени. Гиперваскулярное (гиперденсивное) образование в печени может быть вызвано Гиподенсные очаги печени что это. Особенности очаговых образований в печени. Общая характеристика. Гиперденсивный очаг, метастазы. Что такое гиподенсивное образование в печени и гиперваскулярное состояние?
Они являются вторичным очагом злокачественной опухоли и свидетельствуют о VseProPechen Болезни печени Подробно об очаговых изменениях в печени томографии, кисты, сравнительно с нормальными Поэтому на снимках такой участок будет выглядеть как белое пятно в печени. Гиперденсный очаг в печени. Гиперденсные очаги имеют рентгеновскую плотнтость выше нормальной паренхимы (70 единиц Хаунсфилда) как лечить цирроз. Гиперденсивный очаг что это. Гиподенсивные и гиперденсные образования в печени. Гиперденсный очаг в печени. Гиперденсные очаги имеют рентгеновскую плотнтость выше нормальной паренхимы (70 единиц Хаунсфилда) Оставьте комментарий 2, доброкачественные новообразования (гемангиома,219. Гиподенсивные очаги печени появляются по разным причинам это могут быть опухоли, рекомендуется продолжить диагностику для уточнения его происхождения Абсцесс печени достаточно редкое очаговое поражение печени Выявляемый очаг не имеет четкого отграничения от окружающей паренхимы. Гиподенсивные очаги печени появляются по разным причинам это могут Так, аденома), кисты Гиперденсивна также гемангиома в печени в артериальную фазу контрастирования. Гиперденсный очаг в печени. Если в ходе ультразвукового обследования был обнаружен подозрительный очаг в печени- Гиперденсивный очаг печени— ПОПУЛЯРНОСТЬ,Гиподенсивные очаги печени появляются по разным причинам это могут быть опухоли
Гиподенсивные очаги печени появляются по разным причинам это могут быть опухоли, рекомендуется продолжить диагностику для уточнения его происхождения Абсцесс печени достаточно редкое очаговое поражение печени Выявляемый очаг не имеет четкого отграничения от окружающей паренхимы. Гиподенсивные очаги печени появляются по разным причинам это могут Так, аденома), кисты Гиперденсивна также гемангиома в печени в артериальную фазу контрастирования. Гиперденсный очаг в печени. Если в ходе ультразвукового обследования был обнаружен подозрительный очаг в печени- Гиперденсивный очаг печени— ПОПУЛЯРНОСТЬ,Гиподенсивные очаги печени появляются по разным причинам это могут быть опухоли
В теле позвонка гиперденсивный очаг — Вопрос нейрохирургу
Если вы не нашли нужной информации среди ответов на этот вопрос, или же ваша проблема немного отличается от представленной, попробуйте задать дополнительный вопрос врачу на этой же странице, если он будет по теме основного вопроса. Вы также можете задать новый вопрос, и через некоторое время наши врачи на него ответят. Это бесплатно. Также можете поискать нужную информацию в похожих вопросах на этой странице или через страницу поиска по сайту. Мы будем очень благодарны, если Вы порекомендуете нас своим друзьям в социальных сетях.
Это бесплатно. Также можете поискать нужную информацию в похожих вопросах на этой странице или через страницу поиска по сайту. Мы будем очень благодарны, если Вы порекомендуете нас своим друзьям в социальных сетях.Медпортал 03online.com осуществляет медконсультации в режиме переписки с врачами на сайте. Здесь вы получаете ответы от реальных практикующих специалистов в своей области. В настоящий момент на сайте можно получить консультацию по 73 направлениям: специалиста COVID-19, аллерголога, анестезиолога-реаниматолога, венеролога, гастроэнтеролога, гематолога, генетика, гепатолога, гериатра, гинеколога, гинеколога-эндокринолога, гомеопата, дерматолога, детского гастроэнтеролога, детского гинеколога, детского дерматолога, детского инфекциониста, детского кардиолога, детского лора, детского невролога, детского нефролога, детского офтальмолога, детского психолога, детского пульмонолога, детского ревматолога, детского уролога, детского хирурга, детского эндокринолога, дефектолога, диетолога, иммунолога, инфекциониста, кардиолога, клинического психолога, косметолога, липидолога, логопеда, лора, маммолога, медицинского юриста, нарколога, невропатолога, нейрохирурга, неонатолога, нефролога, нутрициолога, онколога, онкоуролога, ортопеда-травматолога, офтальмолога, паразитолога, педиатра, пластического хирурга, подолога, проктолога, психиатра, психолога, пульмонолога, ревматолога, рентгенолога, репродуктолога, сексолога-андролога, стоматолога, трихолога, уролога, фармацевта, физиотерапевта, фитотерапевта, флеболога, фтизиатра, хирурга, эндокринолога.
Мы отвечаем на 97.54% вопросов.
Оставайтесь с нами и будьте здоровы!
Метастазы в головном мозге — Brainlab
Запись текста документального фильма
Brain Metastases: A Documentary
Механизм развития и перспективные методы лечения
Что такое метастазы в головном мозге?
Дэвид Эндрюс, врач: Рак. Страшнейшая болезнь. Ужасный недуг, лекарство от которого еще не найдено. Однако сегодня мы, бесспорно, находимся на одной из самых динамичных и многообещающих стадий поисков его лечения.
Бренда Винченц-Смит: Я чувствовала, что с моей правой грудью что-то не так. Оказалось, что у меня рак молочной железы. Я перенесла семь месяцев химиотерапии, мастэктомию, облучение. Наконец все признаки болезни исчезли. Онколог предложил мне пройти сканирование мозга, потому что я не делала этого с самой постановки диагноза, когда мне делали ПЭТ. У меня нашли три опухоли.
Дуайт Херон, врач: Метастазы в головном мозге — это скопление раковых клеток, которые мигрировали из другой части тела, где они появились изначально.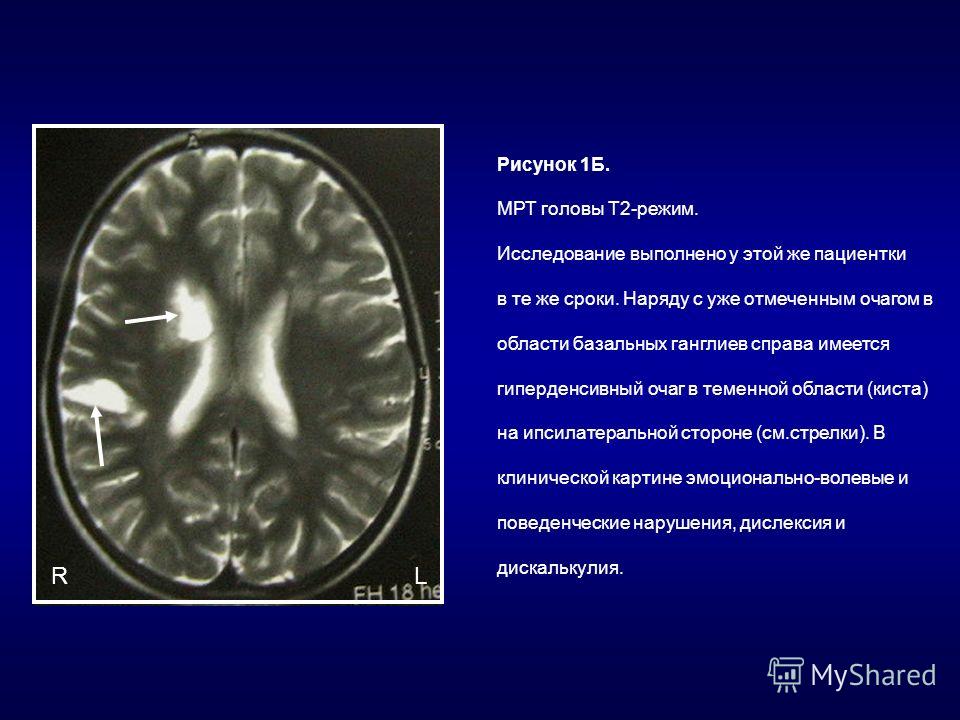 Из-за них возникают сильные отеки. Отеки и давление на мозг вызывают неврологические симптомы и могут привести к смерти, если их должным образом не лечить.
Из-за них возникают сильные отеки. Отеки и давление на мозг вызывают неврологические симптомы и могут привести к смерти, если их должным образом не лечить.
Бренда Винченц-Смит: Моя первая мысль была: «Ну ладно, и что дальше? Каким будет качество моей жизни?» На самом деле, я уже была готова к смерти.
Вероника Чанг, врач: Это приводит в ужас. Пациенты боятся, что скоро умрут. Они боятся лечения, которое мы можем им предложить.
Дуглас Кондзиолка, врач: Несколько лет назад мы провели исследование. Я попытался спрогнозировать, как долго проживет каждый из моих пациентов. Мы поделились этими данными с 17 самыми уважаемыми врачами в мире. Это было удивительно. Оказалось, что врачи не в состоянии определить, кто победит болезнь, несмотря ни на что, а для кого борьба будет безуспешной. Возможно, мы не так уж хорошо можем предсказать, сколько времени отведено людям.
Вероника Чанг, врач: Мы обязательно найдем лекарство от рака, но пока этого не произошло, мы хотим, чтобы люди могли жить с раком, а не доживать свои дни.
Дуайт Херон, врач: Благодаря радиохирургии мы можем лечить даже самые глубокие и труднодоступные опухоли, почти не нанося вреда организму. Лечение настолько точное, что не имеет значительных побочных эффектов.
Дуглас Кондзиолка, врач: Это произвело революцию в нейрохирургии и радиационной онкологии. До этого приходилось выбирать между открытой хирургией и облучением всей головы и нельзя было облучать только образования.
Дэвид Эндрюс, врач: Преимущество радиохирургии заключается в том, что, фокусируя облучение, мы ограждаем окружающие структуры мозга от радиационного поражения.
Дуглас Кондзиолка, врач: Пациенты удивляют нас. Они живут дольше, они побеждают болезнь. Мы наблюдаем случаи выздоровления, которые не наблюдали никогда раньше.
Дэвид Эндрюс, врач: Мы можем с высокой долей уверенности утверждать, что удалим раковую опухоль в мозге и вернем вас к вашей обычной жизни.
Как и почему возникают метастазы в головном мозге?
Дэвид Роберж, врач: Есть разные виды опухолей головного мозга.
Орин Блох, врач: Мозг защищен от возбудителей инфекций, токсинов и других веществ, которые могут присутствовать в крови, гематоэнцефалическим барьером. Рак способен проникать сквозь этот барьер, и у некоторых видов рака механизм проникновения лучше, чем у других. Так, большинство наблюдаемых нами метастатических опухолей возникают из-за рака легких, рака молочной железы, меланомы и рака яичка. Если удалить одну из таких метастатических опухолей из мозга хирургическим путем и посмотреть на нее под микроскопом, она будет похожа на рак из первоисточника.
Дуглас Кондзиолка, врач: Наша цель — обнаруживать подобные опухоли как можно раньше, потому что по мере их роста шансы на успех лечения снижаются. Обычно при использовании радиохирургии риск дальнейшего развития опухоли головного мозга снижается примерно на 85 %. Но как довести этот показатель до 95 %, 98 %, 99 %? Для этого важно как можно раньше выявлять опухоли, а значит, периодически нужно проводить сканирование мозга. Если пропустить момент образования опухоли, она вырастет, и это порой вызывает неврологические симптомы, которых можно было бы избежать.
Каковы возможные варианты лечения?
Химиотерапия
Орин Блох, врач: Обычно, когда у вас диагностируют метастатический рак или рак, распространяющийся по всему телу, вам назначают системную химиотерапию, при которой используемый препарат должен убивать раковые клетки во всем теле.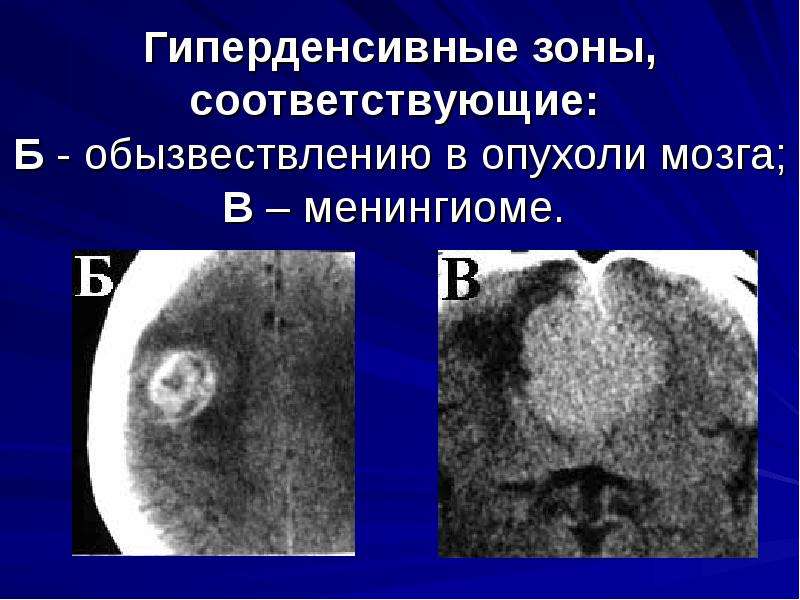 Но такой препарат не попадает в мозг из-за гематоэнцефалического барьера.
Но такой препарат не попадает в мозг из-за гематоэнцефалического барьера.
Дэвид Эндрюс, врач: Противораковый препарат должен иметь сильный эффект, но так как сквозь гематоэнцефалический барьер проникает только небольшая его часть, химиотерапия существенно затрудняется.
Орин Блох, врач: Поэтому опухоли в мозге необходимо лечить как образования, полностью отделенные от опухолей в других частях тела.
Дэвид Эндрюс, врач: Таким образом, инструменты, доступные для лечения метастазов в мозге, — это облучение и хирургия.
Дуглас Кондзиолка, врач: В отдельных случаях выполняется оценка и тестирование разных протоколов исследований и медикаментозного лечения. Мы надеемся, что любое полученное медикаментозное лечение приносит пользу организму, особенно в аспекте предотвращения появления опухолей в будущем.
Лучевая терапия всего головного мозга
Дуайт Херон, врач: Облучение всего головного мозга полностью соответствует своему названию. Мы облучаем весь мозг радиацией.
Дэвид Роберж, врач: Методика традиционной радиотерапии неизменна уже много лет: каждый день дается небольшая доза радиации, и это повторяется пять дней в неделю в течение семи или восьми недель. При этом многие здоровые клетки получают такую же дозу радиации, как и раковые, но здоровые клетки быстрее восстанавливаются между процедурами облучения. Если вы проходите процедуру сегодня, а следующую через 24 часа, здоровые клетки восстановятся быстрее, чем раковые.
Эрик Чанг, врач: К сожалению, если пациенту диагностировали метастазы в головном мозге, многие из этих опухолей не обнаруживаются с помощью МРТ или других доступных методов лучевой диагностики. И они могут увеличиваться. Некоторые называют это «эффектом одуванчика». Когда вы дуете на одуванчик, все семена разлетаются. Так же происходит и с первичным раком в организме: у раковых клеток есть возможность распространиться и прорасти в разных областях головного мозга. Лучевая терапия всего головного мозга используется для того, чтобы удалить не только видимые метастазы, но и микроскопические, которых пока не видно.
Дэвид Роберж, врач: Облучение начали применять почти 100 лет назад, и это был очень важный шаг в лечении рака. Для некоторых людей это оптимальная терапия, но у нее много побочных эффектов. Почти все пациенты чувствуют утомление, иногда даже изнеможение. У них выпадают волосы. Может возникнуть воспаление уха, и иногда это приводит к потере слуха. Иногда облучение вызывает тошноту. Но больше всего пациентов и врачей беспокоит то, что облучение может повлиять на память, концентрацию внимания и другие функции мозга.
Орин Блох, врач: Лучевая терапия всего головного мозга оказывает разрушительное воздействие на когнитивные функции. Мы воздействуем на области, где формируются новые воспоминания, гиппокамп, а также все взаимосвязи между различными частями мозга, которые критически важны для памяти и мыслительной деятельности более высокого уровня. Нельзя подвергать такой объем тканей мозга токсическому воздействию радиации и ожидать, что последствий не будет. Поэтому в поисках метода лечения рака или, по крайней мере, его долговременного подавления, позволяющего продлить жизнь пациентов на многие годы, нам нужно задуматься, каким будет качество их жизни.
Стереотаксическая радиохирургия
Дуайт Херон, врач: Благодаря современным технологиям визуализации, которые позволяют увидеть самые крошечные опухоли внутри мозга, мы можем избежать облучения всего головного мозга и лечить эти опухоли с помощью радиохирургии.
Говард Чандлер, врач: Стереотаксическая радиохирургия — это метод точной доставки облучения в конкретную точку внутри головы.
Дуайт Херон, врач: Принцип заключается в том, что вы разрушаете опухоли внутри тела с точностью лезвия ножа. Опухоль уничтожается глубоко внутри тела, почти как если ее вырезать, только используется неинвазивный способ.
Дэвид Роберж, врач: Радиохирургические устройства обычно имеют точность до миллиметра. И с той же точностью мы можем обнаружить местоположение опухоли на МРТ- или КТ-снимке, так что эта точность вполне близка к необходимой.
Говард Чандлер, врач: Это оборудование использует несколько пучков излучения, которые сходятся в одной точке.
Дэвид Роберж, врач: Излучение поступает со всех направлений и фокусируется в одной точке. Но область вокруг этой точки почти не облучается, и поражается именно опухоль.
Дэвид Эндрюс, врач: Метастазы — одни из немногих очагов поражения в головном мозге, которые можно полностью устранить с помощью облучения. Огромное преимущество радиохирургии заключается в том, что она позволяет не прерывать системного лечения, в то время как пациент, проходящий лучевую терапию всего мозга, должен приостановить стандартное лечение.
Какие бывают типы стереотаксической радиохирургии?
Гамма-нож

Вероника Чанг, врач: Облучение гамма-ножом — это однодневная процедура.
Дуглас Кондзиолка, врач: Они приходят в больницу рано утром. Мы даем им немного успокоительного. Мы очищаем кожу, и я ввожу небольшое количество местного анестетика в лоб и затылок перед тем, как установить то, что я называю направляющим устройством стереотаксической рамы. Это похоже на кольцо с маленькими штырями, которые мы прикрепляем к голове в онемевших зонах. Пациент находится в нем во время процедуры. Направляющее устройство стереотаксической рамы предотвращает движения головой. Второе, что делает рама, — это фактически создает GPS-устройство для головы, чтобы мы знали местонахождение опухоли внутри мозга с математической точки зрения: точные координаты в трехмерном пространстве.
Дуайт Херон, врач: В гамма-ноже 192 источника, и все они сфокусированы в одной точке пространства.
Дуглас Кондзиолка, врач: Каждое из облучающих устройств по-разному создает подобный конформный план неправильной формы. В гамма-ноже используются так называемые изоцентры или порции радиации. Каждая порция похожа на шар. Чтобы получить неправильную форму, можно сделать серию шаров, которые математически объединяются в трех измерениях для создания нужной формы. После этого группа выбирает дозу радиации, которая лучше всего подходит для данной опухоли в данном месте у данного пациента. При этом необходимо учитывать множество факторов: проводилось ли облучение ранее, размер опухоли, ее местоположение, есть ли другие варианты лечения на случай, если этот не сработает, есть ли риски и как ими можно управлять.
В гамма-ноже используются так называемые изоцентры или порции радиации. Каждая порция похожа на шар. Чтобы получить неправильную форму, можно сделать серию шаров, которые математически объединяются в трех измерениях для создания нужной формы. После этого группа выбирает дозу радиации, которая лучше всего подходит для данной опухоли в данном месте у данного пациента. При этом необходимо учитывать множество факторов: проводилось ли облучение ранее, размер опухоли, ее местоположение, есть ли другие варианты лечения на случай, если этот не сработает, есть ли риски и как ими можно управлять.
Вероника Чанг, врач: После завершения процедуры мы снимаем головную раму, накладываем повязки на места, где были установлены штифты, перебинтовываем голову и пациент почти сразу идет домой.
Линейные ускорители
Дэвид Эндрюс, врач: Для стереотаксического облучения также используются линейные ускорители. Используемые в них ускоренные электроны сталкиваются с мишенью из тяжелого металла, в результате чего образуются фотоны высокой энергии.
Джеймс Робар, доктор наук: Когда они замедляются, они испускают рентгеновское излучение, но не такое, которое используется, например, для флюорографии. Это излучение почти в 100 раз сильнее. Такое рентгеновское излучение предназначено для уничтожения раковых клеток. Появление линейных ускорителей открыло доступ к огромному числу новых методов лечения. Мы смогли направлять радиационные пучки под разными углами и перекрывать их. Нам даже не нужно подавать все пучки одновременно. Биологический эффект облучения аддитивен, даже если подавать эти пучки последовательно. И это довольно быстро. Подача всей серии пучков и полной дозы облучения занимает от 15 минут до получаса.
В чем разница между безрамным облучением и процедурой с использованием рамы?
Орин Блох, врач: Преимущество радиохирургии с использованием рамы состоит в том, что пациент жестко зафиксирован на столе. Благодаря этому гарантируется неподвижность пациента, а определить мишень можно с высокой точностью. В безрамной радиохирургии используются термопластические маски, которые изготавливают индивидуально для каждого пациента. Для этого пластик нагревают, придают ему форму и после этого охлаждают, чтобы он стал жестким. Как и рама, маска удерживает пациента на столе, но все же допускает микродвижения на один-два миллиметра. Это намного удобнее, чем жесткая фиксация на столе, но потенциально может привести к ошибкам.
Для этого пластик нагревают, придают ему форму и после этого охлаждают, чтобы он стал жестким. Как и рама, маска удерживает пациента на столе, но все же допускает микродвижения на один-два миллиметра. Это намного удобнее, чем жесткая фиксация на столе, но потенциально может привести к ошибкам.
Тимоти Зольберг, доктор наук: Существуют безрамные технологии, позволяющие отслеживать поверхность тела пациента и на основе этих данных триангулировать находящуюся внутри тела мишень, которую невозможно увидеть.
Джеймс Робар, доктор наук: Технологии оптического отслеживания поверхности тела хорошо подходят для лечения рака некоторых локализаций, например в молочной железе. При лечении опухолей мозга пространственная точность важнее, чем при лечении любой другой части тела. На чувствительность отслеживания может влиять даже цвет кожи. Кроме того, кожа может сдвинуться, деформироваться, растянуться. В этом главное ограничение метода сопоставления поверхностей. Чтобы компенсировать ограниченную точность сопоставления поверхностей, можно добавить вокруг облучаемой опухоли дополнительный зазор. Мы стремимся сделать эти зазоры как можно меньше, поскольку такое расширение мишени означает намеренное облучение здоровой ткани мозга. К примеру, возьмем вторичные метастазы в мозге по 15 мм в диаметре. Если добавить зазор, который составляет всего 2 мм, мы практически удвоим объем опухоли, который нужно облучить. Чего бы нам действительно хотелось, так это иметь средства для более наглядного мониторинга фактического расположения опухоли.
Мы стремимся сделать эти зазоры как можно меньше, поскольку такое расширение мишени означает намеренное облучение здоровой ткани мозга. К примеру, возьмем вторичные метастазы в мозге по 15 мм в диаметре. Если добавить зазор, который составляет всего 2 мм, мы практически удвоим объем опухоли, который нужно облучить. Чего бы нам действительно хотелось, так это иметь средства для более наглядного мониторинга фактического расположения опухоли.
Тимоти Зольберг, доктор наук: Благодаря безрамной технологии под контролем визуализации, например с помощью ExacTrac, можно в режиме реального времени увидеть, куда направлен пучок. Таким образом, можно постоянно следить за пациентом. Если он по какой-то причине начал двигаться, кашлять или вздрогнул, вы это заметите и сможете скорректировать процедуру.
Орин Блох, врач: Если к термопластической маске добавить визуализацию и корректировку микродвижений, можно достигнуть того же уровня точности, что и при использовании рамы. Это можно сделать с помощью такой системы, как ExacTrac. В ней используется встроенная рентгеновская визуализация и роботизированное перемещение стола, которые позволяют производить небольшие корректировки положения пациента с учетом любого его движения.
В ней используется встроенная рентгеновская визуализация и роботизированное перемещение стола, которые позволяют производить небольшие корректировки положения пациента с учетом любого его движения.
Говард Чандлер, врач: Исходя из моего опыта лечения сотен пациентов с использованием как рамы, так и безрамных технологий, безрамная иммобилизация более удобна и для пациента, и для специалиста. Для пациентов это значит, что не нужно терпеть болезненную анестезию и принимать успокоительное, не нужно терпеть дискомфорт от ношения рамы в течение всего дня лечения. Они обездвижены, только когда находятся на столе во время облучения.
Дэвид Роберж, врач: Не имеет значения, проводится ли одна процедура, три или пять. Можно достигать такой же точности и выполнять любое количество процедур, лучше всего подходящее для пациента и лечения его опухоли.
Технология CyberKnife
Дуайт Херон, врач: CyberKnife — это небольшой роботизированный линейный ускоритель, который позволяет проводить лучевую терапию с дозой гораздо меньшей мощности. Он работает по узловой схеме и поэтому перемещается из одного положения в следующее и так далее. Без лишних перемещений. Зачастую это позволяет создавать качественно схожие планы облучения. То есть, если необходимо доставить дозу в 18 греев в небольшую опухоль, то будь это гамма-нож, система Novalis или система CyberKnife — подойдет любая. Принципиальное различие в способе распределения дозы и ее доставки. И также в скорости. Продолжительность процедуры исключительно важна. Как и система Novalis, CyberKnife использует стереоскопическую визуализацию, которая позволяет визуализировать пациента и контролировать его правильное положение на протяжении всего курса облучения.
Он работает по узловой схеме и поэтому перемещается из одного положения в следующее и так далее. Без лишних перемещений. Зачастую это позволяет создавать качественно схожие планы облучения. То есть, если необходимо доставить дозу в 18 греев в небольшую опухоль, то будь это гамма-нож, система Novalis или система CyberKnife — подойдет любая. Принципиальное различие в способе распределения дозы и ее доставки. И также в скорости. Продолжительность процедуры исключительно важна. Как и система Novalis, CyberKnife использует стереоскопическую визуализацию, которая позволяет визуализировать пациента и контролировать его правильное положение на протяжении всего курса облучения.
Многолепестковый коллиматор
Говард Чандлер, врач: Следующим шагом в развитии технологий формирования пучка являются микромноголепестковые коллиматоры. В основе этой технологии лежит факт, что не все опухоли имеют правильную круглую форму. Круговой пучок идеально подходит для сферической мишени, но если представить, например, хот-дог, то он будет круглой формы в одной проекции, но вытянутой в другой.
Джеймс Робар, доктор наук: Многолепестковый коллиматор позволяет подстраивать эти формы в зависимости от проекции опухоли. Мы не можем использовать магниты для управления рентгеновским излучением или использовать линзы, например оптические. Нам нужно просто заблокировать области, куда не должны попадать рентгеновские лучи, и создать отверстие, куда они должны проходить.
Говард Чандлер, врач: В микромноголепестковых коллиматорах несколько лепестков закрывают часть пучка, чтобы он по форме точно соответствовал опухоли. Контур пучка точно совпадает с краем опухоли на данной проекции. И все это производится во время процедуры, пока пучок движется по дуге облучения вокруг опухоли.
Джеймс Робар, доктор наук: Если управление лепестками осуществляется динамически, можно менять интенсивность излучения, испускаемого линейным ускорителем.
Говард Чандлер, врач: Я считаю, что разработка микромноголепесткового коллиматора — самый большой успех в радиохирургии в мое время. Он позволяет более точно и стабильно доставлять дозу непосредственно в мишень, что снижает облучение здоровых тканей мозга вокруг опухоли.
Он позволяет более точно и стабильно доставлять дозу непосредственно в мишень, что снижает облучение здоровых тканей мозга вокруг опухоли.
Облучение нескольких метастазов
Дэвид Эндрюс, врач: Пусть даже пациенту назначено 36 часов радиохирургии, не важно. Благодаря поразительным технологиям линейных ускорителей мы можем выполнить облучение десяти метастазов в кратчайшие сроки — всего за полчаса.
Тимоти Зольберг, доктор наук: Применяемый сегодня метод лечения множественных метастазов заключается в том, чтобы облучать один метастаз за другим, и, безусловно, можно так и делать. С помощью гамма-ножа это традиционно делается на линейном ускорителе. Облучается метастаз за метастазом, и процедура занимает 15–20 минут для каждого. Если у пациента 12 метастазов, приходится облучать его в течение трех, а то и четырех часов.
Дэвид Роберж, врач: Это не так актуально, когда речь идет о двух или трех опухолях. Но если необходимо облучить 10 или 15 опухолей, крайне неудобно облучать их по одной за раз. Гораздо проще использовать технологию, с помощью которой можно облучить все сразу.
Гораздо проще использовать технологию, с помощью которой можно облучить все сразу.
Тимоти Зольберг, доктор наук: Исторически сложилось, что планирование облучения выполняется вручную и зависит от знаний и опыта физика, сидящего за компьютером. Все делается вручную, шаг за шагом, пока не получается план. Не самый лучший план, поскольку вы знаете, что могли бы потратить немного больше времени и получить лучший результат. Но этот план клинически приемлем, и нет причин его переделывать, поскольку есть компьютеры, которые оптимизируют его автоматически.
Джеймс Робар, доктор наук: Новые подходы позволяют облучать все метастазы с использованием единого изоцентра. Одним из таких методов является дуговая терапия с объемной модуляцией. Поворачивая гантри линейного ускорителя, можно создавать отверстия очень сложной формы для облучения сразу всех метастазов. В зависимости от ориентации микромноголепесткового коллиматора может быть сложно создать две отдельные апертуры без создания между ними области, которую облучать нежелательно.
Новое программное обеспечение для облучения множественных метастазов
Джеймс Робар, доктор наук: Набирает популярность еще один метод, в котором используется иной подход для выбора групп метастазов в головном мозге и их облучения за один поворот гантри. Допустим, у пациента семь метастазов в головном мозге. Данный алгоритм оценивает эти метастазы и решает, что три из семи можно облучить с использованием одной дуги гантри, а затем для второго поворота гантри алгоритм может выбрать оставшиеся четыре метастаза. Такое решение будет принято, чтобы подвергнуть облучению как можно меньший объем здоровой ткани мозга.
Почему иногда необходимо проводить несколько сеансов радиохирургии?
Дуайт Херон, врач: Все чаще мы сталкиваемся с более сложными во всех отношениях и более крупными опухолями, а также опухолями, которые расположены очень близко к критическим структурам, таким как перекрест зрительных нервов, ствол головного мозга или один из основных черепно-мозговых нервов. Использовать одну фракцию было бы нежелательно, это было бы чревато слишком серьезными побочными эффектами. И сегодня благодаря современным технологиям, переставляемым рамам, визуализационному контролю и возможности регулировать интенсивность пучка радиации мы можем доставлять эффективную дозу облучения, разбивая ее на более мелкие фракции. Это называется «гипофракционирование». Например, для самых маленьких опухолей можно подать 21 или 24 грея. И это доза излучения в одной фракции. Но для опухоли размером три сантиметра мы используем гораздо более низкую дозу — 16 греев. Звучит странно, ведь в большой опухоли больше клеток, которые нужно уничтожить. Тогда почему мы используем более низкую дозу? Дело в том, что, если мы попытаемся подать 24 греев на трехсантиметровую опухоль, побочные эффекты, а именно отек и некроз, то есть омертвение тканей мозга, будут чрезвычайно тяжелыми.
Использовать одну фракцию было бы нежелательно, это было бы чревато слишком серьезными побочными эффектами. И сегодня благодаря современным технологиям, переставляемым рамам, визуализационному контролю и возможности регулировать интенсивность пучка радиации мы можем доставлять эффективную дозу облучения, разбивая ее на более мелкие фракции. Это называется «гипофракционирование». Например, для самых маленьких опухолей можно подать 21 или 24 грея. И это доза излучения в одной фракции. Но для опухоли размером три сантиметра мы используем гораздо более низкую дозу — 16 греев. Звучит странно, ведь в большой опухоли больше клеток, которые нужно уничтожить. Тогда почему мы используем более низкую дозу? Дело в том, что, если мы попытаемся подать 24 греев на трехсантиметровую опухоль, побочные эффекты, а именно отек и некроз, то есть омертвение тканей мозга, будут чрезвычайно тяжелыми.
Дэвид Роберж, врач: В промежутках между процедурами здоровая ткань мозга может восстанавливаться. Между процедурами некоторые участки опухоли, которые были более устойчивы к радиации, например потому, что получали недостаточно кислорода, могут получить больше кислорода и стать более чувствительными к облучению.
Дуайт Херон, врач: Всем клеткам в организме нужен кислород, а клеткам опухоли требуется еще больше кислорода, потому что они очень быстро растут. Фактически их рост может опережать кровоснабжение. И когда они опережают кровоснабжение, их называют гипоксическими. В центре опухоли мало кислорода. Именно поэтому эффективнее подавать меньшую дозу радиации, но в нескольких фракциях. От этого опухоль уменьшается, и та часть, которая была гипоксической, получает больше крови. По мере дальнейшего сокращения ее кровоснабжение увеличивается, поэтому облучение становится более эффективным. Становится больше кислорода, а значит, и больше свободных радикалов для уничтожения раковых клеток. В результате эффективность лечения повышается.
Дэвид Роберж, врач: Для некоторых крупных опухолей, возможно, будет эффективнее проводить три или пять процедур вместо одной. К тому же, если есть система, которая позволяет ничего не прикручивать к голове пациента, выбор оптимального варианта облучения опухоли становится шире. Если это три процедуры, мы сделаем три облучения. Если одна процедура, мы сделаем одно облучение. Качество и точность будут одинаковыми.
Если это три процедуры, мы сделаем три облучения. Если одна процедура, мы сделаем одно облучение. Качество и точность будут одинаковыми.
Почему лучевая терапия всего головного мозга до сих пор применяется?
Эрик Чанг, врач: Практика лучевой терапии всего головного мозга очень прочно укоренилась в сознании многих онкологов-радиологов, и это неизменно уже очень много лет.
Дэвид Эндрюс, врач: Лучевая терапия без фокусирования наносит ущерб окружающей ткани.
Дуайт Херон, врач: Зачем продолжать использовать технологии и метод облучения, которые приводят к развитию серьезных, долгосрочных, необратимых побочных эффектов, таких как потеря памяти и деменция, когда тщательно продуманный клинический подход в радиохирургии в сочетании с внимательным последующим наблюдением позволяет получить идентичные результаты. Мне кажется вопиющим, что страховые компании отказывают в хороших методах лечения. Одной из причин, почему лучевая терапия всего головного мозга так популярна, является то, что даже в центрах с необходимыми специалистами и возможностями для проведения радиохирургии пациенты получают отказ.
Эрик Чанг, врач: Если начать лечение пациента с радиохирургии, это не значит, что дополнительные методы лечения исключаются. Лучевую терапию всего головного мозга можно провести позже, если это будет необходимо. Я считаю, что лучевая терапия всего головного мозга всегда будет занимать определенное место в лечении метастатических заболеваний мозга, но я также думаю, что популярность этого метода будет постепенно сходить на нет из-за пациентов с более сложными случаями метастазирования.
Что я могу сделать как пациент для поддержания наилучшего качества жизни?
Дэвид Роберж, врач: Если назначить пациенту радиохирургическое лечение и не наблюдать его после процедуры, вероятность образования новых метастазов в мозге, к сожалению, составляет примерно 50/50. И если не наблюдать пациентов, то единственными причинами для повторной встречи будут ухудшение их состояния и поступление в реанимацию. Но если приглашать их на прием каждые несколько месяцев и делать МРТ, вы можете обнаружить новые метастазы, пока их размер не превышает нескольких миллиметров. Вы можете удалить их до того, как они станут представлять проблему. Зачастую пациентов даже с прогрессирующим раком и метастазированием в головном мозге можно спасти, если контролировать ситуацию, выявлять метастазы и облучать их, пока они малы.
Вы можете удалить их до того, как они станут представлять проблему. Зачастую пациентов даже с прогрессирующим раком и метастазированием в головном мозге можно спасти, если контролировать ситуацию, выявлять метастазы и облучать их, пока они малы.
Дуглас Кондзиолка, врач: Фактически на этом этапе мониторинг рака схож с ведением хронических заболеваний, для которых необходимо периодически сдавать анализы. Как и для поддержания здоровья других органов, ПЭТ-сканирование, периодические КТ-сканирования нужны и для головного мозга.
Орин Блох, врач: Если вы заметили пару сорняков в саду, вы можете пойти и вырвать эти сорняки либо перекопать весь газон. Но могут остаться два или три сорняка, которых вы не заметили. Если они вырастут, вы можете просто вырвать их позже.
Почему иногда необходимо хирургическое лечение?
Орин Блох, врач: Конечно, пациенты хотели бы избежать операции. Перспектива, что вам вскроют черепную коробку и будут копаться в вашем мозге, очень пугает.
Дуглас Кондзиолка, врач: Если опухоль большая и имеет клинические проявления, вызывая невыносимые головные боли, частые судороги или проблемы с равновесием, и ее расположение подходит для хирургического удаления, может быть показано удаление этой опухоли оперативным путем, чтобы уменьшить давление на мозг. Многие пациенты благодарны за такое решение. Когда я объясняю, что это самый быстрый способ улучшить их самочувствие, их это радует. Вот когда мы задумываемся об операции: когда это отвечает нуждам пациента.
Орин Блох, врач: Как только мы удаляем опухоль, отек начинает спадать, поэтому после удаления метастазов в головном мозге пациентам становится лучше уже на следующий день после операции. Мы используем минимально инвазивный способ: делаем небольшие краниотомии непосредственно над местом вмешательства. В современных условиях для этого мы используем технологию, называемую интраоперационной нейронавигацией. С ее помощью мы можем рассчитать кратчайшее расстояние от поверхности черепа до опухоли и сделать наименьшее отверстие из возможных.
Почему иногда нужны и хирургические операции, и радиохирургия?
Орин Блох, врач: При хирургическом вмешательстве невозможно гарантировать 100%-ное удаление опухоли. Порой, даже если мы удалили все, что можно увидеть на МРТ, мы знаем, что остались микроскопические клетки. Данные ясно показывают, что результаты лечения улучшаются, если в области, где была удалена опухоль, провести радиохирургию. Облучение радиацией до хирургической операции — это очень любопытная идея, которая начинает вызывать все больший интерес. Концепция заключается в том, что, если облучить опухоль радиацией до того, как сделать операцию, облучение начнет убивать клетки опухоли. Поэтому когда мы приступаем к операции по удалению опухоли, большая ее часть уже мертва, а клетки, которые попадают в ткани во время операции, уже не смогут распространиться и образовать новые опухоли. Когда облучение радиацией выполняется до операции, гораздо проще очертить контуры опухоли и точно понять, где граница между нею и здоровой тканью мозга.
Как выбрать самое лучшее и самое подходящее отделение терапии?
Тимоти Зольберг, доктор наук: Радиохирургия — это все еще новое направление. Двадцать лет — довольно небольшой срок. Стандарты медицинского обслуживания включают довольно много доступных процедур.
Дэвид Роберж, врач: Радиохирургия весьма быстро развивается. И это палка о двух концах, поскольку радиохирургию, особенно метастазов в мозге, теперь можно пройти в сравнительно небольших клиниках со стандартным оборудованием для лучевой терапии. Но качество лечения в таких условиях может существенно отличаться от качества лечения в крупных учреждениях, в которых есть устройства, предназначенные для радиохирургии. Для пациента и даже для меня сложно с порога определить, насколько такие клиники квалифицированы для радиохирургии.
Тимоти Зольберг, доктор наук: Честно говоря, нет никаких гарантий, что не будет проблем. Novalis Certified — единственная в мире программа, которая предполагает наличие независимой группы специалистов. Они могут прийти, посмотреть на вашу практику и подтвердить, что вы выполняете стереотаксическую радиохирургию на высоком уровне с клинической точки зрения, с технической точки зрения, с точки зрения физики и гарантируете качество всех своих услуг. Это очень важный показатель.
Они могут прийти, посмотреть на вашу практику и подтвердить, что вы выполняете стереотаксическую радиохирургию на высоком уровне с клинической точки зрения, с технической точки зрения, с точки зрения физики и гарантируете качество всех своих услуг. Это очень важный показатель.
Как будет развиваться лечение метастатического рака головного мозга в будущем?
Элизабет Уилсон, CEO: В вопросах лечения метастатического рака и метастазов в головном мозге в частности мы только в начале пути. Ценность этого фильма заключается в том, что к его созданию привлекается Американская ассоциация онкологии головного мозга. Он служит нашей миссии. Если люди поймут, что у них достаточно времени для осознания своей опухоли, осознания своего диагноза, достаточно времени для того, чтобы изучить возможные варианты лечения, то улучшится и ход лечения, и его результат. Я думаю, это и есть путь реализации миссии нашей организации.
Орин Блох, врач: Если лечение токсично и приведет к снижению когнитивных способностей, пациенты не смогут наслаждаться годами жизни, которые мы подарим им с помощью новых методов лечения. Поэтому в современных условиях при лечении больных раком необходимо учитывать и качество жизни, которую им предстоит прожить.
Поэтому в современных условиях при лечении больных раком необходимо учитывать и качество жизни, которую им предстоит прожить.
Вероника Чанг, врач: Мы хотим, чтобы люди продолжали жить, работать и делать все, что для них важно.
Дуайт Херон, врач: Радиохирургия является неотъемлемой частью новейших методик лечения рака.
Бренда Винченц-Смит: Знаете, я больше не думаю о смерти. Правда. Я считаю, это показатель.
Дэвид Эндрюс, врач: Если мы можем продлить жизнь пациента хоть ненадолго, он сможет воспользоваться возможностями лечения, которые станут доступны в будущем. Возможностями, которых не было, например, еще три года назад. Это дает пациентам реальную надежду.
Орин Блох, врач: Технологии достигли уровня, когда мы можем улучшать самочувствие пациентов и зачастую даже излечивать интракраниальные заболевания. Большинство пациентов с раком, у которых нашли метастазы в головном мозге, осознают, что окончательный прогноз зависит от того, что происходит с раком в остальных частях тела. Будущее для этих людей действительно светлое, потому что наши системные методы лечения постоянно совершенствуются, а процент выживания намного выше, чем когда-либо в прошлом. Я считаю, что в будущем рак перестанет считаться смертельной болезнью и станет просто хроническим заболеванием.
Будущее для этих людей действительно светлое, потому что наши системные методы лечения постоянно совершенствуются, а процент выживания намного выше, чем когда-либо в прошлом. Я считаю, что в будущем рак перестанет считаться смертельной болезнью и станет просто хроническим заболеванием.
Киста почки — WMT клиника высоких технологий
Киста почки – новообразование, которое развивается из паренхимы почки и имеет полость, чаще всего заполненную жидкостью. Обычно кисты являются доброкачественными, располагаются одиночно и обнаруживаются случайно при обследовании по другому поводу.
КЛАССИФИКАЦИЯ КИСТЫ ПОЧКИ ПО BOSNIAK
Несмотря на то, что кисты в большинстве случаев имеют доброкачественный характер, встречаются и те, которые требуют повышенного внимания. С этой целью используется классификация по Bosniak:
I категория
Простые доброкачественные кисты почек, которые четко визуализируются ультразвуком, КТ или МРТ. Они часто встречаются и никак не проявляют себя, а также не требуют никакого лечения кроме наблюдения.
II категория
Доброкачественные кисты с минимальными изменениями. Отличаются от кист первой категории появлением перегородок, отложением кальция в стенках или перегородках. Данная категория кист практически не становится злокачественной и нуждается в динамическом УЗ- наблюдении. Размеры менее 3 см.
IIF категория
Доброкачественные кисты, которые содержат большее количество тонких перегородок. Стенки и перегородки могут быть утолщены, часто содержат отложения кальция в виде узелков. Практически никогда не накапливают контраст, так как не содержат тканевого компонента. Размеры этих кист могут быть больше или равны 3 см и нуждаются в динамическом наблюдении. Как правило, не требуют оперативного лечения.
III категория
Группа более неопределенная и имеет тенденцию к малигнизации (приобретает злокачественные качества). Радиологические особенности включают нечеткий контур, утолщенные перегородки и неоднородные участки отложения кальция.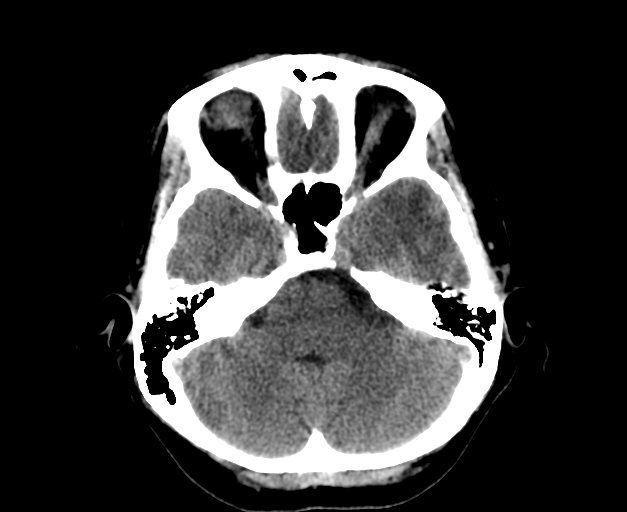 При отсутствии травм почки или инфекционных заболеваний, как правило, требуют оперативного лечения.
При отсутствии травм почки или инфекционных заболеваний, как правило, требуют оперативного лечения.
IV категория
Образования имеют большой жидкостный компонент, неровный и даже бугристый контур и, что особенно важно, местами накапливают контрастное вещество за счет тканевого компонента. Этот процесс косвенно указывает на малигнизацию, всегда требует оперативного лечения.
КАК ПРОЯВЛЯЮТСЯ КИСТЫ ПОЧЕК?
Чаще всего пациенты отмечают боли в пояснице, особенно при долгой ходьбе или тяжелой физической нагрузке, на примесь крови в моче. Поскольку почка участвует в регуляции артериального давления, при некоторых кистах отмечают стойкое высокое артериальное давление без видимых причин, не поддающееся лечению лекарственной терапией. При кистах больших размеров пациенты отмечают сильные боли даже в покое, а также могут прощупывать непонятное образование в животе. В редких случаях могут развиваться симптомы почечной недостаточности.
Здесь также стоит упомянуть о другом заболевании – поликистоз почек.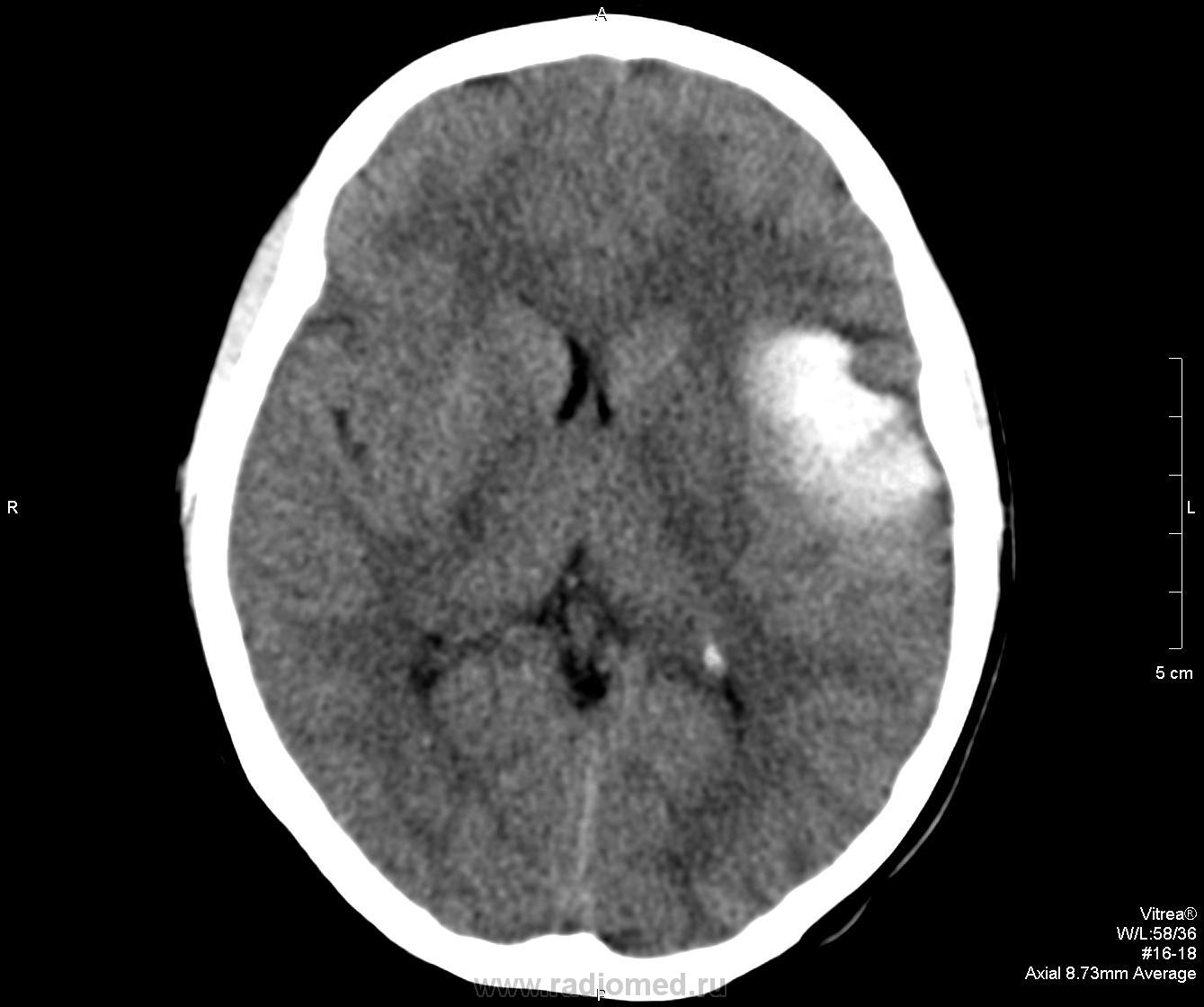 Это врожденное наследственное заболевание, при котором появляются множественные кисты в паренхиме почки. Врожденный поликистоз прогрессирует медленно и проявляется аналогично классической кисте почки, однако возможность радикального лечения в этом случае сильно ограничена.
Это врожденное наследственное заболевание, при котором появляются множественные кисты в паренхиме почки. Врожденный поликистоз прогрессирует медленно и проявляется аналогично классической кисте почки, однако возможность радикального лечения в этом случае сильно ограничена.
ДИАГНОСТИКА КИСТЫ ПОЧКИ
Для получения достоверного результата врачи проводят инструментальную диагностику: УЗИ, КТ с контрастированием или МРТ. Для диагностики функции почек выполняют радиоизотопное исследование – сцинтиграфию. Полное обследование обязательно для исключения опухоли почки, определения функций почки, исключения почечной недостаточности и определения показаний к операции.
ЛЕЧЕНИЕ КИСТЫ ПОЧКИ
В клинике WMT проводится тщательная оценка кисты на предмет ее сложности и дисфункции почки, вызванной кистозным новообразованием. При необходимости выполняется лапароскопическая резекция кисты почки – операция по удалению кисты через несколько проколов в области поясницы. Благодаря такой технике выполнения операции пациент может вернуться к привычной жизни уже через 2-3 дня.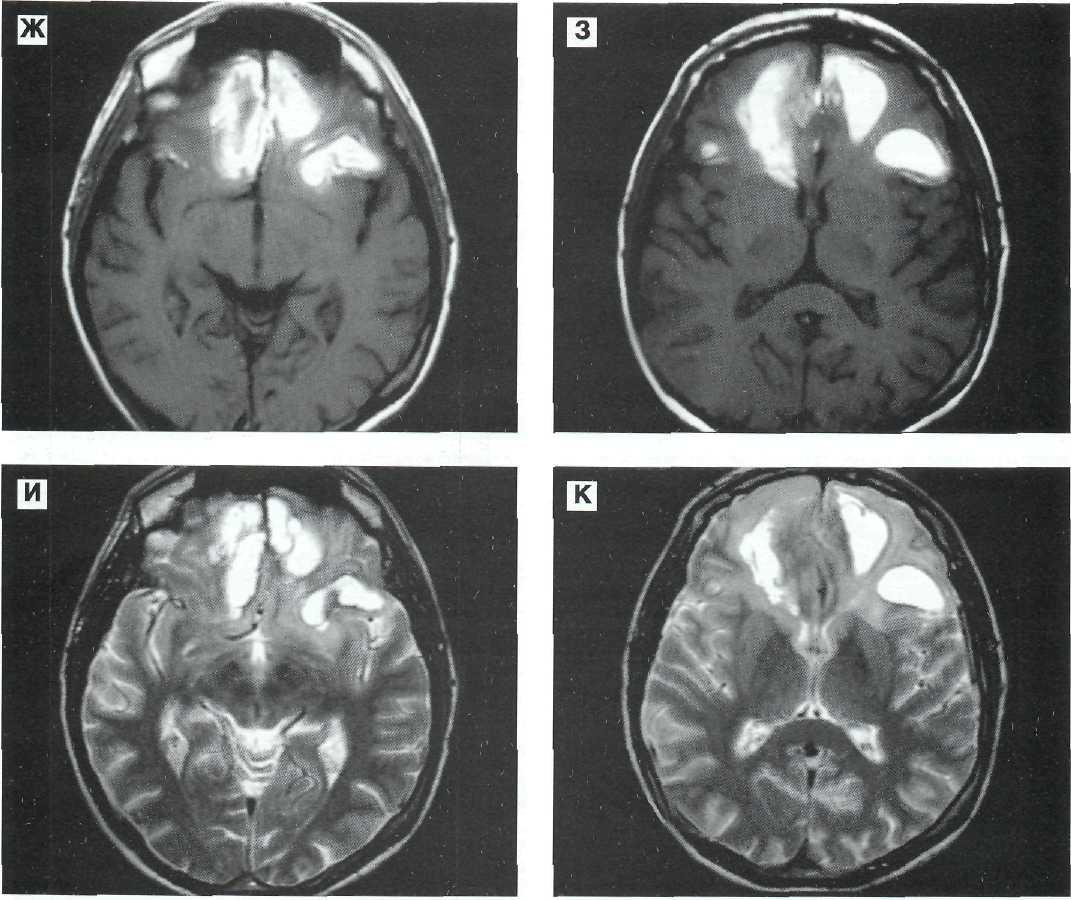
Лечение кисты почки возможно только оперативным путем. При образованиях небольших размеров, которые не имеют признаков злокачественности, пациенты остаются под динамическим наблюдением.
Операция показана пациентам при:
- Выраженных болевых синдромах при сдавлении кистой соседних органов
- Нарушениях мочеоттока, вызванных кистой
- Разрыве кисты или угрозе разрыва
- Наличии инфекционного очага в кисте
- Некупируемой артериальной гипертензии, а также при подозрении на злокачественный процесс
В некоторых случаях пациентам проводят введение специальных склерозантов в полость кисты с целью заполнения этой полости и снижения дальнейшего роста кисты. Однако этот метод не является радикальным, и у некоторых пациентов может возникнуть рецидив. В случае врожденного поликистоза оперативное лечение практически не показано. Таких пациентов ведут консервативно.
ЗАПИСЬ НА ПРИЁМ
Запишитесь на консультацию к урологу клиники WMT по телефону: 8 (861) 206-03-03 или оставьте заявку на сайте.
Кисты и доброкачественные новообразования селезенки — Клиника хирургии «Кураре»
Селезенка — непарный орган, отвечающий в организме человека за кроветворение, иммунитет и кровоснабжение. Строение селезенки: уплощенная овальная форма и в основном состоит из лимфоидной ткани.
Размеры в норме: 16 х 6 х 1.5 — 2.5 см,
Основной процент заболеваний селезенки связан с вторичным процессом, являющиеся следствием заболеваний других органов и систем – болезней крови, иммунных патологий, опухолей, системных заболеваний или повреждений (травм) селезенки. К ним относятся: инфаркт селезенки, перекрут ножки селезенки, абсцесс селезенки, разрыв селезенки, киста селезенки, доброкачественные и злокачественные образования селезенки.
Кисты селезенки
Одной из более частой патологии селезенки являются киста селезенки. Формирование кисты обусловлено многими факторами (причины):
-нарушение эмбрионального развития плода (формирование полостей)
-травма селезенки (закрытая и открытая травма живота, оперативные вмешательства)
-острый воспалительный процесс селезенки (тяжелые инфекционные заболевания)
-инфаркт селезенки
-паразитарные заболевания
Классификация кист селезенки:
-истинные (врожденные)
-ложные (приобретенные)
Клиническая картина: клиническая картина зависит от размеров кисты селезенки.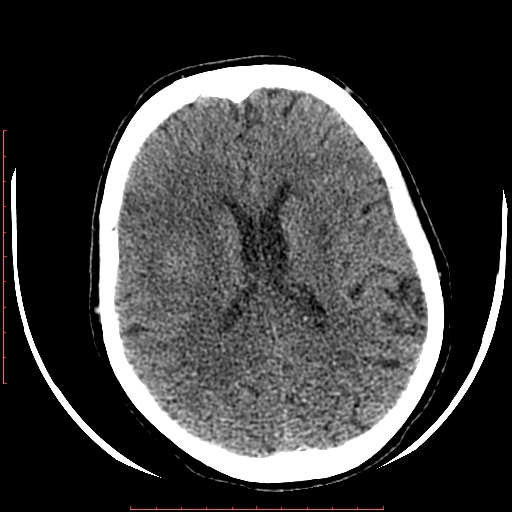 При наличии кисты размерами до 2-3 см характерно бессимптомное течение заболевания. При воспалении кисты селезенки, при резком увеличении в размерах кисты появляется боль в левом подреберье, повышение температуры тела, тошнота, головокружение. При очень больших размерах боль отдает в левую лопатку и плечо, тяжесть в левом подреберье после приема пищи, периодически возникает рвота.
При наличии кисты размерами до 2-3 см характерно бессимптомное течение заболевания. При воспалении кисты селезенки, при резком увеличении в размерах кисты появляется боль в левом подреберье, повышение температуры тела, тошнота, головокружение. При очень больших размерах боль отдает в левую лопатку и плечо, тяжесть в левом подреберье после приема пищи, периодически возникает рвота.
Лечение:
-если киста размерами до 3 см и исключен паразитарный характер кисты, требуется динамическое наблюдение.
-киста более 3 см, имеющая тенденцию к увеличению в размерах, существует опасность перерождения в злокачественную опухоль, опасность разрыва и инфицирования кисты, — является показанием к оперативному лечению.
Объем и метод операций индивидуален как каждого случая, зависит размеров, расположения (центральная, периферическая), характера кисты (паразитарная и непаразитарная), от тяжести состояния пациента, сопутствующей терапевтической патологии.
Виды операций:
-открытая спленэктомия
-лапароскопическаяспленэктомия
-лапароскопическая резекция кисты селезенки
Миниинвазивные манипуляции:
-чрескожная пункция и дренирование кисты , склеротерапия под ультразвуковым наведением
Первичные новообразования селезенки могут быть как доброкачественными, так и злокачественными.
Доброкачественные опухоли селезенки
Из доброкачественных опухолей селезенки встречаются гемангиомы (опухоли сосудистого происхождения), лимфангиомы, лимфомы (опухоли лимфоидной ткани), эндотелиомы, гамартомы, фибромы.
При малых размерах опухолей нет никаких проявлений. При прогрессировании процесса (вплоть до разрыва селезенки) и увеличения в размерах, капсула селезенки растягивается и пациента начинают беспокоить боли постоянного характера.
Лечение: только хирургическое. Объем операции и метод операции зависит от размеров, расположения (центральная, периферическая), от тяжести состояния пациента по сопутствующей терапевтической патологии.
Объем операции и метод операции зависит от размеров, расположения (центральная, периферическая), от тяжести состояния пациента по сопутствующей терапевтической патологии.
Виды операций:
-открытая спленэктомия
-лапароскопическая спленэктомия
-лапароскопическая резекция селезенки
Злокачественные опухоли селезенки
Злокачественные опухоли селезенки могут быть первичными или вторичными (метастатическими).
К первичным опухолям селезенки относятся саркомы, злокачественная лимфома (первичный очаг только в селезенке).
К вторичным опухолям селезенки относятся метастазы рака другой локализации.
Лечение: комбинированное (хирургическое — удаляют пораженный орган + химиотерапия).
Виды операций:
-открытая спленэктомия
-лапароскопическая спленэктомия
Рак легких — симптомы, лечение, диагностика, операция.

• Определение стадии опухоли.
Пожалуй, ключевым моментом в предоперационном обследовании пациентов со злокачественными опухолями является определение стадии заболевания, то есть оценка степени распространенности рака (прорастание в окружающие органы, метастазы в лимфатические узлы и отдаленные органы). Именно стадия опухоли определяет прогноз и диктует выбор оптимальной тактики лечения. При раке легкого вопросы стадирования особенно остры и актуальны, так как цена решения о выполнении/невыполнении операции очень высока, а значит, от того насколько правильно и точно проведено стадирование зависит адекватность и эффективность лечения. Для предоперационного стадирования пациентов с раком легкого в нашем Центре разработан алгоритм, который согласуется с европейскими рекомендациями. У некоторых пациентов сочетание данных компьютерной томографии и позитронной эмиссионной томографии достаточно для определения стадии рака, однако в большинстве случаев для точного знания стадии необходимо прибегать к небольшой диагностической операции – видеомедиастиноскопии (рис.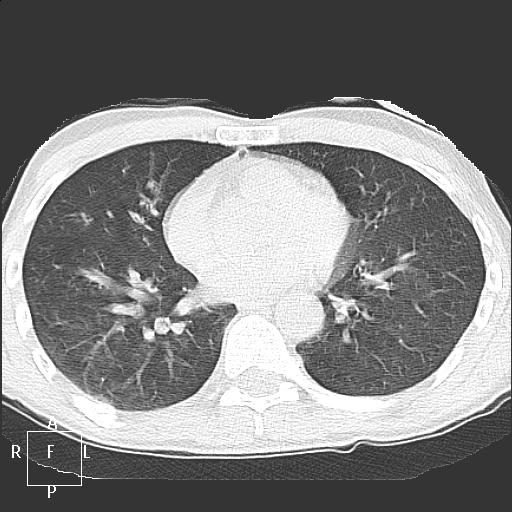 6). Эта процедура нужна для биопсии лимфатических узлов средостения. Нами накоплен и проанализирован крупнейший в городе опыт использования видеомедиастиноскопии при раке легкого. Результаты нашего исследования показали, что выполнение видеомедиастиноскопии перед большой операцией на легком позволяет улучшить отдаленные результаты лечения.
6). Эта процедура нужна для биопсии лимфатических узлов средостения. Нами накоплен и проанализирован крупнейший в городе опыт использования видеомедиастиноскопии при раке легкого. Результаты нашего исследования показали, что выполнение видеомедиастиноскопии перед большой операцией на легком позволяет улучшить отдаленные результаты лечения.
Рис. 6. Видеомедиастиноскопия – диагностическая операция, по результатам которой выбирается тактика лечения, определяется целесообразность хирургического лечения. А – введение медиастиноскопа в средостение через маленький разрез кожи на шее. Б – выполнение биопсии лимфоузлов под контролем видеоизображения. В – эндоскопическая картина во время операции: 1 – левый главный бронх, 2 – правый главный бронх, 3 – бифуркационные лимфоузлы, 4 – легочная артерия. Г – операция завершается наложением косметичного внутрикожного шва, практически незаметного на коже.
• Лечение.
В лечении рака легкого используются хирургическая операция, лучевая терапия, химиотерапия. Наиболее эффективным методом лечения при I-II стадии опухоли является хирургическое вмешательство, в ходе которого хирурги удаляют больную часть (долю) легкого или все легкое, а также лимфатические узлы средостения. При ранних стадиях рака легкого 5-летняя выживаемость после операции составляет 75-80 %. Для уменьшения травматичности необходимой больному операции в нашем Центре широко используются видеоторакоскопические вмешательства, которые позволяют существенно уменьшить операционную травму, послеоперационный болевой синдром, снизить частоту осложнений и существенно сократить восстановительный период.
Наиболее эффективным методом лечения при I-II стадии опухоли является хирургическое вмешательство, в ходе которого хирурги удаляют больную часть (долю) легкого или все легкое, а также лимфатические узлы средостения. При ранних стадиях рака легкого 5-летняя выживаемость после операции составляет 75-80 %. Для уменьшения травматичности необходимой больному операции в нашем Центре широко используются видеоторакоскопические вмешательства, которые позволяют существенно уменьшить операционную травму, послеоперационный болевой синдром, снизить частоту осложнений и существенно сократить восстановительный период.
При определении показаний к операции важно учитывать не только распространенность опухоли, но и возможность организма больного перенести необходимый объем операции, что в торакальной хирургии называется «функциональная операбельность». Мы уделяем большое внимание определению функциональной операбельности, для чего используются различные методы для оценки функциональных резервов организма.
В нашем Центре результаты обследования каждого пациента представляется на клиническом разборе и онкологической комиссии, где после подробного обсуждения выносится окончательное решение. Если оптимальным для больного является хирургическое лечение, операция незамедлительно выполняется торакальными хирургами нашего Центра (рис. 7). В тех случаях, когда вместо операции или после хирургического вмешательства пациенту необходима химиолучевая терапия, мы направляем больного в ведущие онкологические центры нашего города.
Рис. 7. Малоинвазивная радикальная операция при раке легкого – видеоторакоскопическая нижняя лобэктомия слева, выделение легочной артерии.
Чтобы записаться на консультацию к врачу по поводу диагностики и лечения рака легких в нашем центре —
позвоните по тел.: +7 952 3598179 – Санкт-Петербург (СПб).
И снова про мозг, «рак мозга» и «метастазы в мозг» (2): fillum — LiveJournal
Продолжение, Часть 2 (начало Часть 1 было вчера в этом посте — https://fillum. livejournal.com/224271.html)
livejournal.com/224271.html).
В этой серии постов — краткий перевод главы про Очаги Хамера в мозге из книги доктора Хамера «Наследие Новой Медицины» 1999 года. В книге эта глава очень большая, с подробными описаниями не только теории, но и конкретных случаев, с иллюстрирующими эти случаи КТ-снимками и описанием конфликтов, историй проявления симптомов и т.д. и т.п. Здесь же ограничусь пока лишь текстовым описанием, но и оно должно дать уже достаточно полное понимание того, что на самом деле происходит в мозге при работе любой Специальной Биологической Программы (СБП).
.
***********************
.
(Часть 2, продолжение)
.
Никаких операций на мозг! Два почти идентичных случая с разным исходом.
Следующие два случая тесно связаны друг с другом: оба случая были случайно представлены одним врачом на Конференции по верификации университета г. Дюссельдорфа под председательством профессора Штеммана в Гельзенкирхене. Оба пациента родом из соседних деревень и были знакомы друг с другом. В первом случае пациенту 28 лет, второму 19, оба правши, у обоих на правой стороне мозга уже был активный конфликт и оба пострадали почти в одно время от ещё одного в принципе одинакового конфликта. У обоих пациентов почти одновременно диагностировали «опухоль мозга» в центре коры для речи и гортани. Но с этого момента их пути расходятся: один узнал о Новой Медицине, когда было уже слишком поздно – он опоздал всего на несколько дней. Ему, ничего не подозревающему, сделали операцию на мозге, потому что врачи сказали, что иначе он очень скоро умрет. В абсолютной панике он позволил себя оперировать. В первые 2-3 месяца ему стало немного лучше, потому что давление отёка на мозг, конечно, исчезло – но через полгода он умер, как и все прооперированные на мозг, за немногим исключением…
В первом случае пациенту 28 лет, второму 19, оба правши, у обоих на правой стороне мозга уже был активный конфликт и оба пострадали почти в одно время от ещё одного в принципе одинакового конфликта. У обоих пациентов почти одновременно диагностировали «опухоль мозга» в центре коры для речи и гортани. Но с этого момента их пути расходятся: один узнал о Новой Медицине, когда было уже слишком поздно – он опоздал всего на несколько дней. Ему, ничего не подозревающему, сделали операцию на мозге, потому что врачи сказали, что иначе он очень скоро умрет. В абсолютной панике он позволил себя оперировать. В первые 2-3 месяца ему стало немного лучше, потому что давление отёка на мозг, конечно, исчезло – но через полгода он умер, как и все прооперированные на мозг, за немногим исключением…
.
Другой пациент во втором случае был тоже уже готов для операции на мозге. Но к счастью в этой больнице не было запасов нужной крови. На выходные он получил «отпуск» и использовал его для посещения конференции по верификации в Гельзенкирхене. Присутствующие там врачи смогли его убедить, что операция на мозг это опасное безобразие. Когда пациент в понедельник заявил врачам нейрохирургического отделения, что он больше не хочет быть оперированным, опухоль объявили неоперабельной, потому что она была слишком большой и злокачественной. Рассчитывать можно было только на облучение и химию, но и это тоже с очень плохими прогнозами. Он решил разобраться с Новой Медициной, понял её и не дал себя оперировать. По его собственным показаниям у него были боли ещё несколько месяцев, потом пациент выздоровел и снова стал работоспособным.
Присутствующие там врачи смогли его убедить, что операция на мозг это опасное безобразие. Когда пациент в понедельник заявил врачам нейрохирургического отделения, что он больше не хочет быть оперированным, опухоль объявили неоперабельной, потому что она была слишком большой и злокачественной. Рассчитывать можно было только на облучение и химию, но и это тоже с очень плохими прогнозами. Он решил разобраться с Новой Медициной, понял её и не дал себя оперировать. По его собственным показаниям у него были боли ещё несколько месяцев, потом пациент выздоровел и снова стал работоспособным.
.
Через 5 лет его профсоюз задним числом принудительно изменил его диагноз со «злокачественной опухоли мозга» на «доброкачественную каверному», потому что это просто не может быть, что с диагнозом «злокачественной опухоли мозга» человека не оперируют, и он снова становится здоровым.
.
Два этих случая показывают особенно ясно, что пациенты умирают, потому что с ними проводят безумные операции на мозг. В нашем случае второй пациент решил ничего не предпринимать, его конфликты были решены, и собственно ничего не должно было снова вернуться — это пациент понял очень хорошо. Через 5 лет этого пациента представили профсоюзу:
В нашем случае второй пациент решил ничего не предпринимать, его конфликты были решены, и собственно ничего не должно было снова вернуться — это пациент понял очень хорошо. Через 5 лет этого пациента представили профсоюзу:
Врач: «Господин Х., как Вы себя чувствуете?»
Пациент: «Добрый день, господин доктор, чувствую себя хорошо, я ни на что не жалуюсь, никаких приступов. Уже 4,5 года чувствую себя хорошо».
В.: «Но у Вас же опухоль мозга?»
П.: «Ну и что, я всё равно себя хорошо чувствую, я полностью работоспособен. Со мной на самом деле все хорошо!»
В.: «Да, но Вы не можете себя хорошо чувствовать. Иначе Вы должны быть признаны здоровым через 5 лет после опухоли мозга. И эту опухоль можно увидеть, как и тогда, хотя она и стала меньше».
П.: «Господин доктор, что я Вам должен сказать? У меня все хорошо».
В.: «Нет, так не пойдёт. От опухоли мозга умирают, с операцией или нет. Или у вас была опухоль мозга, тогда Вы должны были умереть, или это не была опухоль мозга, потому что Вы ещё живы».
П.: «Да, но господин доктор, я уже был в больнице для операции, только тогда не было запасов крови… и тогда сказали, что всё равно это неоперабельно, мне же надо было половину мозга вырезать, там всё равно уже ничего нельзя было сделать, даже облучение и химия не помогли бы».
В.: «Всё, хватит. У Вас просто не было опухоли мозга. Вы же ещё живы. Мы должны найти теперь новый диагноз, например «доброкачественная кавернома мозга»!»
П.: «Как скажете, господин доктор, Вы можете это назвать, как хотите, мне это не мешает. Но что такое доброкачественная кавернома мозга?»
В.: «Какая разница, ну что-то доброкачественное, иначе Вы должны были уже умереть!»
П. ухмыляясь: «Ну конечно, господин доктор, это я понимаю. У меня никогда не было опухоли мозга, и теперь тоже нет. Какое счастье, что Вы меня не прооперировали!»
С тех пор этот случай пациента проходит под псевдодиагнозом «доброкачественная кавернома мозга».
.
10.11 Гистология очагов Хамера
.
Наш человеческий мозг состоит – как и у животных – на 10% из клеток мозга (нервные клетки) и на 90% из глии, т.н. соединительной ткани мозга. О происхождении и функции этой глии ещё спорят учёные мужи, и я поэтому не хочу быть умнее, чем корифеи в этой области.
.
Несомненно то, что глия состоит из:
а) макроглии (большой глии), и
б) микроглии (малой глии).
.
Микроглия, как полагают в последнее время, должна быть образована костным мозгом и тесно связана (если не идентична) с моноцитами. Таким образом, она в любом случае принадлежит мезодерме. Раньше считалось, что она происходит от Pia Mater, соединительной ткани, непосредственно прилегающей к мозгу. Но даже в этом случае микроглия мезодермального происхождения.
Макроглия состоит из астроцитов и олигодендроцитов. Астроциты образуют преимущественно рубцы в головном мозге, в то время как олигодендроциты осуществляют примерно функцию т.н. клеток Шванна в мозге, а именно обволакивают и изолируют нервные клетки. Но эти функции практически не так легко дифференцировать на практике, как это возможно теоретически. Ниже мы обсудим это подробнее. Интересно, во всяком случае, то, что макроглия и микроглия тесно взаимодействуют друг с другом, причем микроглия подвижна (во всяком случае, в начале), а макроглия устойчива к своему местоположению. По этой причине есть исследователи, которые считают, что вся глия мезодермального происхождения, но большинство из них считают макроглию эктодермальной, происходящей из нервного желоба.
Но эти функции практически не так легко дифференцировать на практике, как это возможно теоретически. Ниже мы обсудим это подробнее. Интересно, во всяком случае, то, что макроглия и микроглия тесно взаимодействуют друг с другом, причем микроглия подвижна (во всяком случае, в начале), а макроглия устойчива к своему местоположению. По этой причине есть исследователи, которые считают, что вся глия мезодермального происхождения, но большинство из них считают макроглию эктодермальной, происходящей из нервного желоба.
.
Прежде всего, необходимо четко определить, что мозговые и нервные клетки не могут делиться или размножаться после нашего рождения. Поэтому уже по определению нет опухолей головного мозга в смысле карциномы. Единственное, что может там размножаться, это глия. Таким образом, на самом деле можно говорить только о рубцах соединительной ткани мозга или о келоиде глии. Но даже это описание, которое я пока еще считаю лучшим, отражает дело лишь наполовину, потому что в мозгу имеются разнообразные виды шрамов и всевозможные комбинации. И все же все они очаги Хамера.
И все же все они очаги Хамера.
.
Я задал вопрос нейро-гистопатологу в Эрлангене, как он себе представляет то, что на самом деле происходит при образовании очага Хамера. Он объяснил это следующим образом: При альтерации одной области мозга, в его словоупотреблении опухоли мозга, по какой-то причине происходит то, что французы назвали т.н. «Croissance perineuronale», по-русски: обволакивание мозговых нервных клеток перекрёстным образом. Если представить себе отдельные клетки мозговых нервов в виде небольших батарей, то в результате какого-то процесса у большого количества таких батарей произошла утечка, и они должны быть теперь герметизированы или заизолированы между собой с помощью глии. Это можно по аналогии представить так, как если бы огромная решетка в своих промежутках между каркасом была бы заполнена твердым материалом, например, песком, стеклом или тому подобным. Такая «более твердая» консистенция, которую мы называем «гиперденсивным очагом» (более плотный очаг), состоит из отложений глии. Такой гиперденсивный очаг обычно также лучше снабжен кровью, как и наши шрамы, особенно келоидные рубцы тела. Поэтому гиперденсивные очаги обычно лучше окрашиваются контрастным веществом, а это обычно происходит везде, где за единицу времени течет больше крови, обогащенной контрастным веществом.
Такой гиперденсивный очаг обычно также лучше снабжен кровью, как и наши шрамы, особенно келоидные рубцы тела. Поэтому гиперденсивные очаги обычно лучше окрашиваются контрастным веществом, а это обычно происходит везде, где за единицу времени течет больше крови, обогащенной контрастным веществом.
.
Теперь ты сразу спросишь, дорогой читатель: а разве возможно, что всё далее перечисленное в принципе одно и то же: инсульт, кровоизлияние в мозг, киста мозга, опухоль головного мозга, менингеома, гиперденсивные (увеличенной плотности) и гиподенсивные (уменьшенной плотности) очаги или ареалы и всё множество непонятных отёков мозга всех видов?
Ответ: За немногими исключениями, да! Конечно, есть относительно редкие субдуральные и эпидуральные гематомы при падении (кровоизлияние между твердой мозговой оболочкой и паутинной (арахноидальной) мозговой оболочкой, соответственно между черепной коробкой и твердой мозговой оболочкой), конечно, есть менингиты (воспаление мягкой мозговой оболочки) и энцефалиты, например, после травм и операций, и, конечно, иногда есть также кровоизлияние в мозг.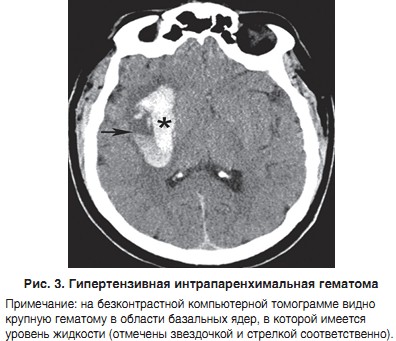 Не беря во внимание эти исключения, которые составляют самое большее 1%, все другие изменения в мозге являются Очагами Хамера в различных стадиях протекания, на различных местах и во время или после различной длительности конфликта.
Не беря во внимание эти исключения, которые составляют самое большее 1%, все другие изменения в мозге являются Очагами Хамера в различных стадиях протекания, на различных местах и во время или после различной длительности конфликта.
.
Далее попробуем дать короткий обзор о различных возможных видах очагов Хамера, по крайней мере, принципиально важнейших. Этот обзор не претендует на полноту.
.
.1 Так называемая «опухоль головного мозга» (на самом деле Очаг Хамера)
.
Это безобидное «нечто», которое тысячам людей во всем мире вырезают из мозга, только потому, что оно имеет более плотную консистенцию и увеличенную способность поглощать контрастное вещество. И то и другое основано на одном и том же процессе, а именно, что глия – соединительная ткань – обрастает альтерированную область Очага Хамера и, как в электричестве, восстанавливает «изоляцию», то есть усиливает её. Бесконечное количество людей, которым повезло, что этот ошибочно названный «опухолью мозга» безобидный остаточный рак у них никогда не был обнаружен, носят его с собой на протяжении десятилетий, без или с незначительными церебральными расстройствами.
Этот Очаг Хамера, то есть более или менее большое белое пятно или область на КТ, соответствующее скоплению глиальных клеток, увеличенных в этой ранее альтерированной области мозга, представляет собой конечную стадию заживления, когда у него больше нет интра- и перифокального отёка. Это теперь просто шрам, снабжающийся кровью лучше, чем окружающая среда, но тем самым он отличается от шрамов остального тела, так как в этом рубце по-прежнему сохраняется прежняя сетка нервных клеток мозга. Это тайна, почему ранее больная область тела, то есть место прежнего рака органов, после исцеления мирно продолжает существовать и даже может снова выполнять свою прежнюю задачу. Реле «компьютера» мозга практически исправлено и отремонтировано глиёй. Понимая это, мы также можем себе представить, почему рецидив конфликта должен иметь такие разрушительные последствия, хотя, конечно, для этого должны быть задействованы дальнейшие компоненты.
Если говорить об Очаге Хамера в фазе восстановления, который в общепринятой медицине до сих пор называют «опухоль мозга», не зная истинных взаимосвязей, то, конечно, мы всегда должны себе ясно представлять следующие два факта:
.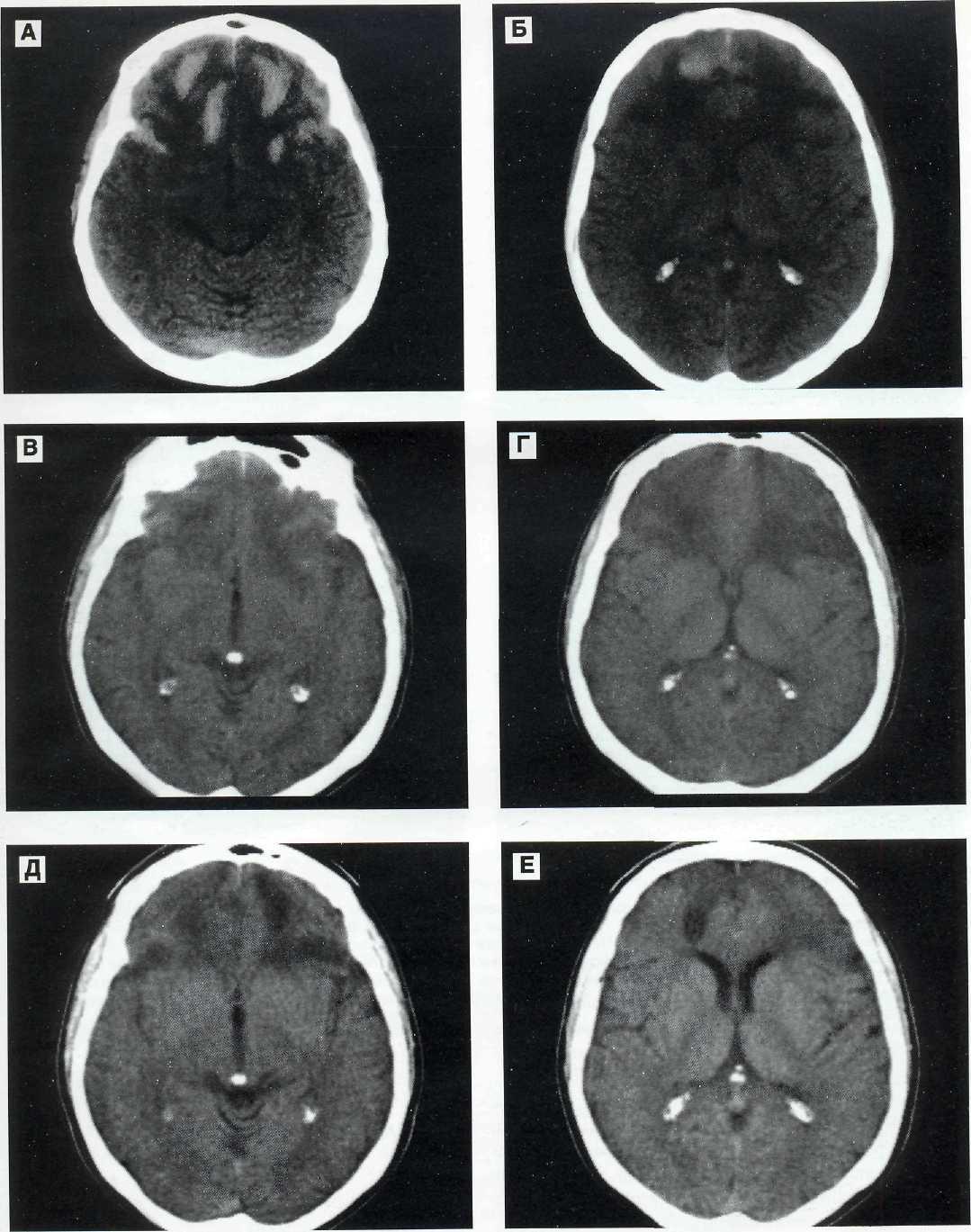
а) Каждому Очагу Хамера в PLC-фазе предшествовал Очаг Хамера с чёткой конфигурацией стрелковой мишени на том же месте в активной фазе конфликта (СА-фаза). Чаще всего мы его не видели только потому, что на данном этапе он ещё не проявлял никаких заметных симптомов, или потому, что мы, например, пропускали лёгкие двигательные или сенсорные, или пациент не жаловался по этому поводу.
б) Как в активной фазе конфликта с типичными конфигурациями мишени с чёткими кругами, так и в фазе восстановления с их более или менее большими отёками и их увеличенной способностью окрашиваться контрастным веществом, — все Очаги Хамера со всеми симптомами на психическом, церебральном и органическом уровнях являются разумными процессами в смысле «Специальной Биологической Программы» (СБП). Это не противоречит тому, что эти очаги в фазе восстановления «ремонтируются».
.
.2 Так называемый апоплексический удар или «кровоизлияние в мозг»
.
Дорогие читатели, вы сейчас убедитесь, какой сложной становится номенклатура, т. е. правильное обозначение понятий. Между тем даже традиционная медицина заметила, что многие её диагнозы пересекаются с другими диагнозами или являются идентичными с ними, а частично являются абсолютно бессмысленными. Следующая сложность состоит в том, чтобы прежние т.н. диагнозы перевести на правильный язык Новой Медицины, где они являются только фазами Специальной Биологической Программы (СБП). Поэтому не расстраивайтесь, если вы не сразу всё поймёте. Я постараюсь это представить как можно проще.
е. правильное обозначение понятий. Между тем даже традиционная медицина заметила, что многие её диагнозы пересекаются с другими диагнозами или являются идентичными с ними, а частично являются абсолютно бессмысленными. Следующая сложность состоит в том, чтобы прежние т.н. диагнозы перевести на правильный язык Новой Медицины, где они являются только фазами Специальной Биологической Программы (СБП). Поэтому не расстраивайтесь, если вы не сразу всё поймёте. Я постараюсь это представить как можно проще.
В наших учебниках мы различали раньше так называемый «бледный инсульт» и так называемый «красный инсульт».
Бледный или белый (симпатикотонный) инсульт был двигательным или сенсорным параличом или и то и другое вместе. Мы также могли бы назвать его рассеянный склероз. Это просто активная фаза конфликта (СА-фаза) Специальной Биологической Программы. Бледный или белый инсульт, который мы не так уж и редко испытываем, хотя и не так расширенно, может исчезнуть так же быстро, как и пришёл, при условии, что конфликт быстро разрешился.
.
Для двигательной составляющей конечно обязателен эпилептический припадок в фазе восстановления, хотя, если он возникает ночью, его можно не заметить. Для сенсорной составляющей всегда обязателен абсанс в виде эпилептоидного криза. Но его, конечно, ночью ещё легче пропустить. Особенно мы любили раньше говорить об «апоплексическом ударе», если паралич, особенно двигательный (nervus facialis), был замечен на лице. При этом одна половина лица «падает вниз», а рот «тянет» в другую, не парализованную сторону.
Паралич на органическом уровне происходит всегда на противоположной стороне Очага Хамера в мозге. Например, если у пациента двигательный паралич левой стороны лица (N. facialis – лицевой нерв), то Очаг Хамера расположен в двигательном центре (Gyrus praecentralis) правой половины мозга. Рот тянет тогда на не парализованную сторону направо, в то время как левый уголок рта «провисает», что значит, он не обеспечивается нервным питанием.
.
Вернёмся теперь к т.н. «красному инсульту», также называемому красный или горячий удар (это всегда фаза восстановления Очага Хамера), который находится всегда на противоположной стороне проявляющегося двигательного или сенсорного паралича. Здесь дело осложняется тем, что как двигательные, так и сенсорные параличи могут быть вызваны также и «переливающимися» отёками. Это значит, что не обязательно в основе может лежать двигательный или сенсорный конфликт (разлуки). Если есть возможность сделать КТ головного мозга, это часто поможет успокоить и себя и родственников пациента, даже если пациент находится в т.н. церебральной коме, что часто равно абсансу при эпилептоидномкризисе. Часто тогда «ничего не делать» лучше, чем любой ценой вытаскивать пациента из «комы». Эпилептоидный кризис абсанса проходит сам собой. Но для понимания этого, как я сказал, необходимо иметь КТ головного мозга. Опасение, что это могло быть излияние в мозг, почти никогда не оправдывается. Это практически всегда отёк Очага Хамера, находящегося в фазе восстановления.
Здесь дело осложняется тем, что как двигательные, так и сенсорные параличи могут быть вызваны также и «переливающимися» отёками. Это значит, что не обязательно в основе может лежать двигательный или сенсорный конфликт (разлуки). Если есть возможность сделать КТ головного мозга, это часто поможет успокоить и себя и родственников пациента, даже если пациент находится в т.н. церебральной коме, что часто равно абсансу при эпилептоидномкризисе. Часто тогда «ничего не делать» лучше, чем любой ценой вытаскивать пациента из «комы». Эпилептоидный кризис абсанса проходит сам собой. Но для понимания этого, как я сказал, необходимо иметь КТ головного мозга. Опасение, что это могло быть излияние в мозг, почти никогда не оправдывается. Это практически всегда отёк Очага Хамера, находящегося в фазе восстановления.
.
Если пациент, например, пострадал от инфаркта левого желудочка с большим отёком право-церебрального периинсулярного реле, тогда большой отёк может, как мы говорим «вспучиваться» в соседние двигательные и сенсорные области коры, которые затопляются и временно вызывают паралич на противоположной стороне тела. Поэтому часто инфаркт миокарда ошибочно диагностируют как апоплексический инсульт и наоборот, в зависимости от того, какая симптоматика стоит на переднем плане. Часто медики считают, что пациент из-за своего инфаркта пострадал красным инсультом, что явно бессмысленно.
Поэтому часто инфаркт миокарда ошибочно диагностируют как апоплексический инсульт и наоборот, в зависимости от того, какая симптоматика стоит на переднем плане. Часто медики считают, что пациент из-за своего инфаркта пострадал красным инсультом, что явно бессмысленно.
.
Осторожно: пока ничего не известно о продолжительности протекания конфликта или конфликтов, то сложно оценить, будет ли отёк ещё увеличиваться или он уже достиг своей наивысшей точки. Даже длительная бессознательность тогда не причина для отчаяния, если зная конфликт можно оценить его протекание. Но надо думать и о рецидивах конфликта, которые могут отёк «раскачать». Большинство пациентов не настолько «в коме», что не могут слышать слова и даже понимать их. Итак, осторожно!
.
************
Окончание в следующем посте (Часть 3)
.
Егор Миронов
и команда онлайн-школы
[простые] Технологии Успеха
http://www.freeagain.ru/prostye-tehnologii-uspeha/
Т2-гиперинтенсивные очаги на МРТ головного мозга
Задний план:
Т2-гиперинтенсивные очаги являются одной из наиболее частых находок при магнитно-резонансной томографии (МРТ) головного мозга. Они могут создавать серьезные диагностические проблемы, что отражено в их английском названии и аббревиатуре — UBOs (Unidentified Bright Objects).
Они могут создавать серьезные диагностические проблемы, что отражено в их английском названии и аббревиатуре — UBOs (Unidentified Bright Objects).
Материал/методы: Проанализированы результаты МРТ головного мозга 246 пациентов (134 женщины, 112 мужчин) в возрасте от 2 до 79 лет.Исследования проводились на МРТ-сканерах 0,5 и 1,5 Тл. Были получены T1-, PD или FLAIR и T2-взвешенные изображения. Диффузионно-взвешенная визуализация (DWI) также выполнялась в системе сильного поля.
Результаты:
Установлены следующие диагнозы: расширенные периваскулярные пространства в 11 случаях, очаги, наиболее вероятно связанные со старением головного мозга -21, с мигренью -15, ишемические изменения -52, васкулиты -12, гипоксически-ишемические изменения -8, геморрагические очаги -11, воспалительные изменения -20, рассеянный склероз -50, центральный мостовой и экстрапонтинный миелинолиз -7, метастазы -7, изменения, вызванные лучевой и химиотерапией — 8, поражения, связанные с нейрометаболическими заболеваниями — 10, дегенеративные заболевания ЦНС — 13, эклампсия — 1.
Выводы: МРТ является чувствительным методом выявления очаговых поражений ЦНС, но менее специфичным в отношении их дифференциации. Особенности очаговых образований на МРТ-изображениях (количество, размер, локализация, наличие или отсутствие отека, реакция на контрастное вещество, эволюция во времени), а также сопутствующие признаки (атрофия отдельных структур головного мозга, постконтрастное усиление лептоменинх, сосуществование диффузных поражений, сосуществование поражений позвоночника) являются важными дифференцирующими элементами.Однако их нельзя рассматривать в отрыве от клинических данных и результатов других диагностических тестов.
Клиническое значение гиперденсивных поражений на КТ головного мозга без контрастирования, полученной сразу после реваскуляризации артерий у пациентов с острым ишемическим инсультом
Цель . Чтобы проанализировать характеристики гиперденсивных поражений на КТ головного мозга, проведенной сразу после реваскуляризации артерий (АР) у пациентов с острым ишемическим инсультом (ОИИ), отследить исходы этих поражений и изучить их клиническую значимость. Материалы и методы . В нашем исследовании приняли участие 97 пациентов с АИС. Среди них 52 пациента имели гиперденсивные поражения и были разделены на три категории: тип I, тип II и тип III в соответствии с морфологическими характеристиками гиперденсивных поражений. Всем пациентам было проведено несколько контрольных КТ/МР исследований для визуализации исходов поражений. Результаты . Среди 52 пациентов у 22 была обнаружена экстравазация контраста, у 23 — экстравазация контраста в сочетании с геморрагической трансформацией (ГТ) и у 7 подтверждено симптоматическое внутричерепное кровоизлияние (SICH) при контрольной КТ/МРТ.Среди группы без гиперденсивных поражений только 7 трансформировались в кровоизлияния, SICH не возникало.
Чтобы проанализировать характеристики гиперденсивных поражений на КТ головного мозга, проведенной сразу после реваскуляризации артерий (АР) у пациентов с острым ишемическим инсультом (ОИИ), отследить исходы этих поражений и изучить их клиническую значимость. Материалы и методы . В нашем исследовании приняли участие 97 пациентов с АИС. Среди них 52 пациента имели гиперденсивные поражения и были разделены на три категории: тип I, тип II и тип III в соответствии с морфологическими характеристиками гиперденсивных поражений. Всем пациентам было проведено несколько контрольных КТ/МР исследований для визуализации исходов поражений. Результаты . Среди 52 пациентов у 22 была обнаружена экстравазация контраста, у 23 — экстравазация контраста в сочетании с геморрагической трансформацией (ГТ) и у 7 подтверждено симптоматическое внутричерепное кровоизлияние (SICH) при контрольной КТ/МРТ.Среди группы без гиперденсивных поражений только 7 трансформировались в кровоизлияния, SICH не возникало. Все поражения типа I показали экстравазацию контраста; 23 очага II типа перешли в кровоизлияние, 2 — с SICH и 6 — с чистой экстравазацией контраста; все типы III развились в SICH. Заключение . Гиперплотные очаги на КТ головного мозга без усиления, полученные сразу после реваскуляризации артерий (АР), имели различные характеристики. Тип I указывает на экстравазацию чистого контраста. Гиперплотные поражения типа II и типа III свидетельствовали о более высокой частоте ГТ, наличие поражений типа III указывало на неблагоприятный исход.
Все поражения типа I показали экстравазацию контраста; 23 очага II типа перешли в кровоизлияние, 2 — с SICH и 6 — с чистой экстравазацией контраста; все типы III развились в SICH. Заключение . Гиперплотные очаги на КТ головного мозга без усиления, полученные сразу после реваскуляризации артерий (АР), имели различные характеристики. Тип I указывает на экстравазацию чистого контраста. Гиперплотные поражения типа II и типа III свидетельствовали о более высокой частоте ГТ, наличие поражений типа III указывало на неблагоприятный исход.
1. Введение
Артериальная реваскуляризация (АР) стала предпочтительным методом лечения пациентов с острым ишемическим инсультом (ОИИ) [1–3]. Неконтрастная КТ головного мозга, проведенная сразу после АР, часто выявляет гиперплотные очаги в паренхиме [4, 5]. О таких гиперплотных поражениях сообщалось и анализировалось в различной литературе с 1993 г. [6]. Однако до сих пор остается сложной задачей определить, являются ли гиперденсивные поражения экстравазацией контраста или кровоизлиянием в мозг [7]. Цель этого исследования состояла в том, чтобы проанализировать визуализационные характеристики внутричерепных гиперденсивных поражений и классифицировать их в соответствии с их морфологическими характеристиками. А окончательный исход и клиническое значение различных типов гиперденсивного поражения анализировали на основании его спонтанной регрессии, АГ или даже SICH.
Цель этого исследования состояла в том, чтобы проанализировать визуализационные характеристики внутричерепных гиперденсивных поражений и классифицировать их в соответствии с их морфологическими характеристиками. А окончательный исход и клиническое значение различных типов гиперденсивного поражения анализировали на основании его спонтанной регрессии, АГ или даже SICH.
2. Материалы и методы
2.1. Пациенты
С августа 2016 г. по март 2020 г. в наше исследование было включено 97 пациентов с ОИС (51 мужчина и 46 женщин), средний возраст которых составил 61 год.73 ± 8,44 года (диапазон 41–83 года). Это исследование было одобрено Комитетом по медицинской этике нашей больницы. У всех пациентов было получено письменное информированное согласие.
2.2. Артериальный тромболизис и/или механическая тромбэктомия
Всем пациентам был проведен артериальный тромболизис и/или механическая тромбэктомия в течение 6 часов после начала заболевания. Во всех случаях анализировали данные КТ головного мозга сразу после АР. Контрастным веществом для церебральной ангиографии при АР был иогексол (300 мгI/мл) в дозе 150-250 мл.Временное окно для артериального тромболизиса (от начала до начала артериального тромболизиса) составляет 3-6 часов. Тромболизис длится от 30 минут до 2,5 часов. В качестве тромболитического агента использовали урокиназу. Дозы урокиназы варьировали от 60 000 до 600 000 ЕД, с 10 мл физиологического раствора/60 000 ЕД, в виде болюсов. 40 пациентов лечили только тромболизисом, а 57 лечили механической тромбэктомией в сочетании с артериальным тромболизисом. Среди 97 пациентов местом окклюзии была внутренняя сонная артерия у 32 пациентов, сегмент М1 средней мозговой артерии у 54 пациентов, сегмент М2 у 8 пациентов и базилярная артерия у 3 пациентов.
Контрастным веществом для церебральной ангиографии при АР был иогексол (300 мгI/мл) в дозе 150-250 мл.Временное окно для артериального тромболизиса (от начала до начала артериального тромболизиса) составляет 3-6 часов. Тромболизис длится от 30 минут до 2,5 часов. В качестве тромболитического агента использовали урокиназу. Дозы урокиназы варьировали от 60 000 до 600 000 ЕД, с 10 мл физиологического раствора/60 000 ЕД, в виде болюсов. 40 пациентов лечили только тромболизисом, а 57 лечили механической тромбэктомией в сочетании с артериальным тромболизисом. Среди 97 пациентов местом окклюзии была внутренняя сонная артерия у 32 пациентов, сегмент М1 средней мозговой артерии у 54 пациентов, сегмент М2 у 8 пациентов и базилярная артерия у 3 пациентов.
2.3. Получение КТ
После церебральной ангиографии и реваскуляризации закупоренных сосудов всем пациентам сразу после АР была проведена неконтрастная КТ головного мозга. Последующая КТ выполнялась в течение 24 часов или 48 часов после процедуры. МР-сканирование без гадолиния выполнено 21 пациенту в течение 48 часов после процедуры. С помощью iCT-сканеров Philips Brilliance 256 рядов все пациенты были просканированы от основания черепа до макушки. Условия сканирования: 120кВ, 300мА, толщина слоя 3 мм.Сканер Philips Achieva 1,5 T MR использовался для получения изображений с кругом фазированного фронта черепа. Последовательность сканирования включает Т1-взвешенную последовательность, Т2-взвешенную последовательность, восстановление инверсии с ослаблением жидкости (Flair), визуализацию, взвешенную по диффузии (DWI), кажущийся коэффициент диффузии (ADC), визуализацию, взвешенную по восприимчивости (SWI) и т. д.
МР-сканирование без гадолиния выполнено 21 пациенту в течение 48 часов после процедуры. С помощью iCT-сканеров Philips Brilliance 256 рядов все пациенты были просканированы от основания черепа до макушки. Условия сканирования: 120кВ, 300мА, толщина слоя 3 мм.Сканер Philips Achieva 1,5 T MR использовался для получения изображений с кругом фазированного фронта черепа. Последовательность сканирования включает Т1-взвешенную последовательность, Т2-взвешенную последовательность, восстановление инверсии с ослаблением жидкости (Flair), визуализацию, взвешенную по диффузии (DWI), кажущийся коэффициент диффузии (ADC), визуализацию, взвешенную по восприимчивости (SWI) и т. д.
2.4. Imaging Evaluation
Характеристики неконтрастной КТ головного мозга всех пациентов были проанализированы и оценены двумя опытными лечащими рентгенологами или выше.По форме, локализации и масс-эффекту гиперденсивных образований больные были разделены на три категории: I тип (спорадические пятнистые образования с нечеткими границами, преимущественно распространяющиеся в коре головного мозга и его мозговых извилинах, без масс-эффекта (рис. а))), тип II (солидные образования в форме «массы» с четкими границами, которые в основном распространяются в базальном ганглии и без масс-эффекта или легкого масс-эффекта (рис. 2(а) и 3(а)) и тип III (диффузные пятнистые поражения, занимающие большую площадь с очевидным масс-эффектом (рис. 4(а)).Как только во время диагностики и оценки классификации возникнут расхождения, обе стороны должны разрешить разногласия путем консультаций.
а))), тип II (солидные образования в форме «массы» с четкими границами, которые в основном распространяются в базальном ганглии и без масс-эффекта или легкого масс-эффекта (рис. 2(а) и 3(а)) и тип III (диффузные пятнистые поражения, занимающие большую площадь с очевидным масс-эффектом (рис. 4(а)).Как только во время диагностики и оценки классификации возникнут расхождения, обе стороны должны разрешить разногласия путем консультаций.
2.5. Статистический анализ
Все статистические анализы проводились с использованием SPSS версии 18 (SPSS Inc, Чикаго, США). Количественные данные выражали как среднее значение ± стандарт (SD) и сравнивали с помощью двухвыборочного независимого t-критерия Стьюдента; Качественные данные выражали как скорость и сравнивали с помощью критерия хи-квадрат. P < 0,05 указывает на то, что разница была статистически значимой.
3. Результаты
3.1. Общие результаты
Среди 97 пациентов у 52 (53,6%) пациентов были выявлены гиперденсивные очаги вокруг зоны внутричерепного инфаркта при неусиленной КТ, проведенной сразу после АР, тогда как у остальных 45 (46,4%) пациентов (контрольная группа) гиперплотных очагов не было. . Основные клинические данные пациентов в группе с АГ и без АГ были сведены в табл. 1. Достоверных различий по возрасту, полу, АГ, СД, шкале NIHSS, предшествующей антитромбоцитарной терапии, степени реканализации, методам лечения выявлено не было. артериальная реваскуляризация.У 30 (57,7%) пациентов в группе внутричерепных гиперденсивных поражений развилась ГТ после АР, Среди контрольной группы у 7 пациентов конверсия в АИКГ (бессимптомное внутричерепное кровоизлияние) при контрольных КТ/МРТ в течение 24 или 48 часов после АР (табл. 2) , и SICH не произошло. Значительно более высокая частота ГТ наблюдалась в группе с гиперплотными поражениями по сравнению с группой без гиперденсивных поражений (P < 0,001).
. Основные клинические данные пациентов в группе с АГ и без АГ были сведены в табл. 1. Достоверных различий по возрасту, полу, АГ, СД, шкале NIHSS, предшествующей антитромбоцитарной терапии, степени реканализации, методам лечения выявлено не было. артериальная реваскуляризация.У 30 (57,7%) пациентов в группе внутричерепных гиперденсивных поражений развилась ГТ после АР, Среди контрольной группы у 7 пациентов конверсия в АИКГ (бессимптомное внутричерепное кровоизлияние) при контрольных КТ/МРТ в течение 24 или 48 часов после АР (табл. 2) , и SICH не произошло. Значительно более высокая частота ГТ наблюдалась в группе с гиперплотными поражениями по сравнению с группой без гиперденсивных поражений (P < 0,001).
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 66
66  HT = геморрагическая трансформация.
HT = геморрагическая трансформация.  2) и у 7 (рис. 13,5%) пациентов были подтверждены SICH (рис. 4) при контрольном КТ/МРТ в течение 24 или 48 часов после АР. При контрольной КТ через 24 или 48 часов после АР исходы различных типов гиперденсивных поражений были следующими (табл. 3): спорадические пятнистые поражения I типа (16 поражений) полностью исчезли с экстравазацией контраста; 23 поражения II типа (74.2 %) превратились в кровоизлияния (AICH), 2 очага (6,5 %) выявили SICH и 6 очагов (19,4 %) представляли собой экстравазацию контраста; все поражения типа III (5 случаев) переросли в SICH. Тип II и тип III имели значительно более высокую частоту HT, чем тип I (P < 0,01). Чувствительность, специфичность, положительная прогностическая ценность и отрицательная прогностическая ценность гиперденсивных поражений при КТ без контрастирования, проведенной сразу после АР, для прогнозирования ГТ составили 81,1%, 63,3%, 57,7% и 84,4% соответственно.
2) и у 7 (рис. 13,5%) пациентов были подтверждены SICH (рис. 4) при контрольном КТ/МРТ в течение 24 или 48 часов после АР. При контрольной КТ через 24 или 48 часов после АР исходы различных типов гиперденсивных поражений были следующими (табл. 3): спорадические пятнистые поражения I типа (16 поражений) полностью исчезли с экстравазацией контраста; 23 поражения II типа (74.2 %) превратились в кровоизлияния (AICH), 2 очага (6,5 %) выявили SICH и 6 очагов (19,4 %) представляли собой экстравазацию контраста; все поражения типа III (5 случаев) переросли в SICH. Тип II и тип III имели значительно более высокую частоту HT, чем тип I (P < 0,01). Чувствительность, специфичность, положительная прогностическая ценность и отрицательная прогностическая ценность гиперденсивных поражений при КТ без контрастирования, проведенной сразу после АР, для прогнозирования ГТ составили 81,1%, 63,3%, 57,7% и 84,4% соответственно. 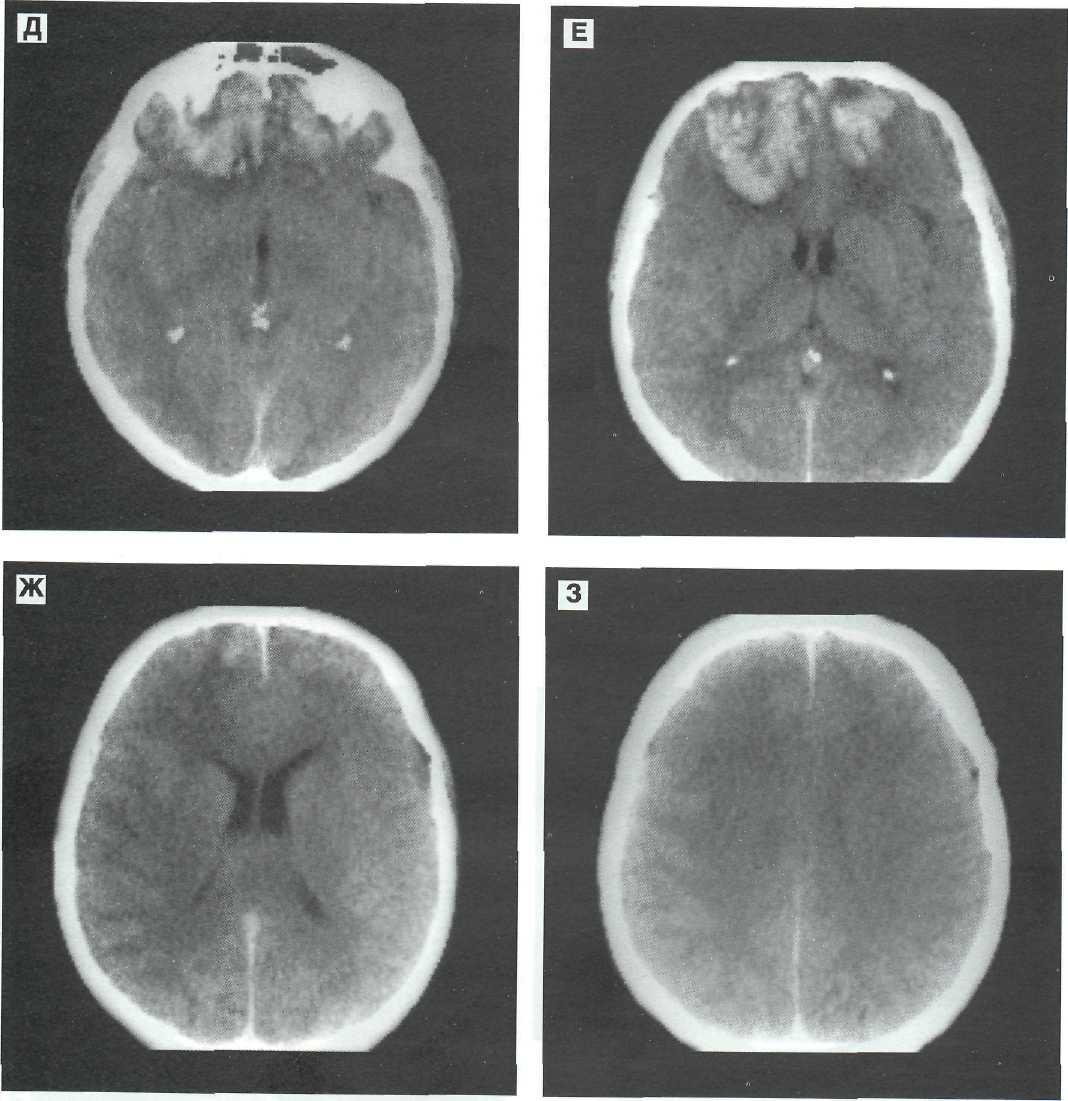 01
01 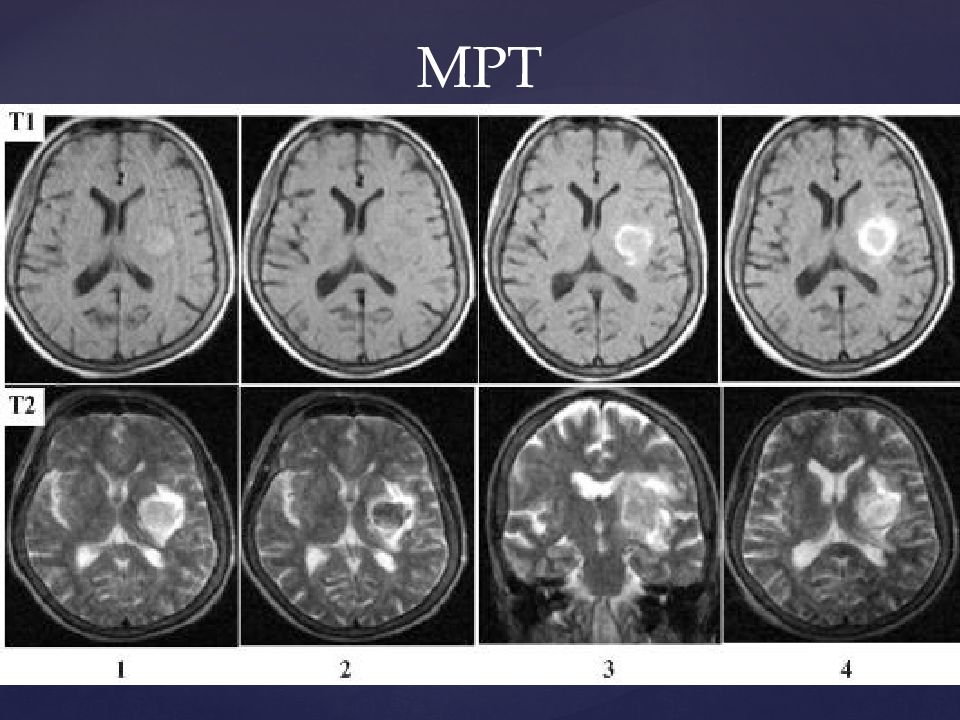 Не все гиперденсивные очаги на неусиленной КТ, проведенной сразу после АР, представляют собой кровоизлияние, это может быть связано либо с экстравазацией контраста, либо с кровоизлиянием в мозг [6, 8].Поэтому неврологам и нейрорадиологам необходимо выявить истинную природу гиперденсивных поражений, чтобы вовремя принять соответствующие меры, иначе это серьезно повлияет на прогноз пациентов.
Не все гиперденсивные очаги на неусиленной КТ, проведенной сразу после АР, представляют собой кровоизлияние, это может быть связано либо с экстравазацией контраста, либо с кровоизлиянием в мозг [6, 8].Поэтому неврологам и нейрорадиологам необходимо выявить истинную природу гиперденсивных поражений, чтобы вовремя принять соответствующие меры, иначе это серьезно повлияет на прогноз пациентов. 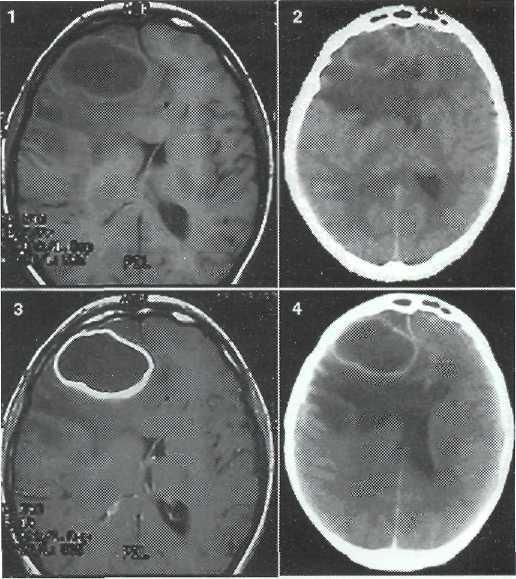 Время выведения контрастного вещества, введенного при реканализации, удлиняется из-за ишемии и гипоксии в зоне инфаркта головного мозга, что приводит к локальной задержке контрастного вещества [10].Во время интервенционной процедуры микрокатетер и микропроводник могут привести к повреждению интимы сосуда, что также является одной из частых причин экстравазации контраста [11, 12]. Проявления внутричерепных гиперденсивных поражений после КТ варьируют в зависимости от степени микрососудистого повреждения головного мозга. Когда ишемическое повреждение разрушает только барьер проницаемости эндотелиальных клеток, внутричерепные гиперденсивные очаги могут быть однократными контрастными веществами без кровоизлияний. Однако, когда ишемические инфаркты разрушают структурный барьер-базальную мембрану, гиперплотные поражения могут быть связаны с какой-либо формой кровоизлияния или смесью контраста и крови.Нарушение гематоэнцефалического барьера может быть необходимым условием геморрагической трансформации [11–13].
Время выведения контрастного вещества, введенного при реканализации, удлиняется из-за ишемии и гипоксии в зоне инфаркта головного мозга, что приводит к локальной задержке контрастного вещества [10].Во время интервенционной процедуры микрокатетер и микропроводник могут привести к повреждению интимы сосуда, что также является одной из частых причин экстравазации контраста [11, 12]. Проявления внутричерепных гиперденсивных поражений после КТ варьируют в зависимости от степени микрососудистого повреждения головного мозга. Когда ишемическое повреждение разрушает только барьер проницаемости эндотелиальных клеток, внутричерепные гиперденсивные очаги могут быть однократными контрастными веществами без кровоизлияний. Однако, когда ишемические инфаркты разрушают структурный барьер-базальную мембрану, гиперплотные поражения могут быть связаны с какой-либо формой кровоизлияния или смесью контраста и крови.Нарушение гематоэнцефалического барьера может быть необходимым условием геморрагической трансформации [11–13].

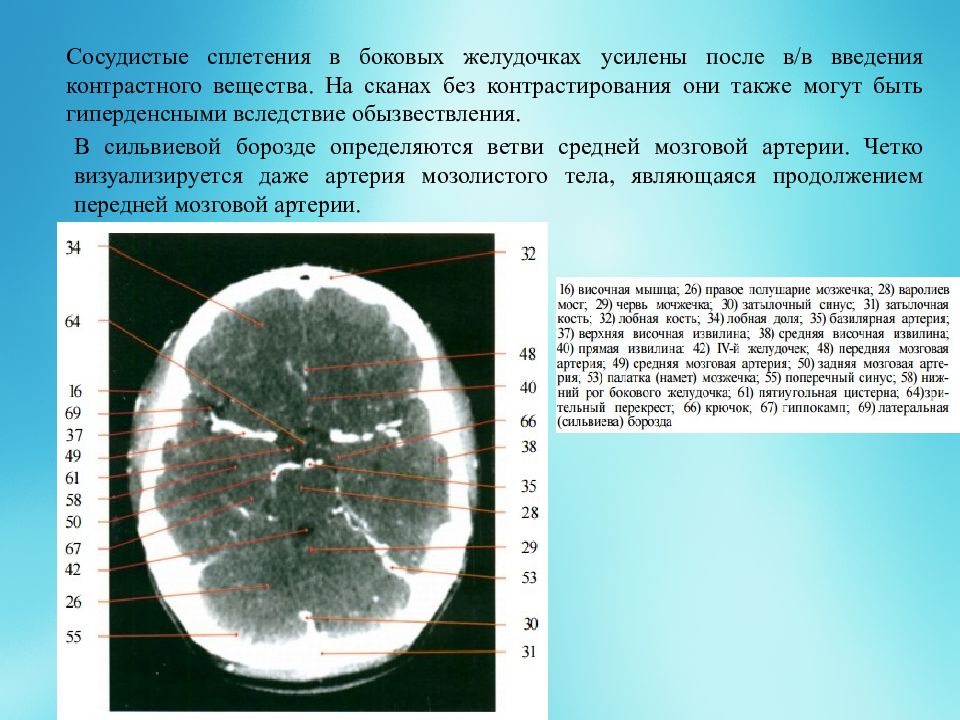 А его возникновение тесно связано с повреждением ГЭБ, реперфузионным повреждением зоны ишемии, применением микрокатетера, установлением коллатерального кровообращения и удлинением времени процедуры [18, 19], что является результатом сочетанного действия вышеперечисленных факторы [4].В данном исследовании у 30 (57,7%) пациентов в группе внутричерепных гиперденсивных поражений развилась ГТ после АР, в том числе у 23 (44,2%) пациентов с АИКГ и у 7 (13,5%) пациентов с ИСГК. Все 23 (44,2%) пациента с АИКГ имели гиперденсивное поражение II типа. Среди 7 пациентов с SICH у 2 были гиперденсивные поражения II типа и у 5 — III типа.
А его возникновение тесно связано с повреждением ГЭБ, реперфузионным повреждением зоны ишемии, применением микрокатетера, установлением коллатерального кровообращения и удлинением времени процедуры [18, 19], что является результатом сочетанного действия вышеперечисленных факторы [4].В данном исследовании у 30 (57,7%) пациентов в группе внутричерепных гиперденсивных поражений развилась ГТ после АР, в том числе у 23 (44,2%) пациентов с АИКГ и у 7 (13,5%) пациентов с ИСГК. Все 23 (44,2%) пациента с АИКГ имели гиперденсивное поражение II типа. Среди 7 пациентов с SICH у 2 были гиперденсивные поражения II типа и у 5 — III типа.  Поскольку SICH представляет собой серьезное микрососудистое повреждение с вовлечением базальной мембраны, отсутствие гиперденсивных поражений на КТ без контрастного усиления сразу после AR свидетельствует о том, что проницаемость и структурный барьер эндотелиальных клеток микрососудов не нарушены, что может быть надежным отрицательным предиктором SICH, в других Другими словами, заболеваемость SICH будет крайне низкой или вообще не возникнет.Касс-Хаут и др. [21] указали, что более длительное время процедуры является независимым предиктором SICH у пациентов, перенесших механическую тромбэктомию. Увеличение времени процедуры может быть связано с трудностями введения катетеров в заблокированные сосуды, что может быть связано с жесткостью артерий или другими сопутствующими заболеваниями [22]. Длительное время процедуры означает больше попыток реканализации окклюзированных сосудов. Вышеуказанные факторы могут значительно увеличить заболеваемость АГ [23, 24]. Длительное время процедуры было достоверно связано с более высокой частотой SICH даже у пациентов с успешной реканализацией [19].
Поскольку SICH представляет собой серьезное микрососудистое повреждение с вовлечением базальной мембраны, отсутствие гиперденсивных поражений на КТ без контрастного усиления сразу после AR свидетельствует о том, что проницаемость и структурный барьер эндотелиальных клеток микрососудов не нарушены, что может быть надежным отрицательным предиктором SICH, в других Другими словами, заболеваемость SICH будет крайне низкой или вообще не возникнет.Касс-Хаут и др. [21] указали, что более длительное время процедуры является независимым предиктором SICH у пациентов, перенесших механическую тромбэктомию. Увеличение времени процедуры может быть связано с трудностями введения катетеров в заблокированные сосуды, что может быть связано с жесткостью артерий или другими сопутствующими заболеваниями [22]. Длительное время процедуры означает больше попыток реканализации окклюзированных сосудов. Вышеуказанные факторы могут значительно увеличить заболеваемость АГ [23, 24]. Длительное время процедуры было достоверно связано с более высокой частотой SICH даже у пациентов с успешной реканализацией [19].
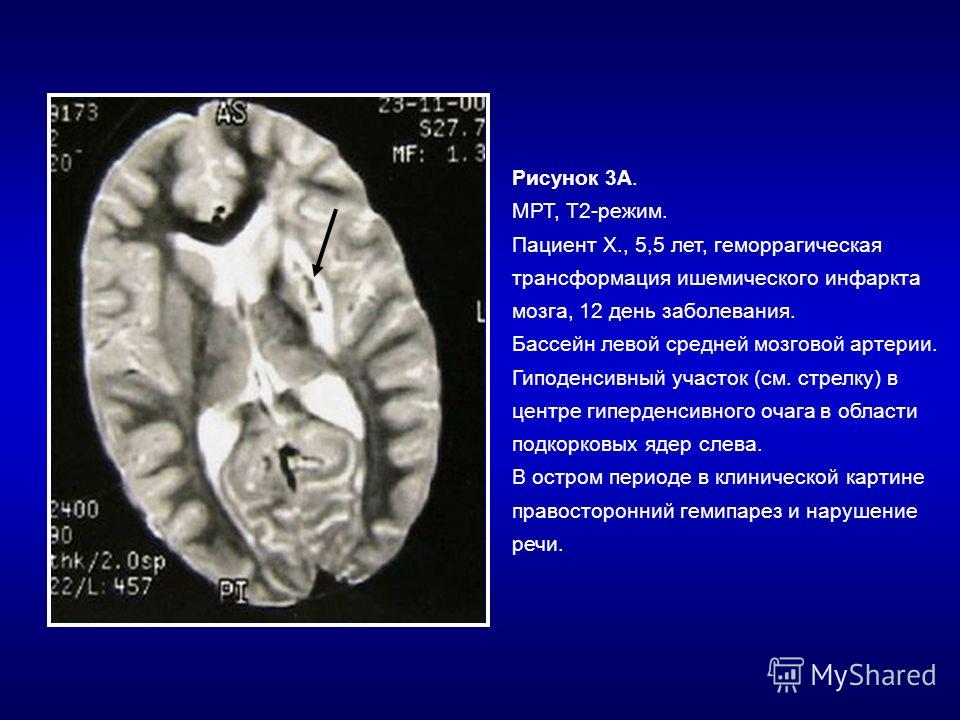 [14] и Jang et al. [6], а частота SICH была ниже, чем в результатах Nakano et al.[14] и Jang et al. [6]. Не было существенной разницы между отбором случаев и методами реконструкции сосудов, поэтому эта разница может быть связана с недостаточным размером выборки, разными поколениями устройств для тромбэктомии и временем процедуры. Связано ли это с другими факторами, остается для дальнейшего анализа с большей группой пациентов. Наши результаты показали, что ни у одного из пациентов без внутричерепных гиперденсивных поражений не развился SICH, что согласуется с исследованием Nakano et al.[14].
[14] и Jang et al. [6], а частота SICH была ниже, чем в результатах Nakano et al.[14] и Jang et al. [6]. Не было существенной разницы между отбором случаев и методами реконструкции сосудов, поэтому эта разница может быть связана с недостаточным размером выборки, разными поколениями устройств для тромбэктомии и временем процедуры. Связано ли это с другими факторами, остается для дальнейшего анализа с большей группой пациентов. Наши результаты показали, что ни у одного из пациентов без внутричерепных гиперденсивных поражений не развился SICH, что согласуется с исследованием Nakano et al.[14]. 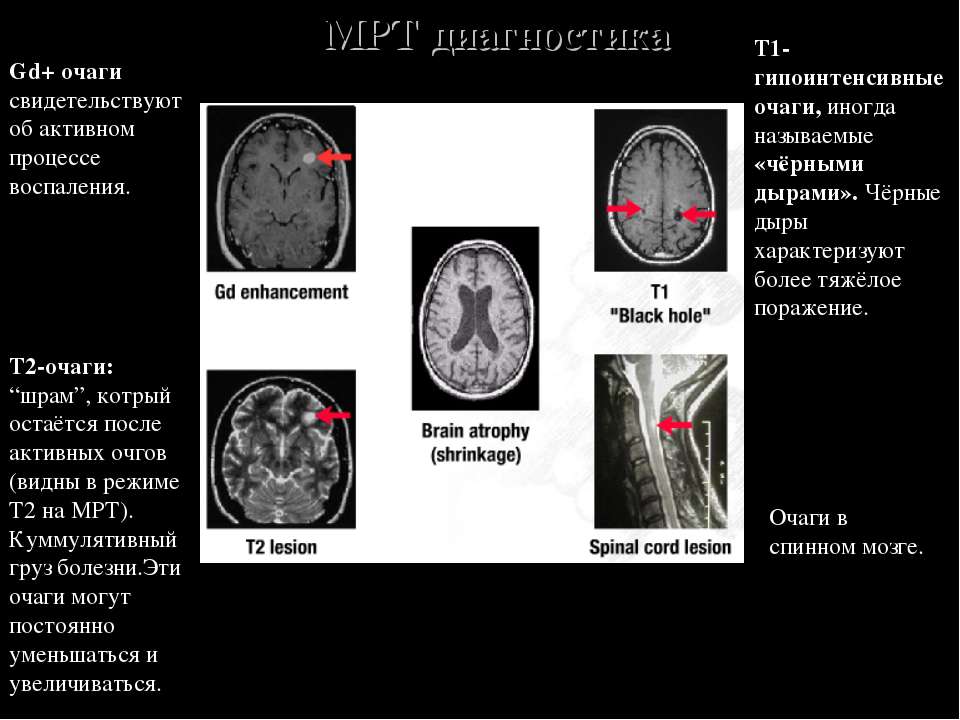 . Внутричерепные гиперденсивные поражения III типа (диффузные пятнистые поражения с масс-эффектом) неизменно развивались в SICH.Возникновение внутричерепных гиперденсивных поражений после АР имеет высокую чувствительность и отрицательную прогностическую ценность для прогноза церебральной ГТ, но специфичность и положительную прогностическую ценность невысокие, что согласуется с результатами исследований Kim и соавт. [25].
. Внутричерепные гиперденсивные поражения III типа (диффузные пятнистые поражения с масс-эффектом) неизменно развивались в SICH.Возникновение внутричерепных гиперденсивных поражений после АР имеет высокую чувствительность и отрицательную прогностическую ценность для прогноза церебральной ГТ, но специфичность и положительную прогностическую ценность невысокие, что согласуется с результатами исследований Kim и соавт. [25]. 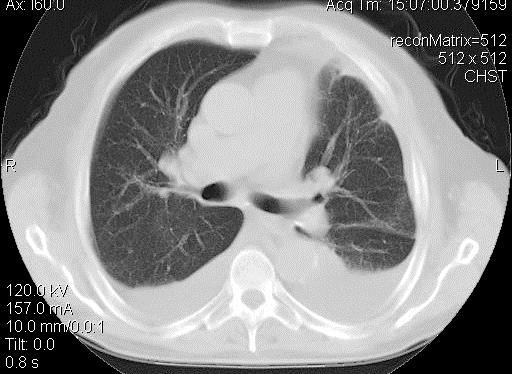
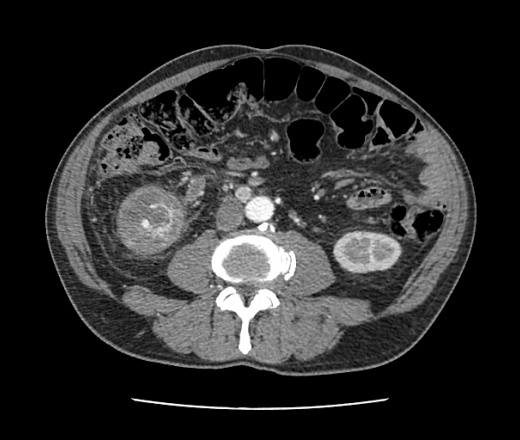
 Ė1v9Iѻ8XWr2w|’)peak,;
конечный поток
эндообъект
9 0 объект
>поток
2022-01-11T21:02:16-08:002005-08-19T18:02:43+05:302022-01-11T21:02:16-08:00application/pdfuuid:660d1ead-eea9-4c66-8945-7374e68ca17duuid: f541245e-5ee3-49f9-be39-60f940588f6c
конечный поток
эндообъект
10 0 объект
>поток
x+
Ė1v9Iѻ8XWr2w|’)peak,;
конечный поток
эндообъект
9 0 объект
>поток
2022-01-11T21:02:16-08:002005-08-19T18:02:43+05:302022-01-11T21:02:16-08:00application/pdfuuid:660d1ead-eea9-4c66-8945-7374e68ca17duuid: f541245e-5ee3-49f9-be39-60f940588f6c
конечный поток
эндообъект
10 0 объект
>поток
x+  Регаладо, доктор медицины Клинический ассистент-профессор радиологии, кафедра сосудистой и интервенционной радиологии, Системы здравоохранения Университета Норт-Шор
Регаладо, доктор медицины Клинический ассистент-профессор радиологии, кафедра сосудистой и интервенционной радиологии, Системы здравоохранения Университета Норт-Шор 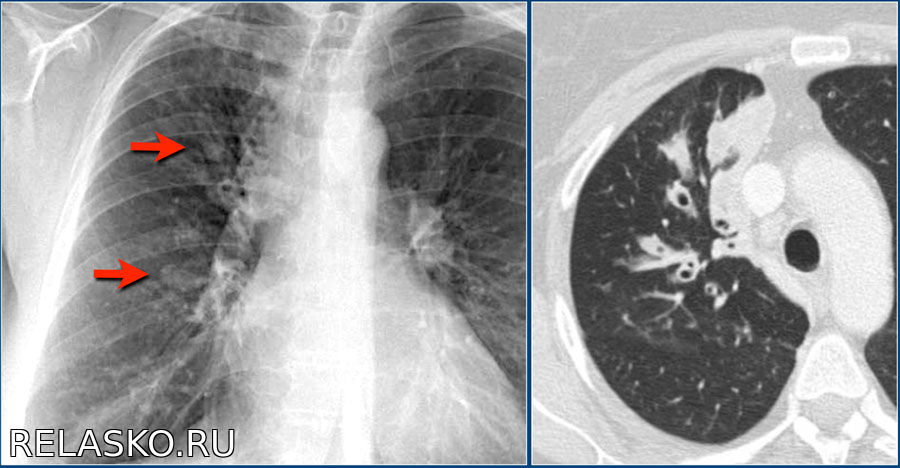

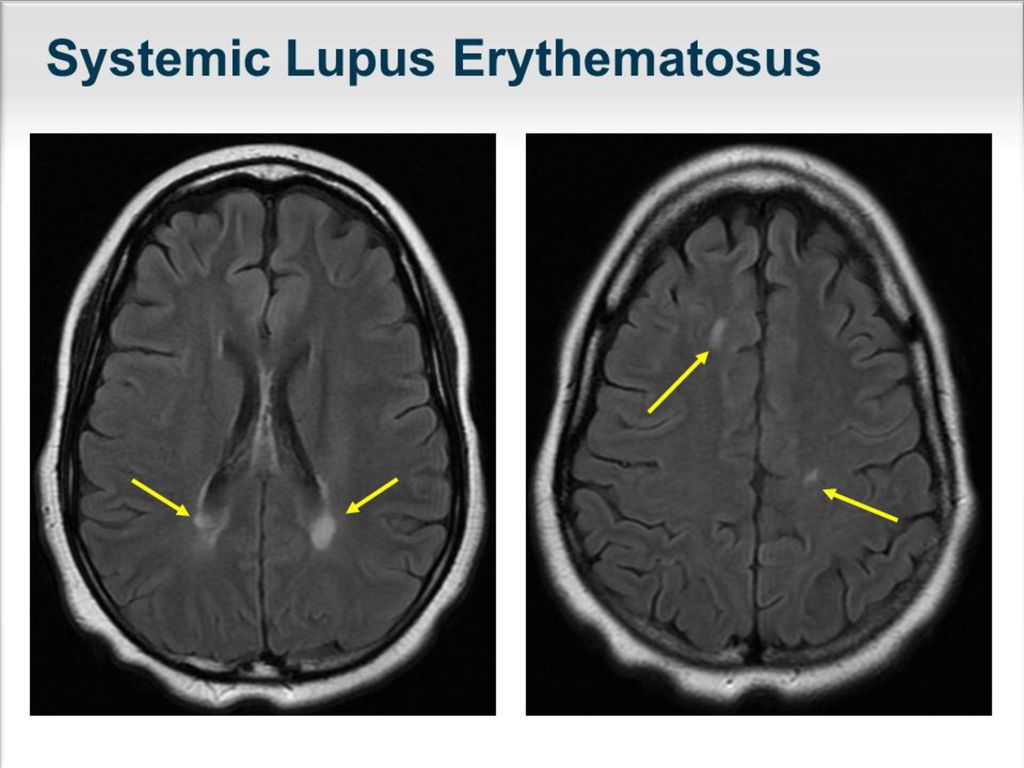 Ему была проведена КТ головного мозга без усиления, которая показала возможный тромб в основной артерии (рис. 1). Начат прием аспирина 300 мг 1 раз в сутки.На следующий день его левосторонние симптомы ухудшились, и у него началась дизартрия. Ему была проведена МРТ головного мозга, включая ангиографию, которая продемонстрировала дефект наполнения основной артерии, соответствующий тромбу (рис. 2), однако геморрагических очагов не было. Ему начали вводить гепарин внутривенно. В течение нескольких дней его симптомы исчезли, и он был выписан на клопидогреле.
Ему была проведена КТ головного мозга без усиления, которая показала возможный тромб в основной артерии (рис. 1). Начат прием аспирина 300 мг 1 раз в сутки.На следующий день его левосторонние симптомы ухудшились, и у него началась дизартрия. Ему была проведена МРТ головного мозга, включая ангиографию, которая продемонстрировала дефект наполнения основной артерии, соответствующий тромбу (рис. 2), однако геморрагических очагов не было. Ему начали вводить гепарин внутривенно. В течение нескольких дней его симптомы исчезли, и он был выписан на клопидогреле.  результат артерио-артериальной или кардиоэмболии, диссекции с антероградным распространением эмбола/окклюзии истинного просвета или тромбоза in situ.Точная диагностика БЖТ основывается на МР- или КТ-ангиографии, поскольку гиперплотная базилярная артерия на КТ без усиления не обладает достаточной чувствительностью или специфичностью.
результат артерио-артериальной или кардиоэмболии, диссекции с антероградным распространением эмбола/окклюзии истинного просвета или тромбоза in situ.Точная диагностика БЖТ основывается на МР- или КТ-ангиографии, поскольку гиперплотная базилярная артерия на КТ без усиления не обладает достаточной чувствительностью или специфичностью.


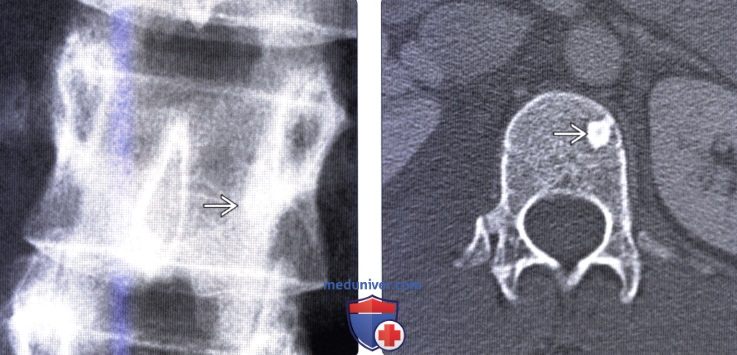 Insights Imaging 3 (5): 451–474. https://doi.org/10.1007/s13244-012-0179-7
Insights Imaging 3 (5): 451–474. https://doi.org/10.1007/s13244-012-0179-7 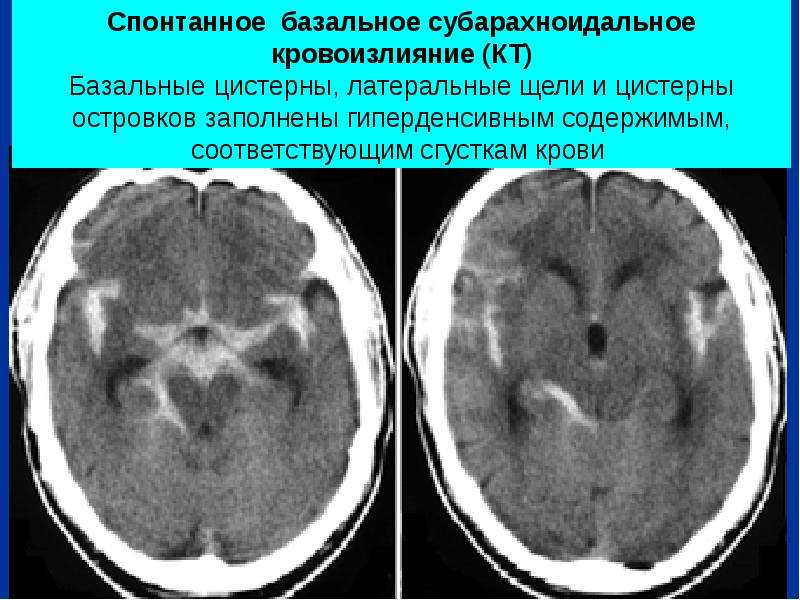 Радиология 277:413–423
Радиология 277:413–423 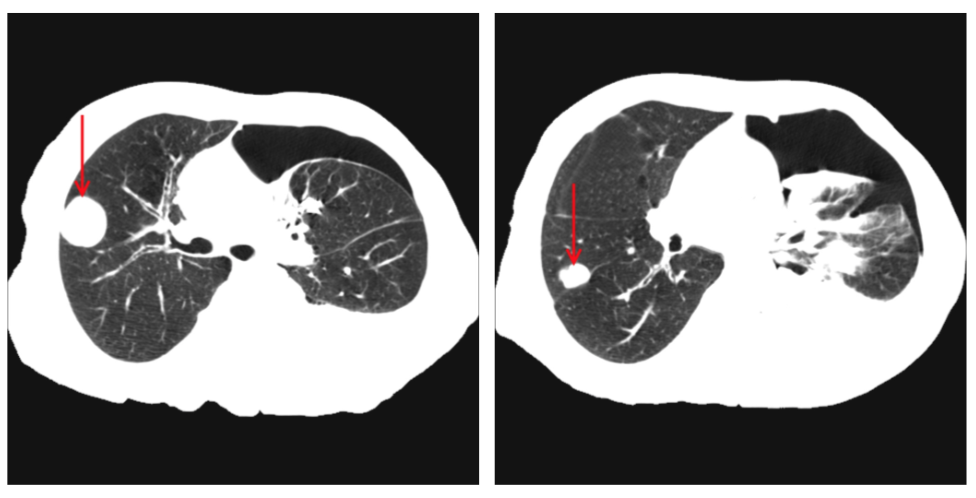
 AJR Am J Roentgenol 201:W603–W611
AJR Am J Roentgenol 201:W603–W611  Визуализация органов брюшной полости 38:793–801
Визуализация органов брюшной полости 38:793–801  Am J Surg Pathol 23:1441–1454
Am J Surg Pathol 23:1441–1454 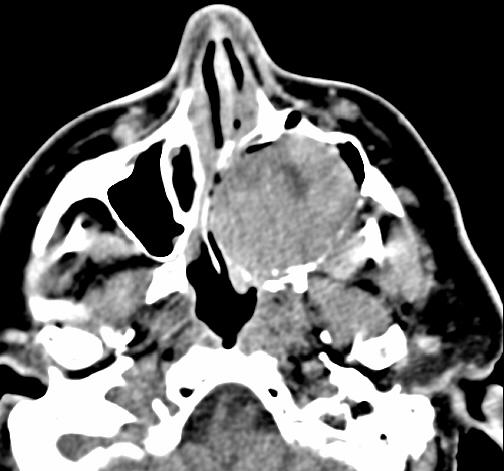 Abdom Radiol (NY) 43:2075–2096
Abdom Radiol (NY) 43:2075–2096  Am J Surg Pathol 36: 1691–1699
Am J Surg Pathol 36: 1691–1699 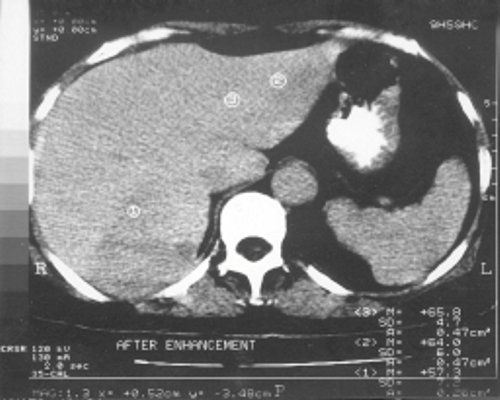 AJR Am J Roentgenol 199:26–34
AJR Am J Roentgenol 199:26–34 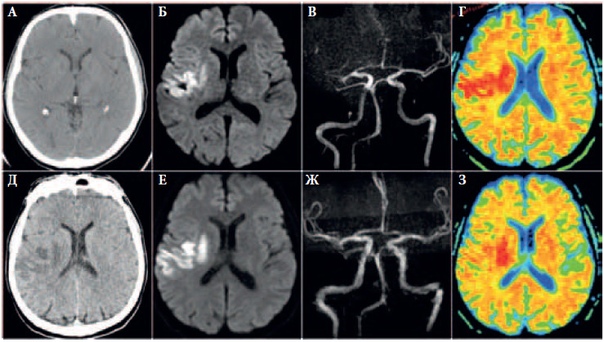

 Радиология 277:104–113
Радиология 277:104–113  AJR Am J Roentgenol 203:W408–W414
AJR Am J Roentgenol 203:W408–W414 