Кардиты у детей классификация: Неревматические кардиты у детей. Что такое Неревматические кардиты у детей?
56, 113. Врожденные кардиты. Клиника, диагностика, лечение.Приобретенные кардиты. Классификация, диагностика, клиника, лечение.
Врождённые кардиты могут манифестировать сразу после рождения или в первые 6 мес жизни, реже — на 2-3-м году.
Ранний врождённый
кардит проявляется малой массой тела
при рождении или плохой её прибавкой в
последующем, быстрой утомляемостью при
кормлении, беспричинным беспокойством,
потливостью, бледностью. Характерны
кардиомегалия, «сердечный горб», глухие
сердечные тоны при аускультации,
прогрессирующая сердечная недостаточность
(нередко тотальная с преобладанием
левожелудочковой), рефрактерная к
лечению. Часто возникают одышка в покое,
кашель, афония, умеренный цианоз (иногда
с малиновым оттенком), разнокалиберные
влажные и свистящие хрипы в лёгких,
увеличение печени, отёки или пастозность
тканей. Аритмии (за исключением тахикардии)
возникают редко. Появление систолического
шума может быть связано с относительной
или органической недостаточностью
митрального клапана, но чаще шум
отсутствует.
На рентгенограмме сердце шаровидной или овоидной, а при фиброэластозе — трапециевидной формы. На ЭКГ выявляют ригидный ритм, признаки гипертрофии левого желудочка за счёт увеличения толщины миокарда вследствие инфильтрации, повреждение его субэндокардиальных отделов. При фиброэластозе появляются признаки перегрузки обоих желудочков, глубокие зубцы Q во II и III стандартных отведениях, aVF, V5, V6. При ЭхоКГ помимо кардиомегалии и дилатации полостей сердца выявляют снижение сократительной и особенно релаксационной функции миокарда левого желудочка, повреждение клапанов, чаще митрального, лёгочную гипертензию.
Поздний врождённый
кардит характеризуется умеренной
кардиомегалией, различными нарушениями
ритма и проводимости вплоть до полной
поперечной блокады сердца и трепетания
предсердий, громкими сердечными тонами,
менее выраженной (по сравнению с ранним
врождённым кардитом) сердечной
недостаточностью. Часто выявляют
признаки поражения двух или трёх оболочек
сердца. У некоторых больных возникают
приступы внезапного беспокойства,
одышки, тахикардии с усилением цианоза,
судорог, что отражает сочетанное
поражение сердца и ЦНС, обусловленное
предшествующей инфекцией, особенно
вызванной вирусами Коксаки.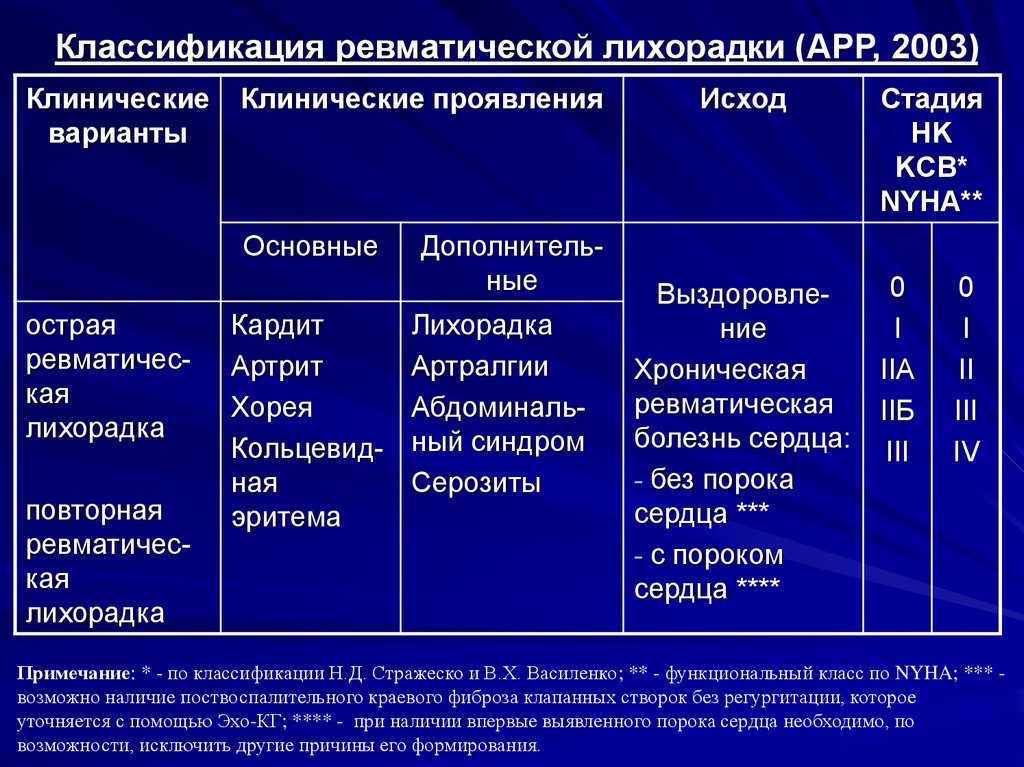
Лечение кардитов включает два этапа: стационарный (острый период или обострение) и поликлинический, или санаторный (период поддерживающего лечения). Необходимо проведение мероприятий по устранению причины заболевания (воздействие лекарственными препаратами на вирус, воздействие на иммунную систему организма, борьба с сердечно-сосудистой недостаточностью). Проводят мероприятия общего плана и медикаментозное лечение. К мероприятиям общего плана относится соблюдение двигательного, пищевого, питьевого режима.
Приобретённые кардиты
Приобретённые кардиты могут возникать в любом возрасте, но чаще у детей первых 3 лет жизни.
Острый кардит
На
фоне текущей или вскоре после перенесённой
инфекции появляются вялость,
раздражительность, бледность, навязчивый
кашель, нарастающий при перемене
положения тела; возможны приступы
цианоза, тошнота, рвота, боли в животе,
энцефалитические реакции. Постепенно
или достаточно остро развиваются
симптомы левожелудочковой недостаточности
(одышка, тахикардия, застойные хрипы в
лёгких).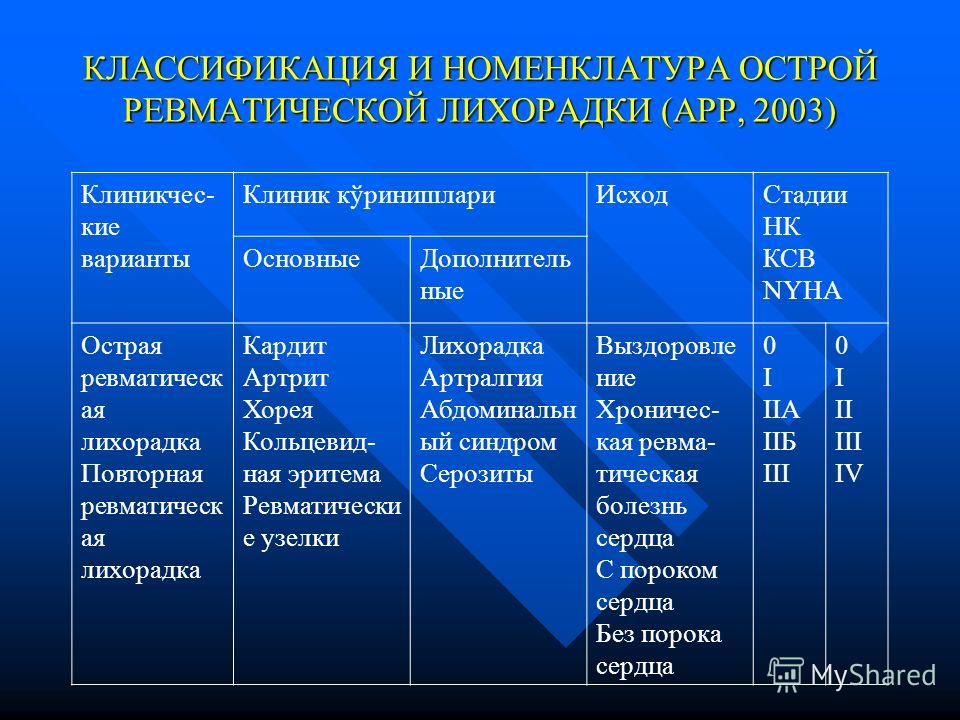 Объективно определяют пульс
слабого наполнения, ослабление
верхушечного толчка, увеличение размеров
сердца, преимущественно влево, ослабление
I тона, ритм галопа, разнообразные
аритмии. Систолический шум отсутствует,
но возможен при развитии недостаточности
(относительной или органической)
митрального клапана.
Объективно определяют пульс
слабого наполнения, ослабление
верхушечного толчка, увеличение размеров
сердца, преимущественно влево, ослабление
I тона, ритм галопа, разнообразные
аритмии. Систолический шум отсутствует,
но возможен при развитии недостаточности
(относительной или органической)
митрального клапана.
Рентгенологически
выявляют увеличение размеров сердца
различной выраженности, венозный застой
в лёгких, снижение амплитуды
систоло-диастолических колебаний,
иногда — увеличение вилочковой железы.
На ЭКГ обнаруживают снижение вольтажа
комплекса QRS, признаки перегрузки левого
или обоих желудочков, различные нарушения
ритма и проводимости (синусовая тахи-
или брадиаритмия, экстрасистолия,
атриовентрикулярные и внутрижелудочковые
блокады, смещение сегмента ST, сглаженный
или отрицательный зубец Т. Возможны
инфарктоподобные изменения и ЭКГ-признаки
сопутствующего перикардита. На ЭхоКГ
определяют дилатацию правого желудочка
и левого предсердия, гипокинезию
межжелудочковой перегородки и задней
стенки левого желудочка, снижение
фракции выброса, увеличение
конечно-систолического и
конечно-диастолического размеров левого
желудочка, признаки недостаточности
митрального клапана, выпот в полости
перикарда.
У детей раннего возраста заболевание протекает тяжело, с выраженными клиническими проявлениями и прогрессированием сердечной недостаточности. У детей старшего возраста кардиты обычно протекают в лёгкой или среднетяжёлой форме, с менее яркими симптомами заболевания, редкой и менее выраженной декомпенсацией, но часто сопровождаются разнообразными нарушениями ритма и проводимости, нередко определяющими клиническую картину.
На фоне лечения острого кардита постепенно исчезают клинические симптомы. Изменения на ЭКГ сохраняются более длительно. Обратное развитие процесса наступает через 3 мес от его начала; кроме того, кардит может принимать подострое или хроническое течение.
Подострый кардит
Подострый
кардит чаще наблюдают у детей в возрасте
от 2 до 5 лет. Он может развиться либо
после острого кардита, либо самостоятельно
(первично подострый кардит) спустя
продолжительное время после ОРВИ,
проявляясь бледностью, повышенной
утомляемостью, раздражительностью,
снижением аппетита, дистрофией. Исподволь
(иногда внезапно) развивается сердечная
недостаточность, или случайно обнаруживают
аритмии, увеличение размеров сердца,
систолический шум.
Исподволь
(иногда внезапно) развивается сердечная
недостаточность, или случайно обнаруживают
аритмии, увеличение размеров сердца,
систолический шум.
Симптомы подострого кардита аналогичны таковым при остром его варианте. Возможно формирование «сердечного горба», сердечные тоны громкие, выражен акцент II тона над лёгочной артерией. На ЭКГ — признаки перегрузки не только желудочков, но и предсердий, стойкого нарушения ритма и проводимости. Сердечная недостаточность трудно поддаётся лечению. Эти изменения связаны с длительностью процесса, развитием компенсаторной гипертрофии миокарда левого желудочка, одновременным снижением его сократительной функции, начальными проявлениями лёгочной гипертензии. Обратное развитие процесса происходит через 12-18 мес, либо он приобретает хроническое течение.
Хронический кардит
Хронический
кардит развивается чаще у детей старше
7 лет либо в первично хроническом
варианте, либо как исход острого или
подострого кардита. Клиническая картина
хронического кардита отличается
многообразием, что связано, в частности,
с большой продолжительностью заболевания
и разнообразным соотношением
воспалительных, склеротических и
гипертрофических изменений в сердце.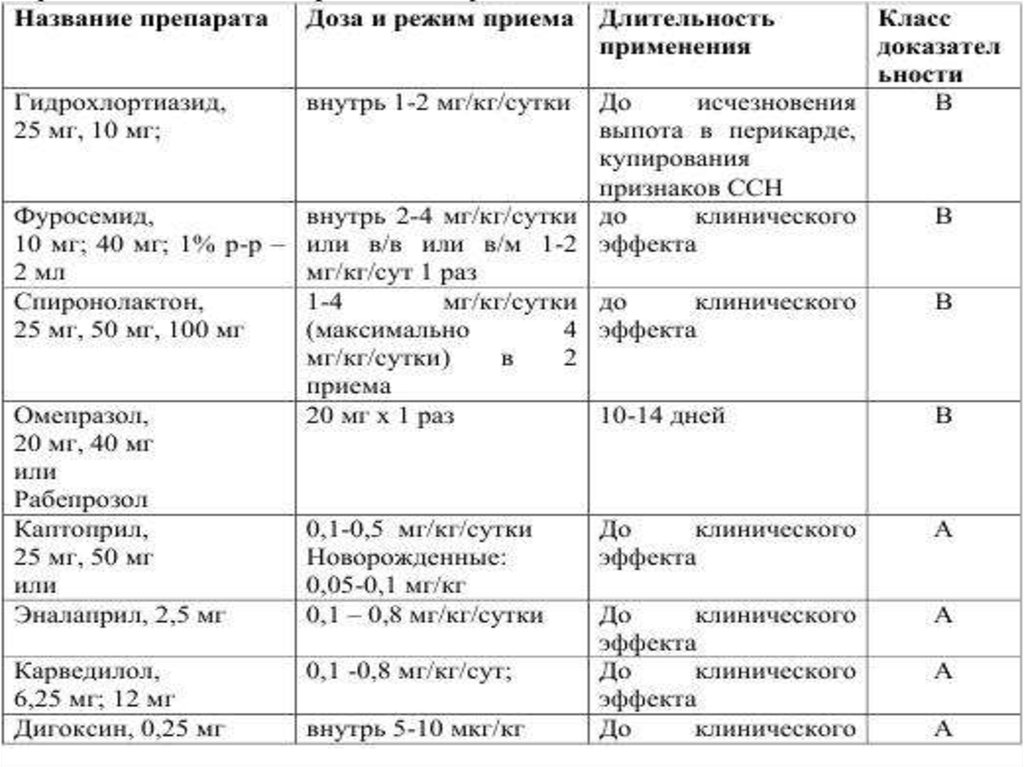
Первично
хроническому варианту неревматического
кардита свойственно длительное
малосимптомное течение с преобладанием
экстракардиальных проявлений (отставание
в физическом развитии, слабость,
повышенная утомляемость, снижение
аппетита, потливость, бледность,
рецидивирующие пневмонии). Дети нередко
ведут обычный образ жизни, могут
заниматься спортом. Периодически
возникают головокружение, одышка, боли
в области сердца, сердцебиение, навязчивый
кашель, тошнота, рвота, боли в правом
подреберье, обусловленные сердечной
недостаточностью. Возможно острое
развитие приступов бледности, беспокойства,
потери сознания, судорог, связанных с
сердечной декомпенсацией или
воспалительными изменениями в ЦНС,
сопутствующими кардиту. Нередко
предположение о сердечной патологии
возникает лишь при манифестации сердечной
декомпенсации или обнаружении
кардиомегалии, стойких аритмий,
систолического шума, гепатомегалии во
время профилактического осмотра либо
при осмотре в связи с перенесённым
интеркуррентным заболеванием.
Лечение при неревматическом кардите зависит от его этиологии, варианта, периода заболевания, наличия или отсутствия недостаточности кровообращения. Лечение проводят в два этапа.
На первом этапе (стационар) ограничивают двигательную активность, назначают диету, обогащенную витаминами и солями калия, налаживают питьевой режим. Постельный режим на 2-4 нед назначают при остром или подостром кардитах, а также при обострении хронического. Расширение двигательного режима необходимо проводить постепенно, под контролем функционального состояния сердечно-сосудистой системы и динамики ЭКГ.
 Обязательны занятия ЛФК. Лекарственная
терапия включает следующие препараты.
Обязательны занятия ЛФК. Лекарственная
терапия включает следующие препараты.Нестероидные противовоспалительные средства (НПВС) — индометацин, диклофенак и другие в течение 1 — 1,5 мес.
При тяжёлом течении, распространённом процессе, высокой степени активности, преимущественном поражении проводящей системы сердца — глюкокортикоиды (преднизолон в дозе 0,5-0,75 мг/кг/сут).
При затяжном и хроническом течении кардита — производные аминохинолина (гидроксихлорохин, хлорохин).
При сердечной недостаточности — сердечные гликозиды, ингибиторы АПФ, диуретики, вазодилататоры и др.
Проводят обязательную коррекцию метаболических нарушений в миокарде, микроциркуляторных расстройств, по показаниям назначают антикоагулянты, антиагреганты, антиаритмические препараты.
При установленном этиологическом факторе (вирусы, бактериальная флора) — противовирусные (Ig, интерферон) и антибактериальные препараты, иммуностимуляторы.

На втором этапе (после выписки из стационара) ребёнок нуждается в продолжении лечения и проведении реабилитационных мероприятий в условиях местного кардиоревматологического санатория. В последующем детей с кардитами наблюдает кардиоревматолог по месту жительства. Диспансеризацию больных, перенёсших острый или подострый кардит, осуществляют до полного выздоровления (в среднем 2-3 года), а при врождённых и хронических вариантах — постоянно. Регулярность контроля, объём исследований (рентгенография, ЭКГ, ЭхоКГ) определяют индивидуально. В период наблюдения в поликлинике при необходимости проводят коррекцию лечения, назначают препараты, стимулирующие обменные процессы, санируют очаги хронической инфекции. Профилактические прививки можно проводить после перенесённого острого или подострого кардита не ранее чем через 3 года; при наличии хронического процесса вакцинация противопоказана.
причины, симптомы, классификация, диагноз, лечение и профилактика заболевания
Такое понятие, как кардит, довольно недавно было введено в педиатрическую клиническую практику. Под ним понимается одновременное поражение сердечных оболочек – пери-, эндо- и миокарда.
Под ним понимается одновременное поражение сердечных оболочек – пери-, эндо- и миокарда.
Для обозначения воспаления миокарда, вызванного бактериальными и вирусными агентами, до недавнего времени использовался термин «миокардит».
Но как было показано в многочисленных новейших исследованиях, у детей с бактериальными и вирусными миокардитами в болезнетворный процесс почти во всех случаях включаются пери- и эндокард. Именно по этой причине использование понятия «миокардит» не отражает полностью суть патологического процесса. На основании этого было предложено пользоваться в педиатрии таким термином, как «кардит».
Чтобы обозначить различия кардитов, которые имеют нестрептококковое происхождение, до недавнего времени применяли понятие «инфекционно-аллергический». Но с позиции настоящего положения вещей в патогенезе болезни такой термин нельзя считать верным. Сейчас нестрептококковый кардит в педиатрии обозначается как неревматический.
Описание данной патологии
У детей неревматические кардиты представляют собой воспалительные процессы в одной либо нескольких сердечных оболочках, не обусловленные ревматической либо прочей системной патологией. Протекание этого заболевания сопровождается одышкой, тахикардией, цианозом, недостаточностью сердца, аритмией, отставанием ребенка в физическом развитии. Во время диагностики у детей берутся в расчет лабораторные, клинические, рентгенологические и электрокардиографические сведения. В лечении патологии в педиатрии применяются сердечные гликозиды, гормоны, НВПС, метаболические, антимикробные, мочегонные и противовирусные лекарственные средства.
Протекание этого заболевания сопровождается одышкой, тахикардией, цианозом, недостаточностью сердца, аритмией, отставанием ребенка в физическом развитии. Во время диагностики у детей берутся в расчет лабораторные, клинические, рентгенологические и электрокардиографические сведения. В лечении патологии в педиатрии применяются сердечные гликозиды, гормоны, НВПС, метаболические, антимикробные, мочегонные и противовирусные лекарственные средства.
Развитие болезни в педиатрии
У детей неревматические кардиты (по МКБ 10 — I51.8) являются группой воспалительных процессов в сердце, главным образом инфекционно-аллергического происхождения. Целесообразность классификации их в педиатрии обусловлена как изолированным, так и во многих случаях сочетанным поражением двух и трех сердечных оболочек у маленьких пациентов. В детской кардиологии в числе неревматических кардитов встречаются эндо-, пери- и миокардиты, а также панкардиты и миоперикардиты. Настоящая распространенность данной патологии среди детского населения точно не известна; сведения аутопсии говорят о том, что заболевание диагностируется у 3-9% пациентов. Выявляются неревматические кардиты у детей любой возрастной категории, но среди них подавляющее количество пациентов раннего возраста, в основном мужского пола.
Выявляются неревматические кардиты у детей любой возрастной категории, но среди них подавляющее количество пациентов раннего возраста, в основном мужского пола.
Причины данного заболевания
У ребенка недуг может быть вызван аллергоиммунологическими или инфекционными факторами. В числе инфекционных агентов особенно сильными являются вирусы (Коксаки В и А, ЕСНО, вирусы гриппов типов В или А, аденовирусы), бактерии (стафило- и стрептококки), грибы, риккетсии, ассоциированная флора.
Врожденный неревматический кардит у детей возникает по причине внутриутробных инфекций, которые влияют на плод. Бактериальные кардиты часто представляют собой осложнение сепсиса, назофарингеальной инфекции, дифтерии, гематогенного остеомиелита и сальмонеллеза.
Аллергоиммунологические кардиты
Аллергоиммунологические кардиты способны развиваться в качестве следствия вакцинации, приема медикаментозных средств и введения пациенту сывороток. Зачастую отмечается инфекционно-аллергическое происхождение поражения сердца. У примерно 10% маленьких пациентов этиология неревматического кардита остается неизвестной.
У примерно 10% маленьких пациентов этиология неревматического кардита остается неизвестной.
Предрасполагающие факторы к развитию болезни
Предрасполагающими факторами, из-за которых усиливается вирусно-бактериальная микрофлора, а также восприимчивость к аллергенам и токсинам, происходят изменения иммунологической реактивности, могут становиться инфекции, перенесенные ребенком, интоксикации, физические и психоэмоциональные перегрузки, переохлаждения, предшествующие оперативные вмешательства на сосудах и сердце, тимомегалия. У некоторых детей с такой патологией выявляются наследственные дефекты иммунной толерантности.
Классификация неревматических кардитов у детей
В зависимости от происхождения, таким образом, различаются идиопатические, вирусные, аллергические, бактериальные, грибковые, паразитарные кардиты у маленьких пациентов. У инфекционно-аллергического кардита существует такая разновидность, как миокардит Абрамова-Фидлера.
Учитывая временной фактор, кардиты подразделяют на врожденные (могут быть ранними и поздними), а также приобретенные. Течение патологии по продолжительности может быть хроническим (свыше 18-ти месяцев), подострым (не более 18-ти месяцев) и острым (не более трех месяцев). Заболевание по степени тяжести может быть легким, тяжелым и среднетяжелым. Это наиболее распространенная классификация неревматических кардитов у детей.
Течение патологии по продолжительности может быть хроническим (свыше 18-ти месяцев), подострым (не более 18-ти месяцев) и острым (не более трех месяцев). Заболевание по степени тяжести может быть легким, тяжелым и среднетяжелым. Это наиболее распространенная классификация неревматических кардитов у детей.
Кардиты врожденные: симптомы
Врожденный ранний кардит чаще всего заявляет о себе сразу после рождения либо в первые полгода жизни ребенка. Малыш рождается с гипотрофией умеренного типа, у него с первых дней отмечаются быстрая утомляемость и вялость при кормлении, периоральный цианоз и бледность покровов кожи, потливость, беспокойство без причины. Одышка и тахикардия в состоянии покоя усиливаются еще больше при плаче, сосании, купании, дефекации и пеленании. У детей с неревматическими врожденными кардитами отмечаются заметные отставания в физическом развитии и наборе веса. Уже в первые месяцы жизни у малышей отмечаются сердечный горб, кардиомегалия, отеки, гепатомегалия, недостаточность сердца, рефрактерность к терапии.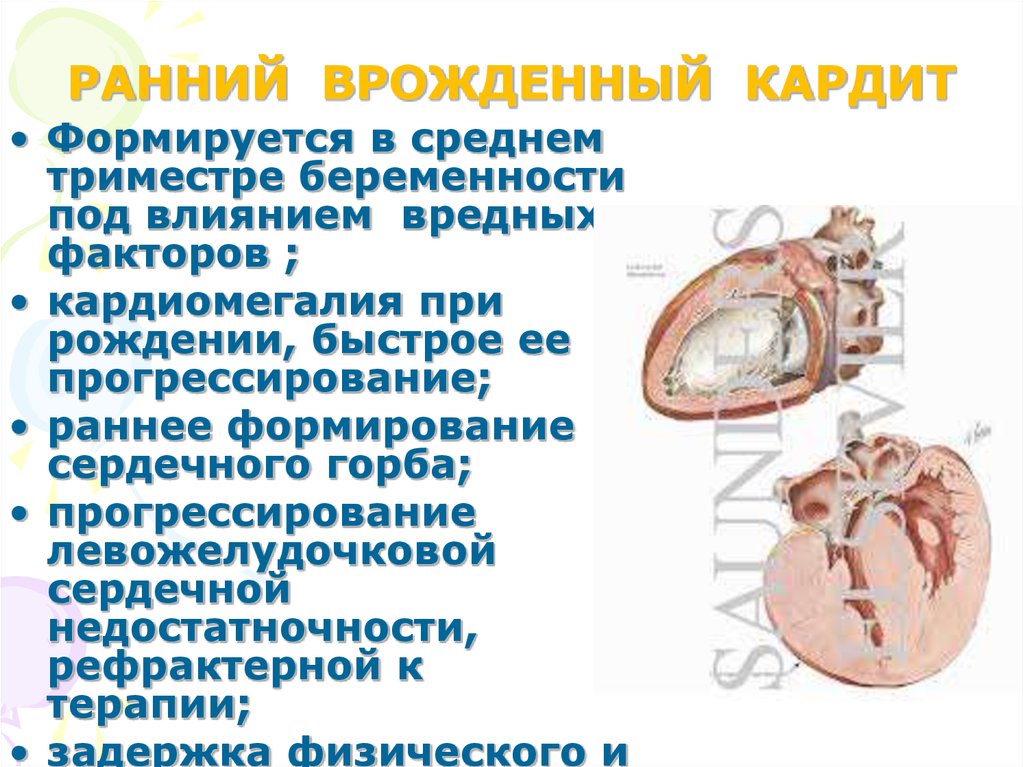
Клиника врожденного позднего неревматического кардита в педиатрии получает развитие на 2-3-ем году жизни. Зачастую поражает две либо три сердечные оболочки. Симптомы сердечной недостаточности и кардиомегалии получают выражение в меньшей степени в сравнении с кардитом ранним, но в клинической картине особо сильные нарушения проводимости и ритма (полная сердечная атриовентрикулярная блокада, трепетания предсердий и т.д.). Если у ребенка имеется судорожный синдром, это говорит об инфекционном поражении центральной нервной системы.
Кардиты приобретенные
Неревматические кардиты у детей особенно часто развиваются в раннем возрасте на фоне инфекционного процесса. Среди неспецифических признаков отмечаются раздражительность, слабость, приступы цианоза, навязчивый кашель, энцефалитические и диспепсические реакции. Постепенно или остро появляется недостаточность левого желудочка, характеризующаяся застойными хрипами и одышкой в легких. Клиническая картина детского неревматического кардита обычно характеризуется различными дефектами проводимости и ритма (синусовая брадикардия или тахикардия, атриовентрикулярные и внутрижелудочковые блокады, экстрасистолия).
Подострый кардит — чем он характеризуется?
Подострый кардит отличается сильной утомляемостью, аритмией, бледностью, недостаточностью деятельности сердца. Неревматический хронический кардит преимущественно отмечается у школьников, протекает с малой симптоматикой, в основном с экстракардиальными проявлениями (утомляемостью, слабостью, отставаниями физического развития, потливостью, болями в животе, тошнотой, сухим навязчивым кашлем). Очень трудно распознать хронический кардит. Нередко дети безрезультатно и долго лечатся у педиатра с такими диагнозами, как гепатит, пневмония и хронический бронхит.
Диагностика данного заболевания
Диагностика неревматического кардита в педиатрии требует обязательного присутствия детского кардиолога. Во время сбора истории болезни важно установить связь проявления болезни с предшествующими инфекциями и прочими провоцирующими факторами.
Диагноз неревматический кардит может быть установлен с помощью ряда клинико-инструментальных сведений. Электрокардиография не показывает патогномоничных симптомов: у детей обычно определяются долгое время сохраняющиеся дефекты сердечного ритма; блокады ножек пучка Гиса, АВ-блокады, симптомы гипертрофии левых сердечных отделов.
Электрокардиография не показывает патогномоничных симптомов: у детей обычно определяются долгое время сохраняющиеся дефекты сердечного ритма; блокады ножек пучка Гиса, АВ-блокады, симптомы гипертрофии левых сердечных отделов.
При рентгенографии грудной клетки определяются кардиомегалия, усиление рисунка легких из-за венозного застоя, изменение формы тени сердца, симптомы легочного интерстициального застоя.
При неревматическом кардите на эхокардиограмме можно выявить дилатацию сердечных полостей, уменьшение сократительной активности миокарда левого желудочка, а также фракции выброса.
Во время иммунологического кровяного анализа обнаруживается повышение иммуноглобулинов, рост титров вирусных антител. Самые точные диагностические данные можно получить посредством эндомиокардиальной биопсии мышцы сердца.
Неревматические врожденные кардиты у детей нужно отличать от врожденных пороков сердца (в первую очередь синдрома Бланда-Уайта-Гарланда, аномалии Эбштейна, открытого атривентрикулярного канала), перинатальной гипоксии.
Приобретенные кардиты нуждаются в разграничении с кардиомиопатией, сердечными опухолями, ревматизмом, пролапсом митрального клапана, аритмиями иного генеза, констриктивным перикардитом.
Лечение неревматических кардитов
Лечение патологии включает в себя стационарный и амбулаторное реабилитационный этапы. Во время госпитализации двигательная активность пациента ограничивается – постельный режим требуется соблюдать на протяжении 2-4-х недель. В основе рациона лежит диета с усиленным содержанием витаминов и солей калия. Ребенку назначаются занятия ЛФК в сопровождении инструктора.
Лечение неревматического кардита вирусной этиологии включает в себя ингибиторы АПФ, НПВС, антиаритмические средства, глюкокортикостероиды, антикоагулянты, гликозиды, антиагреганты, сердечные диуретики, средства метаболического действия и т.п. Если этиологический фактор заболевания известен, пациенту назначается необходимая этиотропная терапия (антибиотики, интерфероны, иммуноглобулины).
Что происходит на амбулаторной стадии?
На амбулаторной стадии лечения неревматического кардита у детей требуются реабилитационные процедуры в санаторных условиях кардиоревматологического профиля. У малышей после подострого и острого недуга диспансерное наблюдение осуществляется на протяжении двух-трех лет, хронический и врожденный типы требуют наблюдения в течение всей жизни. Профилактические прививки маленьким пациентам, которые перенесли заболевание, делаются после того, как они были сняты с диспансерного учета, а при хроническом кардите вакцинация противопоказана.
У малышей после подострого и острого недуга диспансерное наблюдение осуществляется на протяжении двух-трех лет, хронический и врожденный типы требуют наблюдения в течение всей жизни. Профилактические прививки маленьким пациентам, которые перенесли заболевание, делаются после того, как они были сняты с диспансерного учета, а при хроническом кардите вакцинация противопоказана.
Теперь вы знаете, чем опасны неревматические кардиты в педиатрии. Чтобы защитить своего малыша от нежелательного недуга, следует следить за состоянием его здоровья и соблюдать профилактические меры.
Прогноз и профилактика данной патологии у малышей
Если события развиваются благоприятно, то симптомы недостаточности сердца понемногу регрессируют, размеры сердца уменьшаются, сердечный ритм приходит в норму. Легкие типы детского неревматического кардита чаще всего оканчиваются полным выздоровлением. Тяжелые формы могут привести к летальному исходу в 80% случаев. Факторы, которые отягощают прогноз, следующие: прогрессирующая недостаточность сердца, гипертензия легких, кардиосклероз, стойкие дефекты проводимости и ритма.
Профилактика неревматического врожденного кардита в педиатрии заключается в предупреждении возможности инфицирования плода внутри утробы. Исключить патологию помогут также закаливание малыша, предотвращение осложнений после вакцинации, терапия очаговых инфекций.
Мы рассмотрели клинические рекомендации при неревматическом кардите.
Миокардит у младенцев и детей: обзор для педиатра
Педиатр Здоровье ребенка. 2001 г., октябрь; 6(8): 543–545.
doi: 10.1093/pch/6.8.543
Язык: английский | Французский
Информация об авторе Информация об авторских правах и лицензии Отказ от ответственности
Клинический миокардит редко встречается у младенцев и детей. Наиболее распространенным возбудителем является вирус Коксаки В. Возбудитель вызывает иммунный ответ, который приводит к отеку миокарда с последующим нарушением систолической и диастолической функции. Новорожденные и младенцы страдают более тяжело, поскольку незрелый миокард имеет ограниченные возможности адаптации к острому инсульту. У детей обычно выявляют синусовую тахикардию и галоп при аускультации, кардиомегалию при рентгенографии органов грудной клетки и небольшие вольтажи на электрокардиограмме. Эхокардиограмма показывает снижение функции желудочков. Вирусные исследования могут изолировать возбудителя. Биопсия миокарда полезна с диагностической точки зрения, но сопряжена со значительным риском для больного младенца. Первая линия лечения включает такие меры, как покой, кислород и диуретики. Инотропные средства полезны при умеренной и тяжелой сердечной недостаточности. Роль иммуносупрессивной терапии в педиатрической возрастной группе еще четко не установлена. Прогноз у новорожденных осторожный, но более благоприятный у детей старшего возраста.
У детей обычно выявляют синусовую тахикардию и галоп при аускультации, кардиомегалию при рентгенографии органов грудной клетки и небольшие вольтажи на электрокардиограмме. Эхокардиограмма показывает снижение функции желудочков. Вирусные исследования могут изолировать возбудителя. Биопсия миокарда полезна с диагностической точки зрения, но сопряжена со значительным риском для больного младенца. Первая линия лечения включает такие меры, как покой, кислород и диуретики. Инотропные средства полезны при умеренной и тяжелой сердечной недостаточности. Роль иммуносупрессивной терапии в педиатрической возрастной группе еще четко не установлена. Прогноз у новорожденных осторожный, но более благоприятный у детей старшего возраста.
Ключевые слова: Дети, Младенцы, Миокардит
Клинический миокардит является редким среди детей и новорожденных. Le pathogene le plus courant est le вирус Coxsackie B. L’agent déclenchant provoque une immunitaire qui entraîne un œdème du myocarde suivi d’une défaillance de la fonction systolique et diastolique. Les nouveau-nés et les nourrissons sont plus touchés parce que le myocarde immature possède peu de moyens de s’adapter à une оскорбление aiguë. D’ordinaire, les enfants présentent une sinusal tachycardie et un bruit de galop à l’аускультация, une amégalie à la рентгенография легких et une faible voltage à l’ektrocardiogramme. L’échocardiogramme révèle une réduction de la ventriculaire fulction. Les études вирусных peuvent isoler ле патогенеза. Биопсия миокарда является полезной для диагностической точки зрения, более рискованной и важной для болезни ребенка. Le traitement de première ligne inclut des mesures comme le repos, l’oxygène et les diurétiques. Des агенты inotropes sot utiles en cas de défaillance cardiaque modérée à серьезно. Le rôle d’un traitement aux иммунодепрессанты n’est pas encore clairement établi dans la pédiatrique pédiatrique. Le pronostic est reservé chez les nouveau-nés, mais plus благоприятный chez les enfants plus agés.
Les nouveau-nés et les nourrissons sont plus touchés parce que le myocarde immature possède peu de moyens de s’adapter à une оскорбление aiguë. D’ordinaire, les enfants présentent une sinusal tachycardie et un bruit de galop à l’аускультация, une amégalie à la рентгенография легких et une faible voltage à l’ektrocardiogramme. L’échocardiogramme révèle une réduction de la ventriculaire fulction. Les études вирусных peuvent isoler ле патогенеза. Биопсия миокарда является полезной для диагностической точки зрения, более рискованной и важной для болезни ребенка. Le traitement de première ligne inclut des mesures comme le repos, l’oxygène et les diurétiques. Des агенты inotropes sot utiles en cas de défaillance cardiaque modérée à серьезно. Le rôle d’un traitement aux иммунодепрессанты n’est pas encore clairement établi dans la pédiatrique pédiatrique. Le pronostic est reservé chez les nouveau-nés, mais plus благоприятный chez les enfants plus agés.
Миокардит определяется как воспаление миокарда. Клинически проявления миокардита относительно редки у младенцев и детей. Это составляет всего 0,3% от 14 322 пациентов, наблюдавшихся за 23-летний период в Детской больнице Техаса, Хьюстон, штат Техас (1). Субклинический миокардит встречается гораздо чаще. С другой стороны, классические гистологические признаки миокардита были зарегистрированы у младенцев и детей, ставших жертвами внезапной неожиданной смерти (2).
Клинически проявления миокардита относительно редки у младенцев и детей. Это составляет всего 0,3% от 14 322 пациентов, наблюдавшихся за 23-летний период в Детской больнице Техаса, Хьюстон, штат Техас (1). Субклинический миокардит встречается гораздо чаще. С другой стороны, классические гистологические признаки миокардита были зарегистрированы у младенцев и детей, ставших жертвами внезапной неожиданной смерти (2).
Большинство случаев миокардита являются вторичными по отношению к вирусной инфекции. Наиболее распространенным возбудителем у детей является вирус Коксаки В, особенно серотипы 1–6 (3, 4). Вирус Коксаки В обычно вызывает спорадические случаи, хотя сообщалось о вспышках (5). Другие энтеровирусы (6), грипп (7), краснуха (8) и аденовирусы (9), и множество других агентов, также были вовлечены в случаи миокардита ().
TABLE 1:
Some causes of myocarditis
| Viral |
| Coxsackievirus B |
| Coxsackievirus A |
| Adenoviruses |
| Echoviruses |
| Hepatitis viruses |
| Вирус простого герпеса |
| Epstein-Barr virus |
| Cytomegalovirus |
| Polio viruses |
| Varicella virus |
| Influenza viruses |
| Bacterial |
| Diphtheria |
| Salmonella |
| Лептоспиры |
| Стрептококки |
| Микоплазменные бактерии |
| Legionella |
| Rickettsial |
| Rickettsia ricketsii |
| Protozoal |
| Trypanosoma cruzi |
| Parasitic |
| Toxocara canis |
| Шистосомоз |
| Цистеркоз |
| Висцеральная мигрирующая личинка |
| Fungal |
| Histoplasmosis |
| Candida |
| Drugs |
| Amphotericin B |
| Tetracycline |
| Sulfonamides |
| Phenylbutazone |
| Cyclophosphamide |
| Аутоиммунный |
| Системная красная волчанка |
| Rheumatic fever |
| Ulcerative colitis |
| Rheumatoid arthritis |
| Other |
| Sarcoidosis |
| Idiopathic |
Open in a separate window
At gross При осмотре миокард бледный, дряблый. Полости желудочков расширены, с истончением стенки и увеличением массы миокарда. Иногда присутствует пристеночный тромб.
Полости желудочков расширены, с истончением стенки и увеличением массы миокарда. Иногда присутствует пристеночный тромб.
При микроскопическом исследовании обнаруживается инфильтрат преимущественно мононуклеарных воспалительных клеток. Присутствуют интерстициальный отек и, в более тяжелых случаях, некроз миоцитов.
Эксперименты на мышах показали, что миокардит представляет собой иммунный процесс, запускаемый локально продуцируемым неоантигеном (10,11). Клеточно-опосредованная цитотоксичность, осуществляемая цитотоксическими Т-клетками и естественными клетками-киллерами, является первичным патологическим процессом, при этом гуморальная защита способствует поражению (12,13). Иммунный ответ модулируется локально продуцируемыми цитокинами, которые играют важную роль в развитии хронического миокардита (14).
Первичными патофизиологическими процессами являются развитие некроза миокарда и интерстициального отека с последующим нарушением сократительной способности сердечной мышцы. Расширение камер и истончение стенки желудочка увеличивает напряжение стенки, увеличивает потребность миокарда в кислороде и стимулирует гипертрофию. Резерв преднагрузки минимален в незрелом миокарде, и поддержание адекватного сердечного выброса в условиях недостаточной сократимости зависит от хронотропной повышающей регуляции. Сопутствующая лихорадка и анемия могут вызвать дополнительную нагрузку на сердце. Когда компенсаторные механизмы истощены, сердце выходит из строя, что приводит к состоянию низкого выброса. Снижение податливости сердца наряду с неполным опорожнением левого желудочка повышает диастолическое давление в левом желудочке и давление в легочных венах и предрасполагает пациентов к отеку легких.
Расширение камер и истончение стенки желудочка увеличивает напряжение стенки, увеличивает потребность миокарда в кислороде и стимулирует гипертрофию. Резерв преднагрузки минимален в незрелом миокарде, и поддержание адекватного сердечного выброса в условиях недостаточной сократимости зависит от хронотропной повышающей регуляции. Сопутствующая лихорадка и анемия могут вызвать дополнительную нагрузку на сердце. Когда компенсаторные механизмы истощены, сердце выходит из строя, что приводит к состоянию низкого выброса. Снижение податливости сердца наряду с неполным опорожнением левого желудочка повышает диастолическое давление в левом желудочке и давление в легочных венах и предрасполагает пациентов к отеку легких.
В большинстве случаев инфаркт миокарда носит ограниченный характер, и сердце восстанавливает нормальную функцию в течение нескольких месяцев. При более обширном поражении миокарда рубцовая ткань замещает некротический миокард во время заживления, и восстановление функции происходит не полностью.
Одышка при кормлении, рвота и бледность являются частыми жалобами у младенцев. У детей более старшего возраста наблюдается заметное снижение выносливости и одышка на фоне вирусной инфекции. Жалобы на сердцебиение свидетельствуют о сопутствующей аритмии. Боль в груди неспецифична и указывает на возможное сопутствующее воспаление плевры или перикарда.
При физикальном обследовании у ребенка тахипноэ, тахикардия и лихорадка. Гипотензия предполагает серьезное снижение сердечной функции. Обычно отмечаются бледность и сужение периферических сосудов из-за симпатической активации. Наполнение периферических капилляров замедлено. У детей самым ранним признаком задержки жидкости вследствие застойной сердечной недостаточности является отечность век. Более тяжелая недостаточность проявляется гепатомегалией и генерализованными отеками. Шум трения перикарда и отдаленные тоны сердца указывают на наличие сопутствующего перикардиального выпота. Мягкий первый тон сердца является обычным, но неспецифическим, и его часто трудно оценить у младенцев с тахикардией. Ритм галопа, производимый третьим тоном сердца, част и лучше всего выслушивается на верхушке. Высокочастотный шум регургитации на верхушке указывает на сопутствующую митральную недостаточность.
Ритм галопа, производимый третьим тоном сердца, част и лучше всего выслушивается на верхушке. Высокочастотный шум регургитации на верхушке указывает на сопутствующую митральную недостаточность.
Сепсис, тяжелое обезвоживание или анемию следует рассматривать как диагностические возможности у больного новорожденного или младенца. Первичный эндокардиальный фиброэластоз и метаболическая дилатационная кардиомиопатия являются заболеваниями миокарда, которые могут проявляться схожим образом. Необходимо исключить врожденные структурные поражения, такие как критическая коарктация аорты или аномальное отхождение левой коронарной артерии от легочной артерии.
Рентген грудной клетки классически показывает кардиомегалию и легочный венозный застой. Сопутствующий перикардиальный выпот может усилить степень кардиомегалии.
Электрокардиограмма в 12 отведениях обычно показывает синусовую тахикардию и низковольтные комплексы QRS (общая амплитуда менее 5 мм во всех отведениях от конечностей), с малоамплитудными или слегка инвертированными зубцами T и небольшими или отсутствующими зубцами Q в отведениях V5 и V6. Удлинение интервала PR и QT является обычным, но неспецифическим явлением.
Удлинение интервала PR и QT является обычным, но неспецифическим явлением.
Наличие аритмии на фоне лихорадочного заболевания должно указать врачу на возможность миокардита. Пароксизмальная предсердная тахикардия (15), желудочковая эктопия (16–18) и различные степени блокады сердца (19).) все были описаны в связи с миокардитом.
Эхокардиограмма необходима для диагностики и последующего наблюдения за миокардитом. Можно легко исключить структурную болезнь сердца и перикардит. Функция миокарда оценивается во время постановки диагноза и служит отправной точкой для будущего мониторинга прогрессирования заболевания и ответа на терапевтические вмешательства.
Выделение вируса-возбудителя из кала, смывов из горла или крови возможно на ранних стадиях заболевания (20). В противном случае серологический диагноз основывается на четырехкратном увеличении титра вирусспецифических антител между образцами крови острого и выздоравливающего периода.
Роль биопсии миокарда в постановке диагноза миокардита противоречива. Эндомиокардиальная биопсия может установить диагноз и степень поражения (21). Недавно было показано, что полимеразная цепная реакция, проводимая на ткани миокарда, чувствительна и специфична для диагностики энтеровирусного и аденовирусного миокардита (9). Полезность биопсии необходимо сопоставлять с риском перфорации и смерти, особенно у больного ребенка (22). Кроме того, очаговое поражение правого желудочка или изолированное поражение левого желудочка могут остаться незамеченными, если выборочные образцы биопсии ограничены перегородкой правого желудочка.
Эндомиокардиальная биопсия может установить диагноз и степень поражения (21). Недавно было показано, что полимеразная цепная реакция, проводимая на ткани миокарда, чувствительна и специфична для диагностики энтеровирусного и аденовирусного миокардита (9). Полезность биопсии необходимо сопоставлять с риском перфорации и смерти, особенно у больного ребенка (22). Кроме того, очаговое поражение правого желудочка или изолированное поражение левого желудочка могут остаться незамеченными, если выборочные образцы биопсии ограничены перегородкой правого желудочка.
Лечение младенцев и детей с миокардитом зависит от тяжести заболевания. Ребенка госпитализируют, и при наличии сопутствующей аритмии проводят телеметрию. Вспомогательные терапевтические меры включают дополнительный кислород, диуретики и постельный режим. Анемия корректируется всякий раз, когда она присутствует. Потребление жидкости и соли контролируется. При более тяжелом течении болезни добавляют инотропный агент, такой как допамин или добутамин, особенно если сердечная функция угнетена на эхокардиограмме. Назначение этих препаратов требует госпитализации в отделение реанимации и внутрисосудистого контроля артериального давления. Нитропруссид, внутривенное средство, снижающее постнагрузку, можно рассматривать при отсутствии артериальной гипотензии. Наперстянку следует использовать с особой осторожностью в острой фазе заболевания, поскольку ее повышенное действие на воспаленный миокард может спровоцировать серьезную аритмию (23). Если миокардит приводит к дилатационной кардиомиопатии и хронической сердечной недостаточности, терапевтически полезны дигоксин и ингибитор ангиотензинпревращающего фермента (24).
Назначение этих препаратов требует госпитализации в отделение реанимации и внутрисосудистого контроля артериального давления. Нитропруссид, внутривенное средство, снижающее постнагрузку, можно рассматривать при отсутствии артериальной гипотензии. Наперстянку следует использовать с особой осторожностью в острой фазе заболевания, поскольку ее повышенное действие на воспаленный миокард может спровоцировать серьезную аритмию (23). Если миокардит приводит к дилатационной кардиомиопатии и хронической сердечной недостаточности, терапевтически полезны дигоксин и ингибитор ангиотензинпревращающего фермента (24).
Применение иммунодепрессантов при остром лечении миокардита у детей вызывает споры. Небольшие размеры когорт в большинстве педиатрических исследований и отсутствие крупных двойных слепых контролируемых исследований не позволяют давать какие-либо четкие рекомендации. Стероиды, азатиоприн и гамма-глобулины применялись с переменным успехом. В исследовании Myocarditis Treatment Trial в основном взрослые пациенты, получавшие азатиоприн и преднизолон или циклоспорин и преднизолон, не чувствовали себя лучше, чем пациенты, получавшие только традиционное лечение (25). В небольшом педиатрическом исследовании у пациентов, получавших иммуносупрессивные препараты, наблюдалось лучшее состояние, чем у пациентов, получавших только консервативные меры (26). Недавно были получены обнадеживающие результаты использования гамма-глобулина (27,28).
В небольшом педиатрическом исследовании у пациентов, получавших иммуносупрессивные препараты, наблюдалось лучшее состояние, чем у пациентов, получавших только консервативные меры (26). Недавно были получены обнадеживающие результаты использования гамма-глобулина (27,28).
Миокардит имеет неблагоприятный прогноз у новорожденных, с 75% смертностью, когда подозревается вирус Коксаки B (29). Дети старшего возраста чувствуют себя лучше; смертность составляет менее 25%, а еще 25% детей будут страдать хроническими симптомами сердечной недостаточности. Полное выздоровление наступает примерно в половине диагностированных случаев (30).
1. Фридман Р.А., Шовенгердт К.О., младший, Таубин Дж.А. Миокардит. В: Garson A Jr, Bricker JT, Fisher DJ, Neish SR, редакторы. Наука и практика детской кардиологии. 2-е изд. Балтимор: Уильямс и Уилкинс; 1998. стр. 1777–94. [Google Scholar]
2. Burch GE, Sun SC, Chu KC, Sohal RS, Colcolough HL. Интерстициальный миокардит и миокардит вируса Коксаки В у младенцев и детей: сравнительное гистологическое и иммунофлуоресцентное исследование 50 вскрытых сердец. ДЖАМА. 1968; 203:1–8. [PubMed] [Google Scholar]
ДЖАМА. 1968; 203:1–8. [PubMed] [Google Scholar]
3. Дери П., Маркс М.И., Шапера Р. Клинические проявления вирусных инфекций Коксаки у детей. Am J Dis Чайлд. 1974; 128: 464–8. [PubMed] [Google Scholar]
4. Hosier DM, Newton WA., Jr Серьезная инфекция Коксаки у младенцев и детей. Am J Dis Чайлд. 1958;96:251–67. [PubMed] [Google Scholar]
5. Helin M, Savola J, Lapinleimu K. Сердечные проявления во время эпидемии Коксаки B5. БМЖ. 1968; 2: 97–99. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. Лернер А.М., Уилсон Ф.М., Реймс М.П. Энтеровирус и сердце (с особым акцентом на возможную роль вирусов Коксаки, группа В, типы 1–5) Mod Concepts Cardiovasc Dis. 1975; 64: 7–10. [PubMed] [Google Scholar]
7. Karjalainen J, Nieminen MS, Heikkila J. Миокардит гриппа А1 у призывников. Акта Мед Сканд. 1980;20:27–30. [PubMed] [Google Scholar]
8. Эйнгер Л.Э., юрист Н.Г., Fitch CW. Неонатальный краснушный миокардит. Бр Харт Дж. 1966; 28: 691–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Martin AB, Webber S, Fricker FJ, et al. Острый миокардит. Экспресс-диагностика методом ПЦР у детей. Тираж. 1994;90:330–9. [PubMed] [Google Scholar]
Martin AB, Webber S, Fricker FJ, et al. Острый миокардит. Экспресс-диагностика методом ПЦР у детей. Тираж. 1994;90:330–9. [PubMed] [Google Scholar]
10. Вудрафф Дж. Ф. Вирусный миокардит: обзор. Ам Джей Патол. 1980; 101: 425–84. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Godeny EK, Gauntt CJ. Мышиные естественные клетки-киллеры ограничивают репликацию вируса Коксаки B3. Дж Иммунол. 1987;139:913–8. [PubMed] [Google Scholar]
12. Вонг С.Ю., Вудрафф Дж.Дж., Вудрафф Дж.Ф. Генерация цитотоксических Т-лимфоцитов при инфекции Коксаки В-3. II. Характеристика эффекторных клеток и демонстрация цитотоксичности против инфицированных вирусом миофибрилл1. Дж Иммунол. 1977; 118:1165–9. [PubMed] [Google Scholar]
13. Maisch B, Trostel-Soeder R, Stechemesser E, Berg PA, Kochsiek K. Диагностическая значимость гуморальных и клеточно-опосредованных иммунных реакций у пациентов с острым вирусным миокардитом. Клин Эксп Иммунол. 1982;48:533–545. [Бесплатная статья PMC] [PubMed] [Google Scholar]
14. Kroemer G, Martinez AC. Цитокины и аутоиммунные заболевания. Клин Иммунол Иммунопатол. 1991; 61: 275–95. [PubMed] [Google Scholar]
Kroemer G, Martinez AC. Цитокины и аутоиммунные заболевания. Клин Иммунол Иммунопатол. 1991; 61: 275–95. [PubMed] [Google Scholar]
15. Черри Д.Д., Ян Кл., Мейер Т.С. Пароксизмальная предсердная тахикардия, связанная с эхо-9 вирусной инфекцией. Am Heart J. 1967; 73: 681–6. [PubMed] [Google Scholar]
16. Хуанг М., Бигос Д., Левин М. Желудочковая аритмия, связанная с респираторно-синцитиальной вирусной инфекцией. Педиатр Кардиол. 1998;19:498–500. [PubMed] [Google Scholar]
17. Balaji S, Wiles HB, Sens MA, Gillette PC. Иммуносупрессивная терапия миокардита и пограничного миокардита у детей с желудочковым эктопическим ритмом. Бр Харт Дж. 1994; 72: 354–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Friedman RA, Kearney DL, Moak JP, Fenrich AL, Perry JC. Сохранение желудочковой аритмии после разрешения скрытого миокардита у детей и молодых людей. J Am Coll Кардиол. 1994; 24:780–3. [PubMed] [Академия Google]
19. Шикен Р.М., Майерс М.Г. Полная блокада сердца при вирусном миокардите. J Педиатр. 1975; 87: 831–2. [PubMed] [Google Scholar]
J Педиатр. 1975; 87: 831–2. [PubMed] [Google Scholar]
20. Беркович С., Родрикес-Торрес Р., Лин Дж. С. Вирусологические исследования у детей с острым миокардитом. Am J Dis Чайлд. 1968; 115: 207–12. [PubMed] [Google Scholar]
21. Fenoglio JJ, Jr, Ursell PC, Kellogg CF, Drusin RE, Weiss MB. Диагностика и классификация миокардита с помощью эндомиокардиальной биопсии. N Engl J Med. 1983; 308: 12–8. [PubMed] [Академия Google]
22. Pophal SG, Sigfusson G, Booth KL, et al. Осложнения эндомиокардиальной биопсии у детей. J Am Coll Кардиол. 1999;34:2105–10. [PubMed] [Google Scholar]
23. Мацумори А., Игата Х., Оно К. и соавт. Высокие дозы наперстянки увеличивают выработку миокардом провоспалительных цитокинов и ухудшают повреждение миокарда при вирусном миокардите: возможный механизм токсичности наперстянки. Jpn Circ J. 1999; 63: 934–40. [PubMed] [Google Scholar]
24. Льюис А.Б., Шабо М. Влияние лечения ингибиторами ангиотензинпревращающего фермента на выживаемость педиатрических пациентов с дилатационной кардиомиопатией. Педиатр Кардиол. 1993;14:9–12. [PubMed] [Google Scholar]
Педиатр Кардиол. 1993;14:9–12. [PubMed] [Google Scholar]
25. Mason JW, O’Connell JB, Herkowitz A, et al. Клинические испытания иммуносупрессивной терапии миокардита. N Engl J Med. 1995; 333: 270–5. [Google Scholar]
26. Camargo PR, Snitcowsky R, da Luz PL, et al. Благоприятные эффекты иммуносупрессивной терапии у детей с дилатационной кардиомиопатией и активным миокардитом. Педиатр Кардиол. 1995; 16: 61–8. [PubMed] [Google Scholar]
27. Drucker NA, Colan SD, Lewis AB, et al. Гамма-глобулиновая терапия острого миокардита у детей. Тираж. 1994;89:252–7. [PubMed] [Google Scholar]
28. Lee KJ, McCrindle BW, Bohn DJ, et al. Клинические исходы острого миокардита в детском возрасте. Сердце. 1999; 82: 226–33. [PMC free article] [PubMed] [Google Scholar]
29. Kibrick S, Benirschke K. Тяжелое генерализованное заболевание (энцефалогепатомиокардит), возникающее в период новорожденности и обусловленное инфицированием вирусом Коксаки группы B. Доказательства внутриутробного инфицирования этим возбудителем. Педиатрия. 1958; 22: 857–74. [PubMed] [Академия Google]
Педиатрия. 1958; 22: 857–74. [PubMed] [Академия Google]
30. Хастрейтер А.Р., Миллер Р.А. Лечение первичного эндомиокардиального заболевания: синдром миокардита-эндокардиального фиброэластоза. Педиатр Клин Норт Ам. 1964; 11: 401–30. [PubMed] [Google Scholar]
Диагностический и клинический подход к детскому миокардиту: обзор современной литературы
1. Magnani JW, Dec GW. Миокардит: современные тенденции диагностики и лечения. Тираж. 2006; 113: 876–890. https://doi.org/10.1161/CIRCULATIONAHA.105.584532 PMid: 16476862. [PubMed] [Google Scholar]
2. Купер Л.Т., мл. Миокардит. N Engl J Med. 2009; 360:1526–1538. https://doi.org/10.1056/NEJMra0800028 PMid: 19357408 PMCid: PMC5814110. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Richardson P, McKenna W, Bristow M, et al. Доклад Целевой группы Всемирной организации здравоохранения/Международного общества и Федерации кардиологов 1995 г. по определению и классификации кардиомиопатий. Тираж. 1996; 93: 841–842. https://doi.org/10.1161/01.CIR.93.5.841 PMid: ↖070. [PubMed] [Академия Google]
https://doi.org/10.1161/01.CIR.93.5.841 PMid: ↖070. [PubMed] [Академия Google]
4. Фельдман А.М., Макнамара Д. Миокардит. N Engl J Med. 2000; 343:1388–1398. https://doi.org/10.1056/NEJM200011093431908 PMid: 11070105. [PubMed] [Google Scholar]
5. Schultheiss HP, Kühl U, Cooper LT. Лечение миокардита. Европейское сердце J. 2011; 32: 2616–2625. https://doi.org/10.1093/eurheartj/ehr165 PMid: 21705357. [PubMed] [Google Scholar]
6. Barth C, Mahfoud F, Ukena C, Lenski M, Yilmaz A, Klingel K, Kandolf R, Sechtem U, Cooper LT, Böhm M. Обновление по миокардиту. J Am Coll Кардиол. 2012;59: 779–792. https://doi.org/10.1016/j.jacc.2011.09.074 PMid: 22361396. [Google Scholar]
7. Esfandiarei M, McManus BM. Молекулярная биология и патогенез вирусного миокардита. Анну Рев Патол. 2008;3:127–155. https://doi.org/10.1146/annurev.pathmechdis.3.121806.151534 PMid: 18039131. [PubMed] [Google Scholar]
Детский миокардит: клинические данные отделения неотложной помощи и диагностическая оценка. Педиатрический. 2007; 120:1278–1285. https://doi.org/10.1542/peds.2007-1073 PMid: 18055677. [PubMed] [Google Scholar]
Педиатрический. 2007; 120:1278–1285. https://doi.org/10.1542/peds.2007-1073 PMid: 18055677. [PubMed] [Google Scholar]
9. Окада Р., Каваи С., Касюя Х. Неспецифический миокардит: статистическое и клинико-патологическое исследование вскрытий. Jpn Circ J. 1989; 53: 40–48. https://doi.org/10.1253/jcj.53.40 PMid: 2523982. [PubMed] [Google Scholar]
10. Сагар С., Лю П.П., Купер Л.Т., мл. Миокардит. Ланцет. 2012; 379: 738–747. https://doi.org/10.1016/S0140-6736(11)60648-X. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Elamm C, Fairweather D, Cooper LT. Патогенез и диагностика миокардита. Сердце. 2012;98:835–840. https://doi.org/10.1136/heartjnl-2012-301686 PMid: 22442199. [PubMed] [Google Scholar]
Клинические особенности и исходы дилатационной кардиомиопатии у детей: результаты национального популяционного исследования. Тираж. 2006; 114: 2671–2678. https://doi.org/10.1161/CIRCULATIONAHA.106.635128 PMid: 17116768. [PubMed] [Google Scholar]
Внезапная смерть у молодых людей: 25-летний обзор вскрытий новобранцев. Энн Интерн Мед. 2004;141:829–834. https://doi.org/10.7326/0003-4819-141-11-200412070-00005 PMid: 15583223. [PubMed] [Google Scholar]
Энн Интерн Мед. 2004;141:829–834. https://doi.org/10.7326/0003-4819-141-11-200412070-00005 PMid: 15583223. [PubMed] [Google Scholar]
. Аутоиммунитет. 2004; 37: 375–386. https://doi.org/10.1080/08916930410001713089 PMid: 15621561. [PubMed] [Google Scholar]
15. Bowles NE, Towbin JA. Молекулярные аспекты миокардита. Карр Опин Кардио. 1998; 13: 179–184. PMid:9649940. [PubMed] [Google Scholar]
16. Canter CE, Simpson KE. Диагностика и лечение миокардита у детей в современное время. Тираж. 2014;129(1): 115–28. https://doi.org/10.1161/CIRCULATIONAHA.113.001372 PMid: 24396015. [PubMed] [Google Scholar]
17. Kühl U, Schultheiss H-P. Миокардит у детей. Клиника сердечной недостаточности. 2010;6:483–496. https://doi.org/10.1016/j.hfc.2010.05.009 PMid: 20869648. [PubMed] [Google Scholar]
18. Foerster SR. Кантер С. Э. Современная этиология, исходы и терапия детского миокардита. Прог Педиатр Кардиол. 2011; 31: 123–128. https://doi.org/10.1016/j.ppedcard.2011. 02.010. [Академия Google]
02.010. [Академия Google]
19. May LJ, Patton DJ, Fruitman DS. Развивающийся подход к педиатрическому миокардиту: обзор современной литературы. Кардиол Янг. 2011;21:241–251. https://doi.org/10.1017/S1047951110001964 PMid: 21272427. [PubMed] [Google Scholar]
20. Lippi G, Salvagno GL, Guidi GC. Сердечные тропонины при детском миокардите. Педиатрия. 2008; 121:864. https://doi.org/10.1542/peds.2008-0031 PMid: 18381554. [PubMed] [Google Scholar]
21. Molina KM, Garcia X, Denfield SW, Fan Y, Morrow WR, Towbin JA, Frazier EA , Нельсон Д.П. Парвовирус B19Миокардит вызывает значительную заболеваемость и смертность у детей. Педиатр Кардиол. 2013; 34: 390–397. https://doi.org/10.1007/s00246-012-0468-4 PMID: 22∐19. [PubMed] [Google Scholar]
22. Bowles NE, Ni J, Kearney DL, et al. Выявление вирусов в тканях миокарда методом полимеразной цепной реакции. Доказательства аденовируса как частой причины миокардита у детей и взрослых. J Am Coll Кардиол. 2003; 42: 466–472. https://doi. org/10.1016/S0735-1097(03)00648-X. [PubMed] [Академия Google]
org/10.1016/S0735-1097(03)00648-X. [PubMed] [Академия Google]
23. Kuhl U, Pauschinger M, Seeberg B, et al. Персистенция вируса в миокарде связана с прогрессирующей сердечной дисфункцией. Тираж. 2005; 112:1965–1970. https://doi.org/10.1161/CIRCULATIONAHA.105.548156 PMid: 16172268. [PubMed] [Google Scholar]
24. Bratincsak A, El-Said HG, Bradley JS и соавт. Фульминантный миокардит, связанный с пандемическим вирусом гриппа А h2N1 у детей. J Am Coll Кардиол. 2010;55:928–929. https://doi.org/10.1016/j.jacc.2010.01.004 PMid: 20153131. [PubMed] [Google Scholar]
25. Леонард Э.Г. Вирусный миокардит. Pediatr Infect Dis J. 2004; 23:665–666. https://doi.org/10.1097/01.inf.0000132280.36984.a9 PMid: 15247607. [PubMed] [Google Scholar]
Молекулярная диагностика миокардита и дилатационной кардиомиопатии у детей: клинико-патологические особенности и прогностическое значение. Диагност Мол Патол. 2002; 11: 212–221. https://doi.org/10.1097/00019606-200212000-00004 PMid: 12459637. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
27. Durani Y, Egan M, Baffa J, et al. Детский миокардит: представление клинических характеристик. Am J Emerg Med. 2009; 27: 942–947. https://doi.org/10.1016/j.ajem.2008.07.032 PMid: 19857412. [PubMed] [Google Scholar]
28. Kern J, Modi R, Atalay MK, et al. Клинический миокардит, маскирующийся под острый коронарный синдром. J Педиатр. 2009; 154: 612–615. https://doi.org/10.1016/j.jpeds.2008.10.018 PMid: 19324224. [PubMed] [Google Scholar]
29. Ellis CR, Di Salvo T. Миокардит: основные и клинические аспекты. Cardiol Rev. 2007; 15:170–177. https://doi.org/10.1097/CRD.0b013e31806450c4 PMid: 17575480. [PubMed] [Google Scholar]
30. Chang YJ, Chao HC, Hsia SH, Yan DC. Миокардит в виде гастрита у детей. Педиатр Неотложная помощь. 2006; 22: 439–440. 31. Yasukochi S, Arakaki Y, Joo K, Nakazawa M. Сравнение клинической картины, лечение и исход молниеносного и острого миокардита у детей. Цирк J. 2012; 76: 1222–1228. https://doi.org/10.1253/circj.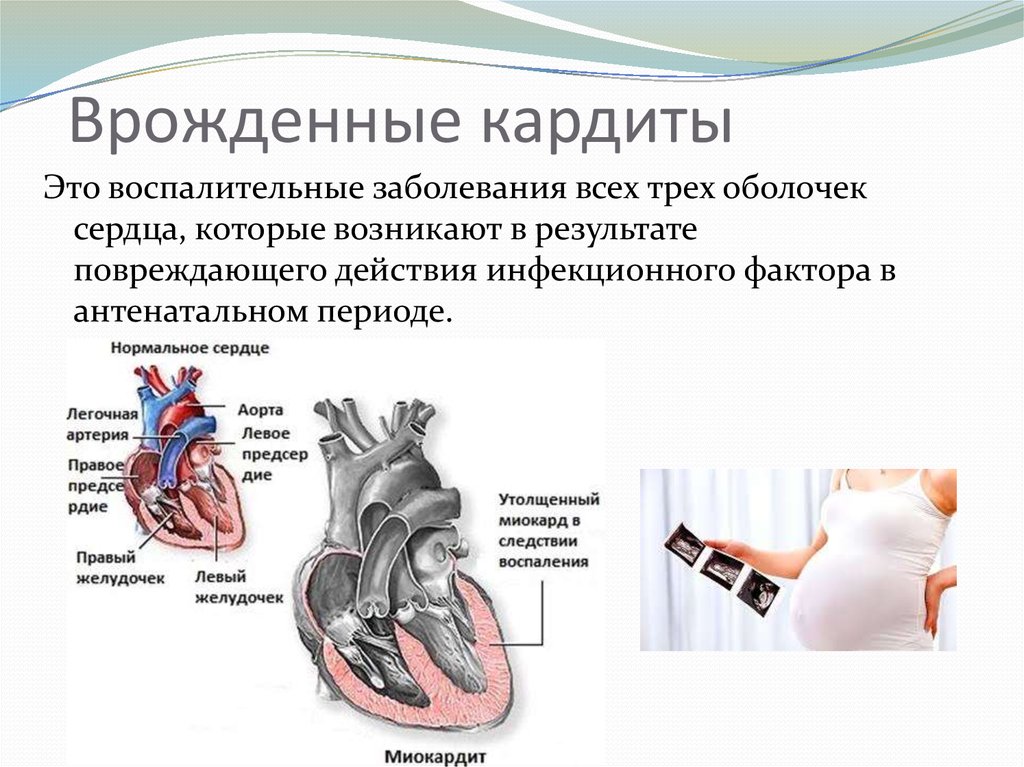 CJ-11-1032 PMid: 22307381. [PubMed] [Google Scholar]
CJ-11-1032 PMid: 22307381. [PubMed] [Google Scholar]
32. Чеккия П.А., Кулик Т.Я. Острый вирусный миокардит: диагностика. Pediatr Crit Care Med. 2006;7:S8–S11. https://doi.org/10.1097/01.PCC.0000244336.60719.8C. [Google Scholar]
33. Керн Дж., Моди Р., Аталай М.К., Кочилас Л.К. Клинический миокардит, маскирующийся под острый коронарный синдром. J Педиатр. 2009; 154: 612–615. https://doi.org/10.1016/j.jpeds.2008.10.018 PMid: 19324224. [PubMed] [Google Scholar]
34. Итикава Р., Сумитомо Н., Комори А., Абэ Ю., Накамура Т., Фукухара Дж., Мацумура М., Мияшита М., Канамару Х., Аюсава М., Мугисима Х. Последующая оценка электрокардиограммы и аритмий у детей с флуминантным миокардитом. Журнал тиражей. 2011;75(4):932–8. https://doi.org/10.1253/circj.CJ-10-0918 PMid: 21343655. [PubMed] [Google Scholar]
35. Батра А.С., Эпштейн Д., Силка М.Дж. Клиническое течение приобретенной полной блокады сердца у детей с острым миокардитом. Детская кардиология. 2003;24(5):495–7. https://doi. org/10.1007/s00246-002-0402-2 PMid: 14627323. [PubMed] [Google Scholar]
org/10.1007/s00246-002-0402-2 PMid: 14627323. [PubMed] [Google Scholar]
36. Gassenmaier T, Buchner S, Birner C, Jungbauer CG, Resch M, Debl K, Endemann DH, Riegger GA, Lehn P, Schmitz G, Luchner A. Высокочувствительный тропонин I при острых сердечных заболеваниях: значение исходных и последовательных измерений для диагностики инфаркта миокарда. Атеросклероз. 2012; 222:116–122. https://doi.org/10.1016/j.atherosclerosis.2012.02.007 PMid: 22405442. [PubMed] [Google Scholar]
37. Липпи Г., Сальваньо Г.Л., Гвиди Г.К. Сердечные тропонины при детском миокардите. Педиатрический. 2008; 121:864–865. https://doi.org/10.1542/peds.2008-0031 PMid: 18381554. [PubMed] [Google Scholar]
38. Nussinovitch U, Shoenfeld Y. Клиническое и диагностическое значение антимиозиновых аутоантител при заболеваниях сердца. Клин Рев Аллергия Иммунол. 2013;44:98–108. https://doi.org/10.1007/s12016-010-8229-8 PMid: 21207194. [PubMed] [Google Scholar]
39. Soongswang J, Durongpisitkul K, Nana A, et al. Сердечный тропонин Т: маркер в диагностике острого миокардита у детей. Педиатр Кардиол. 2005; 26: 45–49. https://doi.org/10.1007/s00246-004-0677-6 PMid: 15793653. [PubMed] [Google Scholar]
Сердечный тропонин Т: маркер в диагностике острого миокардита у детей. Педиатр Кардиол. 2005; 26: 45–49. https://doi.org/10.1007/s00246-004-0677-6 PMid: 15793653. [PubMed] [Google Scholar]
40. Симпсон К., Ли С.К., Каннингем М., Саймон С., Делани Дж., Уорд К., Тонг А., Данон С., Кантер С. Распространенность аутоиммунитета и связь с сердечным статусом при педиатрическом миокардите и недавней дилатационной кардиомиопатии. J Am Coll Кардиол. 2013;61:A312. https://doi.org/10.1016/S0735-1097(13)61265-6. [Google Scholar]
41. Шекердемян Л., Бон Д. Острый вирусный миокардит: эпидемиология и патофизиология. Pediatr Crit Care Med. 2006;5:С2–С7. https://doi.org/10.1097/01.ПКС.0000244338.73173.70. [Google Scholar]
42. Анджелини А., Кальцолари В., Калабрезе Ф., Боффа Г.М., Маддалена Ф., Чиоин Р., Тиене Г. Миокардит, имитирующий острый инфаркт миокарда: роль эндомиокардиальной биопсии в дифференциальной диагностике. Сердце. 2000; 84: 245–250. https://doi.org/10.1136/heart.84.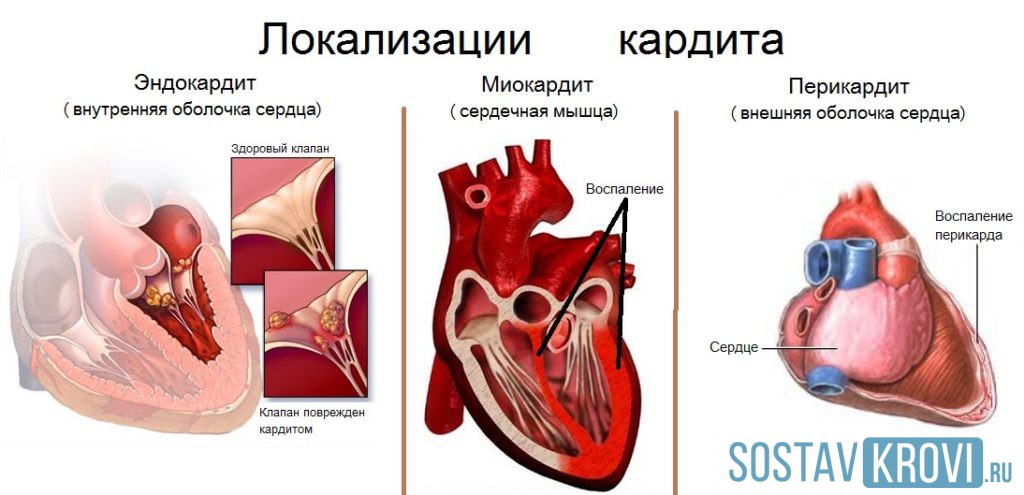 3.245 PMid: 10956283 PMCid: PMC1760950. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3.245 PMid: 10956283 PMCid: PMC1760950. [Бесплатная статья PMC] [PubMed] [Google Scholar]
43. Jeserich M, Konstantinides S, Pavlik G, et al. Неинвазивная визуализация в диагностике острого вирусного миокардита. Клин Рез Кардиол. 2009 г.;98:753–763. https://doi.org/10.1007/s00392-009-0069-2 PMid: 19756815 PMCid: PMC2789929. [Бесплатная статья PMC] [PubMed] [Google Scholar]
44. Skouri HN, Dec GW, Friedrich MG, et al. Неинвазивная визуализация при миокардите. J Am Coll Кардиол. 2006;48:2085–2093. https://doi.org/10.1016/j.jacc.2006.08.017 PMid: 17112998. [PubMed] [Google Scholar]
45. Friedrich MG, Sechtem U, Schulz-Menger J, et al. Сердечно-сосудистый магнитный резонанс при миокардите: Белая книга JACC. J Am Coll Кардиол. 2009 г.;53:1475–1487. https://doi.org/10.1016/j.jacc.2009.02.007 PMid: 19389557 PMCid: PMC2743893. [Бесплатная статья PMC] [PubMed] [Google Scholar]
46. Friedrich MG. Отек миокарда – новая клиническая форма? Нат Рев Кардиол. 2010;7:292–296. https://doi.org/10.1038/nrcardio.2010.28 PMid: 20309007. [PubMed] [Google Scholar]
https://doi.org/10.1038/nrcardio.2010.28 PMid: 20309007. [PubMed] [Google Scholar]
47. Абдель-Ати Х., Симонетти О., Фридрих М.Г. Т2-взвешенная магнитно-резонансная томография сердечно-сосудистой системы. J Magn Reson Imaging. 2007; 26: 452–459. https://doi.org/10.1002/jmri.21028 PMid: 17729358. [PubMed] [Google Scholar]
48. Кокер М., Фридрих М.Г. Сердечно-сосудистый магнитно-резонансный миокардит. Curr Cardiol Rep. 2010; 12:82–89. https://doi.org/10.1007/s11886-009-0077-x PMid: 20425188. [PubMed] [Google Scholar]
49. Felker GM, Boehmer JP, Hruban RH, Hutchins GM, Kasper EK, Baughman KL, Заяц Дж.М. Эхокардиографические данные при молниеносном и остром миокардите. J Am Coll Кардиол. 2000; 36: 227–232. https://doi.org/10.1016/S0735-1097(00)00690-2. [PubMed] [Академия Google]
50. Брауман К.Л. Диагноз миокардита: смерть по критерию Далласа. Тираж. 2006; 113: 593–59. https://doi.org/10.1161/CIRCULATIONAHA.105.589663 PMid: 16449736. [PubMed] [Google Scholar]
J, Starling RC, Towbin J, Virmani R, Американская кардиологическая ассоциация. Американский колледж кардиологов; Европейское общество кардиологов. Роль эндомиокардиальной биопсии в лечении сердечно-сосудистых заболеваний: научное заявление Американской кардиологической ассоциации, Американского колледжа кардиологов и Европейского общества кардиологов. Тираж. 2007;116:2216–2233. https://doi.org/10.1161/CIRCULATIONAHA.107.1↡3 PMid: 17959655. [PubMed] [Google Scholar]
Американский колледж кардиологов; Европейское общество кардиологов. Роль эндомиокардиальной биопсии в лечении сердечно-сосудистых заболеваний: научное заявление Американской кардиологической ассоциации, Американского колледжа кардиологов и Европейского общества кардиологов. Тираж. 2007;116:2216–2233. https://doi.org/10.1161/CIRCULATIONAHA.107.1↡3 PMid: 17959655. [PubMed] [Google Scholar]
52. Cooper LT, Jr, ElAmm C. Гигантоклеточный миокардит: диагностика и лечение. Герц. 2012; 37: 632–636. 53. Maron BJ, Doerer JJ, Haas TS, Tierney DM, Mueller FO. Внезапная смерть молодых спортсменов: анализ 1866 смертей в США, 1980–2006 гг. Тираж. 2009;119(8):1085–92. https://doi.org/10.1161/CIRCULATIONAHA.108.804617 PMid: 19221222. [PubMed] [Google Scholar]
54. Daubeney PE, Nugent AW, Chondros P, Carlin JB, Colan SD, Cheung M, Davis A, Chow CW Weintraub RG; Национальное австралийское исследование детской кардиомиопатии. Клинические особенности и исходы дилатационной кардиомиопатии у детей: результаты национального популяционного исследования. Тираж. 2006; 114: 2671–2678. https://doi.org/10.1161/CIRCULATIONAHA.106.635128 PMid: 17116768. [PubMed] [Google Scholar]
Тираж. 2006; 114: 2671–2678. https://doi.org/10.1161/CIRCULATIONAHA.106.635128 PMid: 17116768. [PubMed] [Google Scholar]
55. Towbin JA, Lowe AM, Colan SD, Sleeper LA, Orav EJ, Clunie S, Messere J, Cox GF, Lurie PR, Hsu D, Canter C. Заболеваемость, причины и исходы дилатационной кардиомиопатии у детей. Джама. 2006;296 (15): 1867–76. https://doi.org/10.1001/jama.296.15.1867 PMid: 17047217. [PubMed] [Google Scholar]
56. Andrews RE, Fenton MJ, Ridout DA, Burch M. Впервые возникшая сердечная недостаточность вследствие сердечной недостаточности мышечные заболевания у детей: проспективное исследование в Соединенном Королевстве и Ирландии. Тираж. 2008;117(1):79–84. https://doi.org/10.1161/CIRCULATIONAHA.106.671735 PMid: 18086928. [PubMed] [Google Scholar]
57. Klugman D, Berger JT, Sable CA, He J, Khandelwal SG, Slonim AD. Педиатрические пациенты, госпитализированные с миокардитом: анализ нескольких учреждений. Детская кардиология. 2010;31(2):222–8. https://doi.org/10. 1007/s00246-009-9589-9 PMid: 19936586. [PubMed] [Google Scholar]
1007/s00246-009-9589-9 PMid: 19936586. [PubMed] [Google Scholar]
58. Amabile N, Fraisse A, Bouvenot J, Chetaille P, Ovaert C. Исход острого фульминантного миокардита у детей. Сердце. 2006;92(9):1269–73. https://doi.org/10.1136/hrt.2005.078402 PMid: 16449512 PMCid: PMC1↣80. [Бесплатная статья PMC] [PubMed] [Google Scholar]
59. English RF, Janosky JE, Ettedgui JA, Webber SA. Исходы у детей с острым миокардитом. Кардиология в молодости. 2004;14(5):488–93. https://doi.org/10.1017/S1047951104005049 PMid: 15680069. [PubMed] [Google Scholar]
60. Годсел Л.М., Леон Дж.С., Энгман Д.М. Ингибиторы ангиотензинпревращающего фермента и антагонисты рецепторов ангиотензина II при экспериментальном миокардите. Текущий фармацевтический дизайн. 2003;9(9):723–35. https://doi.org/10.2174/1381612033455440 PMid: 12570790. [PubMed] [Google Scholar]
61. Xiao J, Shimada M, Liu W, Hu D, Matsumori A. Противовоспалительные эффекты эплеренона при вирусном миокардите . Европейский журнал сердечной недостаточности. 2009 г.;11(4):349–53. https://doi.org/10.1093/eurjhf/hfp023 PMid: 19213804. [PubMed] [Google Scholar]
2009 г.;11(4):349–53. https://doi.org/10.1093/eurjhf/hfp023 PMid: 19213804. [PubMed] [Google Scholar]
62. Bohn D, Benson L. Диагностика и лечение детского миокардита. Детский препарат. 2002; 4: 171–181. https://doi.org/10.2165/00128072-200204030-00004 PMid: 11909009. [PubMed] [Google Scholar]
63. Sezai A, Hata M, Niino T, et al. Механическая поддержка кровообращения при молниеносном миокардите. Серж сегодня. 2008; 38: 773–777. https://doi.org/10.1007/s00595-007-3724-0 PMid: 1∯940. [PubMed] [Академия Google]
64. Потапов Е.В., Стиллер Б., Хетцер Р. Вентрикулярные вспомогательные устройства у детей: современные достижения и перспективы на будущее. Педиатр трансплантат. 2007; 11: 241–255. https://doi.org/10.1111/j.1399-3046.2006.00611.x PMid: 17430478. [PubMed] [Google Scholar]
65. Jones CB, Cassidy JV, Kirk R, et al. Успешный переход к выздоровлению с помощью механической поддержки в течение 120 дней у младенца с миокардитом. Трансплантация легкого сердца J. 2009; 28: 202–205. https://doi.org/10.1016/j.healun.2008.11.902 PMid: 19201349. [PubMed] [Google Scholar]
2009; 28: 202–205. https://doi.org/10.1016/j.healun.2008.11.902 PMid: 19201349. [PubMed] [Google Scholar]
66. Yuan Z, Shioji K, Kihara Y, Takenaka H, Onozawa Y, Kishimoto C. Кардиопротекторное действие карведилола при остром аутоиммунном миокардите: противовоспалительное действие, связанное с антиоксидантными свойствами. Американский журнал физиологии сердца и кровообращения. 2004; 286(1):H83–90. https://doi.org/10.1152/ajpheart.00536.2003 PMid: 14684360. [PubMed] [Google Scholar]
67. Yuan Z, Shioji K, Kihara Y, Takenaka H, Onozawa Y, Kishimoto C. Кардиопротекторные эффекты карведилола при остром аутоиммунном миокардите: противовоспалительное действие связано с антиоксидантным свойством. Американский журнал физиологии сердца и кровообращения. 2004; 286(1):H83–90. https://doi.org/10.1152/ajpheart.00536.2003 PMid: 14684360. [PubMed] [Google Scholar]
68. Dickstein K, Cohen-Solal A, Filippatos G, McMurray JJ, Ponikowski P, Poole-Wilson PA, Stromberg A, Van Veldhuisen DJ, Atar D, Hoes AW, Keren A. Linee guida ESC per la diagnosi e il trattamento dello scompenso hearto acuto e cronico 2008 = Руководство по диагностике и лечению острой и хронической сердечной недостаточности 2008. Giornale Итальяно ди Кардиология. 2009;10(3):141–98. [Академия Google]
Linee guida ESC per la diagnosi e il trattamento dello scompenso hearto acuto e cronico 2008 = Руководство по диагностике и лечению острой и хронической сердечной недостаточности 2008. Giornale Итальяно ди Кардиология. 2009;10(3):141–98. [Академия Google]
69. Хант С.А., Авраам В.Т., Чин М.Х., Фельдман А.М., Фрэнсис Г.С., Ганиатс Т.Г., Джессуп М., Констам М.А., Манчини Д.М., Михл К., Оутс Дж.А., Рахко П.С., Сильвер М.А., Стивенсон Л.В., Янси К.В. 2009 Специальное обновление включено в рекомендации ACC/AHA 2005 по диагностике и лечению сердечной недостаточности у взрослых: отчет Фонда Американского колледжа кардиологов/ Целевой группы Американской кардиологической ассоциации по практическим рекомендациям: разработан в сотрудничестве с Международным обществом сердца и трансплантация легких. J Am Coll Кардиол. 2009 г.;53:e1–e90. https://doi.org/10.1016/j.jacc.2008.11.013 PMid: 19358937. [PubMed] [Google Scholar]
70. Kühl U, Pauschinger M, Seeberg B, Lassner D, Nutsias M, Poller W, Шультайс ХП. Персистенция вируса в миокарде связана с прогрессирующей сердечной дисфункцией. Тираж. 2005; 112(13):1965–70. https://doi.org/10.1161/CIRCULATIONAHA.105.548156 PMid: 16172268. [PubMed] [Google Scholar]
Персистенция вируса в миокарде связана с прогрессирующей сердечной дисфункцией. Тираж. 2005; 112(13):1965–70. https://doi.org/10.1161/CIRCULATIONAHA.105.548156 PMid: 16172268. [PubMed] [Google Scholar]
71. Hia CP, Yip WC, Tai BC, et al. Иммуносупрессивная терапия при остром миокардите: систематический обзор за 18 лет. Арч Дис Чайлд. 2004;89: 580–584. https://doi.org/10.1136/adc.2003.034686 PMid: 15155409 PMCid: PMC1719952. [Бесплатная статья PMC] [PubMed] [Google Scholar]
72. Robinson JL, Hartling L, Crumley E, et al. Систематический обзор внутривенного гамма-глобулина для лечения острого миокардита. BMC Сердечно-сосудистые расстройства. 2005;5:12. https://doi.org/10.1186/1471-2261-5-12 PMid: 15932639 PMCid: PMC1173096. [Бесплатная статья PMC] [PubMed] [Google Scholar]
73. Maisch B, Pankuweit S. Современные варианты лечения (пери) миокардита и воспалительной кардиомиопатии. Герц. 2012;37(6):644–56. https://doi.org/10.1007/s00059-012-3679-9 PMid: 22996288. [PubMed] [Google Scholar]
74. Гельфанд Е.В. Внутривенный иммуноглобулин при аутоиммунных и воспалительных заболеваниях. Медицинский журнал Новой Англии. 2012;367(21):2015–25. https://doi.org/10.1056/NEJMra1009433 PMid: 23171098. [PubMed] [Google Scholar]
Гельфанд Е.В. Внутривенный иммуноглобулин при аутоиммунных и воспалительных заболеваниях. Медицинский журнал Новой Англии. 2012;367(21):2015–25. https://doi.org/10.1056/NEJMra1009433 PMid: 23171098. [PubMed] [Google Scholar]
75. Kuhn B, Shapiro ED, Walls TA, et al. Предикторы исхода миокардита. Педиатр Кардио. 2004; 25: 379–384. https://doi.org/10.1007/s00246-003-0568-2 PMid: 15085306. [PubMed] [Google Scholar]
76. Лин Ч., Чанг Дж. С., Ли ПК. Спасение острого фульминантного миокардита экстракорпоральной мембранной оксигенацией у педиатрических больных. Acta Pediatr Тайвань. 2005; 46: 201–205. Вечернее сообщение: 16381333. [PubMed] [Google Scholar]
77. Wu ET, Huang SC, Chen YS, et al. Дети с молниеносным миокардитом спасены экстракорпоральной мембранной оксигенацией. Слышать. 2006;92:1325–1326. https://doi.org/10.1136/hrt.2005.077511 PMid: 1690∅. [Бесплатная статья PMC] [PubMed] [Google Scholar]
78. Неонатальная ЭК. реестр организации экстракорпорального жизнеобеспечения (ELSO) nn Arbor, MI: 1995. Jul, [Google Scholar]
Jul, [Google Scholar]
79. Rajagopal SK, Almond CS, Laussen PC, et al. Экстракорпоральная мембранная оксигенация для поддержки младенцев, детей и молодых людей с острым миокардитом: обзор регистра организаций экстракорпорального жизнеобеспечения. Крит Уход Мед. 2010; 38: 382–387. https://doi.org/10.1097/CCM.0b013e3181bc8293 PMid: 19789437. [Бесплатная статья PMC] [PubMed] [Google Scholar]
80. Dennert R, Velthuis S, Schalla S, Eurlings L, van Suylen RJ, van Paassen P, Tervaert JW, Wolffs P, Goossens VJ, Bruggeman C, Waltenberger J. Внутривенная иммуноглобулиновая терапия для пациентов с идиопатической кардиомиопатией и подтвержденным биопсией эндомиокарда высоким PVB19вирусная нагрузка. Антивир Тер. 2010;15(2):193–201. https://doi.org/10.3851/IMP1516 PMid: 203↟4. [PubMed] [Google Scholar]
81. Берч М. Иммуносупрессивная терапия при миокардите у детей: все еще ожидаются доказательства [бесплатная статья PMC] [PubMed] [Google Scholar]
82. Camargo PR, Okay TS, Yamamoto L, Дель Негро ГМ, Лопес АА. Миокардит у детей и обнаружение вирусов в ткани миокарда: значение иммуносупрессивной терапии. Международный журнал кардиологии. 2011;148(2):204–8. https://doi.org/10.1016/j.ijcard.2009.11.002 PMid: 19945184. [PubMed] [Google Scholar]
Миокардит у детей и обнаружение вирусов в ткани миокарда: значение иммуносупрессивной терапии. Международный журнал кардиологии. 2011;148(2):204–8. https://doi.org/10.1016/j.ijcard.2009.11.002 PMid: 19945184. [PubMed] [Google Scholar]
83. Teele SA, Allan CK, Laussen PC, Newburger JW, Gauvreau K, Thiagarajan RR. Лечение и исходы у детей с острым фульминантным миокардитом. Журнал педиатрии. 2011;158(4):638–43. https://doi.org/10.1016/j.jpeds.2010.10.015 PMid: 21195415. [PubMed] [Google Scholar]
угрожающее жизни событие. Клиническая педиатрия. 2003;42(7):649–52. https://doi.org/10.1177/000992280304200713 PMid: 14552526. [PubMed] [Google Scholar]
85. Kim HS, Sohn S, Park JY, Seo JW. Фульминантный миокардит успешно лечится высокими дозами иммуноглобулина. Международный журнал кардиологии. 2004;96(3):485–6. https://doi.org/10.1016/j.ijcard.2003.05.037 PMid: 15301907. [PubMed] [Google Scholar]
86. Wang CY, Li Lu F, Wu MH, et al. Смертельная инфекция вирусом Коксаки А16.

 Обязательны занятия ЛФК. Лекарственная
терапия включает следующие препараты.
Обязательны занятия ЛФК. Лекарственная
терапия включает следующие препараты.