Кератокиста челюсти: Кератокиста — лечение и удаление
Кератокиста — лечение и удаление
В Центре челюстно-лицевой хирургии и имплантологии проводится лечение и удаление такого доброкачественного образования верхней или нижней челюсти как кератокиста.
Что такое челюстные кисты, причины их появления и симптоматика
Профилактика и лечение заболеваний зубов пропагандируется с раннего детства, поэтому большинство из нас ответственно подходит к этому вопросу. Однако мало кто знает, что в ротовой полости могут возникать и другие проблемы, которые часто требуют хирургического вмешательства. Речь идет о челюстных кистах. Согласно статистике, это совсем не редкое явление и множество пациентов обращается к стоматологам с такого рода проблемами. Что же собой представляет киста челюсти и как следует лечить данную патологию? Виды и особенности кист челюстей Киста представляет собой тканевую полость, которая выстлана изнутри эпителием и заполнена жидкостью. Возникает такое новообразование в результате дегенерации ткани прорезывающихся зубов или тех зубов, которые только развиваются. Согласно медицинским данным, киста нижней челюсти встречается в три раза реже, чем киста верхней челюсти. При этом как киста нижней челюсти, так и киста верхней челюсти может привести к таким неприятным последствиям, как остеомиелит, поэтому лечить кисту нужно обязательно. В стоматологии диагностируют три вида кист челюсти: радикулярную кисту челюсти, фолликулярную и примордиальную кисту челюсти (кератокисту).
Согласно медицинским данным, киста нижней челюсти встречается в три раза реже, чем киста верхней челюсти. При этом как киста нижней челюсти, так и киста верхней челюсти может привести к таким неприятным последствиям, как остеомиелит, поэтому лечить кисту нужно обязательно. В стоматологии диагностируют три вида кист челюсти: радикулярную кисту челюсти, фолликулярную и примордиальную кисту челюсти (кератокисту).
Речь идет о кисте нижней челюсти, возникающей на месте образования зуба мудрости. Она представляет собой мягкое тканевое образование с тонкими стенками, заполненное особенным веществом — холестеатомой. Такая киста может быть многокамерной или однокамерной.
Ее появление обычно протекает бессимптомно, не вызывает болезненности или дискомфорта, и чаще всего обнаруживается врачом случайно при проведении рентгенологического исследования по какому-то иному поводу. Киста может развиваться довольно длительное время от нескольких месяцев до нескольких лет не вызывать беспокойства.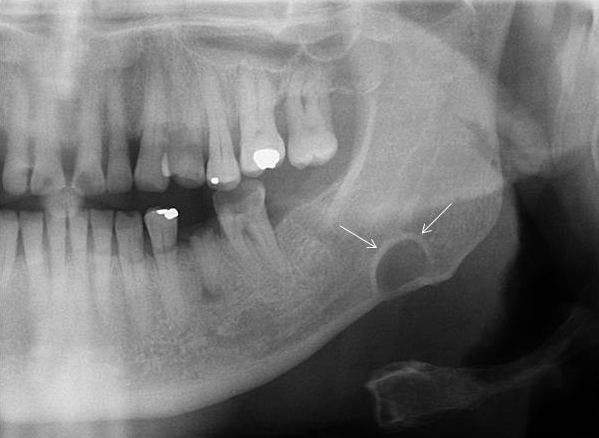 Тем не менее, при обнаружении этого новообразования необходимо провести соответствующее лечение, иначе киста может со временем увеличиться в размерах, множиться, стать источником инфекции ротовой полости, воспалиться, а также послужить причиной разрушения (рассасывания) челюстной кости.
Тем не менее, при обнаружении этого новообразования необходимо провести соответствующее лечение, иначе киста может со временем увеличиться в размерах, множиться, стать источником инфекции ротовой полости, воспалиться, а также послужить причиной разрушения (рассасывания) челюстной кости.
Лечение челюстных кист
На начальных стадиях развития кератокисты может быть достаточно электролечения, и врач-терапевт назначит процедуру депофорез. При значительных размерах кисты необходимо хирургическое вмешательство, которое проводится под местной или общей анестезией.
Для лечения челюстных кист стоматологи прибегают к оперативному лечению. Проводя цистостомию и цистэктомию, иногда корневые кисты хорошо поддаются лечению без оперативных вмешательств. Но осложнения кист и их нагноения требуют обязательного вскрытия с последующим дренированием полости.
Основная задача хирургического лечения — сохранить зубы, которые находятся в зоне кисты, и восстановить их нарушенные функции. Цистэктомия помимо вскрытия полости кисты позволяет одномоментно произвести резекцию корня зуба.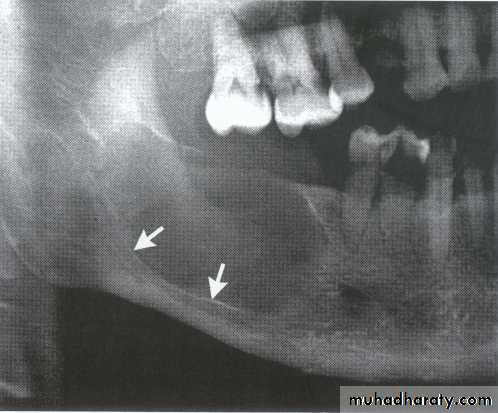 Эту процедуру проводят, если корень зуба погружен в полость кисты не более, чем на 1/3 всей его длины. Если же погружение более глубокое, то зубы становятся непригодными с точки зрения функциональности и довольно рано выпадают. Основной недостаток этого метода в том, что после резекции, снижается функциональность зубов, отмечаются случаи реинфекции со стороны срезанных микроканальцев, кроме этого операция довольно травматична. Костные полости, которые остаются после резекции снижают прочность челюстных костей. Современные технологии позволяют улучшить процедуру цистэктомии. Биокомпозитный материал, которым заполняют костную полость, предотвращает возникновение ранних осложнений. Это связано с отсутствием кровяного сгустка, что значительно снижает инфицирование полости. Биокомпозитные материалы, заполняя полость кисты, способствуют восстановлению формы и функций челюсти за счет ускорения регенерации.
Эту процедуру проводят, если корень зуба погружен в полость кисты не более, чем на 1/3 всей его длины. Если же погружение более глубокое, то зубы становятся непригодными с точки зрения функциональности и довольно рано выпадают. Основной недостаток этого метода в том, что после резекции, снижается функциональность зубов, отмечаются случаи реинфекции со стороны срезанных микроканальцев, кроме этого операция довольно травматична. Костные полости, которые остаются после резекции снижают прочность челюстных костей. Современные технологии позволяют улучшить процедуру цистэктомии. Биокомпозитный материал, которым заполняют костную полость, предотвращает возникновение ранних осложнений. Это связано с отсутствием кровяного сгустка, что значительно снижает инфицирование полости. Биокомпозитные материалы, заполняя полость кисты, способствуют восстановлению формы и функций челюсти за счет ускорения регенерации.
Прогноз после оперативного лечения благоприятный, однако, крупные челюстные кисты могут осложняться патологическими переломами челюсти.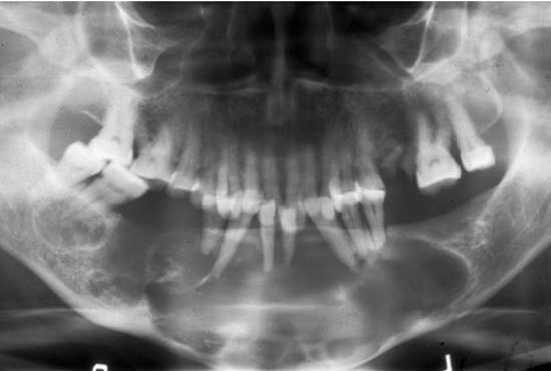
В Центре челюстно-лицевой хирургии и имплантологии эта операция проводится хирургами высшей категории с использованием самого современного оборудования и новейших анестезирующих препаратов. В сложных случаях послеоперационная реабилитация может быть проведена в условиях собственного стационара, которым располагает Центр. Уютные палаты, комфортные условия и постоянное медицинское наблюдение сделают период восстановления легким и приятным для пациента.
CLDH: Кератокиста. Клинический случай
20.09.2019
Кератокисты челюстных костей составляют по данным разных авторов от 5,4 до 17,4% от всех одонтогенных кист (Kreidler J.F., 1993, Cawson R.A., Odell E.W., 1998). В некоторых случаях кератокисты включаются в симптомокомплекс при врожденной патологии (синдром Горлина, синдром Марфана и др.).
Специфика клинического проявления кератокист заключается в том, что эти образования не имеют четких характерных симптомов, позволяющих уверенно диагностировать их до оперативного вмешательства.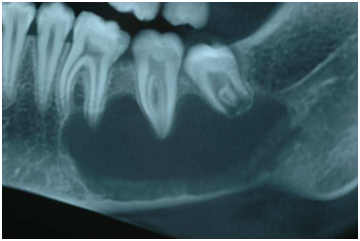 И только в тех случаях, когда киста достигает больших размеров, могут появиться симптомы в виде деформации челюсти, нарушения прорезывания зубов или их смещения.
И только в тех случаях, когда киста достигает больших размеров, могут появиться симптомы в виде деформации челюсти, нарушения прорезывания зубов или их смещения.
Небольшие кератокисты могут локализоваться в периапикальных тканях, напоминая околокорневые воспалительные кисты или окружать коронку непрорезавшегося зуба, имитируя фолликулярную кисту (зубосодержадцою).
Известно, что кератокисты челюстей имеют тенденцию к рецидивированию даже через несколько лет после операции. Возможность рецидивирования, а также схожесть рентгенологического проявления кератокисты больших размеров с амелобластомой и другими кистовидными новообразованиями (одонтогенными воспалительными кистами, фолликулярными кистами, одонтоамелобластомой, остеокластомой) позволяет ряду авторов относить их к новообразованиям, обладающих агрессивным ростом. В последней гистологической классификации Организации Всемирного Здравоохранения (2005) одонтогенных опухолей — Pathology and Genetics, Head and Neck Tumours — кератокисты отнесены к опухолям и называются -«доброкачественная кератокистозная одонтогенная опухоль».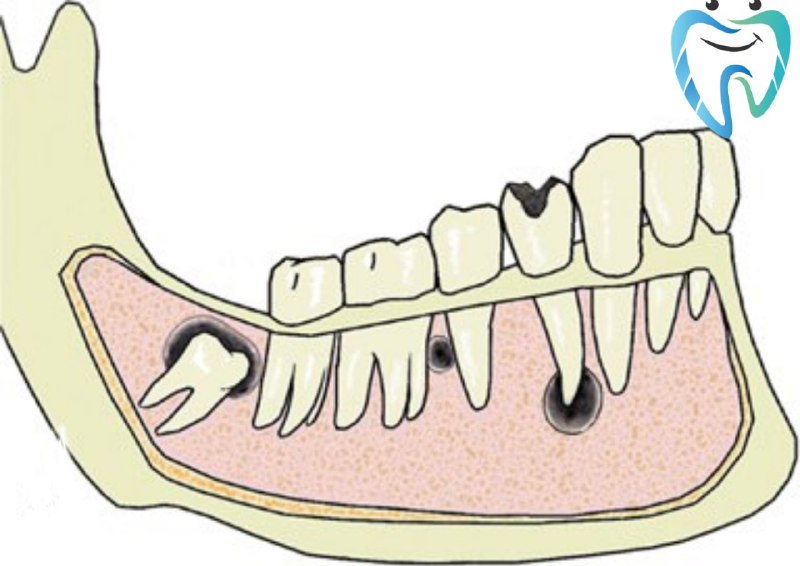
Патогистологическое исследование диагностического операционного материала имеет решающее значение в постановке диагноза, но иногда предшествующие операции нагноения делают затруднительной патогистологическую верификацию, так как разрушается их характерная эпителиальная выстилка.
Относительно лечения кератокисты нет единого мнения. Лечебная тактика при кератокистах челюстей должна быть направлена на полное удаление кистозной оболочки, так как она способна рецидивировать.
Предложены разные методы лечения: цистэктомия, цистотомия-эктомия, обработка кистозной полости химическими препаратами, с криодеструкцией, и т.п. Некоторые авторы, учитывая склонность кератокист к рецидивированию, отдают предпочтение радикальному подходу в лечении — резекции челюстной кости.
В литературе крайне мало работ, посвященных этиологии, клиническим проявлениям, особенностям роста кератокист в детском возрасте. В имеющихся исследованиях не отражена специфика морфологического строения оболочки в детском возрасте, связь ее с окружающей костной тканью, корнями и зачатками зубов, надкостницей, мягкими тканями. Отсутствуют чёткие рекомендации выбора адекватного метода лечения (цистотомия, цистэктомия или резекция костной ткани) в зависимости от возраста больного, размеров и локализации образования.
Отсутствуют чёткие рекомендации выбора адекватного метода лечения (цистотомия, цистэктомия или резекция костной ткани) в зависимости от возраста больного, размеров и локализации образования.
Мы стали свидетелями удаления кератокисты у девочки 12-ти лет.
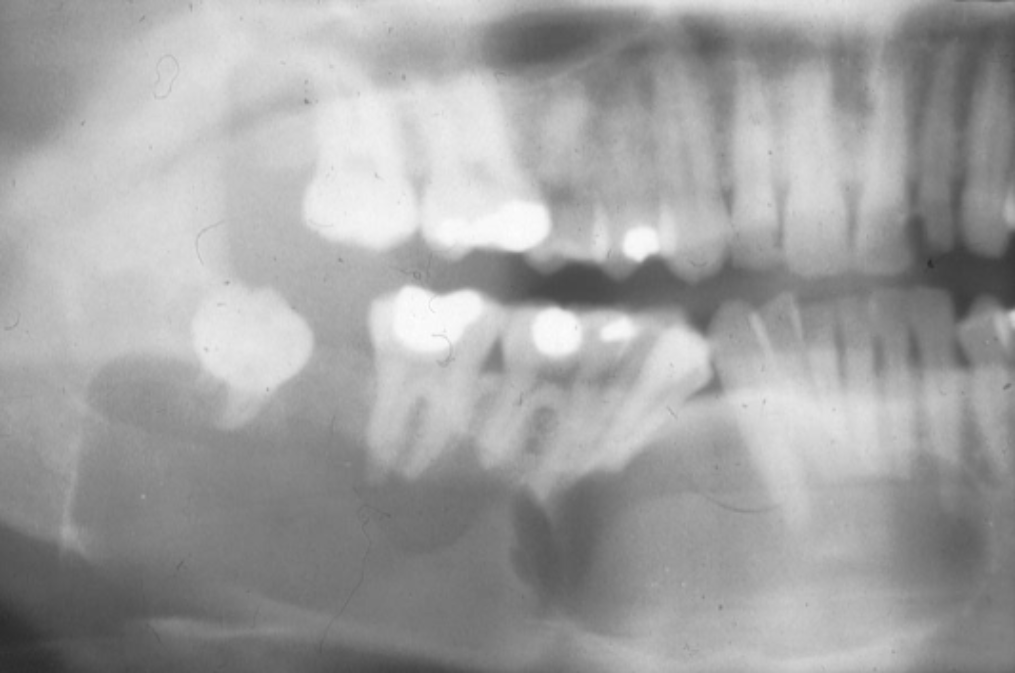
На рентгенологических снимках видна характерная картина: новообразование находиться в типичном для кертокисты месте имеет структуру зуба полностью в объемном образовании и белесое молочное содержимое.
Удаление кератокисты произошло на базе клиники ОХМАДЕТ
Опубликовано в Статьи
Двусторонняя одонтогенная кератоциста нижней челюсти
1. Fickling BW. Кисты челюстей: многолетняя хирургия, виды и лечение. Proc R Soc Med. 1965; 58: 847–854. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2. Фалаки Ф., Делавариан З., Салехинежад Дж., Сагафи С. Плоскоклеточный рак, возникающий из одонтогенной кератоцисты: клинический случай. Med Оральный патол Oral Cir Bucal. 2009;14(4):E171–E174. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
3. Jensen J, Sinde-Pedersen S, Simonsen EK. Сравнительное исследование лечения кератоцист путем энуклеации или энуклеации в сочетании с криотерапией: предварительный отчет. J Краниомаксиллофак Хирург. 1988;16(8):362–365. doi: 10.1016/S1010-5182(88)80080-5. [PubMed] [CrossRef] [Google Scholar]
4. Irvine GH, Bowerman JE. Кератоцисты нижней челюсти: хирургическое лечение. Br J Oral Maxillofac Surg. 1985;23(3):204–209. doi: 10.1016/0266-4356(85)-9. [PubMed] [CrossRef] [Google Scholar]
5. Шмидт Б.Л., Погрель М.А. Применение энуклеации и криотерапии жидким азотом при лечении одонтогенных кератоцист. J Oral Maxillofac Surg. 2001;59(7):720–725. doi: 10.1053/joms.2001.24278. [PubMed] [CrossRef] [Академия Google]
6. Столинга П.Я. Долгосрочное наблюдение за кератоцистами, пролеченными в соответствии с определенным протоколом. Int J Oral Maxillofac Surg. 2001;30(1):14–25. doi: 10.1054/ijom.2000.0027. [PubMed] [CrossRef] [Google Scholar]
7. Bataineh AB, Al Qudah M. Лечение одонтогенных кератоцист нижней челюсти. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 1998;86(1):42–47. doi: 10.1016/S1079-2104(98)
Bataineh AB, Al Qudah M. Лечение одонтогенных кератоцист нижней челюсти. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 1998;86(1):42–47. doi: 10.1016/S1079-2104(98)
8. Haring JI, Van Dis ML. Одонтогенная кератоциста: клиническое, рентгенологическое и гистопатологическое исследование. Оральный хирург Oral Med Oral Pathol. 1988;66(1):145–153. doi: 10.1016/0030-4220(88)-5. [PubMed] [CrossRef] [Google Scholar]
9. Шир М. Агрессивный характер одонтогенной кератоцисты: доброкачественное ли это кистозное новообразование? Часть 1. Клинические и ранние экспериментальные признаки агрессивного поведения. Оральный онкол. 2002;38(3):219–226. doi: 10.1016/S1368-8375(01)00065-3. [PubMed] [CrossRef] [Google Scholar]
10. Браннон Р.Б. Одонтогенная кератоциста: клинико-патологическое исследование 312 случаев. Часть II. Гистологические особенности. Oral Surg Oral MedOral Pathol. 1977;43(2):233–255. doi: 10.1016/0030-4220(77)
-X.
 [PubMed] [CrossRef] [Google Scholar]
[PubMed] [CrossRef] [Google Scholar]11. Браннон Р.Б., полковник Л. Одонтогенная кератоциста: клинико-патологическое исследование 312 случаев I клинических признаков. Оральный хирург Oral Med Oral Pathol. 1976;42(1):54–72. doi: 10.1016/0030-4220(76)
-1. [PubMed] [CrossRef] [Google Scholar]12. Райт Дж.М. Одонтогенная кератоциста: ортокератинизированный вариант. Oral Surg Oral Med Oral Pathol. 1981; 51 (6): 609–618. doi: 10.1016/S0030-4220(81)80011-4. [PubMed] [CrossRef] [Академия Google]
13. Браун Р.М. Одонтогенные кератоцисты. Клинические аспекты. Бр Дент Дж. 1970;128(5):225–231. doi: 10.1038/sj.bdj.4802449. [PubMed] [CrossRef] [Google Scholar]
14. Forssell K, Forssell H, Kahnberg KE. Рецидив кератоцист: долгосрочное последующее исследование. Int J Oral Maxillofac Surg. 1988;17(1):25–28. doi: 10.1016/S0901-5027(88)80224-8. [PubMed] [CrossRef] [Google Scholar]
15. Ogunsalu C, Daisley H, Kamta A, Kanhai D, Mankee M, Maharaj A. Одонтогенная кератоциста на Ямайке: обзор пяти новых случаев и пяти случаев рецидива вместе с сравнительный анализ четырех методов лечения. West Indian Med J. 2007; 56 (1): 90–95. doi: 10.1590/S0043-31442007000100017. [PubMed] [CrossRef] [Google Scholar]
West Indian Med J. 2007; 56 (1): 90–95. doi: 10.1590/S0043-31442007000100017. [PubMed] [CrossRef] [Google Scholar]
16. Ода Д., Ривера В., Гани Н., Кенни Э.А., Доусон К.Х. Одонтогенная кератоциста: опыт Северо-Западного УЗИ. J Контемп Дент Практ. 2000;1(2):60–74. [PubMed] [Google Scholar]
17. Yoshiura K, Higuchi Y, Ariji Y, Shinohara M, Yuasa K, Nakayama E, et al. Повышенное затухание одонтогенной кератоцисты при компьютерной томографии: новое открытие. Дентомаксиллофак Радиол. 1994;23(3):138–142. дои: 10.1259/дмфр.23.3.7530666. [PubMed] [CrossRef] [Google Scholar]
18. Minami M, Kaneda T, Ozawa K, Yamamoto H, Itai Y, Ozawa M, et al. Кистозные поражения челюстно-нижнечелюстной области: отличие одонтогенной кератоцисты и амелобластомы от других кист на МРТ. AJR Am J Рентгенол. 1996;166(4):943–949. doi: 10.2214/ajr.166.4.8610578. [PubMed] [CrossRef] [Google Scholar]
19. Ninomiya T, Kubota Y, Koji T, Shirasuna K. Марсупиализация ингибирует экспрессию интерлейтина-1 альфа и пролиферацию эпителиальных клеток в одонтогенных кератоцистах.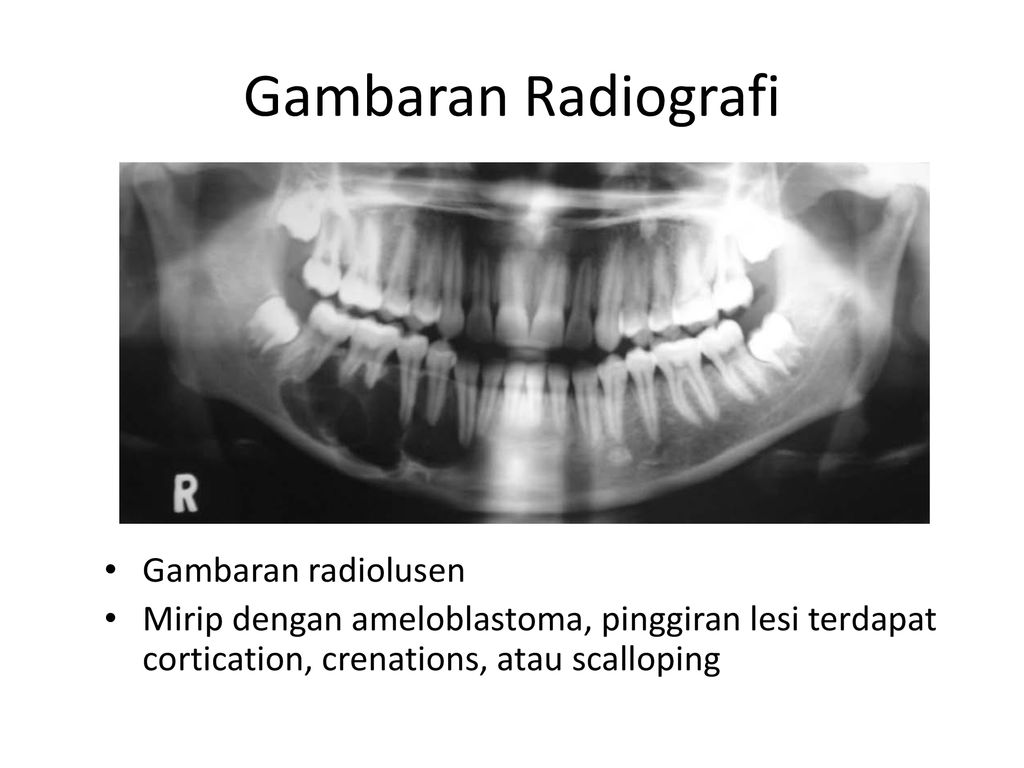 Дж Орал Патол Мед. 2002;31(9): 526–533. doi: 10.1034/j.1600-0714.2002.00029.x. [PubMed] [CrossRef] [Google Scholar]
Дж Орал Патол Мед. 2002;31(9): 526–533. doi: 10.1034/j.1600-0714.2002.00029.x. [PubMed] [CrossRef] [Google Scholar]
20. Погрел М.А., Джордан Р.С. Марсупиализация как окончательное лечение одонтогенной кератоцисты. J Oral Maxillofac Surg. 2004;62(6):651–655. doi: 10.1016/j.joms.2003.08.029. [PubMed] [CrossRef] [Google Scholar]
21. August M, Faquin WC, Troulis M, Kaban LB. Дифференциация одонтогенных кератоцист от неороговевающих кист с помощью тонкоигольной аспирационной биопсии и окрашивания цитокератином-10. J Oral Maxillofac Surg. 2000;58(9): 935–940. doi: 10.1053/joms.2000.8731. [PubMed] [CrossRef] [Google Scholar]
22. Piattelli A, Fioroni M, Rubini C. Дифференциация одонтогенных кератоцист от других одонтогенных кист по экспрессии иммунореактивности bcl-2. Оральный онкол. 1998;34(5):404–407. doi: 10.1016/S1368-8375(98)00026-8. [PubMed] [CrossRef] [Google Scholar]
23. Yonetsu K, Bianchi JG, Troulis JM, Curtin HD. Необычное появление на КТ одонтогенной кератоцисты Mnadible: клинический случай. AJNR Am J Нейрорадиол. 2001; 22(10):1887–1889.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
AJNR Am J Нейрорадиол. 2001; 22(10):1887–1889.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
24. Freitas DQ, Tempest LM, Sicoli E, Lopes Neto FC. Двусторонние зубочелюстные кисты: обзор литературы и отчет о необычном случае. Дентомаксиллофак Радиол. 2006;35(6):464–468. doi: 10.1259/dmfr/26194891. [PubMed] [CrossRef] [Google Scholar]
25. Dunsche A, Babendererde O, Luttges J, Springer IN. Зубочелюстная киста против однокистозной амелобластомы — дифференциальный диагноз в рутинной гистологии. Дж Орал Патол Мед. 2003; 32(8):486–49.1. doi: 10.1034/j.1600-0714.2003.00118.x. [PubMed] [CrossRef] [Google Scholar]
26. Горлин Р.Дж. Синдром невоидной базально-клеточной карциномы. Дирматол клин. 1995;13(1):113–125. [PubMed] [Google Scholar]
27. Altas E, Karasen RM, Yilmaz AB, Aktan B, Kocer I, Erman Z. Случай большой зубочелюстной кисты, содержащей клык в антральном отделе верхней челюсти, что привело к эпифоре. Ж Ларынгол Отол. 1997;111(7):641–643. doi: 10. 1017/S0022215100138198. [PubMed] [CrossRef] [Академия Google]
1017/S0022215100138198. [PubMed] [CrossRef] [Академия Google]
28. Горлин Р.Дж. Синдром невоидной базально-клеточной карциномы (Горлина) без ответа. J Lab Clin Med. 1999;134(6):551–552. doi: 10.1016/S0022-2143(99)
-6. [PubMed] [CrossRef] [Google Scholar]29. Kimonis VE, Goldstein AM, Pastakia B, Yang ML, Kase R, Di Giovanna JJ, et al. Клинические проявления у 105 больных с синдромом базалиомы. Am J Med Genet. 1997;69(3):299–308. doi: 10.1002/(SICI)1096-8628(19970331)69:3<299::AID-AJMG16>3.0.CO;2-M. [PubMed] [CrossRef] [Академия Google]
30. Madras J, Lapointe H. Кератокистозная одонтогенная опухоль: реклассификация одонтогенной кератоцисты из кисты в опухоль. J Can Dent Assoc. 2008;74(2):165–175. [PubMed] [Google Scholar]
31. Voorsmit RA, Stoelinga PJ, van Haelst UJ. Лечение кератоцист. J Maxillofac Surg. 1981;9(4):228–236. doi: 10.1016/S0301-0503(81)80049-5. [PubMed] [CrossRef] [Google Scholar]
32. Holmlund A, Anneroth G, Lundquist G, Nordenram A. Возникновение амелобластомы из одонтогенной кисты. Дж Орал Патол Мед. 1991;20(1):318–321. doi: 10.1111/j.1600-0714.1991.tb00937.x. [PubMed] [CrossRef] [Google Scholar]
Возникновение амелобластомы из одонтогенной кисты. Дж Орал Патол Мед. 1991;20(1):318–321. doi: 10.1111/j.1600-0714.1991.tb00937.x. [PubMed] [CrossRef] [Google Scholar]
33. Sokler K, Grgurevic J, Kobler P, Josko Grgurevic. Хирургическое лечение одонтогенных кератоцист методом внутриротовой послеоперационной аспирации. Акта Стоматол Хорват. 2003;37(1):2003. [Google Scholar]
34. Уильямс Т.П., Коннор Ф.А., мл. Хирургическое лечение одонтогенной кератоцисты: агрессивный подход. J Oral Maxillofac Surg. 1994;52(9):964–966. doi: 10.1016/S0278-2391(10)80081-3. [PubMed] [CrossRef] [Академия Google]
35. Zhang L, Sun ZJ, Zhao YF, Bian Z, Fan MW, Chen Z. Ингибирование стратегии молекулярного лечения сигнального пути SHH при одонтогенных кератоцистах. Мед Гипотезы. 2006;67(5):1242–1244. doi: 10.1016/j.mehy.2006.04.062. [PubMed] [CrossRef] [Google Scholar]
Одонтогенная кератоциста: что в названии?
J Nat Sci Biol Med. 2013 июль-декабрь; 4(2): 282–285.
doi: 10. 4103/0976-9668.116968
4103/0976-9668.116968
, , , и
Информация об авторе Информация об авторских правах и лицензии Отказ от ответственности
Классификация одонтогенных кист сложна и может создать путаницу как для клиницистов, так и для патологоанатомов. Одонтогенная кератоциста (ОКК) представляет собой загадочную развивающуюся кисту, которая заслуживает особого внимания. Он имеет характерные гистопатологические и клинические особенности; но что делает эту кисту особенной, так это ее агрессивное поведение и высокая частота рецидивов. Несмотря на множество классификаций и номенклатур, к сожалению, клиницисты все еще сталкиваются с трудностями при лечении этого часто встречающегося поражения челюстей. Эта статья представляет собой попытку предоставить обзор различных аспектов OKC с акцентом на номенклатуру, рецидивы, молекулярные аспекты и лечение OKC.
Ключевые слова: Классификация, керато-кистозная одонтогенная опухоль, номенклатура, одонтогенная кератоциста, одонтогенная киста, одонтогенная опухоль
Одонтогенные кисты являются относительно частыми поражениями и составляют большую часть всех биопсий, полученных любой патологоанатомической службой. Эта разнообразная группа поражений демонстрирует различные проявления: от небольшого безобидного поражения, которое может быть обнаружено случайно, до очень агрессивного и деструктивного поражения, которое может даже трансформироваться в злокачественное новообразование. Среди последних наиболее известны одонтогенные кератоцисты (ОКК).
Эта разнообразная группа поражений демонстрирует различные проявления: от небольшого безобидного поражения, которое может быть обнаружено случайно, до очень агрессивного и деструктивного поражения, которое может даже трансформироваться в злокачественное новообразование. Среди последних наиболее известны одонтогенные кератоцисты (ОКК).
OKC – одна из редких одонтогенных кист, привлекающая внимание многих исследователей благодаря своим уникальным характеристикам. OKC возникает из остатков зубной пластинки на нижней и верхней челюстях до завершения одонтогенеза. Он также может происходить из базальных клеток вышележащего эпителия. OKC был впервые идентифицирован и описан в 1876 году. Далее он был классифицирован Phillipsen в 1956 году. В 1962 году Pindborg и Hansen предложили гистологические критерии, необходимые для диагностики OKC. В последние годы Всемирная организация здравоохранения (ВОЗ) рекомендовала термин кистозное новообразование (теперь известное как кератокистозная одонтогенная опухоль (ККО)) для этого поражения, поскольку оно лучше отражает агрессивное клиническое поведение, гистологически высокую скорость митоза и связь с генетическими и хромосомными аномалиями. OKC — загадочная киста развития, заслуживающая особого внимания. OKC демонстрирует предполагаемый высокий потенциал роста и высокую частоту рецидивов из-за своей природы формирования компартментов внутри.
OKC — загадочная киста развития, заслуживающая особого внимания. OKC демонстрирует предполагаемый высокий потенциал роста и высокую частоту рецидивов из-за своей природы формирования компартментов внутри.
Эти поражения представляют большую трудность для хирургов и патологоанатомов. Хирурги с самого начала экспериментировали с методами лечения OKC, чтобы найти способ лечения без рецидивов. С другой стороны, выдающиеся патологоанатомы изо всех сил пытались определить истинную природу OKC, чтобы можно было разработать определенную линию действий.
В течение многих лет оральные патологи пытались понять природу, идентификацию и лечение заболеваний, поражающих ротовую и челюстно-лицевую области. В этом процессе все, что было достигнуто, — это классифицировать, классифицировать и переклассифицировать эти болезни.
Ранее было предпринято много попыток логически классифицировать эти кисты. Все началось еще в 1887 году, когда Бланд-Саттон разделил одонтомы на кисты. Позже Гэбелл, Джеймс и Пейн в 1914 году; Тома и Гольдман в 1946 году; Пиндборг и Клаузен, 1958 г . ; Всемирная организация здравоохранения (ВОЗ) в 1971 г.; и, наконец, ВОЗ в 1992 году последовала этому ритуалу классификации и переклассификации одонтогенных кист.[1]
; Всемирная организация здравоохранения (ВОЗ) в 1971 г.; и, наконец, ВОЗ в 1992 году последовала этому ритуалу классификации и переклассификации одонтогенных кист.[1]
Несмотря на множество классификаций и номенклатур, к сожалению, клиницисты все еще сталкиваются с трудностями при лечении этого часто встречающегося поражения челюстей. Эта статья представляет собой попытку предоставить обзор различных аспектов OKC с акцентом на номенклатуру, рецидивы, молекулярные аспекты и лечение OKC.
«Холестеатома»
Одонтогенная кератоциста (ОКК) представляет собой загадочную развивающуюся кисту, которую Микулич в 1876 году впервые описал как часть семейного заболевания, поражающего челюсти. Однако в 1926 году она была впервые известна как «холестеатома».[2] Холестеатома просто означает кистозную или «открытую» массу кератиновых чешуек с живой «матрицей».[3] Чтобы узнать историю этой загадочной кисты, мы должны взглянуть на учет кист челюстей в целом. Кистозные опухоли челюстей впервые были описаны Скультетом в 1654 г. , и только в 1728 г. Фошар предположил, что они могут быть связаны с зубами. Кисты были обнаружены задолго до изобретения рентгеновских лучей в 189 г.6, Джоном Хантером, описавшим кисту зуба в 1774 году.[5] Продолжалась серия статей Фошара по описанию кист зубов. Paget’s в 1853 г. ввел термин «зубная киста». происхождения, так как они возникли из остатков пластинки зуба или эмалевых органов до того, как произошло формирование эмали. Forssell и Sainio [8] отдали предпочтение термину «примордиальная киста» и показали, что в этих поражениях (настоящие кератоцисты) эпителий был отчетливо паракератотическим с базальными клетками кубической или столбчатой формы, а иногда и ортокератотическим.
, и только в 1728 г. Фошар предположил, что они могут быть связаны с зубами. Кисты были обнаружены задолго до изобретения рентгеновских лучей в 189 г.6, Джоном Хантером, описавшим кисту зуба в 1774 году.[5] Продолжалась серия статей Фошара по описанию кист зубов. Paget’s в 1853 г. ввел термин «зубная киста». происхождения, так как они возникли из остатков пластинки зуба или эмалевых органов до того, как произошло формирование эмали. Forssell и Sainio [8] отдали предпочтение термину «примордиальная киста» и показали, что в этих поражениях (настоящие кератоцисты) эпителий был отчетливо паракератотическим с базальными клетками кубической или столбчатой формы, а иногда и ортокератотическим.
«Одонтогенная кератоциста»
Филипсен в 1956 году[9], будучи еще студентом-стоматологом старшего курса, работавшим с Йенсом Дж. Пиндборгом в Копенгагене, назвал и описал «одонтогенную кератоцисту». Обозначение «кератоциста» использовалось для описания любой кисты челюсти, в которой в значительной степени образовался кератин.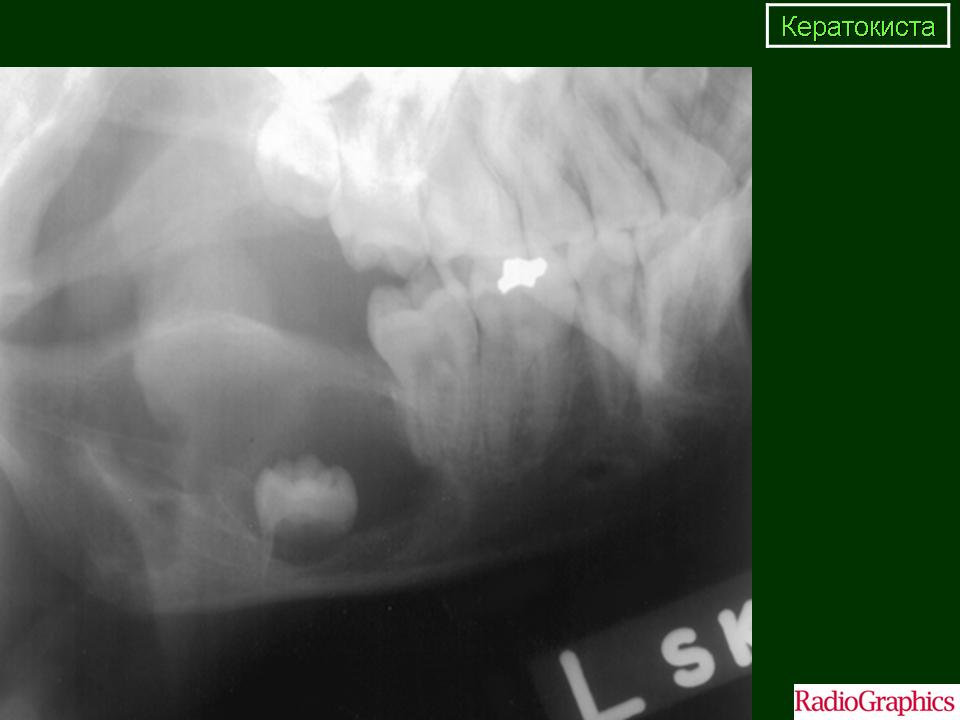 Гистопатология OKC типична и хорошо охарактеризована.[9] Он включает: тонкую однородную выстилку из многослойного плоского эпителия с тенденцией к отслоению от подлежащей соединительнотканной капсулы; тонкий гофрированный поверхностный слой паракератина; слой шиповидных клеток толщиной от 8 до 4 клеток, часто с внутриклеточным отеком; плоское соединение эпителиально-волокнистой ткани, обычно лишенное эпителиальных сетчатых гребней; и относительно тонкая фиброзная капсула, в которой отсутствует воспалительный клеточный инфильтрат.
Гистопатология OKC типична и хорошо охарактеризована.[9] Он включает: тонкую однородную выстилку из многослойного плоского эпителия с тенденцией к отслоению от подлежащей соединительнотканной капсулы; тонкий гофрированный поверхностный слой паракератина; слой шиповидных клеток толщиной от 8 до 4 клеток, часто с внутриклеточным отеком; плоское соединение эпителиально-волокнистой ткани, обычно лишенное эпителиальных сетчатых гребней; и относительно тонкая фиброзная капсула, в которой отсутствует воспалительный клеточный инфильтрат.
Доброкачественное новообразование?
Пиндборг и Хансен[10] были первыми, кто указал на агрессивное поведение OKC. Toller [4] еще в 1967 году предположил, что OKC следует рассматривать как доброкачественное новообразование, а не как обычную кисту, в основном из-за их клинического поведения. Альфорс и др. [11] в 1984 г. предложили классифицировать ОКК как доброкачественное кистозное эпителиальное новообразование и предложили модифицированные схемы лечения.
Shear [12] опубликовал свою обширную работу об агрессивной природе одонтогенной кератоцисты и, наконец, назвал ее доброкачественной кистозной опухолью. Шир агрессивно использовал термин «кератоцистома» в названии этой кисты.
Regezi и др. [13] попытались объяснить патогенетические механизмы OKC. Они упоминают механизмы, которые способствуют росту и распространению OKC, — это высокая скорость пролиферации, избыточная экспрессия антиапоптотических белков (bcl-2) и экспрессия матриксной металлопротеиназы (MMP 2 и 9). Мутация в гене PTCH 1 («заплата») также рассматривается как ответственная за патогенез этой кисты. [14] Большая степень вариаций в этих отчетах связана главным образом с тем, что некоторые серии включали кисты у пациентов с синдромом невоидной базально-клеточной карциномы (NBCCS), в то время как другие причины этих вариаций могут быть связаны с продолжительностью периода наблюдения и используемым методом лечения. [14]
В 1976 г. Brannon [15] предложил три механизма рецидива OKC: неполное удаление слизистой оболочки кисты, рост нового OKC из сателлитных кист (или одонтогенных остатков, оставшихся после операции) и развитие нового OKC в соседнем область.
Гистопатологические признаки, позволяющие прогнозировать рецидивы.
Основными признаками, которые можно учитывать для прогнозирования рецидивов ОКК, являются
Более высокий уровень пролиферативной активности клеток в эпителии
Почкование в базальном слое эпителия
Паракератинизация поверхностного слоя
Надэпителиальное расщепление эпителиальной выстилки
Субэпителиальный раскол эпителиальной выстилки
Наличие остатков/клетки остатки, а также дочерние кисты.
Переименован в
Между тем, Reichart и Philipsen [16] реклассифицировали одонтогенные опухоли в 2002 г. и переименовали OKC в ороговевающую кистозную одонтогенную опухоль (KCOT) и поместили ее в подзаголовок «доброкачественное новообразование одонтогенного эпителия со зрелой фиброзной стромой». ; одонтогенная эктомезенхима отсутствует». Эта классификация была одобрена ВОЗ/IARC на Редакционно-консенсусной конференции, состоявшейся в Лионе, Франция, в июле 2003 г. , и в настоящей классификации OKC был переименован в «кератокистозную одонтогенную опухоль» (КОТ). КОТ в настоящее время определяется как «доброкачественная моно- или мультикистозная внутрикостная опухоль одонтогенного происхождения с характерной выстилкой из паракератинизированного многослойного плоского эпителия и потенциалом для агрессивного инфильтративного поведения». [3] ВОЗ «рекомендует термин кератокистозная одонтогенная опухоль как это лучше отражает его неопластическую природу». [3] Недавние молекулярные исследования, показывающие потерю гетерозиготности определенных генов-супрессоров опухоли во многих одонтогенных кератоцистах, поддержали это переименование ВОЗ. [17]
, и в настоящей классификации OKC был переименован в «кератокистозную одонтогенную опухоль» (КОТ). КОТ в настоящее время определяется как «доброкачественная моно- или мультикистозная внутрикостная опухоль одонтогенного происхождения с характерной выстилкой из паракератинизированного многослойного плоского эпителия и потенциалом для агрессивного инфильтративного поведения». [3] ВОЗ «рекомендует термин кератокистозная одонтогенная опухоль как это лучше отражает его неопластическую природу». [3] Недавние молекулярные исследования, показывающие потерю гетерозиготности определенных генов-супрессоров опухоли во многих одонтогенных кератоцистах, поддержали это переименование ВОЗ. [17]
Генетика
Ген PTCH был картирован на хромосоме 9q22.3-q31 и, вероятно, действует как супрессор опухоли.[3] PTCh2 является важной молекулой в так называемом сигнальном пути Hedgehog (Hh) [14]. Обычно PTCH образует рецепторный комплекс с онкогеном SMO («сглаженный») для лиганда SHH («звуковой еж»). Исследования NBCCS и спорадической KCOT предоставили молекулярные доказательства двухударного механизма в патогенезе этих опухолей, демонстрирующего потерю аллелей в двух или более локусах 9q22[19,20], что приводит к сверхэкспрессии bcl-1 и TP53 в NBCCS. Это подтверждает концепцию о том, что KCOT представляет собой новообразование.[20] Также накапливаются данные о том, что ген PTCH может быть важным фактором в развитии спорадического KCOT. Кроме того, предварительные результаты показали сверхэкспрессию и амплификацию генов, расположенных в 12q.[21]
Исследования NBCCS и спорадической KCOT предоставили молекулярные доказательства двухударного механизма в патогенезе этих опухолей, демонстрирующего потерю аллелей в двух или более локусах 9q22[19,20], что приводит к сверхэкспрессии bcl-1 и TP53 в NBCCS. Это подтверждает концепцию о том, что KCOT представляет собой новообразование.[20] Также накапливаются данные о том, что ген PTCH может быть важным фактором в развитии спорадического KCOT. Кроме того, предварительные результаты показали сверхэкспрессию и амплификацию генов, расположенных в 12q.[21]
Эпителиальная выстилка OKC/KOT экспрессирует более высокие уровни p53, чем любые другие типы кист. Эта гиперэкспрессия не связана с мутацией гена р53, а скорее отражает гиперпродукцию и/или стабилизацию нормального белка р53.[14] Другими генами, которые могут быть связаны с OKC/KOT, являются PTCh3 и SUFU. Несколько авторов также продемонстрировали потерю гетерозиготности в генах p16, MCC, TSLC1, LTAS2 и FHIT.[14] Эти данные помогают объяснить агрессивное поведение OKC.
Лечение
OKC хорошо известны своей сильной склонностью к рецидивам.[11] Было проведено много дискуссий и проведены различные исследования, чтобы определить идеальный метод лечения OKC/KOT. В основном эти аргументы вращаются вокруг того, следует ли лечить OKC как кисту или как доброкачественное новообразование. Какой бы модальность ни подразумевалась, ни одна из них не показала полного предотвращения рецидива поражения, проблема все еще усугубляется в случае NBCCS и множественных поражений.
Эйр и Закрезевская[22] в 1985, заявили следующие методы лечения OKC/KOT-
Энуклеация
С первичным закрытием
С тампонадой
С химической фиксацией
С криохирургией
Марсупиализация
Только
С последующей энуклеацией
Резекция
Выбор лечения всегда был трудным, так как благополучие пациента имеет первостепенное значение, хотя и не снижает вероятность рецидивов. Морган и его коллеги [23] классифицировали хирургические методы лечения КОТ как консервативные и агрессивные. Консервативное лечение ориентировано на кисту и, таким образом, включает энуклеацию с кюретажем или без них или марсупиализацию. Преимуществом является сохранение анатомических структур и снижение болезненности для пациента. Агрессивное лечение проводится с учетом «неопластической природы» КОТ и включает периферическую остеэктомию, химический кюретаж или резекцию единым блоком. Это в основном рекомендуется для больших поражений, рецидивирующих случаев и синдромальных пациентов. Декомпрессия также использовалась для лечения КОТ, которые имеют агрессивное поведение и склонны к рецидивам.
Морган и его коллеги [23] классифицировали хирургические методы лечения КОТ как консервативные и агрессивные. Консервативное лечение ориентировано на кисту и, таким образом, включает энуклеацию с кюретажем или без них или марсупиализацию. Преимуществом является сохранение анатомических структур и снижение болезненности для пациента. Агрессивное лечение проводится с учетом «неопластической природы» КОТ и включает периферическую остеэктомию, химический кюретаж или резекцию единым блоком. Это в основном рекомендуется для больших поражений, рецидивирующих случаев и синдромальных пациентов. Декомпрессия также использовалась для лечения КОТ, которые имеют агрессивное поведение и склонны к рецидивам.
Немногие авторы рекомендуют подход «на основе места и размера» для лечения КОТ. Dammer и соавт. [24] предложили консервативный подход при небольших КОТ (максимум 1 см в диаметре) вблизи альвеолярного отростка и радикальное иссечение при более крупных поражениях у основания черепа, проросших в мягкие ткани. Напротив, Forsell и его коллеги сообщили, что размер поражения не влияет на частоту рецидивов.[25]
Напротив, Forsell и его коллеги сообщили, что размер поражения не влияет на частоту рецидивов.[25]
Будущие модальности
Благодаря недавним достижениям и, таким образом, определению молекулярной основы этого объекта, была разработана новая новая методология, сосредоточенная на молекулярных аспектах. Путь Hh может быть заблокирован на разных уровнях, и ингибиторы Hh могут служить привлекательными противоопухолевыми агентами. Согласно некоторым исследованиям, циклопамин, стероидный алкалоид растительного происхождения, блокирует активацию пути SHh, вызванную онкогенной мутацией.[27] Другие исследования также показывают, что антагонисты сигнальных факторов SHh могут эффективно лечить КОТ.
Таким образом, весь процесс классификации и переименования одонтогенных кист и опухолей продолжается, поскольку понимание этих поражений совершает гигантский скачок вперед. Так что же есть в имени? Роза есть роза, как ни назови. Эта концепция, безусловно, неверна, когда речь идет об OKC/KOT.
Известный челюстно-лицевой хирург Гордон Хардман сказал: «Мы всегда знали, что некоторые кисты рецидивируют, поэтому каждые 5-10 лет пациенты приходили на их удаление. Так что же, нам никогда не приходилось давать им отдельные имена». [6] Такое отношение хирургов, игнорирующих множественные рецидивы, всегда подавляло концепцию переклассификации этих поражений (любимая работа патологоанатомов). Споры по поводу природы OKC на самом деле являются отражением наших ограниченных знаний об этой удивительной сущности.[14] «Роза — это роза, это не роза», когда это подразумевает OKC/KOT. Термин «одонтогенная кератоциста» настолько укоренился в литературе, что только время может сказать нам, сможет ли термин «кератокистозная одонтогенная опухоль» успешно заменить этот термин. Недавние достижения в генетическом и молекулярном понимании привели в конечном итоге к устранению необходимости в агрессивных методах лечения.
Источник поддержки: Нет
Конфликт интересов: Не объявлено.
1. Philipsen HP, Reichart PA. Классификация одонтогенных опухолей. Исторический обзор. Дж Орал Патол Мед. 2006; 35: 525–9. [PubMed] [Google Scholar]
2. Hauer A. Ein Cholesteatom im linken Unterkiefer unter einem retinierten Weisheitszahn. Zeitsschrift меховая стоматология. 1926; 24: 40–59. [Google Scholar]
3. Barnes L, Eveson JW, Reichart P, Sidransky D, редакторы. Лион: IARC Press; 2005. Патология и генетика опухолей головы и шеи. [Академия Google]
4. Толлер П. Происхождение и рост кист челюстей. Энн Р. Колл Surg Engl. 1967; 40: 306–36. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Robinson HB. Примордиальные кисты в сравнении с кератоцистами. Oral Surg Oral Path Oral Med. 1975; 40: 362–4.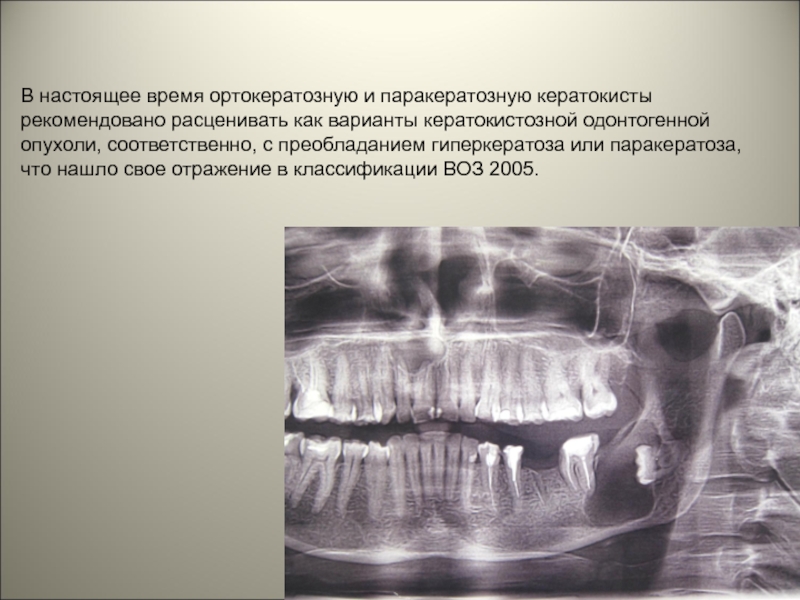 [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
6. Погрель М.А., Шмидт Б.Л. Одонтогенная кератоциста. Oral Maxillofac Surg Clin North Am. 2003;15:311–5. [PubMed] [Google Scholar]
7. Соскольне В.А., Шир М. Наблюдения за патогенезом первичных кист. Бр Дент Дж. 1967;123:321–6. [PubMed] [Google Scholar]
8. Forssell K, Sainio P. Клинико-патологическое исследование ороговевших кист челюстей. Proc Fin Dent Soc. 1979; 75: 36–45. [PubMed] [Google Scholar]
9. Philipsen HP. Кератоциста (колестеатом) и кеберне. Клинок Тандлаеге. 1956; 60: 963–81. [Google Scholar]
10. Pindborg JJ, Hansen J. Исследования эпителия одонтогенных кист. 2. Клинико-рентгенологические аспекты одонтогенных кератоцист. Acta Pathol Microbiol Scand. 1963; 58: 283–9.4. [PubMed] [Google Scholar]
11. Альфорс Э., Ларссон А., Шегрен С. Одонтогенная кератоциста: доброкачественная кистозная опухоль? J Oral Maxillofac Surg. 1984; 42:10–9. [PubMed] [Google Scholar]
12. Шир М. Агрессивная природа одонтогенной кератоцисты: это доброкачественное кистозное новообразование? Часть 1 Оральная онкология. 2002; 38: 219–26. [PubMed] [Google Scholar]
2002; 38: 219–26. [PubMed] [Google Scholar]
13. Регези, Скиубба, Джордан. 4-е изд. Сент-Луис, штат Миссури: компания Saunders; 2003. Клинико-патологические корреляции патологии полости рта; стр. 250–2. [Академия Google]
14. Ли Т.Дж. Одонтогенная кератоциста: киста или кистозное новообразование? Джей Дент Рез. 2011;90:133–42. [PubMed] [Google Scholar]
15. Брэннон Р.Б. Одонтогенная кератоциста Клинико-патологическое исследование 312 случаев. Часть I. Клинические особенности. Oral Surg Oral Med Oral Pathol. 1976; 42: 54–72. [PubMed] [Google Scholar]
16. Reichart PA, Philipsen HP. Лондон: Издательство Quintessence; 2004. Одонтогенные опухоли и родственные поражения. [Google Scholar]
17. Невилл Б.В. Обновленная информация о современных тенденциях в области патологии полости рта и челюстно-лицевой области. Голова шеи патол. 2007; 1: 75–80. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Madras J, Lapointe H. Кератокистозная одонтогенная опухоль: Реклассификация одонтогенной кератоцисты из кисты в опухоль. J Can Dent Assoc. 2008;74:165–65ч. [PubMed] [Google Scholar]
J Can Dent Assoc. 2008;74:165–65ч. [PubMed] [Google Scholar]
19. Леванат С., Горлин Р.Дж., Фаллет С., Джонсон Д.Р., Фантазия Дж.Е., Бэйл А.Е. Двухэтапная модель дефектов развития при синдроме Горлина. Нат Жене. 1996; 12:85–87. [PubMed] [Google Scholar]
20. Lo Muzio L, Staibano S, Pannone G, Bucci P, Nocini PF, Bucci E, et al. Экспрессия белков клеточного цикла и апоптоза в спорадических одонтогенных кератоцистах и одонтогенных кератоцистах, связанных с синдромом невоидной базально-клеточной карциномы. Джей Дент Рез. 1999;78:1345–53. [PubMed] [Google Scholar]
21. Heikinheimo K, Jee KJ, Morgan PR, Nagy B, Happonen RP, Knuutila S, et al. Профилирование экспрессии генов одонтогенной кератоцисты. Дж Орал Патол Мед. 2004; 33:462. [Google Scholar]
22. Эйр Дж., Закрезевска Дж.М. Консервативное лечение больших одонтогенных кератоцист. Br J Oral Maxillofac Surg. 1985; 23: 195–203. [PubMed] [Google Scholar]
23. Morgan TA, Burton CC, Qian F. Ретроспективный обзор лечения одонтогенной кератоцисты.