Лапароскопическая пластика лоханочно мочеточникового сегмента: Пластика лоханочно-мочеточникового сегмента в Москве, цены в клинике АО «Медицина» (клиника академика Ройтберга)
Пластика лоханочно-мочеточникового сегмента в Москве, цены в клинике АО «Медицина» (клиника академика Ройтберга)
Лапароскопическая пластика ЛМС (лоханочно-мочеточникового сегмента) при стриктурах
Благодаря вовремя проведенной операции почка не потеряет свою функцию.
Показания к операции:
-
сужение мочеточников, которое вызывает нарушенный отток почки – гидронефроз;
-
стриктура, которая диагностируется по УЗИ (расширение чашечно-лоханочной системы).
Как проходит операция
1. Иссекается стриктура (сужение мочеточника).
2. Мочеточник сшивается заново.
3. Устанавливается внутренний стент, на котором заживает место сшивания мочеточника.
Операция – лапароскопическая.
Осуществляется обязательный видеоконтроль операции под большим увеличением, с высоким разрешением (High Definition).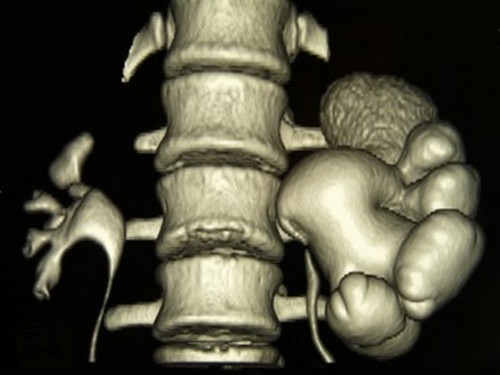
Быстрый период восстановления – госпитализация всего 1-2 дня.
Для того чтобы, получить медицинскую помощь в АО «Медицина» (клиника академика Ройтберга) в рамках ОМС, пациентам необходимо иметь ряд документов:
1. Документ удостоверяющий личность (паспорт).
2. СНИЛС.
3. Действующий полис обязательного медицинского страхования.
4. Результаты обследования по профилю заболевания, в соответствии со стандартами медицинской помощи, проведенного по месту жительства.
5. Должным образом оформленное направление на консультацию к специалистам АО «Медицина» с указанием диагноза, кода по МКБ-10, цели направления (форма 057/у).
При обращении пациента в регистратуру клиники администратор записывает его на прием к врачу-специалисту по профилю. В ходе приема врач определяет дальнейшую тактику, вид необходимого хирургического вмешательства и показания к лечению в рамках ОМС.
Цены
Лапароскопическая пластика лоханочно-мочеточникового сегмента — Клиника доктора Парамонова
Лапароскопическая пластика лоханочно-мочеточникового сегмента (ЛМС) — это вид хирургического лечения сужения (стриктуры) лоханочно-мочеточникового сегмента. Показанием к операции является стриктура ЛМС при функционирующей почке.
Преимущество лапароскопической пластики ЛМС:
- малоинвазивность,
- короткий период госпитализации,
- короткий восстановительный период,
- незначительная кровопотеря во время операции,
- низкий уровень боли, отсутствует необходимость использовать наркотические анальгетики после операции,
- меньше раневых воспалительных осложнений, в связи с минимальной раневой поверхностью и экспозиции внутренних органов.
Как проводится операция?
Лапароскопическая пластика ЛМС является эндоскопическим видом хирургического лечения в ходе которого через 4-5 троакарных проколола в брюшной стенке выделяется почка с верхней третью мочеточника.
Операция проводится под общим обезболиванием. В ходе операции на 2 недели в мочеточник устанавливают внутренний стент-дренаж, который необходим для правильного заживления вновь сформированного соустья. Продолжительность операции порядка 1,5 часов.
Послеоперационный период
На следующий день после операции пациент активизируется, принимает легкую пищу. Через 3-4 суток пациент выписывается.
Через 2 недели больному следует явится для удаления внутреннего мочеточникового дренажа и ультразвукового контроля. Через 6 месяцев после операции необходимо выполнить контрольное урографическое исследование.
В Клинике доктора Парамонова эта операция выполняется высококлассными специалистами, врачами урологами-онкологами высшей категории на современном немецком оборудовании. Мы всегда готовы и будем рады Вам помочь.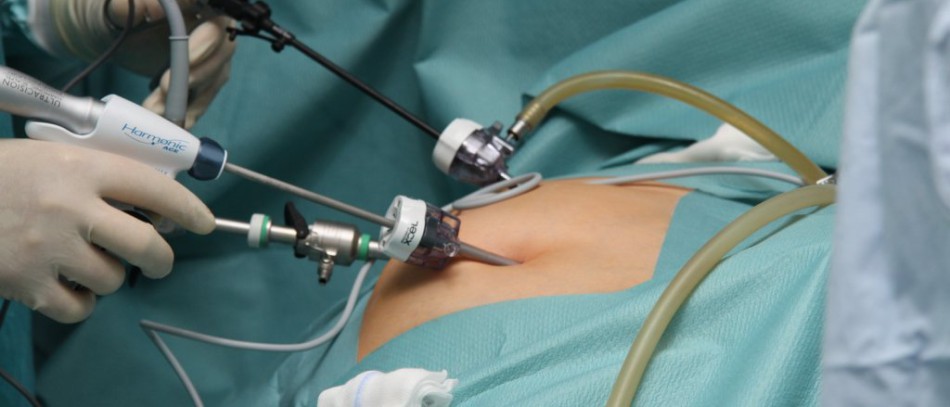 Для получения дополнительной информации и записи на консультацию к урологу в г. Саратов: +7(8452)66-03-03.
Для получения дополнительной информации и записи на консультацию к урологу в г. Саратов: +7(8452)66-03-03.
|
СМТ на Московском проспекте
|
пр-т Московский, д. 22 22
|
||||||
|
|||||||
|
СМТ на Римского-Корсакова
пр-т Римского-Корсакова, д. 87 |
пр-т Римского-Корсакова, д. 87 87
|
||||||
|
|||||||
|
ОрКли на Среднем проспекте В.О.
Средний пр-т В.О., д. 48/27 |
Средний пр-т В. О., д. 48/27 О., д. 48/27
|
||||||
|
|||||||
|
Согаз на Малой Конюшенной
ул. |
ул. Малая Конюшенная, д. 8А | ||||||
|
|||||||
|
СМТ на Валерия Гаврилина
ул. |
ул. Валерия Гаврилина, д. 15 | ||||||
|
|||||||
Санкт-Петербургская больница РАН
 72, лит. А 72, лит. А
|
пр-т Тореза, д. 72, лит. А | ||||||
|
|||||||
|
Клиника имени Петра Великого
Пискаревский пр-т, д. |
Пискаревский пр-т, д. 47 | ||||||
|
|||||||
|
ВЦЭиРМ им. А.М. Никифорова МЧС РФ на Ак. Лебедева
ул. |
ул. Академика Лебедева, д. 4/2 | ||||||
|
|||||||
ВЦЭиРМ им. А.М. Никифорова МЧС РФ на Оптиков А.М. Никифорова МЧС РФ на Оптиков
ул. Оптиков, д. 54 |
ул. Оптиков, д. 54 | ||||||
|
|||||||
НИИ СП им. И.И. Джанелидзе И.И. Джанелидзе
ул. Будапештская, д. 3 лит. А |
ул. Будапештская, д. 3 лит. А | ||||||
|
|||||||
Военно-медицинская академия им. С.М.Кирова С.М.Кирова
ул. Академика Лебедева, д. 6 |
ул. Академика Лебедева, д. 6 | ||||||
|
|||||||
|
ГКБ №31 в Санкт-Петербурге
пр-т Динамо, д. |
пр-т Динамо, д. 3 | ||||||
|
|||||||
|
Ленинградская областная клиническая больница
пр-т Луначарского, д. |
пр-т Луначарского, д. 45-49 | ||||||
|
|||||||
|
Александровская больница на проспекте Солидарности
пр-т Солидарности, д. 4 |
пр-т Солидарности, д. 4 | ||||||
|
|||||||
|
Городская больница №40 в Сестрорецке
г. Сестрорецк, ул. Борисова, д. 9 |
г. Сестрорецк, ул. Борисова, д. 9 | ||||||
|
|||||||
|
НИИ фтизиопульмонологии СПб на Политехнической
ул. Политехническая, д. 32 |
ул. Политехническая, д. 32 | ||||||
|
|||||||
|
Дорожная клиническая больница ОАО «РЖД»
пр-т Мечникова, д. 27 |
пр-т Мечникова, д. 27 | ||||||
|
|||||||
|
КБ №122 им. Л.Г. Соколова
пр-т Культуры, д. 4 |
пр-т Культуры, д. 4 | ||||||
|
|||||||
|
НИИ фтизиопульмонологии СПб на Лиговском проспекте
Лиговский пр-т, д. |
Лиговский пр-т, д. 2-4 | ||||||
|
|||||||
|
Городская Мариинская больница на Литейном
Литейный пр-т, д. |
Литейный пр-т, д. 56 | ||||||
|
|||||||
|
Клиника СПб ГПМУ
ул. |
ул. Литовская, д. 2 | ||||||
|
|||||||
|
МСЧ МВД России на проспекте Культуры
пр-т Культуры, д. |
пр-т Культуры, д. 2 | ||||||
|
|||||||
|
Городская больница Святого Георгия на Северном
Северный пр-т, д. |
Северный пр-т, д. 1 | ||||||
|
|||||||
Клиника им. Э.Э.Эйхвальда Э.Э.Эйхвальда
ул. Кирочная, д. 41 |
ул. Кирочная, д. 41 | ||||||
|
|||||||
|
Городская больница № 33 в Колпино
г. |
г. Колпино, ул. Павловская, д. 16А | ||||||
|
|||||||
ДГБ № 2 Св. Марии Магдалины на 2-ой линии В. О. О.
2-я линия В. О., д. 47 |
2-я линия В. О., д. 47 | ||||||
|
|||||||
|
МСЧ №38 в Сосновом Бору
г. |
г. Сосновый Бор (Ленинградская область), Больничный городок, д. 3/13 | ||||||
|
|||||||
Лапароскопическая пластика при первичных стриктурах лоханочно-мочеточникового сегмента Текст научной статьи по специальности «Клиническая медицина»
ЛАПАРОСКОПИЧЕСКАЯ ПЛАСТИКА ПРИ ПЕРВИЧНЫХ СТРИКТУРАХ ЛОХАНОЧНО-МОЧЕТОЧНИКОВОГО СЕГМЕНТА
ОРИГИНАЛЬНАЯ СТАТЬЯ. УРОЛОГИЯ
УРОЛОГИЯ
DOI: 10.17709/2409-2231-2017-4-4-1
Н.В.Поляков, Н.Г.Кешишев, Ш.Ш.Гурбанов, М.В.Григорьева, Л.Д.Арустамов, А.В.Казаченко, Б.Я.Алексеев
НИИ урологии и интервенционной радиологии имени Н.А. Лопаткина — филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Министерства здравоохранения Российской Федерации, 105425, Россия, Москва, ул. 3-я Парковая, д. 51, стр. 4
Определение показаний к выполнению реконструктивно-пластических оперативных вмешательств при стриктурах лоханочно-мочеточникового сегмента (ЛМС) является сложной задачей. При принятии некорректного решения проведенное лечение может быть неэффективным. Функциональная и анатомическая сохранность почки в значительной мере может повлиять на исход операции.
Цель исследования. Оценка эффективности лапароскопической пластики стриктур ЛМС в зависимости от анато-мо-функционального состояния ипсилатеральной почки.
Оценка эффективности лапароскопической пластики стриктур ЛМС в зависимости от анато-мо-функционального состояния ипсилатеральной почки.
Материалы и методы. Проанализированы результаты лечения 134 пациентов, которым за период с 2012 по 2015 гг. были выполнены различные виды реконструктивных оперативных вмешательств по поводу стриктуры ЛМС: лоскутная пластика ЛМС по Са1р de Virde, уретеропиелоанастомоз по Андерсену-Хайнцу и анте-вазальный уретеропиелоанастомоз.
Для анализа эффективности проведенного лечения в пред- и послеоперационном периоде оценивали следующие параметры: наличие болевого синдрома, наличие пиелоэктазии, функциональное состояние почечной паренхимы (по данным радиоизотопной ренографии), отсутствие рецидива стриктуры ЛМС.
Результаты. Общая эффективность лапароскопической реконструкции ЛМС составила 94,7%. Результаты лечения не зависели от выбранной методики оперативного вмешательства.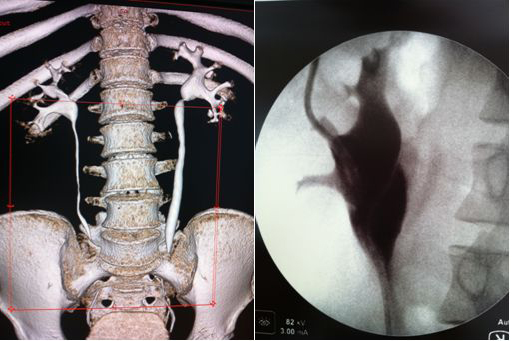 При этом эффективность проведенного лечения зависела от исходного дефицита функции почки: наилучшие результаты лечения отмечены у пациентов с дефицитом функции почки менее 25%, а доля неэффективных вмешательств была наиболее высока среди пациентов с дефицитом более 75%. Степень дилятации лоханки в послеоперационном периоде также была ассоциирована с предоперационными показателями дефицита функции почки, это может быть обусловлено наличием атонии чашечно-лоханочной системы (ЧЛС).
При этом эффективность проведенного лечения зависела от исходного дефицита функции почки: наилучшие результаты лечения отмечены у пациентов с дефицитом функции почки менее 25%, а доля неэффективных вмешательств была наиболее высока среди пациентов с дефицитом более 75%. Степень дилятации лоханки в послеоперационном периоде также была ассоциирована с предоперационными показателями дефицита функции почки, это может быть обусловлено наличием атонии чашечно-лоханочной системы (ЧЛС).
Заключение. Таким образом, результаты нашей работы продемонстрировали высокую эффективность лапароскопической пластики ЛМС. Эффективность лечения определяется своевременностью выполнения вмешательства. В качестве основного прогностического критерия эффективности предстоящего вмешательства следует рассматривать степень дефицита функции почки.
Ключевые слова:
пластика ЛМС, стриктуры ЛМС, лапароскопические вмешательства на верхних мочевых путях, лоскутная пластика ЛМС по Са1р de Virde, пластика ЛМС по Андерсену-Хайнцу, антевазальный уретеропиелоанастомоз
Оформление ссылки для цитирования статьи
Поляков Н. В., Кешишев Н.Г., Гурбанов Ш.Ш., Григорьева М.В., Арустамов Л.Д., Казаченко А.В., Алексеев Б.Я. Лапароскопическая пластика при первичных стриктурах лоханочно-мочеточникового сегмента. Исследования и практика в медицине. 2017; 4(4): 10-17. DOI: 10.17709/2409-2231-2017-4-4-1
В., Кешишев Н.Г., Гурбанов Ш.Ш., Григорьева М.В., Арустамов Л.Д., Казаченко А.В., Алексеев Б.Я. Лапароскопическая пластика при первичных стриктурах лоханочно-мочеточникового сегмента. Исследования и практика в медицине. 2017; 4(4): 10-17. DOI: 10.17709/2409-2231-2017-4-4-1
Для корреспонденции
Гурбанов Шамиль Шукурович, к.м.н., старший научный сотрудник отдела эндоурологии НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина — филиал ФГБУ «НМИЦ радиологии» Минздрава России. Адрес: 105425, Россия, Москва, ул. 3-я Парковая, д. 51, стр. 4 E-mail: gurbanovsh@gmai[.com
Информация о финансировании. Финансирование данной работы не проводилось. Конфликт интересов. Все авторы сообщают об отсутствии конфликта интересов.
Статья поступила 23.09.2017 г., принята к печати 30. 11.2017 г.
11.2017 г.
Резюме
LAPAROSCOPIC PLASTIC WITH PRIMARY STRICTURES OF THE URETEROPELVIC SEGMENT
ORIGINAL ARTICLE. UROLOGY
DOI: 10.17709/2409-2231-2017-4-4-1
N.V.Polyakov, N.G.Keshishev, Sh.Sh.Gurbanov, M.V.Grigoryeva, L.D.Arustamov, A.V.Kazachenko, B.Ya.Alekseev
N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology — Branch of the National Medical Radiology Research Centre of the Ministry of Health of the Russian Federation, 51/4, 3rd Parkovaya str., Moscow, 105425, Russia
Determination of indications for performing reconstructive and plastic surgical interventions in stricture of UPS is a difficult task.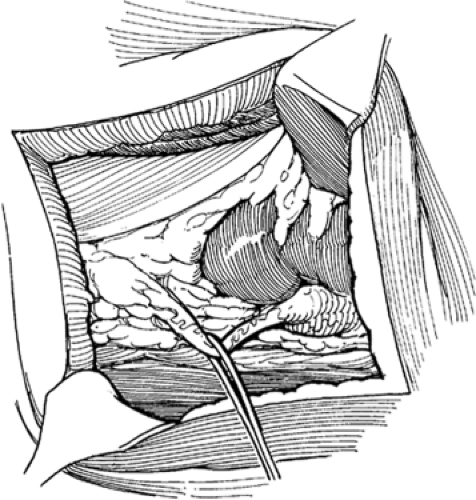 When making an incorrect decision, the treatment can be ineffective. Functional and anatomical preservation of the kidney can significantly affect the outcome of the operation.
When making an incorrect decision, the treatment can be ineffective. Functional and anatomical preservation of the kidney can significantly affect the outcome of the operation.
Purpose. Evaluation of the effectiveness of laparoscopic plastic surgery of stricture of UPS, depending on the anatomical and functional state of the ipsilateral kidney.
Material and method. The results of treatment of 134 patients, who underwent for the period from 2012 to 2015 the different types of reconstructive surgical interventions for stricture of the pelvic-ureteral segment (Calp de Virde scrappy plastic surgery, Andersen-Heinz ureteropyelanastomosis, and antineoplastic ureteropyeloanastomosis), were analyzed. To analyze the effectiveness of the treatment, in the pre- and postoperative period, the following parameters were evaluated: the presence of pain syndrome, the presence of pyeloectasia, the functional state of the renal parenchyma (according to radioisotope renography), and the absence of recurrence of the UPS stricture.
Result. The overall efficacy of laparoscopic UPS reconstruction was 94.7%. The results of treatment did not depend on the chosen technique of operative intervention. In this case, the effectiveness of the treatment was dependent on the initial deficiency of kidney function: the best results were seen in patients with kidney function deficiency of less than 25%, and the proportion of ineffective interventions was highest among patients with a deficit of more than 75%. The degree of dilatation of the pelvis in the postoperative period was also associated with preoperative indicators of kidney function deficiency, this may be due to the presence of cup-pelvis-plating system atony.
Conclusion. Thus, the results of our work demonstrated the high efficiency of laparoscopic plastics of UPS. The effectiveness of treatment is determined by the timeliness of the intervention. As a basic prognostic criterion for the effectiveness of the forthcoming intervention, the degree of deficiency of the kidney function should be considered.
Keywords:
UPS plastic surgery, UPS stricture, laparoscopic interventions on the upper urinary tract, UPS flap plastic by Calp de Virde, UPS plastic by Andersen-Heinz, antevasal ureteropyeloanastomosis
For citation
Polyakov N.V., Keshishev N.G., Gurbanov Sh.Sh., Grigorieva M.V., Arustamov L.D., Kazachenko A.V., Alekseev B.Ya. Laparoscopic plastic with primary strictures of the ureteropelvic segment. Research’n Practical Medicine Journal. 2017; 4(4): 10-17. (In Russian). DOI: 10.17709/2409-2231-2017-4-4-1
For correspondence
Shamil Sh. Gurbanov, PhD, senior researcher, Department of Endourology, N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology — Branch of the National Medical Radiology Research Centre of the Ministry of Health of the Russian Federation. Address: 51/4, 3rd Parkovaya str., Moscow, 105425, Russia. E-mail: [email protected]
Address: 51/4, 3rd Parkovaya str., Moscow, 105425, Russia. E-mail: [email protected]
Information about funding. No funding of this work has been held. Conflict of interest. All authors report no conflict of interest.
The article was received 23.09.2017, accepted for publication 30.11.2017
Abstract
Обструкция лоханочно-мочеточникового сегмента (ЛМС), обусловленная функциональными либо анатомическими нарушениями транспортировки мочи из чашечно-лоханочной системы (ЧЛС) в мочеточник, является одним из наиболее распространенных урологических заболеваний. Врожденная анатомическая обструкция пиело-уретрального соустья может быть обусловлена следующими причинами: наличие фиброза стенки мочеточника, добавочного перекрестного сосуда, полипов слизистой, а также высокое отхождение мочеточника от лоханки [1-3]. Нередко нарушение пассажа мочи может быть обусловлено уродинамическими изменениями в верхних мочевыводящих путях (ВМП) [1, 4-7].
До недавнего времени пластические операции на ЛМС относились к разряду сложных вмешательств, так как выполнялись лишь открытым способом. В начале 80-х годов ХХ в. появились первые публикации, посвященные возможности эндоскопической коррекции ЛМС. Так, в 1983 г. J. E. Wickham и M. J. Kellet сообщили о своем опыте выполнения эндопиелотомии перкутанным доступом у троих пациентов [8]. Однако последующие исследования показали, что эндопиелотомия может быть эффективна лишь при непротяженных стриктурах ЛМС [915]. Эффективность эндоскопических вмешательств, по данным различных авторов, варьирует в пределах 32-76% и, конечно же, зависит от протяженности, локализации и характера стриктуры [16, 17].
Бурное развитие эндоскопического оборудования послужило поводом к активному внедрению в клиническую практику эндовидеохирургических методов выполнения реконструктивных операций на ВМП. В связи с совершенствованием и отработкой техники выполнения подобных вмешательств практикующие урологи все чаще предпочитают открытым вмешательствам лапароскопическую пластику ЛМС, которая характеризуется меньшей инвазивностью и сравнительно более короткими сроками реабилитации [18-21]. По данным различных авторов, эффективность лапароскопических пластик ЛМС составляет более 90% (табл. 1).
Однако крайне дискутабельным остается вопрос о выборе показаний к выполнению реконструктив-но-пластических операций при стриктурах ЛМС. Во всех ли случаях оправданы подобные вмешательства? Так, нередко не учитываются анатомо-функциональные особенности почечной единицы, особенно если у пациента по причине длительности заболевания имеется значительный дефицит секреторной активности почечной паренхимы в сочетании с выраженной атонией ЧЛС. В таких случаях выполненное оперативное вмешательство не приводит к ожидаемому результату.
Все вышеизложенное определило актуальность данной проблемы и послужило причиной анализа отдаленных результатов реконструктивно-пласти-ческих операций на пиело-уретральном соустье.
Цель данного исследования — оценка эффективности лапароскопической пластики стриктур ЛМС в зависимости от анатомо-функционального состояния ипсилатеральной почки.
МАТЕРИАЛЫ И МЕТОДЫ
Материалом для данного исследования послужили наши собственные результаты лечения 134 пациентов (78 женщин и 56 мужчин), которым за период с 2012 по 2015 гг. были выполнены различные виды реконструктивных оперативных вмешательств по поводу стриктуры ЛМС (табл. 2).
Возраст пациентов варьировал от 18 до 58 лет (медиана 28,7). Из особенностей следует отметить, что у 13 пациентов на момент госпитализации имелись нефростомические дренажи и у 11 были диагностированы камни почек от 6 до 25 мм (медиана 13,6 мм). Непосредственно до реконструкции ЛМС 5 больным выполнена перкутанная нефролитотрип-сия (ПНЛ). У 6 пациентов с относительно небольшими размерами чашечковых камней и у 1 с ре-зидуальным фрагментом было принято решение выполнить вмешательства по эрадикации конкрементов после пластики ЛМС. Следует отметить, что при отсутствии осложнений после ПНЛ реконструк-
Таблица 1. Эффективность лапароскопических пластик ЛМС [12, 17, 20-22] Table 1. The effectiveness of laparoscopic plastic of UPS [12, 17, 20-22]
Авторы Число пациентов Эффективность, %
Klingler H.C. et al., 2003 25 96
Zhang X. et al., 2006 56 98,2
Bansal P. et al., 2011 28 92,8
Abdel-Karim A.M. et al., 2016 24 91,7
цию пиело-уретрального соустья выполняли в среднем через 7-8 дней.
Все операции выполняли под эндотрахеальной анестезией лапароскопическим доступом в интегрированной операционной OR1 (Karl Storz). В зависимости от используемой методики пластической реконструкции все пациенты были разделены на три группы: 1-я группа (n = 34) — лоскутная пластика ЛМС по Calp de Virde, 2-я группа (n = 59) — уретеропиелоанастомоз по Андерсену-Хайнцу и 3-я группа (n = 41) — антева-зальный уретеропиелоанастомоз (табл. 3). Все вмешательства заканчивались установкой внутреннего мочеточникового стента сроком на 6-8 нед.
По степени дефицита функции почки все пациенты также были разделены на три подгруппы в следующих интервалах: менее 25%, 25-50% и более 50%. На основании результатов предоперационного обследования отмечена вариация толщины почечной паренхимы на стороне поражения, медиана которой составила 12,3 мм.
Контрольное обследование пациентов проводили в сроки 6, 12 мес и далее — 1 раз в год.
Максимальный срок наблюдения составил 3 года у 98 больных (73,1%), средний — 2,6 ± 0,8 года.
Прогностическими критериями эффективности проведенного лечения были следующие параметры: исчезновение болевого синдрома, уменьшение степени пиелоэктазии, стабилизация или улучшение функционального состояния почечной паренхимы по данным радиоизотопной реногра-фии и отсутствие рецидива стриктуры ЛМС.
Статистические расчеты выполняли в программе Statistica 6. Для описания данных использованы медиана, минимум, максимум. Для анализа зависимости эффективности лечения от метода оперативного вмешательства использовали критерий хи-квадрат. Для анализа корреляционных взаимосвязей применяли непараметрический критерий Спирмена.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Учитывая, что основным показателем эффективности оперативного вмешательства по поводу стриктуры ЛМС является улучшение либо стабилизация
Таблица 2. Общая характеристика группы больных со стриктурой ЛМС (n Table 2. General characteristics of a group of patients with stricture of UPS (n = 134) = 134)
Параметр Показатель Значение
Возраст больных Медиана (мин-макс.), лет 28,7 (18-58)
Мужчины Абсолютный (относительный, %) 56 (41,8)
Женщины Абсолютный (относительный, %) 78 (58,2)
Инфекция ВМП Абсолютный (относительный, %) 44 (32,8)
Сочетание стриктуры ЛМС и нефролитиаза Абсолютный (относительный, %) 11 (8,2)
Наличие нефростомического дренажа Абсолютный (относительный, %) 13 (9,7)
Пиелоэктазия Медиана (мин.-макс.), мм 43,8 (22-71)
Дефицит функции почки Медиана (мин.-макс.), % 41,6 (18-79)
Толщина паренхимы Медиана (мин.-макс.), мм 12,3 (9-18)
Таблица 3. Распределение пациентов в зависимости от методики выполненной операции Table 3. Patient distribution depending on the procedure of the performed operation
Методика операции Абсолютный показатель Относительный показатель, %
Calp de Virde (1-я группа) 34 25,4
Андерсен-Хайнц (2-я группа) 59 44
Антевазальный уретеропиелоанастомоз (3-я группа) 41 30,6
функционального состояния почки [3, 22-27], абсолютные и относительные показатели количества положительных результатов каждой из примененных методик представлены в зависимости от изначальных данных радиоизотопной ренографии (табл. 4).
Различия между результатами лечения, в зависимости от метода операции, были недостоверными (р > 0,05). Наилучшие результаты лечения отмечены у пациентов с дефицитом функции почки менее 25%. При дефиците более 50% эффективность составила 82,6% (19 из 23). Наибольший процент неэффективных вмешательств (66,6%) был отмечен среди пациентов с дефицитом более 75%. Отмечена обратная корреляционная взаимосвязь между эффективностью операции и степенью дефицита функции почки (г = -0,645, р < 0,05).
В результате проведенного оперативного лечения уменьшение степени болевого синдрома было отмечено у 121 (90,3%) больного. У остальных пациентов сохранялись периодические тупые ноющие боли в поясничной области на стороне поражения. Мы считаем, что эти симптомы не всегда были обусловлены болезнью самой почки, и оценка данного параметра, конечно же, носила субъективный характер (табл. 5).
Степень пиелоэктазии оценивали через 3 ч после удаления внутреннего стента. В 128 (95,5%) случаях, несмотря на выполненную реконструкцию ЛМС, сохранялась дилатация ЧЛС ипсилатеральной почки. Причем у 80 больных (62,5%) расширение лоханки
было больше исходного размера, у 30 (23,4%) — оставалось практически неизменным и у 18 (14%) — отмечалось некоторое уменьшение степени пиелоэктазии. Контрольное обследование через 3 мес показало сокращение лоханки на стороне операции приблизительно в 2 раза у 75 (55,9%) пациентов. При последующем наблюдении отмечена достоверная корреляционная взаимосвязь между степенью дилятации лоханки в послеоперационном периоде и исходным дефицитом функции почки на стороне поражения (г = 0,71, р < 0,05). Сохраняющаяся пие-лоэктазия у больных в отдаленные сроки после операции, вероятнее всего, была обусловлена атонией ЧЛС и, как следствие, нарушением эвакуаторной функции ВМП. В последующем отдаленные результаты лечения этих больных оценивали на основании данных радиоизотопной ренографии либо динамической нефросцинтиграфии (табл. 5).
У 6 пациентов при дальнейшем наблюдении диагностирован рецидив стриктуры ЛМС. Это были больные с начальным дефицитом функции почки >50% (4 пациента) и >40% (2 пациента), у которых в послеоперационном периоде было отмечено значительное ухудшение функции почки (табл. 5). Всем больным был установлен нефростомический дренаж с последующей эндопиелотомией не ранее чем через 6 мес после пластики ЛМС.
Таким образом, общая эффективность лапароскопической реконструкции ЛМС составила 94,7% (127 из 134).
Таблица 4. Абсолютное и относительное количество пациентов с положительными результатами лечения в зависимости от изначальной степени дефицита функции почки
Table 4. Absolute and relative number of patients with positive treatment outcomes, depending on the initial degree of kidney function deficiency
Параметры <25% 25-50% >50%
1-я группа (n = 34) 10 из 10 (100%) 16 из 17 (94%) 6 из 7 (85,7%)
2-я группа (n = 59) 19 из 19 (100%) 29 из 30 (96,6%) 8 из 10 (80%)
3-я группа (n = 41) 15 из 15 (100%) 18 из 20 (90%) 5 из 6 (83,3%)
Таблица 5. Результаты лапароскопической пластики ЛМС Table 5. Results of laparoscopic plastics of UPS
Параметр Абсолютный показатель Относительный показатель, %
Уменьшение болевого синдрома 121 90,3
Уменьшение дилатации ЧЛС 105 78,3
Стабилизация или улучшение функции почки 127 94,7
Отсутствие рецидива стриктуры ЛМС 128 95,5
ЗАКЛЮЧЕНИЕ
На сегодняшний день лапароскопическая пластика является общепринятым в мировом сообществе золотым стандартом реконструктивных операций при стриктурах ЛМС. Однако до сих пор остаются дискутабельными вопросы — в каких случаях необходимо выполнять реконструкцию, в каких достаточно динамического наблюдения и когда показана органоуносящая операция. Полученные нами данные продемонстрировали высокую эффективность лапароскопической пластики ЛМС (94,7%). Своевре-
менно предпринятое оперативное вмешательство позволяет достигнуть максимального количества положительных результатов лечения у пациентов с гид-ронефротической трансформацией, обусловленной стриктурой ЛМС, либо наличием добавочного сосуда почки. Основным прогностическим критерием эффективности предстоящей операции следует считать степень дефицита функции почки. Следует отметить, что при дефиците функции почки более 50% возрастает число неэффективных вмешательств, а при дефиците более 75% показания к выполнению реконструкции ЛМС должны определяться индивидуально.
Список литературы
1. Kletscher BA, Segura JW. Surgical management of UPJ obstruction in adults. AUA Update Series 1996; XV: lesson 18.
2. Kausik S, Segura JW. Surgical management of ureteropelvic junction obstruction in adults. Int Braz J Urol. 2003 Jan-Feb; 29
(I): 3-10. Available at: http://www.brazjurol.com.br/january_ february_2003/Kausik_ing_03_10.htm
3. Nishi M, Matsumoto K, Fujita T, Iwamura M. Improvement in Renal Function and Symptoms of Patients Treated with Laparoscopic Pyeloplasty for Ureteropelvic Junction Obstruction with Less Than 20% Split Renal Function. J Endourol. 2016 Nov;30
(II):1214-1218. DOI: 10.1089/end.2016.0553
4. Мартов А. Г., Гурбанов Ш. Ш., Мудрая И. С. Оценка сократительной функции верхних мочевыводящих путей методом многоканальной импедансной уретерографии до и после эн-доуретеропиелотомии. Урология. 2009; 4: 25-30.
5. Мартов А. Г., Гурбанов Ш. Ш., Токарева Е. В., Щербинин С. Н., Корниенко С. И. Сравнительная оценка результатов магнитно-резонансной урографии и других методов исследования у пациентов с ятрогенным повреждением мочеточника и ло-ханочно-мочеточникового сегмента. Урология. 2009; 3: 7-12.
6. Павлов А. Ю., Пугачев А. Г., Поляков Н. В., Лисенок А. А. Прогностическое значение метода оперативного лечения гидронефроза у детей. В кн.: Пленум правления Российского общества урологов. Материалы пленума, Тюмень, 24-27 мая 2005 г., с. 147-148.
7. Павлов А. Ю., Поляков Н. В., Игнашин Н. С., Голованов С. А. Алгоритм диагностики и лечения обструктивных уропатий верхних мочевых путей у детей и подростков. В кн.: Пленум правления Российского общества урологов. Материалы пленума, Тюмень, 24-27 мая 2005 г., с. 148-149.
8. Wickham JE, Kellet MJ. Percutaneous pyelolysis. Eur Urol 1983; 9 (2): 122-124
9. Мартов А. Г., Кваша В. И. Перкутанная эндопиелотомия. Урология и нефрология. 1990; 6: 22-25.
10. Мартов А. Г., Ергаков Д. В., Салюков Р. В., Гущин Б. Л., Чернов Н. А. Рентгеноэндоскопические методы лечения стриктур верхних мочевыводящих путей (обзор литературы). Урология. 2000; 1: 38-43.
11. Chen WN, Ye XJ, Liu SJ, Xiong LL, Huang XB, Xu T, Wang XF. Comparison of three surgical methods of ureteropelvic junction obstruction in therapeutic effect and complication. Beijing Da Xue Xue Bao. 2016 Oct 18;48 (5):817-821. (In Chinese)
12. Corbett HJ, Mullassery D. Outcomes of endopyelotomy for pelviureteric junction obstruction in the paediatric population: A systematic review. J Pediatr Urol. 2015 Dec;11 (6):328-36. DOI: 10.1016/j.jpurol.2015.08.014
13. Lai WR, Stewart CA, Thomas R. Technology Based Treatment for UreteroPelvic Junction Obstruction. J Endourol. 2017 Apr;31 (S1): S59-S63. DOI: 10.1089/end.2016.0592.
14. Мартов А. Г., Гурбанов Ш. Ш., Степанов В. С., Корниенко С. И. Рентгеноэндоскопическая диагностика и лечение ятрогенных повреждений верхних мочевыводящих путей. Урология. 2009; 2: 25-32.
15. Забиров К. И., Яровой С. К. Антибактериальная профилактика при эндоскопических оперативных вмешательствах в урологии. Consilium medicum. 2010; 12 (7): 51-54.
16. Бондаренко С. Г. Дифференцированный подход к выбору способа малоинвазивной хирургической коррекции гидронефроза. Автореф. дис. … канд. мед. наук. Волгоград, 2007, 27 с.
17. Комяков Б. К., Гулиев Б. Г., Шиблиев Р. Г. Эндоскопические вмешательства при стриктурах верхних мочевыводящих путей. Первый Российский конгресс по эндоурологии: тезисы докладов. М., 2008, с. 83-85.
18. Bansal P, Gupta A, Mongha R, Narayan S, Kundu AK, Chakraborty SC, et al. Laparoscopic versus open pyeloplasty: Comparison of two surgical approaches- a single centre experience of three years. J Minim Access Surg. 2008 Jul; 4 (3): 76-9.
19. Iwamura M, Soh S, Irie A, Kadowaki K, Matsusita Y, Fujioka T, Baba S. Laparoscopic pyeloplasty for ureteropelvic junction obstruction: outcome of initial 12 procedures. Int J Urol 2004; 11 (7): 449-55. DOI: 10.1111/j.1442-2042.2004.00830.x
20. Juliano RV, Mendonca RR, Meyer F, Rubinstein M, Lasmar MT, Korkes F, et al. Long-term outcome of laparoscopic pyeloplasty: multicentric comparative study of techniques and accesses. J Laparoendosc Adv Surg Tech A. 2011 Jun;21 (5):399-403. DOI: 10.1089/lap.2010.0281.
21. Abdel-Karim AM, Fahmy A, Moussa A, Rashad H, Elbadry M, Badawy H, Hammady A. Laparoscopic pyeloplasty versus open pyeloplasty for recurrent ureteropelvic junction obstruction in children. J Pediatr Urol. 2016 Dec;12 (6):401.e1-401.e6. DOI: 10.1016/j.jpurol.2016.06.010
22. Schlomer BJ, Smith PJ, Barber TD, Baker LA. Nephrectomy for hypertension in pediatric patients with a unilateral poorly functioning kidney: a contemporary cohort. J Pediatr Urol. 2011 Jun; 7 (3): 373-7. DOI: 10.1016/j.jpurol.2011.02.020.
23. El-Hout Y, Licht C, Pippi Salle JL, Ngan BY, Bagli DJ, Lorenzo AJ, Farhat WA. Hypertension in children with poorly functioning unilateral kidney: predictors of resolution after nephrectomy. BJU Int. 2010 Nov;106 (9):1376-80. DOI: 10.1111/j.1464-410X.2010.09308.x
24. Autorino R, Eden C, El-Ghoneimi A, Guazzoni G, Buffi N, References
1. Kletscher BA, Segura JW. Surgical management of UPJ obstruction in adults. AUA Update Series 1996; XV: lesson 18.
2. Kausik S, Segura JW. Surgical management of ureteropelvic junction obstruction in adults. Int Braz J Urol. 2003 Jan-Feb; 29
(I): 3-10. Available at: http://www.brazjurol.com.br/january_ february_2003/Kausik_ing_03_10.htm
3. Nishi M, Matsumoto K, Fujita T, Iwamura M. Improvement in Renal Function and Symptoms of Patients Treated with Laparoscopic Pyeloplasty for Ureteropelvic Junction Obstruction with Less Than 20% Split Renal Function. J Endourol. 2016 Nov; 30
(II): 1214-1218. DOI: 10.1089/end.2016.0553
4. Martov AG, Gurbanov ShSh, Mudraya IS. Estimation of the contractile function of the upper urinary tract by multichannel impedance ureterography before and after endoureteropy-elotomy Urology. 2009; 4: 25-30. (In Russian).
5. Martov AG, Gurbanov ShSh, Tokareva EV, Scherbinin SN, Korn-ienko SI. Comparison of the results of MR-urography and other examination methods in patients with iatrogenic injuries of the ureter and pelvioureteral segment. Urology. 2009; 3: 7-12. (In Russian).
6. Pavlov AYu, Pugachev AG, Polyakov NV, Lisenok AA. Prognos-ticheskoe znachenie metoda operativnogo lecheniya gidronefro-za u detei [Prognostic value of the method of surgical treatment of hydronephrosis in children]. In: The Plenum of the Russian society of urology. Materials of the Plenum. Tyumen, 24-27 May 2005, pp. 147-148. (In Russian).
7. Pavlov AYu, Polyakov NV, Ignashin NS, Golovanov SA. Algoritm diagnostiki i lecheniya obstruktivnykh uropatii verkhnikh mo-chevykh putei u detei i podrostkov [Algorithm for diagnosis and treatment of obstructive uropathy of the upper urinary tract in children and adolescents]. In: The Plenum of the Russian society of urology. Materials of the Plenum. Tyumen, 24-27 May 2005, pp. 148-149. (In Russian).
8. Wickham JE, Kellet MJ. Percutaneous pyelolysis. Eur Urol 1983; 9 (2): 122-124
9. Martov AG, Kvasha VI. Perkutannaya endopielotomiya. Urologiya i nefrologiya. 1990; 6: 22-25. (In Russian).
10. Martov AG, Ergakov DV, Salyukov RV, Gushchin BL, Chernov
Peters CA, et al. Robot-assisted laparoscopic repair of uretero-pelvic junction obstruction: A systematic review and meta-anal-ysis. Eur Urol. 2014 Feb;65 (2):430-52. DOI: 10.1016/j.euru-ro.2013.06.053.
25. Wagner M, Mayr J, Hacker FM. Improvement of renal split function in hydronephrosis with less than 10% function. Eur J Pediatr Surg. 2008 Jun;18 (3):156-9. DOI: 10.1055/s-2008-1038445
26. Bansal R, Ansari MS, Srivastava A, Kapoor R. Long-term results of pyeloplasty in poorly functioning kidneys in the pediatric age group. J Pediatr Urol. 2012 Feb;8 (1):25-8. DOI: 10.1016/j. jpurol.2010.12.012
27. Ortapamuk H, Naldoken S, Tekdogan UY, Aslan Y, Atan A. Differential renal function in the prediction of recovery in adult obstructed kidneys after pyeloplasty. Ann Nucl Med. 2003 Dec;17 (8):663-8.
NA. Rentgenoendoskopicheskie metody lecheniya striktur verkhnikh mochevyvodyashchikh putei (obzor literatury). Urology. 2000; 1: 38-43. (In Russian).
11. Chen WN, Ye XJ, Liu SJ, Xiong LL, Huang XB, Xu T, Wang XF. Comparison of three surgical methods of ureteropel-vic junction obstruction in therapeutic effect and complication. Beijing Da Xue Xue Bao. 2016 Oct 18;48 (5):817-821. (In Chinese)
12. Corbett HJ, Mullassery D. Outcomes of endopyelotomy for pelviureteric junction obstruction in the paediatric population: A systematic review. J Pediatr Urol. 2015 Dec;11 (6):328-36. DOI: 10.1016/j.jpurol.2015.08.014
13. Lai WR, Stewart CA, Thomas R. Technology Based Treatment for UreteroPelvic Junction Obstruction. J Endourol. 2017 Apr;31 (S1): S59-S63. DOI: 10.1089/end.2016.0592.
14. Martov AG, Gurbanov ShSh, Stepanov VS, Kornienko SI. X-ray endoscopic diagnosis and treatment of iatrogenic injuries of the upper urinary tract. Urology. 2009; 2: 25-32. (In Russian).
15. Zabirov KI, Yarovoi SK. Antibakterial’naya profilaktika pri en-doskopicheskikh operativnykh vmeshatel’stvakh v urologii. Con-silium medicum. 2010; 12 (7): 51-54. (In Russian).
16. Bondarenko SG. A differentiated approach to the choice of the method of minimally invasive surgical correction of hydronephrosis. Diss. Volgograd, 2007, 27 p. (In Russian).
17. Komyakov BK, Guliev BG, Shibliev RG. Endoskopicheskie vme-shatel’stva pri strikturakh verkhnikh mochevyvodyashchikh putei [Endoscopic interventions for strictures of the upper urinary tract]. Proceedings of the first Russian Congress on endourology. Moscow, 2008, pp. 83-85. (In Russian).
18. Bansal P, Gupta A, Mongha R, Narayan S, Kundu AK, Chakraborty SC, et al. Laparoscopic versus open pyeloplasty: Comparison of two surgical approaches- a single centre experience of three years. J Minim Access Surg. 2008 Jul; 4 (3): 76-9.
19. Iwamura M, Soh S, Irie A, Kadowaki K, Matsusita Y, Fujioka T, Baba S. Laparoscopic pyeloplasty for ureteropelvic junction obstruction: outcome of initial 12 procedures. Int J Urol 2004; 11 (7): 449-55. DOI: 10.1111/j.1442-2042.2004.00830.x
20. Juliano RV, Mendonca RR, Meyer F, Rubinstein M, Lasmar MT,
Korkes F, et al. Long-term outcome of laparoscopic pyeloplasty: multicentric comparative study of techniques and accesses. J Laparoendosc Adv Surg Tech A. 2011 Jun;21 (5):399-403. DOI: 10.1089/lap.2010.0281.
21. Abdel-Karim AM, Fahmy A, Moussa A, Rashad H, Elbadry M, Badawy H, Hammady A. Laparoscopic pyeloplasty versus open pyeloplasty for recurrent ureteropelvic junction obstruction in children. J Pediatr Urol. 2016 Dec;12 (6):401.e1-401.e6. DOI: 10.1016/j.jpurol.2016.06.010
22. Schlomer BJ, Smith PJ, Barber TD, Baker LA. Nephrectomy for hypertension in pediatric patients with a unilateral poorly functioning kidney: a contemporary cohort. J Pediatr Urol. 2011 Jun; 7 (3): 373-7. DOI: 10.1016/j.jpurol.2011.02.020.
23. El-Hout Y, Licht C, Pippi Salle JL, Ngan BY, Bagli DJ, Lorenzo AJ, Farhat WA. Hypertension in children with poorly functioning unilateral kidney: predictors of resolution after nephrecto-
my. BJU Int. 2010 Nov;106 (9):1376-80. DOI: 10.1111/j.1464-410X.2010.09308.x
24. Autorino R, Eden C, El-Ghoneimi A, Guazzoni G, Buffi N, Peters CA, et al. Robot-assisted laparoscopic repair of ureteropelvic junction obstruction: A systematic review and meta-analysis. Eur Urol. 2014 Feb;65 (2):430-52. DOI: 10.1016/j.eururo.2013.06.053.
25. Wagner M, Mayr J, Häcker FM. Improvement of renal split function in hydronephrosis with less than 10% function. Eur J Pediatr Surg. 2008 Jun;18 (3):156-9. DOI: 10.1055/s-2008-1038445
26. Bansal R, Ansari MS, Srivastava A, Kapoor R. Long-term results of pyeloplasty in poorly functioning kidneys in the pediatric age group. J Pediatr Urol. 2012 Feb;8 (1):25-8. DOI: 10.1016/j. jpurol.2010.12.012
27. Ortapamuk H, Naldoken S, Tekdogan UY, Aslan Y, Atan A. Differential renal function in the prediction of recovery in adult obstructed kidneys after pyeloplasty. Ann Nucl Med. 2003 Dec;17 (8):663-8.
Информация об авторах:
Поляков Николай Васильевич, к.м.н., заведующий отделом реконструктивной урологии с группой микрохирургии и урологической травмы НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина — филиал ФГБУ «НМИЦ радиологии» Минздрава России. E-mail: [email protected] Кешишев Николай Георгиевич, к.м.н., заведующий инновационным отделом НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина — филиал ФГБУ «НМИЦ радиологии» Минздрава России. E-mail: [email protected]
Гурбанов Шамиль Шукурович, к.м.н., старший научный сотрудник отдела эндоурологии НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина — филиал ФГБУ «НМИЦ радиологии» Минздрава России . E-mail: [email protected]
Григорьева Мария Викторовна, к.м.н., младший научный сотрудник инновационного отдела НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина — филиал ФГБУ «НМИЦ радиологии» Минздрава России. E-mail: [email protected]
Арустамов Левон Дмитриевич, к.м.н., научный сотрудник отдела эндоурологии НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина -филиал ФГБУ «НМИЦ радиологии» Минздрава России
Казаченко Александр Викторович, д.м.н., профессор, заместитель директора по лечебной работе, главный врач НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина — филиал ФГБУ «НМИЦ радиологии» Минздрава России
Алексеев Борис Яковлевич, д.м.н., профессор, заместитель директора по науке Московского научно-исследовательского онкологического института им. П.А. Герцена — филиал ФГБУ «НМИЦ радиологии» Минздрава России
Information about authors:
Nikolay V. Polyakov, PhD, head of the Department of Reconstructive Urology with a group of microsurgery and urological trauma, N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology — Branch of the National Medical Radiology Research Centre of the Ministry of Health of the Russian Federation. E-mai1: [email protected]
Nikolay G. Keshishev, PhD, head of the Innovation Department, N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology — Branch of the National Medical Radiology Research Centre of the Ministry of Health of the Russian Federation. E-mail: [email protected]
Shamil Sh. Gurbanov, PhD, senior researcher, Department of Endourology, N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology -Branch of the National Medical Radiology Research Centre of the Ministry of Health of the Russian Federation. E-mail: [email protected] Maria V. Grigorieva, PhD, junior researcher, Innovation Department, N. Lopatkin Scientific Research Institute of Uro1ogy and Interventiona1 Radio1ogy — Branch of the Nationa1 Medica1 Radio1ogy Research Centre of the Ministry of Hea1th of the Russian Federation. E-mai1: [email protected]
Levon D. Arustamov, PhD, researcher, Department of Endouro1ogy, N. Lopatkin Scientific Research Institute of Uro1ogy and Interventiona1 Radio1ogy — Branch of the Nationa1 Medica1 Radio1ogy Research Centre of the Ministry of Hea1th of the Russian Federation
A1exander V. Kazachenko, MD, professor, deputy director for medica1 work, chief physician, N. Lopatkin Scientific Research Institute of Uro1ogy and Interventiona1 Radio1ogy — Branch of the Nationa1 Medica1 Radio1ogy Research Centre of the Ministry of Hea1th of the Russian Federation
Boris Ya. A1ekseev, MD, Professor; deputy director for science, P. Hertsen Moscow Onco1ogy Research Institute — Branch of the Nationa1 Medica1 Radio1ogy Research Centre of the Ministry of Hea1th of the Russian Federation
Урология » Эффективность лапароскопической пластики при первичных стриктурах лоханочно-мочеточникового сегмента
1. Kletscher B.A., Segura J.W. Surgical management of UPJ obstruction in adults. AUA Update Series. 1996;XV:18.
2. Kausik S., Segura J.W. Surgical management of ureteropelvic junction obstruction in adults. International Braz J Urol Official Journal of the Brazilian Society of Urology. 2003;29(1):3–10.
3. Nishi M., Matsumoto K., Fujita T., Iwamura M. Improvement in Renal Function and Symptoms of Patients Treated with Laparoscopic Pyeloplasty for Ureteropelvic Junction Obstruction with Less than 20% Split Renal Function. Department of Urology, Kitasato University School of Medicine, Kanagawa, Japan. J Endourol. 2016 Oct 14.
4. Kletscher B.A., Segura J.W. Surgical management of UPJ obstruction in adults. AUA Update Series. 1996;XV:18.
5. Martov A.G., Gurbanov Sh.Sh., Mudraya I.S.: Evaluation of the contractile function of the upper urinary tract using multichannel impedance ureterography before and after endoureteropyelotomy. Urologiia. 2009;(4),:25–30. Russian (Мартов А.Г., Гурбанов Ш.Ш., Мудрая И.С.: Оценка сократительной функции верхних мочевыводящих путей методом многоканальной импедансной уретерографии до и после эндоуретеропиелотомии. Урология. 2009;(4),:25–30).
6. Martov A.G., Gurbanov Sh.Sh.. Tokareva E.V., Shcherbinin S.N., Kornienko S.I. Comparative evaluation of the results of magnetic resonance urography and other diagnostic methods in patients with iatrogenic injury of the ureter and the ureteropelvic junction. Urologiia. 2009;(3):7–12. Russian (Мартов А.Г., Гурбанов Ш.Ш., Токарева Е.В., Щербинин С.Н., Корниенко С.И. Сравнительная оценка результатов магнитно-резонансной урографии и других методов исследования у пациентов с ятрогенным повреждением мочеточника и лоханочно-мочеточникового сегмента. Урология. 2009;(3):7–12).
7. Pavlov A.Yu., Pugachev A.G., Polyakov N.V., Lisenok A.A. Prognostic implications of surgical treatment of pediatric hydronephrosis. In: Plenum pravleniya Rossiiskogo obshchestva urologov. Materialy plenuma, Tyumen’, 24-27 maya 2005 g. Р. 147–148. Russian (Павлов А.Ю., Пугачев А.Г., Поляков Н.В., Лисенок А.А. Прогностическое значение метода оперативного лечения гидронефроза у детей. В кн.: Пленум правления Российского общества урологов. Материалы пленума, Тюмень, 24–27 мая 2005 г. С. 147–148).
8. Pavlov A.Yu., Polyakov N.V., Ignashin N.S., Golovanov S.A. Algorithm of diagnosis and treatment of obstructive uropathies of the upper urinary tract in children and adolescents. In: Plenum pravleniya Rossiiskogo obshchestva urologov. Materialy plenuma, Tyumen’, 24-27 maya 2005 g. p. 148–149. Russian (Павлов А.Ю., Поляков Н.В., Игнашин Н.С., Голованов С.А. Алгоритм диагностики и лечения обструктивных уропатий верхних мочевых путей у детей и подростков. В кн.: Пленум правления Российского общества урологов. Материалы пленума, Тюмень, 24–27 мая 2005 г. С. 148–149).
9. Wickham J.E., Kellet M.J. Percutaneous pyelolysis. Eur Urol. 1983;9:122–124.
10. Martov A.G., Kvasha V.I. Percutaneous endopyelotomy. Urologiya i nefrologiya. 1990;6:22–25. Russian (Мартов А.Г., Кваша В.И. Перкутанная эндопиелотомия. Урология и нефрология. 1990;6:22–25).
11. Martov A.G., Ergakov D.V., Salyukov R.V., Gushchin B.L., Chernov N.A. X-ray guided endoscopic treatment of strictures of the upper urinary tract (A literature review). Urologiia. 2000;1:38–43. Russian (Мартов А.Г., Ергаков Д.В., Салюков Р.В., Гущин Б.Л., Чернов Н.А. Рентгеноэндоскопические методы лечения стриктур верхних мочевыводящих путей (обзор литературы). Урология. 2000;1:38–43).
12. Chen W.N., Ye X.J., Liu S.J., Xiong L.L., Huang X.B., Xu ., Wang X.F. Comparison of three surgical methods of ureteropelvic junction obstruction in therapeutic effect and complication. Beijing Da Xue Xue Bao. 2016;48(5):817–821.
13. Corbett H.J., Mullassery D. Outcomes of endopyelotomy for pelviureteric junction obstruction in the paediatric population: A systematic review. J Pediatr Urol. 2015;11(6):328–336. Doi: 10.1016/j.jpurol.2015.08.014.
14. Lai W.R., Stewart C.A., Thomas R.: From Endopyelotomy to Robotic Pyeloplasty: What a Safari! J Endourol. 2016.
15. Martov A.G., Gurbanov Sh.Sh., Stepanov V.S., Kornienko S.I. X-ray guided endoscopic diagnosis and treatment of iatrogenic injuries of the upper urinary tract. Urologiia. 2009;2:25–32. Russian (Мартов А.Г., Гурбанов Ш.Ш., Степанов В.С., Корниенко С.И. Рентгеноэндоскопическая диагностика и лечение ятрогенных повреждений верхних мочевыводящих путей. Урология. 2009;2:25–32).
16. Zabirov K.I., Yarovoi S.K. Antibacterial prophylaxis for endoscopic surgical interventions in urology. Consilium medicum. 2010;7(12):51–54. Russian (Забиров К.И., Яровой С.К.: Антибактериальная профилактика при эндоскопических оперативных вмешательствах в урологии. Consilium medicum. 2010;7(12):51–54).
17. Bondarenko S.G. A differentiated approach to the choice of the method of minimally invasive surgical correction of hydronephrosis: Ph.D. Thesis. Volgograd, 2007. 27 p. Russian (Бондаренко С.Г. Дифференцированный подход к выбору способа малоинвазивной хирургической коррекции гидронефроза: автореф. дис. канд. мед. наук. Волгоград, 2007. 27 с.).
18. Komyakov B.K., Guliev B.G., Shibliev R.G. Endoscopic interventions for strictures of the upper urinary tract. Pervyi Ros. kongress po endourologii: tez. dokl. M., 2008. S. 83–85. Russian (Комяков Б.К., Гулиев Б.Г., Шиблиев Р.Г. Эндоскопические вмешательства при стриктурах верхних мочевыводящих путей. Первый Рос. конгресс по эндоурологии: тез. докл. М., 2008. С. 83–85).
19. Bansal P., Gupta A., Mongha R. et al. Laparoscopic versus open pyeloplasty: Comparison of two surgical approaches – a single centre experience of three years. J Minim Access Surg. 2008;4:76–79.
20. Iwamura M., Soh S., Irie A. et al. Laparoscopic pyeloplasty for ureteropelvic junction obstruction: outcome of initial 12 procedures. Int J Urol. 2004;11:449–455.
21. Juliano R.V., Mendonca R.R., Meyer F. et al. Long-term outcome of laparoscopic pyeloplasty: multicentric comparative study of techniques and accesses. J Laparoendosc Adv Surg Tech A. 2011;21:399–403.
22. Abdel-Karim A.M., Fahmy, Moussa A., Rashad H., Elbadry M., Badawy H., Hammady A. Laparoscopic pyeloplasty versus open pyeloplasty for recurrent ureteropelvic junction obstruction in children. J Pediatr Urol. 2016. pii: S1477-5131(16)30186-3.
23. Juliano R.V., Mendonça R.R., Meyer F., Rubinstein M., Lasmar M.T., Korkes F., Tavares A., Pompeo A.C., Tobias-Machado M. Long-term outcome of laparoscopic pyeloplasty: multicentric comparative study of techniques and accesses. J Laparoendosc Adv Surg Tech A. 2011;21(5):399–403.
24. El-Hout Y., Licht C., Pippi Salle J.L. et al. Hypertension in children with poorly functioning unilateral kidney: predictors of resolution after nephrectomy. BJU Int. 2010;106:1376–1380.
25. Autorino R., Eden C., El-Ghoneimi A. et al. Robot-assisted laparoscopic repair of ureteropelvic junction obstruction: A systematic review and meta-analysis. Eur Urol. 2014;65:430–452.
26. Wagner M., Mayr J., Häcker F.M. Improvement of renal split function in hydronephrosis with less than 10 % function. Eur J Pediatr Surg. 2008;18:156–159.
27. Bansal R., Ansari M.S., Srivastava A., Kapoor R. Long-term results of pyeloplasty in poorly functioning kidneys in the pediatric age group. J Pediatr Urol. 2012;8:25–28.
28. Ortapamuk H., Naldoken S., Tekdogan U.Y., Aslan Y., Atan A. Differential renal function in the prediction of recovery in adult obstructed kidneys after pyeloplasty. Ann Nucl Med. 2003;17:663–668.
Отделения
Гидронефроз – расширение собирательной системы почки, возникающее вследствие нарушения оттока мочи в области отхождения мочеточника от лоханки, которое может приводить к снижению почечной функции вплоть до полной ее утраты. Пластические вмешательства на лоханочно-мочеточниковом сегменте высокоэффективная операция, обеспечивающая успех в 94-96% случаев. Развитие малоинвазивных технологий позволило вытеснить открытую хирургию и в настоящий момент лапароскопическая пиелопластика является ,,золотым стандартом,, хирургии гидронефроза.
Для коррекции данной патологии применяются следующие виды малоинвазивных вмешательств:
1. Лапароскопическая пластика пиелоуретерального сегмента с применением трансабдоминального и ретроперитонеоскопического доступов;
2. Лапароскопически-ассистированная открытая пиелопластика.
3. Эндоскопические вмешательства.
4. Роботизированная пиелопластика.
Пластические операции при гидронефрозе у детей в течении длительного времени выполнялись открытым доступом, который имеет существенные недостатки: достаточно высокая травматичность, вследствие рассечения большого массива мышц при разрезе, болевой синдром, необходимость в длительной реабилитации и нахождении ребенка в стационаре, невысокий косметический результат.
В настоящее время лапароскопическая хирургия занимает лидирующие позиции при выполнении многих оперативных вмешательств. Лапароскопическая пиелопластика у детей обладает рядом неоспоримых преимуществ, открывая для лечения гидронефроза у детей совершенно новые возможности. Операция существенно уменьшает болевой синдром, сводит к минимуму кровопотерю. Ребенок, перенесший лапаросокпическую пиелопластику, быстро восстанавливается и успешно проходит курс послеоперационной реабилитации. На теле пациента отсутствуют шрамы и рубцы. Оптическое увеличение, которое обеспечивает лапароскопическая технология, позволяет добиться высокого качества аппроксимации тканей в области пиелоуретерального анастомоза.
Суть вмешательства заключается в иссечении суженного участка мочеточника и/или лоханки, и формирования широкого соединения между мочеточником и лоханкой.
Показанием к хирургическому вмешательству является не сам факт наличия расширения чашечно-лоханочной системы, а возникающее в следствии расширения чашечно-лоханочной системы и нарушения оттока мочи повреждение паренхимы почки и снижение почечной функции. Без выявления факта снижения функции почки показание к пиелопластике могут формироваться только в случае если заболевание сопровождается болью или рецидивирующей инфекцией мочевыводящих путей.
ПРОЯВЛЕНИЕ ГИДРОНЕФРОЗА
В подавляющем большинстве случаев у детей раннего возраста односторонний гидронефроз на фоне обструкции лоханочно-мочеточникового сегмента протекает бессимптомно.
У пациентов этой группы клинические проявления могут сводиться к появлению инфекции мочевыводящих путей.
У детей старшего возраста вероятность клинических проявлений значительно повышается.
Наиболее частым симптомом гидронефроза является боль, иногда сопровождающаяся рвотой. Боль обусловлена повышением внутрилоханочного давления.
Инфекция мочевыводящих путей является вторым по частоте клиническим проявлением у пациентов с гидронефрозом. В общем анализе мочи обнаруживается повышение лейкоцитов, эритроцитов, белка, наличие бактерий. Иногда проявлением гидронефроза может быть пальпируемое опухолевидное образование в брюшной полости.
При появлении вышеперечисленных симптомов следует обязательно проконсультироваться с врачом.
При выявлении на послеродовом УЗИ размера лоханки более 18мм в диаметре считается угрожаемым с точки зрения необходимости хирургии. Тем не менее размер лоханки не может быть единственным критерием который определяет показания к хирургии и в каждом конкретном случае решение принимается индивидуально по совокупности симптомов и особенностей течения заболевания.
После лапаросокпической пиелопластики послеоперационном периоде в нашем отделении используются различные варианты дренирования мочевыводящих путей. По степени социальной адаптации для пациента, мочеточниковый стент является оптимальным вариантом, однако при этом виде дренирования существует риск нарушения функции дренажа, которое может потребовать дополнительного вмешательства.
Использование пиелостомических дренажей имеют низкую социальную адаптацию для пациента так как дренаж выводится наружу. Этот тип дренирования является полностью контролируемым. Для оценки восстановления проходимости пиелоуретерального анастомоза мы используем исследование внутрилоханочного давления, которое регистрируем после постепенного перекрытия стомы начиная с 3х часов. Использование указанного подхода позволяет исключить риск развития острого обструктивного пиелонефрита.
ДИАГНОСТИКА
1.Ультразвуковое исследование(УЗИ) — Первичный и самый доступный метод диагностики гидронефроза. Позволяет выявить расширение полостной системы почки. Несомненным плюсом метода является простота и доступность.
Эпоха лапароскопической пиелопластики у детей началась в 1993 году. Одним из первых кто выполнил подобный вид вмешательства был Schuessler. Вначале лапароскопическую пиелопластику использовали у детей старших возрастных групп. С 2006 года появились сообщения о лапароскопических пиелопластиках у детей первого года жизни. Продолжением эволюции малоинвазивных технологий с 2000 года стало внедрение роботической хирургии. Отличие от классической лапароскопической хирургии заключается в том, что оперирующий хирург манипулирует установленными инструментами дистанционно при этом обеспечивается более четкие и плавные движения в совокупности с трехмерным изображением. Однако существенным минусом роботической хирургии является дороговизна оборудования и расходных материалов. В детской практике относительным ограничением можно считать отсутсвие инструментов малых диаметров.
Для лечения гидронефроза у детей в урологическом отделении ОДКБ на протяжении последних 10 лет с успехом применяется лапароскопическая пиелопласика. Вопрос о целесообразности и технике хирургического вмешательства решается индивидуально для каждого ребёнка.
2. Спиральная компьютерная (СКТ)- дополнительный метод диагностики обладающий лучшей визуализацией и позволяющий установить диагноз в тех случаях когда экскреторная урографии малоинформативна.
Гидронефроз 3ст по SFU слева
3.Диуретическая радиоизотопная ренография является одним из важнейших методов в изучении состояния почек, определения их функции и степени выраженности обструкции в области пиелоуретерального сегмента. Наше отделение тесно сотрудничает с радиоизотопной лабораторий мед. Университете г. Ростова-на-Дону к нашим пациентам выполняется данная процедура. К сожалению не во всех клиниках России есть возможность проведения данного обследования.
4.Развитие технологии функциональной МРТ (магнитно-резонансной томографии) в последние годы позволяет предположить, что в ближайшем будущем исследование встанет на второе место по диагностической важности после ультразвукового исследования.
Начиная с 2018 года пациентам нашего отделения внедрен новый многообещающий тип обследования – функциональная магнитно-резонансная урография. Это обследование позволяет объединить преимущества компьютерной томографии и одновременно оценить функциональное состояние почек, исследуемое в настоящий момент с помощью радиоизотопного исследования. Это несомненно упрощает алгоритм обследования пациента и сокращает время принятия важных решений по дальнейшему ведению пациента.
ПРИЧИНЫ ГИДРОНЕФРОЗА
· Сужение мочеточника в области отхождения его от лоханки
· Образование клапанов из слизистой в области лоханочно-мочеточникового сегмента
· Эмбриональные спайки вызывающие искривление мочеточника за счет его фиксации с лоханкой
· Высокое отхождение мочеточника от лоханки
· Пересекающие сосуды приводящие к сдавлению мочеточника в месте его отхождения от лоханки
Гидронефроз у детей достаточно коварное заболевание которое иногда специалисты именуют как -,,молчаливый убийца,,. Такое грозное определение патология получила из-за того, что в большинстве случаев может протекать бессимптомно, никак не проявляя себя. Однако с течением времени пораженная почка может терять свою функцию безвозвратно. Задача детского уролога своевременно выявить и при необходимости устранить проблему сохранив функцию почки.
Диагностика и лечение гидронефроза — Клиники Беларуси
Диагностика и лечение гидронефроза
Гидронефроз – заболевание, характеризующееся прогрессирующим расширением чашечно-лоханочной системы почки вследствие нарушенния оттока мочи в лоханочно-мочеточниковом сегменте.
При прогрессировании заболевания происходит постепенное истончение коркового вещества почки и развитие почечной недостаточности. Особую опасность представляет попадание инфекции в гидронефротически измененную почку, так как могут развиваться гнойно-воспалительные осложнения, которые могут повлечь за собой удаление почки (нефрэктомию).
Выделяют два вида гидронефроза.
• Врожденный гидронефроз может быть обусловлен множеством причин. К ним относят врожденную обструкцию, аномальное расположение мочевыводящих путей. При врожденном гидронефрозе нарушение оттока мочи может быть обусловлено стенозом лоханочно-мочеточникового сегмента либо сдавлением лоханочно-мочеточникового сегмента извне аномально расположенным артериальным сосудом.
• При приобретенном гидронефрозе нарушение оттока мочи из почки чаще всего происходит из-за наличия в почке камня либо опухоли. Кроме того, он может возникнуть вследствие повреждения мочеточников.
В целом причины нарушения оттока мочи при гидронефрозе в зависимости от расположения можно разделить на 5 групп:
1. Проблемы в зоне мочеиспускательного канала или мочевого пузыря;
2. Сдавление мочеточника снаружи;
3. Наличие препятствия внутри просвета мочеточника;
4. Наличие препятствия в стенке лоханки или мочеточника;
5. Аномальное расположение мочеточника или его перегиб.
Наличие гидронефроза может длительное время протекать незаметно. Со временем со стороны пораженной почки в пояснице может появляться тупая ноющая боль, не связанная с переменой положения тела пациента. Иногда может наблюдаться выделение крови при мочеиспускании. При прогрессировании процесса, особенно если поражаются обе почки, постепенно может развиваться почечная недостаточность. Наличие вышеуказанных симптомов является показанием для обследования.
Диагностика гидронефроза включает в себя следующие методы:
1. Ультразвуковое исследование почек с целью определения их размеров, контуров, состояния чашечно-лоханочной системы и толщины паренхимы органа.
2. Обзорная и внутривенная урография – надежный информативный метод, который позволяет судить о выделительной функции и состоянии чашечно-лоханочной системы почек. Для этого внутривенно вводится специальный препарат, который выделяется с мочой и становится видимым на рентгеновских снимках. При выполнении серии снимков можно определить, насколько своевременно контрастное вещество выделяется почками.
3. Нефросцинциграфия позволяет определить процент фукционирующей почечной ткани.
4. Компьютерная томография может использоваться с целью уточнения диагноза в сомнительных случаях.
В качестве лечения при вторичном гидронефрозе показано восстановление проходимости лоханочно-мочеточникового сегмента путем удаления камня. При врожденном гидронефрозе необходимо выполнять пластику лоханочно-мочеточникового сегмента пораженной почки с целью восстановления нормального оттока мочи. Однако пластика лоханочно-мочеточникового сегмента показана только в том случае, если пораженная почка еще сохраняет свою функциональную способность, что подтверждается наличием не менее 15% функционирующих нефронов почки по данным нефросцинциграфии. В ином случае показана нефрэктомия. На сегодняшний день самым современным методом лечения первичного гидронефроза является лапароскопическая пластикалоханочно-мочеточникового сегмента.
Лапароскопическая пластика гидронефроза – малоинвазивный современный метод коррекции гидронефротической трансформации почки. Операция заключается в иссечении пораженного участка лоханочно-мочеточникового сегмента и создании широкого соустья для обеспечения беспрепятственного оттока мочи из почки. Операция выполняется под общим наркозом. Перед началом пластики лоханочно-мочеточникового сегмента выполняется установка специального внутреннего стента в пораженную почку. Стент удаляется в среднем через 1 месяц после операции. Длительность лапароскопической пластики гидронефроза составляет около 2-3 часов. Пребывание в стационаре составляет в среднем 4-5 суток.
В медицинских учреждениях Республики Беларусь, оснащенных самым современным оборудованием, работает квалифицированный персонал, готовый оказать Вам весь спектр медицинских услуг для своевременной диагностики и лечения гидронефроза.
Лапароскопическая пиелопластика | Johns Hopkins Medicine
Лапароскопический доступЛапароскопическая пиелопластика — это способ выполнения реконструктивной хирургии сужения или рубцевания, когда мочеточник (трубка, отводящая мочу из почки в мочевой пузырь) прикрепляется к почке с помощью минимально инвазивной процедуры.
Эта операция используется для устранения закупорки или сужения мочеточника в месте выхода из почки. Эта аномалия называется обструкцией лоханочно-мочеточникового соединения (UPJ), которая приводит к плохому и медленному оттоку мочи из почки.Обструкция UPJ может потенциально вызвать боль в животе и в боку, камни, инфекцию, высокое кровяное давление и ухудшение функции почек.
По сравнению с традиционной открытой хирургической техникой лапароскопическая пиелопластика привела к значительно меньшей послеоперационной боли, более короткому пребыванию в больнице, более раннему возвращению к работе и повседневной деятельности, более благоприятному косметическому результату и результатам, идентичным результатам открытой процедуры .
Хирургия
Обструкция лоханочно-мочеточникового перехода (UPJ)Лапароскопическая пиелопластика проводится под общим наркозом.Типичная продолжительность операции составляет от трех до четырех часов. Операция проводится через три небольших (1 см) разреза в брюшной полости. Через эти замочные отверстия в брюшную полость вводятся телескоп и небольшие инструменты, которые позволяют хирургу устранить закупорку / сужение, не помещая руки в брюшную полость.
Небольшая пластиковая трубка (называемая мочеточниковым стентом) остается внутри мочеточника в конце процедуры, чтобы перекрыть восстановление после пиелопластики и помочь опорожнить почку.Этот стент остается на месте в течение четырех недель и обычно удаляется в кабинете врача. Также будет оставлен небольшой дренаж, выходящий из вашего бока, чтобы слить жидкость вокруг почки и восстановить пиелопластику.
Возможные риски и осложнения
Лапароскопическая рассеченная пиелопластикаХотя эта процедура оказалась очень безопасной, как и в любой хирургической процедуре, есть риски и потенциальные осложнения. Показатели безопасности и осложнений аналогичны по сравнению с открытой операцией.К потенциальным рискам относятся:
Кровотечение : Кровопотеря во время этой процедуры обычно незначительна (менее 100 см3), и переливание крови требуется редко. Если вы все еще заинтересованы в переливании аутологичной крови (сдаче собственной крови) до операции, вы должны сообщить об этом своему хирургу. Когда пакет с информацией о вашей операции будет отправлен вам по почте или передан вам, вы получите форму разрешения, которую вы можете передать в Красный Крест в вашем районе.
Инфекция : Все пациенты проходят лечение внутривенными антибиотиками широкого спектра действия до начала операции, чтобы снизить вероятность заражения после операции. Если после операции у вас появятся какие-либо признаки или симптомы инфекции (лихорадка, выделения из разреза, частое мочеиспускание, дискомфорт, боль или что-то еще, что вас может беспокоить), немедленно свяжитесь с нами.
Повреждение ткани / органа : Хотя и нечасто, возможное повреждение окружающих тканей и органов, включая кишечник, сосудистые структуры, селезенку, печень, поджелудочную железу и желчный пузырь, может потребовать дальнейшего хирургического вмешательства.Может возникнуть травма нервов или мышц, связанных с позиционированием.
Пиелопластика: определение, восстановление и восстановление
Обзор
Что такое пиелопластика?
Пиелопластика — это операция по исправлению состояния, называемого обструкцией лоханочно-мочеточникового соединения (UPJ).«Пиело» относится к почке (почечной лоханке). «Пластика» — это термин, обозначающий хирургическую процедуру, при которой что-то ремонтируется, восстанавливается или заменяется.
Кому нужна пиелопластика?
Взрослым и детям может потребоваться пиелопластика. Один ребенок из каждых 1500 рождается с непроходимостью UPJ. У мужчин он вдвое больше, чем у женщин.
Для младенцев, если их состояние не улучшится в течение 18 месяцев, им, вероятно, потребуется пиелопластика.
Дети старшего возраста, подростки и взрослые также могут получить обструкцию UPJ и могут нуждаться в пиелопластике, если их почка заблокирована.
Детали процедуры
Насколько инвазивна пиелопластика?
Младенцы или младенцы подвергаются открытой пиелопластике. Открытая операция означает, что при разрезании кожи и тканей хирург может видеть все органы, к которым он обращается, непосредственно своим зрением, а не камерой (как при лапароскопии).Для младенцев эта открытая операция более безопасна, чем лапароскопическая (замочная скважина) операция у взрослых с обструкцией верхнечелюстного сустава.
У детей старшего возраста и взрослых хирург делает только небольшой разрез, через который они могут оперировать с помощью камеры (лапароскопия). Также можно использовать робота.
Пиелопластика — амбулаторная или стационарная операция?
Стационар. Вы или ваш ребенок можете находиться в больнице от одного до двух дней.
Кто выполняет пиелопластику?
Общий хирург или уролог.
Сколько длится пиелопластика?
Около трех часов.
Я буду спать во время пиелопластики?
Да. Вы или ваш младенец будете находиться под общим наркозом и полностью спать.
Как мне подготовить себя или своего ребенка к пиелопластике?
За день до процедуры вам или вашему ребенку нельзя будет есть или пить в течение определенного времени, назначенного вашим лечащим врачом. Если вы не будете следовать их инструкциям, пиелопластика может быть отложена.Перед операцией вам нужно будет подписать форму согласия, пройти процедуру с анестезиологом и следовать всем остальным инструкциям, которые требует ваша больница.
Как работает пиелопластика?
- Младенцы / младенцы: Во время открытой пиелопластики делается разрез на два-три дюйма чуть ниже ребер ребенка и удаляется непроходимый сегмент мочеточника. Затем к почечной лоханке прикрепляют мочеточник нормального калибра. Стент (крошечная силиконовая трубка) ставится для отвода мочи из почки.После заживления стент будет удален.
- Дети старшего возраста / взрослые: Хирург сделает несколько небольших разрезов — каждый от восьми до 10 миллиметров. Робот, который помогает вашему хирургу, имеет от трех до четырех роботизированных рук. Двое или трое используют инструменты, а один держит камеру. Инструменты имеют такой же диапазон движений, что и человеческая рука, и могут исправить обструкцию верхнечелюстного сустава, вырезая узкую / поврежденную часть и повторно соединяя нормальную ткань.
Риски / преимущества
Каковы преимущества пиелопластики?
Он имеет самый высокий процент успеха по сравнению с другими хирургическими вариантами обструкции UPJ.
Каковы риски или осложнения пиелопластики?
Как и при любой операции, существует множество рисков, включая дополнительное кровотечение, повреждение окружающих органов и переход от лапароскопической операции к открытой. Существует риск получить наркоз, который рассмотрит ваш анестезиолог. После операции риски включают рубцы, инфекцию, грыжу, сгустки крови и необходимость дополнительных операций, если непроходимость вернется. Вы или ваш ребенок также можете испытывать утечку мочи из места, где почка соединяется с мочеточником.
Редко может быть травма:
- Основные кровеносные сосуды.
- Тонкая кишка.
- Толстая кишка.
- Желудок.
- Печень, селезенка или поджелудочная железа
- Яичник.
- Фаллопиевы трубы.
- Мочевой пузырь.
Болезненно ли пиелопластика?
Вы или ваш ребенок можете почувствовать боль после пиелопластики. Боль может пройти через неделю, и вам или вашему ребенку будут назначены лекарства, которые помогут свести к минимуму эту боль.
Восстановление и Outlook
Что происходит после пиелопластики?
Пиелопластика должна предотвратить ухудшение функции почек, помогая им дренироваться. Сразу после процедуры, проведенной вами или вашим ребенком, во время пребывания в больнице вы или ваш ребенок испытаете следующее:
- Вы останетесь в больнице на день или два после операции.Восстановление обычно происходит быстро, и вы сможете есть и пить уже через несколько часов после операции.
- После операции вам следует попытаться встать и передвигаться, но не делайте ничего слишком сложного.
- Вам будут вводить антибиотики внутривенно (через трубку, которая вводится в руку). Вас могут отправить домой с пероральными антибиотиками.
- Ваш мочевой катетер или катетер Фолея будут обслуживать.
- У вас может быть катетер двойной J (JJ) или трубка для чрескожной нефростомии (PCN).Эта трубка находится внутри вашей мочевыделительной системы, помещается либо внутри вашего желудка (JJ), либо снаружи (PCN). Эти трубки выполняют работу вашего мочеточника, давая ему время на заживление. Трубка PCN будет удалена вскоре после операции.
- Иногда к брюшной полости рядом с разрезом прикрепляют дренаж для отвода лишней жидкости. Его следует удалить перед тем, как отправиться домой.
- Возможно, ваш мочеточник опух. В течение нескольких дней после операции у вас могут быть боли. Ваш лечащий врач назначит вам обезболивающее перорально (внутрь), через внутривенный зонд или в виде инъекции.
- Еще один источник боли — спазм мочевого пузыря. Вы можете почувствовать, как внезапно сжимается мочевой пузырь. Это потому, что катетеры и другие трубки могут его раздражать. Есть лекарство, которое поможет ему расслабиться и уменьшить боль.
- Поначалу может быть плохой дренаж почек. Это часто улучшается со временем по мере заживления области.
Позаботьтесь о себе после операции. Лучше хотя бы какое-то время иметь с собой опекуна. Во время выздоровления вам или вашему ребенку следует:
- Пейте много жидкости.
- Храните повязки (повязки) на животе столько, сколько рекомендует ваш лечащий врач (обычно от 24 до 48 часов).
- Принимайте душ. Избегайте ванн, так как они могут вызвать инфекцию.
- Обратитесь к своему врачу, чтобы снять швы, если они не растворяются.
- Через несколько недель после операции стент будет удален во время короткой процедуры с местной анестезией, и ваш лечащий врач может использовать ультразвук для проверки опухших почек.
Каков прогноз (перспективы) после пиелопластики?
Пиелопластика имеет хороший долгосрочный успех. Но, как и при любом хирургическом вмешательстве, существует риск возврата рубцовой ткани и повторной обструкции почки. Ваш лечащий врач будет продолжать следить за этим в течение нескольких месяцев после операции
Насколько эффективна пиелопластика?
Пиелопластика эффективна в 85–100% случаев.
Как скоро я смогу вернуться к нормальной жизни?
Слушайте инструкции вашего лечащего врача, как вернуться к «нормальному состоянию».«Попробуйте короткие прогулки сразу после операции. Через четыре-шесть недель вы можете поднимать тяжелые вещи и снова возобновлять тренировки. Между тем, вы можете принять душ, если потом вытираетесь насухо. Начинайте водить машину только тогда, когда вам это удобно, если вы можете сделать экстренную остановку и если вы не принимаете наркотические обезболивающие.
Когда звонить доктору
Когда мне следует связаться с хирургом или другим поставщиком медицинских услуг?
Обязательно приходите на все контрольные встречи.Обратитесь к своему хирургу или другому поставщику медицинских услуг раньше, если вы или ваш ребенок испытываете одно из следующего:
- Тошнота или рвота.
- Признаки инфекции, такие как лихорадка, теплая кожа вокруг разреза, покраснение вокруг разреза, гной или дренаж.
- Сильная боль, которую не снимают обезболивающие.
- Увеличенная припухлость вокруг разрезов.
- Сильное кровотечение в моче (она густая и красная, как кетчуп).
- Боль в груди, одышка или обморок.
Медицинская терапия, хирургическая терапия, показатели успешности вариантов лечения
Саймонс С.Дж., Бхируд П.С., Джайн В., Шетти А.С., Десаи М.Р. Лапароскопическая пиелопластика: наш новый золотой стандарт. Дж Эндоурол . 2009 23 марта (3): 463-7. [Медлайн].
Эль-Нахас А.Р., Абу-Эль-Гар М., Шома А.М., Эраки И., Эль-Кенави М.Р., Эль-Каппани Х. Роль многофазной спиральной компьютерной томографии в планировании хирургического лечения обструкции тазово-мочеточникового перехода. БЖУ Инт . 2004 сентябрь 94 (4): 582-7. [Медлайн].
Conway JJ, Maizels M. Ренограмма с «хорошо выдержанным» диуретиком: стандартный метод обследования бессимптомных новорожденных с гидронефрозом или гидроуретеронефрозом. Отчет о совместных собраниях Общества урологии плода и членов Педиатрической ядерной медицины C. J Nucl Med . 1992 ноябрь 33 (11): 2047-51. [Медлайн].
фон Рундштедт FC, Scovell JM, Bian SX, Lee D, Mayer WA, Link RE.Процент клиренса индикатора за 40 минут при сканировании почек MAG3 более чувствителен, чем T 1/2 для симптоматической обструкции лоханочно-мочеточникового перехода. Урология . 2017 май. 103: 245-250. [Медлайн].
Ниши М., Мацумото К., Фудзита Т., Ивамура М. Улучшение функции почек и симптомы у пациентов, получавших лапароскопическую пиелопластику по поводу обструкции лоханочно-мочеточникового перехода с расщеплением функции почек менее чем на 20%. Дж Эндоурол . 2016 ноя.30 (11): 1214-1218. [Медлайн].
Singla N, Lay AH, Cadeddu JA. Плохая раздельная функция почек и возраст у взрослых пациентов с обструкцией лоханочно-мочеточникового перехода не влияют на функциональные результаты пиелопластики. Банка Дж. Урол . 2016 23 октября (5): 8457-8464. [Медлайн].
Li XD, Wu YP, Wei Y, Chen SH, Zheng QS, Cai H и др. Предикторы восстановления функции почек после пиелопластики у взрослых с обструкцией лоханочно-мочеточникового перехода. Урол Инт . 18 января 2018 г. [Medline].
Ким С., Джейкоб Дж.С., Ким Д.К., Ривера Р., Лим Р.П., Ли В.С. Динамическая МР-урография с временным разрешением и контрастным усилением для оценки перистальтики мочеточника: начальный опыт. Дж. Магнитно-резонансная томография . 2008 28 ноября (5): 1293-8. [Медлайн].
Ritter L, Götz G, Sorge I, Lehnert T., Hirsch FW, Bühligen U, et al. Значение МР-ангиографии в диагностике аберрантных почечных артерий как причины обструкции лоханочно-мочеточникового перехода у детей. Рофо . 2015 Январь 187 (1): 42-48. [Медлайн].
Strother MC, Mucksavage P. Минимально инвазивные методы лечения обструкции UPJ у взрослых. Curr Urol Rep . 2016 май. 17 (5): 39. [Медлайн].
Сорокин И., О’Мэлли Р.Л., МакКэндлесс Б.К., Кауфман Р.П. мл. Успешные результаты роботизированной лапароскопической пиелопластики с использованием однонаправленного шовного материала с зазубринами. Дж Эндоурол . 2016 июн.30 (6): 660-4. [Медлайн].
Jacobs BL, Lai JC, Seelam R, Hanley JM, Wolf JS Jr, Hollenbeck BK и др. Сравнительная эффективность лечения обструкции лоханочно-мочеточникового перехода. Урология . 2017 21 сентября [Medline].
Parente A, Angulo JM, Burgos L, Romero RM, Rivas S, Ortiz R. Чрескожная эндопиелотомия над баллоном высокого давления для рецидивирующей обструкции мочеточниково-лоханочного перехода у детей. Дж Урол . 2015 июл.194 (1): 184-9.[Медлайн].
Gill IS, Desai MM, Kaouk JH, Wani K, Desai MR. Чрескожная эндопиелопластика: описание новой техники. Дж Урол . 2002 Ноябрь 168 (5): 2097-102. [Медлайн].
Shapiro EY, Cho JS, Srinivasan A, Seideman CA, Huckabay CP, Andonian S, et al. Долгосрочное наблюдение после спасительной лапароскопической пиелопластики после неудачной открытой пиелопластики. Урология . 2009 Январь 73 (1): 115-8. [Медлайн].
Сингх В., Синха Р.Дж., Гупта Д.К., Кумар В., Пандей М., Ахтар А.Проспективное рандомизированное сравнение трансперитонеальной лапароскопической пиелопластики и ретроперитонеоскопической пиелопластики при первичной обструкции лоханочно-мочеточникового перехода. ЖСЛС . 2014 18 июля (3): [Medline]. [Полный текст].
Казале П. Роботизированная пиелопластика в педиатрии. Curr Urol Rep . 2009 10 (1): 55-9. [Медлайн].
Казале П. Роботизированная пиелопластика в педиатрии. Curr Opin Urol .2009 января 19 (1): 97-101. [Медлайн].
Tugcu V, Sönmezay E, Ilbey YO, Polat H, Tasci AI. Трансперитонеальная лапароэндоскопическая одноцентровая пиелопластика: первые опыты. Дж Эндоурол . 2010 24 декабря (12): 2023-7. [Медлайн].
Stein RJ, Berger AK, Brandina R и др. Лапароэндоскопическая одноцентровая пиелопластика: сравнение со стандартной лапароскопической техникой. БЖУ Инт . 2011 Март 107 (5): 811-5. [Медлайн].
Seideman CA, Tan YK, Faddegon S, Park SK, Best SL, Cadeddu JA и др.Роботизированная лапароэндоскопическая одноцентровая пиелопластика: техника с использованием роботизированной платформы da Vinci Si. Дж Эндоурол . 2012 26 августа (8): 971-4. [Медлайн].
Исояма Т., Ивамото Х., Иноуэ С., Моризане С., Хината Н., Яо А. и др. Гидронефроз после забрюшинной лапароскопической рассеченной пиелопластики Андерсона-Хайнса у взрослых пациентов с обструкцией лоханочно-мочеточникового перехода: продольный анализ. Cent European J Urol . 2014. 67 (1): 101-5. [Медлайн].
Сепильведа Дж. К., Родо Салас Дж., Манье С., Таррадо Х, Моралес Л. [Эволюция до и послеоперационных ренографических параметров при синдроме обструкции пиелоретерального перехода]. Цир Педиатр . 2004, 17 октября (4): 179-84. [Медлайн].
Molina CA, Facincani I, Muglia VF, Araujo WM, Cassini MF, Tucci S. Jr. Постнатальная оценка внутриутробного гидронефроза из-за обструкции лоханочно-мочеточникового перехода. Бюстгальтеры Acta Cir . 2013. 28 Дополнение 1: 33-6.[Медлайн].
Бэгли DH, Лю JB. Эндоуретральная сонография для определения анатомии обструкции лоханочно-мочеточникового перехода. Урол Клин Норт Ам . 1998 Май. 25 (2): 271-9. [Медлайн].
Баниел Дж., Ливне П.М., Савир А. Расчлененная пиелопластика у детей со стентами и без них. Евро Урол . 1996. 30 (3): 400-2. [Медлайн].
Бартоли Ф, Пенза Р, Ацето Г и др. Фактор роста эпидермиса в моче, хемотаксический белок-1 моноцитов и ß2-микроглобулин у детей с обструкцией лоханочно-мочеточникового перехода. Дж. Педиатр Хирургия . 2011 Март 46 (3): 530-6. [Медлайн].
Boylu U, Oommen M, Lee BR, Thomas R. Обструкция лоханочно-мочеточникового соединения, вторичная по причине пересечения сосудов — транспонировать или нет? Роботизированный опыт. Дж Урол . 2009 Апрель 181 (4): 1751-5. [Медлайн].
Casale P, Grady RW, Joyner BD, Zeltser IS, Figueroa TE, Mitchell ME. Сравнение расчлененной и неразрушенной лапароскопической пиелопластики у педиатрического пациента. Дж Эндоурол . 2004 18 ноября (9): 875-8. [Медлайн].
Чоу Г.К., Гейзингер М.А., Стрим С.Б. Результат эндопиелотомии как функция высокой или зависимой фиксации мочеточника. Урология . 1999 г., 54 (6): 999-1002. [Медлайн].
эль-Нахас АР, Шома AM, Эраки I, эль-Кенави MR, эль-Каппани HA. Проспективное рандомизированное сравнение уретероскопической эндопиелотомии с использованием гольмиевого: YAG-лазера и баллонного катетера. Дж Урол .2006 февраль 175 (2): 614-8; обсуждение 618. [Medline].
Эль-Щербины М.Т., Муса О.М., Шокейр А.А., Гонейм М.А. Роль концентрации трансформирующего фактора роста-бета1 в моче в диагностике обструкции верхних мочевых путей у детей. Дж Урол . 2002, октябрь 168 (4, часть 2): 1798-800. [Медлайн].
Figenshau RS, Clayman RV. Эндоурологические варианты лечения обструкции лоханочно-мочеточникового перехода у педиатрических пациентов. Урол Клин Норт Ам .1998 Май. 25 (2): 199-209. [Медлайн].
Frauscher F, Janetschek G, Helweg G. Пересечение сосудов в лоханочно-мочеточниковом переходе: обнаружение с помощью цветного допплеровского изображения с контрастным усилением. Радиология . 1999 Mar.210 (3): 727-31. [Медлайн].
Джаббур ME, Goldfischer ER, Klima WJ. Эндопиелотомия после неудачной пиелопластики: отдаленные результаты. Дж Урол . 1998 сентябрь 160 (3 Pt 1): 690-2; обсуждение 692-3. [Медлайн].
Джонстон Дж. Х., Эванс Дж. П., Глассберг К. И..Гидронефроз таза у детей: обзор 219 личных случаев. Дж Урол . 1977, январь, 117 (1): 97-101. [Медлайн].
Kajbafzadeh AM, Elmi A, Talab SS, Emami H, Esfahani SA, Saeedi P. Углеводный антиген 19-9 в моче и сыворотке как биомаркер обструкции лоханочно-мочеточникового перехода у детей. Дж Урол . 2010 июн. 183 (6): 2353-60. [Медлайн].
Кумар Р., Капур Р., Мандхани А. Оптимальная продолжительность наложения шин после эндопиелотомии. Дж Эндоурол . 1999 марта, 13 (2): 89-92. [Медлайн].
Lee RS, Retik AB, Borer JG, Peters CA. Педиатрический робот ассистировал лапароскопической расчлененной пиелопластике: сравнение с группой открытых хирургических вмешательств. Дж Урол . 2006 февраль 175 (2): 683-7; Обсуждение 687. [Медлайн].
Lopez-Pujals A, Leveillee RJ, Wong C. Применение строгих радиологических критериев для определения успеха лапароскопической пиелопластики. Дж Эндоурол .2004 18 октября (8): 756-60. [Медлайн].
Matlaga BR, Shah OD, Singh D, Streem SB, Assimos DG. Уретерокалиостомия: современный опыт. Урология . 2005 января 65 (1): 42-4. [Медлайн].
МакДэниел ББ, Джонс Р.А., Шерц Х., Кирш А.Дж., Литтл С.Б., Граттан-Смит Дж. Д.. Динамическая МР-урография с контрастным усилением в оценке гидронефроза у детей: Часть 2, анатомическая и функциональная оценка обструкции лоханочно-маточного перехода. AJR Am J Roentgenol . 2005 декабрь 185 (6): 1608-14. [Медлайн].
Mitterberger M, Pinggera GM, Neururer R, Peschel R, Colleselli D, Aigner F, et al. Сравнение контрастного цветного допплера (CDI), компьютерной томографии (CT) и магнитно-резонансной томографии (MRI) для обнаружения пересекающихся сосудов у пациентов с обструкцией лоханочно-мочеточникового соединения (UPJO). Евро Урол . 2008 июнь 53 (6): 1254-60. [Медлайн].
Муракумо М., Нономура К., Ямасита Т., Ушики Т., Абэ К., Коянаги Т.Структурные изменения компонентов коллагена и уменьшение нервов при врожденной обструкции лоханочно-мочеточникового перехода. Дж Урол . 1997 Май. 157 (5): 1963-8. [Медлайн].
Niemczyk P, Krisch EB, Zeiger L. Использование диуретической ренограммы при оценке состояния пациентов до и после эндопиелотомии. Урология . 1999 Февраль 53 (2): 271-5. [Медлайн].
Park JM, Bloom DA. Патофизиология обструкции UPJ. Текущие концепции. Урол Клин Норт Ам .1998 Май. 25 (2): 161-9. [Медлайн].
Patel V. Роботизированная лапароскопическая рассеченная пиелопластика. Урология . 2005 июл.66 (1): 45-9. [Медлайн].
Редди П.П., Манделл Дж. Пренатальная диагностика. Терапевтическое значение. Урол Клин Норт Ам . 1998 Май. 25 (2): 171-80. [Медлайн].
Richstone L, Seideman CA, Reggio E, Bluebond-Langner R, Pinto PA, Trock B и др. Патологические данные у пациентов с обструкцией лоханочно-мочеточникового перехода и перекрещивающимися сосудами. Урология . 2 февраля 2009 г. [Medline].
Грачи VJ, Лебовиц Р.Л. Внешняя обструкция лоханочно-мочеточникового перехода от пересекающего почечного сосуда: демография и изображения. Педиатр Радиол . 2001, 31 февраля (2): 120-4. [Медлайн].
Shalhav AL, Giusti G, Elbahnasy AM. Эндопиелотомия у взрослых: влияние этиологии и антеградного и ретроградного подходов на исход. Дж Урол . 1998 сентябрь 160 (3, часть 1): 685-9. [Медлайн].
Сиддик FM, Левелли Р.Дж., Вилликана П., Берд В.Г.Компьютерная лапароскопическая пиелопластика: опыт Университета Майами с хирургической системой daVinci. Дж Эндоурол . 2005 апреля 19 (3): 387-92. [Медлайн].
Smith AD, Horgan JD. Эндопиелотомия и пиелопластика. Клиническая урология . Филадельфия, Пенсильвания: Дж. Б. Липпинкотт; 1994. 433-43.
Томас Д.Ф. Уропатия плода. Бр Дж Урол . 1990 Сентябрь 66 (3): 225-31. [Медлайн].
Ван Й, Пури П., Хассан Дж., Миякита Х., Рин Ди-джей.Аномальная иннервация и измененный фактор роста нервов являются посредниками в экспрессии рибонуклеиновой кислоты при обструкции лоханочно-мочеточникового перехода. Дж Урол . 1995, август, 154 (2, часть 2): 679-83. [Медлайн].
Юрканин JP, Fuchs GJ. Лапароскопическая расчлененная пиелоуретеропластика: трехлетний опыт работы в одном учреждении. Дж Эндоурол . 2004, 18 октября (8): 765-9. [Медлайн].
Mizuno K, Kojima Y, Kurokawa S, Kamisawa H, Nishio H, Moritoki Y, et al.Роботизированная лапароскопическая пиелопластика при обструкции лоханочно-мочеточникового перехода: сравнение педиатрических и взрослых пациентов — японская серия. J Робот Surg . 2017 июн.11 (2): 151-157. [Медлайн].
% PDF-1.3 % 138 0 объект > эндобдж xref 138 91 0000000016 00000 н. 0000002171 00000 п. 0000002366 00000 н. 0000002997 00000 н. 0000003348 00000 п. 0000003414 00000 н. 0000003660 00000 н. 0000003768 00000 н. 0000003857 00000 н. 0000003917 00000 н. 0000004022 00000 н. 0000004082 00000 н. 0000004186 00000 п. 0000004246 00000 н. 0000004347 00000 п. 0000004407 00000 н. 0000004523 00000 н. 0000004582 00000 н. 0000004697 00000 н. 0000004756 00000 н. 0000004871 00000 н. 0000004986 00000 н. 0000005100 00000 н. 0000005215 00000 н. 0000005330 00000 н. 0000005445 00000 н. 0000005560 00000 н. 0000005675 00000 н. 0000005790 00000 н. 0000005905 00000 н. 0000006020 00000 н. 0000006135 00000 н. 0000006248 00000 н. 0000006553 00000 н. 0000007047 00000 н. 0000007619 00000 н. 0000014206 00000 п. 0000014533 00000 п. 0000014926 00000 п. 0000017900 00000 п. 0000018179 00000 п. 0000018239 00000 п. 0000019430 00000 п. 0000019702 00000 п. 0000019834 00000 п. 0000020050 00000 н. 0000020545 00000 п. 0000020586 00000 п. 0000020608 00000 п. 0000021059 00000 п. 0000021440 00000 п. 0000025940 00000 п. 0000026286 00000 п. 0000027179 00000 п. 0000027201 00000 п. 0000028611 00000 п. 0000028752 00000 п. 0000029033 00000 п. 0000031080 00000 п. 0000031335 00000 п. 0000031649 00000 п. 0000031875 00000 п. 0000032055 00000 п. 0000032794 00000 п. 0000032816 00000 п. 0000033793 00000 п. 0000033815 00000 п. 0000034724 00000 п. 0000034746 00000 п. 0000034962 00000 п. 0000035132 00000 п. 0000035199 00000 п. 0000036132 00000 п. 0000037064 00000 п. 0000037086 00000 п. 0000037312 00000 п. 0000037489 00000 п. 0000037563 00000 п. 0000037862 00000 п. 0000038727 00000 п. 0000038749 00000 п. 0000039655 00000 п. 0000039677 00000 п. 0000039784 00000 п. 0000039861 00000 п. 0000040147 00000 п. 0000042822 00000 н. 0000043580 00000 п. 0000049575 00000 п. 0000002407 00000 н. 0000002975 00000 н. трейлер ] >> startxref 0 %% EOF 139 0 объект > эндобдж 140 0 объект > эндобдж 227 0 объект > поток Hb«f`Lg`g` * bb @
% PDF-1.3 % 151 0 объект > эндобдж xref 71 81 0000002090 00000 н. 0000002874 00000 н. 0000003255 00000 н. 0000003548 00000 н. 0000004340 00000 н. 0000004664 00000 н. 0000007169 00000 н. 0000007961 00000 п. 0000008330 00000 н. 0000011955 00000 п. 0000012806 00000 п. 0000013251 00000 п. 0000019500 00000 н. 0000020357 00000 п. 0000020872 00000 п. 0000027419 00000 н. 0000028204 00000 п. 0000028452 00000 п. 0000029532 00000 п. 0000030331 00000 п. 0000030583 00000 п. 0000031041 00000 п. 0000031834 00000 п. 0000032100 00000 н. 0000033135 00000 п. 0000033927 00000 п. 0000034335 00000 п. 0000038113 00000 п. 0000038964 00000 п. 0000039453 00000 п. 0000044811 00000 п. 0000045611 00000 п. 0000045867 00000 п. 0000046355 00000 п. 0000046557 00000 п. 0000046653 00000 п. 0000046915 00000 п. 0000047429 00000 п. 0000053767 00000 п. 0000053836 00000 п. 0000053878 00000 п. 0000056566 00000 п. 0000057330 00000 п. 0000058028 00000 п. 0000058659 00000 п. 0000059284 00000 п. 0000060012 00000 п. 0000060734 00000 п. 0000061451 00000 п. 0000062012 00000 н. 0000062129 00000 п. 0000062246 00000 п. 0000062363 00000 п. 0000062460 00000 п. 0000062523 00000 п. 0000062621 00000 п. 0000062718 00000 п. 0000062815 00000 п. 0000062911 00000 п. 0000063008 00000 п. 0000063104 00000 п. 0000063201 00000 п. 0000063298 00000 п. 0000063395 00000 п. 0000063491 00000 п. 0000063587 00000 п. 0000063683 00000 п. 0000063778 00000 п. 0000063875 00000 п. 0000063971 00000 п. 0000064629 00000 н. 0000064685 00000 п. 0000065266 00000 п. 0000065334 00000 п. 0000065574 00000 п. 0000065691 00000 п. 0000065811 00000 п. 0000065931 00000 п. 0000066055 00000 п. 0000002301 00000 п. 0000000017 00000 н. трейлер ] >> startxref 0 %% EOF 71 0 объект > эндобдж 150 0 объект > поток xc«a` A 00130pL (P`x`
Сравнение эффективности и безопасности забрюшинной лапароскопии
1 Отделение хирургии мочевыводящих путей, Больница филиала Медицинского университета Сюйчжоу, 2 Клинический колледж, Медицинский университет Сюйчжоу, Сюйчжоу, Народная Республика Китай
Цель: Целью данного исследования было сравнение клинической эффективности и безопасности забрюшинной лапароскопической и открытой хирургии для коррекции ретрокавального мочеточника.
Пациенты и методы: Ретроспективно проанализированы клинические данные 14 пациентов с ретрокавальным мочеточником. Из них девяти пациентам была проведена открытая хирургическая терапия, а пяти — забрюшинная лапароскопическая хирургия. Мочеточник был перемещен в нормальное анатомическое положение с последующим лапароскопическим интракорпоральным уретеро-мочеточниковым анастомозом.
Результат: Открытые операции успешно выполнены в девяти случаях. Среднее время операции 95,6 ± 22,0 мин, кровопотеря 108.6 ± 34,5 мл. Среднее время госпитализации составило 14,8 ± 1,1 дня, время восстановления — 52,8 ± 1,3 дня. Забрюшинная лапароскопическая операция была успешно выполнена в пяти случаях без преобразования в открытую операцию и без тяжелых периоперационных осложнений. Среднее время операции составило 112,0 ± 42,1 мин, кровопотеря — 45,3 ± 15,1 мл. Среднее время госпитализации составило 7,3 ± 1,9 дня, время восстановления — 23,6 ± 2,4 дня. Послеоперационное подтекание мочи произошло у одного пациента. У пациентов, перенесших забрюшинную лапароскопическую операцию, послеоперационного стеноза мочеточника не было.
Заключение: Забрюшинная лапароскопическая пластика мочеточника у пациентов с ретрокавальным мочеточником безопасна и эффективна с меньшими травмами и более быстрым восстановлением и может быть использована в качестве первого выбора для лечения ретрокавального мочеточника.
Введение
Заболеваемость ретрокавальными мочеточниками составляет приблизительно 1: 1000 в общей популяции, причем у мужчин преобладает от трех до четырех раз. Ретрокавальный мочеточник обычно протекает бессимптомно до третьего или четвертого десятилетия жизни.Однако Sun et al. -1 ретроспективно проанализировали клинические данные восьми пациентов с ретрокавальным мочеточником и обнаружили, что средний возраст пациентов составлял 9,2 года (диапазон 2–13 лет). Состояние чаще всего правостороннее с левосторонним поражением, которое чаще всего связано с обратным сидением или дупликацией полой полости. Наличие ретрокавального мочеточника с левой стороны — очень редкая находка и имеет важное клиническое и хирургическое значение. Если субкардинальная вена сохраняется в системе левой полой вены, встречается левая преуретеральная полая вена.Kozyrakis et al., , 2, сообщили о случае левого ретрокавального мочеточника, связанного с уротелиальным злокачественным новообразованием, без situs inversus.
Сообщалось о различных методах лечения ретрокавального мочеточника, включая открытую хирургию, ретроперитонеоскопическую хирургию и чисто роботизированную ретрокавальную пластику мочеточника. Открытая хирургия является традиционным лечением и обычно бывает успешным; тем не менее, это требует длинного разреза кожи и вызывает значительную послеоперационную боль с длительным периодом выздоровления.В последнее время лапароскопия стала стандартным методом для многих урологических процедур. С мая 2001 г. по октябрь 2014 г. мы использовали открытую операцию и забрюшинную лапароскопическую операцию для лечения 14 случаев ретрокавального мочеточника в нашей больнице. Мы сравнили эффективность и безопасность забрюшинной лапароскопической и открытой хирургии для коррекции ретрокавального мочеточника.
Пациенты и методы
Субъекты
С мая 2001 г. по октябрь 2014 г. было зарегистрировано 14 пациентов с ретрокавальным мочеточником, в том числе 11 мужчин и 3 женщины.Возраст составлял от 17 до 40 лет, а средний возраст составлял 33,0 года. Течение болезни составило от 1 до 24 месяцев. Основное клиническое проявление включало 13 случаев повторяющейся боли при люмбаго справа, один случай мочекаменной болезни и три случая перемежающейся гематурии. Гидронефроз был обнаружен в четырех случаях при физикальном обследовании. Всем пациентам не проводилось хирургическое лечение правой почки или мочеточника. Это исследование было одобрено этическим комитетом больницы-филиала Медицинского колледжа Сюйчжоу, и все пациенты дали информированное согласие.
Методы диагностики
Все 14 пациентов были обследованы с помощью В-ультразвука, рентгенограммы брюшной полости и внутривенной пиелографии. Среди них девять были ретроградной пиелографией, пять были многослойной компьютерной томографией (КТ) урографией с трехмерным (3D) дисплеем. В-ультразвуковое исследование показало, что все 14 случаев имели разную степень расширения правой чашечки почки, лоханки и верхнего мочеточника. Внутривенная урография (ВВУ) показала, что девять случаев были умеренным гидронефрозом, а четыре случая — тяжелым гидронефрозом.Визуализирующее обследование показало, что правый мочеточник смещен до средней линии перед третьим-четвертым поясничными отделами и был окольным, как типичный тип «S» или «J». Он прошел по средней линии после полой вены, а затем переместился через переднюю часть нижней полой вены (НПВ). Типичная особенность смещения ретрокавального мочеточника показана на рисунке 1.
Рисунок 1 CTU выявил гидронефроз и дилатацию правого проксимального отдела мочеточника. |
Открытая хирургия
Открытая операция выполнена девяти больным. После общей анестезии отрезок мочеточника был выше 1 см в точке поворота верхнего мочеточника (ближайший участок обструкции), а ретрокавальный мочеточник был перемещен к латеральной части полой вены. В случае отсутствия натяжения анастомоз конец в конец выполнялся рассасывающейся нитью 5-0 после установки двойной J-образной трубки.Операционную область промыли и проверили на отсутствие кровотечения, в забрюшинное пространство поместили дренажную трубку, а двойную J-трубку удалили с помощью цистоскопа через 1 месяц.
Забрюшинная лапароскопическая хирургия
Забрюшинная лапароскопическая операция выполнена 5 пациентам. После общей анестезии на коже делали небольшие разрезы под 12-м реберным краем задней подмышечной линии, на 12-м реберном кончике передней подмышечной линии и на два пальца выше гребня подвздошной кости средне-подмышечной линии, прокалывали 10-миллиметровую оболочку (рис. 2), визуальный ретроперитонеальный расширитель вводили в забрюшинное пространство и расширяли для расширения операционного пространства в течение 5 минут, затем создавали искусственный пневмоперитонеум путем заполнения CO 2 , и давление было между 1.33 и 2,0 кПа. Лапароскоп вводили в точку прокола гребня подвздошной кости; рассечена периренальная фасция и жировая капсула; обнажены почечная лоханка и верхний мочеточник; мочеточник и НПВ освобождены; анатомическое соотношение было определено, а затем были освобождены нижний мочеточник и ретрокавальный мочеточник. Перерезана дистальная часть расширенной почечной лоханки. Мочеточник был отделен от НПВ и перемещен передне-латерально к ней. Переднюю стенку мочеточника периодически зашивали рассасывающейся нитью 5-0, при лапароскопии вводили двойную J-образную трубку, а затем непрерывно зашивали противоположную сторону (рис. 3).
Рис. 2 Размещение порта при забрюшинной лапароскопической хирургии в нашем центре. |
Рисунок 3 Процедуры забрюшинной лапароскопии. |
Результаты
Открытая хирургия
Открытая операция была успешно проведена в девяти случаях, средняя продолжительность операции составила 95,6 ± 22,0 мин (диапазон 60–130 мин). Средняя кровопотеря во время операции составила 106,7 ± 32,2 мл (диапазон 50–160 мин).Среднее время госпитализации составило 15,3 ± 1,2 дня (диапазон 14-17 дней), а время выздоровления — 52,8 ± 1,3 дня (диапазон 45-56 дней). Послеоперационное наблюдение составило от 5 месяцев до 3 лет (в среднем 14 месяцев). Симптомы исчезли, гидронефроз исчез или уменьшился, послеоперационных осложнений не было.
Забрюшинная лапароскопическая хирургия
Забрюшинная лапароскопическая операция успешно выполнена в пяти случаях без преобразования в открытую операцию. Среднее время операции 112.0 ± 42,1 мин (диапазон 70–180 мин), а кровопотеря во время операции составила 50,0 ± 17,0 мл (диапазон 30–70 мин). Среднее время госпитализации составило 7,4 ± 1,1 дня (диапазон 6–9 дней), а время восстановления — 23,6 ± 2,4 дня (диапазон 16–32 дня). Послеоперационное наблюдение составило от 6 месяцев до 2 лет (в среднем 11 месяцев). Послеоперационное обследование с помощью В-ультразвука показало, что гидронефроз и расширение верхней части мочеточника были значительно уменьшены, а послеоперационного стеноза стомы или других осложнений не было (Таблица 1).
Таблица 1 Клинические данные пациентов |
Обсуждение
Ретрокавальный мочеточник — это редкая эмбриологическая венозная мальформация, приводящая к дорсальному смещению мочеточника в каудальную полую вену. Описаны два типа ретрокавального мочеточника: тип I (низкая петля; 90% случаев) приводит к появлению «рыболовного крючка» или формы «s» среднего сегмента мочеточника, где у 50% развивается гидронефроз, и тип II (высокая петля). мочеточник пересекает полую часть в области лоханочно-мочеточникового соединения (UPJ), что приводит к минимальной дилатации или ее отсутствию.Изолированный левый ретрокавальный мочеточник с единственной левосторонней НПВ встречается очень редко, и только четыре случая описаны в литературе. Thirugnanasambandam et al. 3 сообщили о случае изолированного левого ретрокавального мочеточника с единственной левой нижней полой вене без обратного сидения.
Открытая операция — это классическое лечение ретрокавального мочеточника, но оно требует большого разреза кожи и вызывает значительную послеоперационную боль с длительным периодом выздоровления. Следовательно, минимально инвазивное хирургическое лечение стало методом выбора для ретрокавального мочеточника.Лапароскопия в настоящее время является основной процедурой для лечения многих урологических заболеваний. Варианты описанных лапароскопических методов включают трансперитонеальную лапароскопическую пластику, забрюшинную лапароскопическую пластику и однопортовую лапароскопическую пластику, и каждый из них имеет свои преимущества и ограничения.
Многие хирурги предпочитают трансперитонеальный доступ из-за большего рабочего пространства и лучшей ориентации благодаря знакомым анатомическим ориентирам. El Harrech et al. –4– описали опыт трех случаев трансперитонеальной лапароскопической пиелопиелостомии ретрокавального мочеточника без иссечения ретрокавального сегмента.Ding et al. 5 выполнили трансперитонеальную лапароскопическую пиелопиелостомию или уретероуретеростомию у девяти пациентов с ретрокавальным мочеточником.
Забрюшинный доступ обеспечивает прямой доступ к почке и не требует мобилизации кишечника и других органов вокруг почки и мочеточника, что, возможно, снижает частоту осложнений. Mugiya et al., , 6, , представили первый отчет о ретроперитонеоскопическом интракорпоральном анастомозе мочеточника с использованием автоматического шовного устройства для коррекции ретрокавального мочеточника, при котором время операции было сокращено.Недавно Liu et al. 7 сообщили об опыте ретроперитонеальной лапароскопической пластики мочеточника в девяти случаях ретрокавального мочеточника и предложили его в качестве лечения первой линии ретрокавального мочеточника из-за его преимуществ, заключающихся в минимальной инвазии и более коротком пребывании в больнице. Искусный лапароскопический анастомоз с забрюшинным доступом может сократить продолжительность операции.
Лапароскопическая реконструкция мочеточника зависит от нескольких портов. В последнее время для улучшения косметических результатов и дальнейшего снижения заболеваемости использовалась лапароэндоскопическая хирургия на одном участке (LESS).Abdel-Karim et al., , 8, описали случай женщины с патологическим ожирением и ретрокавальным мочеточником, получавшей LESS. Kumar et al. 9 выполнили многопортовую лапароэндоскопию с одним разрезом для восстановления ретрокавального мочеточника, используя технику фиксации мочеточника прихватками, разработанную Институтом последипломного образования Сантоша (PGI), которая позволяет легко и быстро наложить шов с помощью обычных лапароскопических инструментов. Кроме того, Chen et al. 10 описали случай ретрокавального мочеточника, связанного с камнем мочеточника, который лечили с помощью забрюшинной уретеролитотомии LESS и уретероуретеростомии.Аналогичным образом, Kang et al. –11– выполнили пиелопиелостомию LESS для ретрокавального мочеточника у четырех пациентов. Однопортовое устройство было изготовлено с хирургической перчаткой и катетером Фолея и позволило ввести три троакара. Однако Rebouças et al. 12 описали случай ретрокавального мочеточника, обработанного LESS без использования каких-либо специальных устройств, таких как однопортовые или изогнутые инструменты. В целом, LESS может представлять собой возможный новый вариант лечения ретрокавального мочеточника.
Хотя такие симптомы, как почечная колика, устойчивая гематурия или прогрессирование гидроуретеронефроза, могут указывать на необходимость раннего хирургического вмешательства, функционально беспрепятственные и бессимптомные ретрокавальные мочеточники, которые показывают гидронефроз на анатомической визуализации, могут не требовать немедленного хирургического вмешательства.Yen et al. -13 предположили, что немедленное хирургическое вмешательство не всегда необходимо, поскольку они сообщили о консервативном лечении двух случаев ретрокавального мочеточника со значительным проксимальным гидроуретеронефрозом.
В данном исследовании мы выполнили ретроперитонеоскопическую пластику мочеточника в пяти случаях ретрокавального мочеточника. Мы обобщили наш опыт следующим образом: 1) сохранение ретрокавального сегмента облегчило восстановление и сократило время операции с хорошим исходом и без симптомов.2) Двойной J-стент был введен антеградно лапароскопически. Стент удален через 4–6 недель после операции. 3) Мочеточник был рассечен всего на 1 см выше ретропавеломного сегмента, чтобы избежать стеноза анастомоза. Переднюю стенку мочеточника зашивали прерывисто, а затем непрерывно зашивали противоположную сторону, чтобы уменьшить инфильтрацию мочи.
У нашего исследования есть несколько ограничений. Во-первых, размер выборки невелик. Мы набрали всего 14 пациентов. Во-вторых, наблюдение непродолжительное, всего 2 года.Дальнейшие исследования с большим размером выборки и длительным периодом наблюдения помогут подтвердить наш вывод.
Заключение
Забрюшинная лапароскопическая пластика мочеточника — безопасная, эффективная и минимально инвазивная хирургическая альтернатива лечению ретрокавального мочеточника и может быть использована в качестве первого выбора для лечения ретрокавального мочеточника.
Благодарность
Это исследование было поддержано грантами Китайского научного фонда провинции Цзянсу (№ BK2007032), проекта «Укрепление здравоохранения с помощью науки, технологий и образования» и таланта молодых врачей провинции Цзянсу.
Раскрытие информации
Авторы сообщают об отсутствии конфликта интересов в этой работе.
Список литературы
1. | Sun JS, Zhang G, Lin T. Ретрокавальный мочеточник у детей: сообщение о восьми случаях. Вест-Индская медицина J . 2015; 64 (4): 397–399. | |
2. | Козыракис Д., Промбонас I, Кирикос В., Григоракис А., Плиотас Г., Маловроувас Д. Левый ретрокавальный мочеточник, связанный с уротелиальным злокачественным новообразованием: представление редкого случая. Урол Дж . 2012. 9 (2): 527–529. | |
3. | Thirugnanasambandam V, Nayak P, Mossadeq A. Левый ретрокавальный мочеточник без задней задней поверхности или дупликации нижней венакавы. Индийский Дж. Урол . 2015. 31 (4): 372–373. | |
4. | El Harrech Y, Ghoundale O, Kasmaoui EH, Touiti D. Трансперитонеальная лапароскопическая пиелостомия ретрокавального мочеточника без иссечения ретрокавального сегмента: опыт трех случаев. Адв. Урол . 2016; 2016: 5709134. | |
5. | Ding GQ, Xu LW, Li XD и др. Чистая трансперитонеальная лапароскопическая коррекция ретрокавального мочеточника. Chin Med J (англ.) . 2012. 125 (13): 2382–2385. | |
6. | Mugiya S, Suzuki K, Ohhira T, Un-No T, Takayama T, Fujita K. Ретроперитонеоскопическое лечение ретрокавального мочеточника. Int J Urol . 1999. 6 (8): 419–422. | |
7. | Лю Э, Сунь Х, Гуо Х и др. Ретроперитонеоскопическая пластика мочеточника ретрокавального мочеточника: отчет о девяти случаях и обзор литературы. Сканд Дж. Урол . 2016; 50 (4): 319–322. | |
8. | Абдель-Карим А.М., Яхия Э., Хассуна М., Миссири М. Лапароскопическая операция на одном участке для восстановления ретрокавального мочеточника у пациента с патологическим ожирением. Urol Case Rep .2015; 4: 61–63. | |
9. | Kumar S, Shankaregowda SA, Devana SK, Jain S, Singh SK. Многопортовая лапароэндоскопическая техника с одним разрезом для восстановления ретрокавального мочеточника с использованием мочеточниковой фиксации Santosh PGI. Азиатская J Endosc Surg . 2014. 7 (4): 337–341. | |
10. | Chen Z, Chen X, Luo YC и др. Забрюшинная лапароэндоскопическая одноцентровая уретеролитотомия и уретероуретеростомия по поводу ретрокавального мочеточника с камнем мочеточника: отчет о первом клиническом случае. Сканд Дж Урол Нефрол . 2012. 46 (6): 437–440. | |
11. | Канг Н., Чжан Дж. Х., Ню Ю. Н. и др. Забрюшинная лапароэндоскопическая хирургия в одном месте для лечения ретрокавального мочеточника. Мир Дж. Урол . 2013. 31 (1): 205–211. | |
12. | Ребусас РБ, Монтейро Р.К., Медейрос П.Ф. младший и др. Лапароэндоскопическая пластика ретрокавального мочеточника на одном участке без использования специальных приспособлений. Инт Браз Дж Урол . 2013. 39 (1): 141–142. | |
13. | Yen JM, Lee LS, Cheng CW. Консервативное лечение ретрокавального мочеточника: серия клинических случаев. Int J Surg Case Rep . 2015; 15: 93–95. |
V04-12: Лапароскопическая замена левого мочеточника с использованием отростка слепой кишки после ректосигмоидэктомии en-bloc
V04-12: Лапароскопическая замена левого мочеточника с использованием отростка слепой кишки после ректосигмоидэктомии en-bloc 9009: отчет о клиническом случае и видеодемонстрация
Видео
ВВЕДЕНИЕ
Иногда местнораспространенные опухоли малого таза требуют блочной резекции, потому что они вторгаются в соседние органы, такие как мочеточник 1.Лечение отдела мочеточника выше уровня подвздошных сосудов сопряжено с высокой степенью сложности и представляет собой проблему для хирурга 2, 3. Существует несколько вариантов реконструкции мочеточника, таких как реимплантат, лоскут Боари и поясничная сцепка 4. Менее распространенным вариантом является использование трансплантата слепой кишки на ножке, который можно использовать в качестве канала между мочевым пузырем и мочеточником 5,6,7 . Принятие этой техники на правой стороне полезно из-за анатомической близости, однако использование на левой стороне более проблематично, особенно при лапароскопическом выполнении.Цель этого видеофорума — продемонстрировать возможность лапароскопической реконструкции левой мочевыделительной системы с использованием аутотрансплантата нативного отростка во время блочного иссечения мочеточника, вызванного удалением местнораспространенной аденокарциномы верхнего отдела прямой кишки.
МЕТОДЫ
Пациент 69 лет с опухолью сигмовидной кишки, диагностированной на расстоянии 13 см от анального края и занимающей 90% просвета толстой кишки. Пациенту выполнена блочная лапароскопическая ректосигмоидэктомия опухоли с инвазией левого мочеточника над подвздошными сосудами.Левая стенка мочевого пузыря также продемонстрировала прямую инвазию опухоли. Операция была завершена лапароскопически, и была выполнена первичная сквозная колопроктостомия с использованием техники двойного скрепления скобами. Следующие шаги показаны на дополнительном видеофоруме. В частности, мочевыводящие пути были реконструированы с использованием транспозиции аппендикса, используемого в качестве канала для преодоления разрыва между разделенным сегментом левого мочеточника и мочевым пузырем.
РЕЗУЛЬТАТЫ
Несмотря на техническую сложность, лапароскопическая реимплантация была успешно выполнена.Операция без интраоперационных осложнений. Время операции составило 310 минут, неблагоприятных последствий не было, а через 12 месяцев послеоперационное сканирование почек показало сохранение функции мочеиспускания.
ЗАКЛЮЧЕНИЕ
Это видео демонстрирует, что лапароскопическое использование слепой кишки при реконструкции левого мочеточника является возможным вариантом, и для подтверждения эффективности этого подхода необходимо более длительное наблюдение с дополнительными пациентами.
Финансирование: 1. Р. Ландманн, М.Weiser Хирургическое лечение местнораспространенного и местно-рецидивирующего рака толстой кишки, Clin Colon Rectal Surg. Авг; 18 (3): 182–189. DOI: 10.1055 / s-2005-916279 2. Санкт-Лезин М.А., Столлер М.Л. Хирургические травмы мочеточника. Урология 1991; 38: 497–506. 3. Франк Н. Беркс, Ричард А. Сантуччи, Лечение ятрогенного повреждения мочеточника, Ther Adv Urol. 2014 июн; 6 (3): 115–124. DOI: 10.1177 / 1756287214526767 4. Андерсен П., Андерсен Л. М. и Иверсен Л. Х. Ятрогенное повреждение мочеточника при хирургии колоректального рака: общенациональное исследование, сравнивающее лапароскопический и открытый доступы Surg Endosc (2015) 29: 1406.DOI: 10.1007 / s00464-014-3814-1 5.

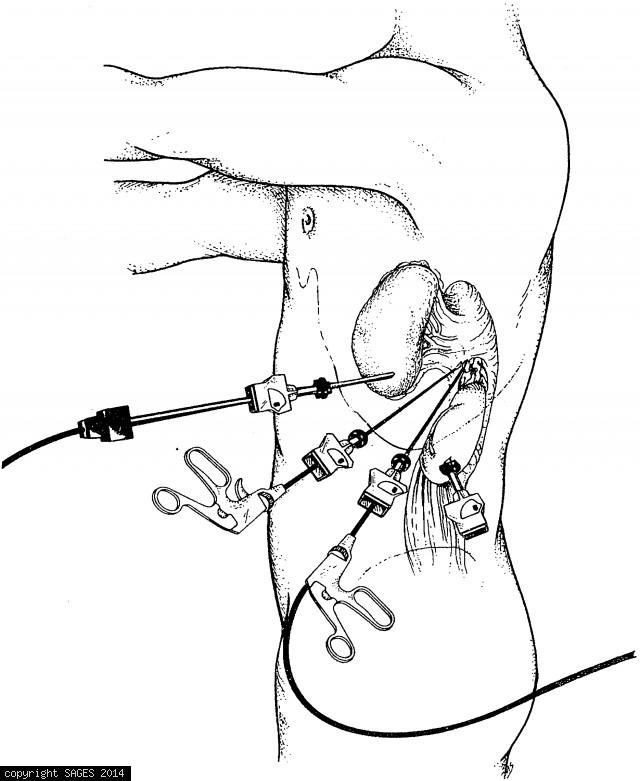 Малая Конюшенная, д. 8А
Малая Конюшенная, д. 8А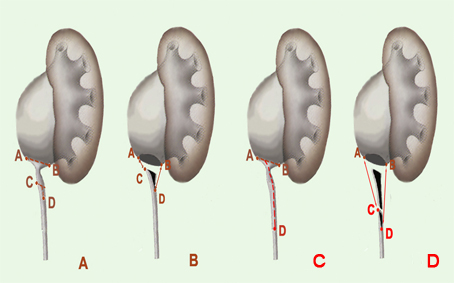
 47
47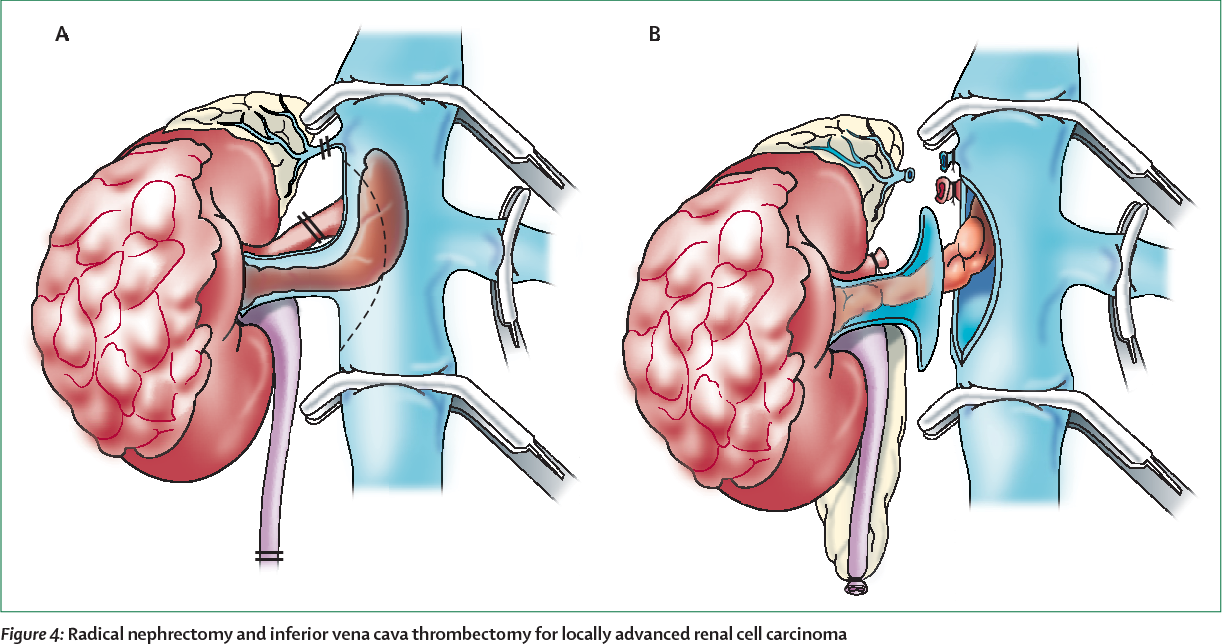 Академика Лебедева, д. 4/2
Академика Лебедева, д. 4/2 3
3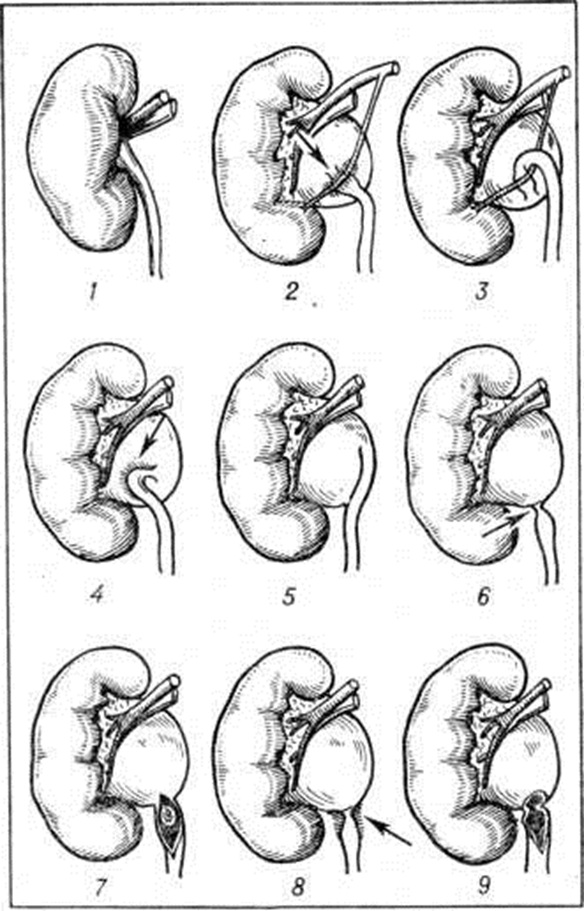 45-49
45-49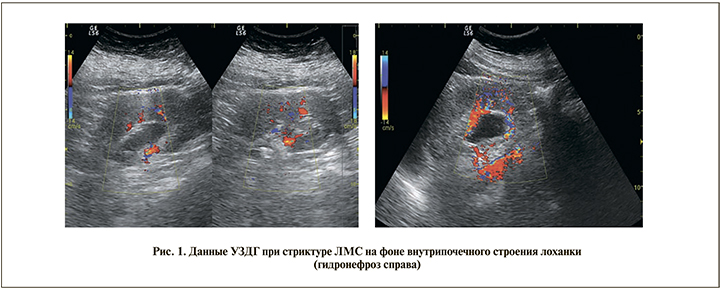
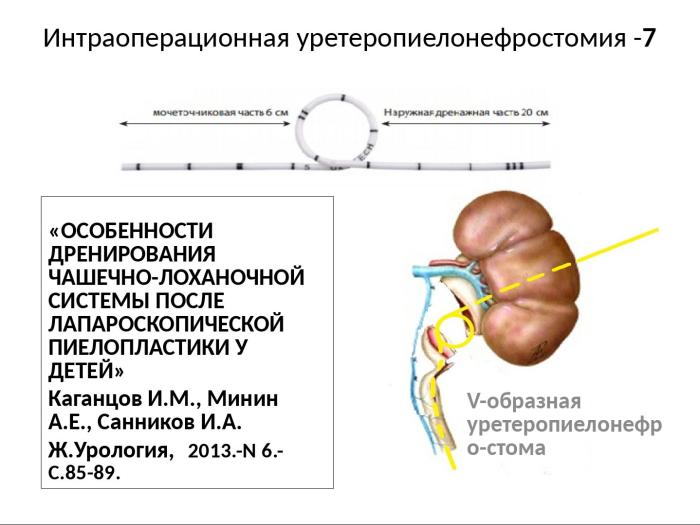
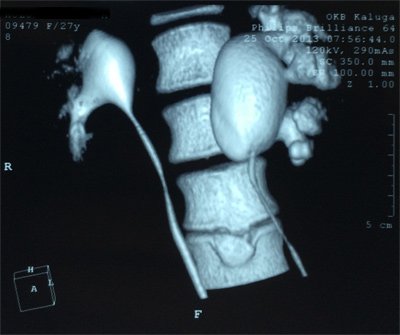
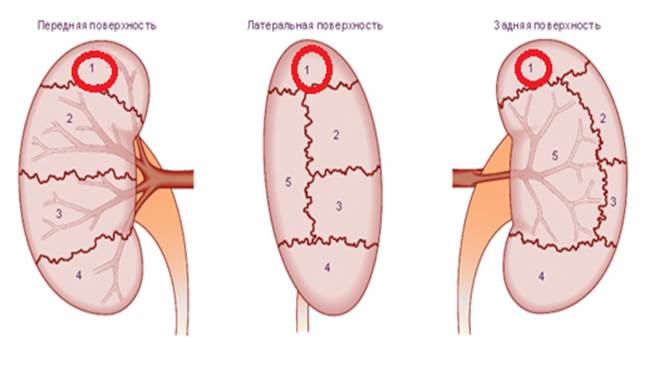
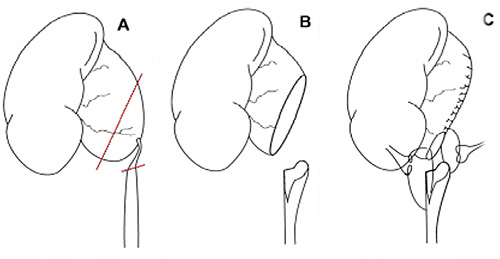
 2-4
2-4 56
56 Литовская, д. 2
Литовская, д. 2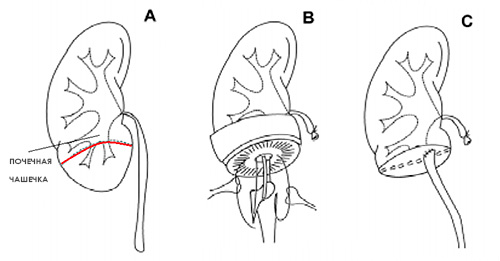 2
2 1
1 Колпино, ул. Павловская, д. 16А
Колпино, ул. Павловская, д. 16А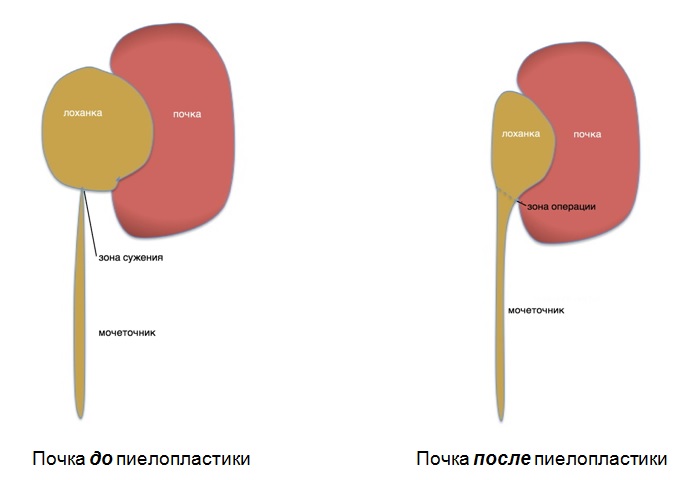 Сосновый Бор (Ленинградская область), Больничный городок, д. 3/13
Сосновый Бор (Ленинградская область), Больничный городок, д. 3/13