Лечение народными средствами канцероматоз брюшины: Вопрос врачу
Народное лечение канцероматоза брюшной полости
Доброе время суток! Меня зовут Халисат Сулейманова — я фитотерапевт. В 28 лет себя вылечила от рака матки травами (больше про мой опыт выздоровления и почему я стала фитотерапевтом читайте здесь: Моя история). Перед тем как лечиться по народным методам описанным в интернете, просьба, консультируйтесь со специалистом и лечащим врачом! Это сэкономит ваше время и деньги, поскольку заболевания разные, травы и методы лечения разные, а есть еще сопутствующие заболевания, противопоказания, осложнения и так далее. Пока добавить нечего, но если Вам нужна помощь в подборе трав и методик лечения, можете меня найти вот по контактам:
Халисат Сулейманова
Страничка Instagram: instagram.com/fitoterapevt1
Телефон: 8 918 843 47 72
Почта: [email protected]
Консультирую бесплатно.
Письмо читательницы:
Здравствуйте Халисат! Прошу помощи у вас, хотя бы добрым словом, советом. . У моей любимой мамочки онкология… Моя мама Аселя, 49 лет, все было хорошо, и в конце декабря резко заболела, 2 недели лечилась от язвы желудка, а потом был поставлен диагноз Рак желудка 4 стадия, канцероматоз брюшины. 15 января сделана операция, к сожалению ничего не делали, открыли и зашили…затем она немножко восстановилась после операции, начала кушать только жидкое все и ее все время тошнило, и по вечерам и ночью рыгала постоянно, сделали рентген снимок желудка сказали непроходимость в месте перехода желудка в ДПК, и вот 31 января сделана повторная операция, врач сказал что ДПК прикрепит к другому месту в желудке , чтобы пища могла проходить. Мама после повторной операции очень слабая….. пока лежит в реанимации.. хочу у вас заказать настойки , может начать травами лечить?..я в отчаянии…
. У моей любимой мамочки онкология… Моя мама Аселя, 49 лет, все было хорошо, и в конце декабря резко заболела, 2 недели лечилась от язвы желудка, а потом был поставлен диагноз Рак желудка 4 стадия, канцероматоз брюшины. 15 января сделана операция, к сожалению ничего не делали, открыли и зашили…затем она немножко восстановилась после операции, начала кушать только жидкое все и ее все время тошнило, и по вечерам и ночью рыгала постоянно, сделали рентген снимок желудка сказали непроходимость в месте перехода желудка в ДПК, и вот 31 января сделана повторная операция, врач сказал что ДПК прикрепит к другому месту в желудке , чтобы пища могла проходить. Мама после повторной операции очень слабая….. пока лежит в реанимации.. хочу у вас заказать настойки , может начать травами лечить?..я в отчаянии…
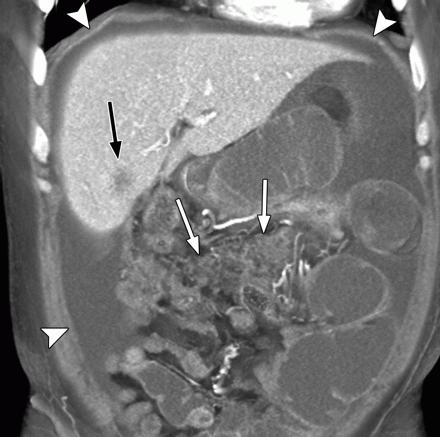
С каждым годом такой диагноз как онкология ставится все чаще и чаще. Страшнее всего то, что клетки данного недуга можно найти в любом органе и не всегда вовремя диагностировать. В связи с некоторыми негативными факторами достаточное распространение получил рак брюшины.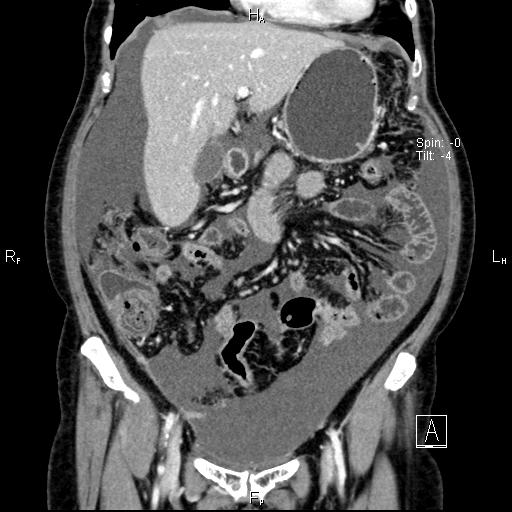 Чтобы решить эту проблему, можно прибегнуть не только к традиционным методам, но и народным средствам лечения канцероматоза.
Чтобы решить эту проблему, можно прибегнуть не только к традиционным методам, но и народным средствам лечения канцероматоза.
Что это и как проявляется
Данный термин относят к злокачественным новообразованиям со многими метастазами, которые проникают в паренхиму и серозные оболочки. Само по себе это тонкая полупрозрачная пленка, которая покрывает поверхности внутренних органов и внутренние стенки. Зачастую его обнаруживают при диагностировании рака желудка. Если во время не приступит к лечению, то это может привести к летально исходу.
Основными признаками наличия данного недуга является:
- сильная острая, тупая, постоянная или периодическая боль в брюшной области;
- потеря веса из-за рвоты и тошноты;
- увеличение поврежденного органа.
Многие симптомы есть достаточно индивидуальными и зависят полностью от особенностей организма человека. Но всех их нужно учитывать при подборе народных средств лечения канцероматоза брюшины.
В основном опухоли образуются в местах, где происходят ослабления или нарушения. Если диагностику провести не вовремя, то отростки начинают поражать все соседние органы. Поэтому при малейших подозрениях необходимо обратится к врачу. Многие врачи считают, что это вторичное заболевание. Первоначально начинают проявляться симптомы первого заболевания.
Если диагностику провести не вовремя, то отростки начинают поражать все соседние органы. Поэтому при малейших подозрениях необходимо обратится к врачу. Многие врачи считают, что это вторичное заболевание. Первоначально начинают проявляться симптомы первого заболевания.
Народная терапия
Есть несколько видов традиционного лечения. Наиболее часто сегодня используют:
- радио и генную иммунотерапию,
- фотодинамическую,
- использование ингибиторов ангиогенеза.
Но есть и лечение канцероматоза брюшной полости народными средствами. Она проводит исцеление с помощью трав и растений. Наиболее часто в рецептах встречаются: полынь, пижма, сныть, сабельник. Не лишним будет и использование трав, которые нормализуют процессы обмена веществ и выводят продукты жизнедеятельности из организма. Положительное противовоспалительное и общеукрепляющее влияние оказывают отвары из ромашки, мяты, тысячелистника, подорожника.
Чай из чистотела
Залейте 200 мл чайную ложку сухого измельченного чистотела. Дайте постоять 30 минут и принимайте трижды в день перед едой по 1/3 стакана.
Дайте постоять 30 минут и принимайте трижды в день перед едой по 1/3 стакана.
Простые способы лечения сложных заболеваний:
Болиголов на спирту
Также народное лечение канцероматоза брюшины можно проводить и настойкой болиголова. Купите в аптеке спиртовую настойку, ее можно приготовить и самостоятельно, но так как растение ядовито, то необходимо строго соблюдать дозировку при приготовлении.
Для этого залейте 50 г травы 0,5 л водки. Сырье залейте и поставьте на 2 недели в защищенное от солнечного света место. Регулярно взбалтывайте содержимое. Схема приема заключается в приеме препарата с 1 по 4 день четырежды в сутки по 1 капле. С 5 по 8 – по 2 капли. Далее каждые 3 дня стоит повышать количество на 1. Максимальной дозой 5. прием стоит проводить в одно и тоже время через равные промежутки.
Для приема настойки купленной в атеке другая схема:
- в первый день – по капле дважды перед едой,
- на следующий – увеличьте еще на одну,
- таким образом увеличивайте ежедневно на такое количество, пока не достигните 20,
- после этого идите в обратном порядке, постепенно снижая объем.

По завершению курса сделайте перерыв на 14 дней и снова повторите. Максимальное количество таких приемов в год 2-3, чтобы избежать привыкания к препарату.
Настойка цветов картофеля
Соберите на пике цветения цветы картофеля, желательно не белого цвета. Высушите их без попадания прямых солнечных лучей. Влага должна полностью уйти из них. Отделите 2 ладони и залейте 0,5 л спирта. Настаивайте на протяжении 14 дней в темном помещении. Процедите и принимайте по 6-7 капель на 50 мл воды 3 раза в день.
Алоэ с коньяком
Соедините 500 мл коньяка и 2-3 столовые ложки сока алоэ. Сорвите с молодого куста пеларгонии 2 листа и залейте 50 мл кипяченной воды. Закутайте и поместите в теплое место на сутки. Эту настойку добавляйте в алкогольную смесь. Параллельно введите еще и пару капель йода. Прием утром и вечером.
Травяной сбор
Есть неплохое соединение: травы душицы, корня лопуха и аира, а также цветок календулы. Залейте все пол литром кипятка и дайте настоятся. Принимайте на протяжении дня.
Принимайте на протяжении дня.
Лопух
Народное лечение канцероматоза брюшной полости можно также проводить лопухом. Возьмите корень весеннего лопуха. Его необходимо натереть и принимать постоянно.
Целебный состав
Соедините 7 г почек черного тополя, 10 г аира, 23 г соцветий лопуха, 40 г корня этого растения, 55 г соцветий бодяка полевого. Залейте все литром кипятка и настаивайте. Пейте по 250 мл 3 раза в день перед приемом пищи.
Здоровья Вам!
Полезные статьи:
лечение, срок жизни и симптомы. Продолжительность жизни пациентов с канцероматозом брюшной полости
При любых злокачественных образованиях могут развиться метастазы. При наличии вторичных очагов опухоли шансы пациента на выздоровление снижаются. Многие пациенты, которые обращаются к врачам-онкологам, интересуются, что такое канцероматоз брюшины и может ли он развиться при онкологии.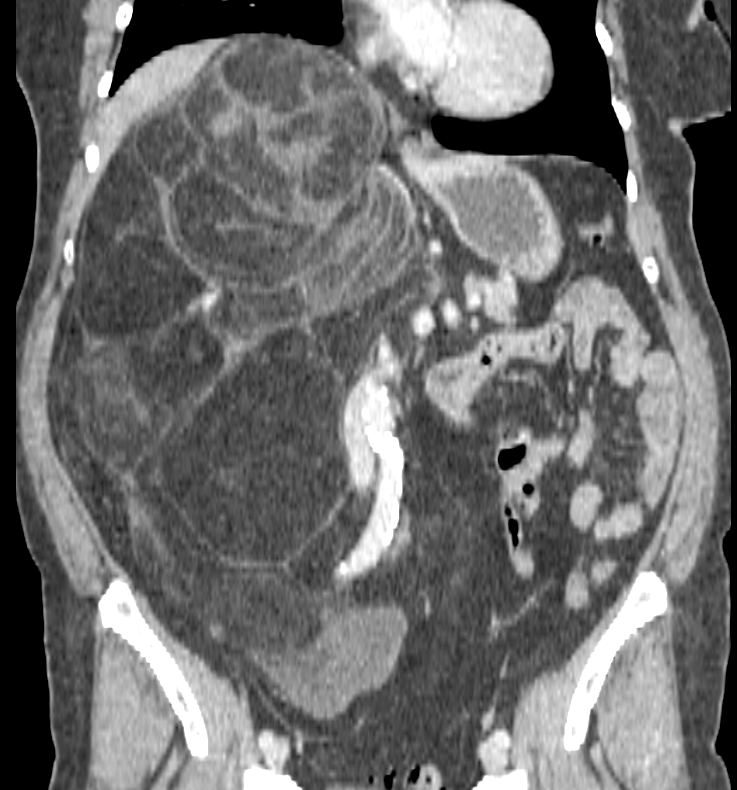
Канцероматоз брюшины является вторичным онкологическим заболеванием, прогноз которого в большинстве случаев неблагоприятен. Пациентам с данным диагнозом назначается паллиативное лечение, методы которого направлены на поддержание жизнедеятельности. Лечение канцероматоза брюшной полости осуществляется в Юсуповской больнице, опытные специалисты которой принимают даже тех пациентов, от которых отказались в других клиниках.
Канцероматоз — что это?
Канцероматоз брюшной полости является онкологическим заболеванием, формирование которого происходит из-за распространения раковых клеток из первичного очага. Лечение данного заболевания предполагает оперативное вмешательство с последующим проведением химиотерапии.
Данное заболевание может развиваться на фоне злокачественной опухоли любого органа, у женщин диагностируется канцероматоз брюшины при раке яичников.
Врачами-онкологами при постановке диагноза применяется классификация в зависимости от локализации и количества метастазов:
- степень Р1 – локальное развитие онкологического процесса
- степень Р2 –несколько пораженных участков серозной оболочки
- степень Р3 – множественные очаги пораженной ткани.

Если у пациента диагностирован канцероматоз брюшины, продолжительность жизни сокращается. Опытные врачи-онкологи Юсуповской больницы при лечении пациентов проводят полную диагностику для определения текущего состояния, разрабатывают программу лечения. Современное оборудование, которым оснащена Юсуповская больница, позволяет проводить комплексное обследование.
Вопросы многих пациентов связаны с лечением канцероматоза брюшины. Благоприятность прогноза при данном онкологическом процессе зависит от степени поражения и выбранного лечения. Для установления степени поражения проводится лабораторно-инструментальное обследование.
Признаки и симптомы
Канцероматоз брюшины, лечение которого требует пребывания пациента в стационаре и круглосуточного наблюдения, является вторичным заболеванием. Клиническая картина при данном диагнозе определяется признаками первичного злокачественного образования. Канцероматоз брюшины при раке характеризуется формированием асцита – скоплением в брюшной полости свободной жидкости..jpg)
Основные признаки канцероматоза брюшины:
- быстро снижается масса тела и увеличивается живот
- нарушение пищеварения
- обильное потоотделение;
- тупые, сильные боли в области живота
- характеризуют канцероматоз брюшины боли под грудью
- у больного отмечаются признаки сильной интоксикации
- жидкий стул, в котором может присутствовать кровь.
По мере прогрессирования онкологического процесса у больного может происходить потеря сознания и наблюдаться состояние бреда. Канцероматоз брюшины при раке требует незамедлительного лечения, поэтому Юсуповская больница принимает пациентов в тяжелом состоянии ежедневно 24 часа в сутки.
Канцероматоз и асцит могут угрожать жизни больного, поэтому люди, находящиеся в зоне риска, должны знать симптомы болезни, чтобы своевременно обратиться к врачу-онкологу. Специалисты Юсуповской больницы отвечают на вопросы пациентов: канцероматоз брюшной полости — что это такое, какие способы лечения существуют и какова продолжительность жизни..jpg)
Причины развития
Канцероматоз брюшины, лечение которого сочетает оперативное вмешательство и химиотерапию, формируется на фоне имеющегося первичного очага. Раковые клетки при развитии становятся подвижными, поэтому они начинают отделяться от опухоли и распространяться по организму.
Канцероматоз брюшины и асцит распространяется стремительно, так как перемещение раковых клеток осуществляется несколькими путями:
- с током крови и лимфатической жидкости
- при удалении первичной раковой опухоли, например, канцероматоз брюшины при раке яичников
- при прорастании злокачественной опухоли в брюшину.
Масштаб поражения при данном заболевании может быть достаточно большим, так как площадь брюшины может достигать двух квадратных метров. Канцероматоз брюшины, лечение и срок жизни при котором взаимосвязаны, быстро распространяется из-за анатомического строения брюшной полости. Канцероматоз брюшины с гиперметаболизмом сопровождается такими же симптомами.
Обратитесь в Юсуповскую больницу, если у Вас диагностирован канцероматоз брюшины, лечение онкологического процесса осуществляется в клинике онкологии. Специалисты клиники онкологии, входящей в состав Юсуповской больницы, помогают даже тем пациентам, у которых выявлен канцероматоз брюшины 4 стадии.
Диагностика заболевания
Актуальные вопросы пациентов, у которых выявлен канцероматоз брюшины, включают лечение и продолжительность жизни. Заподозрить онкологический процесс способен врач при взаимодействии с пациентами, имеющими раковое заболевание.
Если у пациента происходит снижение массы тела и присутствуют признаки интоксикации, врач назначает обследование, чтобы опровергнуть или подтвердить диагноз.
Диагностические меры при подозрении на канцероматоз брюшины и асцит:
- ультразвуковое исследование органов малого таза и брюшной полости
- анализ крови
- проведение лапароскопии для осмотра брюшины и забора тканей для биопсии
- компьютерная томография
- МСКТ с контрастным веществом позволяет выявить поражение лимфатических узлов.

Канцероматоз брюшины, продолжительность жизни при котором зависит от степени поражения тканей, может вызвать сложности при диагностике в том случае, если не определен первичный очаг. Врачи-онкологи Юсуповской больницы при консультации пациента оценивают прогноз на основе имеющихся данных обследования, назначают терапию и регулярно контролируют ее эффективность.
Лечение
Канцероматоз брюшной полости, прогноз при котором во многом зависит от адекватности терапии, серьезно отражается на здоровье пациента. Первым этапом лечения злокачественной опухоли является выявление первичного очага, его расположение и стадию. Терапия при патологии назначается только после получения специалистом необходимых данных.
Хирургические методы терапии применимы в том случае, когда это позволяет стадия и расположение раковой опухоли. Канцероматоз брюшной полости 4 степени, прогноз при котором неблагоприятен, не предполагает оперативного вмешательства. Канцероматоз брюшины и асцит требуют лечения химиотерапией.
При данном заболевании проводится симптоматическая терапия, которая предполагает обезболивание, удаление скопившейся жидкости, предотвращение интоксикации, вывод лишней жидкости и улучшение пищеварения.
Продолжительность жизни
Канцероматоз брюшины и асцит, прогноз при которых зависит от многих факторов, может затрагивать небольшую часть брюшины. Если операция проведена своевременно, то прогноз является относительно благоприятным. Однако для этого больному необходимо строго придерживаться рекомендаций врача-онколога.
Если онкологическое заболевание распространилось на большую площадь серозной оболочки, в течение нескольких месяцев может наступить летальный исход. Однако качественная паллиативная терапия способна улучшить прогноз и облегчить состояние больного.
Чтобы начать лечение канцероматоза и улучшить прогноз, обратитесь в клинику онкологии Юсуповской больницы. Опытные специалисты в области лечения раковых заболеваний проведут комплексное обследование и совместно с другими специалистами разработают эффективную программу лечения..png) Записаться на прием к врачу-онкологу Юсуповской больницы можно через форму обратной связи на сайте или по телефону.
Записаться на прием к врачу-онкологу Юсуповской больницы можно через форму обратной связи на сайте или по телефону.
Перитонеальный канцероматоз
Перитонеальный канцероматозВам поставили диагноз: перитонеальный канцероматоз (опухоль брюшины)
Наверняка вы задаётесь вопросом: что же теперь делать? Подобный диагноз всегда делит жизнь на «до» и «после». Все эмоциональные ресурсы пациента и его родных брошены на переживания и страх. Но именно в этот момент необходимо изменить вектор «за что» на вектор «что можно сделать». Очень часто пациенты чувствуют себя безгранично одинокими вначале пути. Но вы должны понимать — вы не одни. Мы поможем вам справиться с болезнью и будем идти с Вами рука об руку через все этапы вашего лечения.
Предлагаем Вашему вниманию краткий, но очень подробный обзор перитонеального канцероматоза.
Филиалы и отделения, где лечат перитонеальный канцероматозМНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Перитонеальный канцероматоз (опухоль брюшины) — одно из самых грозных вариантов прогрессирования целого ряда онкологических заболеваний. Канцероматоз является формой метастазирования, при которой опухолевые клетки распространяются по внутренней выстилке анатомической полости (брюшной или плевральной) и формируют на ней мелкие узелки, так называемые диссеминаты. Ее возникновение в большинстве случаев подразумевает IV стадию заболевания, и сопряжено с неблагоприятным прогнозом для пациента. Лечение пациентов с перитонеальным канцероматозом является одной из самых сложных задач в онкологии. Наиболее часто он развивается при злокачественных новообразованиях желудочно-кишечного тракта, дыхательной системы и женских репродуктивных органов. При каких опухолях может развиваться перитонеальный канцероматоз? При раке желудка, раке легкого, раке толстой и тонкой кишки, раке яичников, муцинозных опухолях червеобразного отростка.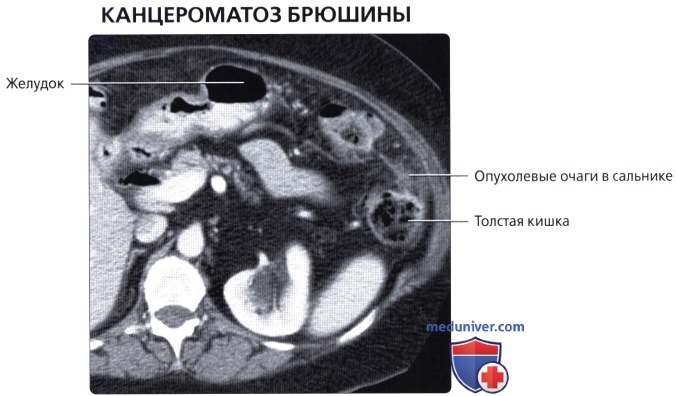
Согласно данным статистики, перитонеальный канцероматоз встречается у 20-35% пациентов с онкопатологией: в 40% случаев данное осложнение формируется при опухолях желудочно-кишечного тракта, в 30% — при раке яичников (причем на момент верификации диагноза рака яичников у подавляющего большинства пациенток уже имеет место поражение брюшины). Перитонеальный канцероматоз (опухоль брюшины) является неблагоприятным прогностическим фактором; данная форма прогрессирующего опухолевого поражения практически не поддается хирургическому лечению, а применение только системной химиотерапии улучшает состояние лишь на некоторое время.
Причины возникновения перитонеального канцероматозаПеритонеальный канцероматоз является вторичным опухолевым поражением, результатом прогрессирования рака различной локализации. Наиболее часто поражение брюшины осложняется раком желудка, тонкого кишечника, поджелудочной железы, злокачественными опухолями яичников, матки, маточных труб, печеночноклеточным раком, реже — первичными опухолями брюшины (перитонеальная мезотелиома)..jpg)
Развитие перитонеального канцероматоза является поэтапным процессом. Первый этап – распространение опухолевых клеток из первичного очага поражения. Это связано с нарушением межклеточного взаимодействия и приобретением клетками опухоли подвижности. При этом эпителиальные клетки меняют фенотип на мезенхимальный, происходит деградация межклеточного матрикса. Распространение опухолевых клеток может происходить в ходе оперативного вмешательства. Их механическое отделение возможно при повреждении лимфатических или кровеносных сосудов. Попавшие в брюшную полость клетки опухоли мигрируют под действием силы тяжести, сокращений внутренних органов, имплантируются в местах повышенной резорбции: большом сальнике, в области слепой кишки, дугласовых карманах.
На втором этапе опухолевые клетки взаимодействуют с мезотелием брюшины. Механизмы адгезии определяются природой клеток, особенностями морфологии брюшины, а также наличием участков ее повреждения. Далее клетки закрепляются в мезотелии, происходит их горизонтальное распространение по поверхности перитонеума, а затем инвазивный рост – прорастание в базальную мембрану, соединительную ткань. Следующим этапом является стимуляция неоангиогенеза – обязательного фактора развития опухоли. Морфопатогенетические механизмы формирования канцероматоза брюшины еще недостаточно изучены, в связи с чем отсутствуют радикальные методы лечения.
Далее клетки закрепляются в мезотелии, происходит их горизонтальное распространение по поверхности перитонеума, а затем инвазивный рост – прорастание в базальную мембрану, соединительную ткань. Следующим этапом является стимуляция неоангиогенеза – обязательного фактора развития опухоли. Морфопатогенетические механизмы формирования канцероматоза брюшины еще недостаточно изучены, в связи с чем отсутствуют радикальные методы лечения.
Частота развития канцероматоза брюшины зависит не только от первичной локализации опухоли, но и от ее размеров, глубины инвазии, гистотипа, степени дифференцировки (недифференцированный рак желудка осложняется поражением брюшины в 60% случаев, ограниченный – в 15%).
Классификация перитонельного канцероматозаЕдиная классификация данного заболевания отсутствует, поскольку характеристики первичных опухолей, приводящих к поражению брюшины, весьма разнообразны. Наиболее распространена классификация перитонеального канцероматоза брюшины в зависимости от числа, локализации метастазов, которая предусматривает три степени:
Р1 – локальное поражение брюшины
Р2 – несколько областей канцероматоза, разделенных здоровыми участками брюшины
Р3 – многочисленные очаги поражения
Также используется метод определения индекса канцероматоза брюшины: суммируются баллы измерения максимальных очагов поражения (0-3 балла) в каждой из 13 наиболее вероятных областей поражения брюшины.
Перитонеальный канцероматоз брюшины является вторичным поражением, поэтому его клиническая картина во многом определяется проявлениями первичной опухоли. Характерным признаком является обильный выпот в брюшную полость – формирование асцита. Зачастую асцитический синдром, развивающийся вследствие обструкции лимфатического дренажа, является единственным признаком заболевания, и пациенты могут поступать в отделение гастроэнтерологии или терапии для диагностики причин асцита. Состояние больных тяжелое, характерна значительная потеря веса. Неспецифическими признаками являются тошнота, рвота, выраженная слабость, утомляемость. При наличии крупных метастазов возможно их прощупывание через брюшную стенку.
Диагностика перитонеального канцероматоза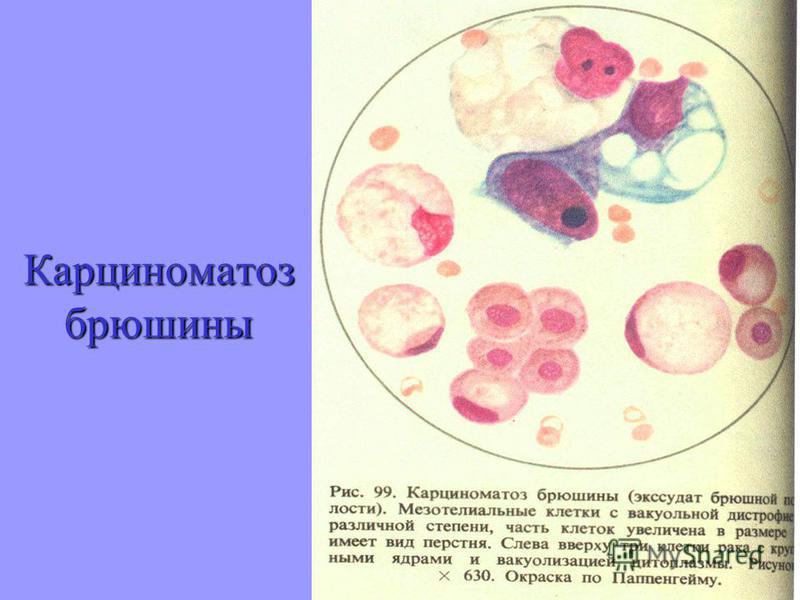 Лабораторные анализы не выявляют специфических изменений: определяется лейкоцитоз, ускорение СОЭ. Диагностическая программа обязательно должна включать УЗИ органов брюшной полости и малого таза, позволяющее обнаружить распространенное поражение, а также МСКТ брюшной полости с контрастированием. Обязательно проводится цитологическое исследование асцитической жидкости, полученной при лапароцентезе, которое дает возможность впервые установить или подтвердить диагноз, а также определить гистогенез клеток опухоли.
Лабораторные анализы не выявляют специфических изменений: определяется лейкоцитоз, ускорение СОЭ. Диагностическая программа обязательно должна включать УЗИ органов брюшной полости и малого таза, позволяющее обнаружить распространенное поражение, а также МСКТ брюшной полости с контрастированием. Обязательно проводится цитологическое исследование асцитической жидкости, полученной при лапароцентезе, которое дает возможность впервые установить или подтвердить диагноз, а также определить гистогенез клеток опухоли.Информативным методом диагностики перитонеального канцероматоза является лапароскопия с осмотром перитонеума, дугласова пространства, диафрагмы, сопровождающаяся биопсией. Высокой специфичностью обладает обратнотранскриптазная полимеразная цепная реакция (ОТ-ПЦР), которая позволяет определить источник диссеминации даже при малом количестве опухолевых клеток.
Сложности диагностики возникают при наличии перитонеального канцероматоза без выявленного первичного очага. Данная форма заболевания, встречающаяся в 3-5 % случаев, проявляется клинически только при уже сформировавшемся поражении брюшины. При этом первичный очаг может иметь настолько малые размеры, что его прижизненное обнаружение невозможно.
Данная форма заболевания, встречающаяся в 3-5 % случаев, проявляется клинически только при уже сформировавшемся поражении брюшины. При этом первичный очаг может иметь настолько малые размеры, что его прижизненное обнаружение невозможно.
В качестве дополнительных методов может использоваться определение онкомаркеров (кислой фосфатазы, раково-эмбрионального антигена, альфа-фетопротеина, бета-субъединицы ХГЧ). Такая диагностика не обладает высокой специфичностью, но применяется для оценки прогноза, раннего выявления диссеминации, рецидивов, а также для контроля эффективности лечения.
Лечение перитонеального канцероматоза Однако даже при определении индекса СС-0 нельзя полностью исключить возможность диссеминации, поэтому обязательно проводится химиотерапия.
Однако даже при определении индекса СС-0 нельзя полностью исключить возможность диссеминации, поэтому обязательно проводится химиотерапия.Эффективные подходы к лечению, как правило, подразумевают проведение комбинированной терапии, например, сочетания хирургического вмешательства и системной химиотерапии. Одним из наиболее эффективных методов является локальная химиотерапия. Идея локальной химиотерапии состоит в том, чтобы обеспечить доставку лекарственного препарата непосредственно к опухолевым клеткам, находящимся на внутренней выстилке анатомической полости. Из-за крайне низкой проницаемости этой области для лекарственных препаратов, например, при внутривенном их введении или приеме в виде таблеток, доставка препаратов в виде аэрозоля под давлением углекислого газа даёт накопление препарата в опухоли в значительно больших концентрациях.
Методы лечения перитонеального канцероматозаДлительное время канцероматоз брюшины и плевры считали терминальной стадией болезни, не подлежащей специальному лечению.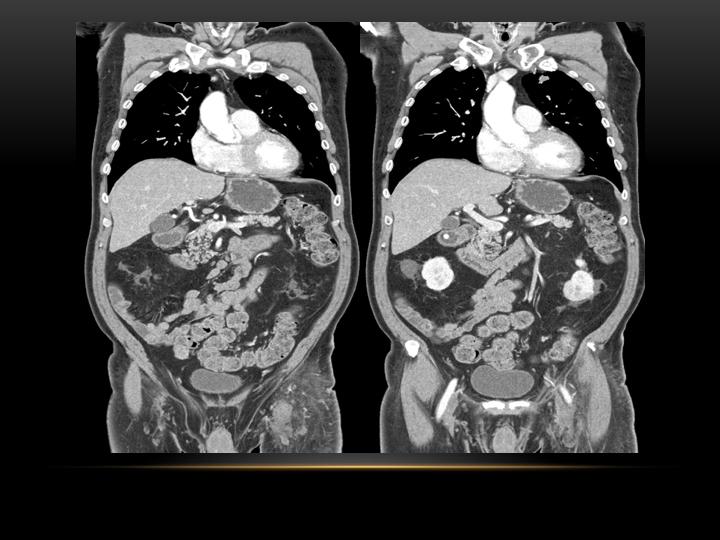 Разработка методик непосредственного воздействия на брюшину и плевру позволила улучшить прогноз при этом состоянии. МНИОИ им. П.А. Герцена обладает уникальными возможностями лечения больных с канцероматозом, имея в арсенале весь комплекс новейших методов терапии.
Разработка методик непосредственного воздействия на брюшину и плевру позволила улучшить прогноз при этом состоянии. МНИОИ им. П.А. Герцена обладает уникальными возможностями лечения больных с канцероматозом, имея в арсенале весь комплекс новейших методов терапии.
Это методика, при которой во время операции в брюшную или плевральную полость вводится подогретый до 42,5С, высококонцентрированный раствор химиотерапевтических препаратов, что обеспечивает их воздействие непосредственно на раковые клетки в брюшной (плевральной) полости при минимальном воздействии на другие органы. Сеанс проводится в течение часа, что позволяет разрушить опухолевые клетки, оставшиеся после так называемой циторедуктивной операции.
Внутрибрюшная (внутриплевральная) аэрозольная химиотерапия под давлением (PIРAC)Это новейший инновационный метод лечения перитонеального канцероматоза, который обеспечивает доставку лекарственного препарата непосредственно к опухолевым клеткам, находящимся на внутренней выстилке анатомической полости. Метод совсем недавно появился в России. Процедуру проводят посредством лапароскопии (торакоскопии). В брюшной или плевральной полости под давлением углекислого газа распыляют аэрозоль химиопрепаратов и оставляют в течение 30 мин. При таком способе введения химиопрепаратов их воздействие на опухоль многократно возрастает при полном отсутствии системной токсичности. Ноу-хау МНИОИ имени П.А. Герцена в этом методе лечения стала разработка собственной специальной форсунки, которая формирует поток мелкодисперсного аэрозоля с размером капель от 1 до 40 мкм. Изделие выполнено из специализированных материалов и не уступает по качеству импортному аналогу, а по ряду технических характеристик его превосходит.
Метод совсем недавно появился в России. Процедуру проводят посредством лапароскопии (торакоскопии). В брюшной или плевральной полости под давлением углекислого газа распыляют аэрозоль химиопрепаратов и оставляют в течение 30 мин. При таком способе введения химиопрепаратов их воздействие на опухоль многократно возрастает при полном отсутствии системной токсичности. Ноу-хау МНИОИ имени П.А. Герцена в этом методе лечения стала разработка собственной специальной форсунки, которая формирует поток мелкодисперсного аэрозоля с размером капель от 1 до 40 мкм. Изделие выполнено из специализированных материалов и не уступает по качеству импортному аналогу, а по ряду технических характеристик его превосходит.
Программа лечения перитонеального канцероматоза определяется междисциплинарным консилиумом врачей, в который входят специалисты экспертного класса ФГБУ «НМИЦ радиологии» Минздрава России.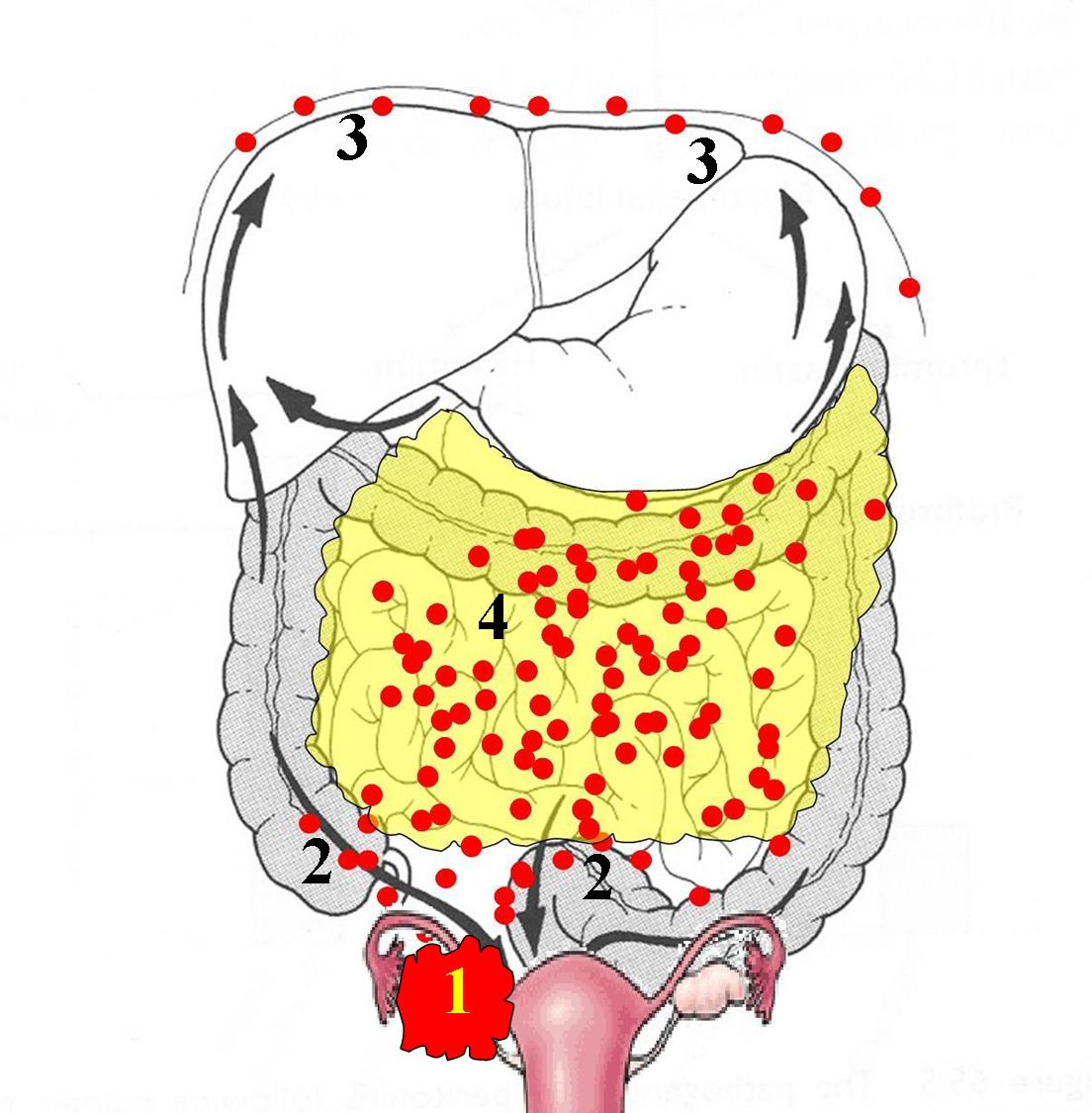 Метод применения аэрозольной химиотерапии под давлением (PIPAC) был впервые испытан в Германии, а Московский научно-исследовательский онкологический институт им. П.А. Герцена — филиал «НМИЦ радиологии» Минздрава России еще в 2013 году стал вторым в мире центром, приступившим к изучению и внедрению данной методики. Проведённая за истекшие 6 лет масштабная научно-практическая работа позволила институту занять лидирующие позиции в этой области и первым в мире доказать целесообразность применения аэрозольной химиотерапии в качестве одного из основных методов лечения у пациентов, страдающих перитонеальным канцероматозом.
Метод применения аэрозольной химиотерапии под давлением (PIPAC) был впервые испытан в Германии, а Московский научно-исследовательский онкологический институт им. П.А. Герцена — филиал «НМИЦ радиологии» Минздрава России еще в 2013 году стал вторым в мире центром, приступившим к изучению и внедрению данной методики. Проведённая за истекшие 6 лет масштабная научно-практическая работа позволила институту занять лидирующие позиции в этой области и первым в мире доказать целесообразность применения аэрозольной химиотерапии в качестве одного из основных методов лечения у пациентов, страдающих перитонеальным канцероматозом.
Возможности лечения канцероматоза
Канцероматоз представляет собой один из наиболее неблагоприятных вариантов метастазирования некоторых злокачественных опухолей, при котором на брюшине (то есть внутренней оболочке, покрывающей брюшную полость и внутренние органы) образуются многочисленные опухолевые узлы или диссеминаты. Наиболее часто он наблюдается при раке желудка, злокачественных опухолях червеобразного отростка, раке толстой кишки, раке яичников и т.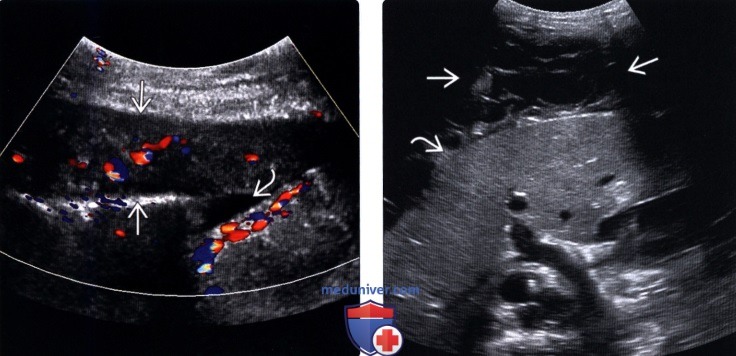 д.
д.
Наличие канцероматоза свидетельствует о далеко зашедшем опухолевом процессе, то есть о IV стадии заболевания. Кроме того, выделяют первичные злокачественные поражения брюшины, к которым относится мезотелиома брюшины. Редким вариантом метастатического поражения брюшины является псевдомиксома брюшины, при которой в полости брюшины накапливаются слизеподобные массы различной плотности. При данном заболевании первичная злокачественная опухоль локализуется в червеобразном отростке (муцинозная аденокарцинома) или в яичниках (пограничная муцинозная опухоль). Довольно часто, особенно при раке желудка, канцероматоз развивается в отдаленные сроки после радикальной операции, негативно влияя на прогноз заболевания.
Симптомы
Поскольку канцероматоз не является самостоятельным заболеванием, то его клиническая картина определяется как клиническими проявлениями первичной опухоли, так и собственно признаками злокачественного поражения брюшины. Наиболее типичным симптомом является появление в брюшной полости свободной жидкости, так называемого асцита. Зачастую асцит является единственным симптомом у данных пациентов. Кроме этого, могут иметь место ряд неспецифических признаков, таких как значительная потеря веса, тошнота, рвота, выраженная утомляемость, слабость.
Зачастую асцит является единственным симптомом у данных пациентов. Кроме этого, могут иметь место ряд неспецифических признаков, таких как значительная потеря веса, тошнота, рвота, выраженная утомляемость, слабость.
Лечение
Наиболее распространенным вариантом лечения большинства злокачественных опухолей, осложненных формированием канцероматоза, является проведение системной химиотерапии, эффективность которой в данной ситуации крайне сомнительна. Дело в том, что благодаря наличию так называемого гематоперитонеального барьера противоопухолевые препараты практически не достигают опухолевых узелков (диссеминатов) на брюшине.
Новые перспективы открывает применение проведение внутрибрюшной перфузионной термохимиотерапии, при которой во время хирургической операции наряду с удалением первичного очага (рак желудка, рак толстой кишки и т.д.) и пораженной брюшины (перитонэктомия) в брюшную полость вводят подогретый до 420С раствор, содержащий противоопухолевые препараты..jpg) Процедуру выполняют с применением современного оборудования (рисунок).
Процедуру выполняют с применением современного оборудования (рисунок).
На фоне высокой температуры, создаваемой вводимым в брюшную полость раствором, создаются условия не только для уничтожения опухолевых клеток, но и для проникновения противоопухолевых препаратов в диссеминаты, находящиеся на поверхности брюшины. Эффективность подобного комплексного воздействия повышается в случае возможности выполнения так называемой циторедуктивной операции, которая заключается в удалении первичной опухоли с регионарными метастазами и отсевами по брюшине. После операции таким пациентам назначается системная химиотерапия, направленная на предупреждение возврата болезни.
Проведение внутрибрюшной термохимиотерапии абсолютно показано пациентам, у которых диагностирован рак желудка, особенно при массивном поражении желудочной стенки. В данной ситуации даже удаление желудка с опухолью не гарантирует выздоровление, поскольку в различные сроки после проведения лечения возможно развитие канцероматоза. Внутрибрюшная термохимиотерапия в данной ситуации как раз дает надежду на предупреждение прогрессирования опухолевого процесса в последующем.
Внутрибрюшная термохимиотерапия в данной ситуации как раз дает надежду на предупреждение прогрессирования опухолевого процесса в последующем.
Консультация специалиста строго по целевому направлению с предварительно записью по телефонам +375 (17) 389-99-00 и +375 (17) 389-99-10 с 8.00 до 20.00 понедельник — пятница.
провоцирующие факторы, характерные признаки, методы терапии и прогноз
Канцероматоз брюшной полости представляет собой вторичное онкологическое образование. Клетки опухолей метастазируют из других очагов поражения.
Согласно медицинской статистике, узнать, что такое канцероматоз брюшной полости, приходиться 35% пациентам с онкологией. В большинстве случаев это люди, с раковыми образованиями в органах желудочно-кишечного тракта и яичников.
Последнее говорит о том, что женская половина подвержена патологии больше мужской.
Канцероматоз брюшины
Из-за вторичности заболевания, изначально у человека присутствуют первичные симптомы рака в виде боли и нарушенного пищеварения.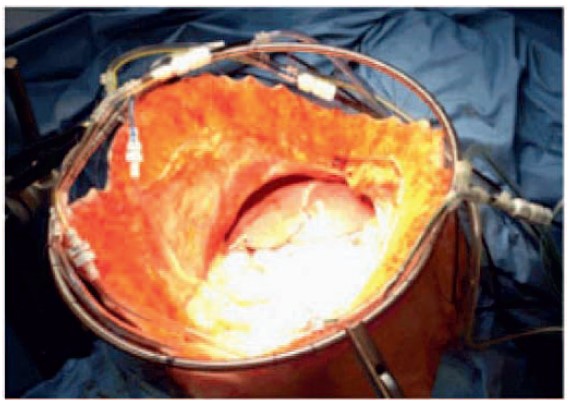 Одним из признаков канцероматоза и чаще всего единственным является асцит брюшины, что это такое пациенты узнают при осложнении онкологии органов и циррозе.
Одним из признаков канцероматоза и чаще всего единственным является асцит брюшины, что это такое пациенты узнают при осложнении онкологии органов и циррозе.
Заболевание проявляет себя скоплением жидкости в животе, давящей на органы. Исходя из статистики, каждый третий пациент умирает от водянки. При наличии больших метастаз, врач может их прощупать.
В стационар человек при канцероматозе поступает в тяжелом состоянии, у него увеличен живот, наблюдается:
- потеря веса;
- тошнота, рвота;
- головная боль;
- низкая или
высокая температура; - вялость.
Канцероматоз брюшной полости входит в международный класс мкб 10. Целью классифицирования является сбор статистики данных о ситуации со здоровьем групп населения, подсчете смертности и влиянии различных факторов.
Причины возникновения
Концероматоз брюшной
полости вызывает распространение раковых клеток от других органов, что
происходит через лимфатическую и кровеносною систему или после операции по удалению первичной опухоли.
Стремительному распространению способствует:
- Тесный контакт брюшины с пищеварительными органами.
- Соприкосновение складок живота друг с другом.
- Внушительное количество лимфоузлов и кровеносных сосудов в области.
Методы мсследования
Диагностировать заболевание врач начинает с изучения анамнеза, симптомов, и после сдачи анализов. При подозрениях на канцероматоз, пациенту назначают аппаратное исследование, оно помогает выявить расположение новообразования, оценить состояние брюшной полости.
Компьютерная томография
Эффективные методы диагностики также включают в себя:
- компьютерную томографию;
- цитологическое исследование жидкости;
- анализ крови ОТ-ПЦР;
- лапароскопию;
- МСКТ.
В 3-5% ситуаций размеры первичного образования настолько малы, что затрудняют диагностику или не выявляются. В таких случаях клиника канцероматоза брюшной полости наблюдается уже при обширном поражении, что делает лечение неэффективным, а состояние пациента контролируют паллиативной терапией.
Медицинская помощь
Лечение канцероматоза брюшной полости длительное и сложное. Медикам приходится бороться за жизнь пациента. К больному применяют химиотерапию, делают операцию, снимают острые симптомы. Дополнить лечение канцероматоза можно нетрадиционной медициной, несмотря на то что, она не доказана научно, сами врачи рекомендуют некоторые рецепты, но только в комплексе с основной терапией.
Хирургическое лечение
Операция проводится в случаях, если позволяет стадия канцеромотоза и локализация поражения. Она направлена на иссечение первичной опухоли, поврежденных лимфатических узлов, метастаз в области живота.
Так как первичные очаги раковых клеток при канцероматозе в большинстве случаев образуются в пищеварительных органах и яичниках, хирурги могут удалить желчный пузырь, сигмовидную кишку, доли толстого или тонкого кишечника, матку, придатки.
Химиотерапия
Прогноз для пациентов 4 степени канцероматоза неутешителен. Операцию в таких случаях не проводят, лечат обычной химиотерапией, снимают симптомы, при асците удаляют жидкость.
В современных клиниках, введение лекарств осуществляют посредством горячего воздуха в пораженную область. На ранних стадиях канцероматоза брюшной полости, процедуру можно осуществить в процессе оперативного вмешательства.
При таком способе, жидкость убивает онкологические клетки на протяжении 60 минут, в дальнейшем усиливает эффективность лечения.
Симптоматическая терапия
Чтоб облегчить жизнь больному, задача врачей – снять клинику канцероматоза брюшной области и асцита, для этого прибегают к следующим методам:
- Прокалывают область живота, чтоб выпустить скопившуюся воду.
- Сильные боли притупляют путем инъекций с наркотическим анальгетиком.
- Интоксикацию снимают капельницами.
- Для вывода жидкости также используют мочегонные препараты (Фурациллин).
Народные средства
Перед тем как использовать народные методы лечения канцероматоза брюшной полости, врачи настоятельно рекомендуют обсудить рецепты, в противном случае можно усугубить ситуацию и уменьшить продолжительность жизни.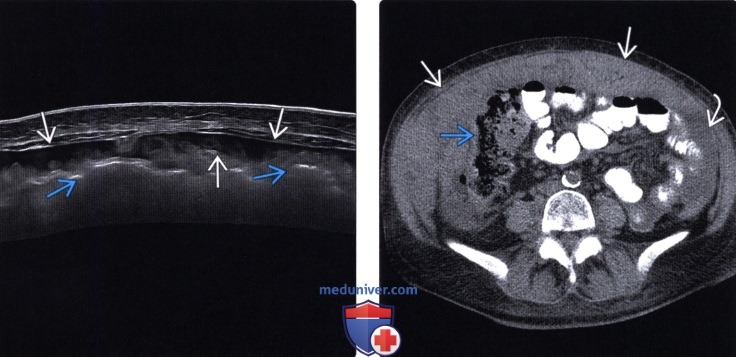 Опасения связаны с индивидуальностью каждого человека, сопутствующими заболеваниями, противопоказаниями, возможными осложнениями и отравлениями после употребления составов.
Опасения связаны с индивидуальностью каждого человека, сопутствующими заболеваниями, противопоказаниями, возможными осложнениями и отравлениями после употребления составов.
Чаще всего в составе противораковых рецептов преобладают:
- пижма;
- полынь;
- сабельник;
- сныть;
- ромашка;
- мята;
- подорожник;
- чистотел;
- тысячелистник и другие.
На основе трав готовят отвары и настои, в отсутствии противопоказаний составы можно употреблять в целях профилактики. При канцероматозе брюшной области эффективны следующие рецепты.
Пеларгония с коньяком
Для этого рецепта при канцероматозе необходимо 2 листа пеларгонии, которые заливают 50 мл кипятка и настаивают сутки в термосе. Полученную жидкость соединяют с 500 мл конька, 3 суповыми ложками сока алое, 2 каплями йода. Лекарство пьют с утра и перед сном.
Настойка болиголова
Растение ядовитое, поэтому важно соблюдать дозировку. Лекарство можно купить в готовом виде или сделать самостоятельно.
Лекарство можно купить в готовом виде или сделать самостоятельно.
В приготовлении понадобиться 0,5 л спирта и 50 г сухого болиголова, которые ставят на 14 дней в темное место и регулярно перемешивают.
Средство при канцероматозе употребляют: 4 дня подряд по 1 капле, 4 раза в сутки; с 5 по 8 день количество капель 2; на 9 день 3 капли;на 10 сутки 4 капли; на 11 день 5 капель. Готовую настойку пьют при канцеромотозе по 2 капли перед приемом пищи в 1 сутки, на следующий день 3 капли.
Количество капель увеличивают на 1 каждый день, пока не дойдут до 20, после чего прием идет в обратном порядке на уменьшение. Закончив курс, организму дают время на отдых, через 2 недели схему повторяют. В год разрешено не более 3 курсов.
Настой картофельных цветов
В лечении канцероматоза эффективны соцветия картофеля. Собранные цветы высушивают без воздействия солнца. Смесь в количестве 2 горстей заливают 0,5 л спирта и оставляют на 2 недели в темном месте. Далее жидкость процеживают, разводят в пропорции 7 капель на 50 мл воды и пьют 3 раза в сутки.
Далее жидкость процеживают, разводят в пропорции 7 капель на 50 мл воды и пьют 3 раза в сутки.
Травяной сбор №1
Для лекарства от канцеромотоза нужны почки черного тополя в количестве 5 г, аир 8 г, 25 г соцветий лопуха и 35 г корня, цветы полевого бодяка 50 г. Смесь заливают 0,9 мл кипятка, настаивают и пьют перед едой, разделив на 3 суточных приема.
Травяной сбор №2
Следующий рецепт при канцероматозе включает экстракты чаги и столетника по 200 г, шиповник, тысячелистник, сосновые шишки по 50 г, полынь 5 г, коньяк 250 г, мед 500 г. Ингредиенты заливают 3 литрами кипятка, варят 2 часа, настаивают сутки, употребляют по 1 большой ложке перед приемами пищи на протяжении 2 недель.
Настойка полыни
Трава хорошо зарекомендовала себя в лечении онкологии, на ее основе делается одно из противораковых лекарство Артемизинин. При канцероматозе можно пить аптечную настойку полыни в количестве 15 капель, не более 3 раз в сутки, курсом 14 дней.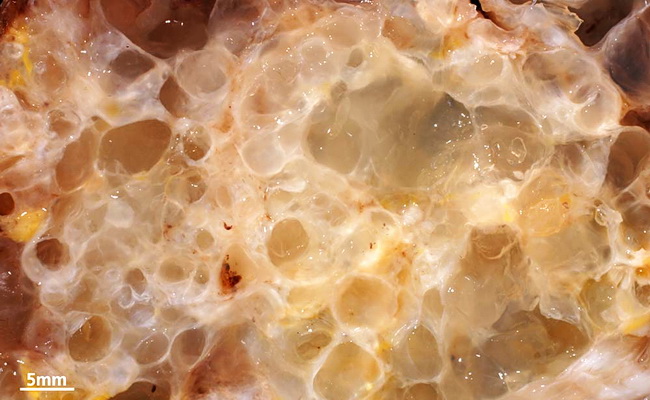
Настойка одуванчика
Корни растения промывают и оставляют обсыхать, используют после прекращения выделения молока. Траву подсушивают при температуре 40-50 градусов, берут в количестве 3 суповых ложек, заливают 500 мл кипятка, варят на медленном огне 20 минут. Процеженную жидкость употребляют при канцероматозе после еды, 2 раза в день по 250 мл.
Продолжительность и прогноз жизниКанцероматоз брюшной полости имеет неблагоприятный прогноз жизни, учитывая, что заболевание – это уже метостазы, а его симптомы обычно проявляются, когда клетки достаточно распространились.
Продолжительность жизни пациентов при канцероматозе брюшной полости 4 степени менее 12 месяцев, начальные стадии имеют прогноз 5-летней выживаемости 10%, таким образом, сколько точно живут пациенты, определяет своевременная диагностика и лечение.
Источник: https://OtekOff.ru/otek/otek-zhivota/kantseromatoz-bryushnoj-polosti
Канцероматоз брюшной полости — прогноз, лечение, причины
Канцероматозом брюшины называется один из вариантов метастазов, поражающих, обычно, плевру и брюшину. При наличии диагноза рака, независимо от места локализации опухоли, может возникнуть метастазирование, а в случае у пациента наличия вторичных очагов поражения, его шансы на излечения значительно уменьшаются.
Канцероматоз не является отдельной болезнью, а относится к серьезным осложнениям других злокачественных раковых заболеваний, например, таких как рак поджелудочной железы, печени или матки, с весьма неблагоприятным прогнозом.
Что такое канцероматоз
В онкологии канцероматоз брюшной полости — один из вариантов метастазирования злокачественных новообразований, независимо от их локализации, при котором происходит поражение серозной оболочки – брюшины.
Патология характеризуется отделением злокачественных клеток от локализации первичного очага заболевания с последующим их распространением с серозной жидкостью в брюшину.
Очаги диаметром могут быть от нескольких миллиметров, до нескольких сантиметров, при этом их расположение может быть единичным или сливаться воедино.
В ходе развития болезни и распространения опухолевых клеток, может образоваться асцит — уменьшение общей массы тела и нарастающая интоксикация с выделением жидкости в брюшную полость. Что такое канцероматоз знают немногие.
Стоит отметить, что прогнозы на выздоровление для пациентов с канцероматозом сводятся к минимуму, так как патология практически не подлежит хирургическому лечению, а химиотерапия может только временно поддерживать жизнедеятельность больных.
Исходя из статистических исследований, канцероматоз диагностируется у 20-35% случаев злокачественных форм рака, из них в 40% случаев патология возникает у пациентов с опухолью в области органов пищеварения, в частности поджелудочной железы. Рак яичников вызывает канцероматоз в 30% случаев. Также причиной образования канцероматоза может стать злокачественная опухоль с другой локализацией.
Причины возникновения
Канцероматоз (карциноматоз) брюшины представляет собой вторичное раковое поражение, возникающее вследствие прогрессирования злокачественной опухоли, независимо от ее места расположения. Чаще всего возникновение этой патологии наблюдается:
К развитию канцероматоза более склонны пациенты с наличием злокачественных опухолей в области печени. Главной причиной канцероматоза брюшины является наличие первичной опухоли. Нередко исходный очаг поражения установить не удается.
Развитие канцероматоза происходит в несколько этапов:
- Первый этап — злокачественные клетки распространяются от первичного ракового очага, что обусловлено приобретением клеток собственной подвижности, при этом возникает деградация межклеточного матрикса. Спровоцировать распространение клеток может внешнее механическое воздействие, например, оперативное вмешательство или повреждение лимфатической системы и кровеносных сосудов. После попадания раковых клеток в область брюшины, их распространение обусловливается силой тяжести и сокращениями внутренних органов.

- Второй этап — злокачественные раковые клетки начинают взаимодействовать с оболочками брюшины, при этом механизм взаимодействия зависит от природы клеток и морфологических особенностей брюшины. Постепенно клетки укрепляются в мезотелии, развивается их горизонтальное распространение с последующим инвазивным ростом.
- Третий этап — происходит стимуляция неоангиогенеза (возникновение кровеносных сосудов питающих опухоль), что в свою очередь стимулирует активный рост ракового новообразования.
В связи с недостаточно изученным морфологическим развитием канцероматоза, результативных методов его лечения пока нет.
Ускоренное развитие канцероматоза может быть вызвано следующими факторами:
- регулярное соприкосновение брюшинных складок;
- соприкосновение брюшины с другими органами пищеварительной системы;
- поражение раковыми клетками органа, содержащего обширные сети кровеносных сосудов.
Также вероятность развития канцероматоза во многом зависит от размеров исходной злокачественной опухоли и степени ее прорастания вглубь пораженного органа.
Классификация
В онкологии для классификации канцероматоза брюшины применяется классификация, в зависимости от места расположения метастазов и их количества. Перитонеальный канцероматоз имеет следующую единую классификацию:
- P1 — метастазы поражают один участок брюшины;
- P2 — у пациентов обнаруживают несколько очагов, между которыми находятся здоровые участки брюшины;
- P3 — большое количество очагов канцероматоза, сливающихся вместе.
Канцероматоз брюшины и асцит характеризуются тяжелым для пациента состоянием, с ярко выраженной клинической картиной. Такие пациенты нуждаются в немедленной госпитализации в специализированное медицинское учреждение.
Основные симптомы
Так как канцероматоз представляет собой уже вторичное поражение, то его клиническая картина, в первую очередь, зависит от исходной раковой опухоли. В случае образования канцероматоза брюшины, симптомы могут быть следующими:
- возникновение болевого синдрома ноющего характера;
- резкое уменьшение массы тела с увеличением живота;
- нарушенная работа системы пищеварения, в частности кишечника;
- интоксикация.
Характерным признаком канцероматоза брюшины является образование асцита, в связи с чем, пациенты изначально поступают в гастроэнтерологическое отделение, где врачи определяют причину вызванного асцита.
Диагностика
Когда возникают симптоматические проявления, связанные с болями в животе и стремительной потерей массы тела, состояние больных может указывать на канцероматоз только в том случае, когда у пациентов уже диагностировано раковое заболевание. Диагностика канцероматоза брюшины проводится посредством следующих процедур:
- ультразвуковое исследование (УЗИ) — позволяет выявить место локализации исходной раковой опухоли, а также изменения в брюшной полости, расположения очагов поражения и их размеры;
- компьютерная томография (КТ) — необходима для исследования всех слоев брюшной области, выявления очагов поражения и определения их структуры;
- лапароскопия — проводится для осмотра брюшины и исследования асцитической жидкости, полученной в процессе проведения процедуры;
- анализ крови ОТ-ПЦР — детализированное определение локализации первичного очага.
Анализ асцитической жидкости, полученной при помощи лапароскопии или пункции серозной полости, необходим для изучения на предмет наличия опухолевых клеток. Иногда, примерно в 5% из всех случаев болезни, диагностика не позволяет определить первичную опухоль, так как она может иметь очень маленький размер. Бывают случаи, когда диагностика раковой опухоли выполняется уже посмертно.
Способы лечения
После проведения всех диагностических мероприятий лечение канцероматоза проводится достаточно трудно, и не всегда результативно. Если у пациента есть шансы на излечение, ему может быть назначена операция, после которой проводят химиотерапию.
Иногда пациенты пытаются лечить канцероматоз брюшины народными средствами, что так же не дает желаемого результата.
Сейчас в медицине применяется множество разных методик для противоракового лечения, возможно в ближайшем будущем ученые смогут найти эффективный способ для терапии злокачественного поражения брюшины.
Хирургическое лечение
При диагностированном канцероматозе брюшины, лечение при помощи хирургического вмешательства подразумевает удаление опухоли, продуцирующей раковые клетки, а также очагов канцероматоза и пораженных лимфоузлов.
Нередко во время проведения такой операции проводится удаление других органов, пораженных клетками опухоли, например, частей толстого и тонкого кишечника, матки и ее придатков или мочевого пузыря.
Химиотерапия
В процессе лечения канцероматоза брюшиной полости сейчас актуально применение интраперитонеальной гипертермической химиотерапии, которую можно проводить непосредственно в процессе операции.
Метод основан на введение химических препаратов посредством горячего воздуха, поток которого направляется непосредственно в брюшину.
Раствор, содержащий необходимые химические средства, находится в брюшине один час, в течение которого он уничтожает злокачественные клетки.
Лечение первичного очага
Важно при диагностированном канцероматозе выявить первичных очаг и определить стадию его развития, место расположения и уровень метастазирования.
После проведения всех диагностических манипуляций врачи определяют способы лечения злокачественного новообразования.
Если стадия развития опухоли и ее локализация позволяют провести операцию, новообразование удаляют при помощи хирургического вмешательства, после которого пациенту назначается комплекс лучевой и химической терапии.
Симптоматическая терапия
Проведение симптоматической терапии направлено на то, чтобы устранить или хотя бы снизить основную симптоматику заболевания. Обычно проводится:
- лечение асцита — удаление скопившейся жидкости посредством пункции брюшной стенки;
- устранение болевого синдрома — если у пациента наблюдаются сильнейшие боли, ему могут быть назначены болеутоляющие средства с наркотическим содержимым;
- улучшение работы пищеварительной системы — необходимо для улучшения усвоения организмом пищи;
- внутривенное вливание растворов — направлено на дезинтоксикацию и нормализацию состава крови;
- использование мочегонных средств — необходимо для выведения избытков жидкости в организме.
Также пациентам могут быть назначены и другие лекарственные средства, необходимые для улучшения функциональности сердечной мышцы или сосудистой системы. Пациенты обязательно должны находиться в условиях стационара под наблюдением медицинских сотрудников.
Прогноз
Обычно вовлечение брюшиной оболочки характеризует раковую опухоль 3-4 степени. Прогнозы для пациентов с диагностированным канцероматозом брюшины не самые благоприятные.
Точно сказать, сколько жить больным с этим диагнозом, нельзя, так как многое зависит от размеров пораженной области и распространенности метастазов.
В случае, когда поражена небольшая область брюшины, можно провести ее удаление, что позволит увеличить продолжительность жизни больного на несколько лет.
Если канцероматоз поражает обширную часть брюшины, срок жизни составляет всего несколько месяцев. Таким больным назначают паллиативную терапию, которая предусматривает поддержание жизнедеятельности пациента в течение этого периода.
Источник: https://rakuhuk.ru/opuholi/kanceromatoz-bryushnoj-polosti
Канцероматоз брюшины: лечение, срок жизни, симптомы и диагностика
Канцероматоз брюшины – это вторичные метастазы, поражающие плевру с брюшиной. Вторичный очаг считается опасным проявлением злокачественной патологии, снижающим шанс на выздоровление больному.
Канцероматоз не относят к отдельному заболеванию. Болезнь является серьезным последствием злокачественного новообразования в печени, поджелудочной железе либо матке.
Проявляется выраженными признаками онкологической интоксикации, потерей веса и асцитом.
Характеристика заболевания
Канцероматоз брюшной полости – это вторичный онкологический очаг, возникающий как следствие злокачественного процесса органов брюшины. Вторичный злокачественный процесс провоцирует метастазирование опухоли, развивающейся в органе малого таза или другого участка. Первичный очаг патологии при разрастании выпускает множественные метастазы в отдаленные участки организма.
Лимфогенный перенос аномальных клеток провоцирует развитие канцероматоза в брюшной полости и плевры с выраженными признаками интоксикации. Новообразование прорастает в эпителиальный слой брюшины.
Раковый патоген проникает в серозный слой и закрепляется на стенках полости. Диссеминация сопровождается последующим формированием злокачественных узелков, напоминающих зерно. Узелки увеличиваются в размерах и постепенно сливаются, образуя опухоль большого размера.
Внутрибрюшная оболочка, пораженная злокачественным новообразованием, не способна выполнять экссудативную и резорбтивную функции. В связи с этим в полости накапливается жидкость, развивается асцит.
Чаще всего патология развивается у людей с наличием раковой опухоли органов пищеварительного тракта – желудка, толстой кишки, кишечника, поджелудочной железы. Кишечный и желудочный недуг развивается стремительно, вовлекая в процесс жизненно важные системы организма. Спровоцировать заболевание у женщин может рак матки или яичников.
Поражение брюшной полости злокачественным процессом вторичного характера считается врачами неблагоприятным прогнозом течения. Болезнь плохо поддаётся терапии, что значительно усложняет жизнь пациента.
Карцинома в ткани лёгкого может спровоцировать вторичный очаг – канцероматоз лёгких. Встречаются единичные образования и множественные. Может формироваться в одном органе или сразу в обоих.
Развитие протекает стремительно, что негативно сказывается на лечении и выздоровлении больного. Курсы химиотерапии останавливают увеличение опухоли на короткий период времени. Но после курса химиотерапии злокачественная клетка увеличивается в размерах ещё быстрее.
Заболевание встречается у 35% больных раком. Из этого количества у 40% первичный очаг присутствовал в органах пищеварительного тракта – желудка и поджелудочной железы. Но в медицинской практике есть примеры развития патологии из-за злокачественного процесса совершенно другого участка.
Код по МКБ-10 болезнь имеет С78.6 «Вторичное злокачественное новообразование брюшины и забрюшинного пространства. Злокачественный асцит».
Причины развития заболевания
Главной причиной развития канцероматоза считается первичный очаг злокачественного процесса. Раковая опухоль способна формировать метастазные ростки, которые проникают в ближайшие и отдалённые участки человеческого тела. Происходит это обычно на последней стадии болезни.
Распространение метастазов по организму происходит:
- С кровью либо лимфой.
- Первичный раковый очаг проникает в брюшную полость с последующим закреплением на стенках полости.
- После хирургического удаления первой раковой опухоли.
Внутрибрюшная полость совместно с серозной оболочкой имеет площадь равную 2 м2. Раковые ростки, проникая в данную область, способны сформироваться на огромном участке. Стенки и складки органа соприкасаются друг с другом, что увеличивает скорость развития патологии.
Стремительное формирование патологии провоцирует наличие сопутствующих факторов:
- Брюшная полость находится в опасной близости с органами желудочно-кишечного тракта.
- Внутренние складки постоянно соприкасаются друг с другом.
- Присутствует огромное количество кровеносных и лимфатических сосудов.
Формирование новообразований происходит на участках, не подверженных перистальтике кишечника. Размер первичного очага влияет на риск развития канцероматоза. Чем крупнее опухоль, тем быстрее и глубже происходит проникание метастазов в ткани брюшины.
Недифференцированный рак желудка всегда сопровождается формированием канцероматоза.
Признаки патологии
При раке первичного очага у больного присутствуют выраженные симптомы поражения конкретного органа. Но в некоторых ситуациях первые признаки опасного заболевания появляются при канцероматозе. Именно это позволяет заподозрить болезнь и поставить правильный диагноз.
Патология обнаруживает следующие признаки:
- Появляются приступообразные болевые спазмы в области живота – постоянные или периодические, с ноющим характером.
- У больного резко увеличивается живот при заметной общей потере веса – в брюшной полости происходит накопление жидкости.
- Наблюдаются приступы тошноты с ротными позывами.
- Болевые ощущения с коликами в области живота.
- Сбой в работе кишечника – длительный запор сменяет диарея.
- Отмечается выраженная мышечная слабость.
- Температура тела принимает термальные показатели на фоне яркого озноба.
- Усиленное потоотделение.
- Сильные головные боли и боли в мышцах.
Болезнь протекает на фоне стремительного ухудшения самочувствия больного. Человек доставляется по скорой в отделение хирургии или гастроэнтерологии. В стационаре после диагностирования ставится правильный и точный диагноз.
Классификация болезни
Канцероматоз брюшной полости классифицируют согласно расположению метастазных отростков и их количеству:
- Стадия Р1 характеризуется локальным расположением узла с одним злокачественным поражением.
- На стадии Р2 присутствует несколько раковых участков, подтверждающих болезнь. Между пораженными очагами выявляются участки здоровых тканей.
- Стадия Р3 соответствует 4 степени злокачественности. Выявляется множество злокачественных новообразований с признаками слияния в единый очаг.
Диагностика заболевания
Выявить болезнь без проведения обследования врач может у пациента онкологического центра с терапией раковой болезни. В остальных случаях требуется проведение расширенного обследования организма больного. Диагностика включает следующие процедуры:
- На УЗИ исследуют органы брюшины с малым тазом. Здесь же выявляется первичный очаг с признаками внутренних изменений в ткани органа. Врач определяет размер, форму и точную локализацию образования.
- При помощи компьютерной томографии изучают орган структурно. По КТ определяются все злокачественные участки, структура с локализацией.
- МРТ и МСКТ проводят с использованием контраста – это позволяет обнаружить отдаленные метастазы и степень поражения лимфатических узлов.
- Лапароскопия требуется для внутреннего изучения поражённых стенок брюшины и получения биологического образца. Образец исследуется в лаборатории биопсическим методом.
- Кровь изучается анализом ОТ-ПЦР. Врачи на основе данного анализа точно выясняет место первичного очага болезни.
Порой установить первичный участок развития патологии не удаётся. В остальных случаях методы диагностики дают подробную информацию о заболевании. Обследование позволяет установить степень поражения организма и назначить адекватное лечение.
Лечение заболевания
Процесс лечения пациента с диагнозом канцероматоза брюшины долгий и сложный. Результат может быть положительным и отрицательным. Неблагоприятный результат терапии случается чаще.
Болезнь можно вылечить на ранних сроках развития и с применением новейших методик и аппаратуры в медицине. В основном применяется хирургическое иссечение злокачественного уплотнения с курсами химиотерапии.
В последние годы разработано много новых эффективных методов борьбы с онкологией. Медицина не останавливается на этом и ищет новые варианты лечения.
Удаление опухоли хирургическим методом проводится с иссечением первичного очага, больных лимфатических узлов. Также возможно удаление органов, поражённых раковыми клетками – матки, желчного пузыря, участка толстого или тонкого кишечника и сигмовидной кишки.
Химиотерапия применяется как отдельное лечение, так и совместное с оперативным методом. В последнее время врачи предпочитают использовать перитонеальный гипертермический способ химиотерапии. Основа метода характеризуется вводом лекарственных препаратов в брюшную полость при помощи горячего воздуха. Иногда это делают сразу после операции или в период проведения операции.
Противоопухолевый раствор держат в полости 60 мин. Затем выводят. За это время происходит непрерывная циркуляция лечебного раствора, который уничтожает злокачественные патогены.
Выявление первичного очага патологии считается первоочередной задачей врачей. Обнаружение болезни с точными размерами и степенью развития позволяет провести полное лечение. Это повышает шанс пациента на выздоровление.
Локализация патологии в доступном и операбельном месте позволяет провести хирургическое иссечение узла. После операции назначаются курсы химиотерапии и облучения гамма-лучами. Дозировки и курсы подбираются индивидуально согласно физическим показателям и медицинским исследованиям пациента.
Параллельно основным способам лечения используется симптоматическое купирование негативных симптомов болезни:
- Делается специальный прокол для вывода лишней жидкости из брюшины.
- Болевой синдром блокируется приемом обезболивающих препаратов.
- Назначаются пробиотики для улучшения перистальтики органов пищеварения.
- Вводятся капельницы с физрастворами для восполнения витаминного и минерального дефицита.
- Мочегонные средства способствуют выводу лишней жидкости.
- Корректируется питание – назначается специальная диета.
Пациент постоянно находится под наблюдением лечащего врача. После курса терапии проводится повторное диагностирование организма. Требуется это для корректировки терапии.
Прогноз лечения
Срок жизни больного зависит от степени поражения организма онкологическим процессом. Сколько проживёт человек, врач сказать не сможет точно. Зависит это от физических показателей и психологического настроя больного.
Поражение незначительного участка брюшины – процент выживаемости выше у пациентов. Продолжительность жизни составляет до 3 лет и более. Если первичный очаг поддаётся лечению, шансы увеличиваются.
При поражении большей площади органа прогноз для пациента неблагоприятный. Летальный исход диагностируется через несколько месяцев. Применяется паллиативная терапия для купирования болевых синдромов и психологического дискомфорта.
При данном заболевании всё зависит от срока выявления и психологического настроя пациента. Доказано учёными, что позитивный настрой на выздоровление значительно увеличивал шансы на выздоровление и долгую жизнь.
Источник: https://onko.guru/zlo/kantseromatoz-bryushiny.html
Канцероматоз брюшины: лечение, срок жизни и симптомы. Продолжительность жизни пациентов с канцероматозом брюшной полости
При любых злокачественных образованиях могут развиться метастазы. При наличии вторичных очагов опухоли шансы пациента на выздоровление снижаются. Многие пациенты, которые обращаются к врачам-онкологам, интересуются, что такое канцероматоз брюшины и может ли он развиться при онкологии.
Канцероматоз брюшины является вторичным онкологическим заболеванием, прогноз которого в большинстве случаев неблагоприятен.
Пациентам с данным диагнозом назначается паллиативное лечение, методы которого направлены на поддержание жизнедеятельности.
Лечение канцероматоза брюшной полости осуществляется в Юсуповской больнице, опытные специалисты которой принимают даже тех пациентов, от которых отказались в других клиниках.
Канцероматоз брюшины: что это такое
Канцероматоз брюшной полости является онкологическим заболеванием, формирование которого происходит из-за распространения раковых клеток из первичного очага. Лечение данного заболевания предполагает оперативное вмешательство с последующим проведением химиотерапии.
Данное заболевание может развиваться на фоне злокачественной опухоли любого органа, у женщин диагностируется канцероматоз брюшины при раке яичников.
Врачами-онкологами при постановке диагноза применяется классификация в зависимости от локализации и количества метастазов:
- степень Р1 – локальное развитие онкологического процесса;
- степень Р2 –несколько пораженных участков серозной оболочки;
- степень Р3 – множественные очаги пораженной ткани.
Если у пациента диагностирован канцероматоз брюшины, продолжительность жизни сокращается. Опытные врачи-онкологи Юсуповской больницы при лечении пациентов проводят полную диагностику для определения текущего состояния, разрабатывают программу лечения. Современное оборудование, которым оснащена Юсуповская больница, позволяет проводить комплексное обследование.
Вопросы многих пациентов связаны с лечением канцероматоза брюшины. Благоприятность прогноза при данном онкологическом процессе зависит от степени поражения и выбранного лечения. Для установления степени поражения проводится лабораторно-инструментальное обследование.
Признаки канцероматоза брюшины
Канцероматоз брюшины, лечение которого требует пребывания пациента в стационаре и круглосуточного наблюдения, является вторичным заболеванием. Клиническая картина при данном диагнозе определяется признаками первичного злокачественного образования. Канцероматоз брюшины при раке характеризуется формированием асцита – скоплением в брюшной полости свободной жидкости.
Основные признаки канцероматоза брюшины:
- быстро снижается масса тела и увеличивается живот;
- нарушение пищеварения;
- обильное потоотделение;
- тупые, сильные боли в области живота;
- характеризуют канцероматоз брюшины боли под грудью;
- у больного отмечаются признаки сильной интоксикации;
- жидкий стул, в котором может присутствовать кровь;
По мере прогрессирования онкологического процесса у больного может происходить потеря сознания и наблюдаться состояние бреда. Канцероматоз брюшины при раке требует незамедлительного лечения, поэтому Юсуповская больница принимает пациентов в тяжелом состоянии ежедневно 24 часа в сутки.
Канцероматоз и асцит могут угрожать жизни больного, поэтому люди, находящиеся в зоне риска, должны знать симптомы болезни, чтобы своевременно обратиться к врачу-онкологу. Специалисты Юсуповской больницы отвечают на вопросы пациентов: канцероматоз брюшной полости — что это такое, какие способы лечения существуют и какова продолжительность жизни.
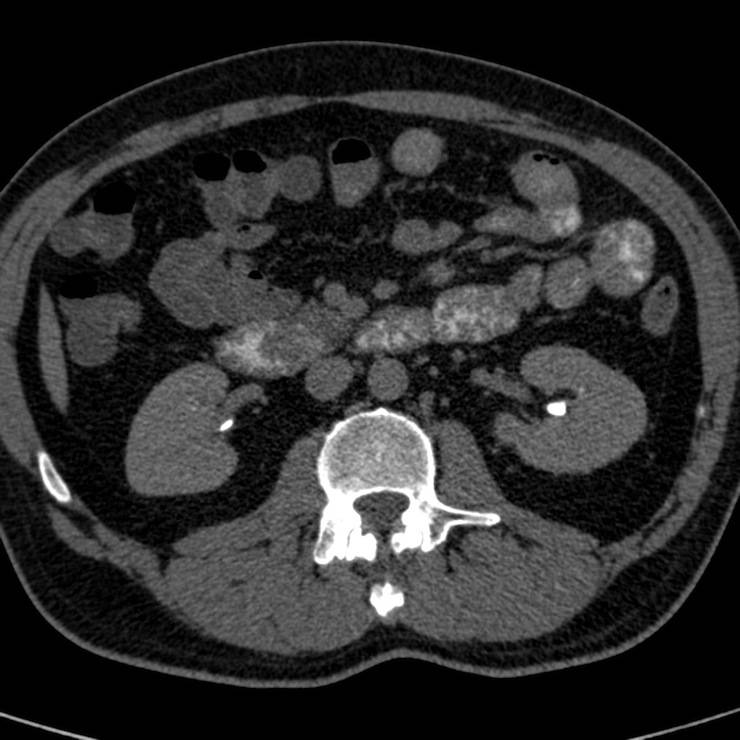
Канцероматоз брюшины (на КТ): причины развития
Канцероматоз брюшины, лечение которого сочетает оперативное вмешательство и химиотерапию, формируется на фоне имеющегося первичного очага. Раковые клетки при развитии становятся подвижными, поэтому они начинают отделяться от опухоли и распространяться по организму.
Канцероматоз брюшины и асцит распространяется стремительно, так как перемещение раковых клеток осуществляется несколькими путями:
- с током крови и лимфатической жидкости;
- при удалении первичной раковой опухоли, например, канцероматоз брюшины при раке яичников;
- при прорастании злокачественной опухоли в брюшину.
Масштаб поражения при данном заболевании может быть достаточно большим, так как площадь брюшины может достигать двух квадратных метров. Канцероматоз брюшины, лечение и срок жизни при котором взаимосвязаны, быстро распространяется из-за анатомического строения брюшной полости. Канцероматоз брюшины с гиперметаболизмом сопровождается такими же симптомами.
Обратитесь в Юсуповскую больницу, если у Вас диагностирован канцероматоз брюшины, лечение онкологического процесса осуществляется в клинике онкологии. Специалисты клиники онкологии, входящей в состав Юсуповской больницы, помогают даже тем пациентам, у которых выявлен канцероматоз брюшины 4 стадии.
Канцероматоз брюшной полости: диагностика заболевания
Актуальные вопросы пациентов, у которых выявлен канцероматоз брюшины, включают лечение и продолжительность жизни. Заподозрить онкологический процесс способен врач при взаимодействии с пациентами, имеющими раковое заболевание.
Если у пациента происходит снижение массы тела и присутствуют признаки интоксикации, врач назначает обследование, чтобы опровергнуть или подтвердить диагноз.
Диагностические меры при подозрении на канцероматоз брюшины и асцит:
- ультразвуковое исследование органов малого таза и брюшной полости;
- анализ крови;
- проведение лапароскопии для осмотра брюшины и забора тканей для биопсии;
- компьютерная томография;
- МСКТ с контрастным веществом позволяет выявить поражение лимфатических узлов.
Канцероматоз брюшины, продолжительность жизни при котором зависит от степени поражения тканей, может вызвать сложности при диагностике в том случае, если не определен первичный очаг. Врачи-онкологи Юсуповской больницы при консультации пациента оценивают прогноз на основе имеющихся данных обследования, назначают терапию и регулярно контролируют ее эффективность.
Лечение канцероматоза брюшной полости
Канцероматоз брюшной полости, прогноз при котором во многом зависит от адекватности терапии, серьезно отражается на здоровье пациента. Первым этапом лечения злокачественной опухоли является выявление первичного очага, его расположение и стадию. Терапия при патологии назначается только после получения специалистом необходимых данных.
Хирургические методы терапии применимы в том случае, когда это позволяет стадия и расположение раковой опухоли. Канцероматоз брюшной полости 4 степени, прогноз при котором неблагоприятен, не предполагает оперативного вмешательства. Канцероматоз брюшины и асцит требуют лечения химиотерапией.
При данном заболевании проводится симптоматическая терапия, которая предполагает обезболивание, удаление скопившейся жидкости, предотвращение интоксикации, вывод лишней жидкости и улучшение пищеварения.
Многие пациенты, у которых диагностирован канцероматоз брюшины, лечение народными средствами рассматривают в качестве метода, который способен улучшить их состояние. Врачи-онкологи Юсуповской больницы не рекомендуют использовать народные методы, так как некоторые из них могут ухудшать состояние и вызывать прогрессирование болезни.
Канцероматоз брюшины: продолжительность жизни
Канцероматоз брюшины и асцит, прогноз при которых зависит от многих факторов, может затрагивать небольшую часть брюшины. Если операция проведена своевременно, то прогноз является относительно благоприятным. Однако для этого больному необходимо строго придерживаться рекомендаций врача-онколога.
Если онкологическое заболевание распространилось на большую площадь серозной оболочки, в течение нескольких месяцев может наступить летальный исход. Однако качественная паллиативная терапия способна улучшить прогноз и облегчить состояние больного.
Источник: https://yusupovs.com/articles/oncology/kantseromatoz-bryushiny/
Канцероматоз брюшины при раке: что это такое, симптомы, причины канцероматоза брюшной полости, прогноз
Канцероматоз брюшины — опухолевое поражение листков слизистой оболочки, покрывающей органы и внутреннюю стенку живота. Преимущественно обусловлен разрастанием метастазов рака в брюшной полости, иногда возможно развитие первичного злокачественного процесса — мезотелиомы в самой брюшине.
Метастатическое поражение правильнее называть «карциноматоз», поскольку карцинома — синоним рака. Аналогично метастазы саркомы в брюшину именуют «саркоматоз».
Частое, но не обязательное проявление перитонеального канцероматоза — выработка асцитической жидкости. С асцитом или без, но поражение брюшины злокачественным процессом всегда угрожает жизни больного и требует очень непростого лечения.
Причины канцероматоза брюшины
Не всякая оторвавшаяся от материнской раковой опухоли клетка способна стать метастазом, в кровеносном русле погибает львиная доля циркулирующих злокачественных клеток. Для обретения способности стать метастазом раковая клетка должна измениться внутренне — научиться вырабатывать вещества, позволяющие самостоятельно жить и внедриться в другом месте, подавляя нормальные клетки.
Оторвавшиеся от узла клетки мигрируют на большие расстояния, раздвигая нормальные клетки, имплантируются в брюшную слизистую, способны даже внедряться внутрь других клеток. После закрепления на местности, начинается размножение и образование целой клеточной колонии.
Кроме переноса метастатических клеток по крови и лимфе, распространение идёт и внутри полости живота — трансцеломически.
Не совсем ясно почему злокачественные клетки задерживаются в брюшине, предполагается благотворное действие микроклимата.
Большинство метастазов находят в местах с более спокойной обстановкой и слабой перистальтикой органов, или там, где активно всасывается внутрибрюшная жидкость.
Часто клетки «разбрасываются» во время операции, причём при лапароскопическом вмешательстве вероятность обсеменения вдвое ниже, чем при классической хирургии.
Во время операции обязательно проводится профилактика раковой диссеминации путём неоднократной обработки специальными растворами, но самый эффективный способ очищения от диссеминатов — внутриполостная химиотерапия на фоне гипертермии (HIPEC).
При каких заболеваниях развивается
Перитонеальный канцероматоз диагностируют у каждого третьего пациента с новообразованием желудочно-кишечного тракта. Метастазы по брюшине характерны для карцином желудка и поджелудочной железы — поражается до 40% пациентов.
При раке кишечника канцероматоз обнаруживают только у десятой части больных.
Максимально высокий процент обусловлен злокачественными процессами яичников — на момент выявления болезни две из трёх пациенток уже имеют опухолевые узлы на брюшине.
Вероятность канцероматоза зависит от степени агрессивности раковых клеток и величины первичной опухоли, так при тотальном инфильтративном раке желудка его выявляют чаще, чем при локальном процессе, не разрушившем наружную серозную оболочку органа.
Тем не менее, ни при одном из злокачественных процессов любой локализации, будь то рак молочной железы или простаты, лёгкого или носоглотки, не исключается внутрибрюшинное метастазирование. Посмертно канцероматозные изменения выявляют у каждого третьего, погибшего от прогрессирования заболевания.
Для сарком такая локализация метастазов нетипична, саркоматоз брюшины констатируется едва ли у трёх из сотни больных. В редчайших случаях совершенно доброкачественные по гистологии муцинозные аденома аппендикса и цистаденома яичников тоже способны привести к обсеменению брюшины с выработкой гелеобразного секрета.
У одного из миллиона, и много чаще это будет женщина, выявляют муцинозную аденому аппендикса или муцинозную цистаденому яичников, в последующем часто приводящие к обсеменению брюшины. Распространение аденомуцинозных клеток в полости живота с выработкой гелеобразного секрета именуют уже «псевдомиксома», зачастую при в этой стадии заболевания не удаётся определить первоисточник опухоли.
Диагностика канцероматоза брюшины
Не представляет трудности выявление опухолевого поражения брюшины при асците, в отсутствии выработки патологического секрета диагностика опирается на визуализацию — УЗИ и КТ с контрастированием.
При УЗИ на внутреннем листке, прилежащем к мышцам брюшной стенки, в норме очень тонком и незаметном, можно увидеть напластования толщиной в несколько сантиметров, практически не прослеживаются только мелкие узелки.
КТ с контрастным усилением много информативнее УЗИ, способно выявить сантиметровые образования. Наиболее точный диагностический метод — лапароскопия. Это обследование обязательно при карциноме желудка, при раке яичников предпочтительна операция — диагностика и лечение одновременно.
Для точного определения первоисточника злокачественного процесса исследуется асцитическая жидкость, получаемая при лапароскопии или пункции. Из экссудата выделяют осадок, который изучают под микроскопом и проводят специфические реакции — ПЦР и ИГХ.
На этапе первичной диагностики ПЭТ не всегда информативна, поскольку далеко не все злокачественные клетки легкого, печени, почек способны накапливать изотопы.
Вне всяких сомнений, самый оптимальный метод диагностики — получение кусочка опухолевой ткани для исследования. Биопсия не целесообразна при известном источнике метастазов и после недавнего лечения первичного рака.
Стадии канцероматоза брюшной полости
Стадирование перитонеального канцероматоза нельзя назвать точным, все классификации приблизительны в определении объёма повреждений и не уточняют локализацию узлов.
Зачастую, стадирование даёт общее представление о прогнозе эффективности лечебных мероприятий, нежели информирует о настоящем состоянии внутри полости живота.
Разработанная японскими специалистами градация опухолевого распространения по трём степеням, учитывает общий объём поражения, без числа и размеров очагов:
- P1 — ограниченное;
- P2 — разделённые нормальной тканью очаги;
- P3 — множество узлов.
Во время операции хирурги определяют индекс перитонеального канцероматоза (РСI), измеряя узелки в 13 регионах полости, общая сумма баллов влияет на тактику лечения, в первую очередь, на возможность удаления брюшины — перитонэктомию и целесообразность внутриполостной химиотерапии. При некоторых злокачественных процессах прибегают к сложным формулам расчёта РСI.
Наибольшее представление о размерах ракового повреждения даёт стадирование по степеням:
- 0 — в полости чисто;
- I — в одной анатомической зоне узелки до 5 мм;
- II — множественные узелки до 5 мм;
- III — локальное поражение 0.5–2 см;
- IV — 2-сантиметровые узелки
Течение канцероматоза определяется не столько размером метастатического узла, сколь клеточной потенцией к прогрессии и выработке асцитической жидкости, общей площадью опухолевой трансформации и клиническими проявлениями.
Симптомы канцероматоза брюшной полости
Перитонеальный канцероматоз небольшой протяжённости может не проявлять себя симптомами, особенно в отсутствии выработки асцитической жидкости. С другой стороны, жидкость может продуцироваться и при отсутствии видимых метастазов.
Как правило, симптоматика неспецифична и в разном наборе могут отмечаться:
- меняющие локализацию болезненные ощущения, а чаще — непонятный дискомфорт в полости живота;
- нарастающая слабость до утраты работоспособности;
- потеря веса при стабильном диетическом режиме;
- прогрессирующее снижение аппетита;
- функциональные нарушения со стороны органов ЖКТ.
Дальнейшее нарастание раковых повреждений сопровождается опухолевой интоксикацией, сдавление желудка опухолевыми узлами осложняется тошнотой и рвотой, кишечника — запорами и поносами с усугублением частичной непроходимости. Распад крупных узлов может вызывать боли и повышение температуры.
Асцит нарушает процесс дыхания и вызывает сердечную недостаточность с постоянными отёками, а частая эвакуация патологической жидкости приводит к белковой недостаточности.
Как лечат канцероматоз брюшины
Ни один из современных методов лечения канцероматоза не гарантирует радикального удаления опухоли, не способен излечить, но может улучшить состояние и существенно продлить жизнь.
Хирургическое лечение канцероматоза технически сложное для оперирующей бригады и трудно переносимое пациентом, поскольку предполагает удаление первичного рака, увеличенных лимфатических узлов, сальниковых сумок и всех видимых опухолевых образований вместе с брюшиной.
Перитонэктомия — многоэтапное вмешательство, включающее удаление нескольких органов и отделов брюшной полости. В результате операции пациент может остаться без селезёнки, желчного пузыря, части кишечника, матки с придатками.
Стандарт терапии канцероматоза — химиотерапия системная и локальная — внутрибрюшинная после удаления асцита или через лапаропорт, установленный во время операции. Эффективность лекарственной терапии невысокая, за исключением случаев первичного рака яичников. Таргетные и иммуно-онкологические препараты только изучаются в клинических испытаниях.
Какие методики терапии дают лучший результат
Наиболее высокий эффект демонстрирует комбинация 3 методов лечения рака:
- операция с максимально возможным удалением злокачественных новообразований — циторедукция;
- локальная внутрибрюшинная гипертермия;
- внутриполостное введение химиопрепаратов.
Использование во время хирургического вмешательства интраперитонеальной гипертермической химиотерапии (ИГХТ или HIPEC) позволяет максимально долго поддерживать очень высокую концентрацию цитостатика непосредственно в зоне поражения и усилить лекарственное воздействие нагреванием тканей.
При весьма скромных исторических результатах хирургического вмешательства устойчивой к цитостатикам псевдомиксомы только HIPEC открывает пациентам перспективу на долгую жизнь.
Технология ИГХТ такова: в течение полутора часов внутрь брюшной полости под давлением подаётся нагретый химиопрепарат в дозе, существенно превышающей максимально разрешённую для внутривенного введения.
За счёт локального использования изменяется спектр токсических реакций, исключается опасное для жизни повреждение кроветворения, но возможна боль в животе и временное нарушение функционирования органов ЖКТ.
Интраоперационная фотодинамическая терапия (ФДТ), когда на выявленные с помощью фотосенсибилизатора очаги опухоли воздействуют лазером, уступает HIPEC по результативности, поскольку лазером невозможно проникнуть во все «закоулки» брюшной полости. Тем не менее, целесообразно использование фотодинамический терапии при крупных и немногочисленных раковых узлах.
Прогноз при канцероматозном поражении
На течение процесса влияет объём поражения на момент начала терапии, степень злокачественности опухоли, в свою очередь определяющая чувствительность к химиотерапии. Основополагающее влияние оказывает талант и опыт хирурга, и несомненно, правильность выбора лечебной тактики.
Однозначно революционные результаты в клинических испытаниях показала только HIPEC.
После интраоперационной гипертермической ХТ пятилетняя выживаемость при канцероматозе рака желудка выросла максимально до 20%, все прочие методы исключали столь долгое дожитие.
При раке толстой кишки с метастазами по брюшине каждый третий пациент прожил более 5 лет, при карциноме слепой кишки и аппендикса — шестеро из десяти вступили во вторую пятилетку жизни.
Источник: https://www.euroonco.ru/terms-from-a-z/kantseromatoz-bryushiny
Лечение рака народными средствами в два раза повышает риск смерти
Люди, использующие гомеопатию, травяные настои и другие альтернативные способы лечения рака, имеют в два раза большую вероятность умереть, чем те, кто лечится только традиционной медициной, гласит исследование Йельского университета.
Те, кто прибегает к нетрадиционной медицине, склонны частично или полностью пренебрегать советами врачей. В результате их прогнозы ухудшаются, сообщает Journal of the American Medical Association Oncology.
Альтернативная медицина предлагает множество способов избавления от рака, эффективность которых не доказана современной наукой. Сюда входят прием травяных настоев, гомеопатия, пищевые добавки, очищающие организм диеты, йога и массаж.
Эксперты отмечают, что побочные эффекты от медикаментозного лечения рака могут быть мучительны: тошнота, боль в суставах, упадок сил и даже бесплодие.
Массаж и акупунктура способны улучшить качество жизни пациента и помочь ему справиться с негативными побочными эффектами лечения. 48-88 % пациентов признались, что пользовались такими методами оздоровления в ходе основной терапии.
Но, к сожалению, многие заблуждаются насчет эффективности таких мер, считая, что они повышают шансы на выживание. Облегчение после сеансов люди принимают за доказательство того, что альтернативная медицина «лечит» онкологию. Сказывается также массовое недоверие к крупным фармакологическим компаниям.
Ученые изучили данные 258 пациентов, которые прибегали к методам нетрадиционногго лечения в период с 2003 по 2014 годы, и сравнили с результатами 1032 больных, которые этого не делали. Для исследования взяли людей с неизлечимыми формами рака, которым лучевая и химиотерапия может продлить жизнь, но ценой мучительных побочных симптомов.В первой группе после пяти лет с момента завершения лечения в живых остались 82,2%, во второй – 86,6%. Сравнивая результаты, специалисты пришли к выводу, что риск умереть среди любителей альтернативных методов оказался выше в 2,08 раз. Такие пациенты гораздо чаще отказывались от различных видов лечения: от хирургического вмешательства – 7% (против 0,1% во второй группе), от химиотерапии – 34,1% (против 3,2%), от лучевой терапии – 53% (против 2,3%), от гормонотерапии – 33,7% (против 2,8%).
Авторы исследования сделали вывод, что нетрадиционные виды лечения связаны с частыми случаями отказа от проверенных методов терапии и более высокой смертностью. Прежде чем принимать решение, каждый пациент должен четко понимать, чем грозит отказ от официальной медицины в пользу сомнительных методов.
Можно ли повторить чудо самоизлечения от рака?
- Дэвид Робсон
- BBC Future
Автор фото, Thinkstock
Несколько пациентов неожиданно вылечились от рака, чем сильно удивили медиков. Корреспондент BBC Future задается вопросом, можно ли на основании этих редких случаев разработать методику для борьбы с раком.
История болезни одной пациентки озадачила всех, кто имел к ней какое-либо отношение. 74-летнюю женщину беспокоила сыпь, которая никак не проходила. К тому времени, как она добралась до больницы, нижняя половина ее правой ноги покрылась бугорками с восковым налетом и яркой красно-фиолетовой сыпью. Анализы подтвердили худшие подозрения: у женщины диагностировали карциному – одну из форм рака кожи.
Прогнозы выглядели неутешительно. Учитывая распространение опухоли, радиотерапия оказалась бы неэффективной, а удалить очаги воспаления из кожи доктора не могли. Скорее всего, лучшим решением оказалась бы ампутация, рассказывает лечащий врач пациентки Алан Ирвайн из больницы Св. Джеймса в Дублине – однако пожилой возраст женщины вряд ли позволил бы ей нормально адаптироваться к протезу. После долгой и откровенной дискуссии было решено подождать, пока будет выбран оптимальный вариант. «Мы долго мучались, что же делать», — объясняет Ирвайн.
А затем началось чудо. Хотя пациентку никак не лечили, опухоли уменьшались и съеживались буквально на глазах. «Мы наблюдали ее в течение нескольких месяцев, и опухоли просто исчезли», — говорит врач. Спустя 20 недель рак исчез. «Сомнений в ее диагнозе не было, — уточняет он. — Однако ни результаты биопсии, ни УЗИ не показали никаких следов карциномы».
Каким-то образом женщина излечилась от, пожалуй, самой страшной болезни наших дней. «Все были в восторге, но несколько озадачены, — сдержанно комментирует ситуацию Алан Ирвайн. — Получается, организм самостоятельно может избавиться от рака – даже если это случается крайне редко».
Вопрос в том, как именно это произошло? Пациентка Ирвайна была уверена, что помогло божественное вмешательство: она поцеловала религиозную святыню ровно перед тем, как начался процесс выздоровления. Однако ученых интересует биологическая подоплека произошедшего, так называемая спонтанная регрессия. Исследовав ее, они надеются найти зацепки, благодаря которым можно было бы провоцировать самоизлечение. «Если вообще получится обучить организм делать подобные вещи, подобная методика получит самое широкое применение», — считает Ирвайн.
Автор фото, SPL
Подпись к фото,Ученые ищут способ спровоцировать иммунную систему на ответ раку
Теоретически наша иммунная система должна вычислять и уничтожать мутировавшие клетки, предупреждая развитие рака. Однако иногда этим клеткам удается остаться незамеченными, и они начинают размножаться, что ведет к росту опухоли.
К тому моменту, когда рак привлекает внимание врачей, самостоятельно вылечиться пациент уже вряд ли сможет: по статистике лишь один из ста тысяч раковых больных избавляется от болезни без помощи медицины.
Внезапное исчезновение
Среди этих редких случаев попадаются и совершенно невероятные. Так, недавно была опубликована история пациентки одной из британских больниц, долгое время страдавшей от бесплодия. Спустя некоторое время врачи нашли у нее опухоль между прямой кишкой и маткой, но когда женщина была уже готова ложиться на операцию, ей наконец удалось забеременеть. Все прошло хорошо, родился здоровый ребенок. Обследование показало, что во время беременности рак мистическим образом улетучился. Через девять лет никаких следов рецидива не наблюдается.
Не менее впечатляющие истории выздоровления отмечались у пациентов с самыми разными видами рака, включая особо агрессивные формы – такие как острый миелоидный лейкоз, предполагающий патологическое размножение белых кровяных клеток. «Если пациента не лечить, он обычно умирает в течение нескольких недель, а иногда и дней», — рассказывает Армин Рашиди из Университета Вашингтона в Сент-Луисе. Однако ему удалось обнаружить 46 случаев, когда острый миелоидный лейкоз отступил сам. Правда, лишь в восьми из них удалось избежать последующего рецидива. «Если спросить случайно взятого онколога, может ли подобное произойти, 99% ответят, что нет, так не бывает», — говорит Рашиди, вместе с коллегой Стивеном Фишером опубликовавший исследование на эту тему.
Мучительное ожидание
В то же время случаи радикального излечения от детской формы рака под названием нейробластома происходят удивительно часто, что дает ученым простор для гипотез относительно причин спонтанной ремиссии. Этот вид рака характеризуется опухолями в нервной системе и эндокринных железах. Если он затем распространяется (дает метастазы), на коже могут появиться узлы, а в печени – новообразования. Из-за опухоли в брюшной полости ребенку становится сложно дышать.
Автор фото, Thinkstock
Подпись к фото,Быстрое и относительно безболезненное избавление от рака сейчас считается чудом
Нейробластома крайне неприятное заболевание, однако порой оно исчезает так же быстро, как появилось, даже без медицинского вмешательства. Более того, если возраст пациента составляет меньше года, регрессия встречается так часто, что врачи обычно не начинают химиотерапию сразу, надеясь, что опухоль рассосется самостоятельно. «Помню три случая, когда на коже были видны внушительных размеров метастазы, а печень увеличилась, однако мы просто наблюдали больных – и они справились сами», — говорит Гарретт Бродер из Детской больницы Филадельфии.
Но принять решение сидеть сложа руки и наблюдать может быть непросто: хотя возможность избежать мучительного лечения одним родителям приносит облегчение, другим бездействие и беспомощность даются несладко. Бродер стремится понять причину исчезновения рака, чтобы избежать подобных страданий. «Мы хотим разработать конкретный препарат, который может запустить механизм регрессии – чтобы нам не приходилось ждать милости природы или «божественного вмешательства», — поясняет он.
Ключи к пониманию
К настоящему моменту Гарретту Бродеру удалось обнаружить несколько интересных зацепок. Так, в отличие от других нервных клеток, клетки опухоли при нейробластоме, похоже, научились выживать в отсутствие так называемого «фактора роста нервов» (NGF) – секретируемого организмом белка, который стимулирует развитие и активность нейронов. Спонтанная ремиссия может быть вызвана естественными изменениями в опухолевых клетках нейробластомы – не исключено, что в этом процессе участвуют клеточные рецепторы, с которыми связывается NGF. Каковы бы ни были изменения, это может значить, что клетки не смогут дальше выживать без важнейшего для них питательного вещества.
В таком случае лекарство, воздействующее непосредственно на рецепторы, могло бы способствовать выздоровлению других пациентов. По словам Бродера, две фармацевтические компании уже подобрали несколько возможных вариантов, и он надеется, что вскоре начнутся клинические испытания. «Оно бы избирательно уничтожало опухолевые клетки, чувствительные к подобному метаболическому пути, и пациенты смогли бы обойтись без химиотерапии, радиотерапии или хирургического вмешательства, — полагает он. — Их бы не тошнило, их волосы не выпадали бы, а анализы крови не ухудшались».
Ответный иммунный огонь
К сожалению, случаи неожиданного избавления от других форм рака изучены хуже — возможно, потому что они так редки. Однако некоторые ориентиры имеются, их появлению способствовала в том числе новаторская деятельность малоизвестного американского врача более ста лет назад.
Автор фото, Thinkstock
Подпись к фото,Ученые не хотят ждать милости от природы или «божественного вмешательства»
В конце XIX века Уильям Брэдли Коли пытался спасти пациента, в шее которого нашли большую опухоль. Пять проведенных операций не помогли излечить рак. Затем мужчина заболел неприятной кожной инфекцией, сопровождавшейся высокой температурой. К тому моменту, как он оправился от инфекции, опухоль исчезла. Коли решил проверить этот принцип на небольшой группе других пациентов и обнаружил, что неоперабельные опухоли рассасываются, если больной принимает микробные токсины или его намеренно заразили бактериями.
Может ли инфицирование в общем случае стимулировать спонтанную ремиссию? Анализ недавних данных явно говорит в пользу дальнейшего изучения этого вопроса. Так, исследование Рашиди и Фишера показало, что 90% пациентов, излечившихся от лейкемии, перенесли другое заболевание – например, воспаление легких – незадолго до исчезновения рака. В других работах отмечается, что опухоли отступали после того, как пациент заболевал дифтерией, гонореей, гепатитом, гриппом, малярией, корью, оспой и сифилисом. Вот уж воистину – что не убивает вас, делает вас сильнее.
Причиной излечения становятся не сами микробы; считается, что инфекция вызывает иммунный ответ, неблагоприятный для существования опухоли. Например, высокая температура может сделать опухолевые клетки более уязвимыми и вызвать их «самоубийство». Или же важную роль играет тот факт, что при борьбе нашего организма с бактериями или вирусами в нашей крови содержится много молекул воспаления, которые активируют клетки-макрофаги, и эти иммунные клетки становятся воинами, уничтожающими и поглощающими микробы – а потенциально и рак.
«Думаю, инфекция способствует тому, чтобы иммунные клетки организма переставали способствовать развитию опухолевых клеток и начинали их уничтожать», — считает Хенрик Шмидт из больницы Орхусского университета в Дании. Это, в свою очередь, может также стимулировать другие составляющие иммунной системы – например, дендритные клетки и Т-клетки – к тому, чтобы распознавать опухолевые клетки и в случае рецидива рака атаковать их вновь.
По мысли Шмидта, понимание процесса спонтанной ремиссии необходимо для развития новейшей методики иммунотерапии, использующей систему естественной защиты организма для борьбы с раком. Так, один способ лечения предполагает инъекцию воспалительных «цитокинов», благодаря которой начинает работать иммунная система. Побочные эффекты – высокая температура и другие симптомы гриппа – обычно смягчаются лекарствами вроде парацетамола для облегчения состояния пациента.
Автор фото, Thinkstock
Подпись к фото,Стандартная противотуберкулезная прививка, по всей видимости, снижает вероятность рецидива меланомы после химиотерапии
Однако учитывая, что температура сама по себе может вызвать ремиссию, Шмидт предположил, что парацетамол способен уменьшить действенность методики. И действительно, он обнаружил, что в два раза больше пациентов – 25% против 10% – смогли пережить двухлетний период, если им не сбивали температуру.
Возможны и другие простые, но действенные способы борьбы с раком, основанные на этих данных. Так, у одного человека произошла спонтанная ремиссия после вакцинации от столбняка и дифтерии – возможно, благодаря тому, что прививки также активизируют иммунную систему. Исходя из этого, Рашиди указывает, что стандартная ревакцинация – например, противотуберкулезная прививка БЦЖ – по всей видимости, снижает вероятность рецидива меланомы после химиотерапии.
Переформатировать иммунную систему
Другие исследователи считают нужным применять более радикальные методы воздействия. Так, приверженцы одного из подходов утверждают, что необходимо намеренно заражать раковых больных тропическим заболеванием.
Этот метод, разработанный американским стартапом под названием PrimeVax, предполагает борьбу сразу по двум направлениям. Дендритные клетки из крови пациента, способствующие координации иммунного ответа на угрозу, подвергаются воздействию его опухолевых клеток в лабораторных условиях. Таким образом они программируются на распознавание раковых клеток. Одновременно пациента заражают лихорадкой денге, разносчиком которой обычно являются насекомые, после чего ему делают инъекцию «обученных» дендритных клеток.
Автор фото, SPL
Подпись к фото,Раковых больных предлагают заражать тропическими болезнями, чтобы активизировать их иммунную систему
Под наблюдением врачей температура пациента поднимается до 40,5 градуса, в то же самое время в его кровь выбрасывается множество молекул воспаления – в результате иммунная система организма начинает работать в авральном режиме. Опухоль, ранее остававшаяся незамеченной, становится мишенью для атаки иммунных клеток, которыми управляют запрограммированные дендритные клетки. «Лихорадка денге вторгается и переформатирует иммунную систему таким образом, что она начинает уничтожать опухолевые клетки», — рассказывает Брюс Лайдей из PrimeVax.
Заразить ослабленных пациентов тропической лихорадкой – казалось бы, рискованный шаг, однако для среднего взрослого человека вероятность умереть от лихорадки денге меньше, чем от обычной простуды, так что это самая безопасная из возможных инфекций. Когда температура спадет, запрограммированные иммунные клетки продолжат сохранять бдительность в отношении опухолевых клеток, если они вновь появятся. «Рак – это движущаяся мишень. В большей части методик его атакуют только с одной стороны, мы же стараемся поставить его раз и навсегда в заведомо проигрышное положение», — говорит Лайдей.
Сложно усомниться в мотивации, движущей разработчиками этого метода лечения. «Наша миссия – воссоздать спонтанную ремиссию максимально стандартным образом», — объясняет коллега Лайдея Тони Чен. Тем не менее, сотрудники PrimeVax подчеркивают, что их идея пока находится на раннем этапе разработки – и, пока не начались клинические испытания, они не знают, как все обернется. Исследователи надеются, что первыми на себе методику опробуют больные меланомой в развитой стадии, это может произойти уже к концу года.
Очевидно, нужно действовать осторожно. Как указывает Ирвайн, «спонтанная ремиссия – лишь крошечная зацепка в огромной сложной головоломке». Но если ученым все-таки удастся одержать победу (что совершенно не факт), то последствия их работы будут колоссальными. Быстрое и относительно безболезненное избавление от рака сейчас считается чудом. Как хотелось бы, чтобы оно стало нормой!
Причина, симптомы, диагностика и лечение
Карциноматоз брюшины — редкая форма рака, поражающая брюшину — тонкую оболочку, окружающую ваши органы брюшной полости. Обнаружить, что он есть у вас или у вашего любимого человека, может быть сложно, а понимание этого рака может помочь вам обрести чувство контроля.
Карциноматоз брюшины чаще всего развивается, когда другие опухоли брюшной полости распространяются на брюшину, приводя к множественным новым опухолям на поверхности этой оболочки. Если у вас карциноматоз брюшины, это обычно означает, что ваш рак брюшной полости находится на поздней стадии.Также очень редки случаи первичного карциноматоза брюшины, который начинается в самой брюшине. Эти случаи обычно случаются у женщин с высоким риском развития рака яичников.
Факторы риска карциноматоза брюшины
Поскольку карциноматоз брюшины чаще всего развивается при распространении существующего рака, основным фактором риска являются другие запущенные формы рака, в том числе:
Первичный карциноматоз брюшины почти всегда встречается у женщин. Помимо пола, к другим факторам риска первичного перитонеального карциноматоза относятся:
Симптомы перитонеального карциноматоза
На ранних стадиях симптомы могут отсутствовать, или у вас могут быть нечеткие симптомы, напоминающие другие состояния.На более поздних стадиях рак вызывает такие симптомы, как:
Эти проблемы могут быть вызваны многими другими причинами.
Карциноматоз брюшины, вызванный раком брюшной полости, может привести к асциту (скоплению жидкости в брюшине), что затем приводит к другим симптомам, таким как:
Как врачи диагностируют перитонеальный карциноматоз
Если врач считает, что у вас перитонеальный карциноматоз, вы можете сделать анализ крови, компьютерную томографию, МРТ или биопсию, чтобы подтвердить это. Иногда карциноматоз брюшины диагностируется во время операции по поводу другого рака, когда хирург замечает опухоль в брюшине.
Лечения перитонеального карциноматоза
Поскольку перитонеальный карциноматоз обычно представляет собой запущенную форму инвазивного рака, который распространился из другой опухоли, его трудно лечить. Большинство опухолей перитонеального карциноматоза не сокращаются в значительной степени или вообще не уменьшаются в ответ на химиотерапию. Из-за этого многие врачи сосредотачиваются на паллиативной помощи, чтобы справиться с симптомами, облегчить боль и улучшить качество вашей жизни. Есть врачи, специализирующиеся на паллиативной помощи, которая предназначена для всех, кто страдает серьезным заболеванием.Уход в хосписе — это вариант, если проблемы с окончанием жизни становятся необходимостью.
В зависимости от вашего конкретного случая могут быть доступны и другие варианты лечения.
- Циторедуктивная хирургия. Хирург удаляет опухоли брюшины и, в некоторых случаях, близлежащих органов брюшной полости.
- Гипертермическая внутрибрюшинная химиотерапия . Этот метод, который часто используется сразу после циторедуктивной хирургии, омывает внутреннюю часть живота, где находится брюшина, нагретыми химиотерапевтическими препаратами, чтобы убить оставшиеся раковые клетки.
- Перитонэктомия — это операция по удалению брюшины.
Карциноматоз брюшины (злокачественная опухоль поверхности брюшины)
Почему мы выбираем нас для лечения карциноматоза брюшины?
Карциноматоз брюшины — это рак, который распространяется на ткани, составляющие слизистую оболочку брюшной полости. Это может быть сложно лечить. В онкологическом центре Mays, где находится онкологический центр UT Health San Antonio MD Anderson, вы можете получить доступ к лучшим вариантам лечения недалеко от дома.
Команда высококвалифицированных онкологических врачей с различными областями знаний сотрудничает, чтобы определить наиболее подходящее лечение для вас.
Наши специалисты проводят специализированное лечение, сочетающее хирургическое вмешательство с химиотерапией. Эта процедура, называемая циторедуктивной хирургией с HIPEC (гипертермическая внутрибрюшинная химиотерапия), требует интенсивного обучения. Мы — один из немногих центров Сан-Антонио, который предлагает это.
Что нужно знать о карциноматозе брюшины
- Карциноматоз брюшины также называют злокачественным новообразованием на поверхности брюшины.Это относится к любому раку, который распространяется в брюшную полость (пространство между внутренними органами в брюшной полости) после развития в другом месте тела (например, в толстой кишке).
- Карциноматоз брюшины отличается от первичного рака брюшины, который возникает в ткани брюшины. Врачи лечат эти два состояния по-разному.
- Карциноматоз брюшины требует участия нескольких специалистов. Наши врачи предлагают индивидуальное обследование и современные методы лечения карциноматоза брюшины.
Как поговорить с врачом о карциноматозе брюшины
Диагноз карциноматоза брюшины может вызвать много вопросов. Вы попали в нужное место. Наша команда имеет опыт лечения этого сложного состояния.
Ваш врач объяснит вам все варианты лечения, включая то, как рак или лечение могут повлиять на вашу жизнь. Мы заботимся о вас и учитываем, что для вас важно, когда даем рекомендации по лечению.
Типы
Многие виды рака могут распространяться в брюшную полость, приводя к перитонеальному карциноматозу.К ним относятся:
Первичный рак брюшины — это раковые клетки, которые возникают в тканях брюшины (клетки, выстилающие брюшную стенку и органы), такие как мезотелиома.
Вы можете спросить своего врача о:
- Возможно, вам понадобится дополнительное обследование , и как тесты помогут составить план лечения
- Стадия рака, включая любые другие области, пораженные раком, и то, что это означает для вашего здоровья
- Варианты лечения, , включая то, являетесь ли вы кандидатом на циторедуктивную операцию (операция по удалению раковых клеток) с HIPEC или без него.
- Клинические испытания, на участие в которых вы можете претендовать , на любом этапе вашего лечения
- Поддержка Услуги , чтобы помочь вам вылечиться после операции или справиться с побочными эффектами лечения
Мы рекомендуем вам включить в свою заботу члена семьи или друга, который вас поддерживает, если это вас утешит.Мы приветствуем вашего специалиста по поддержке на ваших встречах.
Лечение выявленного во время операции карциноматоза брюшины колоректального происхождения с помощью циторедуктивной хирургии и внутрибрюшинной химиотерапии | Всемирный журнал хирургической онкологии
Franko J, Shi Q, Goldman CD, Pockai BA, Nelson GD, Goldberg RM, et al. Лечение колоректального перитонеального карциноматоза с помощью системной химиотерапии: объединенный анализ исследований N9741 и N9841 группы лечения рака Северной Центральной группы III фазы.J Clin Oncol. 2012; 30: 263–7.
Артикул PubMed Google Scholar
Schwartzberg LS, Rivera F, Karthaus M, Fasola G, Canon JL, Hecht JR, et al. ПИК: рандомизированное многоцентровое исследование фазы II панитумумаба плюс модифицированный фторурацил, лейковорин и оксалиплатин (mFOLFOX6) или бевацизумаб плюс mFOLFOX6 у пациентов с ранее нелеченым неоперабельным метастатическим колоректальным раком KRAS экзона 2 дикого типа. J Clin Oncol.2014. 32 (21): 2240–7.
CAS Статья PubMed Google Scholar
Дуйяр Дж., Сиена С., Кэссиди Дж., Табернеро Дж., Беркес Р., Баругель М. и др. Окончательные результаты PRIME: рандомизированное исследование III фазы панитумумаба с FOLFOX4 для лечения первой линии метастатического колоректального рака. Энн Онкол. 2014; 25 (7): 1346–55.
CAS Статья PubMed Google Scholar
Quere P, Facy O, Manfredi S, Jooste V, Faivre J, LEpage C и др. Эпидемиология, лечение и выживаемость перитонеального карциноматоза от колоректального рака: популяционное исследование. Dis Colon Rectum. 2015; 58: 743–52.
CAS Статья PubMed Google Scholar
Sugarbaker PH. Процедуры перитонэктомии. Ann Surg. 1995; 221: 29–42.
CAS Статья PubMed PubMed Central Google Scholar
Жаке П., Sugarbaker PH. Методики клинических исследований в диагностике и стадировании больных карциноматозом брюшины. В: Sugarbaker PH, редактор. Карциноматоз брюшины: принципы лечения. Бостон: Kluwer Academic; 1996. стр. 359–74.
Google Scholar
Jacquet P, Sugarbaker PH. Современные методики клинической оценки пациентов с карциноматозом брюшины. J Exp Clin Cancer Res. 1996; 15: 49–58.
Google Scholar
Thomassen I, van Gestel YR, Lemmens VE, de Hingh IH. Заболеваемость, прогноз и варианты лечения пациентов с синхронным карциноматозом брюшины и метастазами в печень колоректального происхождения. Dis Colon Rectum. 2013; 56: 1373–80.
Артикул PubMed Google Scholar
Chu DZ, Lang NP, Thompson C, Osteen PK, Westbrook KC.Карциноматоз брюшины при негинекологических злокачественных новообразованиях. Проспективное исследование прогностических факторов. Рак. 1989; 63: 364–7.
CAS Статья PubMed Google Scholar
Sadeghi B, Arvieux C, Glehen O, Beaujar AC, Rivoire M, Baulieux J, et al. Карциноматоз брюшины от негинекологических злокачественных новообразований: результаты многоцентрового проспективного исследования EVOCAPE 1. Рак. 2000; 88: 358–63.
CAS Статья PubMed Google Scholar
Элиас Д., Лефевр Дж. Х., Шевалье Дж., Бруже А., Маршал Ф. и др. Полная циторедуктивная операция плюс внутрибрюшинная химиогипертермия оксалиплатином при перитонеальном карциноматозе колоректального происхождения. J Clin Oncol. 2009. 27: 681–5.
Артикул PubMed Google Scholar
Verwaal VJ, Bruin S, Boot H, van Slooten G, van Tinteren H. 8-летнее наблюдение за рандомизированным исследованием: циторедукция и гипертермическая внутрибрюшинная химиотерапия в сравнении с системной химиотерапией у пациентов с перитонеальным карциноматозом колоректального рака.Энн Сург Онкол. 2008; 9: 2426–32.
Артикул Google Scholar
Хуанг К.К., Мин И, Ван Си, Ян XJ, Лю И, Сюн Б. и др. Циторедуктивная хирургия в сочетании с гипертермической внутрибрюшинной химиотерапией улучшает выживаемость при перитонеальном карциноматозе, вызванном колоректальным раком: систематический обзор и метаанализ текущих данных. Oncotarget. 2017; 8: 55657–83.
PubMed PubMed Central Google Scholar
Li Y, Yu Y, Liu Y. Отчет о 9-м международном конгрессе по злокачественным новообразованиям на поверхности брюшины. Cancer Biol Med. 2014; 11: 281–4.
PubMed PubMed Central Google Scholar
Лам Дж. Я., МакКоннелл Ю. Дж., Ривард Дж. Д., Темпл В. Дж., Мак Лос-Анджелес. Гипертермическая внутрибрюшинная химиотерапия + ранняя послеоперационная внутрибрюшинная химиотерапия по сравнению с одной только гипертермической внутрибрюшинной химиотерапией: оценка результатов выживаемости при колоректальном и высокодифференцированном перитонеальном карциноматозе.Am J Surg. 2015; 210 (3): 424–30.
Артикул PubMed Google Scholar
NCCN, «Рак прямой кишки NCCN 2016 v2», 2016.
Google Scholar
Де Бри Э, Купс В., Крёгер Р., Ван Рут С., Виткамп А. Дж., Зётмалдер ФАН. Карциноматоз брюшины от колоректального или аппендикулярного происхождения: корреляция предоперационной КТ с интраоперационными данными и оценка согласия между наблюдателями.J Surg Oncol. 2004. 86: 64–73.
Артикул PubMed Google Scholar
Эскивель Дж., Чуа Т.К., Стоядинович А., Мелеро Дж. Т., Левин Е. А., Гутман М. и др. Точность и клиническая значимость интерпретации компьютерной томографии индекса рака брюшины при колоректальном раке перитонеальный карциноматоз: мультиинституциональное исследование. J Surg Oncol. 2010; 6: 565–70.
Артикул Google Scholar
Марин Д., Каталано С., Баски М. Многодетекторная компьютерная томография с 64 секциями в предоперационной диагностике перитонеального карциноматоза: корреляция с гистопатологическими данными. Визуализация брюшной полости. 2010; 6: 694–700.
Артикул Google Scholar
Кох Дж.Л., Ян Т.Д., Гленн Д., Моррис Д.Л. Оценка предоперационной компьютерной томографии в оценке индекса рака брюшины при колоректальном перитонеальном карциноматозе. Энн Сург Онкол. 2009. 16: 327–33.
Артикул PubMed Google Scholar
van Oudheusden TR, Braam HJ, Nienhuijs SW, Wiezer MJ, van Ramshorst B, Luyer MD, et al. Циторедукция и гипертермическая внутрибрюшинная химиотерапия: возможный и эффективный вариант для пациентов с колоректальным раком после экстренной операции при наличии перитонеального карциноматоза. Энн Сург Онкол. 2014; 21: 2621–6.
PubMed Google Scholar
Chua TC, Yan TD, Saxena A, Morris DL. Следует ли рассматривать лечение перитонеального карциноматоза с помощью циторедуктивной хирургии и гипертермической внутрибрюшинной химиотерапии как высокопатологическую процедуру ?: систематический обзор заболеваемости и смертности. Ann Surg. 2009; 249: 900–7.
Артикул PubMed Google Scholar
Цанда А.Е., Сокмен С., Терзи С., Арслан С., Озтоп И., Карабулут Б. Осложнения и токсичность после циторедуктивной хирургии и гипертермической внутрибрюшинной химиотерапии.Энн Сург Онкол. 2013; 20: 1082–7.
Артикул PubMed Google Scholar
Арслан NC, Сокмен S, Авкан-Огуз V, Obuz F, Canda AE, Terzi C и др. Инфекционные осложнения после циторедуктивной хирургии и гипертермической внутрибрюшинной химиотерапии. Surg Infect. 2017; 18: 157–63.
Артикул Google Scholar
Фрёйснес И.С., Ларсен С.Г., Спасоевич М., Дуэланд С., Флэтмарк К.Полная циторедуктивная хирургия и гипертермическая внутрибрюшинная химиотерапия при колоректальных перитонеальных метастазах в Норвегии: факторы прогноза и онкологические исходы в национальной группе пациентов. J Surg Oncol. 2016; 114: 222–7.
Артикул PubMed Google Scholar
Хармон Р.Л., Шугарбейкер PH. Прогностические показатели при карциноматозе брюшины при раке желудочно-кишечного тракта. Int Semin Surg Oncol. 2005; 2: 3.
Артикул PubMed PubMed Central Google Scholar
Первичная перитонеальная артерия — Фонд борьбы с раком у женщин
Рак возникает, когда клетки в определенной части тела растут ненормальным образом. Первичный рак брюшины (PPC ) — относительно редкий вид рака, который чаще всего развивается у женщин. БПК является близким родственником эпителиального рака яичников, который является наиболее распространенным типом злокачественных новообразований, поражающих яичники. Причина первичного рака брюшины неизвестна, но для женщин важно знать, что возможно иметь первичный рак брюшины, даже если их яичники были удалены.
Брюшная полость и вся поверхность всех органов брюшной полости покрыты блестящей влажной тканью, похожей на целлофан, которая называется брюшиной . Он не только защищает органы брюшной полости, но также поддерживает и предотвращает их прилипание друг к другу, а также позволяет им плавно перемещаться в брюшной полости. Клетки слизистой оболочки брюшины развиваются из клеток того же типа, что и поверхность яичника и маточной трубы. Некоторые клетки брюшины могут трансформироваться в раковые клетки, и когда это происходит, в результате возникает первичный рак брюшины. Это может произойти в любом месте брюшной полости и затронуть поверхность любого содержащегося в ней органа.Он отличается от рака яичников, потому что яичники при ППК обычно лишь в минимальной степени поражены раком.
Рак маточной трубыФаллопиевы трубы — это пара гибких трубчатых структур, которые берут начало в верхней части (дне) матки, где они сообщаются с полостью эндометрия, и идут от матки с обеих сторон к яичникам, где они «хлопают». над яичниками пальцевидным (бахромчатым) концом. Рак маточной трубы также относительно редок и очень тесно связан с раком яичника и ППК.У них много общего, и новые данные даже предполагают, что многие из ранее считавшихся раком яичников действительно могли быть раком маточной трубы (FTC).
Хотя клиническая картина FTC очень похожа на рак яичников и PPC, есть некоторые различия. Рак маточной трубы возникает внутри (просвете) маточной трубы и обычно вызывает ее набухание, как колбасу. Поражение яичника вторично, но обычно настолько обширно, что невозможно сказать, началось ли оно на яичнике и распространилось на маточную трубу или наоборот.Из-за этого многие виды рака маточных труб можно было классифицировать как рак яичников. Когда маточная труба набухает при раке, она производит жидкость, подобную асциту , которая может «просачиваться» обратно в матку и приводить к водянистым выделениям из влагалища, что является классическим проявлением FTC, когда оно связано с образованием придатков.
Признаки PPC и FTC
К сожалению, из-за нечеткого характера признаков PPC и FTC обычно диагностируются на поздних стадиях заболевания, когда лечение затруднено.
Типичные симптомы обоих заболеваний чаще желудочно-кишечные, чем гинекологические, и включают:
- Вздутие живота
- Изменения в работе кишечника
- Раннее чувство сытости после еды
- Вздутие живота, а в тяжелых случаях — тошнота и рвота.
Иногда у пациентов может наблюдаться закупорка кишечника, связанная с опухолью в кишечнике или рядом с ним. Вагинальное кровотечение нечасто наблюдается у пациентов с ППК, но может быть немного чаще у пациентов с ППК.
Медицинское обследование и диагностика
И PTC, и FTC обычно диагностируются, когда женщина обращается к врачу с жалобами на вздутие живота и вздутие живота. Как описано выше, симптомы любого из этих видов рака чаще носят желудочно-кишечный, чем гинекологический характер. Эти симптомы связаны с накоплением жидкости, также известным как асцит, который обычно возникает при любом раке. Желудочно-кишечные симптомы также возникают из-за того, что проростки опухоли часто выстилают перитонеальную поверхность (внешнюю оболочку) кишечника, и этот процесс называется карциноматозом .Сальник , жировая ткань, свисающая от толстой кишки и желудка, часто содержит объемную опухоль, описываемую как слипание сальника. Хотя сальниковые лепешки можно обнаружить при физическом осмотре, они часто неуловимы и их трудно обнаружить. Когда у женщины обнаруживается жидкости в брюшной полости (асцит) , обычным первым шагом к диагностике является компьютерная томография. Это особый вид рентгеновского обследования, который позволяет врачам оценить всю брюшную полость и таз. Обычно наблюдаются спекание сальника и асцит, а также другие опухолевые образования, которые указывают на диагноз PPC, FTC или рака яичников.Другие виды рака могут вызывать эти результаты, поэтому необходимы дальнейшие тесты, которые обычно сосредоточены на исключении других более распространенных видов рака, таких как рак толстой кишки и груди.
Часто оценка асцита начинается с процедуры, известной как парацентез , при которой жидкость удаляется из брюшной полости с помощью иглы. Жидкость исследуют под микроскопом на предмет наличия раковых клеток. К сожалению, эта процедура сопряжена с определенными рисками, так как процесс парацентеза может фактически «засеять» брюшную стенку раковыми клетками.Поэтому при рассмотрении этой процедуры важно проконсультироваться с гинекологом-онкологом, поскольку в этом может быть нет необходимости, учитывая, что большинство пациентов с такими результатами будут подвергаться хирургическому вмешательству независимо от результатов. Однако это может быть полезно для пациента, который либо не является кандидатом на хирургическое вмешательство, либо у пациента с подозрением на асцит по причинам, отличным от рака, например, болезни печени или сердца. Иногда жидкость даже откачивают из-за дискомфорта пациента до того, как можно будет назначить операцию или химиотерапию.
Существует несколько анализов крови, которые часто выполняются при подозрении на КПП или КФК. Самым распространенным из них является анализ крови CA 125 . CA 125 — это химическое вещество, вырабатываемое опухолевыми клетками, и его уровень обычно повышен у пациентов с PPC и FTC. К сожалению, он также может быть повышен при различных доброкачественных состояниях, а также при других формах рака, и, таким образом, повышенный анализ крови на СА 125 не означает, что у пациента рак. В последнее время также можно использовать новый анализ крови, HE4, поскольку он менее вероятно повышен, чем CA 125 при доброкачественных заболеваниях.Вы можете узнать больше о CA 125 в нашей брошюре «Уровни CA 125: ваше руководство».
Фактический диагноз PPC или FTC часто не может быть полностью определен до тех пор, пока женщина не перенесет операцию. Это связано с тем, что клиническая картина любого заболевания очень похожа на эпителиальный рак яичников. PPC, FTC и рак яичников выглядят идентичными под микроскопом. Происхождение первичного рака указывает на характер распространения опухоли и поражение органов брюшной полости.Пациенты с FTC обычно имеют грубое поражение маточных труб с меньшим поражением яичников. Пациенты с ППК обычно имеют нормальные яичники или только поверхностное поражение яичников во время предоперационных визуализационных тестов или во время операции. Однако диагноз может оставаться неопределенным даже после операции.
Хирургическая стадия
Хирургическая стадия рака проводится для полной оценки степени заболевания. Это позволяет принимать решения относительно дополнительной терапии, которая обычно проводится в форме химиотерапии.Хирургическая стадия обычно включает удаление всех видимых заболеваний, а также удаление яичников, маточных труб и матки. Он также может включать удаление сальника, лимфатических узлов и других органов в зависимости от результатов хирургического вмешательства.
Хотя не существует формальной согласованной системы стадий для ППК, поскольку она очень похожа на рак яичников в отношении лечения, состояние опухоли обычно определяется с использованием руководящих принципов, установленных для рака яичников.
Стадии с I по IV описывают, насколько далеко распространилась опухоль.Почти у всех диагностированных пациентов будет стадия III или выше, потому что предупреждающих знаков обычно мало, пока рак не станет широко распространенным. У пациентов с PPC или FTC может быть жидкость вокруг легких, известная как плевральный выпот. Если присутствует выпот, можно удалить немного жидкости для поиска опухолевых клеток. Если в этой жидкости обнаруживаются опухолевые клетки, у пациента болезнь IV стадии.
Побочные эффекты лечения PPC и FTC
И PPC, и FTC лечат так же, как и рак яичников.Чаще всего их лечат хирургическим вмешательством и химиотерапией, лишь в редких случаях используется лучевая терапия. Ваш конкретный план лечения будет зависеть от нескольких факторов, в том числе:
- Стадия и степень рака
- Размер и расположение опухоли
- Ваш возраст и общее состояние здоровья
Все виды лечения рака имеют побочные эффекты. Большинство побочных эффектов можно контролировать или избежать. Лечение может повлиять на неожиданные аспекты вашей жизни, в том числе на вашу работу, дома, интимные отношения и глубоко личные мысли и чувства.
Перед началом лечения важно узнать о возможных побочных эффектах и поговорить с членами вашей терапевтической бригады о своих чувствах или проблемах. Они могут подготовить вас к тому, чего ожидать, и подскажут, о каких побочных эффектах следует им немедленно сообщить. Они также могут помочь вам найти способы справиться с побочными эффектами, которые вы испытываете.
Последующее наблюдение после лечения
После завершения первоначального лечения пациенты с любым из видов рака тщательно наблюдаются с посещениями каждые два-четыре месяца в течение первых трех лет, а затем каждые шесть месяцев в течение следующих двух лет или около того и, в конечном итоге, ежегодно.Во время каждого визита они проходят медицинский осмотр, включая осмотр органов малого таза, тестирование CA 125, и, в зависимости от пациента и ее ситуации, могут проводиться визуализирующие обследования, такие как компьютерная томография, рентгеновские снимки, МРТ или ПЭТ. Если пациенты не диагностированы на ранней стадии, эти виды рака имеют тенденцию со временем рецидивировать. Следовательно, пациентам часто требуется более одного курса химиотерапии, а также могут потребоваться дополнительные хирургические процедуры.
Рецидивирующее заболевание
Рецидивы часто встречаются у пациентов с PPC или FTC, потому что большинство пациентов с любым из них диагностируются, когда они уже находятся на поздних стадиях заболевания.У большинства пациентов сначала наступает ремиссия, но болезнь обычно возвращается через месяцы или годы, когда уровни СА 125 начинают повышаться или при физикальном осмотре или визуализирующих исследованиях обнаруживаются новые образования. К сожалению, прогноз для этого рака неблагоприятный, если он рецидивирует, но более длительная ремиссия до рецидива связана с лучшими шансами на вторую, третью и даже четвертую ремиссию.
Существует несколько вариантов лечения для пациентов, которые рецидивируют, в зависимости от места рецидива, времени после начальной терапии и общего состояния здоровья пациента.Эти варианты включают повторную операцию, повторное лечение той же химиотерапией, которая была назначена изначально, или другим типом агента. В отдельных случаях также может рассматриваться лучевая терапия. Каждый рецидив индивидуален, поэтому их лечение должно быть индивидуальным, исходя из множества факторов, в том числе перечисленных выше. К сожалению, как только рецидив диагностирован, нужно переориентировать цели лечения, чтобы помочь продлить качество жизни, а не лечить.
Программа по борьбе с злокачественными новообразованиями на поверхности брюшины | Johns Hopkins Medicine
Злокачественное новообразование поверхности брюшины, широко известное как перитонеальный карциноматоз, представляет собой рак внутри брюшной полости.Брюшная полость — это пространство между органами в брюшной полости, выстланное брюшиной, которая обычно представляет собой тонкую защитную мембрану. Рак брюшины часто вызывается распространением раковых клеток из ранее существовавшего рака. Наиболее распространенными видами рака, вызывающими карциноматоз брюшины, являются:
Лечение злокачественных новообразований на поверхности брюшины
Воспроизвести видео:Циторедуктивная хирургия и HIPEC
Благодаря недавним достижениям в хирургических методах, теперь мы можем предложить больше вариантов лечения некоторых поздних стадий рака, чем когда-либо прежде.Было показано, что метод, называемый удалением опухоли или циторедуктивной операцией (CRS), и гипертермической внутрибрюшинной химиотерапией (HIPEC) является эффективным вариантом лечения для некоторых пациентов со злокачественными новообразованиями на поверхности брюшины.
Эта сложная хирургическая процедура представляет собой двухэтапный процесс:
- Хирургическое удаление любой видимой опухоли или рака (CRS)
- Доставка нагретых химиотерапевтических препаратов в брюшную полость (HIPEC)
Первая фаза лечения, CRS, включает удаление любых видимых опухолей в брюшной полости, которые могут включать пораженные органы.Объем операции будет зависеть от размера опухоли в брюшной полости. Хирурги тщательно соотносят риски и преимущества удаления органа с вашим лечением рака и общим состоянием здоровья и подробно обсудят это с вами до операции.
Во время второй фазы лечения в брюшной полости циркулирует нагретый химиотерапевтический раствор для лечения любых раковых клеток, которые могут остаться. Комбинация тепла и химиотерапии, проводимая непосредственно в брюшную полость в операционной, считается более эффективной, чем только хирургическое вмешательство для некоторых пациентов с заболеванием брюшины, потому что оно может получить доступ и убить больше раковых клеток, чем можно обнаружить невооруженным глазом.
Недавние исследования показали, что CRS / HIPEC полезен для некоторых пациентов с поздними стадиями рака желудочно-кишечного тракта и рака яичников. Процедура потенциально может продлить жизнь, а также улучшить качество жизни пациентов. Поскольку химиотерапия вводится в виде разовой дозы непосредственно в брюшную полость, традиционных побочных эффектов пероральных или внутривенных химиотерапевтических препаратов можно избежать; однако многим пациентам все еще требуется внутривенная химиотерапия до или после операции.
Качество обслуживания
Многопрофильная группа специалистов в области здравоохранения внимательно изучит ваши медицинские записи и встретится с вами, чтобы определить, может ли эта операция оказаться для вас эффективным лечением.Два фактора имеют решающее значение для успешных результатов: во-первых, тщательный отбор пациентов для определения того, кто может получить наибольшую пользу с наименьшим риском, и, во-вторых, выполнение этой операции профессионалами в загруженном национальном онкологическом центре, таком как больница Джона Хопкинса. имеет опыт лечения сложных онкологических больных.
Насколько инвазивна процедура?
В настоящее время большая часть CRS / HIPEC выполняется через открытый разрез, проходящий от нижней части грудины до лобковой кости.Мы тесно сотрудничаем с нашими коллегами по анестезии, чтобы минимизировать дискомфорт после операции.
Каково время выздоровления пациента с CRS / HIPEC?
В среднем от двух до трех месяцев требуется большинству пациентов, чтобы почувствовать себя нормальным.
Есть ли побочные эффекты от операции?
- Усталость является обычным явлением, когда организм восстанавливается после этой сложной операции и постепенно улучшается с ежедневной активностью и периодами отдыха по мере необходимости.
- С тошнотой можно справиться с помощью лекарств и постепенного перехода от жидкой пищи к твердой.
- Боль купируется с помощью внутривенных или эпидуральных лекарств, а затем и пероральных лекарств для достижения контроля.
- Потеря аппетита — обычное явление, которое постепенно улучшается при частом приеме пищи небольшими порциями.
- Выпадение волос носит временный характер и обычно улучшается при правильном питании и времени.
- Как и во всех крупных хирургических вмешательствах, существуют стандартные риски кровотечения, инфекции и последствий анестезии.Большинство из них незначительны, но некоторым требуется дальнейшее пребывание в больнице для лечения.
- Другие хирургические риски зависят от степени удаления органа и будут обсуждены с вами во время вашего предоперационного визита.
Как долго я буду в больнице?
Будьте готовы пробыть в больнице 10–14 дней. В среднем пациентов выписывают примерно на 8 или 9 день.
Как на меня повлияет химиотерапия?
Одноразовая доза химиотерапии, вводимая в брюшную полость при повышенной температуре, вызывает следующее:- Кишечник временно замедляется
- Изменения в лабораторных результатах, таких как количество лейкоцитов и тромбоцитов
Мы из другого города; где может остаться моя семья?
Найдите информацию о жилых помещениях, предлагающих скидки для пациентов и членов их семей.
Познакомьтесь с нашими экспертами
Наша многопрофильная команда состоит из хирургов, онкологов, врачей-терапевтов, радиологов, анестезиологов, медсестер, диетологов и социальных работников, которые стремятся предоставить комплексный уход, основанный на лучших доказательствах, для улучшения результатов лечения пациентов и качества лечения. жизнь для людей с диагнозом перитонеальный карциноматоз.
Хирургическая онкология
Крапива, Бренда Смит DNP, ACNP-BC
Практикующая медсестра Школа медицины Университета Джона Хопкинса, Балтимор, Мэриленд
Гинекология и акушерство
Медицинская онкология
Радиология
| Научное название | Используемые части Клеточная линия | 4Тип экстракта | Важные соединения | Эффект на клетки | Механизмы | Литература | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vitis vinifera | Фрукты | 703 HCTo116 , проантоцианидины, стильбеноидыПовышение содержания дигидроцерамидов, сфинголипидных медиаторов, участвующих в остановке клеточного цикла, и снижение скорости пролиферации | (i) Повышение p53 и p21 воротников клеточного цикла (ii) Активация транскрипционного фактора Nrf2 | [26, 27]|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фрукты | Caco-2 | 365 мг / г | Метанол | Катехин, эпикатехин, кверцетин, галловая кислота | Антипролиферативная активность 9047 в прямом инициировании гибели 9047 клеток фаза G2 / M | [28, 29] | Семя | Caco-2 | 10–25 μ г / мл | Водный | Процианидины | (i) Увеличенная глубина крипт (ii) Подавление жизнеспособности клеток и снижение баллов гистологического повреждения | Активность МПО (миелопероксидазы) | [29] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кожа | NM | 7.5, 30, 60 μ г / мл | Метанол | 4-геранилоксиферуловая кислота | NM | NM | [30] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Семена | Стволовые клетки рака толстой кишки 25 μ г / мл | NM | (+) — катехин, (-) — эпикатехин | NM | (i) Увеличение p53, соотношение Bax / Bcl-2 и расщепленный PARP (ii ) Ингибирование передачи сигналов Wnt / β -катенина | [31] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Allium sativum | Корень | HT-29 | 20, 50470 9047 мл Ethanolic | NM | Индукция апоптоза и остановки клеточного цикла | (i) Ингибирование пути PI3K̸Akt (ii) Повышение регуляции PTEN и подавление экспрессии Akt и p-Akt | [32] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Глицин макс | Семя | Caco-2, SW620, HT-29 | 12.5 μ г / мл | Водный | Антоксантин | Гибель клеток и значительное снижение плотности клеток | Повышение уровня белка Rab6 | [33] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Семена | HT-29 240 90 , 600 частей на миллион | Сырой | Сапонин | Подавление активации PKC и повышение активности щелочной фосфатазы | [33] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Семя | HT-29 | NM Сапонин | NM | (i) Подавление деградации I κ B α в PMA-стимулированных клетках (ii) Подавление экспрессии COX-2 и PKC | [34] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Camellia sinensis | Лист | HT-29 | 0, 10, 30, 50 μ M | Водный 9047 0 | Катехин, галлат эпигаллокатехина | 1.9-кратное увеличение апоптоза опухолевых клеток и 3-кратное увеличение апоптоза эндотелиальных клеток | (i) Подавление активации ERK-1 и ERK-2 (ii) Подавление экспрессии VEGF | [35] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Лист | Caco-2, HT-29 | 300 μ M | Водный | Теафлавины (TF-2T, F-3, TF-1) | Индукция апоптоза клеток рака толстой кишки человека | Модуляция NF κ B, AP-1, CREB и / или IL-6 | [36] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Лист | HT-29 | 68-80 0.73 μ г / мл | Экстракт горячей воды | Флаван-3-ол (катехин и танин) и полифенолы (чайденол B) | Ингибирование пролиферации клеток HT-29 | Повышенные уровни экспрессии каспаз 3 / 7, 8 и 9 | [35] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Olea europaea | Фрукты | HT-29 | 150, 55,5 200 и 74 4 9070 моль / л Метанол и хлороформ | Маслиновая кислота, олеаноловая кислота | Антипролиферативная активность | (i) Повышение активности, подобной каспазе 3, до 6 раз (ii) Производство супероксид-анионов в митохондриях | [37] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фрукты, листья | SW480 и HT-29 | 100–400 m / z | Метанол и гексан | Олеиновая кислота, линолевая кислота, гамма-линоленовая кислота, лигнаны, флавоноиды, секоиридоиды | Ред. стимулировал рост клеток в обеих клеточных линиях | (i) Ограниченный клеточный цикл G2M (ii) Подавление экспрессии циклооксигеназы-2 в клетках HT-29 (iii) Подавление передачи сигналов β -катенин / TCF в клетках SW480 (iv ) Содействие вступлению в фазу subG1 | [38] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фрукты | Caco-2 | 50 μ M | Водные | Фенольные соединения, аутентичный гидроксилтирозол (HT) Сниженная пролиферация | клеток Caco-2 | Снижение уровней метилирования промотора CNR1 | [39] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фрукты | HT115 | 25 μ г / мл | Гидроэтанольные соединения | феноловые соединения (фенол-гидрофенол этанол, пинорезинол и дигидроксифенилэтанол) | NM | Ингибирование за счет снижения экспрессии в диапазоне α 5 и β 1 | [40] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Olive сточные воды мельниц | HT-29, HCT116, CT26 | NM | Метанол | Гидрокситирозол | (i) Ингибирование пролиферации (ii) Ингибирование миграции и инвазии | (i) Уменьшение образования ростков 905 Уровни VEGF и IL-8 | [41] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фрукты | Caco-2 | 0-2000 μ г / мл | Этанол | Тирозол, гидрокситирозол, олеуропеин, рутин формы лютеолина и апигенина | NM | (i) Индукция остановки клеточного цикла в S-фазе | [42] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punica granatum | Juice | Juice | 50 мг / л | Водный | Эллагитаннины, пуникалагин | Ингибирование пролиферации раковых клеток | (i) Подавление экспрессии TNFR-индуцированного белка COX-2 на (ii) Сниженное фосфорилирование субъединицы p65 и связывание с ответным элементом NF κ B | [43] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Seed | LS174 | 63.2 μ г / мл | Сверхкритическая жидкость | Пуническая кислота, γ -токоферол, α -токоферол | Цитотоксическая активность | (i) Незначительное снижение развития канальцев из удлиненных клеточных тел (ii) ) Уменьшение количества соединений клеток | [44] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Glycyrrhiza glabra | Корень | HT-29 | 12,2 и 31 4 9070 мл 9070 г / л | Ликохалкон | NM | Повышение уровня протеина проапоптозного Bax | [37] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opuntia ficus-indica | 2M | Водный | Беталаиновый пигмент индикаксантин | Апоптоз пролиферирующих клеток | (i) Деметил действие промотора гена-супрессора p16INK4a (ii) Реактивация подавленной экспрессии мРНК и накопление p16INK4a | [38] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Плод | HT-29 и Caco-2 и NIH 3 T3 (в качестве контроля) | Против HT-29 (4.9 мк мкг / мл) против Caco-2 (8,2 мк г / мл) | Щелочной гидролиз с NaOH | Изорамнетиновые гликозиды (IG5 и IG6) -фенол | Гибель клеток через апоптоз и некроз | Повышенная активность каспазы 3/7[45] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Piper betle | Leaf | HT-29 и HCT116 | 200,0 μ г / мл | Hydroxychavicol | Антиоксидантная способность и индукция большего апоптотического эффекта | (i) Активность по очистке (ii) Образование электрофильных метаболитов | [41, 46] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| a | Фрукты | HT-29 | 0.025, 0,05, 0,25, 0,5% | Этанолик | Аскорбат, эллаговая кислота | Снижение пролиферации клеток HT-29 | Повышение уровня 8OHA и снижение уровня 8OHG | [40] | [40] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sasa quelpaertensis | Лист | HT-29 HCT116 | 0, 100, 200, 300 мг / л | Этаноловый | Ингибированная кислота 90, t-Coumaric | Подавление неадгезионного образования сфер CD133 + и CD44 + популяция | [41] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Salvia chinensis | Стебель | 80HCT116, COLO 205, 20470 мг / л | Полифенольные | Терпеноиды, фенольная кислота, флавоноиды, дибензилциклооктадиен | Апоптоз и потеря митохондриальной мембраны | Инд. вызванный клеточный цикл G0 / G1 | [42] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rubus idaeus L . | Фрукты | HT-29, HT-115, Caco-2 | 3,125, 6,25, 12,5, 25, 50 мг / л | Ацетат | Полифенол, антоцианин, эллагитаннин | NM | клеток в фазе G1[47] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LoVo | 50 μ L | Водный | NM | Подавление пролиферации LoVo | Подавление пути NF | [κ 48] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Curcuma longa | Корень | HT-29, HCT15, DLD1, HCT116 | (i) Краткосрочный анализ: четыре 10-кратных разведения (от 100 до 0.1 мг / л) (ii) Долгосрочный анализ: 5, 10, 20 мг / л | Этаноловый | Куркумин (диферулоилметан) | Ингибирование образования сфероидов HCT116 | NM | [49] | 9047||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eleutherococcus senticosus | Корень | HCT116 | 12,5, 25, 50, 100 NM | Метанольные | Клетки-киллеры | Eleutritins4703 Клетки природного таким образом, усиление иммунной функции[50] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tabernaemontana divaricata L . | Лист | HT-29, HCT15 | 10, 30, 100 мг / л | Этилацетат, хлороформ, метанол | Алкалоиды | NM | Ингибирует раскручивание суперспиральной ДНК | [904] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Millingtonia hortensis | Корень, цветок, лист | RKO | 50, 100, 200, 400, 800 мг / л | Водный гликозид-гликозид | , 2-фенилрутинозид | Индукция апоптоза | (i) Увеличение фрагментированной ДНК (ii) Снижение экспрессии антиапоптотических белков, Bcl-xL и p-BAD | [46] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Порошок | 200, 400, 800 μ г / мл | Водные | Водорастворимые соединения | Антипролиферативный эффект | NM | [51] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Тайский пурпурный рис | Семян | Caco-2, Cat.No. HTB-37 | 16,11 мк г / мл | Подкисленный метанолом | Цианидин-3-глюкозид и пеонидин-3-глюкозид, антоцианы, фенольные соединения | (i) Антиоксидирование антоцианов (фенол). ii) Антипролиферация клеток рака толстой кишки | NM | [52] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Annona muricata | Leaf | HCT116, HT-29 | 4 ацетогенины, эфирные масла | Блокировка миграции и инвазии клеток HT-29 и HCT116 | (i) Остановка клеточного цикла в фазе G1 (ii) Нарушение MMP, утечка и активация цитохрома c | [53] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NM | HT-29, HCT116 | <4, <20 μ г / мл | EtOAc | Аннопентоцин A, аннопентоцин B, аннопентоцин C, цис- и трансанномурический in-D-ones, анномурицин E | NM | Подавление продукции АТФ и НАДН-оксидазы в раковых клетках | [54] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pistacia lentiscus L. вар. чиа | Лист | HCT116 | NM | Этанол | Смола, известная как мастичная камедь Chios (CMG) | Вызывает несколько морфологических изменений, характерных для апоптоза клеточных органелл 3 (i) Индукция | остановка в фазе G1[55] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Смола | HCT116 | 100 μ г / мл | Гексан | Карио Индукция апоптоза аноикис-формы в клетках HCT116 рака толстой кишки человека | (i) Индукция остановки фазы G1 (ii) Потеря адгезии к субстрату | [56] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| American gin (Panax quinquefolius) | Биологические компоненты | HCT116 | 0-2.0 мг / мл | Водный | Женьшень (GE) или его гинзенозид (GF) и полисахарид (PS) | Пролиферация ингибировалась GE, GF и PS в клетках дикого типа и p21 | (i) Клетки останавливают фазу G0 / G1 и увеличивают количество белков p53 и p21 (ii) Увеличение экспрессии белков Bax и каспазы 3 | [57] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Картофель с пурпурной мякотью | Фрукты | Стволовые клетки рака толстой кишки | 5.0 μ г / мл | Этанол, метанол, этилацетат | Антоцианин, β -катенин, цитохром c | Критический регулятор пролиферации CSC и его нижестоящих белков (c-Myc и циклин D1) и повышенный Bax и цитохром c | (i) Уровни цитохрома c были повышены независимо от статуса p53 (ii) Опосредованный митохондриями апоптотический путь (iii) Подавленные уровни цитоплазматического и ядерного β -катенина | [58] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phaseolus vulgaris | Leaf | HT-29 | NM | Этанол | Полисахариды, олигосахариды | 3участвуют в цикле или связаны с | изменениями в генах i70, связанных с | фосфопротеин ретинобластомы[5 9] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opuntia spp. | Фрукты | HT-29 | ,, () | Водно-спиртовые | Бетацианины, флавоноиды (производные изорамнетина) и фенольные кислоты (феруловая кислота) | NM | Индуцированные контрольные точки клеточного цикла , G2 / M и S | [60] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Suillus luteus | NM | HCT15 | 400 μ г / мл | коричная кислота, α -токоферол, β -токоферол, маннит, трегалоза, полиненасыщенные жирные кислоты, мононенасыщенные жирные кислоты, насыщенные жирные кислоты | (i) Повышение клеточных уровней p-h3A.X, который указывает на повреждение ДНК | (i) Ингибирование пролиферации клеток в фазе G1 (ii) Повышение клеточных уровней p-h3A.X | [61] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poncirus trifoliata | Лист | HT-29 | 0,63 μ M | Водный (в ацетоне) | β -ситостерин, 2-гидрокси-1,2,3-пропантрикарбоновая кислота 2-пропантрикарбоновая кислота сложный эфир | Остановка роста клеток наблюдалась с β -ситостерином | NM | [62] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rosmarinus officinalis L. | Leaf | SW 620, DLD-1 | 0-120 μ г / мл | Метанол | Полифенолы | Антипролиферативный эффект 5-FU | , подавление TYMS1 и ферментов TYMS Стойкость к 5-ФУ | [63] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Лист | HT-29 | SC-RE 30 μ г / мл и CA 12,5 μ г / мл | Этанол | Полифенолы (карнозные) кислота (CA) и карнозол) | (i) Повышающая регуляция гена VLDLR как основного фактора наблюдаемого накопления холестерина в обработанных SC-RE клетках (ii) Подавление нескольких генов, участвующих в G1-S | Активация Nrf2 фактор транскрипции и общие регуляторы, такие как ген XBP1 (Xbp1), связанный с развернутым белковым ответом (UPR) | [64] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NM | HT-29 | 10, 20, 30, 40, 50, 60 , 70 мкм г / мл | 90 473 NMКарнозиновая кислота, карнозол, розмариновая кислота, розманол | NM | NM | [65] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Leaf | HGUE-C-1, HT-2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| HGUE-C-1, HT-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CO2-сверхкритический жидкий экстракт | Карнозиновая кислота, карнозол и бетулиновая кислота | NM | (i) Прооксидантная способность за счет увеличения внутриклеточной генерации ROS (ii) Активация Nrf2 | [66 ] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Glehnia littoralis | Leaf | HT-29 | 50 мг / мл | Метанол | Бергаптен фальксин, изоимантопин | Бергаптен фальксин, изоимантопин | Индуцированный апоптоз за счет снижения экспрессии антиапоптотической мРНК Bcl-2 | (i) Пониженная экспрессия Bcl-2 (ii) Пониженные уровни экспрессии iNOS и COX-2 | [67] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вербена лекарственная | Лист | HCT116 | 20 мг / мл | Водный — | -диацетаноид-о-овертиозид фенилэтаноид-гликозид, диацетаноид-о-овертиозид и диацетил-O-бетониозид A | (i) Существенная ингибирующая активность опухолевых клеток (ii) Зависящая от времени цитотоксичность в отношении обеих клеточных линий | (i) Повышенная липофильность молекул, по-видимому, ответственна за повышенную цитотоксичность (ii) ) Антипролиферативная активность определяется количеством ацетильных групп, а также их положением в алифатических кольцах | [68] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mentha spicata | Leaf | RCM-1 | .5 μ г / млN-гексан | 3-метилтиопропиловый эфир уксусной кислоты (AMTP), этиловый эфир метилтиопропионовой кислоты (MTPE) | Проявляет антимутагенную активность | Аураптен, обладающий монотерпеновый фрагмент и β -криптоксантин (один из тетратерпенов) увеличивали продукцию антител | [69] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Euphoria longana Lam. | Семя | SW 480 | 0–100 μ г / мл | Этанол | Корилагин, галловая кислота, эллаговая кислота | (i) Антиангиогенетические свойства (ii) Все фракции проявили антиангиогенные свойства. Активность секреции VEGF | Высвобождение и экспрессия VEGF показали, что все фракции проявляли активность секреции против VEGF | [70] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sutherlandia frutescens | Цветок | 1 / 50 разбавление этанольного экстрактаЭтанол | Аминокислоты, включая L-аргинин и L-канаванин, пинитол, флавоноиды и тритерпеноидные сапонины, а также гексадекановую кислоту и γ -ситостерин | молекулы в пути PI3K, тем самым вызывая апоптоз | Снижение жизнеспособности клеток и увеличение пикноза, а также потеря клеточного m целостность эмбрана | [71] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Melissa officinalis | Лист | HT-29, T84 | 346, 120 мк г / мл | P | (розмариновая кислота, кумаровая кислота, кофейная кислота, протокатеховая кислота, феруловая кислота, хлорогеновая кислота), флавоноиды, сесквитерпены, монотерпены, тритерпены (i) Подавление пролиферации клеток карциномы толстой кишки (ii) Индуцированный апоптоз | (i) Остановка клеточного цикла G2 / M (ii) Расщепление каспаз 3 и 7 (iii) Индуцированная экстернализация фосфатидилсерина в клетках карциномы толстой кишки (iv) Индуцированное образование ROS в клетках карциномы толстой кишки | [72] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sargassum cristaefolium | Лист | HT-29 | 500 мг / мл | Этанол | 9 0473 Fucoidans (i) Уменьшение свободных радикалов (ii) Улавливание радикалов DPPH | Накопление клеток в фазе G0 / G1 | [73] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hedyotis | HT-29 | 400 мг / мл | Этанол, затем ДМСО | Октадецил (E) -p-кумарат, PE-метоксикоричная кислота, феруловая кислота, скополетин, янтарная кислота, ацетат аурантиамида, 470 | рубиадин | Подавляет рост опухолевых клеток и индуцирует апоптоз клеток CRC человека | (i) Блокирует прогрессирование G1 / S (ii) Вызывает активацию каспаз 9 и 3 (iii) Подавляет IL-6-опосредованную активацию STAT3 (iv) Снижение уровня экспрессии мРНК и белка циклина D1, CDK4, Bcl-1 и Bax | [74] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Zingiber officinale Roscoe | Peel | LoVo 00 мг / мл | Этанол | Метиловый эфир линолевой кислоты, α -зингиберен и зингиберон | Интересная антипролиферативная активность против колоректальной карциномы | NM | [75] | 470468 Scutellaria barbataЛист | LoVo | 413.3 мг / л | Метанол | Скутеллареин, скутелларин, картамидин, изокартамидин, вогонин | Вызывают гибель клеток линии клеток рака толстой кишки человека | Увеличение фазы суб-G1 и ингибирование роста клеток | [76] ] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pistacia atlantica, Pistacia lentiscus | Смола | HCT116 | 100 μ г / мл | гексановый экстракт гексана клетки рака толстой кишки человека HCT116 | (i) Вызывают остановку фазы G1 (ii) Потеря адгезии к субстрату | [56] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Citrus reticulata | Кожура | 100 μ г / мл | Метанол | Лимонен, гераниаль, нераль, геранилацетат, гераниол, β -кариофиллен, нерол, нерилацетат | Вызывают апоптоз SNU-C4, раковые клетки толстой кишки человека | Экспрессия проапоптотического гена Bax и главного гена апоптоза каспазы 3 | [77] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 904 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Echinacea pallida, Echinacea angustifolia, Echinacea purpurea | Корень | COLO320 | 150 мг / мл | Гексановая кислота 3 дериватизирующая кислота, полинакфосфамиды | , полициклические соединения, полициклические кислоты фрагментация | (i) Стимулирование апоптоза за счет увеличения активности каспазы 3/7 (ii) Стимулирование фрагментации ядерной ДНК | [78] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nasturtium officinale | Leaf-50 мк л / мл | Метанол | Фенэтилизотиоцианат, 7-мет. гилсульфинилгептил, 8-метилсульфинил | (i) Ингибирование инициации, пролиферации и метастазирования | (i) Ингибирование повреждений ДНК (ii) Накопление клеток в S-фазе клеточного цикла | [79] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Полисифония | NM | SW480, HCT15, HCT116, DLD-1 | 20 и 40 мк г / мл | Метанол | 2,5-Дибром-дибром н-пропиловый эфир | Потенциально можно использовать в качестве химиопрофилактического агента против рака толстой кишки | (i) Ингибированный путь Wnt / β -катенин (ii) Подавленный CRT в клетках рака толстой кишки (iii) Подавленный циклин D1 ( iv) Активировал путь NF κ B | [80] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aristolochia debilis Sieb.et Zucc. | Стебель | HT-29 | 200 μ г / мл | Метаноловая | Аристолоховая кислота, нитрофенантренкарбоновые кислоты | Ингибирование пролиферации и индукция апоптоза (апоптоз | клеток HT-2947) Индукция клеточного цикла суб-G1[81] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Myrtaceae | Лист | HCT116 | 100 μ г / мл (in vitro), 200 и 100 μ г / диск ( in vivo ) | Метанол | Фенолы, флавоноид | , бетулиновая кислотаСильное подавление разрастания микрососудов | (i) Подавление образования трубок на матриксе матригеля (ii) Подавление миграции HUVECS ( in vitro ) (iii) Снижение количества питательных веществ и кислорода pply | [82] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spica prunellae | Leaf | HT-29 | 200 мг / мл ( in vitro ), 600 мг / мл () in vivo | Этанол | Розмариновая кислота | Подавляет рост клеток CRC | (i) Подавляет фосфорилирование STAT3 (ii) Регулирует экспрессию Bcl-2, Bax, циклина D1, CDK4, VEGF-A и VEGFR | [83] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phytolacca americana | Корень | HCT116 | 3200 μ г / мл | квинфероновые кислоты Этаноловые кислоты | глюкозид, изокверцитрин, феруловая кислота | Контроль роста и распространения раковых клеток | Снижение экспрессии MYC, PLAU и TEK | [84] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Morus alba | Лист | HCT15 | 13.8 μ г / мл | Метанол | Эпикатехин, мирицетин, кверцетин гидрат, лютеолин, кемпферол, аскорбиновая кислота, галловая кислота, пеларгонидин, п-кумаровая кислота | Цитотоксическое действие на раковые клетки толстой кишки человека | (i) Индукция апоптоза также участвует в подавлении активности iNOS (ii) Фрагментация ДНК (iii) Повышение активности каспазы 3 | [85] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rhodiola Rhodiola imbricata | HT-29 | 200 μ г / мл | Ацетон и метанол | Фенолы, дубильные вещества и флавоноиды | (i) Антиоксидантная активность (ii) Подавление пролиферации клеток HT-293 ( i) Улавливание свободных радикалов (ii) Активность улавливания радикалов DPPH (iii) Повышенная активность хелатирования металлов | [86] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Сушеный A. radix | HCT116 | 20 мг / мл | Ethanolic | Азаринин и ксантоксилол | Ингибирование роста клеток HCT116 | (i) Casptosis-зависимый 905 Регуляция экспрессии р53 на уровне транскрипции | [87] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Podocarpus elatus | Фрукты | HT-29 | 500 мг / мл | 470 Метанол и метанол | 470 | Снижение пролиферации клеток рака толстой кишки | (i) Задержка клеточного цикла в S-фазе (ii) Подавление теломеразной активности на 93% и уменьшение длины теломер (iii) Вызванные морфологические изменения клеток HT-29 | [88 ] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Эхинацея пурпурная | Цветок | Caco-2, HCT116 | 90 473 0–2000 мг / млГидроэтанол | Цикориевая кислота | (i) Ингибирование пролиферации (ii) Снижение активности теломеразы в клетках HCT116 | (i) Снижение активности теломеразы (ii) Активация теломеразы (ii) 9 (iii) Расщепление PARP (iv) Подавление β -катенина | [89] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Корень | COLO320 | 150 мг / мл | алкилгексановая кислота | 9047 полиацетилены, полисахаридыВызывают апоптоз за счет значительного увеличения активности каспазы 3/7 и способствуют фрагментации ядерной ДНК | (i) Значительно повышают активность каспазы 3/7 (ii) Способствуют фрагментации ядерной ДНК | [78] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Хмель (Humulus lupulus L.), Franseria artemisioides | Лист | NM | 100 мг / кг массы тела / день | Водный | Кумарин, лигнаны, хиноны | 30% снижение индуцированной опухолью неоваскуляризации | NM | NM | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NM | Caco-2 | NM | Ethanolic | Фенольные соединения, флавоноиды, дитерпены | Пищеварительная, гастропротекторная, антисептическая, противовоспалительная и антипролиферативная активность | 70|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фрукты | NL-17 | 0, 50, 100, 150 μ г / мл | Метанол | α -Мангостин (ксантон) | NM | (i) Индукция 3 и активация каспазы 9 (ii) Индуцированная остановка клеточного цикла в фазе G1 / G0 | [92] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стебель, кора | HT-29 | 50 μ г / м L | Растворимый в хлороформе | β -Мангостин, гарцинон D, кратоксиксантон | Цитотоксическая активность против рака толстой кишки человека HT-29 | Ингибирование активации p50 и p65 | [93] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Annona squamosa Linn | Лист | HCT116 | 8.98 мк г / мл | Неочищенный водный этилацетат | Ацетогенины (анноретикуин и изоанноретикуин) и алкалоиды дофамин, сальсолинол и коклаурин | Ингибирование роста и пролиферации кислородно-активных видов опухолевых клеток | (АФК), высвобождение лактатдегидрогеназы (ЛДГ) (ii) Активация каспаз 3/7, 8 и 9 | [94] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Derris scandens | Стержень | HT -29 | 5-15 μ г / мл | Этанолик | Бензилы и изофлавоны (генистеин, кумарины, скандинон) | Апоптоз и митотическая катастрофа рака толстой кишки человека HT-29 клеток | (i) α -глюкозидазная активность (ii) Улавливание свободных радикалов | [95] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eupatorium cannabinum | Ae риальные части | HT-29 | 25 μ г / мл | Этаноловый | Пирролизидиновые алкалоиды (сенеционин, сенкиркин, монокроталин, эхимидин) | Индуцированная морфология колонии | (индуцированное изменение морфологии | ) подавление NCL, FOS и AURKA[96] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 904or99 Sorgh | Дермальный слой стебля | HCT116 и стволовые клетки рака толстой кишки | > 16 и 103 μ г / мл | Этанол, богатый фенолами, ацетон | Апигенинидин и лютеолинидин | 3Противопролиферативное средство | -зависимые и p53-независимые пути | [97] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кожная и семенная головка | CCSC | NM 9047 0 | Метанол | Апигенинидин, лютеолинидин, мальвидин-3-О-глюкозид, апигенин, лютеолин, нарингенин, нарингенин-7-О-глюкозид, эриодиктиол-5-глюкозид, таксифолин, катехины | NM | NM | 3/7 активность[98] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hibiscus cannabinus | Семена | HCT116 | KSE (15.625 μ г / мл до 1000 μ г / мл) | Этанол | Галловая кислота, пара-гидроксибензойная кислота, кофейная кислота, ванилиновая кислота, сиринговая кислота, пара-кумаровая и феруловая кислоты | Цитотоксичность активность против клеток рака толстой кишки человека HCT116 | Апоптоз через блокаду перехода от середины G1 к позднему G1-S, вызывая остановку клеточного цикла фазы G1 | [99] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Salix aegyptiaca L. | Кора | HCT116 & HT-29 | 300 μ г / мл | Этанол | Катехин, салицин, катехол и небольшие количества галловой кислоты, эпигаллокатехин галлат, кумариновая кислота (EGCG) , сиринговая кислота и ванилин | Антиканцерогенные эффекты в раковых клетках толстой кишки | Апоптоз посредством ингибирования фосфатидилинозитол-3-киназы / протеинкиназы B и сигнальных путей митоген-активируемой протеинкиназы | [100] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фрукты | HT-29 | 400 μ г / мл | Водные | Полифенолы, галловая кислота, сангина | Индуцирование апоптоза | индуцированной активности каспина (i) 7 и 9 (ii) Расщепление поли (аденозиндифосфат-рибоза) полимеразы | [101] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Codonopsis lanceolata | Корень | HT-29 | 200 μ г / мл | Фракция N-бутанола | Таннины, сапонины, полифенолы, алкалоиды HT-29 в опухолевых клетках толстой кишки человека Apop | (i) Индуцированная остановка G0 / G1 (ii) Повышение экспрессии каспазы 3 и p53 и отношения Bax / Bcl-2 | [102] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gleditsia sinensis Gleditsia sinensis | Thorn | HCT116 | 800 μ г / мл | Водный | Флавоноид, люпиновая кислота, гликозиды эллаговой кислоты | (i) Повышение уровня p53 (ii) Подавление контрольной точки цикла B , Cdc2 и Cdc25c | Ингибирование пролиферации клеток рака толстой кишки | [90] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thorn | HCT116 | 600 μ г / мл | Et hanolic | NM | Ингибирующий эффект на пролиферацию клеток HCT116 рака толстой кишки человека | (i) Вызвал остановку клеточного цикла в фазе G2 / M вместе с уменьшением циклина B1 и Cdc2 (ii) Переход от фазы G2 / M | [91] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ligustrum lucidum | Фрукты | DLD-1 | 50 мк г / мл | Орсоловая кислота | Орсоловая кислота | 70 | Кислота водная пролиферация | (i) Уменьшение Tbx3 спасло дисрегулируемую передачу сигналов P14ARF-P53 | [94] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Zingiber officinale | HCT11 Этанолик | 6-парадол, 6- и 10-дегидрогингердион, 6- и 10-гингердион, 4-, 6-, 8- и 10-имбирдиол, 6-метилгингердиол, зингерон, 6-гидроксишогаол, 6-, 8-, 10-дегидрошогаол, диарилгептаноиды | Ингибирующее действие на пролиферацию клеток рака толстой кишки человека | (i) Задержка в фазе G0 / G1 (ii) Снижение синтеза ДНК | [103] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grifola frondosa | Фрукты | HT-29 | 10 нг / мл | Водный | Фенольные соединения (пирогалл3 кислоты, протоциклиновая кислота, кофеиновая кислота) TNBS-индуцированного колита крыс | Индуцированное развитие клеточного цикла в фазе G0 / G1 | [104] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cucumaria frondosa | Ферментативно гидролизованный эпителий 9070 47113 150 μ г / мл | Водно-спиртовой | Моносульфатированный тритерпеноидный гликозид фрондозид А, дисульфатный гликозидный лист осид B, трисульфатный гликозид фрондозид C | Ингибирование роста клеток рака толстой кишки человека | (i) Ингибирование в фазах S и G2-M с уменьшением Cdc25c и увеличением p21WAF1 / CIP (ii) Апоптоз, связанный с фосфорилированием h3AX и каспаза 2 | [105] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rolandra fruticosa | Лист и ветки | HT-29 | 10 и 5 мг / кг / день | Methanpenolic (13-ацетоксироландролид)Антипролиферативное действие против раковых клеток толстой кишки человека | Ингибирование пути NF κ B, NF κ B субъединицы p65 (RelA), медиаторов IKK β и онкогенных | K-ras [106]|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cydonia oblonga Miller | Листья и плоды | Caco-2 | 250–500 μ г / мл | Метанольное соединение | Фенольное соединение (флавонол и гетерозиды флавонов, 5-O-кофеилхиновая кислота) | Антипролиферативное действие против клеток рака почки и толстой кишки человека | (i) Подавление активации фактора, ядерного фактора-kB (NF κ B) активация, фактор транскрипции протеина-1 (AP-1), митоген-протеинкиназы (MAPK), протеинкиназы (PK), а именно PKC, пути, опосредованные рецептором фактора роста (GFR-), и ангиогенез ( ii) Остановка клеточного цикла и индукция апоптоза, антиоксидантные и противовоспалительные эффекты | [107] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Morchella esculenta | Фрукты | HT-29 820470 мг / 9047 мг / | Метиленхлорид | Стероиды (в основном производные эргостерина), полисахариды и галактоманнан | Антиоксидантная активность в раковых клетках толстой кишки HT-29 | Ингибирование NF-B activ в анализе NF-B | [108] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sedum kamtschaticum | Воздушная часть | HT-29 | 0–0.5 мг / мл | Метанол | Буддлеясапонин IV | Индуцированный апоптоз в клетках рака толстой кишки человека HT-29 | Индукция апоптоза через митохондриальный путь путем подавления уровней белка Bcl-2, активации каспазы 3 и последующей активации каспазы 3 | [109] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Женьшень и Glycyrrhiza glabra | Leaf | HT-29 | 500 μ μ L | 9047- денин U водный 9047- денин глицирретиновая кислота, квиритинNM | Определение антипролиферативного эффекта уровней белка p21, циклина D1, PCNA и cdk-2, которые являются ключевыми регуляторами развития клеточного цикла | [110] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Orostachys japonicus | Лист и стебель | HT-29 | 2 мг / мл | Водный 9050 0 | Флавоноиды, тритерпеноиды, 4-гидроксибензойная кислота, 3,4-дигидроксибензойная кислота, полисахарид | Антипролиферация в клетках рака толстой кишки HT-29 | Подавление пролиферации в точке G2 клеточного цикла и апоптоза посредством белка-супрессора опухоли | p53 [111]|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Гинкго двулопастный | Фрукты и листья | HT-29 | 20–320 мг / л | Водные | лактоны лактона и терпена 473 лактона 47 (терпен) Ингибирование прогрессирования клеток рака толстой кишки человека (ii) Индуцированный апоптоз клеток HT-29 | Повышение активности каспазы 3 и повышение MRN p53 снижение мРНК Bcl-2 | [112] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oryza sativa | Seed | HT-29, SW 480, HCEC | 100 μ г / мл | Этилацетат | Фенольное соединение (трицин, феруловая кислота, кофейная кислота и метоксикоричная кислота) | Ингибирование роста клеток рака толстой кишки человека | (i) Индуцированный апоптоз за счет повышенной активации каспаз 8 и 3 (ii) Уменьшение количества жизнеспособных Клетки SW480 и HCEC (iii) Снижение колониеобразующей способности этих клеток | [113] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cnidium officinale Makino | Корень | HT-29 | .024 / мл | Этанолик | Остхол, аураптенол, императорин | Подавление пролиферации клеток рака толстой кишки человека (HT-29) | Ингибирование клеточной пролиферации через остановку фазы G0 / G1 клеточного цикла и индуцированный апоптоз | [114] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cnidium officinale Makino | Корень | HT-29 | 0,1-5 мг / мл | Водный | 3 бензил N- ) ацетамидинПодавляет инвазивность клеток HT-29, обработанных цитокинами, через мембрану, покрытую матригелем, в зависимости от концентрации | (i) Снижение инвазии клеток HT-29 через Matrigel (ii) Подавление опосредованной цитокинами Продукция NO, экспрессия iNOS и инвазивность клеток HT-29 (iii) Ингибирование активности MMP-2 | [115] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Длинный пепел per (PLX) | Fruit | HT-29 и HCT116 | 0.10 мг / мл | Этанол | Пиперидиновые алкалоиды, пиперамиды, пиперлонгумин | (i) Индукция апоптоза после фрагментации ДНК в клетках рака толстой кишки HT-29 в зависимости от времени (ii) Индуцированная независимая от каспазы апоптоз | Индуцированная продукция АФК цельными клетками | [116] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Achyranthes aspera | Корень | COLO 205/ | 50-100 мл и мл Этанольный (EAA) и водный (AAA) экстракты корней Водный | Фенольные соединения | (i) Усиленное ингибирующее действие AAA на клетки COLO 205 по сравнению с EAA (ii) Стимулирующая роль AAA в активация ингибиторов клеточного цикла | (i) Запуск митохондриального апоптоза и остановка клеточного цикла в S-фазе (ii) Повышенные уровни каспазы 9, каспазы 3 и каспы se 3/7 активность | [117] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Тимус обыкновенный | Лист | HCT116 | 0.2, 0,4, 0,6, 0,8 мг / мл | Карвакрол и тимол | Подавление пролиферации, адгезии, миграции и инвазии раковых клеток | [118] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NM | SW480 | 40 μ г / мл | Этаноловый | Циклозонарон бензохинон | NM | Индуцирует апоптоз за счет снижения уровня Bcl-2 и нарушения регуляции Bcl-2 мембраны. к активации каспаз 3 и 9 | [119] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dendrobium microspermae | NM | HCT116 | 0.25, 0,5, 1,0 мг / мл | Метанол | NM | NM | Повышающая регуляция Bax и каспаз 9 и 3 и подавление экспрессии генов Bcl-2 | [120] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cannabis sativa | Сухие цветы и листья | DLD-1 и HCT116 | 0,3–5 μ M | Метанол | Каннабидиол, чувствительность к фитоканнабиноидам | 11 в клетках с пониженным содержанием CB70473 a (i) Уменьшение AOM-индуцированных предопухолевых поражений и полипов[121] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phoenix dactylifera L. | Фрукты | Како-2 | 0,2 мг / мл | Водные | Фенольные кислоты (галловая, протокатеховая, гидроксибензойная, ванилиновая, изованилиновая, сиринговая, кофейная, феруловая, синаповая, п-кумароидная) гликозиды (кверцетин, лютеолин, апигенин и кемпферол) и антоцианидины | Повышение роста полезных бактерий и ингибирование пролиферации клеток рака толстой кишки | NM | [122] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фрукты | SW480, CT26 | 0, 10, 20, 30, 40, 50 μ г / мл | Этанол | Тритерпеноиды, флавоноиды, полисахариды, лимоноиды | NM i | пролиферация SW480 и CT26 путем стимулирования апоптоза, на что указывает конденсация ядерного хроматина и фрагментация ДНК[123] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Crocus sativus L. | Цветок | HCT116 | 0,25, 0,5, 1, 2, 4 μ г / мл | Этанолик | Каротиноид, пигмент, кроцин, кроцетин | Индуцированное повреждение ДНК и апоптоз | зависимой от паттерна p53 активации каспазы 3 с полной остановкой G2 / M[124] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Листочки околоцветника и лист | Caco-2 | 0.42 мг / мл | NM | Полифенолы, гликозиды кемпферола, лютеолина и кверцетина | Пролиферация клеток Caco-2 была сильно ингибирована | NM | [125] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Luffa echinata | Фрукты | HT-29 | 50, 100 и 200 μ г / мл | Метанол | Амариин, эхинатин, сапонины, гентриаконтан, гипсогенин, кукурбитин 90 O — β -D-глюкопиранозилкукурбитацин B и 2- O — β -D-глюкопиранозилкукурбитацин S | Увеличение популяции апоптотических клеток | (i) Ингибирует клеточную пролиферацию HT- 29 через остановку фазы G2 / M клеточного цикла (ii) Индуцированная апоптотическая гибель клеток через образование ROS (iii) Накопление транскриптов каспазы 3 клеток HT-29 | [126] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vitis aestivalis hybrid | Фрукты (вино) | CCD-18Co | 25, 50, 100 μ г / мл | NM | Полифенолы | Снижение полифенолов | Экспрессия мРНК липополисахаридных (LPS-) медиаторов воспаления NF κ B, ICAM-1, VCAM-1 и PECAM-1 (ii) Повышенная экспрессия miR-126 (iii) Снижение экспрессии генов и снижение активации фактора транскрипции NF κ B, NF κ B-зависимый (iv) Снижение ROS 113MAH | [127] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Xylopia aethiopica | Dried30, 5, 10, 15, 20, 25, 30 μ г / мл | Этаноловый | Ent-15-оксокаур-16-ен-19-овая кислота (EOKA) | NM | (i) Индуцированное повреждение ДНК, остановка клеточного цикла в фазе G1 и апоптот гибель ic-клеток | [128] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Сорго | Зерно | ER- β ; незлокачественные колоноциты молодых взрослых мышей | 1, 5, 10, 100 мк мкг / мл | Водные | Флавоны (лютеолин и апигенин), 3-дезоксиантоцианы, нарингенин (эриодиктиол и нарингенин целлюлозы), уменьшенный за счет роста апоптоза | Повышенная активность каспазы 3 | [129] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NM | HT-29, HCT116 | 0.9-2,0 мг / мл | Гидроэтанол | Процианидин B1, дельфинидин-3-O-глюкозид, танин, цианидин-3-O глюкозид | (i) Значительно задержанные клетки HT-29 в G1 (ii) Наивысшее ингибирование роста (iii) Повышенный процент апоптотических клеток | (i) Подавление апоптотических белков, таких как cIAP-2, ливин, сурвивин и XIAP, наблюдалось в клетках HCT116 (ii) Ингибирование тирозинкиназы | [ 130] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Panax notoginseng (Burk.) FH Chen | Корень | LoVo и Caco-2 | 0, 100, 250 и 500 мк г / мл | Спиртовой | Сапонин, гинзенозид | NM | Задержка прогрессирования Фазы клеточного цикла G0 / G1, S или G2 / M | [131] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brassica oleracea L. var. italica | Соцветия брокколи | HCT116 | 0, 1, 2.5, 5, 10 μ г / мл | Этанол | Глюкойберин, 3 гидрокси, 4 ( αxylopyranosyranosyranosy) бензилглюкозинолат 4-винил-3-пиразолидинон 4- (метилсульфинил), бутилтиомочевина, β -тиоглюкозид N-гидроксисульфаты | NM | NM | [132] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Высушенный стебель | SW480 | In vivo: 0.4 г / кг / день In vitro: 100 μ г / мл | Водный | Полисахариды, фенилэтаноидные гликозиды | (i) Уменьшение количества гиперплазии слизистой оболочки и кишечной инфекции хеликобактерами (ii) макрофагов селезенки, NK-клеток и макрофагов селезенки | Снижение частоты гиперплазии и инфекции Helicobacter hepaticus кишечника | [133] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 и HT-29 | 10, 25, 50, 75, 100, 125, 150 μ M CE | NM | Процианидины | NM | NM | [134] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prunus mume | Fruit | SW480, COLO и WiDr | 150, 300 и 600 μ г / мл | Гидрофобный 90 500 | Тритерпеноидные сапонины | NM | (i) Подавление роста и лизирование SW480, COLO и WiDr (ii) Индукция массивных цитоплазматических вакуолей | [135] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sol | NM | COLO 205 | 50, 100, 200, 300, 400 μ г / мл | EtOH | β -Lycotetraosyl | Индуцированная остановка S-фазы и апопсед3 (i) | Фрагменты ДНК[136] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Onopordum cynarocephalum | Воздушные части | HCT116, HT-29 | 0, 0.04, 0,12, 0,2, 0,4, 1,2 мг / мл 0, 0,2, 0,4, 1,2, 2,0, 3,0 мг / мл | Водные | Флавоноиды, лигнаны и сесквитерпеновые лактоны | NM | (i) Увеличение в экспрессии проапоптотических белков, таких как p53, p21 и Bax (ii) Ингибирование антиапоптотического белка Bcl-2 (iii) Снижение уровня белка циклина D1 | [137] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eleutherine palmifolia | Луковицы | SW480 | 2.5, 5, 10 мк мкг / мл | MeOH | Элеутерин, изоэлейтерин | NM | (i) Подавляет транскрипцию TCF / β -катенин (ii) Снижение уровня ядерных β -катенин белок | [138] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Спаржа лекарственная | Спирс | HCT116 | 76 мк | г / мл | -1, HTSAP-2, HTSAP-12, HTSAP-6, HTSAP-8)NM | (i) Ингибирование фосфорилирования Akt, p70S6K и ERK (ii) Индукция активности каспазы 3, расщепление PARP-1 , Фрагментация ДНК, остановка клеточного цикла G0 / G1 за счет снижения экспрессии циклинов D, A и E | [139] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phyllanthus emblica L. | Семя, мякоть | HCCSC, HCT116 | 200 μ г / мл | Метанол | Тригонеллин, нарингин, кемпферол, эмбинин, катехин, изоцерамнетин 905 ) Индуцированный апоптоз, независимый от свойства стволовости p53 (в HCCSC) (iii) Антипролиферативные свойства | (i) Подавление клеточной пролиферации и экспрессии c-Myc и циклина D1 (ii) Индуцированный внутренний путь передачи сигналов митохондрий апоптоза | 140473 [||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Красный виноград | NM | HT-29, HCT116 | 0.9-2,0 мг / мл | Гидроэтанол | Гликозиды дельфинидина, производные кверцетина, дельфинидин-3-O-глюкозид (высокий), цианидин-3-O-глюкозид | (i) Максимальное подавление роста (ii) Повышенное процент апоптотических клеток | (i) Подавление апоптотических белков, таких как cIAP-2, ливин, сурвивин и XIAP (ii) Ингибирование тирозинкиназы | [130] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Черная чечевица | NM | HT-29, HCT116 | 0.9-2,0 мг / мл | Гидроэтанол | Гликозиды дельфинидина, процианидин B1, дельфинидин-3-O-глюкозид (высокий), цианидин-3-O-глюкозид | (i) Значительно задержанные клетки HT-29 в G1 (ii) Максимальное подавление роста (iii) Повышенное процентное содержание апоптотических клеток | (i) Подавление апоптотических белков, таких как cIAP-2, ливин, сурвивин и XIAP (ii) Подавление тирозинкиназы | [130 ] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Graptopetalum paraguayense | Leaf | Caco-2, BV-2 | 0.2, 0,4, 0,6, 0,8, 1,0 мг / мл | Гидроэтанол | Щавелевая кислота, гидроксибутандиовая кислота, галловая кислота, кверцетин, глюканы хлорогеновой кислоты с фукозой, ксилозой, рибозой (GW100) арабино-рамногалактаны | 100E473 (i) Большой потенциал в области антипролиферации (i) Удаление α , α -дифенил- β -пикрилгидразильные радикалы (DPPH) (GW100E преуспел в улавливании DPPH), радикалы 2,2-азино-бис [3-этилбензотиазолин-6-сульфоновая кислота] (ABTS), супероксид-анионы (O2) (GW100) (ii) Значительное ингибирование фактора некроза опухоли-a (TNF-a), поглощая ABTS и O2 | [141] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Butea monosperma | Цветок | SW480 | 200 мл | Цветочный | н-бутанол | 9 0473 Значительный антипролиферативный эффект (i) Значительное подавление экспрессии сигнальных белков Wnt, таких как β -катенин, APC, GSK-3 β , циклин D1 и c-Myc (ii) Повышенный внутриклеточный уровень ROS | [142] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Инвазия Rehmannia glutinosa | NM | CT26 | 5, 20, 80 μ M | pol Рост катетера | клеток рака толстой кишки | (i) Подавление экспрессии белков MMP-2 и MMP-9 (ii) Снижение секреции ангиогенных маркеров | [143] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Telectadium Bark4703 | HCT116 | 1.5, 2,0 мк мкг / мл | Экстракт MeOH | 4-дикаффеоилхиновая кислота, кверцетин 3-рутинозид, периплоцин | NM | (i) Ингибирование эффектов β- катенин / TCF на транскрипционную активность Wnt / β -катенин (ii) Подавление экспрессии генов-мишеней Wnt | [144] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gloriosa superba | Корень | SW620 мл | SW620 | Экстракт белкового гидролизата | Белковый гидролизат | NM | (i) Повышенная регуляция p53 (ii) Понижающая регуляция NF κ B | [145] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Смола | HT-29 | 100, 150 μ г | Метанол | Босвеллиевая кислота | Снижение жизнеспособности клеток | (i) Снижение экспрессии mPGES-1, VEGF, CXCR4, MMP-2, MMP-9, HIF-1, PGE2 (ii) Повышение активности каспазы 3 (iii) Ингибирование миграции клеток и прорастания сосудов формация | [146] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Typhonium flagelliforme | Лист | WiDr | 70 мк г / мл | изоид G470 NM | Ингибирование экспрессии ЦОГ-2 | [28] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Diospyros kaki | Фрукты | HT-29 | 2,000 μ | г / мл Экстракт | Полифенол | Нарушение пролиферации и инвазии клеток | NM | [147] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Carpobrotus edulis 90 470 | Лист | HCT116 | 1000 мг / мл | Гидроэтанол | Галловая кислота, кверцетин, синаповая кислота, феруловая кислота, 7-о-глюкозид лютеолина, гиперозид, изокверцитрин, изорллагамицин кислота | Ингибирование пролиферации | (i) Обладание высокой активностью по поглощению DPPH и эффективной способностью связывать железо (ii) Ингибирование радикала NO, перекисного окисления линолевой кислоты, гликирования белка и окислительного повреждения | [148] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Piper methysticum | Корень | HT-29 | 10, 20, 30, 40, 50 μ г / мл | Водный | 11-гидрокси-12k-метаинокси, 11- гидрокси-12k-метаинокси, 11- гидрокси-12k-метаинокси гидрокси-12-метоксидигидрокаваин, пренилкафеат, пиностробин халкон, 11-метокситетрагидроянгонин, аваин, метистицин, дигидрометистицин, 5,6,7,8-тетрагидроянгонин, каваин, 7,8-дигидрокаваин, янгонин, десметоксиянгонин, флавокааин B | Подавляет рост | NM | [26] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Salvia baltiflora | Наземные надземные части7 | .76 мк г / мл | Экстракт хлороформа, промытый гексаном | 19-дезоксиицетексон, 7,20-дигидроанастомозин, айтексон, 19-дезоксиизоицетексон | Цитотоксическая активность | NM | [ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tinospora cordifolia | Стебель | HCT116 | 1, 10, 30, 50 μ M | Гидроалкогольный, ситоловый | Клеродан, фурано-дитерпенефурано-глинозем β , 3 β : 15,16-диэпокси-4 α , 6 β -дигидрокси-13 (16), 14-клеродадиен-17,12: 18,1-диолид | Индуцированная конденсация хроматина и фрагментация ядер небольшого числа клеток | (i) Значительная потеря ММП (ii) Снижение функции митохондрий (iii) Повышение цитохрома c в цитозоле (iv) Индуцированные ROS / окислительный стресс (v) Повышенная аутофагия | 904 73 [150]|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Euterpe oleracea | Фрукты | NM | 35 μ г / мл | Гидроэтаноловая кислота | Ваниновая кислота | Ориент. (i) Способность к улавливанию ROO и HOCl (ii) Ингибирование образования нитрозосоединений | [151] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Salvia miltiorrhiza | NM | 7099 HCTolicДитерпенхинон | NM | Пониженные уровни прокаспаз 3 и 9 | [152] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кофе | Зерна | млмг Водный | Комплекс хлорогеновой кислоты (CGA7) | NM | (i) Фрагментация ДНК, расщепление PARP-1 vage, активация каспазы 9, подавление Bcl-2 и усиление Bax | [153] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Illicium verum | Фрукты | HCT116 | 10 мг | Кверцетин галловой кислоты | Индукция апоптоза и ингибирование ключевых стадий метастазирования | NM | [154] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 90 NM469 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Garcinia propinqua 9047 9047 9047 Leaf Экстракт Ch3Cl2 | Бензофеноны, ксантоны и ксантоны в клетках | Сильная ингибирующая цитотоксичность | NM | [155] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стебель, кора | HCT116 14470 9047.23, 23.95 μ M | MeOH, CH 2 Cl 2 , и экстракт EtOAc | Ксерофенон A, доитунггарциноны A и B, самсонион, 7 β -H-11-бензоил-5 α -идрокси-6,10-тетраметил-1- (3-метил-2-бутенил) тетрациклотетрадекан-2,12,14-трион, гиперсампсон M, ассигуксантон A (кадраксантон Q), 40 10-O-метилмаклураксантон ( 16), 41- и 5-О-метилксантон V1 | NM | NM | [156] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Malus pumila Miller cv.Annurca | Фрукты | Caco-2 | 400 мг / л | Метанол | Хлорогеновая кислота, (+) катехин, (-) эпикатехин, изокверцетин, рутин, флоридзин, B2704, процианидин | , процианидин 9047 Ингибиторы WNT и снижение активности WNT, вызванное WNT5A | NM | [157] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Malus domestica cv. Limoncella | Фрукты | Caco-2 | 400 мг / л | Метанол | Хлорогеновая кислота, (+) катехин, (-) эпикатехин, изокверцетин, рутин, флоридзин, флоридзин | , процианидзин | , процианидзин | Ингибиторы WNT и снижение активности WNT, вызванное WNT5A | NM | [157] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Coix lacryma-jobi var. ma-yuen | Лист | HCT116 | 0,5, 1 мг / мл | Водный | Коиксспиролактам A, коиксспиролактам B, коиксспиролактам C, коикслактам 90-3, 3-диоксиндол 9047 , инвазия и адгезия посредством репрессии путей ERK1 / 2 и Akt в условиях гипоксии | [158] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mesua ferrea | Стебель, кора | HCT116, 3.3, 6,6 и 11,8 μ г / мл | NM | Фракции ( α -амирин, SF-3, n-Hex) | Подавление промотора множественных опухолей | Повышение регуляции p53, Myc / Max и TGF- β сигнальные пути | [159] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Taraxacum | Корень | SGC7901, BGC823 | 70 мл70 3 9047 мл70 3 | NM | Пролиферация и миграция за счет нацеливания lncRNA-CCAT1 | [160] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Portulaca oleracea | Leaf | HT-29 CSCs.25 μ мкг / мл | Алкогольный | Щавелевая, яблочная кислота | NM | Подавление экспрессии Notch2 и β -катениновых генов, регуляторных генов и генов-мишеней, которые опосредуют путь передачи сигнала Notch | [ 161] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hordeum vulgare L. | NM | HT-29 | NM | Водный раствор и сок | Белок, витамины, витамины B, ниаак B , марганец, фосфор, углеводы | (i) Подавление пролиферации раковых клеток (ii) Цитотоксическая активность | Активность по улавливанию свободных радикалов | [162] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Paraconiothyrium sp. | NM | COLO 205 и KM12 | 12,5 μ M | Метилэтилкетоновый экстракт | н-гексан, CH 2 Cl 2 , фракции EtOAc и -DOH (AOAc и -DOH) | (i) Активность ингибирования роста (ii) Антипролиферативное действие | NM | [163] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mentha × piperita | Leaf | 30, 40, 50 μ мкг / мл | Водные | Полифенолы | NM | Подавление репликации ДНК и транскрипции РНК, которые индуцируют АФК | [164] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mammea longifolia Planch.и Triana | Fruit | SW480 | 25, 50, 100 μ г / мл | Метанол | NM | NM | Апоптоз, связанный с митохондриями, и активация p53 165470 904 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rollinia mucosa (Jacq.) Baill. | NM | HCT116, SW-480 | <4, <20 μ г / мл | EtOH | Роллитацин, хименезин, мембранацин, дезацетилварицин, лахеррадурин | 9047 Активность 9047 54] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Annona diversifolia Saff. | NM | SW-480 | 0,5 μ г / мл | NM | Черимолин-2 | Цитотоксическая активность | NM | [54] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| purpurea Moc. & Sessé ex Dunal | NM | HT-29 | 1,47 μ г / мл | CHCl 3 -MeOH | Purpurediolin, пурпуренин, анноглауцин | 3, активность аннонацина 904 A 904[54] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Viguiera decurrens (A.Серый) A. Серый | NM | NM | 3,6 μ г / мл | Hex; EtOAc; МеОН | β -ситостерин-3-O- β -D-глюкопиранозид; β -D-глюкопиранозил олеанолат; β -ситостерин-3-O- β -D-глюкопиранозид и олеаноловая кислота-3-O-метил- β -D-глюкуронопиранозид роноат | Цитотоксическая активность | NM | [54] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Helianthella quinquenervis (крючок.) A. Серый | NM | HT-29 | 2-10 μ г / мл | NM | Деметиленсекалин | Цитотоксическая активность | NM | [54] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Smallanthus maculatus (Cav.) Х. Роб. | NM | HCT15 | <20 μ г / мл | Ацетон | Фракция F-4, фракция F-5, урсоловая кислота | Цитотоксическая активность | NM | 3 [|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bursera fagaroides (Kunth) Engl. | NM | HF6 | 1,8 × 10 -4 от до 2,80 μ г / мл | Водно-спиртовой | Подофиллотоксин, β -пельтатин-A β-метиловый эфир , 5- 9099 -пельтатин-A метиловый эфир, десметокси-ятеин, дезоксиподофиллотоксин, бурсеранин, ацетилподофиллотоксин | NM | (i) Ингибитор микротрубочек (ii) Способность останавливать клеточный цикл в метафазе | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Калина jucundum C.V. Morton | NM | HCT15 | <20 μ г / мл | Ацетон | Урсоловая кислота | Цитотоксическая активность | NM | [54] | Hemiangium excelsum (Kunth) ACSm.NM | HCT15 | <10 ( μ г / мл) | MeOH | PE, EtOAc, MeOH | Цитотоксическая активность | NM | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| [54] | ||||||||||
| Hyptis pectinata (L.) Пуа. | NM | Col2 | <4, <20 μ г / мл | NM | Пектинолид A, пектинолид B, пектинолид C, α -пирон, боронолид, деацетилепиол | активность 904 | NM | [54] | ||
| H. verticillata Jacq. | NM | Col2 | <4, <20 μ г / мл | NM | Дегидро- β -пельтатин, метиловый эфир дибензилбутиролактон, (-) — ятеин, 4-деметил-470-дезоксиподид Неспецифическая цитотоксическая активность | NM | [54] | |||
| H.suaveolens (L.) | NM | HF6 | 2,8-12 μ г / мл | Хлороформ и бутанол | β -Апопикроподофиллин | Неспецифическая цитозная активность 5470473 | ||||
| Salvia leucantha Cav. | Лист, корень, стебель | HF6, HT-29, HCT15 | 14,9, 12,7, 9,9 μ г / мл | CHCl 3 | NM | Цитотоксическая активность | [54]||||
| Vitex trifolia L. | NM | HCT15 | От 3,5 до <1 ( μ г / мл) | Гексан и дихлорметан | Сальвилеукалин B, Hex: лист, Hex: стержень, DCM: лист, DCM: стержень | 9047 Цитотоксическая активностьNM | [54] | |||
| Persea americana Mill. | NM | HT-29 | <4 μ г / мл и <20 μ г / мл | Этанол | 1,2,4-тригидроксинонадекан, 1,2,4-тригидроксигептадек -16-ен, 1,2,4-тригидроксигептадец-16-ин | Цитотоксическая активность | NM | [54] | ||
| Linum scabrellum | Корни, корни | 0.2, 0,5, 2,3 μ г / мл | Хлороформ и бутанол | DCM: MeOH, 6MPTOXPTOX | NM | (i) Индукция остановки клеточного цикла в G2 / M (ii) Ингибирование полимеризации тубулина | [54] | |||
| Phoradendron reichenbachianum (Seem.) Oliv. | NM | HCT15 | 3,6, 3,9 и 4,3 μ г / мл | NM | Мороновая кислота | Цитотоксическая активность | NM | [54] | ||
| NM | HCT15 | 18,70 μ г / мл | Ацетон | NM | Цитотоксическая инактивность | NM | [54] | 81|||
| NM | HCT15 | 0,63, 0,50, 1,99 μ г / мл | EtOH, MeOH, водный | NM | Цитотоксическая активность | NM | [54] | |||
| Mimulus glabratus Kunth | NM | HF6 | 12.64 μ г / мл | MeOH | NM | Цитотоксическая активность | NM | [54] | ||
| Picramnia antidesma Sw. | NM | HCT15 | от 0,6 до 4,5 μ M | NM | 10-эпиувеозид, увеозид, пикрамниозид E, пикрамниозид D | Цитотоксическая активность | NM | |||
| Penstemon barbatus (Cav.) Roth | NM | HF6 | 15,19 μ г / мл | МеОН | NM | Цитотоксическая активность | NM | [54] | ||
| NM | HF6 | 6,74 μ г / мл | МеОН | NM | Цитотоксическая активность | NM | [54] | |||
| NM | HF6 | 0,169 и 1,46 мк г / мл | МеОН | NM | Цитотоксическая активность | NM | [54] | |||
| NM | HCT116, SW-480, SW-620 | NM | NM | 13-гидрокси-10-оксо-транс-11-октадеценовая кислота | Цитотоксическая активность | NM | [54 ] | |||
| Colubrina macrocarpa (Cav.) G. Don | NM | HCT15 | 10, 2,1, 9,1 μ г / мл | PE, EtOAc, MeOH | NM | Цитотоксическая активность | NM | 3 [54]|||
| Coix lacryma-jobi | Семя, эндосперм и оболочка | HT-29 | 0,1–1,000 мк г / мл | Метанол | Метанол | гексан 9047 стигмастерин и β -ситостерол), гамма-линоленовая кислота (GLA), арахидоновая кислота (AA), эйкозапентаеновая кислота (EPA) и докозагексаеновая кислота (DHA), линолевая кислотаNM | Пути передачи сигналов (i) которые включают мембранные фосфолипиды (ii) Повышение выработки АФК и снижение антиоксидантной способности клеток | [166] | ||
| Abutilon indicum | Lea f | HT-29 | 210 μ г / мл | Водные | Флавоноиды (4H-пиран-4-он, 2,3-дигидро-3,5-дигидрокси-6-метил, 2- этокси-4-винилфенол, N, N-диметилглицин, lup-20 (29) -ен-3-он, линоленин, метиловый эфир 1-моно-, 9-гексадекановой кислоты, метиловый эфир линоленовой кислоты), фенол (аминокислоты, терпеноиды, жирные кислоты, метилпальмитолеат) | NM | (i) Повышение уровней активных форм кислорода и одновременное снижение клеточного антиоксиданта, потеря митохондриальной мембраны, повреждение ДНК и остановка клеточного цикла в фазе G1 / S | [167 ] | ||
| Галла Ройс | NM | HCT116, HT-29 | 12.5, 25, 50, 100, 200 μ г / мл | Водный с процессом обработки паром | Галлотаннины | Повышенное содержание галловой кислоты и эллаговой кислоты | (i) Вызванный апоптоз за счет активации каспаз 3, 8, 9 (ii) Модулированная активация митогена и протеинкиназ, p38 и c-Jun Nh3-концевой киназы | [168] | ||
| Artemisia annua Linné | Порошок HC3 HC3 | 20, 30, 40, 60, 80, 100 μ г / мл | Ethanolic | Фенольные соединения | Ингибирование жизнеспособности клеток и повышенное высвобождение ЛДГ | (i) Сигнал PTEN / p53 / PDK1 / Akt пути через PTEN / p53 вызывают апоптоз (ii) Увеличение апоптотических телец, активация каспаз 3 и 7 (iii) Регулируемая транслокация цитохрома c в цитоплазму и транслокация Bax на митохондриальную мембрану | [169] 9 0470 | |||
| Тычинка Nelumbo nucifera | Порошок | HCT116 | 100, 200, 400 μ НМ / мл | 3 Неочищенный этанол 9047 9047 (Неочищенный этанол 9047) 9047 Повышение популяции суб-G1, уровни мРНК каспаз 3 и 8, уровни I κ B α и каспазы 9 (ii) Модуляция экспрессии мРНК семейства Bcl-2 (iii) Снижение уровней мРНК NF κ B | [170] | |||||
| Кукурузный шелк | NM | LoVo, HCT116 | 1.25, 2,5, 5, 10, 20 μ г / мл | Водный | Белки, полисахариды, флавоноиды, витамины, дубильные вещества, алкалоиды, минеральные соли, стероиды | NM | (i) Увеличение Bax , цитохром с, каспазы 3 и 9 уровней | [171] | ||
| Lycium barbarum L. | Порошок | HT-29 | 1, 2, 3, 4, 5 | 1, 2, 3, 4, 5 | 1, 2, 3, 4, 5 г / мл | NM | Неоксантин, полностью транс- β -криптоксантин, полисахариды, каротиноиды, флавоноиды | NM | (i) Повышение регуляции экспрессии p53 и p21K2) ( , Экспрессия CDK1, циклина A и циклина B (iii) Задержка в фазе G2 / M клеточного цикла | [172] |
| Chrysobalanus icaco L. | Сублимированные фрукты | HT-29 | 1, 2.5, 5, 10, 20 μ г / мл | Неочищенный этилацетат | Дельфинидин, цианидин, петунидин и пеонидин | NM | (i) Повышенная внутриклеточная продукция ROS (ii) Снижение TNF- α , IL-1 β , IL-6 и NF κ Выражения B1 | [173] | ||
| Zanthoxylum piperitum De Candolle | Fruit | Caco-2, DLD-1 | 200 μ г / мл | Водный | NM | NM | (i) Повышенная концентрация c- N-концевая киназа Jun (JNK) | [174] | ||
| Celtis aetnensis (Tornab.) Strobl (Ulmaceae) | Веточки | Caco-2 | 5, 50, 100, 250 или 500 μ г / мл | Метанол | Флавоноиды и тритерпеновые соединения | NM | ) Повышение уровней ROS[175] | |||
| Rosa canina | Кожура и мякоть | Caco-2 | 62,5, 125, 250, 500 мк г / мл | Общий экстракт (фракция 1), витамин C (фракция 2), нейтральные полифенолы (фракция 3) и кислые полифенолы (фракция 4) | Полифенолы | Снижение производства активных форм кислорода (АФК) | NM | [176] | ||
| Rhazya stricta | Leaf | HCT116 | и | г / см 2 | Сырой алкалоид | Алкалоиды | NM | (i) Подавление ДНК-связывающей и транскрипционной активности белков NF κ B и AP-1 (ii) Увеличение Bax, каспаз 3/7 и 9, уровни p53, p21 и Nrf-2 (iii) Снижение экспрессии ERK MAPK, Bcl-2, циклина D1, CDK-4, сурвивина и VEGF | [177] | |
| Зеленый кофе | NM | Caco-2 | 10-1,000 μ г / мл | NM | 5-кофеоилхиновая кислота (5-CQA), 3,5-дикаффеоилхиновая кислота (3,5 -DCQA), феруловая кислота (FA), кофейная кислота (CA), дигидрокафеиновая кислота (DHCA), дигидроферуловая кислота (DHFA) | Снижение жизнеспособности раковых клеток | NM | [178] | ||
| Flourensia microphylla | Лист | HT-29 | NM | Этанол и ацетон | Фенольные соединения | NM | (i) Ингибирование IL-8 (ii) Активация апоптоза увеличением отношения Bax / Bcl-2 и экспрессии семейства TNF | [179 ] | ||
Истина, лежащая в основе трех естественных «лекарств» от рака
Сводка
Такие методы лечения, как иглоукалывание и массаж, могут быть полезным дополнением к обычным методам лечения рака.Но «панацеи», которые утверждают, что исключают болезнь естественным путем, не работают — и на самом деле могут быть опасны для людей, больных раком.
Особенности
- Дополнительные методы лечения могут использоваться в качестве дополнения к основному лечению рака.
- Но использование недоказанных лекарств может быть вредным для больных раком.
- Также не было показано, что они работают.
- Некоторые из них могут снизить эффективность лечения.
- Традиционные методы лечения более успешны и менее разрушительны, чем когда-либо.
Интернет полон «чудодейственных лекарств» от рака и якобы верных способов его предотвращения, и благонамеренные люди могут призывать больных раком просто попробовать их в надежде избавиться от болезни.Некоторые пациенты, обеспокоенные тем, что обычные методы лечения не работают или вызывают серьезные побочные эффекты, обращаются за лечением, эффективность которого на самом деле не подтверждается научными данными или даже может оказаться опасным. Понятно, что во времена неуверенности и беспокойства любая надежда на излечение, даже если оно не доказано с медицинской точки зрения, является соблазнительной.
«Пациенты хотят чего-то« естественного », чтобы попытаться вылечить свой рак или предотвратить его повторное появление», — говорит фармацевт и травник из Memorial Sloan Kettering К.Саймон Юнг. «Но люди, продвигающие эти методы лечения, не обязательно имеют медицинское или онкологическое образование. Кроме того, пациенты, которые пробуют эти методы лечения, могут обнаружить, когда они вернутся за обычным лечением, что уже слишком поздно и их рак уже распространился ».
Доктор Юнг — менеджер базы данных About Herbs, созданной и поддерживаемой службой интегративной медицины MSK. Служба предоставляет дополнительные методы лечения, такие как иглоукалывание, музыкальная терапия и массаж, которые используются в дополнение, а не в качестве альтернативы основным методам лечения рака, таким как химиотерапия, лучевая терапия и хирургия.
Здесь доктор Юнг объясняет шумиху и научные данные, окружающие три широко известных, но недоказанных метода лечения: масло каннабиса, лаэтрил и диета с изменением pH (также известная как щелочная).
Масло каннабиса
Шумиха: Масло каннабиса часто называют средством для уничтожения или уменьшения раковых опухолей, а также лекарством от диабета, язв, артрита, мигрени, бессонницы, инфекций и многих других заболеваний. Также называется маслом марихуаны или маслом конопли, оно извлекается из растений марихуаны, часто с более высокой долей соединения, известного как CBD (каннабидиол), которое имеет меньший психоактивный эффект, чем более известное соединение THC (тетрагидроканнабинол), которое вызывает у потребителей марихуаны .
Масло каннабиса доступно в нескольких формах с разной активностью. Его можно вливать в кулинарное масло, которое пользователи брызгают под язык или смешивают с едой. Его пары также можно вдыхать. Согласно федеральному закону, продукты каннабиса являются незаконными, хотя несколько штатов приняли законы, легализующие их медицинское использование.
Доказательства: Хотя коммерчески доступные соединения каннабиса одобрены FDA для уменьшения побочных эффектов, связанных с лечением рака, таких как тошнота и рвота, и для улучшения аппетита, никакие клинические испытания не показали, что продукты каннабиса могут лечить рак.
Утверждения о том, что масло каннабиса лечит рак, являются анекдотическими и в значительной степени неподтвержденными, основываясь на скудных исследованиях, проведенных на мышах и в лабораториях. Побочные эффекты могут включать потерю памяти и внимания. Возможно, наиболее важным является то, что есть доказательства того, что соединения каннабиса могут ингибировать ферменты, которые необходимы пациентам для метаболизма других противоопухолевых препаратов, тем самым увеличивая их токсичность или снижая их эффективность.
Вердикт: «Пока нет исследований на людях, которые показывают, что масло каннабиса можно использовать для лечения рака», — сказал доктор.Юнг говорит. «Пациенты, употребляющие марихуану или любую другую форму марихуаны, должны сообщить об этом своим врачам, чтобы они могли дать вам правильный совет».
Вернуться наверхЛаэтрил
Шумиха: Лаэтрил, впервые популяризированный в качестве средства для лечения рака в России и США более века назад, является торговым названием очищенной формы амигдалина, экстракта, полученного из косточек абрикоса, некоторых орехов и растений. Кишечные ферменты расщепляют лаэтрил с образованием цианида, который, как утверждают сторонники, убивает раковые клетки и оставляет здоровые ткани невредимыми.Некоторые также утверждают, что Лаэтрил на самом деле является витамином B-17, и его дефицит может вызвать определенные виды рака. Запрещенная в США оральная форма лаэтрила доступна в других странах.
Доказательства: Лаэтрил действительно распадается на цианид, но яд не только избирательно поражает раковые клетки — он также может вызывать заболевание или убивать пациентов. Клинические исследования, проведенные в 1970-х и 1980-х годах, в том числе спонсируемые Национальным институтом здравоохранения, показали, что лаэтрил не уменьшал размер или рост злокачественных опухолей, но некоторые пациенты испытали отравление цианидом.
Вердикт: «Эффективность лаэтрила против рака не доказана, и он даже может быть опасен для некоторых пациентов», — говорит д-р Йунг. «Если амигдалин в конечном итоге будет использоваться в противораковом препарате, он должен быть в другой форме, потому что пероральная форма токсична и слишком опасна для использования».
Вернуться наверхУправление уровнем pH с помощью диеты
Шумиха: Основываясь на научном наблюдении, что раковые клетки процветают в кислой среде, то есть с низким уровнем pH, некоторые люди утверждают, что очень «кислые» продукты, такие как мясо, сыр и зерновые продукты, повышают риск рака за счет снижения Уровни pH в крови.Они утверждают, что употребление в пищу «щелочных» продуктов, таких как фрукты, зеленые овощи и другие продукты растительного происхождения, препятствует росту раковых клеток за счет повышения уровня pH в крови и рекламируют преимущества щелочной диеты (также известной как щелочная зольная диета или щелочная диета. кислая диета).
Доказательства: Раковые клетки создают кислую микросреду из-за высокой скорости метаболизма. Раковые клетки не могут жить в сильно щелочной среде, как и здоровые клетки. Ваше тело работает над тем, чтобы поддерживать постоянный уровень pH, и изменение диеты не приведет к существенному изменению уровня pH в крови, который жестко регулируется почками и легкими независимо от потребляемой пищи.
pH жидкостей организма, таких как слюна и моча, временно изменяется в зависимости от продуктов, которые вы едите, но это не влияет на уровень pH в крови (или, следовательно, на среду раковых клеток в организме). Фактически, любое значительное отклонение уровня pH в крови может вызвать серьезные, даже опасные для жизни состояния, известные как ацидоз (низкий pH) или алкалоз (высокий pH).
Вердикт: «Нет никаких доказательств того, что изменение вашей диеты изменит Уровень pH влияет на рост рака », — сказал д-р.Юнг говорит. «Фактическая наука была неправильно истолкована. Изменение pH в слюне не означает изменения pH в крови. Некоторые пациенты пытаются использовать химические вещества, чтобы изменить pH крови, но это может быть чрезвычайно опасно ».
Вернуться наверхИтог
«Естественные» методы лечения рака следует рассматривать с большой осторожностью, поскольку большинство из них не подтверждено доказательствами. Многие люди, рассказывающие об эффективности таких методов лечения, могут приписывать им пользу просто потому, что их состояние улучшилось после их использования — когда фактическая причина улучшения не связана.
Хорошая новость заключается в том, что традиционные методы лечения рака безопаснее и эффективнее, чем когда-либо. Новые химиотерапевтические препараты работают лучше с меньшим количеством побочных эффектов, а новые лекарства воздействуют на определенные мутации в раковых клетках, чтобы минимизировать вред здоровым клеткам. Высокоточные формы лучевой терапии разрушают опухоли, сохраняя при этом здоровые ткани. Новые подходы используют собственные иммунные силы организма для уничтожения раковых клеток. А новые хирургические методы позволяют более безопасно удалять опухоли, сводя к минимуму как риск рецидива, так и время восстановления.
Если вы планируете использовать дополнительную терапию в дополнение к традиционным методам лечения рака, всегда обращайтесь к авторитетному источнику, например, в нашей базе данных About Herbs или в Национальном институте рака, и всегда сообщайте об этом своему врачу.
Вернуться наверх .- См клиника на ярославской отзывы о врачах – , , , 4, . 2
- В митино косметология – Аппаратная косметология в Митино — услуги, отзывы и адреса салонов красоты на карте — Москва