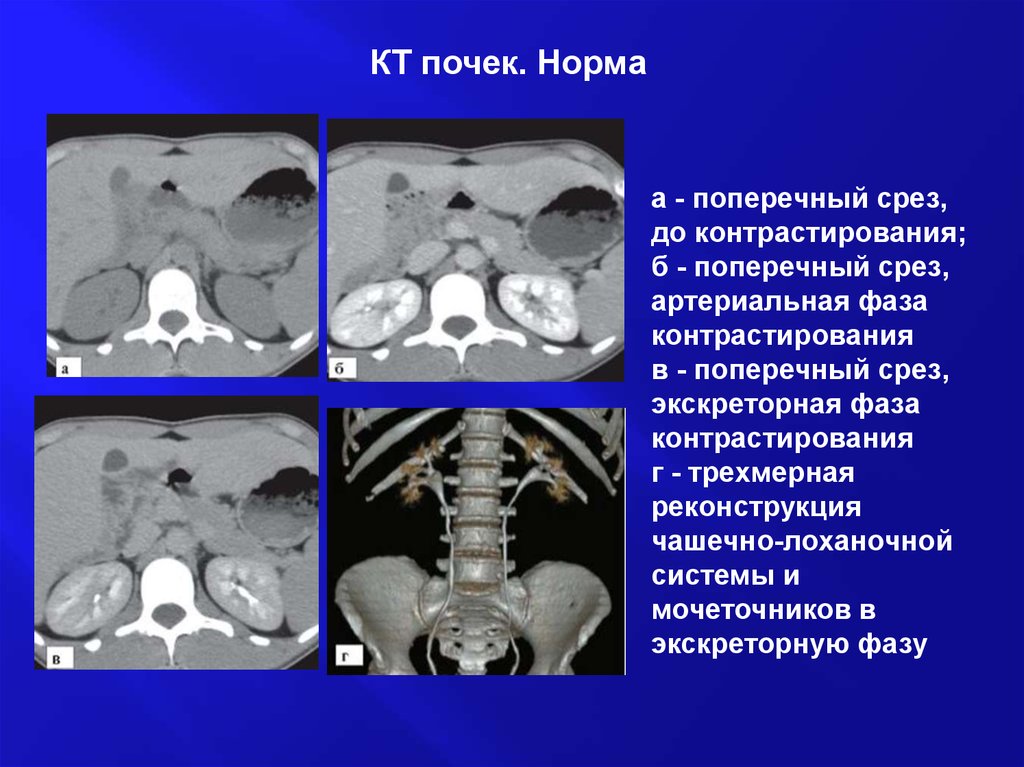
Мскт почек с контрастом: КТ почек с контрастированием – цена в Москве, сделать исследование, адреса и запись на прием в «СМ-Клиника»
КТ почек с контрастом ✔ Цена МСКТ в Москве
Компьютерная томография (КТ) почек применяется для идентификации нефрологических и сосудистых заболеваний. Для данного метода характерны высокая точность, оперативность проведения, финансовая доступность и возможность выявления широкого спектра патологий различного происхождения.
Как делают КТ почек в клинике «Чудо-Доктор»?
Принцип работы метода заключается в облучении исследуемой области рентгеновскими лучами, двигающимися по спиральной или круговой траектории. Современные мультиспиральные томографы позволяют одновременно получить изображения множества срезов. Сканирование при этом длится несколько секунд. За счет высокой скорости исследования снижается влияние движений пациента на качество изображения и уменьшается лучевая нагрузка на организм. Полученные снимки дают возможность воссоздания трехмерной модели интересующего органа. Мы гарантируем нашим пациентам:
Безопасность
Компьютерный томограф Toshiba Aquilion Prime задает передовой стандарт визуализации с низкой лучевой нагрузкой при полноценном объемном охвате органов.
Качественные снимки
Томограф позволяет получать 160 «срезов» за один оборот, который длится 0,5 с. Детектор допускает широкий охват анатомической области исследования. Специальные пакеты программ МСКТ позволяют проводить виртуальную эндоскопию полых органов, исследования минерального состава костей, диагностику параметров кровообращения.
Подходит для пациентов с весом до 300 кг
Оборудование Toshiba Aquilion Prime позволяет проводить обследования пациентов с избыточным весом. Устройства предыдущих поколений выдерживали вес до 100–130 кг.
Комфорт
Устройство томографа предусматривает возможность связи с медперсоналом. Стол с функцией поперечного перемещения упрощает подготовку к обследованию. Записаться на консультацию и обследование можно в любой день недели.
Какие болезни почек выявляет МСКТ?
Исследование позволяет обнаружить любые патологические процессы в органах даже на ранних этапах развития.
Томография почек используется для диагностики:
- опухолей доброкачественного или злокачественного характера, а также метастатических отсевов в клетчатку забрюшинного пространства;
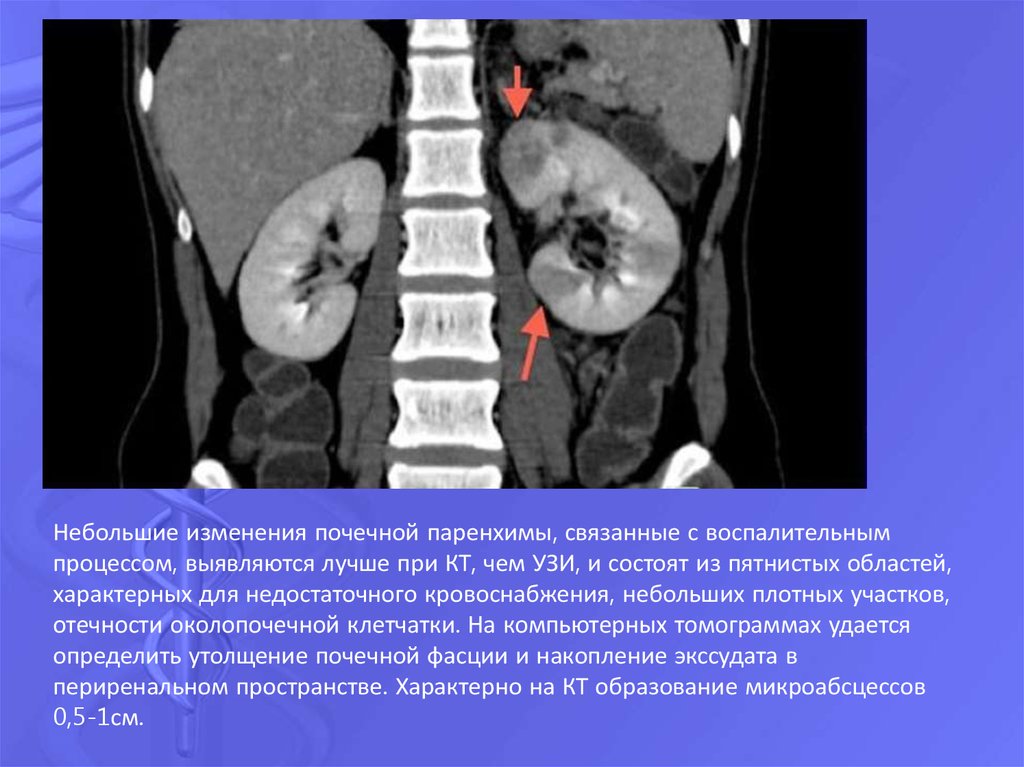
- инфекционных, воспалительных заболеваний как в самой почечной паренхиме, так и в паранефральных клетчаточных пространствах;
- патологий лимфатических узлов и околопочечной клетчатки;
- заболеваний сосудов почек, что может проявляться артериальной гипертензией;
- аномалий развития мочевыводящей системы;
- травм с подозрением на разрыв органа;
- кистозных и опухолевидных перерождений почечной ткани.

Снимки КТ почек без контраста позволяют визуализировать аномалии развития органа, камни, опущение почки, кровоизлияния и нарушения кровоснабжения почечной ткани. КТ с контрастированием почек применяют при выявлении новообразований в забрюшинном пространстве, для изучения сосудистой системы, а также для оценки уродинамики, т.е. наличия препятствий для оттока мочи.
КТ (компьютерная томография) почек позволяет обследовать орган целиком, измерять его размеры и рассмотреть любые отклонения от нормы. Также визуализируется структура надпочечников или мочеточников с мочевым пузырем.
Показания к процедуре
КТ назначается строго по показаниям в ходе установления диагноза. При первичном обращении к врачу проводится осмотр и пальпация болезненных органов, выяснение жалоб пациента. Исследование обычно проводится после более безопасных методов, требующихся для постановки предварительного диагноза – лабораторные исследования, УЗИ.
Компьютерную томографию почек назначают:
- при тянущих болях в области поясницы и нижней части живота;
- наличии крови в моче;
- частых и болезненных позывах к мочеиспусканию;
- травмах спины;
- подозрениях на наличие камней или новообразований.

Кому противопоказана КТ?
Однократное проведение процедуры безопасно для большинства пациентов. Абсолютных противопоказаний нет. Однако классический метод не рекомендован:
- детям до 14 лет;
- беременным женщинам.
Таким пациентам его назначают, если польза превышает возможные риски. При обследовании беременных женщин применяют висмутовые экраны, защищающие уязвимые зоны и не снижающие качество изображения.
Если пациент страдает клаустрофобией, КТ выполняют с помощью компьютерных томографов с открытым контуром.
Противопоказаниями для введения контрастного вещества являются:
- тяжелая почечная, печеночная недостаточность;
- тяжелая форма бронхиальной астмы;
- сильная аллергическая реакция на контрастный препарат;
- гипертиреоз;
- беременность.
Наличие в анамнезе легких аллергических реакций на контрастные вещества допускает проведение исследования с предварительным приемом Преднизолона и выбором неионных контрастных препаратов.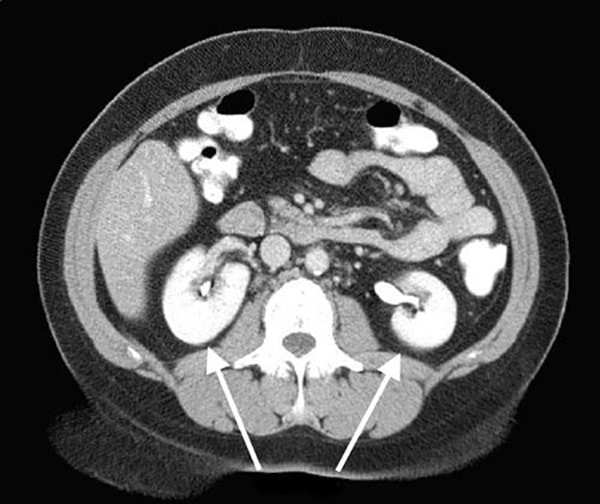 Кормление грудью не является противопоказанием к введению контрастного вещества. Однако следует приостановить грудное вскармливание на период выведения препарата (1–2 суток).
Кормление грудью не является противопоказанием к введению контрастного вещества. Однако следует приостановить грудное вскармливание на период выведения препарата (1–2 суток).
Как часто можно делать КТ?
Поскольку при исследовании пациент подвергается лучевой нагрузке, процедуру проводят только по назначению врача.
Подготовка к процедуре
Для классического КТ почек не требуется специальная подготовка. Дополнительно нужно сдать анализ крови на креатинин, что позволит оценить функциональность почек и предотвратить развитие почечной недостаточности. При необходимости исследовании с контрастным веществом необходимо исключить противопоказания. Если пациент не имеет данных о состоянии здоровья, потребуется пройти ряд исследований, подтверждающих отсутствие заболеваний, препятствующих проведению процедуры. Пациентам с почечной недостаточностью, сахарным диабетом, сердечной недостаточностью показана гидратация (введение внутривенно физраствора) за 6–12 часов до начала компьютерной томографии. За 2 суток до исследования следует приостановить применение нефротоксичных лекарственных средств.
За 2 суток до исследования следует приостановить применение нефротоксичных лекарственных средств.
Перед проведением исследования необходимо снять металлические предметы, аксессуары, съемные зубные протезы. Пациент надевает удобную одежду, располагается на столе томографа лежа лицом вверх. Во время процедуры необходимо следить, чтобы пациент оставался в неподвижном положении, иначе качество снимков будет снижено. В некоторых случаях таз фиксируют специальными ремешками, чтобы исключить непроизвольные движения.
Во время работы томографа врач находится в соседнем помещении и наблюдает за ходом исследования через специальное окно. Связь пациента с медперсоналом осуществляется через встроенный в аппарат микрофон. Длительность процедуры составляет от 10 до 20 минут.
Расшифровка результатов
Качество изображений мягких тканей при проведении компьютерной томографии с контрастированием сопоставимо с результатами магнитно-резонансной томографии. Все снимки записываются на электронный носитель. Врач-рентгенолог проводит расшифровку снимков, описывает внутреннее строение и положение органов.
Врач-рентгенолог проводит расшифровку снимков, описывает внутреннее строение и положение органов.
Почечную ткань можно обследовать с помощью трех разных зон обследования, в зависимости от того, какое заболевание подозревает лечащий врач, назначающий МСКТ. Компьютерная томография почек входит в зону сканирования “органы брюшной полости и забрюшинного пространства”. Эта область используется для получения информации о состоянии всех внутренних органов или при поиске новообразований и их метастатических отсевов. В подавляющем большинстве случаев (более чем в 80%) в таких ситуациях выполняется КТ почек с контрастированием. Подготовка заключается в соблюдении голода в течение минимум 4 часов до исследования. Это необходимо для лучшей визуализации органов, расположенных в брюшной полости.
При диагностировании причины повышения артериального давления или при выявлении опухолевидных образований после ультразвукового исследования (УЗИ) врачи могут назначить томографию почек и надпочечников. Для выполнения этого исследования голод соблюдать не нужно. При обнаружении опухолевых образований также потребуется проведение внутривенного контрастирования.
Для выполнения этого исследования голод соблюдать не нужно. При обнаружении опухолевых образований также потребуется проведение внутривенного контрастирования.
Если требуется исследование всей мочевыводящей системы и оценка уродинамики, применяется диагностика мочевыделительной системы, куда входит обследование почек, мочеточников и мочевого пузыря. Перед этим исследованием также лучше соблюдать голод. Контраст понадобится в ситуациях, когда наблюдается нарушение оттока мочи из почки из-за внешнего сдавления мочеточника. Для исключения опухоли в такой ситуации целесообразно введение контрастирующего препарата.
КТ почек с контрастом
Исследование мягких тканей без введения контрастного вещества малоинформативно, так как позволяет выявить только крупные новообразования. В большинстве случаев КТ проводят с контрастированием. Исследование длится около 40 минут. Введение препарата осуществляется автоматически через внутривенный катетер, установленный на локтевом сгибе. Выполнение снимков совпадает с максимальной концентрацией контрастного вещества в интересующей области. Объем введенного препарата зависит от характера предполагаемой патологии. Для улучшения визуализации лимфоузлов, сосудов, опухоли может проводиться двухфазное контрастирование с интервалом 5 минут.
Объем введенного препарата зависит от характера предполагаемой патологии. Для улучшения визуализации лимфоузлов, сосудов, опухоли может проводиться двухфазное контрастирование с интервалом 5 минут.
Побочные реакции на введение контрастных препаратов на основе йода возникают у 1–3% пациентов. В основном это легкие аллергические проявления в виде зуда, тошноты, искажения вкусовых ощущений, крапивницы.
Злокачественные опухоли, очаги воспаления, кисты, сосудистые новообразования характеризуются усиленным кровоснабжением. Особенность применения контрастного вещества заключается в возможности диагностировать патологию размером от 1 мм и провести раннюю диагностику. В онкологической практике проведение КТ с контрастом позволяет определить опухоли матки, яичников, предстательной железы, мочевого пузыря, лимфоузлов на любой стадии. Исследование показывает характер опухоли, ее отношения со здоровыми тканями, наличие метастазов. КТ проводят также для оценки динамики злокачественного процесса после проведения лучевой терапии, хирургического лечения или химиотерапии.
Что лучше сделать: КТ или МРТ?
Компьютерный томограф дает возможность быстро провести обследование и получить трехмерное изображение. По сравнению с МРТ, КТ органов почек более доступна по цене. Метод оптимален, если нужно проверить физическое состояние исследуемых тканей и органов: их положение, размеры и плотность. В свою очередь магнитно-резонансный томограф предполагает использование радиочастотного излучения в магнитном поле. Он дает информацию преимущественно о химическом строении тканей. Каждый метод по-своему хорош и дополняет другой. Выбирать способ диагностики должен врач в зависимости от целей исследования.
Как записаться?
В клинике «Чудо Доктор» в Москве вы можете сделать КТ почек по доступной цене в удобное время. У нас работают опытные врачи-диагносты. Сразу после обследования вы можете получить консультацию узкого специалиста. Чтобы записаться на прием, позвоните по указанным телефонам или заполните онлайн-форму на сайте.
МСКТ почек, надпочечников с контрастром и без, КТ и МРТ почек: показания
Мочевыделительная система (мочевая система) человека — система органов, формирующих, накапливающих и выделяющих мочу у человека. Состоит из пары почек, двух мочеточников, мочевого пузыря и мочеиспускательного канала.
Состоит из пары почек, двух мочеточников, мочевого пузыря и мочеиспускательного канала.
Почка человека имеет бобовидную форму со слегка закругленными полюсами: верхним и нижним. Масса почки взрослого человека достигает 120−200 грамм.
На вогнутом медиальном крае этого органа есть углубление — так называемые почечные ворота, которые в свою очередь ведут в не большую по размерам почечную пазуху. По своему строению это место, где расположены нервы и сосуды, почечные лоханки и чашки, а также начало мочеточника и жировой ткани. Мочеточники «несут» мочу и впадают в мочевой пузырь, который представляет собой полый мышечный орган, располагающийся забрюшинно в малом тазу. Мочевой пузырь служит для накопления мочи. Вместимость мочевого пузыря в среднем 500—750 мл куб. и подвержена большим индивидуальным колебаниям. Размеры мочевого пузыря меняются в зависимости от его растяжения содержимым. При отсутствии заболеваний, мочевой пузырь может спокойно удерживать 300 мл мочи в течение 2—5 часов.
Почки выполняют очень важную функцию – производят очистку крови от бактерий, токсинов и других вредных веществ, являющихся результатом жизнедеятельности организма. Именно благодаря почкам происходит восстановление нормального состава крови. Поэтому малейшее нарушение их деятельности может привести к серьезным, порой даже необратимым последствиям. Чтобы не пришлось долго болеть, нужно вовремя лечить патологии, а для правильного диагноза необходима точная диагностика.
МСКТ почек позволяет определить анатомическую структуру и функциональное состояние почек, питающих их сосудов, мочевыводящих путей и лимфатической системы. МСКТ успешно применяется для раннего обнаружения патологических процессов исследуемой зоны, особенно этот метод информативен при подозрениях на опухолевые процессы, кисту (поликистоз), абсцесс, метастазы. На снимках МСКТ хорошо видны камни в почках, аномалии развития, нефроптоз, кровоизлияние (в том числе и после травмы).
Время исследования:
30 минут.
Введение контраста:
в некоторых случаях, для лучшей визуализации сосудистых структур и мочевыводящих путей (чашечно-лоханочного комплекса, мочеточников), используют йодсодержащее контрастное вещество (МСКТ почек с контрастом). Это позволяет более чётко исследовать мелкие структуры органов, оценить кровоснабжение, мочеобразование и мочевыделение.
Подготовка к диагностике почек:
- Не есть за 3 часа до исследования.
- Наполненный мочевой пузырь — не мочиться за 1 час до назначенного времени.
- На исследование принести результаты УЗИ, предыдущих КТ или МРТ, медицинские документы, выписки из стационаров (любой документ, который позволит обосновать необходимость выполнения Вам рентгеновского исследования).
- Для исследования с контрастом необходимо сделать анализы мочевины и креатинин.
Противопоказания:
КТ без контраста:
- беременность.
КТ с контрастом:
- аллергия на йод;
- почечная недостаточность;
- тяжёлый сахарный диабет;
- беременность;
- заболевания щитовидной железы.

МРТ или КТ?
В изучении надпочечников предпочтение обычно отдают МРТ. Эта методика хорошо выявляет мельчайшие очаговые образования в мягких тканях, поэтому она очень эффективна при поиске небольших гормонопродуцирующих опухолей этого органа. Впрочем, компьютерная томография надпочечников не менее отчетливо выявляет доброкачественную гиперплазию.
Даже обычная спиральная компьютерная томография забрюшинного пространства более чувствительна при определении камней почек в сравнении с МРТ, поэтому именно ее назначают для уточнения неоднозначных данных урографии и УЗИ, а также во время планирования операций при крупных конкрементах лоханок и т.д. Зачастую именно благодаря результатам КТ удается определить правильную тактику лечения, выбрать метод литотрипсии (удаления камней) и принять решение об операции или другом способе терапии.
Примеры:
Злокачественное новообразование правой почки
S-образно извитый в средней трети правый мочеточник
Коралловидный конкремент в синусе правой почки
Предотвращение индуцированной контрастом почечной недостаточности: руководство
1. Morabito S, Pistolesi V, Benedetti G et al. Частота контраст-индуцированного острого повреждения почек, связанного с диагностической или интервенционной коронарографией. J Нефрол. 2012;25:1098–107. 10.5301/jn.5000101 [PubMed] [Google Scholar]
Morabito S, Pistolesi V, Benedetti G et al. Частота контраст-индуцированного острого повреждения почек, связанного с диагностической или интервенционной коронарографией. J Нефрол. 2012;25:1098–107. 10.5301/jn.5000101 [PubMed] [Google Scholar]
2. Newhouse JH, Kho D, Rao QA, Starren J. Частота изменений креатинина в сыворотке крови в отсутствие йодсодержащего контрастного вещества: последствия для исследований нефротоксичности контраста. Am J Рентгенол. 2008;191: 376–82. 10.2214/AJR.07.3280 [PubMed] [Google Scholar]
3. Caixeta A, Nikolsky E, Mehran R. Профилактика и лечение контраст-ассоциированной нефропатии в интервенционной кардиологии. Curr Cardiol Rep. 2009; 11:377–83. [PubMed] [Google Scholar]
4. Giacoppo D, Madhavan MV, Baber U et al. Влияние контраст-индуцированного острого повреждения почек после чрескожного коронарного вмешательства на краткосрочные и долгосрочные исходы: объединенный анализ исследований HORIZONS-AMI и ACUITY. Circ Cardiovasc Interv. 2015;8:e002475. 10.1161/CIRCINTERVENTIONS.114.002475 [PubMed] [Google Scholar]
10.1161/CIRCINTERVENTIONS.114.002475 [PubMed] [Google Scholar]
5. Toprak O, Cirit M, Yesil M et al. Влияние диабетического и преддиабетического состояния на развитие контраст-индуцированной нефропатии у больных с хронической болезнью почек. Трансплантация нефролового циферблата. 2007; 22:819–26. [PubMed] [Google Scholar]
6. Calvin AD, Misra S. Pflueger A: Контраст-индуцированное острое повреждение почек и диабетическая нефропатия. Нат Рев Нефрол. 2010; 6: 679–88. 10.1038/nrneph.2010.116 [бесплатная статья PMC] [PubMed] [Google Scholar]
7. Rihal CS, Textor SC, Grill DE et al. Частота и прогностическое значение острой почечной недостаточности после чрескожного коронарного вмешательства. Тираж. 2002;105:2259–64. [PubMed] [Google Scholar]
8. От AM, Bartholmai BJ, Williams AW et al. Смертность, связанная с нефропатией после рентгеноконтрастного воздействия. Мэйо Клин Proc. 2008; 83: 1095–100. 10.4065/83.10.1095 [PubMed] [Google Scholar]
9. Weisbord SD, Chen H, Stone RA et al. Ассоциации повышения уровня креатинина в сыворотке крови со смертностью и продолжительностью пребывания в стационаре после коронарографии. J Am Soc Нефрол. 2006; 17: 2871–7. [PubMed] [Google Scholar]
Ассоциации повышения уровня креатинина в сыворотке крови со смертностью и продолжительностью пребывания в стационаре после коронарографии. J Am Soc Нефрол. 2006; 17: 2871–7. [PubMed] [Google Scholar]
10. Dangas G, Iakovou I, Nikolsky E et al. Контраст-индуцированная нефропатия после чрескожных коронарных вмешательств в связи с хронической болезнью почек и гемодинамическими показателями. Ам Джей Кардиол. 2005;95:13–9. [PubMed] [Google Scholar]
11. James MT, Ghali WA, Tonelli M et al. Острое повреждение почек после коронароангиографии связано с долгосрочным снижением функции почек. почки инт. 2010;78:803–9. 10.1038/ki.2010.258 [PubMed] [Google Scholar]
12. Solomon RJ, Mehran R, Natarajan MK et al. Контраст-индуцированная нефропатия и отдаленные нежелательные явления: причина и следствие? Clin J Am Soc Нефрол. 2009;4:1162–9. 10.2215/CJN.00550109 [бесплатная статья PMC] [PubMed] [Google Scholar]
13. Гольденберг И., Чонхол М., Гетта В. Обратимое острое повреждение почек после контрастного воздействия и риск долгосрочной смертности. Am J Нефрол. 2009; 29: 136–44. 10.1159/000151772 [PubMed] [Google Scholar]
Am J Нефрол. 2009; 29: 136–44. 10.1159/000151772 [PubMed] [Google Scholar]
14. Brown JR, Malenka DJ, DeVries JT et al. Преходящая и стойкая почечная дисфункция являются предикторами выживаемости после чрескожного коронарного вмешательства: выводы из Дартмутского динамического регистра. Катетер Cardiovasc Interv. 2008; 72: 347–54. 10.1002/ccd.21619 [бесплатная статья PMC] [PubMed] [Google Scholar]
15. Tumlin J, Stacul F, Panel CINCW et al. Патофизиология контраст-индуцированной нефропатии. Ам Джей Кардиол. 2006; 98:14–20 К. [PubMed] [Google Scholar]
16. Сендески М., Пацак А., Паллоне Т.Л. и соавт. Йодиксанол, сужение мозгового вещества нисходящей прямой кишки и риск нефропатии, вызванной контрастным веществом. Радиология. 2009; 251: 697–704. 10.1148/radiol.2513081732 [бесплатная статья PMC] [PubMed] [Google Scholar]
17. Соломон Р. Контраст-индуцированное острое повреждение почек (CIAKI) Radiol Clin North Am. 2009 г.;47:783–8. 10.1016/j.rcl.2009.06.001 [PubMed] [Google Scholar]
18. Wong PC, Li Z, Guo J, Zhang A. Патофизиология контраст-индуцированной нефропатии. Int J Кардиол. 2012; 158:186–92. 10.1016/j.ijcard.2011.06.115 [PubMed] [Google Scholar]
Wong PC, Li Z, Guo J, Zhang A. Патофизиология контраст-индуцированной нефропатии. Int J Кардиол. 2012; 158:186–92. 10.1016/j.ijcard.2011.06.115 [PubMed] [Google Scholar]
19. Heinrich MC, Kuhlmann MK, Grgic A et al. Цитотоксическое действие ионных высокоосмолярных, неионогенных мономерных и неионогенных изоосмолярных димерных йодсодержащих контрастных веществ на клетки почечных канальцев in vitro . Радиология. 2005; 235:843–9. [PubMed] [Академия Google]
20. Seeliger E, Lenhard DC, Persson PB. Вязкость контрастного вещества по сравнению с осмоляльностью при повреждении почек: уроки исследований на животных. Биомед Рез Инт. 2014; 2014:358136. 10.1155/2014/358136 [Бесплатная статья PMC] [PubMed] [Google Scholar]
21. Hardiek K, Katholi RE, Ramkumar V, Deitrick C. Реакция клеток проксимальных канальцев на рентгеноконтрастные вещества. Am J Physiol Renal Physiol. 2001; 280: F61–70. [PubMed] [Google Scholar]
22. Пир А., Авербух З., Берман С. и соавт.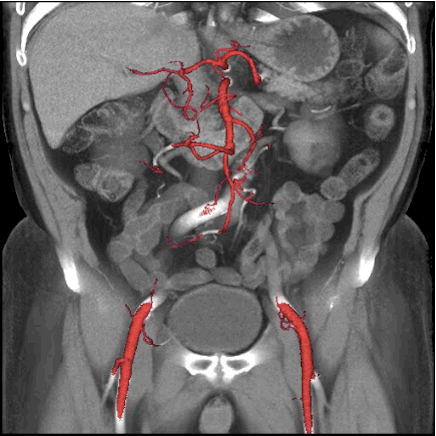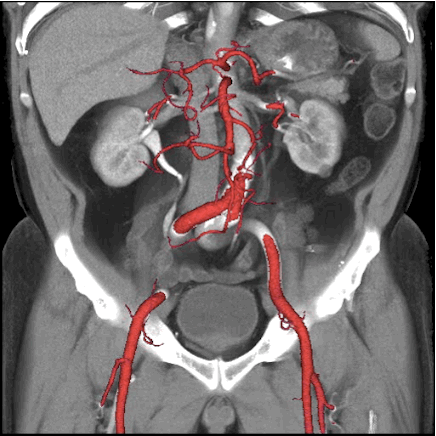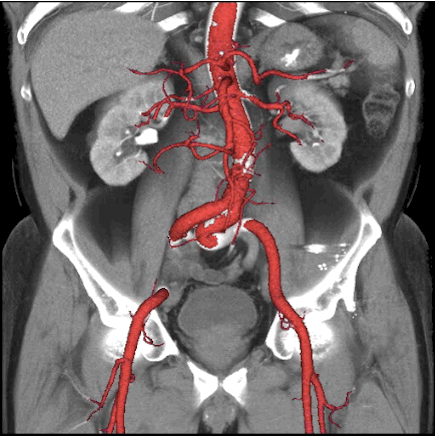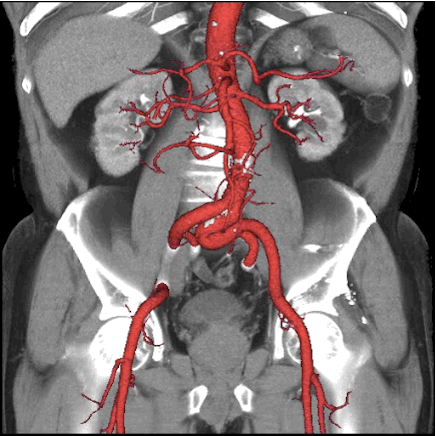 Контрастные среды усиливали апоптоз культивируемых почечных мезангиальных, тубулярных, эпителиальных, эндотелиальных и печеночных клеток. Инвестируйте Радиол. 2003; 38: 177–82. [PubMed] [Академия Google]
Контрастные среды усиливали апоптоз культивируемых почечных мезангиальных, тубулярных, эпителиальных, эндотелиальных и печеночных клеток. Инвестируйте Радиол. 2003; 38: 177–82. [PubMed] [Академия Google]
23. Quintavalle C, Brenca M, De Micco F et al. In vivo и in vitro оценка путей, участвующих в индуцированном контрастным веществом апоптозе почечных клеток. Клеточная смерть Дис. 2011;2:e155. 10.1038/cddis.2011.38 [бесплатная статья PMC] [PubMed] [Google Scholar]
24. Ueda J, Nygren A, Hansell P, Ulfendahl HR. Влияние внутривенных контрастных веществ на гидростатическое давление в проксимальных и дистальных канальцах почек крыс. Акта Радиол. 1993; 34:83–87. [PubMed] [Академия Google]
25. Mehran R, Aymong ED, Nikolsky E et al. Простая оценка риска для прогнозирования контраст-индуцированной нефропатии после чрескожного коронарного вмешательства: разработка и начальная валидация. J Am Coll Кардиол. 2004;44:1393–9. [PubMed] [Google Scholar]
26. Brown JR, DeVries JT, Piper WD et al. Исследование сердечно-сосудистых заболеваний Северной Новой Англии G: Можно прогнозировать серьезную почечную дисфункцию после чрескожных коронарных вмешательств. Am Heart J. 2008; 155: 260–6. 10.1016/j.ahj.2007.10.007 [PubMed] [Google Scholar]
Brown JR, DeVries JT, Piper WD et al. Исследование сердечно-сосудистых заболеваний Северной Новой Англии G: Можно прогнозировать серьезную почечную дисфункцию после чрескожных коронарных вмешательств. Am Heart J. 2008; 155: 260–6. 10.1016/j.ahj.2007.10.007 [PubMed] [Google Scholar]
27. Базиль Д.П., Андерсон М.Д., Саттон Т.А. Патофизиология острой почечной недостаточности. сост. физиол. 2012;2:1303–53. 10.1002/cphy.c110041 [бесплатная статья PMC] [PubMed] [Google Scholar]
28. Топрак О. Глава 10: Коронарная ангиография и контраст-индуцированная нефропатия. В: Достижения в диагностике коронарного атеросклероза. 2011. С. 181–202. Под редакцией Suna F Croatia: InTech,
29. Cheng H, Harris RC. Почечная эндотелиальная дисфункция при диабетической нефропатии. Сердечно-сосудистые мишени для лечения гематолового расстройства. 2014;14:22–33. [Бесплатная статья PMC] [PubMed] [Google Scholar]
30. Stolker JM, McCullough PA, Rao S et al. Уровни глюкозы до процедуры и риск контраст-индуцированного острого повреждения почек у пациентов, перенесших коронарографию. J Am Coll Кардиол. 2010;55:1433–40. 10.1016/j.jacc.2009.09.072 [PubMed] [Google Scholar]
J Am Coll Кардиол. 2010;55:1433–40. 10.1016/j.jacc.2009.09.072 [PubMed] [Google Scholar]
31. Никольский Э., Мехран Р., Туркот Д. и соавт. Влияние хронической болезни почек на прогноз у пациентов с сахарным диабетом, получавших чрескожное коронарное вмешательство. Ам Джей Кардиол. 2004; 94:300–5. [PubMed] [Академия Google]
32. Pakfetrat M, Nikoo MH, Malekmakan L et al. Сравнение факторов риска контраст-индуцированного острого повреждения почек у пациентов с сахарным диабетом и без него. Гемодиал Инт. 2010; 14:38–92. 10.1111/j.1542-4758.2010.00469.x [PubMed] [Google Scholar]
33. Murakami R, Kumita S, Hayashi H et al. Анемия и риск контраст-индуцированной нефропатии у пациентов с почечной недостаточностью, подвергающихся МСКТ с контрастным усилением. Евр Дж Радиол. 2013;82:e521–4. 10.1016/j.ejrad.2013.06.004 [PubMed] [Google Scholar]
34. Peng F, Su J, Lin J, Niu W. Влияние блокаторов ренин-ангиотензин-альдостероновой системы на риск контраст-индуцированного острого повреждения почек: проспективное исследование и метаанализ. J Cardiovasc Pharmacol. 2015;65:262–8. 10.1097/FJC.0000000000000189 [PubMed] [Google Scholar]
J Cardiovasc Pharmacol. 2015;65:262–8. 10.1097/FJC.0000000000000189 [PubMed] [Google Scholar]
35. Cirit M, Toprak O, Yesil M et al. Ингибиторы ангиотензинпревращающего фермента как фактор риска контраст-индуцированной нефропатии. Клиническая практика Нефрона. 2006; 104: c20–7. [PubMed] [Академия Google]
36. Сидху Р.Б., Браун Дж.Р., Робб Дж.Ф. и соавт. Влияние пола и возраста на контраст-индуцированное острое повреждение почек после катетеризации сердца. Ам Джей Кардиол. 2008; 102:1482–6. 10.1016/j.amjcard.2008.07.037 [PubMed] [Google Scholar]
37. Chen R, Kumar S, Timmis A et al. Сравнение взаимосвязи между почечной недостаточностью, ангиографической ишемической болезнью сердца и долгосрочной смертностью у женщин и мужчин. Ам Джей Кардиол. 2006; 97: 630–2. [PubMed] [Google Scholar]
38. Marenzi G, Assanelli E, Campodonico J et al. Объем контраста во время первичного чрескожного коронарного вмешательства и последующей контраст-индуцированной нефропатии и смертности. Энн Интерн Мед. 2009 г.;150:170–7. [PubMed] [Google Scholar]
Энн Интерн Мед. 2009 г.;150:170–7. [PubMed] [Google Scholar]
39. Laskey WK, Jenkins C, Investigators NDR et al. Отношение объема к клиренсу креатинина: фармакокинетический фактор риска для прогнозирования раннего повышения уровня креатинина после чрескожного коронарного вмешательства. J Am Coll Кардиол. 2007; 50: 584–90. [PubMed] [Google Scholar]
40. Ando G, de Gregorio C, Morabito G et al. Объем контраста с поправкой на функцию почек переопределяет исходную оценку риска острого повреждения почек, индуцированного контрастом, у пациентов, перенесших первичное чрескожное коронарное вмешательство. Circ Cardiovasc Interv. 2014;7:465–72. 10.1161/CIRCINTERVENTIONS.114.001545 [PubMed] [Google Scholar]
41. Gurm HS, Dixon SR, Smith DE et al. Дозирование контраста в зависимости от функции почек для определения безопасных пределов рентгеноконтрастного вещества у пациентов, подвергающихся чрескожным коронарным вмешательствам. J Am Coll Кардиол. 2011;58:907–14. 10.1016/j. jacc.2011.05.023 [PubMed] [Google Scholar]
jacc.2011.05.023 [PubMed] [Google Scholar]
42. Anne G, Gruberg L, Huber A et al. Традиционная и автоматизированная система введения контраста в диагностических и чрескожных коронарных интервенционных процедурах: сравнение доставляемого объема контраста. J Инвазивная кардиол. 2004; 16:360–2. [PubMed] [Академия Google]
43. Mariani Jr Jr, Guedes C, Soares P et al. Внутрисосудистое ультразвуковое руководство для сведения к минимуму использования йодсодержащего контраста при чрескожном коронарном вмешательстве: рандомизированное контролируемое исследование MOZART (минимизация использования контраста с помощью внутривенного ультразвукового исследования при коронарной ангиопластике). JACC Cardiovasc Interv. 2014;7:1287–93. 10.1016/j.jcin.2014.05.024 [бесплатная статья PMC] [PubMed] [Google Scholar]
44. Kushner FG, Hand M, Smith SC Jr et al. целенаправленные обновления: рекомендации ACC/AHA по ведению пациентов с инфарктом миокарда с подъемом сегмента ST (обновление рекомендаций 2004 г. и целенаправленное обновление 2007 г.) и рекомендации ACC/AHA/SCAI по чрескожному коронарному вмешательству (обновление рекомендаций 2005 г. и целенаправленное обновление 2007 г.) a отчет Целевой группы Фонда Американского колледжа кардиологов/Американской кардиологической ассоциации по практическим рекомендациям. J Am Coll Кардиол. 2009 г.;2009;54:2205–41. 10.1016/j.jacc.2009.10.015 [PubMed] [Google Scholar]
и целенаправленное обновление 2007 г.) и рекомендации ACC/AHA/SCAI по чрескожному коронарному вмешательству (обновление рекомендаций 2005 г. и целенаправленное обновление 2007 г.) a отчет Целевой группы Фонда Американского колледжа кардиологов/Американской кардиологической ассоциации по практическим рекомендациям. J Am Coll Кардиол. 2009 г.;2009;54:2205–41. 10.1016/j.jacc.2009.10.015 [PubMed] [Google Scholar]
45. Dong M, Jiao Z, Liu T et al. Влияние пути введения контрастных веществ на почечную безопасность: метаанализ рандомизированных контролируемых исследований. J Нефрол. 2012;25:290–301. 10.5301/jn.5000067 [PubMed] [Google Scholar]
46. From AM, Al Badarin FJ, McDonald FS et al. Йодиксанол по сравнению с низкоосмолярными контрастными веществами для профилактики контраст-индуцированной нефропатии: метаанализ рандомизированных контролируемых исследований. Circ Cardiovasc Interv. 2010;3:351–8. 10.1161/ОБХОДЫ.109.917070 [PubMed] [Google Scholar]
47. Mehran R, Nikolsky E, Kirtane AJ et al. Ионное низкоосмолярное контрастное вещество по сравнению с неионным изоосмолярным контрастным веществом для предотвращения ухудшения нефропатии после ангиопластики у пациентов с хронической почечной недостаточностью: исследование ICON (Ионное или неионное контрастирование для предотвращения ухудшения нефропатии после ангиопластики у пациентов с хронической почечной недостаточностью). JACC Cardiovasc Interv. 2009;2:415–21. 10.1016/j.jcin.2009.03.007 [PubMed] [Google Scholar]
Ионное низкоосмолярное контрастное вещество по сравнению с неионным изоосмолярным контрастным веществом для предотвращения ухудшения нефропатии после ангиопластики у пациентов с хронической почечной недостаточностью: исследование ICON (Ионное или неионное контрастирование для предотвращения ухудшения нефропатии после ангиопластики у пациентов с хронической почечной недостаточностью). JACC Cardiovasc Interv. 2009;2:415–21. 10.1016/j.jcin.2009.03.007 [PubMed] [Google Scholar]
48. Trivedi HS, Moore H, Nasr S et al. Рандомизированное проспективное исследование для оценки роли гидратации солевым раствором в развитии контрастной нефротоксичности. Клиническая практика Нефрона. 2003;93: С29–34. [PubMed] [Google Scholar]
49. Никольский Э., Мехран Р. Протоколы гидратации для снижения частоты контраст-индуцированной нефропатии. J Инвазивная кардиол. 2008; 20: 527–38. [PubMed] [Google Scholar]
50. Levine GN, Bates ER, Blankenship JC et al. Руководство по чрескожному коронарному вмешательству. Отчет Фонда Американского колледжа кардиологов/Целевой группы Американской кардиологической ассоциации по практическим рекомендациям и Обществу сердечно-сосудистой ангиографии и вмешательств. J Am Coll Кардиол. 2011;58:e44–122. 10.1016/j.jacc.2011.08.007 [PubMed] [Google Scholar]
Отчет Фонда Американского колледжа кардиологов/Целевой группы Американской кардиологической ассоциации по практическим рекомендациям и Обществу сердечно-сосудистой ангиографии и вмешательств. J Am Coll Кардиол. 2011;58:e44–122. 10.1016/j.jacc.2011.08.007 [PubMed] [Google Scholar]
51. Маккалоу Пенсильвания. Контрастное острое повреждение почек. J Am Coll Кардиол. 2008; 51:1419–28. 10.1016/j.jacc.2007.12.035 [PubMed] [Google Scholar]
52. Brar SS, Aharonian V, Mansukhani P et al. Введение жидкости под гемодинамическим контролем для предотвращения контраст-индуцированного острого повреждения почек: рандомизированное контролируемое исследование POSEIDON. Ланцет. 2014; 383:1814–23. 10.1016/S0140-6736(14)60689-9 [PubMed] [Google Scholar]
53. Zapata-Chica CA, Bello Marquez D, Serna-Higuita LM et al. Бикарбонат натрия по сравнению с изотоническим солевым раствором для предотвращения контраст-индуцированной нефропатии: систематический обзор и метаанализ. Медика Колумбии. 2015;46:90–103. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2015;46:90–103. [Бесплатная статья PMC] [PubMed] [Google Scholar]
54. Brar SS, Hiremath S, Dangas G et al. Бикарбонат натрия для профилактики острого повреждения почек, индуцированного контрастом: систематический обзор и метаанализ. Clin J Am Soc Нефрол. 2009; 4:1584–92. 10.2215/CJN.03120509 [бесплатная статья PMC] [PubMed] [Google Scholar]
55. Mehran R, Caixeta A. N-ацетилцистеин в профилактике контраст-индуцированной нефропатии. Давать или не давать: вот в чем вопрос. Преподобный Эсп Кардиол. 2010;63:9–11. [PubMed] [Google Scholar]
56. Trivedi H, Daram S, Szabo A et al. Высокие дозы N-ацетилцистеина для профилактики контраст-индуцированной нефропатии. Am J Med. 2009;122(874):e9–15. 10.1016/j.amjmed.2009.01.035 [PubMed] [Google Scholar]
57. Sun Z, Fu Q, Cao L et al. Внутривенный N-ацетилцистеин для профилактики контраст-индуцированной нефропатии: метаанализ рандомизированных контролируемых исследований. ПЛОС Один. 2013;8:e55124. 10.1371/journal.pone. 0055124 [бесплатная статья PMC] [PubMed] [Google Scholar]
0055124 [бесплатная статья PMC] [PubMed] [Google Scholar]
58. Weisbord SD, Gallagher M, Kaufman J et al. Профилактика контраст-индуцированного ОПП: обзор опубликованных исследований и дизайн профилактики серьезных нежелательных явлений после ангиографии (PRESERVE). Clin J Am Soc Нефрол. 2013;8:1618–31. 10.2215/CJN.11161012 [бесплатная статья PMC] [PubMed] [Google Scholar]
59. Рабочая группа KDIGO. Руководство по клинической практике при остром повреждении почек. Почки Int Suppl. 2012;2:122–123. 10.1038/kisup.2011.37 [Google Scholar]
60. Rodrigues GJ, Lunardi CN, Lima RG et al. Витамин С улучшает действие нового донора оксида азота на гладкую мускулатуру сосудов крыс с почечной гипертензией. Оксид азота. 2008; 18: 176–83. 10.1016/j.niox.2007.12.002 [PubMed] [Google Scholar]
61. McCullough PA, Akrawinthawong K. Аскорбиновая кислота для профилактики контраст-индуцированного острого повреждения почек. J Am Coll Кардиол. 2013;62:2176–7. 10.1016/j.jacc.2013. 07.066 [PubMed] [Google Scholar]
07.066 [PubMed] [Google Scholar]
62. Brueck M, Cengiz H, Hoeltgen R et al. Полезность N-ацетилцистеина или аскорбиновой кислоты по сравнению с плацебо для предотвращения острого повреждения почек, вызванного контрастом, у пациентов, перенесших плановую катетеризацию сердца: одноцентровое, проспективное, рандомизированное, двойное слепое, плацебо-контролируемое исследование. J Инвазивная кардиол. 2013; 25: 276–83. [PubMed] [Академия Google]
63. Садат У., Усман А., Гиллард Дж. Х., Бойл Дж. Р. Защищает ли аскорбиновая кислота от острого повреждения почек, вызванного контрастированием, у пациентов, перенесших коронарную ангиографию: систематический обзор с метаанализом рандомизированных контролируемых исследований. J Am Coll Кардиол. 2013;62:2167–75. 10.1016/j.jacc.2013.07.065 [PubMed] [Google Scholar]
64. Quintavalle C, Fiore D, De Micco F et al. Влияние высокой нагрузочной дозы аторвастатина на контраст-индуцированное острое повреждение почек. Тираж. 2012;126:3008–16. 10.1161/CIRCULATIONAHA.112.103317 [PubMed] [Google Scholar]
10.1161/CIRCULATIONAHA.112.103317 [PubMed] [Google Scholar]
65. Jo SH, Koo BK, Park JS et al. Профилактика нефропатии, вызванной рентгеноконтрастным веществом, с помощью краткосрочного введения высоких доз симвастатина у пациентов с почечной недостаточностью, проходящих исследование коронарной ангиографии (PROMISS) — рандомизированное контролируемое исследование. Am Heart J. 2008; 155 (499): e1–8. 10.1016/j.ahj.2007.11.042 [PubMed] [Google Scholar]
66. Leoncini M, Toso A, Maioli M et al. Раннее назначение высоких доз розувастатина для профилактики контраст-индуцированной нефропатии при остром коронарном синдроме: результаты исследования PRATO-ACS (защитный эффект розувастатина и антитромбоцитарной терапии на контраст-индуцированное острое повреждение почек и повреждение миокарда у пациентов с острым коронарным синдромом) J Am Колл Кардиол. 2014; 63:71–9. 10.1016/j.jacc.2013.04.105 [PubMed] [Google Scholar]
67. Zhang J, Li Y, Tao GZ et al. Краткосрочное лечение розувастатином для профилактики контраст-индуцированного острого повреждения почек у пациентов, получающих умеренные или большие объемы контрастного вещества: субанализ исследования TRACK-D. Chin Med J. 2015;128:784–9. 10.4103/0366-6999.152620 (англ.) [бесплатная статья PMC] [PubMed] [Google Scholar]
Chin Med J. 2015;128:784–9. 10.4103/0366-6999.152620 (англ.) [бесплатная статья PMC] [PubMed] [Google Scholar]
68. Marenzi G, Cosentino N, Werba JP et al. Метаанализ рандомизированных контролируемых исследований статинов для профилактики контраст-индуцированного острого повреждения почек у пациентов с острым коронарным синдромом и без него. Int J Кардиол. 2015; 183:47–53. 10.1016/j.ijcard.2015.01.046 [PubMed] [Google Scholar]
69. Ukaigwe A, Karmacharya P, Mahmood M et al. Метаанализ эффективности статинов для профилактики контраст-индуцированного острого повреждения почек у пациентов, перенесших коронарографию. Ам Джей Кардиол. 2014; 114:1295–302. 10.1016/j.amjcard.2014.07.059 [PubMed] [Google Scholar]
70. Giacoppo D, Capodanno D, Capranzano P et al. Мета-анализ рандомизированных контролируемых исследований предоперационного введения статинов для уменьшения контраст-индуцированного острого повреждения почек у пациентов, перенесших коронарную катетеризацию. Ам Джей Кардиол. 2014; 114:541–8. 10.1016/j.amjcard.2014.05.036 [PubMed] [Google Scholar]
2014; 114:541–8. 10.1016/j.amjcard.2014.05.036 [PubMed] [Google Scholar]
71. Тумлин Дж.А., Ван А., Мюррей П.Т., Матур В.С. Мезилат фенолдопама блокирует снижение почечного плазмотока после инфузии рентгеноконтрастного красителя: пилотное исследование по профилактике контрастной нефропатии. Am Heart J. 2002; 143: 894–903. [PubMed] [Google Scholar]
72. Landoni G, Biondi-Zoccai GG, Tumlin JA et al. Благотворное влияние фенолдопама на пациентов в критическом состоянии с острой почечной недостаточностью или с риском ее возникновения: метаанализ рандомизированных клинических исследований. Am J почек Dis. 2007; 49: 56–68. [PubMed] [Академия Google]
73. Stone GW, McCullough PA, Tumlin JA et al. Мезилат фенолдопама для профилактики контраст-индуцированной нефропатии: рандомизированное контролируемое исследование. ДЖАМА. 2003; 290:2284–91. [PubMed] [Google Scholar]
74. Allaqaband S, Tumuluri R, Malik AM et al. Проспективное рандомизированное исследование N-ацетилцистеина, фенолдопама и физиологического раствора для профилактики радиоконтрастной нефропатии. Катетер Cardiovasc Interv. 2002; 57: 279–83. [PubMed] [Google Scholar]
Катетер Cardiovasc Interv. 2002; 57: 279–83. [PubMed] [Google Scholar]
75. Dai B, Liu Y, Fu L et al. Влияние теофиллина на предотвращение контраст-индуцированного острого повреждения почек: метаанализ рандомизированных контролируемых исследований. Am J почек Dis. 2012;0:360–70. 10.1053/j.ajkd.2012.02.332 [PubMed] [Google Scholar]
76. Сун К., Цзян С., Ши И. и др. Заместительная почечная терапия для профилактики контраст-индуцированного острого повреждения почек: метаанализ рандомизированных контролируемых исследований. Am J Нефрол. 2010; 32: 497–504. 10.1159/000321344 [PubMed] [Google Scholar]
77. Tasanarong A, Vohakiat A, Hutayanon P, Piyayotai D. Новая стратегия альфа- и гамма-токоферола для предотвращения острого повреждения почек, вызванного контрастом, у пациентов с хронической болезнью почек, которым коронарные процедуры. Трансплантация нефролового циферблата. 2013;28:337–44. 10.1093/ndt/gfs525 [PubMed] [Google Scholar]
Диагностическое значение многослойной спиральной КТ при травме почки
Abstract
Компьютерная томография (КТ) наиболее часто используется как неинвазивный метод диагностики повреждений внутренних органов. Использование многосрезовой спиральной КТ становится все более популярным в диагностике травм из-за ее способности генерировать трехмерную объемную информацию. В данном исследовании оценивалась диагностическая ценность мультиспиральной компьютерной томографии (МСКТ) с усиленным сканированием при травме почки. Всего в период с января 2012 г. по февраль 2016 г. в одной больнице на юге Китая 126 пациентов с повреждением почек прошли МСКТ. на уровне I, 26 на уровне II, 42 на уровне III, 17 на уровне IV, 11 на уровне V. Результаты МСКТ с усиленным сканированием достигают 100% диагностической точности, что подтверждено хирургическими данными. Мы пришли к выводу, что расширенная МСКТ позволяет надежно обнаружить травму почки и связанные с ней повреждения органов или тканей, обеспечивая важную клиническую ценность для диагностики и классификации травмы почки или внутренних органов.
Использование многосрезовой спиральной КТ становится все более популярным в диагностике травм из-за ее способности генерировать трехмерную объемную информацию. В данном исследовании оценивалась диагностическая ценность мультиспиральной компьютерной томографии (МСКТ) с усиленным сканированием при травме почки. Всего в период с января 2012 г. по февраль 2016 г. в одной больнице на юге Китая 126 пациентов с повреждением почек прошли МСКТ. на уровне I, 26 на уровне II, 42 на уровне III, 17 на уровне IV, 11 на уровне V. Результаты МСКТ с усиленным сканированием достигают 100% диагностической точности, что подтверждено хирургическими данными. Мы пришли к выводу, что расширенная МСКТ позволяет надежно обнаружить травму почки и связанные с ней повреждения органов или тканей, обеспечивая важную клиническую ценность для диагностики и классификации травмы почки или внутренних органов.
1Введение
Заболеваемость внутренних органов значительно возрастает с увеличением числа пациентов, получивших травмы в результате дорожно-транспортных происшествий и падений во время строительства зданий в городской застройке в Шэньчжэне, городе на юге Китая [1]. Повреждение почек является третьим по частоте повреждением твердых органов при тупой травме живота, составляя 14,1% случаев повреждений живота, при этом на долю тупой травмы приходится до 70% [2]. Повреждения почек при тупой травме обычно возникают вследствие прямого удара в бок или от резкого торможения. Прямой удар раздавливает почку, вызывая разрыв или разрывы почечной паренхимы и приводя к субкапсулярной, внутрипочечной или паранефральной гематоме. Травма замедления вызывает острое напряжение почечной ножки, что приводит к разрыву почечной вены или артерии, разрыву интимы сосуда, вызывающему тромбоз или разрыв, или отрыву лоханочно-мочеточникового соединения (UPJ) [3].
Повреждение почек является третьим по частоте повреждением твердых органов при тупой травме живота, составляя 14,1% случаев повреждений живота, при этом на долю тупой травмы приходится до 70% [2]. Повреждения почек при тупой травме обычно возникают вследствие прямого удара в бок или от резкого торможения. Прямой удар раздавливает почку, вызывая разрыв или разрывы почечной паренхимы и приводя к субкапсулярной, внутрипочечной или паранефральной гематоме. Травма замедления вызывает острое напряжение почечной ножки, что приводит к разрыву почечной вены или артерии, разрыву интимы сосуда, вызывающему тромбоз или разрыв, или отрыву лоханочно-мочеточникового соединения (UPJ) [3].
Для диагностики внутренних органов, в том числе повреждения почек, часто используются несколько визуализационных исследований (таблица 1). Как один из простых подходов, УЗИ помогает определить степень повреждения почек, экстравазацию мочи и прогрессирование почечных заболеваний, таких как сморщивание почки с образованием фиброза на поздних стадиях после травмы. Тем не менее, ультразвуковое изображение ограничено в точности диагностики и оценки клинической степени [4-6]. Хотя внутривенная пиелография (ВВП) широко используется при исследовании заболеваний мочевыделительной системы, ее часто не выбирают при выявлении травмы почки, поскольку ВВП не позволяет выявить тупые поражения и точно стадировать некоторые виды повреждений почек [7]. Магнитно-резонансная томография (МРТ) обладает высокой точностью, но является дорогостоящей и трудоемкой, в частности, пациенты, спасаемые с помощью медицинского оборудования с металлическими материалами, ограничены. В качестве инвазивного метода ренальная ангиография ценна в диагностике повреждения почечных сосудов и повреждения почечной лоханки [8]. Используемая при оценке тупого повреждения почек, КТ обеспечивает точное определение и стадирование степени повреждения почек, что превосходит другие методы диагностики изображения [3, 9].]. Показаниями к визуализации почек у пациентов с травмой являются массивная гематурия, микроскопическая гематурия при шоке (систолическое артериальное давление [САД] <90 мм рт.
Тем не менее, ультразвуковое изображение ограничено в точности диагностики и оценки клинической степени [4-6]. Хотя внутривенная пиелография (ВВП) широко используется при исследовании заболеваний мочевыделительной системы, ее часто не выбирают при выявлении травмы почки, поскольку ВВП не позволяет выявить тупые поражения и точно стадировать некоторые виды повреждений почек [7]. Магнитно-резонансная томография (МРТ) обладает высокой точностью, но является дорогостоящей и трудоемкой, в частности, пациенты, спасаемые с помощью медицинского оборудования с металлическими материалами, ограничены. В качестве инвазивного метода ренальная ангиография ценна в диагностике повреждения почечных сосудов и повреждения почечной лоханки [8]. Используемая при оценке тупого повреждения почек, КТ обеспечивает точное определение и стадирование степени повреждения почек, что превосходит другие методы диагностики изображения [3, 9].]. Показаниями к визуализации почек у пациентов с травмой являются массивная гематурия, микроскопическая гематурия при шоке (систолическое артериальное давление [САД] <90 мм рт. ст.), микроскопическая гематурия с кровоподтеками на боку, переломы поперечных отростков нижних ребер и поясничного отдела позвоночника, проникающие травмы [10, 11]. . Предпочтительное лечение тупой травмы почки варьируется в зависимости от степени тяжести.
ст.), микроскопическая гематурия с кровоподтеками на боку, переломы поперечных отростков нижних ребер и поясничного отдела позвоночника, проникающие травмы [10, 11]. . Предпочтительное лечение тупой травмы почки варьируется в зависимости от степени тяжести.
Технология многосрезовой спиральной компьютерной томографии (МСКТ) предлагает дополнительные преимущества при обнаружении повреждений внутренних органов, поскольку она может получать изображения разной толщины из одного и того же набора данных. Более того, МСКТ с повышенной скоростью, тонкой коллимацией, большим объемом и исключительной гибкостью обеспечивает дополнительные преимущества по сравнению с однослойной спиральной КТ. Высококачественные интерактивные многоплоскостные и трехмерные (3D) реконструкции изображений требуют создания почти изотропных вокселей, достигаемых за счет увеличения пространственного разрешения по оси z. Скорость МСКТ позволяет визуализировать органы в четко определенные фазы перфузии [12]. МСКТ с высоким пространственным разрешением позволяет получить более подробную информацию о поврежденном органе или ткани, что приводит к улучшению обнаружения и характеристики тупых поражений в ткани почки.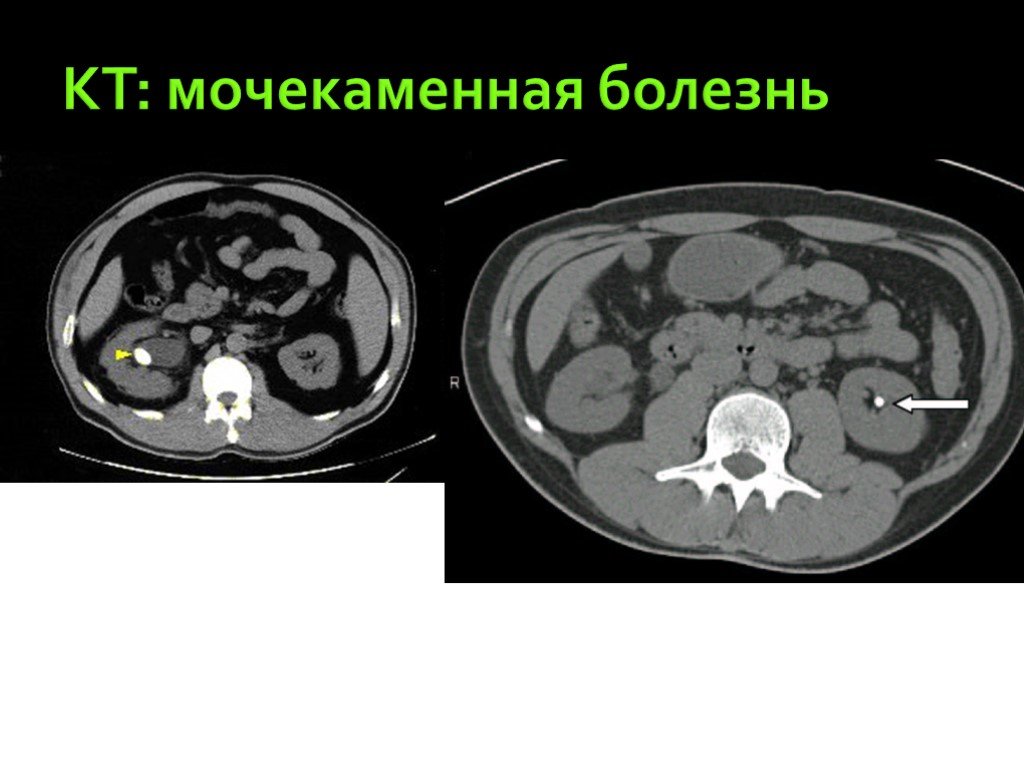 В этом исследовании мы ретроспективно проанализировали диагностику и классификацию качественной ценности МСКТ при травме почки.
В этом исследовании мы ретроспективно проанализировали диагностику и классификацию качественной ценности МСКТ при травме почки.
2Пациенты и методы
Всего было обследовано 126 пациентов (95 мужчин и 31 женщина). Средний возраст пациентов составил 32,6 года (возрастной диапазон от 14 до 61 года). Из общего числа больных 43 случая (34,1%) были связаны с дорожно-транспортным происшествием, 31 случай (24,6%) с падением с высоты, 22 случая (17,5%) с тупыми травмами, 13 случаев (10,3%) с проникающими ранениями, 17 случаев (13,5%). %) другие травмы (такие как патологическое повреждение почек и размозжение почки). Клинические проявления включали боль в пояснице, гематурию, образование в брюшной полости или шок. Все пациенты согласились с МСКТ-диагностикой и прошли курс лечения, в том числе 98 случаев консервативного лечения, 4 случая интервенционной терапии (эмболизация почечных артерий), 24 случая хирургического лечения. Нестабильные жизненные показатели (то есть мгновенные изменения частоты пульса, частоты дыхания и артериального давления) часто рассматривались как показатель для хирургического исследования.
Мультисрезовая КТ Light Speed VCT (GE в США) использовалась для выполнения сканирования или сканирования с усилением. Перед КТ внутривенно вводили неионогенное контрастное вещество (иоверсол) в дозе 350 мг/мл (80~100 мл) со скоростью потока 3,5 мл/с. Пациенты находились в положении лежа на спине при сканировании, а диапазон сканирования был от купола диафрагмы до лобкового симфиза. Время сканирования составляло 30 с в корковой фазе, 60 с в субстантивной фазе, 180 с в экскреторной фазе. Время задержки составляло 10-20 мин в зависимости от состояния изображения, отображаемого с контрастом у пациентов. Толщина сканируемого среза составляла 5 мм с толстым слоем реконструкции до 2,5 мм, а интервал реконструкции составлял 1,2 мм. Серия КТ-изображений была отправлена на рабочую станцию GE Advantage Workstation для трехмерной реконструкции с использованием методов многоплоскостной реорганизации (т.е. реконструкции, проекция максимальной плотности и проекция максимальной интенсивности).
3Результаты
Данные КТ при травмах почек включали контузию почки, подкапсульную гематому, разрыв кортикального слоя почки, перелом почки, разрушенную почку, травматическую окклюзию почечной артерии и травматический тромбоз вены (таблица 2). Все 126 пациентов согласились на МСКТ, в том числе 104 случая с расширенным сканированием и 45 случаев с индивидуальным сканированием для отсроченной фазы. В соответствии со стандартной оценкой Американской ассоциации травматологической хирургии (AAST) 1996 года по шкале оценки повреждений органов (OISI) травмы почек у всех пациентов были перечислены в Таблице 2 для оценки тяжести повреждения почек [11, 13]. При травме I степени из 30 случаев, 13 случаев с простой субкапсулярной и гематомой, почки имели изогнутый край или веретеновидную форму с несколько повышенной плотностью на КТ-изображениях; 11 случаев простой контузии почки имели отсроченную паренхиму почки мелким листком или полоской слабого усиления или без зоны усиления, но не вовлекали оболочку на изображения; 6 случаев имели оба признака изображения одновременно..jpg) При травме II степени в 26 случаях наблюдалась тень низкой плотности (менее или равная 10 мм) в почечной паренхиме, даже контрастное усиление в почечной паренхиме, а также имелись разрывы низкой плотности в околопочечной фасции из-за субкапсулярной или периренальной гематомы. (Рис. 1) При травме III степени в 42 случаях была низкая плотность (> 10 мм) в почечной паренхиме, но не вовлекалась собирательная система, а также неравномерная или искривленная высокая плотность после усиления контрастной инъекцией. При травме IV степени в 17 случаях наблюдалась утечка контрастного вещества в систему сбора из-за разрыва почечных сосудов, очагового инфаркта почки, гигантской периренальной гематомы или забрюшинной гематомы. Травма V степени, в 11 случаях наблюдались множественные разрывы почечной паренхимы, гигантская околопочечная гематома или обширная забрюшинная гематома, повреждение ножки почки или ампутация (рис. 2).
При травме II степени в 26 случаях наблюдалась тень низкой плотности (менее или равная 10 мм) в почечной паренхиме, даже контрастное усиление в почечной паренхиме, а также имелись разрывы низкой плотности в околопочечной фасции из-за субкапсулярной или периренальной гематомы. (Рис. 1) При травме III степени в 42 случаях была низкая плотность (> 10 мм) в почечной паренхиме, но не вовлекалась собирательная система, а также неравномерная или искривленная высокая плотность после усиления контрастной инъекцией. При травме IV степени в 17 случаях наблюдалась утечка контрастного вещества в систему сбора из-за разрыва почечных сосудов, очагового инфаркта почки, гигантской периренальной гематомы или забрюшинной гематомы. Травма V степени, в 11 случаях наблюдались множественные разрывы почечной паренхимы, гигантская околопочечная гематома или обширная забрюшинная гематома, повреждение ножки почки или ампутация (рис. 2).
При лечении травмы почки в группах с I по III в одном случае с множественными ножевыми ранениями с пневмотораксом слева, разрывом правой почки, геморрагическим шоком было проведено экстренное закрытое дренирование левой грудной полости и хирургическое исследование правой почки, а затем выполнена МСКТ-сканирование; остальные 97 случаев были безоперационными. При IV степени четырем пациентам была проведена селективная эмболизация почечных артерий, а в остальных 13 случаях была проведена операция. В 11 случаях V степени проведено оперативное лечение, включающее пластику почки, нефрэктомию, наложение анастомоза почечной лоханки и мочеточника, уретероскопическое стентирование, 1 пациент умер через 15 часов после операции в связи с тяжелым полиорганным поражением.
При IV степени четырем пациентам была проведена селективная эмболизация почечных артерий, а в остальных 13 случаях была проведена операция. В 11 случаях V степени проведено оперативное лечение, включающее пластику почки, нефрэктомию, наложение анастомоза почечной лоханки и мочеточника, уретероскопическое стентирование, 1 пациент умер через 15 часов после операции в связи с тяжелым полиорганным поражением.
4Обсуждение
Почки представляют собой парные забрюшинные структуры, лежащие против поясничных мышц, покрытые паранефральной жировой клетчаткой и окруженные фасцией Герота. Верхняя сторона почки защищена нижними ребрами. Однако нижние полюса почек уступают 12-му ребру и поэтому более подвержены травмам. Заболеваемость почечной недостаточностью составляет около 5/10 млн населения в год, около 72% составляют молодые люди в возрасте от 16 до 44 лет, а соотношение мужчин и женщин составляет около 3 : 1 [14]. Гематурия, боль в спине и низкое кровяное давление после травмы являются клиническими признаками травмы почки. Однако тяжесть гематурии и степень поражения почек не коррелируют. Иногда повреждение почки не проявляется гематурией в виде разрыва или отрыва почечной артерии. Около 24% больных с эмболизацией почечной артерии и повреждением почечной лоханки не имели гематурии [15]. Таким образом, визуальная диагностика имеет решающее значение для оценки состояния почечной недостаточности.
Однако тяжесть гематурии и степень поражения почек не коррелируют. Иногда повреждение почки не проявляется гематурией в виде разрыва или отрыва почечной артерии. Около 24% больных с эмболизацией почечной артерии и повреждением почечной лоханки не имели гематурии [15]. Таким образом, визуальная диагностика имеет решающее значение для оценки состояния почечной недостаточности.
Все случаи тупых и проникающих повреждений почек в этом исследовании классифицированы на основе Американской ассоциации хирургии травм (AAST). Эта классификация позволяет стандартизировать различные травмы почек и выбрать адекватную терапию и прогноз [16]. Медикаментозное лечение зависит от степени травмы почки. Недавние исследования показали, что большинство травм низкой степени тяжести можно лечить консервативно, в то время как повреждения высокой степени часто требуют хирургического вмешательства [17]. До 88% больных с III степенью и 78% с IV степенью получали консервативное лечение; пока 91% повреждений V степени нуждались в хирургическом лечении.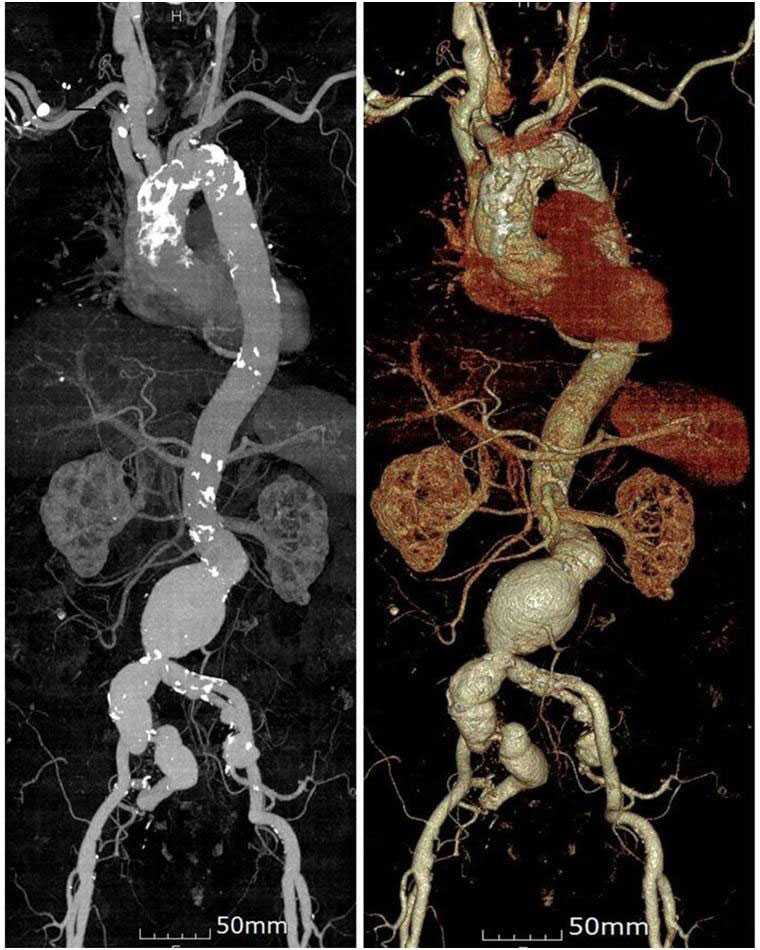 Частота нефрэктомии составила: 13% при III степени, 17% при IV степени и 9% при V степени; частота оперативного вмешательства в целом составляет 7% при всех тупых травмах почки [18]. Показаниями к лапаротомии являются стойкое угрожающее жизни кровотечение, повреждение почечной ножки, расширяющаяся или пульсирующая забрюшинная гематома, свидетельствующая о разрыве почечной артерии.
Частота нефрэктомии составила: 13% при III степени, 17% при IV степени и 9% при V степени; частота оперативного вмешательства в целом составляет 7% при всех тупых травмах почки [18]. Показаниями к лапаротомии являются стойкое угрожающее жизни кровотечение, повреждение почечной ножки, расширяющаяся или пульсирующая забрюшинная гематома, свидетельствующая о разрыве почечной артерии.
Лечение травмы почки обычно основано на точности диагностики изображений на КТ-изображениях. Являясь безопасным, неинвазивным и быстрым методом диагностики, МСКТ позволяет точно оценить каждую степень повреждения почки, определить наличие экстравазации мочи, периренального кровоизлияния и состояние смежного органа [19].]. КТ с контрастированием позволяет быстро определить состояние повреждения паренхимы почек как в артериальную, так и в венозную фазу, четко показать объем и степень поражения почки [20], сосудов почечной ножки. Усовершенствованная КТ обеспечивает прямое преобразование точности в трехмерные изображения, обеспечивая более точные и интуитивно понятные изображения повреждения почек (рис. 4). Кроме того, метод реконструкции почечных сосудов с помощью КТ-ангиографии (КТА) не только может обеспечить большинство обнаружений почечной артериографии, но также может предоставить точную информацию о стабильности гемодинамики и сосудистой интервенционной терапии [21, 22].
4). Кроме того, метод реконструкции почечных сосудов с помощью КТ-ангиографии (КТА) не только может обеспечить большинство обнаружений почечной артериографии, но также может предоставить точную информацию о стабильности гемодинамики и сосудистой интервенционной терапии [21, 22].
В этом исследовании результаты медицинского сканирования и хирургических операций в 104 случаях соответствуют 100%. Однако один пациент в критическом состоянии был обследован хирургическим путем из-за кровотечения из правой почки, выявленного при МСКТ (рис. 3а). Правая интактная почка выделена из-за разрыва поясничной артерии, обнаруженного во время операции (рис. 3б). На МСКТ-изображениях вытекание контраста из собирательной системы почек свидетельствует о разрыве почечной лоханки. Сканирование с задержкой можно использовать у пациентов со степенью поражения почек, чтобы определить, повреждена ли собирательная система или нет. В данном исследовании повреждение почечной лоханки и мочеточника было обнаружено у 6 из 37 больных, которым проводилось отсроченное сканирование.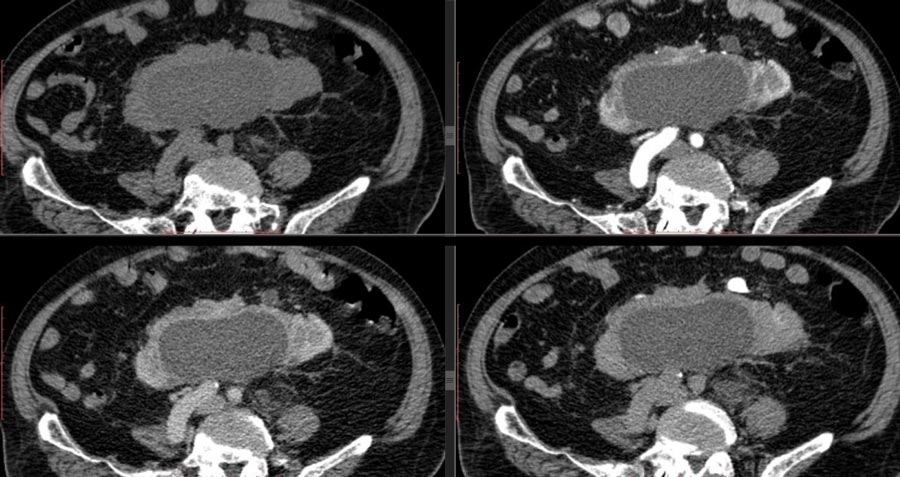 Все 6 пациентов выздоровели после своевременного адекватного лечения.
Все 6 пациентов выздоровели после своевременного адекватного лечения.
5Выводы
Надлежащее лечение травмы почки в значительной степени зависит от точного диагноза и качественной классификации повреждения почки. Трехмерная реконструкция изображения проводится на основе объема собранных данных, которые могут более интуитивно и точно выявить повреждение почек. МСКТ обеспечивает детальное изображение структур брюшной полости и забрюшинного пространства при исследовании травмы почки. Как предпочтительный метод визуализации, расширенная МСКТ обладает преимуществом высокой скорости сканирования, охватывая широкий диапазон изображений с высоким разрешением для острой стадии травмы. Однако диагностическая ценность MCST в функции и структурах почек спустя годы после травмы требует дальнейшего изучения.
Ссылки
[1] | Донгюн Л.
,
Вэй Г.
,
Дапинг В.
Диагностическое значение спиральной КТ закрытой травмы почки. HEBEI Medicine (06) ((2015)), 937–939. |
[2] | Маканинч Дж.В. , Сантуччи Р.А. Травмы почек и мочеточников, В: Gillenwater JY, Grayhack JT, Howwards SS, Mitchell ME, eds Adult andediatric Urology Philadelphia: Lippincott Williams & Wilkins, ((2002)), 479–506. |
[3] | Разали М.Р. , Азиан А.А. , Амран А.Р. и др., Компьютерная томография тупой травмы почки [J], Singapore Med J 51: (6) ((2010)), 468–473; викторина 474. |
[4] | Арагон Ф. , Пепе П. , Патан Д. и др., Лечение тяжелой тупой травмы почки у взрослых пациентов: 10-летний ретроспективный обзор больницы неотложной помощи [J]. BJU Int 110: (5) ((2012)), 744–748. |
[5] | Баверсток Р. , Саймонс Р. , Маклафлин М. Тяжелая тупая травма почки: 7-летний ретроспективный обзор провинциального травматологического центра [J]. Can J Urol 8: (5) ((2001)), 1372–1376. |
[6] | Забковский Т. |
[7] | Талл Э.Х. , Стоун Н.Н. , Ченг Д.Л. и др., Консервативное лечение проникающих и тупых повреждений почек III типа [J]. Бр Дж. Урол 77: (4) ((1996)), 512–517. |
[8] | Бент С. , Ингкаран Т. , Мощность Н. и др., Урологические повреждения после травмы. Clin Radiol 63: (12) ((2008)), 1361–1371. |
[9] | Флейшманн Д. Многорядная КТ-ангиография почечных и мезентериальных сосудов [J]. Eur J Radiol 45: (Приложение 1) ((2003)), S79–S87. |
[10] | Карпио Ф. , Морей А.Ф. Рентгенологическое стадирование повреждений почек [J]. World J Urol 17: (2) ((1999)), 66–70. |
[11] | Федерле М.П.
,
Кайзер Дж. |
[12] | Тиньков Г. , Эспозито Т.Дж. , Рид Дж. и др., Американская ассоциация хирургии травм органов, шкала I: селезенка, печень и почки, валидация на основе Национального банка данных о травмах [J]. J Am Coll Surg 207: (5) ((2008)), 646–655. |
[13] | Лин В.К. , Лин Ч.Х. , Чен Дж.Х. и др., Компьютерная томография при определении необходимости эмболизации при тяжелой тупой травме почки. J Trauma Acute Care Surg 74: (1) ((2013)), 230–235. |
[14] | Мур Э.Э. , Шакфорд С.Р. , Пачтер Х.Л. и др., Масштабирование повреждений органов: селезенка, печень и почки [J]. J Trauma 29: (12) ((1989)), 1664–1666. |
[15] | Алонсо Р.К.
,
Насента С.Б.
,
Мартинес П.Д.
и др., Почка в опасности: КТ-признаки тупой и проникающей травмы почки [J]. |
[16] | Бакли Дж. К. , Маканинч Дж.В. Пересмотр действующей системы классификации Американской ассоциации хирургии травм почек [J]. J Trauma 70: (1) ((2011)), 35–37. |
[17] | Сантуччи Р.А. , Маканинч Дж. М. Травмы почек IV степени: оценка, лечение и исход. World J Surg 25: (12) ((2001)), 1565–1572. |
[18] | Ашебу С.Д. , Дахния М.Х. , Адух П. и др., Разрыв почечной лоханки гидронефроза лоханочно-мочеточникового соединения после тупой травмы живота [J]. Australas Radiol 48: (2) ((2004)), 256–258. |
[19] | Онвубико С. , Муни Д.П. Ценность официальной переинтерпретации результатов компьютерной томографии травм из направляющих больниц[J]. J Pediatr Surg 51: (3) ((2016)), 486–489. |
[20] | Фрейзер Дж.Д.
,
Агуайо П. |
[21] | Смитсон Л. , Моррел Дж. , Ковалик У. и др., Корреляция компьютерно-томографических признаков гипоперфузии и клинической гипоперфузии у взрослых пациентов с тупой травмой [J]. J Trauma Acute Care Surg 78: (6) ((2015)), 1162–1167. |
[22] | Пуиг С. , Шефер-Прокоп С. , Ман Т. и др., Одно- и многослойная спиральная компьютерная томография почек у детей [J]. Eur J Radiol 43: (2) ((2002)), 139–145. |
Рисунки и таблицы
Рис.1
Колотая рана левой почки.
Рис.2
Перелом 11-го ребра слева и деваскуляризация ножки левой почки.
Рис. 3
(а) Правая почка увеличена из-за травмы. (b) Хирургическое исследование показало полную правую почку (кровоизлияние в луночную артерию).
Рис.4
Таблица 1
Сравнение различных методов обследования при повреждении почек
Таблица 2
Шкала травмы почки при многосрезовой спиральной КТ

- Евгений станиславович: Сжёнов Евгений Станиславович — Национальный исследовательский университет «Высшая школа экономики»
- Массаж сладкий: Медовый массаж – сладкая польза для всего организма




 ,
Скиба Р.
,
Сарацин М.
и др., Анализ травмы почки у взрослых пациентов: 6-летний собственный опыт травматологического центра [J]. Урол Ж. 12: (4) ((2015) ), 2276–2279.
,
Скиба Р.
,
Сарацин М.
и др., Анализ травмы почки у взрослых пациентов: 6-летний собственный опыт травматологического центра [J]. Урол Ж. 12: (4) ((2015) ), 2276–2279. А.
,
Маканинч Дж.В.
и др., Роль компьютерной томографии при травме почки [J]. Радиология 141: (2) ((1981) ), 455–460.
А.
,
Маканинч Дж.В.
и др., Роль компьютерной томографии при травме почки [J]. Радиология 141: (2) ((1981) ), 455–460. Рентгенография 29: (7) ((2009)), 2033–2053.
Рентгенография 29: (7) ((2009)), 2033–2053. ,
Остли Д.Дж.
и др., Обзор данных о лечении тупой травмы почки у детей [J]. Pediatr Surg Int 25: (2) ((2009)), 125–132.
,
Остли Д.Дж.
и др., Обзор данных о лечении тупой травмы почки у детей [J]. Pediatr Surg Int 25: (2) ((2009)), 125–132.