Окклюзия цас: диагностика и лечение в Москве, цена
Лечение окклюзии центральной артерии сетчатки глаза в Москве
Окклюзия центральной артерии сетчатки – тяжелое нарушение в главной артерии сетчатки глаза. Причинами заболевания являются тромбоз, спазмы, различного рода кровотечения или травмы. Поражает один глаз, но в редких случаях бывает и двустороннее поражение. У людей молодого возраста окклюзия развивается на фоне сердечных заболеваний, при спазме, дистонии, тромбозе сосудов. У больных среднего возраста заболевание чаще развивается на фоне гипертонической болезни, экзогенных и эндогенных отравлений организма. Заболевание носит внезапный характер с ухудшением зрения и ограничением полей зрения.В десяти процентах наступает кратковременная слепота. Происходит ишемический отек сетчатки ярко выраженным красным пятном в макулярной зоне. Зрительный нерв на начальной стадии заболевания имеет розоватый оттенок, края его немного сглажены. Артериолы узкие и имеют различный калибр. В начале заболевания появляются эмболы: плотные, холестериновые и фибринозные образования. Причиной возникновения окклюзии могут стать: артериальная гипертензия, сахарный диабет, и очень редко, как следствие — воспалительные заболевания сосудов.
Причиной возникновения окклюзии могут стать: артериальная гипертензия, сахарный диабет, и очень редко, как следствие — воспалительные заболевания сосудов.
Симптомы окклюзии
Симптомы заболевания: безболезненная потеря зрения одного глаза, затем через пятнадцать минут в середине глазного дна возникает больших размеров с неровными краями в форме овала, серо-белый очаг помутнения в сетчатке . Очаг распространяется на желтое пятно и захватывает область вокруг диска зрительного нерва. Желтое пятно не меняет цвета. Артерии сетчатки имеют форму четок.Диагноз обычно устанавливается на основании жалоб пациента. Проверяется острота зрения и поле зрения, назначается биохимический анализ крови. По результатам офтальмоскопии проводится дифферинциальный диагноз с тяжёлым нарушением кровообращения в сосудах зрительного нерва. Для эффективного лечения назначается флуоресцентная ангиография глазного дна и лазерная ретинометрия.
Лечение окклюзии
Лечение начинается сразу же после проведения диагностики. В положении лежа больному, очень медленно вводится раствор эуфиллина или глюкозы. Результативным методом лечения является внутривенное капельное введение сермиона. Внутрь назначаются мочегонные препараты.Эффективным считается и массаж глазного яблока через веко. Веко смазывается вазелином, а пальцами большим и указательным делают поглаживающие движения от центра роговицы к экватору глаза. Также круговыми движениями слегка надавливают через веко на глазное яблоко. Массаж длится от двух до пяти минут. Как один из способов лечения – это обогащение артериальной крови кислородом путем вдыхания газовой смеси, состоящей из девяноста пяти процентов кислорода и пяти процентов углекислого газа. В случае непроходимости центральной артерии сетчатки зрение восстанавливается лишь у тех больных, у которых лечение начато не позже сорока минут от начала заболевания.В результате плохого кровоснабжения, начинается процесс атрофии зрительного нерва. Очень редко, но весьма тяжелым осложнением может стать появление вторичной глаукомы, что вызывает полную потерю зрения, без восстановления.
В положении лежа больному, очень медленно вводится раствор эуфиллина или глюкозы. Результативным методом лечения является внутривенное капельное введение сермиона. Внутрь назначаются мочегонные препараты.Эффективным считается и массаж глазного яблока через веко. Веко смазывается вазелином, а пальцами большим и указательным делают поглаживающие движения от центра роговицы к экватору глаза. Также круговыми движениями слегка надавливают через веко на глазное яблоко. Массаж длится от двух до пяти минут. Как один из способов лечения – это обогащение артериальной крови кислородом путем вдыхания газовой смеси, состоящей из девяноста пяти процентов кислорода и пяти процентов углекислого газа. В случае непроходимости центральной артерии сетчатки зрение восстанавливается лишь у тех больных, у которых лечение начато не позже сорока минут от начала заболевания.В результате плохого кровоснабжения, начинается процесс атрофии зрительного нерва. Очень редко, но весьма тяжелым осложнением может стать появление вторичной глаукомы, что вызывает полную потерю зрения, без восстановления. Наблюдается резкое повышение глазного давления, сопровождающееся болью и воспалительным процессом. Для приостановки развития глаукомы назначается лазерное лечение, хотя эти действия не восстановят потерю зрения. Все больные, которые перенесли это заболевание, проходят обследование у терапевта, чтобы выявить и предупредить заболевания, которые непосредственно угрожают жизни – инфаркт миокарда и мозговой инсульт.Наша клиника «Добромед» предлагает широкий спектр услуг по лечению и профилактике многих заболеваний глаз. В нашем центре работают высококвалифицированные специалисты с многолетним стажем работы не только в нашей стране, но и за рубежом. Мы используем только самые современные и передовые методы и технологии в лечении заболеваний, которые известны человечеству. Успеху лечения в нашей клинике способствует также высокоточная диагностическая и лечебная аппаратура, благодаря которой мы выставляем диагнозы максимально точно и быстро. В ответ о нашей работе, приятно видеть тысячи здоровых и счастливых глаз наших клиентов!
Наблюдается резкое повышение глазного давления, сопровождающееся болью и воспалительным процессом. Для приостановки развития глаукомы назначается лазерное лечение, хотя эти действия не восстановят потерю зрения. Все больные, которые перенесли это заболевание, проходят обследование у терапевта, чтобы выявить и предупредить заболевания, которые непосредственно угрожают жизни – инфаркт миокарда и мозговой инсульт.Наша клиника «Добромед» предлагает широкий спектр услуг по лечению и профилактике многих заболеваний глаз. В нашем центре работают высококвалифицированные специалисты с многолетним стажем работы не только в нашей стране, но и за рубежом. Мы используем только самые современные и передовые методы и технологии в лечении заболеваний, которые известны человечеству. Успеху лечения в нашей клинике способствует также высокоточная диагностическая и лечебная аппаратура, благодаря которой мы выставляем диагнозы максимально точно и быстро. В ответ о нашей работе, приятно видеть тысячи здоровых и счастливых глаз наших клиентов!
Направления лечения
Лазерная офтальмология
- Офтальмология
- Терапия
- Косметология
- Хирургия
- Диагностика
Лазерный центр на Волоколамке
Записаться на приём: +7 (4822) 32-41-94Лазерный центр на Радищева
медицинская косметология
Записаться на приём: +7 (4822) 35-39-60Острое нарушение кровообращения в центральной артерии сетчатки (ЦАС) и ее ветвях.
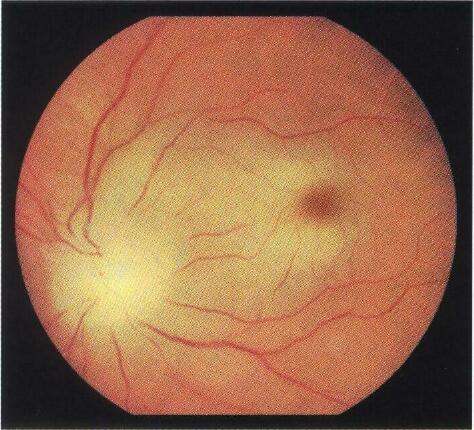
Заболевание начинается внезапным стойким снижением зрения, сужением и секторальным выпадением поля зрения. В основе непроходимости артерии лежат такие состояния как спазм, эмболия, артерииты и тромбоз.
Причины эмболии:
1. Тромбоэмболия может возникать при инфаркте миокарда (вследствие пристеночного тромбообразования), ревматических процессах на клапанах, а также при атеросклеротическом поражении сонных артерий (общей или внутренней).
2. Микробная эмболия возможна при бактериальном эндокардите.
3. Холестериновая эмболия обусловлена распадом атеросклеротической бляшки общей или внутренней сонной артерии.
4. Тромбоэмболии при сердечно – сосудистой патологии: трепетание предсердий, мерцательная аритмия.
5. Более редкие причины окклюзии центральной артерии сетчатки — артерииты или невриты зрительного нерва, приводящие к облитерации сосудов.
6. Также возможна жировая эмболия при переломе крупных трубчатых костей (бедренной, тазовой, плечевой).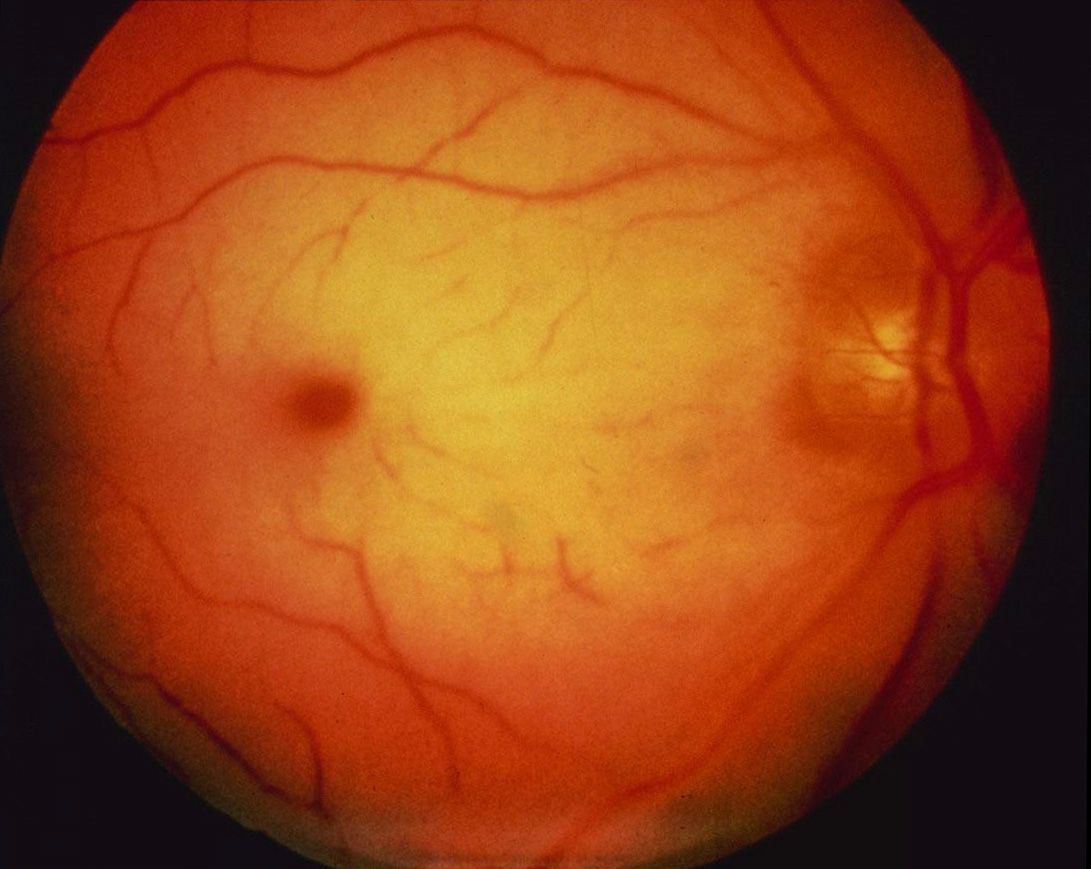
Последствиями острой непроходимости ЦАС является первичная атрофия зрительного нерва, вторичная центральная дегенерация сетчатки и резкое сужение сосудов сетчатки.
Эффективное лечение возможно (медикаментозное, хирургическое и лазерное) в первые часы (в редких случаях в первые сутки) после начала заболевания.
биомикроскопия
ангиография
сразу после ЛКС
через 1,5 месяца
У отдельных пациентов при наличии дополнительной функционирующей (цилиоретинальной) артерии в соответствующей зоне сохраняется небольшой участок практически неизмененной сетчатки. Иногда в таких случаях сохраняется достаточно высокая острота зрения (но поле зрения резко сужено).
Лечение:
Необратимое поражение сетчатки развивается через 1-1,5 ч после полного прекращения артериального кровотока в сетчатке. Поскольку окклюзия редко бывает полной, следует предпринять попытку восстановления кровотока в центральной артерии сетчатки (если длительность снижения остроты зрения составляет менее 24 часов).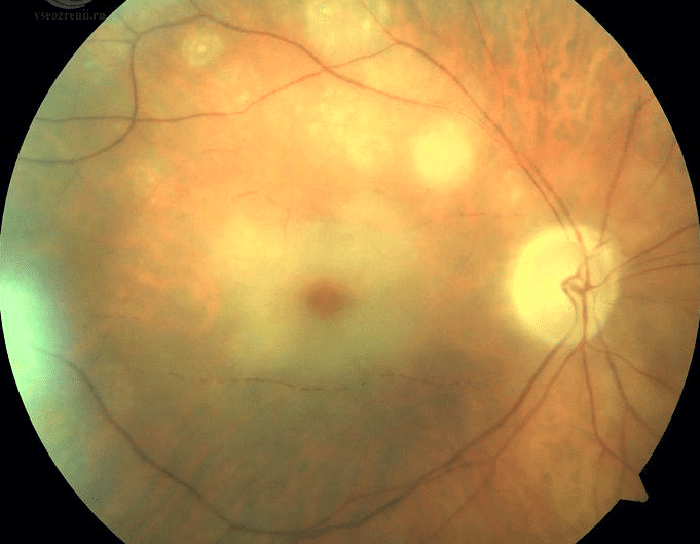
Задача лечения — расширение сосудов и смещение эмбола в более периферические артериальные ветви.
• Пациент должен находиться в положении лежа на спине, чтобы увеличить кровоток в сетчатке.
• Внутриглазное давление следует снизить при помощи массажа глазного яблока, парацентеза передней камеры и приема внутрь 2 таблеток диакарба по 250 мг.
• Спазм артерии устраняют путем внутривенной инъекции 2 мл 2% раствора папаверина, нитроглицерин под язык.
• Вазоконстрикцию артерий сетчатки предотвращают, давая пациенту вдыхать смесь 95% кислорода и 5% углекислого газа (карбоген) в течение 10 мин каждые 2 ч.
• Фибринолитическая терапия (стрептокиназа, гемаза) эффективна в умелых руках и в нашей стране широкого распространения не получила.
При выявлении рубеоза (неоваскуляризации) радужки выполняют панретинальную лазеркоагуляцию сетчатки.
Лечение почти окклюзии внутренней сонной артерии: необходимость в обновленных данных
1. Члены группы авторов, Mozaffarian D, Benjamin EJ, et al. Обновление статистики сердечных заболеваний и инсультов за 2016 год: отчет Американской кардиологической ассоциации.
Тираж
2016;133:e38-360. Опечатка в: Исправление. [Тираж. 2016]. [PubMed] [Google Scholar]
Обновление статистики сердечных заболеваний и инсультов за 2016 год: отчет Американской кардиологической ассоциации.
Тираж
2016;133:e38-360. Опечатка в: Исправление. [Тираж. 2016]. [PubMed] [Google Scholar]
2. Клиническое предупреждение: преимущества каротидной эндартерэктомии у пациентов с выраженным стенозом внутренней сонной артерии. Национальный институт неврологических расстройств и инсульта Отделение инсульта и травм. Североамериканские исследователи симптоматической каротидной эндартерэктомии (NASCET). Гладить 1991;22:816-7. 10.1161/01.STR.22.6.816 [PubMed] [CrossRef] [Google Scholar]
3. Morgenstern LB, Fox AJ, Sharpe BL, et al. Риски и преимущества каротидной эндартерэктомии у пациентов с близкой окклюзией сонной артерии. Североамериканская группа по исследованию симптоматической каротидной эндартерэктомии (NASCET). неврология 1997;48:911-5. 10.1212/WNL.48.4.911 [PubMed] [CrossRef] [Google Scholar]
4. Rothwell PM, Eliasziw M, Gutnikov SA, et al.
Анализ объединенных данных рандомизированных контролируемых исследований эндартерэктомии при симптоматическом каротидном стенозе.
5. Rothwell PM, Eliasziw M, Gutnikov SA, et al. Эндартерэктомия при симптоматическом каротидном стенозе в зависимости от клинических подгрупп и сроков операции. Ланцет 2004;363:915-24. 10.1016/S0140-6736(04)15785-1 [PubMed] [CrossRef] [Google Scholar]
6. Aboyans V, Ricco JB, Bartelink MEL, et al. Выбор редакции — Руководство ESC по диагностике и лечению заболеваний периферических артерий, 2017 г., разработанное в сотрудничестве с Европейским обществом сосудистой хирургии (ESVS). Eur J Vasc Endovasc Surg 2018;55:305-68. 10.1016/j.ejvs.2017.07.018 [PubMed] [CrossRef] [Google Scholar]
7. Meershoek AJA, de Vries EE, Veen D, et al. Метаанализ результатов лечения внутренней сонной артерии вблизи окклюзии. Бр Дж Сург 2019;106:665-71. 10.1002/bjs.11159 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
8. Mylonas SN, Antonopoulos CN, Moulakakis KG, et al.
Ведение пациентов с почти полной окклюзией внутренней сонной артерии: обновленный метаанализ. Энн Васк Сург
2015;29:1664-72. 10.1016/j.avsg.2015.05.015 [PubMed] [CrossRef] [Google Scholar]
Энн Васк Сург
2015;29:1664-72. 10.1016/j.avsg.2015.05.015 [PubMed] [CrossRef] [Google Scholar]
9. Stroup DF, Berlin JA, Morton SC, et al. Метаанализ обсервационных исследований в эпидемиологии: предложение для отчета. Группа метаанализа обсервационных исследований в эпидемиологии (MOOSE). ДЖАМА 2000; 283:2008-12. 10.1001/jama.283.15.2008 [PubMed] [CrossRef] [Google Scholar]
10. Стюарт А., Орд К. Передовая теория статистики Кендалла. London: Edward Arnold, 1994. [Google Scholar]
11. DerSimonian R, Laird N. Повторный взгляд на метаанализ клинических испытаний. Испытания Contemp Clin 2015;45:139-45. 10.1016/j.cct.2015.09.002 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12. Berman SS, Bernhard VM, Erly WK, et al. Критический стеноз сонной артерии: диагностика, сроки операции, исход. Джей Васк Сург 1994; 20:499-508; обсуждение 508-10. 10.1016/0741-5214(94)
-7 [PubMed] [CrossRef] [Google Scholar]
13. Desole A, Campanile F, Tosato F, et al. Хирургическое лечение псевдоокклюзии внутренней сонной артерии.
Interact Cardiovasc Thorac Surg
2015;20:636-40. 10.1093/icvts/ivv016 [PubMed] [CrossRef] [Google Scholar]
Хирургическое лечение псевдоокклюзии внутренней сонной артерии.
Interact Cardiovasc Thorac Surg
2015;20:636-40. 10.1093/icvts/ivv016 [PubMed] [CrossRef] [Google Scholar]
14. Fredericks RK, Thomas TD, Lefkowitz DS, et al. Значение знака ангиографической струны при атеросклерозе сонных артерий. Гладить 1990;21:476-9. 10.1161/01.STR.21.3.476 [PubMed] [CrossRef] [Google Scholar]
15. Greiner C, Wassmann H, Palkovic S, et al. Операции реваскуляризации при псевдоокклюзии внутренней сонной артерии. Acta Neurochir (Вена) 2004; 146:237-43; обсуждение 243. 10.1007/s00701-004-0216-5 [PubMed] [CrossRef] [Google Scholar]
16. Hirata Y, Sakata N, Tsuchimochi H, et al. Каротидная эндартерэктомия при псевдоокклюзии шейной внутренней сонной артерии. Acta Neurochir Suppl 2014;119:91-6. [PubMed] [Google Scholar]
17. Kniemeyer HW, Aulich A, Schlachetzki F, et al.
Псевдо- и сегментарная окклюзия внутренней сонной артерии: новая классификация, оперативное лечение и результаты. Eur J Vasc Endovasc Surg
1996;12:310-20. 10.1016/S1078-5884(96)80250-4 [PubMed] [CrossRef] [Google Scholar]
Eur J Vasc Endovasc Surg
1996;12:310-20. 10.1016/S1078-5884(96)80250-4 [PubMed] [CrossRef] [Google Scholar]
18. Meershoek AJA, Vonken EPA, Nederkoorn PJ, et al. Каротидная эндартерэктомия у пациентов с рецидивирующими симптомами, связанными с близкой окклюзией ипсилатеральной сонной артерии с полным коллапсом. Джей Нейрол 2018; 265:1900-5. 10.1007/s00415-018-8939-z [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
19. Ogata T, Yasaka M, Kanazawa Y, et al. Исходы, связанные с псевдоокклюзией сонных артерий. Цереброваскулярный дис 2011;31:494-8. 10.1159/000324385 [PubMed] [CrossRef] [Google Scholar]
20. Pulli R, Frosini P, Gatti M, et al. Псевдоокклюзия внутренней сонной артерии: ранние и отдаленные результаты. J Cardiovasc Surg (Турин) 1997;38:15-20. [PubMed] [Google Scholar]
21. Regina G, Testini M, Fullone M, et al. Псевдоокклюзия внутренней сонной артерии: отчет о 15 случаях и обзор литературы. Инт Ангиол 1997; 16:147-50. [PubMed] [Google Scholar]
22. Ringelstein EB, Berg-Dammer E, Zeumer H. Так называемая атероматозная псевдоокклюзия внутренней сонной артерии. Диагностическая и терапевтическая задача.
Нейрорадиология
1983;25:147-55. 10.1007/BF00455734 [PubMed] [CrossRef] [Google Scholar]
Ringelstein EB, Berg-Dammer E, Zeumer H. Так называемая атероматозная псевдоокклюзия внутренней сонной артерии. Диагностическая и терапевтическая задача.
Нейрорадиология
1983;25:147-55. 10.1007/BF00455734 [PubMed] [CrossRef] [Google Scholar]
23. Samson RH, Showalter DP, Yunis JP, et al. Цветное сканирование сонной нити может предотвратить ненужное хирургическое вмешательство. Кардиоваскулярный хирург 1999;7:236-41. 10.1016/S0967-2109(98)00123-9 [PubMed] [CrossRef] [Google Scholar]
24. Archie JP, Jr. Каротидная эндартерэктомия, когда дистальный отдел внутренней сонной артерии мал или плохо визуализируется. Джей Васк Сург 1994;19:23-30; обсуждение 30-1. 10.1016/S0741-5214(94)70117-2 [PubMed] [CrossRef] [Google Scholar]
25. Аккан К., Илгит Э., Онал Б. и др. Эндоваскулярное лечение близкой окклюзии внутренней сонной артерии: 30-дневный результат и долгосрочное наблюдение. Клин Нейрорадиол 2018;28:245-52. 10.1007/s00062-016-0546-8 [PubMed] [CrossRef] [Google Scholar]
26. Barker CM, Gomez J, Grotta JC, et al.
Возможности стентирования сонных артерий у больных с ангиографическим симптомом струны.
Катетер Cardiovasc Interv
2010;75:1104-9. [PubMed] [Google Scholar]
Barker CM, Gomez J, Grotta JC, et al.
Возможности стентирования сонных артерий у больных с ангиографическим симптомом струны.
Катетер Cardiovasc Interv
2010;75:1104-9. [PubMed] [Google Scholar]
27. Choi BS, Park JW, Shin JE, et al. Оценка результатов стентирования сонных артерий у пациентов из группы высокого риска с симптоматической окклюзией сонных артерий. Интерв Нейрорадиол 2010;16:309-16. 10.1177/159101991001600314 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
28. González A, Gil-Peralta A, Mayol A, et al. Стентирование внутренней сонной артерии у больных с близкой окклюзией: 30-дневные и отдаленные результаты. AJNR Am J Нейрорадиол 2011;32:252-8. 10.3174/ajnr.A2285 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
29. Nikas DN, Ghany MA, Stabile E, et al.
Стентирование сонных артерий с проксимальной церебральной защитой у пациентов с ангиографическими проявлениями стринг-симптома.
Интервью JACC Cardiovasc
2010;3:298-304. 10.1016/j. jcin.2009.11.018 [PubMed] [CrossRef] [Google Scholar]
jcin.2009.11.018 [PubMed] [CrossRef] [Google Scholar]
30. Oka F, Ishihara H, Kato S, et al. Церебральные гемодинамические преимущества после стентирования сонных артерий у пациентов с близкой окклюзией. Джей Васк Сург 2013;58:1512-7. 10.1016/j.jvs.2013.05.103 [PubMed] [CrossRef] [Google Scholar]
31. Razuk A, Caffaro R, Karakahanian W, et al. Знак каротидной струны: есть ли роль стентирования сонной артерии? 38-й ежегодный симпозиум Общества клинической сосудистой хирургии, Аризона, США, 2010 г. [Google Scholar]
32. Ruiz-Salmerón RJ, Gamero MA, Carrascosa C, et al. Стентирование сонных артерий: клинические и процедурные последствия почти окклюзионного стеноза. Неврология 2013;28:535-42. [PubMed] [Google Scholar]
33. Sakamoto S, Kiura Y, Kajihara Y, et al. Стентирование сонной артерии методом проксимальной или двойной защиты при близкой окклюзии шейной внутренней сонной артерии. Нейрохирург преподобный 2013;36:551-7; обсуждение 557-8. 10.1007/s10143-013-0481-y [PubMed] [CrossRef] [Google Scholar]
34. Сон С., Д.С. Чой, С.К. Ким и др.
Стентирование сонных артерий у пациентов с близкой окклюзией: одноцентровый опыт и сравнение с недавними исследованиями.
Клин Нейрол Нейрохирург
2013;115:1976-81. 10.1016/j.clineuro.2013.06.001 [PubMed] [CrossRef] [Google Scholar]
Сон С., Д.С. Чой, С.К. Ким и др.
Стентирование сонных артерий у пациентов с близкой окклюзией: одноцентровый опыт и сравнение с недавними исследованиями.
Клин Нейрол Нейрохирург
2013;115:1976-81. 10.1016/j.clineuro.2013.06.001 [PubMed] [CrossRef] [Google Scholar]
35. Spacek M, Martinkovicova L, Zimolova P, et al. Среднесрочные результаты стентирования сонных артерий у пациентов с ангиографическим симптомом струны. Катетер Cardiovasc Interv 2012;79:174-9. 10.1002/ccd.23144 [PubMed] [CrossRef] [Google Scholar]
36. Terada T, Tsuura M, Matsumoto H, et al. Эндоваскулярное лечение псевдоокклюзии внутренней сонной артерии. нейрохирургия 2006;59:301-9; обсуждение 301-9. 10.1227/01.NEU.0000222650.09509.DE [PubMed] [CrossRef] [Google Scholar]
37. Ascher E, Markevich N, Hingorani A, et al.
Псевдоокклюзии внутренней сонной артерии: обоснование лечения на основе модифицированного протокола дуплексного сканирования сонных артерий.
Джей Васк Сург
2002;35:340-5. 10.1067/mva. 2002.120379 [PubMed] [CrossRef] [Google Scholar]
2002.120379 [PubMed] [CrossRef] [Google Scholar]
38. Bowman JN, Olin JW, Teodorescu VJ, et al. Псевдоокклюзия сонной артерии: указывает ли конечно-диастолическая скорость на необходимость лечения? Васк эндоваскулярный хирург 2009;43:374-8. 10.1177/1538574409331696 [PubMed] [CrossRef] [Google Scholar]
39. Fox AJ, Eliasziw M, Rothwell PM, et al. Выявление, прогноз и лечение пациентов с окклюзией сонной артерии. AJNR Am J Нейрорадиол 2005; 26:2086-94. [Бесплатная статья PMC] [PubMed] [Google Scholar]
40. O’Leary DH, Mattle H, Potter JE. Атероматозная псевдоокклюзия внутренней сонной артерии. Гладить 1989;20:1168-73. 10.1161/01.STR.20.9.1168 [PubMed] [CrossRef] [Google Scholar]
41. Radak DJ, Tanaskovic S, Ilijevski NS, et al.
Эверсионная каротидная эндартерэктомия в сравнении с лучшим медикаментозным лечением симптоматических пациентов с почти полной окклюзией внутренней сонной артерии: проспективное нерандомизированное исследование.
Энн Васк Сург
2010;24:185-9. 10.1016/j.avsg.2009.07.010 [PubMed] [CrossRef] [Google Scholar]
10.1016/j.avsg.2009.07.010 [PubMed] [CrossRef] [Google Scholar]
42. Kim J, Male S, Damania D, et al. Сравнение каротидной эндартерэктомии и стентирования при симптоматической окклюзии внутренней сонной артерии. AJNR Am J Нейрорадиол 2019;40:1207-12. 10.3174/ajnr.A6085 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
43. Yan D, Tang X, Shi Z, et al. Периоперационные и последующие результаты стентирования сонных артерий и каротидной эндартерэктомии у пациентов с почти окклюзией сонных артерий. Энн Васк Сург 2019;59:21-7. 10.1016/j.avsg.2019.01.019 [PubMed] [CrossRef] [Google Scholar]
44. García-Pastor A, Gil-Núñez A, Ramirez-Moreno JM, et al. Ранний риск повторного инсульта у пациентов с симптоматической окклюзией сонных артерий: результаты многоцентрового регистрового исследования CAOS. Инт J Инсульт 2017;12:713-9. 10.1177/1747493017714177 [PubMed] [CrossRef] [Google Scholar]
45. Lippman HH, Sundt TM, Jr, Holman CB. Признак постстенотической тонкости сонных артерий: ложная гиполазия внутренней сонной артерии. Майо Клин Прок
1970;45:762-7. [PubMed] [Google Scholar]
Майо Клин Прок
1970;45:762-7. [PubMed] [Google Scholar]
46. Йоханссон Э., Фокс А.Дж. Каротидная близость к окклюзии: всесторонний обзор, часть 1 — определение, терминология и диагностика. AJNR Am J Нейрорадиол 2016;37:2-10. 10.3174/ajnr.A4432 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
47. Ricotta JJ, Aburahma A, Ascher E, et al. Обновленные рекомендации Общества сосудистой хирургии по лечению экстракраниального заболевания сонных артерий. Джей Васк Сург 2011;54:e1-31. 10.1016/j.jvs.2011.07.031 [PubMed] [CrossRef] [Google Scholar]
48. Эббот А.Л. Только медикаментозное (нехирургическое) вмешательство в настоящее время лучше всего подходит для профилактики инсульта, связанного с бессимптомным тяжелым каротидным стенозом: результаты систематического обзора и анализа. Гладить 2009;40:e573-83. 10.1161/STROKEAHA.109.556068 [PubMed] [CrossRef] [Google Scholar]
49. Abbott AL, Brunser AM, Giannoukas A, et al.
Заблуждения относительно адекватности лучшего медицинского вмешательства при бессимптомном каротидном стенозе.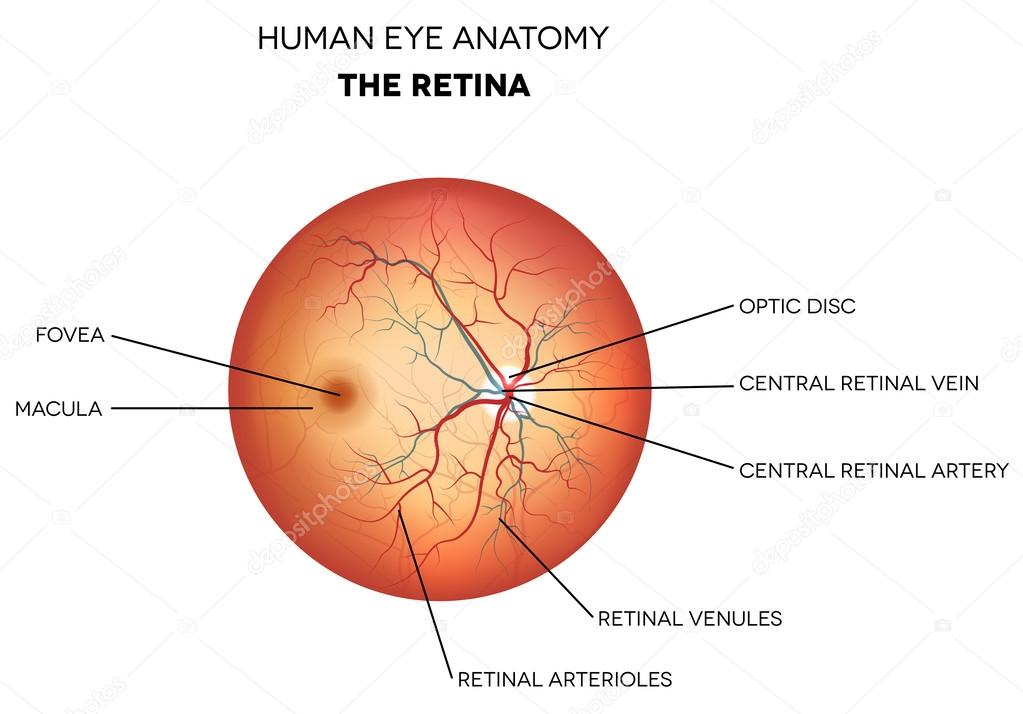 Джей Васк Сург
2020;71:257-69. 10.1016/j.jvs.2019.04.490 [PubMed] [CrossRef] [Google Scholar]
Джей Васк Сург
2020;71:257-69. 10.1016/j.jvs.2019.04.490 [PubMed] [CrossRef] [Google Scholar]
50. Параскевас К.И., Вейт Ф.Дж., Рикко Дж.Б. Одно только лучшее медикаментозное лечение может быть недостаточным для всех пациентов с бессимптомным стенозом сонных артерий. Джей Васк Сург 2018;68:572-5. 10.1016/j.jvs.2018.02.046 [PubMed] [CrossRef] [Google Scholar]
51. Xue S, Tang X, Zhao G, et al. Систематический обзор и обновленный метаанализ окклюзии сонных артерий. Энн Васк Сург 2020;66:636-645.e3. [PubMed] [Google Scholar]
52. Smout J, Macdonald S, Weir G, et al. Стентирование сонных артерий: взаимосвязь между опытом и частотой осложнений. Инт J Инсульт 2010;5:477-82. 10.1111/j.1747-4949.2010.00486.x [PubMed] [CrossRef] [Google Scholar]
53. Johansson E, Ohman K, Wester P. Симптоматическая окклюзия сонных артерий с полным коллапсом может привести к очень высокому риску инсульта. Джей Стажер Мед 2015; 277:615-23. 10.1111/joim.12318 [PubMed] [CrossRef] [Google Scholar]
Проксимальная эндоваскулярная окклюзия для CAS
Стентирование сонных артерий (CAS) является подтвержденным методом лечения для снижения частоты инсульта у пациентов с умеренными и тяжелыми клиническими симптомами сонных артерий. стенозом, а также среди лиц с тяжелым бессимптомным каротидным стенозом. CAS не уступает каротидной эндартерэктомии (CEA) в профилактике инсульта; следовательно, CAS считается адекватной альтернативой CEA, особенно у пациентов с повышенным риском CEA.
стенозом, а также среди лиц с тяжелым бессимптомным каротидным стенозом. CAS не уступает каротидной эндартерэктомии (CEA) в профилактике инсульта; следовательно, CAS считается адекватной альтернативой CEA, особенно у пациентов с повышенным риском CEA.
Из-за возникновения перипроцедурных неврологических ишемических событий использование устройств защиты от эмболии (EPD) во время CAS в настоящее время рекомендуется руководствами и считается, что оно частично отвечает за улучшение результатов. 1 Ни одно рандомизированное исследование не продемонстрировало безопасность и эффективность ЭПД, а ранний метаанализ продемонстрировал снижение риска инсульта или смерти при использовании этих устройств. 2,3
Устройства защиты от эмболии (ЭПЗ)
В продаже имеются два типа ЭПД:
- Дистальные фильтры. Они действуют путем размещения корзины дистальнее поражения с целью захвата эмболического мусора и в настоящее время наиболее часто используются в клинической практике.
 Они не блокируют церебральный кровоток и позволяют визуализировать целевые поражения во время развертывания стента, но обременены некоторым риском эмболии (возможное попадание мелких частиц в мозг) и возможными трудностями при извлечении
Они не блокируют церебральный кровоток и позволяют визуализировать целевые поражения во время развертывания стента, но обременены некоторым риском эмболии (возможное попадание мелких частиц в мозг) и возможными трудностями при извлечении - Проксимальные окклюзионные устройства (POD). Они останавливают или реверсируют поток, пережимая наружную и общую сонную артерии. Теоретически они более эффективны в предотвращении эмболии, потому что они обеспечивают нейропротекцию до пересечения очага поражения.
Проксимальные ЭПД
Единственным коммерчески доступным проксимальным ЭПД является система Mo.Ma (Medtronic), представляющая собой интродьюсер размером 8 или 9 Fr (рабочая длина 95 см), который вводится в общую сонную артерию (ОСА) через введение жесткой проволоки в наружную сонную артерию (ECA). Оболочка имеет дистальный баллон ECA и баллон CCA, расположенный на 60 мм проксимальнее кончика. Размер баллонов соответствует диаметру эталонного сосуда CCA от 5 до 13 мм и ECA от 3 до 6 мм.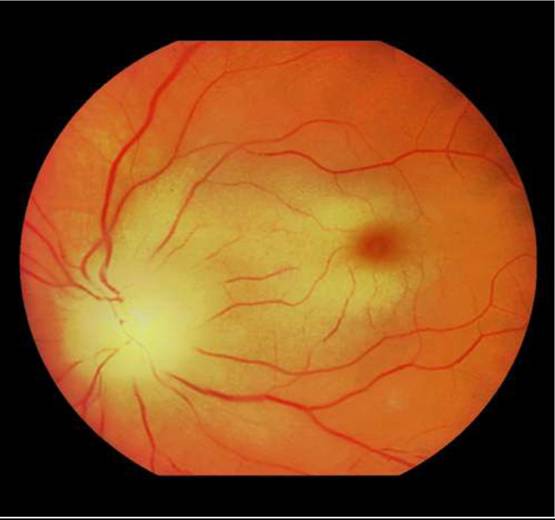 При надувании податливых баллонов как в ОСА, так и в НСА поток во внутренней сонной артерии (ВСА) останавливается. Между баллонами имеется рабочий канал с выходным портом. Кровь аспирируется вручную из интродьюсера, эффективно создавая прерывистое активное изменение направления потока. После остановки кровотока место поражения можно пересечь любым типом проволоки. При аспирации застойного столба крови захватываются как микро-, так и макроэмболы до возобновления антеградного кровотока. Наличие критического стеноза НСА не препятствует безопасному размещению устройства. 4
При надувании податливых баллонов как в ОСА, так и в НСА поток во внутренней сонной артерии (ВСА) останавливается. Между баллонами имеется рабочий канал с выходным портом. Кровь аспирируется вручную из интродьюсера, эффективно создавая прерывистое активное изменение направления потока. После остановки кровотока место поражения можно пересечь любым типом проволоки. При аспирации застойного столба крови захватываются как микро-, так и макроэмболы до возобновления антеградного кровотока. Наличие критического стеноза НСА не препятствует безопасному размещению устройства. 4
Клинический опыт применения проксимальных ЭПД
В проспективном одноцентровом итальянском регистре 1300 последовательных пациентов, которым выполняли КАС с использованием системы Mo.Ma, сообщалось о 30-дневном инсульте и уровне смертности 1,4%. . 5 Авторы обнаружили более высокий риск у пациентов с симптомами и у пациентов с высоким хирургическим риском. Независимыми предикторами неблагоприятного исхода были отсутствие опыта КАС, наличие симптоматического поражения и отсутствие клинической гипертензии. Следует отметить, что в этом регистре риск САС для пациентов старше 80 лет был таким же, как и для более молодых пациентов.
Независимыми предикторами неблагоприятного исхода были отсутствие опыта КАС, наличие симптоматического поражения и отсутствие клинической гипертензии. Следует отметить, что в этом регистре риск САС для пациентов старше 80 лет был таким же, как и для более молодых пациентов.
Исследование ARMOR, 6 — это проспективное многоцентровое исследование, в котором оценивалась 30-дневная безопасность и эффективность CAS у хирургических пациентов с высоким риском, использующих устройство Mo.Ma. Всего было зарегистрировано 34 (15%) симптомных и 188 (75%) бессимптомных пациентов (средний возраст: 74,7; мужчины: 66,7%; старше 80 лет: 29%). Стеноз контралатеральной сонной артерии >70% был критерием исключения. Частота 30-дневного инсульта, смерти и ИМ составила 2,7%, а частота 30-дневного инсульта — 0,9%. Авторы пришли к выводу, что устройство Mo.Ma безопасно и эффективно для хирургических пациентов с высоким риском, перенесших CAS.
Непереносимость проксимальных ЭПД
Проксимальные ЭПД действуют через окклюзию ОСА и подвергают ипсилатеральное полушарие головного мозга гипоперфузии с последующими преходящими неврологическими симптомами. Это явление называется непереносимостью окклюзии (НО) (определяется как любой преходящий неврологический дефицит, наблюдаемый во время окклюзии, но демонстрирующий полное восстановление в течение 20 минут после восстановления антеградного кровотока). 5
Это явление называется непереносимостью окклюзии (НО) (определяется как любой преходящий неврологический дефицит, наблюдаемый во время окклюзии, но демонстрирующий полное восстановление в течение 20 минут после восстановления антеградного кровотока). 5
В исследовании ARMOR НО развился у 13,8% пациентов после проксимального развертывания ЭПД, при этом у большинства симптомы исчезали в течение 20 минут (29у 31 пациента). 6 В итальянском едином центре регистратуры у 20% пациентов развился НО, что все еще позволяет завершить процедуру. Только четыре пациента (0,3%) не могли переносить проксимальную окклюзию с переходом на дистальную ЭПД или прерывистое пережатие. 5 Низкая частота ОИ объясняется кратковременностью пережатия артерий (3–15 мин) и частым наличием путей коллатерализации.
Способность заранее предсказать риск ОИ, который встречается относительно часто, может помочь операторам быть готовыми к этому событию.
Чтобы определить предикторы развития непереносимости окклюзии сонных артерий во время проксимальной защищенной КАС, Giugliano et al. проанализировали более 600 последовательных пациентов, перенесших КАС с использованием устройства Mo.Ma. 7 В этом исследовании НО наблюдался у 30,4% пациентов. Наиболее мощным независимым предиктором НО было давление окклюзии (ПД; давление, которое можно измерить во внутренней сонной артерии при надувании баллонов как ЭСА, так и ОСА) ≤40 мм рт. ст., а наиболее мощным клиническим предиктором такого ОП было наличие окклюзия контралатеральной ВСА. У пациентов с ОР >40 мм рт.ст. перипроцедурное падение артериального давления (≥50 мм рт.ст.) и/или удлиненное время окклюзии (время от надувания до сдувания проксимального баллона в ОСА) (≥300 с) повышают вероятность ОИ. 7
Проксимальные и дистальные ЭПД
Общепризнано, что ЭПД снижают риск инсульта из-за КАС. Проксимальные EPD могут обеспечить лучшую нейропротекцию, поскольку они эффективны на всех этапах процедуры, обладают высокой эффективностью захвата твердых частиц и лучшей эффективностью захвата крупных частиц.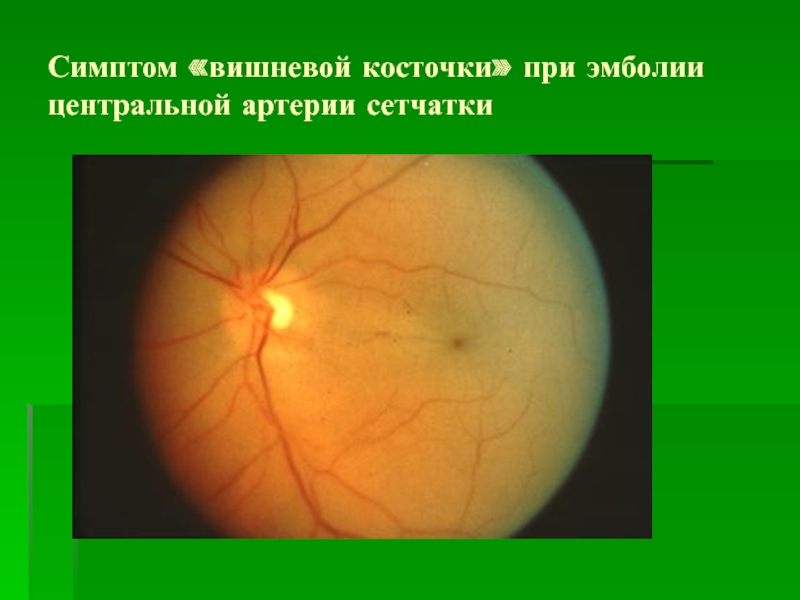
Эмболические сигналы (ES), измеренные с помощью транскраниальной допплерографии (TCD) во время процедуры, могут использоваться в качестве суррогатных маркеров атероэмболии. Рандомизированное исследование Mo.Ma по сравнению с дистальной EPD Filterwire EZ продемонстрировало меньшее количество микроэмболических сигналов (MES) при использовании устройства Mo.Ma на каждом этапе процедуры CAS. 8
Диффузионно-взвешенная магнитно-резонансная томография (ДВ-МРТ) является чувствительным инструментом для выявления церебральной эмболии после острых ишемических неврологических событий и для выявления немых ишемических поражений головного мозга после КЭА, стентирования и диагностической церебральной ангиографии. Рандомизированное клиническое исследование показало, что CAS с проксимальной EPD обеспечивает лучшую защиту головного мозга, чем дистальная EPD, на основании появления новых ишемических поражений, обнаруженных с помощью DW-MRI. 9 Эти результаты согласуются с данными, представленными Montorsi10, но другие исследования показали другие результаты. 11,12
11,12
Метаанализ доступных исследований 13 сравнил эффективность двух систем нейропротекции в предотвращении эмболизации во время КАС, обнаруженной с помощью ДВ-МРТ, оценивая частоту новых ишемических поражений на одного пациента во время процедуры с фильтры или проксимальная окклюзия баллона. У 357 пациентов, включенных в исследование, количество новых ишемических поражений на одного пациента, выявленных с помощью ДВ-МРТ, было значительно ниже при проксимальной баллонной окклюзии. После CAS частота новых ишемических поражений, обнаруженных на контралатеральном участке с помощью DW-MRI, была значительно ниже в группе проксимальной защиты. Этот метаанализ показывает, что использование проксимальной баллонной окклюзии во время КАС связано со значительным снижением количества дистальных эмболизаций по сравнению с использованием дистальных ЭПД. Важно отметить, что в некоторых исследованиях, включенных в этот метаанализ, отсутствовала информация об опыте оператора, который, как известно, влияет на результат. 14,15 Это, вместе с эхогенностью бляшки, конструкцией стента и реакцией пациента на медикаментозную терапию, может объяснить различия в дистальной эмболизации после КАС и расхождения между проанализированными исследованиями.
14,15 Это, вместе с эхогенностью бляшки, конструкцией стента и реакцией пациента на медикаментозную терапию, может объяснить различия в дистальной эмболизации после КАС и расхождения между проанализированными исследованиями.
Метаанализ отдельных пациентов продемонстрировал, что использование проксимальных ЭПД для нейропротекции у пациентов, перенесших КАС, было связано с очень низкой частотой тотального инсульта (1,71%) и комбинированных крупных неблагоприятных кардиальных и цереброваскулярных событий (MACCE; 2,25%) через 30 дней. 16 Отличные достигнутые результаты не зависят от пола пациента, симптоматического статуса и других исходных клинических характеристик, включая наличие окклюзии контралатеральной сонной артерии.
Только возраст пациента и диабетический статус пациента были определены среди исходных клинических характеристик пациента как независимые предикторы риска MACCE. Многочисленные предыдущие исследования с использованием дистальных EPD определили возраст пациента и симптоматический статус как предикторы риска MACCE при CAS.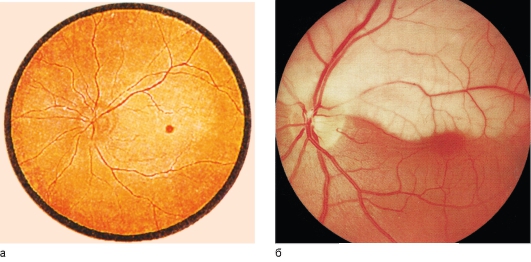 Тот факт, что симптоматический статус не является предиктором MACCE при использовании проксимальных ЭПД, предполагает, что различия в методах нейропротекции, обеспечиваемые каждым типом устройств, могут изменить или нейтрализовать некоторые потенциальные риски, особенно у пациентов с симптомами.
Тот факт, что симптоматический статус не является предиктором MACCE при использовании проксимальных ЭПД, предполагает, что различия в методах нейропротекции, обеспечиваемые каждым типом устройств, могут изменить или нейтрализовать некоторые потенциальные риски, особенно у пациентов с симптомами.
Более поздний метаанализ, включавший 12 281 пациента, не выявил существенной разницы между проксимальной и дистальной ЭПД с точки зрения частоты инсульта, 30-дневной смертности или частоты новых поражений головного мозга или контралатеральных поражений головного мозга, обнаруженных с помощью DW- МРТ. 17 В заключение, потенциальное превосходство проксимальных ЭПД до сих пор окончательно не доказано.
ЭПД при трансрадиальном и трансбрахиальном CAS
При сложной анатомии может потребоваться трансрадиальный (ТР) или трансбрахиальный (ТБ) доступ.
TR CAS с проксимальной защитой не получили широкого распространения из-за большого размера и жесткости устройства, что затрудняет доступ и навигацию по супрааортальным сосудам.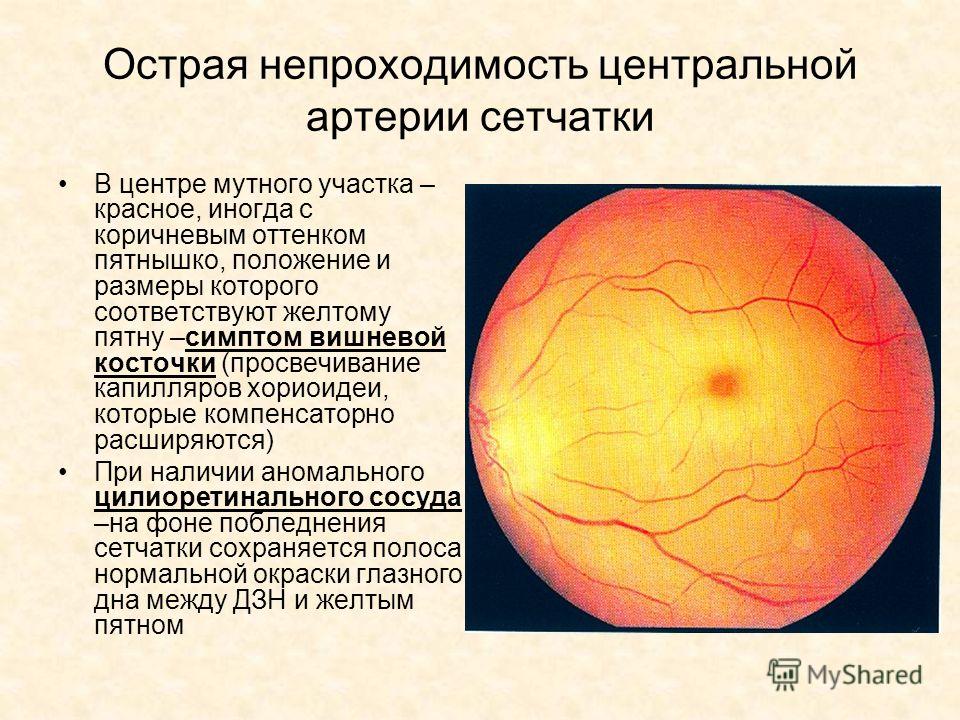 TB CAS является приемлемой альтернативой в отдельных случаях, но связана с более высоким уровнем сосудистых осложнений. Скорость перехода к подходу TF может быть хорошим индикатором осуществимости.
TB CAS является приемлемой альтернативой в отдельных случаях, но связана с более высоким уровнем сосудистых осложнений. Скорость перехода к подходу TF может быть хорошим индикатором осуществимости.
Montorsi 18 проанализировано 214 пациентов с КАС, получавших либо ТР (n=154), либо ТБ (n=60). Систему Mo.Ma использовали у 61 пациента (28%), а дистальную фильтрующую защиту — у 153 (72%) пациентов.
Переход на бедренный доступ потребовался у 1/61 (1,6%) пациента Mo.Ma по сравнению с 11/153 (7,1%) пациента с фильтром. Пациент с TR был переведен на фильтр, потому что система Mo.Ma была слишком короткой. Уровень MACCE составил 0% у пациентов с Mo.Ma и 2,8% в группе с фильтром. Основные сосудистые осложнения с одинаковой частотой в группах были ограничены противотуберкулезным подходом. Хроническая окклюзия лучевой артерии произошла у 6,6% пациентов с Mo.Ma и у 3,2% пациентов с фильтром.
Эти результаты подтверждают, что КАС с устройством проксимальной защиты через ТР или ТБ доступ возможен, безопасен и эффективен, с низкой частотой сосудистых осложнений.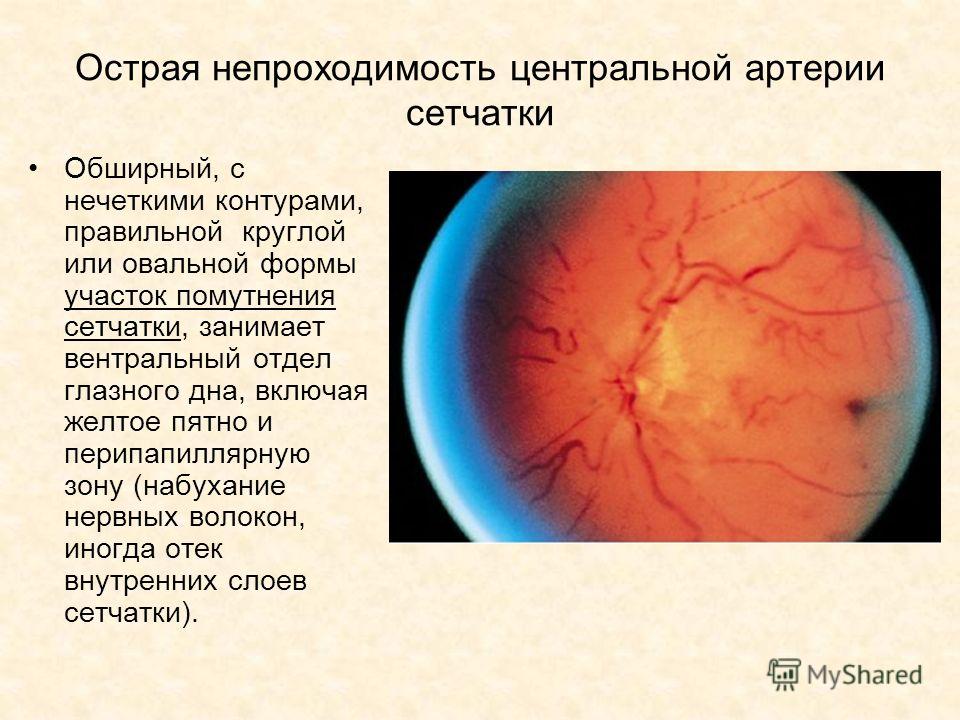
Выводы
Использование ЭПД во время процедуры CAS рекомендовано руководством для снижения риска перипроцедурного инсульта. POD безопасны и эффективны для улучшения результатов даже у хирургических пациентов с высоким риском, с очень высоким уровнем технического успеха и низким уровнем MACCE.
ОИ — возможное осложнение, которое можно прогнозировать, но редко требует перехода на альтернативную систему защиты и не прогнозирует MACCE.
Различные клинические исследования и исследования, основанные на визуализации, подтверждают идею о том, что проксимальная защищенная CAS обеспечивает более эффективную и надежную защиту головного мозга; к сожалению, эта концепция еще нуждается в окончательном подтверждении в клинической практике.
Ссылки
1 Brott TG et al. Руководство ASA/ACCF/AHA/AANN/AANS/ACR/ASNR/CNS/SAIP/SCAI/SIR/SNIS/SVM/SVS по ведению пациентов с поражением экстракраниальных сонных и позвоночных артерий. J Am Coll Cardiol 2011; 57: 1002–44.
J Am Coll Cardiol 2011; 57: 1002–44.
2 Touze E et al. Систематический обзор периоперационных рисков инсульта или смерти после каротидной ангиопластики и стентирования. Инсульт 2009; 40: e683–e693.
3 Гарг Н. и др. Церебральные защитные устройства уменьшают перипроцедурные инсульты во время каротидной ангиопластики и стентирования: систематический обзор современной литературы. Дж. Эндоваск, Тер 2009 г.;16:412–27.
4 Stabile E et al. Применение эндоваскулярного пережатия в качестве нейропротекции при каротидном стентировании при критическом ипсилатеральном стенозе наружной сонной артерии. Европейская интервенция 2008; 3 (5): 588–92.
5 Stabile E et al. Проксимальная эндоваскулярная окклюзия для стентирования сонных артерий: результаты проспективного регистра 1300 пациентов. J Am Coll Cardiol 2010; 55: 1661–7.
6 Ansel GM et al; Следователи для ключевого испытания ARMOR. Безопасность и эффективность устройства проксимальной защиты головного мозга INVATEC MO.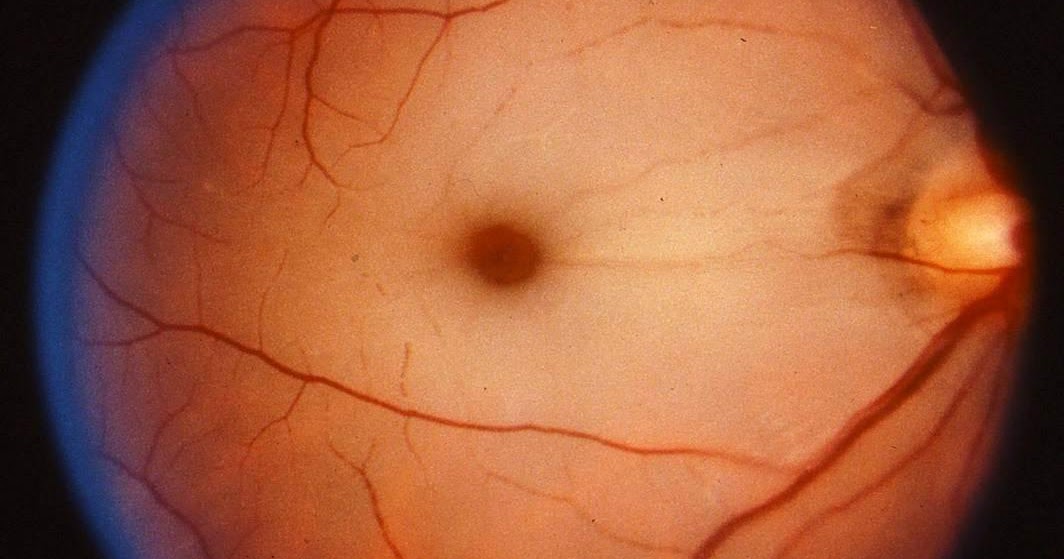 MA во время стентирования сонных артерий: результаты базового исследования ARMOR. Катетер Cardiovasc Interv 2010; 76: 1–8.
MA во время стентирования сонных артерий: результаты базового исследования ARMOR. Катетер Cardiovasc Interv 2010; 76: 1–8.
7 Джулиано Г и др. Предикторы непереносимости каротидной окклюзии при стентировании проксимальных защищенных сонных артерий. JACC Cardiovasc Interv 2014: 1237–44.
8 Schmidt A et al. Влияние двух различных систем нейропротекции на микроэмболизацию при стентировании сонных артерий. J Am Coll Cardiol 2004; 44 (10): 1966–9.
9 Bijuklic K et al. Исследование PROFI (Предотвращение церебральной эмболизации путем проксимальной окклюзии баллона по сравнению с защитой фильтра во время стентирования сонной артерии): проспективное рандомизированное исследование. J Am Coll Cardiol 2012; 59: 1383–9.
10 Montorsi P et al. Микроэмболизация при стентировании сонных артерий у пациентов с бляшками высокого риска, богатыми липидами. Рандомизированное исследование проксимальной и дистальной защиты головного мозга.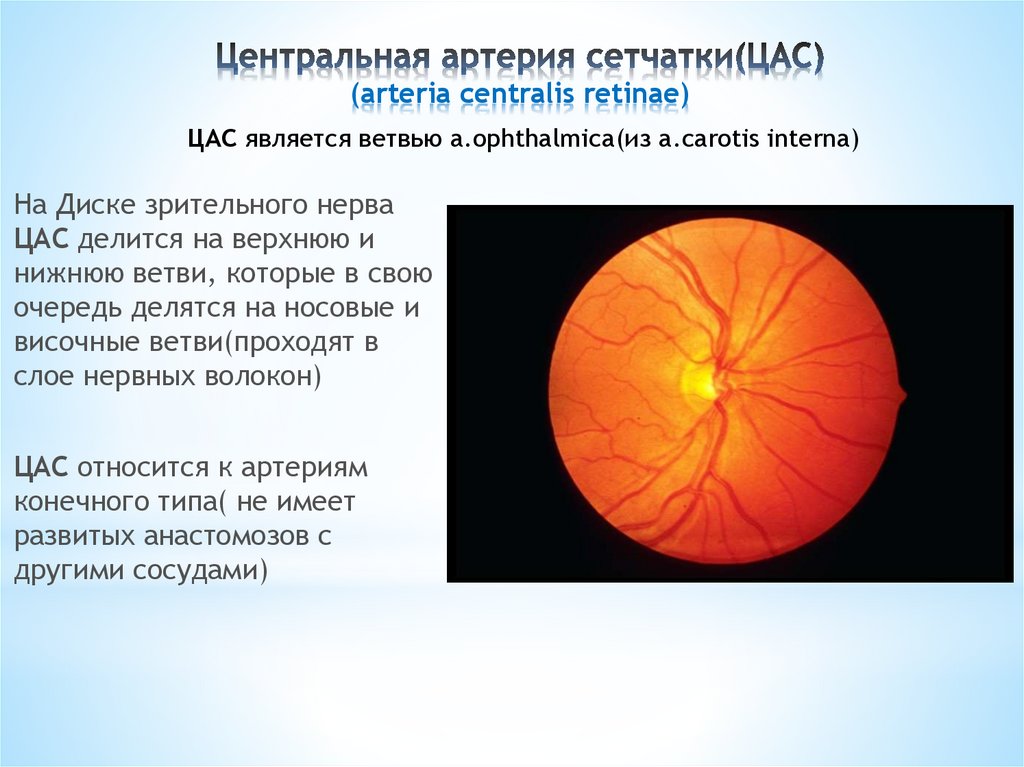 J Am Coll Cardiol 2011; 58: 1656–63.
J Am Coll Cardiol 2011; 58: 1656–63.
11 Cano MN et al. Рандомизированное сравнение дистальной и проксимальной защиты головного мозга при стентировании сонных артерий. JACC Cardiovasc Interv 2013;6:1203–9.
12 Castro-Afonso LH et al. Реверсирование потока в сравнении с защитой фильтром: экспериментальное рандомизированное исследование стентирования сонной артерии. Circ Cardiovasc Interv 2013; 6: 552–9.
13 Stabile E et al. Церебральные эмболические поражения, обнаруженные с помощью диффузионно-взвешенной магнитно-резонансной томографии после стентирования сонной артерии. Метаанализ 8 исследований, в которых сравнивали фильтрующую защиту головного мозга и проксимальную баллонную окклюзию. JACC Cardiovasc Interv 2014;7:1177–83.
14 Stabile E et al. Европейский регистр стентирования сонных артерий: результаты проспективного регистра восьми крупных европейских учреждений. Катетер Cardiovasc Interv 2012;80(2):329–34.

 Они не блокируют церебральный кровоток и позволяют визуализировать целевые поражения во время развертывания стента, но обременены некоторым риском эмболии (возможное попадание мелких частиц в мозг) и возможными трудностями при извлечении
Они не блокируют церебральный кровоток и позволяют визуализировать целевые поражения во время развертывания стента, но обременены некоторым риском эмболии (возможное попадание мелких частиц в мозг) и возможными трудностями при извлечении