Рак и аллергия: АЛЛЕРГИЯ ПРОТИВ РАКА | Новости
АЛЛЕРГИЯ ПРОТИВ РАКА | Новости
АЛЛЕРГИЯ ПРОТИВ РАКА | Новости- Главная
- Новости
- АЛЛЕРГИЯ ПРОТИВ РАКА
Говорят, что аллергия защищает от рака. Как такое может быть?
Попробуем разобраться в данной вопросе.
Как ни странно, действительно есть данные, которые позволяют так думать. Например, есть очень большие исследования американских ученых из Центра по изучению здоровья Техасского технологического университета по женщинам, страдающим аллергией и бронхиальной астмой (эта болезнь тоже имеет аллергическую природу). Оказывается, им в меньшей степени грозит развитие нескольких видов рака.
Чтобы прийти к таким данным, ученые проанализировали истории болезни более 1,1 млн женщин старше 20 лет. Примерно 53 тыс. из них страдали бронхиальной астмой, у 3 тыс. был поллиноз (сенная лихорадка). Их сравнили более чем с миллионом других женщин, которые не имели никаких аллергических заболеваний.
Когда исследователи провели серьезный анализ всех этих заболеваний, учитывая все факторы риска, способствующие их развитию, то выяснилось, что у женщин с бронхиальной астмой:
- риск развития рака шейки матки был ниже на 44%;
- риск рака эндометрия — ниже на 28%;
- риск рака яичников — ниже на 40%.
А наличие сенной лихорадки сокращало риск рака яичников даже на 90%.
Количество женщин было достаточно большим для получения достоверных результатов. К тому же это не единственное исследование, продемонстрировавшее защитный эффект аллергии в отношении рака. Вот еще некоторые из них:
- исследование смертности от рака, проведенное медиками из США и Канады, показало, что аллергики умирали от злокачественных опухолей на 10% реже;
- ученые из США и Канады установили, что у людей с поллинозом рак поджелудочной железы бывает на 57% реже, чем без этой формы аллергии;
- в Дании установили, что при аллергии снижался риск развития рака кожи и молочных желез;
-
даже у детей-аллергиков реже развивается лейкемия, а также злокачественные опухоли кожи и легких.

Как все это объяснить? Большинство исследований были наблюдательными, а они лишь выявляют статистическую закономерность. Какие защитные механизмы лежат в основе этого феномена, ученым пока точно неясно. Но есть предположения.
В основе аллергии и рака лежат иммунологические механизмы. А поскольку аллергию иногда рассматривают как проявление усиленного иммунитета, возможно, этот иммунитет сильнее и против озлокачествляющихся клеток. Но это только предположение. Эти механизмы столь сложны, что требуют детального изучения.
Источник — Мир новостей
+7 4742 515-911, 566-911
398000 г. Липецк, ул. Кузнечная, 10 А
398000 г. Липецк, ул. Гоголя, 60
+7 (4742) 515-911, 566-911
Вызов врача
г.
ФИО налогоплательщика (полностью)
Телефон
ФИО пациента (полностью)
Дата рождения
Родство пациента
Год оказания услуг
Отправляя обращение, Вы соглашаетесь с условиями обработки ваших персональных данных.
Извините, услуга вызов врача на дом временно не оказывается.
Извините, услуга вызов врача на дом временно не оказывается.
Специализация
Выберите специализацию
Врач
Выберите врача
Ваше имя
Отправляя заявку на приём, Вы соглашаетесь с условиями обработки ваших персональных данных.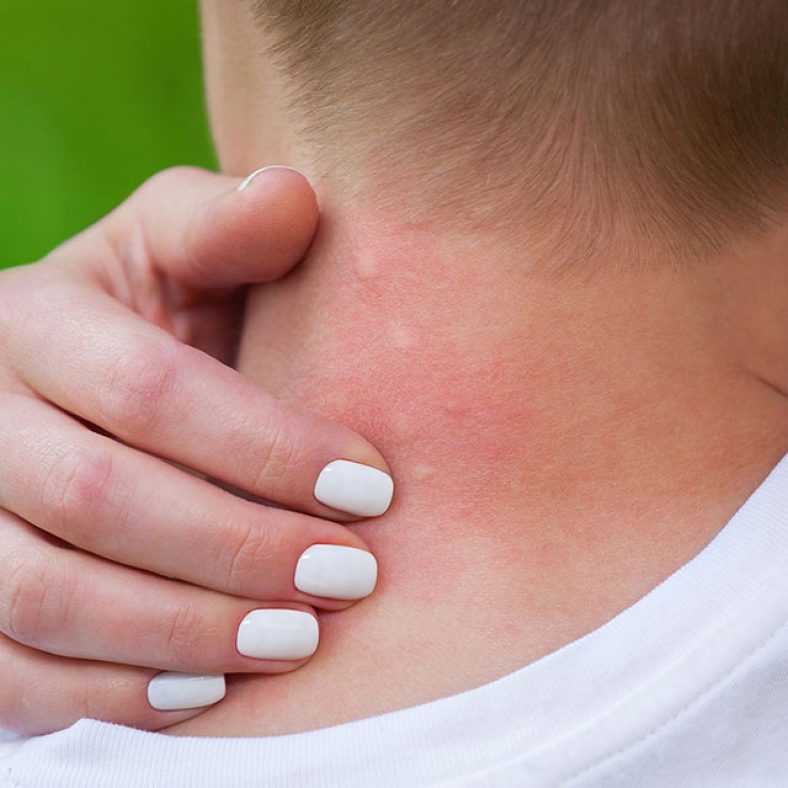
Выберите специалиста, к которому желаете записаться на приём:
Выберите клинику, в которой желаете записаться на приём:
Выберите дату, на которую хотите записаться на приём:
Идёт загрузка календаря…
К сожалению, у выбранного специалиста расписание приёма неизвестно, но Вы можете оставить предварительную заяку на запись.
Не указано имя, по которому к Вам можно обратиться!
Не указан номер телефона, по которому с Вами свяжется оператор для подтверждения записи!
Не пройдена проверка каптчи.
Отправляя заявку на приём, Вы соглашаетесь с условиями обработки ваших персональных данных.
Ваша заявка принята.
С Вами свяжется оператор для подтверждения записи.
Выберите услугу:
Аллерген f320 — рак речной, IgE (ImmunoCAP)
Количественное определение в крови специфических антител, иммуноглобулинов класса E, появляющихся при наличии аллергической реакции к раку речному.
Синонимы русские
Специфический иммуноглобулин класса Е к раку речному (европейскому раку, широкопалому речному раку, раку узкопалому).
Синонимы английские
Allergen f320 — Crayfish (Astacus astacus).
Метод исследования
Иммунофлюоресценция на твердой фазе (ImmunoCAP).
Единицы измерения
МЕ/л (международная единица на литр).
Какой биоматериал можно использовать для исследования?
Венозную, капиллярную кровь.
Как правильно подготовиться к исследованию?
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Аллерген – это вещество, вызывающее аллергическую реакцию. При атопических заболеваниях аллергены стимулируют образование антител класса IgE и являются факторами развития клинических симптомов аллергических заболеваний. Выявление в крови специфических иммуноглобулинов Е к определенному аллергену подтверждает его роль в развитии аллергической реакции I типа (реагиновой), а значит, позволяет определить возможного «виновника» аллергического заболевания и назначить соответствующие лечебные и профилактические мероприятия.
Пищевая аллергия – вызванная приемом пищи реакция, в основе которой лежат иммунные механизмы. Ее нередко можно спутать с пищевой непереносимостью, связанной с другими причинами (особенностями приготовления пищи, составом продукта, метаболическими нарушениями, заболеваниями ЖКТ).
Ее нередко можно спутать с пищевой непереносимостью, связанной с другими причинами (особенностями приготовления пищи, составом продукта, метаболическими нарушениями, заболеваниями ЖКТ).
Пищевые аллергены бывают животного или растительного происхождения. Между собой они различаются по растворимости, ферментативной и температурной стабильности. Некоторые пищевые аллергены в процессе кулинарной обработки, консервирования могут утрачивать свои аллергенные свойства, а другие, напротив, становиться более аллергенными. Среди клинических проявлений пищевой аллергии – острая крапивница, ангиоотек, приступы бронхиальной астмы, анафилактический шок, обострение атопического дерматита и реже аллергический ринит.
Из моллюсков выделено несколько антигенов, способных вызывать аллергические реакции, основным из которых оказался тропомиозин. Тропомиозин является термостойким белком, который выявляется у всех моллюсков и ракообразных, чем объясняется перекрестная аллергия на данные морепродукты.
Морепродукты можно разделить на получаемые из рыб, моллюсков и ракообразных. Ракообразные включают в себя креветки, омары, крабы, раки; моллюски включают гребешки, устрицы, кальмары. Аллергия на морепродукты пожизненна и считается одной из самых распространенных пищевых аллергий у взрослых. Аллергены ракообразных и рыб имеют высокий риск вызвать тяжелую анафилактическую реакцию. По результатам некоторых исследований, распространенность аллергии на разные морепродукты распределяется следующим образом в порядке убывания: ракообразные — моллюски — рыбы. У трети пациентов с аллергией на морепродукты выявлялась сенсибилизация к более чем одному морепродукту.
Первоначально из ракообразных выделили два антигена, один из которых оказался термостойким и вызывал специфическое связывание IgE в сыворотке исследуемых с аллергией – тропомиозин – это белок, который находится в тонких нитях мышечных клетках и в микрофиламентах остальных клеток. Тропомиозин является термостабильным, но его аллергенность может изменяться методами обработки./nginx/o/2017/04/05/6522125t1h5d7e.jpg) Так, при кипячении он подвергается изменению и может вызвать более выраженную аллергическую реакцию. Помимо тропомиозина, выявлены другие аллергены: аргининкиназа, тяжелые цепи миозина и амилаза. Тропомиозин показал очень высокую гомологию, до 98 % среди видов ракообразных, включая омаров, раков и крабов, поэтому пациенты с гиперчувствительностью на один вид беспозвоночных могут иметь аллергическую реакцию на другой вид ракообразных или моллюсков.
Так, при кипячении он подвергается изменению и может вызвать более выраженную аллергическую реакцию. Помимо тропомиозина, выявлены другие аллергены: аргининкиназа, тяжелые цепи миозина и амилаза. Тропомиозин показал очень высокую гомологию, до 98 % среди видов ракообразных, включая омаров, раков и крабов, поэтому пациенты с гиперчувствительностью на один вид беспозвоночных могут иметь аллергическую реакцию на другой вид ракообразных или моллюсков.
Рак речной узкопалый (Аstacus astacus) относится к отряду членистоногих, обитает практически в любых европейских водоёмах (реках, озерах и прудах). Похож на омара, но намного меньше. Употребляется в пищу по всему миру. Несколько исследований показывали перекрестную реактивность между раками и другими ракообразными.
Проявления аллергии на раков варьируются от легких симптомов, например крапивницы, до тяжелых – анафилаксии. Аллергия на морепродукты — один из самых опасных вариантов аллергической чувствительности: сохраняется в течение всей жизни пациента, есть высокий риск анафилактических реакций, часто наблюдается перекрестная чувствительность, провоцирующие вещества не всегда разрушаются при термической обработке или меняют структуру, усиливая собственный аллергопотенциал.
Целью данного исследования является определение специфических IgE к речному раку методом ImmunoCAP. ImmunoCAP характеризуется высокой точностью и специфичностью: в малом количестве крови обнаруживаются даже очень низкие концентрации IgE-антител. Исследование является революционным и основано на иммунофлюоресцентном методе, что позволяет увеличить чувствительность в несколько раз по сравнению с другими анализами. Всемирная организация здравоохранения и Всемирная организация аллергологов признают диагностику с использованием ImmunoCAP как «золотой стандарт», так как она доказала свою точность и стабильность результатов в независимых исследованиях. В Российской Федерации до настоящего момента методика не получила широкого распространения, хотя во всем мире до 80 % анализов на специфические иммуноглобулины класса Е выполняется с помощью ImmunoCAP. Таким образом, выявление специфических IgE с помощью данной методики выводит аллергодиагностику на качественно новый уровень.
Для чего используется исследование?
- Для диагностики сенсибилизации к речному раку у пациентов с аллергическими заболеваниями (пищевая аллергия, острая и хроническая крапивница, ангиоотек, атопический дерматит, бронхиальная астма, аллергический ринит).
- Для оценки риска развития аллергических реакций на речного рака.
Когда назначается исследование?
- При наличии следующих, указывающих на аллергический характер, симптомов при употреблении речных раков: покраснение и зуд кожи, сыпь, ангионевротический отек, отек гортани, кашель и бронхоспазм, тошнота, рвота, боль в области живота и диарея.
- При поливалентной сенсибилизации.
- При сомнительных результатах кожного тестирования и провокационных проб.
Что означают результаты?
Референсные значения: 0 — 0,34 МЕ/л.
Причины повышения уровня специфических IgE:
- наличие аллергических реакций на речного рака;
- пищевая аллергия, обострение атопических заболеваний, обусловленные сенсибилизацией к аллергенам речного рака.

Причины снижения уровня специфических IgE
При повторном исследовании (в динамике) уровень специфических IgE может снижаться по следующим причинам:
- ограничение или исключение контакта с аллергеном;
- проведение медикаментозного лечения.
Важные замечания
- Выполнение данного исследования безопасно для пациента по сравнению с кожными тестами (in vivo), так как исключает контакт пациента с аллергеном.
- Прием антигистаминных препаратов и возрастные особенности не влияют на качество и точность исследования.
Также рекомендуется
- Фадиатоп (ImmunoCAP)
- Фадиатоп детский (ImmunoCAP)
- Суммарные иммуноглобулины E (IgE) в сыворотке
- Смесь пищевых аллергенов № 2 (IgE): треска, тунец, креветки, лосось, мидии
- Аллерген f3 — треска, IgE (ImmunoCAP)
- Аллерген f206 — скумбрия, IgE (ImmunoCAP)
- Аллерген f41 — лосось, IgE (ImmunoCAP)
- Аллерген f204 — форель, IgE (ImmunoCAP)
- Аллерген f40 — тунец, IgE
- Общий анализ крови (без лейкоцитарной формулы и СОЭ)
- Лейкоцитарная формула
- Скорость оседания эритроцитов (СОЭ)
- Копрограмма
Кто назначает исследование?
Аллерголог, педиатр, пульмонолог, гастроэнтеролог, терапевт, врач общей практики.
Литература
- Faria Khan, M.D., Frank Orson, M.D., Yoshiko Ogawa, M.D., Crystal Parker, M.S., Carla McGuire Davis, M.D. Adult seafood allergy in the Texas Medical Center: A 13-year experience. / Allergy Rhinol (Providence). 2011 Apr-Jun; 2(2): e71–e77.
- Karlijn JG Schulkes, Rob JB KlemansEmail, Lidy Knigge, Marjolein de Bruin-Weller, Carla AFM Bruijnzeel-Koomen, Åsa Marknell deWitt, Jonas Lidholm, André C Knulst. Specific IgE to fish extracts does not predict allergy to specific species within an adult fish allergic population. / Clinical and Translational Allergy, 2014, 4:27.
Рак, аллергия, ВИЧ: как прививаются люди с особенностями здоровья
«Вакцинация безопасна только для полностью здоровых людей» — этот миф крайне живуч и теперь, когда среди привитых немало онкобольных, ВИЧ-положительных людей и тех, кто живет с хронической аллергией. Мы поговорили с людьми, которые прошли через этот опыт, и подкрепили рассказы мнением специалистов
Абсолютных противопоказаний для прививки от коронавируса становится все меньше — по мере того, как накапливаются данные.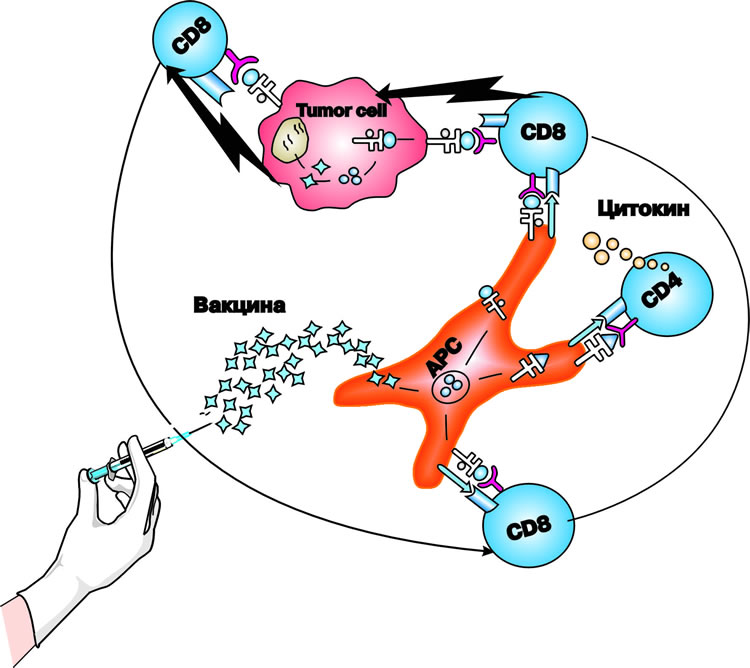 Сейчас к ним относятся возраст до 18 лет, грудное вскармливание, тяжелые аллергические реакции в анамнезе, аллергия на компоненты вакцины, обострение хронических болезней и активный инфекционный процесс. Но при некоторых болезнях и состояниях стоит проявить осторожность, хотя вакцинация и не запрещена. Это прежде всего те, которые напрямую затрагивают иммунную систему — например, ВИЧ, диабет, противораковая терапия, аутоиммунные болезни. Насколько безопасно делать прививку людям с такими состояниями? Вот что на этот счет думают врачи и пациенты, уже сделавшие прививку.
Сейчас к ним относятся возраст до 18 лет, грудное вскармливание, тяжелые аллергические реакции в анамнезе, аллергия на компоненты вакцины, обострение хронических болезней и активный инфекционный процесс. Но при некоторых болезнях и состояниях стоит проявить осторожность, хотя вакцинация и не запрещена. Это прежде всего те, которые напрямую затрагивают иммунную систему — например, ВИЧ, диабет, противораковая терапия, аутоиммунные болезни. Насколько безопасно делать прививку людям с такими состояниями? Вот что на этот счет думают врачи и пациенты, уже сделавшие прививку.
Рак
«Я привился в феврале двойной дозой одной из российских вакцин против ковида и каких-либо побочных эффектов не наблюдал, — рассказал ТАСС патологоанатом Андрей Подольский. — На момент вакцинации я был в ремиссии после курса химиотерапии и облучения (от опухоли носоглотки), закончившихся за год и три месяца до первой инъекции. Укол я даже не почувствовал — спасибо золотым рукам коллеги. Вторая прививка также прошла без каких-либо осложнений и последствий». С тех пор Андрей, по его словам, коронавирусом не болел.
С тех пор Андрей, по его словам, коронавирусом не болел.
Онкологическое заболевание в стадии ремиссии — не противопоказание к вакцинации, но это фактор, к которому нужно относиться с большим вниманием, подчеркивает главный внештатный онколог Минздрава России Андрей Каприн. Решение должен принимать лечащий врач или терапевт, у которого есть доступ к истории болезни. При этом сама вакцинация спровоцировать развитие болезни не может, считает эксперт: «Любая вакцинация не должна влиять на такое мощное снижение иммунного ответа, чтобы вызывать онкологическое заболевание. Может быть совпадение, ведь есть латентные раки, которые развиваются годами».
А что делать, если лечение уже идет? Здесь многое зависит от соотношения риска и пользы. «У пациентов, которые получают иммуносупрессивную терапию, могут быть проблемы с выработкой антител, — объясняет врач-инфекционист ПСПбГМУ им. академика И.П. Павлова Оксана Станевич. — И международные, и российские рекомендации требуют завершить цикл вакцинации до начала терапии, чтобы добиться максимального иммунного ответа. Если откладывать лечение невозможно, до его начала крайне желательно сделать хотя бы введение одной дозы. В этом случае вероятность выработки устойчивого ответа и нейтрализующих антител будет выше».
Если откладывать лечение невозможно, до его начала крайне желательно сделать хотя бы введение одной дозы. В этом случае вероятность выработки устойчивого ответа и нейтрализующих антител будет выше».
Пациентам с онкогематологическими заболеваниями Минздрав России рекомендует прививаться либо до начала лечения, либо в процессе при достижении стабильного уровня лимфоцитов. Если планируется операция, то вакцинировать онкопациента нужно за две недели или ранее до планируемой даты хирургического вмешательства либо после выписки из стационара. Тот же срок специалисты называют и для случаев, когда предстоит химиотерапия.
«Многие препараты, которые применяются во время химиотерапии, убивают кровь (снижают кроветворение). В таком случае в вакцинации нет смысла, потому что будет угнетаться иммунный ответ. Решить, когда и какой вакциной прививаться такому пациенту, может врач, который сопровождает его во время лечения, — поясняет доктор медицинских наук, специалист по особо опасным инфекциям Владислав Жемчугов. — Если же пациент долго, регулярно и циклично лечится и нет признаков гематологической токсичности, то прививаться можно без ограничений, на показатели крови это не повлияет».
— Если же пациент долго, регулярно и циклично лечится и нет признаков гематологической токсичности, то прививаться можно без ограничений, на показатели крови это не повлияет».
Аллергия
Эта тема остается одной из самых сложных и для врачей, и для пациентов. Ведь четких инструкций здесь нет, а состояние человека может меняться ото дня ко дню. «Чашу весов могут качнуть в ту или иную сторону и текущее состояние пациента (прежде всего признаки обострения), и недавнее столкновение с аллергеном, и сопутствующие заболевания», — говорит главный внештатный аллерголог-иммунолог Москвы Александр Пампура.
«Я аллергик с детства, но врачи настаивали на вакцинации, так как есть хронические болезни, — делится Анна из Кемерова. — Список моих аллергенов: солнце, холод, краска на масляной основе, молочные продукты, лидокаин, некоторые антибиотики…У меня крайне редко бывают периоды без сыпи… Боялась я этой вакцинации ужасно! Несколько раз записывалась, и врач, видя мою сыпь, просил приходить в следующий раз. Только на третий раз меня отправили на вакцинацию. Ждала реакцию, но, на мое удивление, вообще ничего не наблюдала у себя кроме того, что немного болела рука один день. Может быть, сработали антигистаминные?»
Только на третий раз меня отправили на вакцинацию. Ждала реакцию, но, на мое удивление, вообще ничего не наблюдала у себя кроме того, что немного болела рука один день. Может быть, сработали антигистаминные?»
А вот Анна Сергеевна из Ижевска получила медотвод: «Зная свой анамнез (отек Квинке), я обратилась в частную клинику, где обслуживалась до этого. Терапевт сказал, что не может дать медотвод без заключения аллерголога, а тот дал мне направление на анализ. Я сдала кровь на IgE — маркер аллергических реакций — и он оказался 386 при норме до 100. Врач в итоге мне отсоветовал». В итоге врач выдал Анне справку с отводом на две недели.
«Иммуноглобулины класса IgE — это особые антитела, они участвуют в развитии аллергических реакций, — поясняет вакцинолог, кандидат медицинских наук Евгений Тимаков. — Если в крови пациента постоянно держится их высокий уровень, это значит, что человек склонен к аллергии. Но повышение иммуноглобулинов Е в анализах еще не говорит о том, что в данный момент аллергия на пике обострения. Нужно смотреть на симптомы. Если у человека заложен нос, воспалена слизистая глаз, сильный кашель, сыпь — тогда нужно пролечиться. И делать прививку уже после снятия этих симптомов».
Нужно смотреть на симптомы. Если у человека заложен нос, воспалена слизистая глаз, сильный кашель, сыпь — тогда нужно пролечиться. И делать прививку уже после снятия этих симптомов».
«Пищевая аллергия (на клубнику, апельсины, мед и т.д.), а также аллергия на пыльцу или пыль не являются поводом для отказа от вакцинации, — поясняет аллерголог Владимир Болибок. — Оснований всего два: это либо тяжелая аллергическая реакция, либо гиперчувствительность в анамнезе пациента на компоненты ранее введенных вакцин».
По словам аллерголога, российские вакцины от коронавируса гипоаллергенны, потому что их компоненты не перекрещиваются с пищевыми продуктами, пыльцой, плесенью или бытовой пылью. «В них нет антибиотиков, консервантов, дрожжей, липополисахаридов бактерий, то есть того, что бывает в других вакцинах и может вызывать перекрестную аллергию», — объясняет он. Не является противопоказанием к вакцинации и крапивница (дерматит аллергического происхождения), отмечает главный внештатный специалист по терапии и общей врачебной практике Минздрава России Оксана Драпкина.
Кстати, вопреки одному из распространенных заблуждений, вакцину можно вводить и тем, у кого есть аллергия на куриный белок. Этот слух родился из данных о других вакцинах — например, противогепатитной — для выращивания вируса используются клетки куриного эмбриона. Но ни в одной из одобренных вакцин компонентов куриного организма нет, а клеточные линии взяты у других животных либо человека.
ВИЧ и СПИД
«Первый компонент «Спутника» я поставил 2 июля, — рассказывает ВИЧ-положительный активист Борис Конаков. — 20 числа был второй укол. Сразу после и на второй день, по ощущениям, была легкая температура. Но в целом какого-то радикального изменения состояния не почувствовал. Перед прививкой я консультировался у своего инфекциониста в СПИД.Центре. Я и без этого знал, что ВИЧ-статус не является противопоказанием к прививке, но на всякий случай все равно сходил уточнить».
Зато, по словам Бориса, в районной поликлинике он столкнулся с плохой осведомленностью местных врачей. «Мне попытались там отказать в день вакцинации из-за ВИЧ-статуса; требовали справку, что мне это можно, хотя вопрос об этом не стоял изначально, — делится он. — Пришлось устроить минутку просвещения на этот счет, хотя мне довольно странно было объяснять врачу особенности своего ВИЧ-статуса. Они были элементарно не в курсе про особенности иммунитета и что мой иммунитет человека, который принимает таблетки, выше даже, чем у иных людей без ВИЧ».
«Мне попытались там отказать в день вакцинации из-за ВИЧ-статуса; требовали справку, что мне это можно, хотя вопрос об этом не стоял изначально, — делится он. — Пришлось устроить минутку просвещения на этот счет, хотя мне довольно странно было объяснять врачу особенности своего ВИЧ-статуса. Они были элементарно не в курсе про особенности иммунитета и что мой иммунитет человека, который принимает таблетки, выше даже, чем у иных людей без ВИЧ».
«При принятии решения о вакцинировании ВИЧ-положительного пациента важно получить информацию о показателях его иммунного статуса (количества CD4+ лимфоцитов в крови), — объясняет Алексей Мазус, главный внештатный специалист по ВИЧ-инфекции Министерства здравоохранения Российской Федерации. — Так, если их уровень более 200 кл/мкл, то вакцинация не имеет ограничений. Если количество клеток CD4+ менее указанной нормы, то к использованию не рекомендованы, к примеру, живые вакцины (корь, эпидемический паротит, краснуха, ветряная оспа)».
При этом сам факт того, что человек является носителем ВИЧ, — не повод для медотвода. «Практика отказа в вакцинации людям с ВИЧ прямо противоречит медицинским рекомендациям, а в первую очередь — интересам пациентов», — добавляет Алексей Мазус. Если вам отказывают в прививке, медицинский директор Фонда «СПИД.ЦЕНТР», врач-инфекционист Антон Еремин советует потребовать от сотрудников медучреждения зафиксировать отказ в письменной форме и обратиться в другой пункт вакцинации. Вы впраче также не сообщать о своем ВИЧ-статусе, подчеркивает он.
«Практика отказа в вакцинации людям с ВИЧ прямо противоречит медицинским рекомендациям, а в первую очередь — интересам пациентов», — добавляет Алексей Мазус. Если вам отказывают в прививке, медицинский директор Фонда «СПИД.ЦЕНТР», врач-инфекционист Антон Еремин советует потребовать от сотрудников медучреждения зафиксировать отказ в письменной форме и обратиться в другой пункт вакцинации. Вы впраче также не сообщать о своем ВИЧ-статусе, подчеркивает он.
Диабет
С 30 декабря — даты старта массовой прививочной кампании — сахарный диабет не считается противопоказанием. Наоборот, именно людям с диабетом советуют прививаться в первую очередь — из-за высокого риска осложнений при болезни. «В первую очередь, это возраст: чем выше возраст, тем выше риск, — объясняет эндокринолог Ольга Рождественская. — Второе — это вес: чем выше вес, тем выше риск. Третье — это плохая компенсация диабета, то есть это высокие сахара и высокий гликированный гемоглобин». По ее словам, сочетание сахарного диабета, ожирения и артериальной гипертензии увеличивает риски летального исхода почти в пять раз.
«Сделала «Спутник» еще зимой, — делится Жанна из Перми. — Перед прививкой был осмотр врача, который померил давление, температуру, сатурацию. Врач сказал, если сахар в норме, то нужно делать. А если нет, то противопоказание. У меня сахар немного гуляет, но врач подумал и дал добро. Побочки от прививки были минимальные в виде небольшой температуры 37,1 и слабости». По словам Розы Грязевой, жительницы Кировской области, вопроса о том, нужно ли вакцинироваться, у нее не возникало. «У меня сахарный диабет и гипертоническая болезнь, у мужа бронхиальная астма, — говорит Роза Петровна, — но ни минуты сомнений у нас не было. Такие болезни — первый показатель, при котором нужно обязательно вакцинироваться! Мы привились еще в марте, потому что к нам приезжают отовсюду гости, поэтому нужно обезопаситься».
«Перед вакцинацией нужно посмотреть общий анализ крови, нет ли там воспаления, проверить, чтобы сахар был в пределах нормы, посмотреть, каков гликированный гемоглобин (показатель, демонстрирующий средний уровень сахара в крови в течение последних трех месяцев — прим. ТАСС). Заболевание не должно быть в острой фазе, также не должно быть признаков ОРВИ», — поясняет эндокринолог Ольга Рождественская.
ТАСС). Заболевание не должно быть в острой фазе, также не должно быть признаков ОРВИ», — поясняет эндокринолог Ольга Рождественская.
«Проведение вакцинации от COVID-19 рекомендовано больным сахарным диабетом первого и второго типа, с другими, более редкими вариантами диабета (кроме гестационного), с соблюдением противопоказаний и правил осторожности, — добавляет директор ФГБУ «НМИЦ эндокринологии» Минздрава России, член-корреспондент РАН Наталья Мокрышева. — Перед вакцинацией обязательно должны быть учтены такие показатели, как наличие аллергических реакций, острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний, острые осложнения, декомпенсация углеводного обмена. В этих случаях вакцинацию возможно провести через две-три недели после выздоровления или после нормализации показателей глюкозы крови».
Таким образом, по последним рекомендациям, пройти вакцинацию могут пациенты с сахарным диабетом первого и второго типа, с другими, более редкими вариантами диабета (кроме гестационного) с соблюдением противопоказаний и правил осторожности.
Аутоиммунные заболевания
«У меня ревматоидный артрит, эта болезнь аутоиммунная. Это значит, что сильная реакция иммунитета может спровоцировать обострение. Врачи рекомендовали мне прививаться вакциной «КовиВак». Я ждала именно ее, пришлось даже ехать в область, так как в самом городе ее было не достать. Сам укол почти не почувствовала, все было нормально в оба раза», — рассказывает Виктория из Санкт-Петербурга. С мнением врачей по поводу выбора вакцины соглашается и специалист НИИ ревматологии им. В.А. Насоновой Борис Белов. «Для наших пациентов принципиально важно, чтобы вакцина была инактивированная, — объясняет он. — Основную ставку мы делаем на «Ковивак», где представлен антигенный набор самого вируса, а не только S-белок. Ведь до конца непонятно, каким образом иммунитет здорового человека и пациента, получающего иммуносупрессивную терапию, будет реагировать на те или иные наборы антигенов».
Пациентам, у которых диагностированы системная красная волчанка, артриты и другие ревматологические заболевания, нужно получить рекомендации по поводу прививки ревматолога, считает профессор СЗГМУ им. Мечникова Вадим Мазуров. Но лучше делать выбор в пользу вакцинации, если острого состояния нет. «Если нет высокой активности иммуновоспалительного процесса, человек не получает препараты для подавления иммунитета, прививка не просто не противопоказана, а рекомендована, — считает он. — Если было острое состояние, нужно понаблюдать хотя бы месяц. Состояние стабилизировалось — можно смело делать прививку. Даже если пациент просто получает поддерживающую терапию малыми дозами, сомнений в эффективности вакцинации нет».
Мечникова Вадим Мазуров. Но лучше делать выбор в пользу вакцинации, если острого состояния нет. «Если нет высокой активности иммуновоспалительного процесса, человек не получает препараты для подавления иммунитета, прививка не просто не противопоказана, а рекомендована, — считает он. — Если было острое состояние, нужно понаблюдать хотя бы месяц. Состояние стабилизировалось — можно смело делать прививку. Даже если пациент просто получает поддерживающую терапию малыми дозами, сомнений в эффективности вакцинации нет».
В ответ на сомнения отдельных врачей и пациентов Европейское общество эндокринологов недавно выпустило собственную согласованную позицию: «Вакцинация против COVID-19 не должна отличаться от таковой у общей популяции у пациентов со стабильным течением эндокринных заболеваний, таких как аутоиммунный тиреоидит (гипотиреоз), болезнь Грейвса, болезнь Аддисона (надпочечниковая недостаточность), аденома гипофиза, сахарный диабет 1-го и 2-го типа, ожирение».
Подготовил Антон Солдатов
Связь между аллергией и раком: что известно на данный момент?
Обзор
. 2007 авг; 99 (2): 102-16; викторина 117-9, 150.
2007 авг; 99 (2): 102-16; викторина 117-9, 150.
doi: 10.1016/S1081-1206(10)60632-1.
Рэй М Меррилл 1 , Райан Т. Исаксон, Роберт Э. Бек
принадлежность
- 1 Департамент медицинских наук, Колледж здоровья и работоспособности человека, Университет Бригама Янга, Прово, Юта 84602, США. Рэй-Меррилл@byu.edu
- PMID: 17718097
- DOI: 10.1016/С1081-1206(10)60632-1
Обзор
Ray M Merrill et al.
Энн Аллергия Астма Иммунол.
2007 авг.
. 2007 авг; 99 (2): 102-16; викторина 117-9, 150.
doi: 10.1016/S1081-1206(10)60632-1.
Авторы
Рэй М Меррилл 1 , Райан Т Исаксон, Роберт Э Бек
принадлежность
- 1 Департамент медицинских наук, Колледж здоровья и работоспособности человека, Университет Бригама Янга, Прово, Юта 84602, США. Рэй-Меррилл@byu.edu
- PMID: 17718097
- DOI: 10.1016/С1081-1206(10)60632-1
Абстрактный
Задача: Предоставить обзор того, что в настоящее время известно о взаимосвязи между аллергией и раком.
Источники данных: Публикации были отобраны из систематического обзора англоязычной литературы из установленных баз данных (например, MEDLINE, EBSCO) и ссылок на материалы, выявленные в этих базах данных.
Выбор исследования: В этот обзор были включены публикации, оценивающие связь между астмой, сенной лихорадкой или другими заболеваниями, связанными с аллергией, и раком.
Полученные результаты: Лица с любым типом аллергии имеют сниженный риск развития рака (по сравнению с общей популяцией), включая глиому, колоректальный рак, рак гортани, неходжкинскую лимфому, рак пищевода, рак ротовой полости, рак поджелудочной железы, рак желудка, и рак тела матки. Однако среди аллергиков существует повышенный риск развития рака мочевого пузыря, лимфомы, миеломы и рака предстательной железы. Исследования, связанные с раком молочной железы, лейкемией, раком легких, меланомой и раком щитовидной железы, не показали связи или противоречивых результатов, связанных с аллергией. Необходимы дополнительные исследования, прежде чем можно будет сделать выводы о связи между аллергией и саркомой Капоши, раком печени и раком яичников.
Исследования, связанные с раком молочной железы, лейкемией, раком легких, меланомой и раком щитовидной железы, не показали связи или противоречивых результатов, связанных с аллергией. Необходимы дополнительные исследования, прежде чем можно будет сделать выводы о связи между аллергией и саркомой Капоши, раком печени и раком яичников.
Выводы: Связь между аллергией и раком зависит от локализации. Необходимы дальнейшие исследования, чтобы проверить эти результаты и определить, почему такие ассоциации существуют.
Похожие статьи
Аллергия, атопия и рак: проспективное исследование когорты Басселтона 1981 года.
Талбот-Смит А., Фричи Л., Дивитини М.Л., Мэллон Д.Ф., Кнуиман М.В. Талбот-Смит А. и соавт. Am J Эпидемиол. 2003 1 апреля; 157 (7): 606-12. дои: 10.1093/aje/kwg020.
 Am J Эпидемиол. 2003.
PMID: 12672680
Am J Эпидемиол. 2003.
PMID: 12672680Связь между аллергическими состояниями и риском рака предстательной железы: систематический обзор и метаанализ, совместимый с Prisma.
Zhu J, Song J, Liu Z, Han J, Luo H, Liu Y, Jia Z, Dong Y, Zhang W, Jiang F, Wu C, Sun Z, Zhong W. Чжу Дж. и др. Научный представитель 21 октября 2016 г .; 6: 35682. дои: 10.1038/srep35682. Научный представитель 2016. PMID: 27767045 Бесплатная статья ЧВК. Обзор.
Использование пестицидов, иммунологические состояния и риск неходжкинской лимфомы у канадских мужчин в шести провинциях.
Пахва М., Харрис С.А., Хоэнадель К., Маклафлин Дж.Р., Спинелли Дж.Дж., Пахва П., Досман Дж.А., Блэр А. Пахва М. и др. Инт Джей Рак. 1 декабря 2012 г .
 ; 131 (11): 2650-9. doi: 10.1002/ijc.27522. Epub 2012 2 апр.
Инт Джей Рак. 2012.
PMID: 22396152
; 131 (11): 2650-9. doi: 10.1002/ijc.27522. Epub 2012 2 апр.
Инт Джей Рак. 2012.
PMID: 22396152Заболевания, связанные с аллергией, и рак: обратная связь.
Vena JE, Bona JR, Byers TE, Middleton E Jr, Swanson MK, Graham S. Вена Дж. Э. и соавт. Am J Эпидемиол. 1985 г., июль; 122 (1): 66–74. doi: 10.1093/oxfordjournals.aje.a114087. Am J Эпидемиол. 1985. PMID: 4014202
Связь атопических заболеваний с раком молочной железы, простаты и колоректальным раком: метаанализ.
Войтехова П., Мартин Р.М. Войтехова П. и др. Рак вызывает контроль. 2009 сен; 20 (7): 1091-105. doi: 10.1007/s10552-009-9334-y. Epub 2009 2 апр. Рак вызывает контроль. 2009. PMID: 19340595 Обзор.
Посмотреть все похожие статьи
Цитируется
Эндометриоз в анамнезе независимо связан с повышенным риском рака яичников.

Саррия-Сантамера А., Хамитова З., Гусманов А., Терзич М., Поло-Сантос М., Ортега М.А., Асунсоло А. Сарриа-Сантамера А. и др. J Pers Med. 2022 авг. 20;12(8):1337. дои: 10.3390/jpm12081337. J Pers Med. 2022. PMID: 36013285 Бесплатная статья ЧВК.
Сывороточный иммуноглобулин G связан со снижением риска рака поджелудочной железы в шведском исследовании AMORIS.
Солли С., Сантаолалла А., Мишо Д.С., Саркер Д., Карагианнис С.Н., Джозефс Д.Х., Хаммар Н., Валдиус Г., Гармо Х., Холмберг Л., Юнгнер И., Ван Хемельрик М. Солли С. и др. Фронт Онкол. 2020 28 фев; 10:263. дои: 10.3389/fonc.2020.00263. Электронная коллекция 2020. Фронт Онкол. 2020. PMID: 32185133 Бесплатная статья ЧВК.
Аллергия и астма в связи с риском рака.

Кантор Э.Д., Хсу М., Ду М., Синьорелло Л.Б. Кантор Э.Д. и соавт. Эпидемиологические биомаркеры рака Prev. 2019 августа; 28 (8): 1395-1403. doi: 10.1158/1055-9965.EPI-18-1330. Epub 2019 5 июня. Эпидемиологические биомаркеры рака Prev. 2019. PMID: 31167755 Бесплатная статья ЧВК.
Аллергия может улучшить выживаемость пациентов с глиомами.
Лерер С., Райнштейн П.Х., Розенцвейг К.Е. Лерер С. и др. Клиника Нейрол Нейрохирург. 2019 фев; 177: 63-67. doi: 10.1016/j.clineuro.2018.12.021. Epub 2018 31 декабря. Клиника Нейрол Нейрохирург. 2019. PMID: 30611004 Бесплатная статья ЧВК.
Непечатаемый Haemophilus Influenzae обнаружение в нижних дыхательных путях больных раком легкого и хронической обструктивной болезнью легких.

Шрирам К.Б., Кокс А.Дж., Сивакумаран П., Сингх М., Уоттс А.М., Уэст Н.П., Криппс А.В. Шрирам К.Б. и др. Мультидисциплинарный респираторный мед. 2018 9 апр;13:11. doi: 10.1186/s40248-018-0123-x. Электронная коллекция 2018. Мультидисциплинарный респираторный мед. 2018. PMID: 29657714 Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
Типы публикаций
термины MeSH
Клиническая и иммунологическая оценка аллергии у онкологических больных
Введение
Связь между раком и аллергией может быть связана с иммунодефицитом и иммунным надзором, запускаемым каждым заболеванием 1,2 . Аллергические реакции возникают в результате гиперактивности (Th)2-вспомогательного Т-иммунного ответа, который активирует эозинофилы, макрофаги и IgE посредством секреции IL-4, IL-5 и IL-13 3,4 . В результате усиливается иммунный надзор и повреждение клеток, в том числе злокачественных 1,3,5 . Повышение уровня IL-4 может направлять выработку антител к изотипу IgE, связанному с реакциями гиперчувствительности I типа. Этот аллергический процесс, опосредованный IgE, способен ингибировать рост опухоли из-за его цитотоксического действия на раковые клетки 6,7,8,9,10,11 .
В результате усиливается иммунный надзор и повреждение клеток, в том числе злокачественных 1,3,5 . Повышение уровня IL-4 может направлять выработку антител к изотипу IgE, связанному с реакциями гиперчувствительности I типа. Этот аллергический процесс, опосредованный IgE, способен ингибировать рост опухоли из-за его цитотоксического действия на раковые клетки 6,7,8,9,10,11 .
Согласно концепции иммунного надзора, иммунная система уничтожает опухолевые клетки посредством врожденного иммунитета, отвечающего за немедленное обнаружение и уничтожение злокачественных клеток 12,13 . При первичном или приобретенном иммунодефиците, как при синдроме приобретенного иммунодефицита, при применении иммунодепрессантов, так и у пациентов пожилого возраста имеется предрасположенность или более высокая вероятность возникновения рака 14,15,16,17 .
Аллергоонкология — новая междисциплинарная область, изучающая возможные связи между раком и Th3-подразделением в иммунной системе, а также отношения между опухолями и иммунитетом, опосредованным IgE и цитокинами, для разработки иммунотерапии для борьбы с раком 1,9, 18,19 . Иммунные механизмы, обнаруженные при аллергических процессах, указывают на новую иммунотерапию и иммунопрофилактику этого заболевания 20 .
Иммунные механизмы, обнаруженные при аллергических процессах, указывают на новую иммунотерапию и иммунопрофилактику этого заболевания 20 .
Клетки Th2 обеспечивают защиту от внутриклеточных патогенов, способствуют возникновению аутоиммунных и хронических воспалительных заболеваний, а также секретируют цитокины, такие как ИЛ-2, ИЛ-12, фактор некроза опухоли-β (ФНО-β) и интерферон -γ (ИФН-γ) 4,21 . В литературе описаны и другие популяции лимфоцитов, особенно для Th27, которые секретируют IL-17, связанные с аутоиммунными заболеваниями и заболеваниями внеклеточной защиты, а также для регуляторных Т-клеток (Treg), связанных с иммунной толерантностью, ингибирующих эффекторные Т-клетки (Tef) , и подавление разрушения аутоантигенами 4,21,22,23,24,25,26 .
ИЛ-1β вызывает мощную воспалительную реакцию и играет решающую роль в борьбе организма с патогенами и вредными агентами. Однако чрезмерная активация или неспособность прерывать воспалительную реакцию может привести к поражению клеток или тканей, приводя к аллергическим процессам, хроническим аутоиммунным воспалительным заболеваниям и раку 27,28 . Трансформирующий фактор роста-β (TGF-β) играет двухфазную роль в развитии рака и прогрессирует: в нормальных клетках TGF-β подавляет опухолевой генез. Однако, как только опухолевый процесс уже начался, TGF-β создает иммуносупрессивную микросреду, ингибируя IL-2, IL-12 и IFN-γ. Таким образом, создается местная иммунная толерантность и повышается концентрация TGF-β в сыворотке крови, что часто встречается у онкологических больных 29,30,31,32 .
Трансформирующий фактор роста-β (TGF-β) играет двухфазную роль в развитии рака и прогрессирует: в нормальных клетках TGF-β подавляет опухолевой генез. Однако, как только опухолевый процесс уже начался, TGF-β создает иммуносупрессивную микросреду, ингибируя IL-2, IL-12 и IFN-γ. Таким образом, создается местная иммунная толерантность и повышается концентрация TGF-β в сыворотке крови, что часто встречается у онкологических больных 29,30,31,32 .
Аллергический процесс оценивают по клинической оценке, кожным пробам и уровням общего или специфического IgE в сыворотке. Однако прямой связи между конкретными сообщениями об аллергии и чувствительностью кожи к одному и тому же аллергену не наблюдалось, при этом следует понимать, что клиническая аллергия может сопровождаться отрицательным кожным тестом на один и тот же чувствительный агент 33 . Положительные кожные пробы наблюдаются у людей, не проявляющих клинической аллергии. При наличии рака в общей популяции наблюдался более низкий уровень сообщений об аллергии, даже при более высокой частоте положительных кожных тестов на аллергены 33 . Измерение IgE в сыворотке крови (маркер реакции гиперчувствительности I типа) используется в качестве объективного метода диагностики аллергии. Обратная связь между концентрацией IgE и раком может быть специфичной для аллергии и типов опухолей 6,20,34,35 .
Измерение IgE в сыворотке крови (маркер реакции гиперчувствительности I типа) используется в качестве объективного метода диагностики аллергии. Обратная связь между концентрацией IgE и раком может быть специфичной для аллергии и типов опухолей 6,20,34,35 .
Механизм, предложенный для объяснения связи между раком и аллергией, заключается в том, что при аллергии преобладает повышенный иммунный ответ, тогда как при раке наблюдается гипореактивный иммунный ответ. Таким образом, у людей с аллергией будет наблюдаться увеличение продукции цитокинов, связанных с ответом Th3, и увеличение продукции IgE против специфического опухолевого антигена, способного активировать эффекторные клетки и разрушать опухоли 36,37,38,39 . Тем не менее, несколько исследований посвящены измерению цитокинов и других биомаркеров в этой ситуации 36,37 . Почти все испытания с участием цитокинов проводятся на животных моделях 19 , и только два исследования с участием людей были выявлены 38,39 .
Цель этого исследования, которое является частью линии исследований 33,40,41 , заключалась в определении взаимосвязи между иммунной средой конкретных видов рака и аллергией, уделяя особое внимание цитокинам, связанным с ответами Th2 и Th3, связанными с IgE.
Результаты
Демографические данные представлены в таблице 1. В группе больных раком преобладали мужчины, а распространенность алкоголизма и курения была выше в группе больных раком. Средний возраст участников составил 63 (± 10) лет, и между группами не было различий (9 лет).0243 р > 0,05). Стадия рака: I — 3%, II — 24%, III — 38%, IV — 35%.
Таблица 1 Характеристика исследуемого образца.Полноразмерная таблица
Об аллергии сообщалось в 50 % контрольной группы и только в 20 % онкологической группы (ОШ 0,46, 95% ДИ 0,26–0,81, p = 0,009). При сравнении контрольной группы и группы с аденокарциномой простаты наблюдалась обратная связь (ОШ 0,17, 95% ДИ 0,04–0,79, p = 0,024). Однако по сравнению с группой аденокарциномы желудка различий не наблюдалось (ОШ 0,25, 95% ДИ 0,06–1,02, p = 0,053), или с группой плоскоклеточного рака головы и шеи (HNSCC) (OR 0,33, 95% ДИ 0,09–1,27, p = 0,108). Наиболее частым видом аллергии был ринит, который наблюдался у 15 % онкологических больных и у 35 % лиц контрольной группы ( p = 0,005) (табл. 1).
Однако по сравнению с группой аденокарциномы желудка различий не наблюдалось (ОШ 0,25, 95% ДИ 0,06–1,02, p = 0,053), или с группой плоскоклеточного рака головы и шеи (HNSCC) (OR 0,33, 95% ДИ 0,09–1,27, p = 0,108). Наиболее частым видом аллергии был ринит, который наблюдался у 15 % онкологических больных и у 35 % лиц контрольной группы ( p = 0,005) (табл. 1).
Совпадение между сообщениями об аллергии и положительным IgE (которое считается концентрацией IgE ≥ 25 МЕ/мл) было слабым во всех группах: κ = 0,000 в контрольной группе, κ = 0,002 в группе больных раком, а именно κ = – 0,037 для аденокарциномы предстательной железы, κ = 0,237 для аденокарциномы желудка и κ =-0,250 для HNSCC.
Повышение IL-2 наблюдалось у пациентов с ПРГШ по сравнению с контролем ( p = 0,005). В группе больных раком наблюдалось снижение ИЛ-4 (предстательная железа: p = 0,001, HNSCC: p = 0,045, желудочный: p = 0,046), IL-17 (предстательная железа: p 9024 0,045). 0,034, HNSCC: p = 0,001, желудочный: p = 0,004) и IL-1β (предстательная железа: p = 0,012, желудочный: p = 0,012, желудочный: p 0=0) группа (простата: p = 0,001 и желудочный: p = 0,001). Никакой связи между цитокинами и стадией рака не наблюдалось. (Таблица 2).
0,034, HNSCC: p = 0,001, желудочный: p = 0,004) и IL-1β (предстательная железа: p = 0,012, желудочный: p = 0,012, желудочный: p 0=0) группа (простата: p = 0,001 и желудочный: p = 0,001). Никакой связи между цитокинами и стадией рака не наблюдалось. (Таблица 2).
Полноразмерная таблица
Не было различий в значениях медиан цитокинов между двумя группами, основанных на концентрациях IgE или классификации IgE в нормальных, пограничных или высоких категориях (p > 0,05) (таблица 3). . В обеих группах наблюдалась слабая корреляция между большинством цитокинов и уровнями IgE (коэффициенты корреляции Спирмена < 0,4 для большинства групп) 45 . Умеренная корреляция выявлена только в группе аденокарциномы простаты для TGF-β (r = 0,54, p = 0,01) и IL-17 (r = 0,42, p = 0,06), а также для аденокарциномы желудка (r = 0,40, p = 0,07) для ИЛ-2 (рис. 1). В группе общего рака (r = 0,25, p = 0,60), рака предстательной железы (r = 0,12, p = 0,62), HNSCC (r = 0,07, p 0,78) и рак желудка (r = 0,22, p = 0,37).
1). В группе общего рака (r = 0,25, p = 0,60), рака предстательной железы (r = 0,12, p = 0,62), HNSCC (r = 0,07, p 0,78) и рак желудка (r = 0,22, p = 0,37).
Полноразмерная таблица
Рисунок 1Диаграммы дисперсии и оси линейной регрессии, основанные на факторах корреляции между цитокинами (пг/мл) и IgE (UI/мл), стратифицированными по группам пациентов. Корреляционный тест Спирмена. * Группы с умеренной корреляцией ( Devore JL 45 ) . Группы: контроль (n = 20), рак предстательной железы (n = 20), ПРГШ (n = 20), рак желудка (n = 20). Сокращения: IgE = иммуноглобулин E, IL = интерлейкин, TGF = трансформирующий фактор роста, HNSCC = плоскоклеточный рак головы и шеи.
Изображение в полный размер
Чтобы определить, связано ли наличие зарегистрированных аллергий с преобладанием некоторых маркеров иммунитета, цитокинов (Th2 (IL-2), Th3 (IL-4), Th27 (IL-17), IL- 1β, TGF-β) и IgE сравнивали между обеими группами. Таблица 4 показывает, что в этом исследовании не было различий между этими переменными.
Таблица 4 показывает, что в этом исследовании не было различий между этими переменными.
Полноразмерный стол
Обсуждение
Связь между раком и аллергией изучалась с 1950-х годов 46 и дала противоречивые результаты из-за разнообразия методов исследования и факторов риска развития рака или аллергии, таких как возраст, использование лекарств и сопутствующие заболевания, часто не контролируется 6,38,39 . Эти переменные наблюдались и тщательно корректировались в этом исследовании, чтобы не мешать интерпретации результатов и сохранить их надежность.
Обнаружена обратная связь между раком и клинически выявленными аллергиями, что подтверждает теорию иммунного надзора 12,47 , что выше при аллергических процессах и может быть связано с поражением злокачественных клеток 1,5 . В этом исследовании, как и в других исследованиях, проведенных в том же направлении, была отмечена более низкая распространенность аллергии у онкологических больных, особенно при наличии аденокарциномы предстательной железы, по сравнению с контрольной группой 33,40 . Также была обнаружена обратная связь между сообщениями об аллергии и наличием ПРГШ, а также аденокарциномы желудка 9.0009 34,37,48,49 . Отсутствие значимости в этом сравнении в настоящем исследовании, которое было выявлено только как тенденция, вероятно, связано с небольшим числом случаев, хотя мы изучили большее количество лиц, чем описано в литературе в аналогичных исследованиях 38,39 .
Также была обнаружена обратная связь между сообщениями об аллергии и наличием ПРГШ, а также аденокарциномы желудка 9.0009 34,37,48,49 . Отсутствие значимости в этом сравнении в настоящем исследовании, которое было выявлено только как тенденция, вероятно, связано с небольшим числом случаев, хотя мы изучили большее количество лиц, чем описано в литературе в аналогичных исследованиях 38,39 .
Основным ограничением этой работы было небольшое количество участников в группе из-за специфичности раковых заболеваний, которые были исследованы. Тщательный статистический анализ всех параметров делает это исследование пригодным для выводов о взаимосвязи между аллергией и раком. В это исследование могут быть включены другие виды рака, которые относятся к будущим обзорам того же направления исследований. Эти предстоящие исследования расширят текущие данные за счет большего числа участников.
Аллергия представляет собой комплексное расстройство, включающее иммунные факторы, которые могут зависеть или не зависеть от IgE, и доступно несколько исследований, в которых оценивается дозировка IgE в сыворотке у онкологических больных 35,50,51,52 . Хотя IgE полезен для выявления аллергии, этот иммуноглобулин не увеличивается при всех типах аллергических реакций, что может объяснить низкую согласованность между зарегистрированными аллергиями и положительным IgE, наблюдаемым в этой работе, как и в другом исследовании 44 .
Хотя IgE полезен для выявления аллергии, этот иммуноглобулин не увеличивается при всех типах аллергических реакций, что может объяснить низкую согласованность между зарегистрированными аллергиями и положительным IgE, наблюдаемым в этой работе, как и в другом исследовании 44 .
Когда обнаруживается обратная связь между раком и аллергией, в качестве объяснения упоминаются теории иммунного надзора и иммунопрофилактики. Теория иммунного надзора предполагает, что реакции на аллергены усиливают иммунный ответ, включая выработку IgE и активацию эффекторных иммунных клеток (моноцитов, макрофагов, естественных киллеров , эозинофилов, мастоцитов и базофилов), способных выявлять и уничтожать рак. клетки. Активация Th3-ответа, наблюдаемая при аллергических состояниях, способствует синтезу родственных цитокинов, таких как IL-4 и IL-3, что способствует синтезу IgE против специфических опухолевых антигенов, способных активировать эффекторные клетки и разрушать опухоли 19,36,37 . Теория иммунопрофилактики связана с вдыханием антигенов и проявлениями аллергических реакций (кашель, чихание и др.), направленных на элиминацию этих антигенов с помощью IgE и активированных эффекторных клеток, повреждающих и удаляющих инфекционные микроорганизмы, мутагенные токсины и канцерогены окружающей среды 34,36, 37 .
Теория иммунопрофилактики связана с вдыханием антигенов и проявлениями аллергических реакций (кашель, чихание и др.), направленных на элиминацию этих антигенов с помощью IgE и активированных эффекторных клеток, повреждающих и удаляющих инфекционные микроорганизмы, мутагенные токсины и канцерогены окружающей среды 34,36, 37 .
Только два исследования оценивали измерение цитокинов и других биомаркеров, связывающих рак и аллергию 38,39 . В исследовании, сравнивающем цитокины от HNSCC с группой аллергического ринита и контрольной группой (без рака или аллергии), не наблюдалось различий между концентрациями исследуемых цитокинов (ответ Th2 (IL-2, IL-12, IFN-γ). , TNF-α), Th3 (IL-4, IL5, IL-13), врожденный иммунитет (IL-1β, IL-8, IL-17), врожденный иммунитет (MCP)-1, макрофагальный воспалительный белок (MIP)- 1β, колониестимулирующий фактор гранулоцитов и макрофагов (G-CSF), колониестимулирующий фактор гранулоцитов и макрофагов (GM-CSF) и иммунитет, связанный с Т-клетками (IL-6, IL-7, IL-10) 38 . Другое исследование с участием пациентов с раком молочной железы не выявило различий в концентрациях цитокинов (IL-1β, IL-6, IFN-γ, IL-4) между группами, страдающими раком и аллергией 39 .
Другое исследование с участием пациентов с раком молочной железы не выявило различий в концентрациях цитокинов (IL-1β, IL-6, IFN-γ, IL-4) между группами, страдающими раком и аллергией 39 .
Тот факт, что группы не были объединены в пары по возрасту, что могло повлиять на результаты, поскольку иммунный ответ меняется с возрастом, и что было задействовано меньшее количество пациентов по сравнению с настоящей работой, являются ограничениями в этих исследованиях. два предыдущих исследования 38,39 . Результаты в этом исследовании, а также в исследованиях, упомянутых в литературе, показали отсутствие различий в цитокинах, связанных с параметрами Th2 и Th3, в связи между раком и аллергическими процессами, связанными с реакциями гиперчувствительности I типа. Это открытие противоречит одной из теорий, предложенных в литературе по эпидемиологическим исследованиям рака и аллергии, в которой предполагалось различие в цитокинах, связанных с параметрами Th2 и Th3 19,36,37 .
Новые исследования расширили знания за пределами парадигмы Th2/Th3 иммунной системы и других подмножеств клеток, участвующих в этом процессе, таких как Th4, Th27, Th9, фолликулярные Th и регуляторные Т, показывая, что эти взаимосвязи шире. Дополнительная гипотеза, отличная от парадигмы Th2/Th3, основана на публикациях, в которых утверждается, что T CD4+ лимфоциты проявляют пластичность и не ведут себя как негибкие Th2 или Th3, продуцируя лишь несколько цитокинов 53,54 , несмотря на гибкость в синтезе медиаторов и в превращении эффекторных клеток Th2, Th3, Th27 или регуляторных T 21,22,23,55 . В зависимости от действия определенных цитокинов часть Т-клеток может трансформироваться в клетки, секретирующие различные цитокины 21,22,23,55,56 .
Иммуномодулирующие цитокины (TGF-β, IL-10, IL-17 и IL-23) способствуют развитию опухоли, в то время как другие (IFN-γ, TNF-α, GM-CSF, IL-2, IL-6, IL-17 и IL-12) способствуют иммунному надзору и задерживают его рост 19,57 . Исследования, посвященные раку и аллергии, должны оценивать эти литературные данные.
Исследования, посвященные раку и аллергии, должны оценивать эти литературные данные.
Чтобы определить, существует ли корреляция других медиаторов, потенциально участвующих в связи между раком и аллергией, были изучены другие цитокины. Было обнаружено увеличение уровня регуляторных цитокинов IL-2 и TGF-β, а также снижение уровня IL-4, IL-17 и IL-1β, отражающее иммуносупрессивную среду онкологического больного и более низкую распространенность аллергии. Такие данные и характерные уровни цитокинов в опухолях подтверждают специфичность иммунного ответа в зависимости от типа рака 32 . Умеренная корреляция между IgE и IL-17 и TGF-β в группе аденокарциномы предстательной железы предполагает наличие маркера аллергии с иммуносупрессивным ответом и специфичностью иммунного ответа в зависимости от типа опухоли. Исследования показывают, что TGF-β не оказывает прямого влияния на происхождение клеток Th27; однако это может способствовать его развитию, чтобы подавить дифференцировку Th2 58,59 .
Для лучшего понимания механизмов взаимосвязи между раком и аллергией необходимы исследования, включающие большее количество цитокинов и их связь с молекулярным мессенджером (информационная РНК), ответственным за синтез цитокинов, участвующих в аллергии и воспалении 23,60 . Будущие исследования должны включать оценку в контрольной среде иммунной системы к экзогенным антигенам, вызывающим аллергию у онкологических больных, в динамическом исследовании антигенного стимула и его реакции в иммунной системе 61,62,63 .
Выводы
Выявлена обратная связь между раком и клиническими проявлениями аллергии. При раке головы и шеи, желудка и предстательной железы преобладала опухолевая среда с иммуносупрессивной сывороткой. Не было различий в цитокинах, связанных с параметрами Th2 и Th3, по отношению к IgE. Корреляции между клинически доказанной аллергией и маркерами иммунитета, относящимися к одним и тем же аллергенам, обнаружено не было.
Методы
Одобрение этических норм и согласие на участие
Это исследование проводилось в соответствии с принципами, изложенными в Хельсинкской декларации 1964 г. и во всех последующих редакциях. Эта работа была одобрена Комитетом по этике исследований Больничного фонда штата Минас-Жерайс в соответствии с протоколом № 075/2009. Информированное согласие было получено от всех участников.
и во всех последующих редакциях. Эта работа была одобрена Комитетом по этике исследований Больничного фонда штата Минас-Жерайс в соответствии с протоколом № 075/2009. Информированное согласие было получено от всех участников.
Набор пациентов, характеристики и сбор образцов
В этом контрольном исследовании оценивались цитокины, связанные с параметрами Th2 (IL-2) и Th3 (IL-4), по отношению к уровням IgE и сообщениям об аллергии у контрольных людей. и больных раком. Уровни иммунных медиаторов, участвующих в ответе Th27 (IL-17), как в иммуносупрессии/иммунорегуляции (TGF-β), так и в провоспалении IL1-β по отношению к уровням IgE и зарегистрированным аллергиям у контрольных людей и больных раком, также были оценивается.
В это исследование были включены пациенты с недавним гистологическим диагнозом рака, и они были допущены к исследованию только до прохождения какого-либо лечения. Включенные лица были старше 18 лет, обоих полов, которые представили Eastern Cooperative Oncology Group p (ECOG) оценку эффективности от нуля до двух 42 , стадию TNM от I до IV 43 , и нет предшествующая история других видов рака, аутоиммунных заболеваний или иммунного лечения, терапии кортикостероидами, химиотерапии или лучевой терапии.
Контрольная группа состояла из 20 добровольцев, не страдающих раком и не принимавших лекарств, отобранных по возрасту для включения в группу больных раком. Клиническая оценка проводилась с целью выявления вредных привычек, алкоголизма и курения, сопутствующих заболеваний, медикаментозного анамнеза, аллергии в анамнезе, типа аллергии (аллергический ринит, атопический дерматит, астма, пищевая и лекарственная аллергия), а также аллергических симптомов после воздействия некоторых аллергенов, таких как как лекарства, продукты питания, пыль, плесень или животные. Информация, связанная с аллергией, специально запрашивалась у всех пациентов и добровольцев, подчеркивая детали, связанные с каждым аллергическим проявлением. Все зарегистрированные аллергии были подтверждены медицинской диагностикой с определением аллергенов для каждого случая.
Настоящее исследование включало 60 больных раком, разделенных на три подгруппы (n = 20): аденокарциному желудка, аденокарциному предстательной железы и плоскоклеточный рак головы и шеи (HNSCC). Эти опухоли были выбраны потому, что они показали обратную связь с аллергией в предыдущем эпидемиологическом исследовании в рамках того же направления исследований 40 . Все пациенты обеих групп были идентифицированы по полу и возрасту. Больные раком подвергались той же клинической оценке, что и контрольная группа, в отношении аллергии и ее связи с раком, учитывая его гистологию, локализацию, стадирование и диагностические данные.
Эти опухоли были выбраны потому, что они показали обратную связь с аллергией в предыдущем эпидемиологическом исследовании в рамках того же направления исследований 40 . Все пациенты обеих групп были идентифицированы по полу и возрасту. Больные раком подвергались той же клинической оценке, что и контрольная группа, в отношении аллергии и ее связи с раком, учитывая его гистологию, локализацию, стадирование и диагностические данные.
Дозы сывороточных цитокинов были получены с использованием метода ELISA в соответствии с инструкциями производителя. В этом исследовании рассматривали общий IgE (ALPCO, Салем, Нью-Гэмпшир, США), IL-2 (Enzo Life Sciences, Фармингдейл, Нью-Йорк, США), IL-4 (Enzo Life Sciences, Фармингдейл, Нью-Йорк, США), TGF-β (Xpressbio Life Science, Фредерик, Мэриленд, США), IL1-β (Xpressbio Life Science, Фредерик, Мэриленд, США) и IL-17 (Xpressbio Life Science, Фредерик, Мэриленд, США).
Статистический анализ
Статистический анализ проводился с использованием Статистический пакет программного обеспечения для социальных наук, версия 25 [https://www. ibm.com/support/pages/downloading-ibm-spss-statistics-25] 44 . Для оценки нормальности каждого параметра был проведен критерий нормальности Колмогорова-Смирнова. Непараметрический тест использовался, когда не было нормальных данных, а параметрический тест использовался для сравнения нормальных средних значений данных с их соответствующими стандартными отклонениями. Отношение шансов (OR) (OR) с доверительным интервалом 95% использовалось для оценки ассоциации с фактором риска, что указывает на ассоциацию, если значение 1 не задействовано. Корреляция между переменными была сделана с помощью корреляции Спирмена. Множественные сравнения были сделаны с помощью теста Крускала-Уоллиса. Все тесты были двусторонними, и величина разницы считалась значимой, если она соответствовала р < 0,05.
ibm.com/support/pages/downloading-ibm-spss-statistics-25] 44 . Для оценки нормальности каждого параметра был проведен критерий нормальности Колмогорова-Смирнова. Непараметрический тест использовался, когда не было нормальных данных, а параметрический тест использовался для сравнения нормальных средних значений данных с их соответствующими стандартными отклонениями. Отношение шансов (OR) (OR) с доверительным интервалом 95% использовалось для оценки ассоциации с фактором риска, что указывает на ассоциацию, если значение 1 не задействовано. Корреляция между переменными была сделана с помощью корреляции Спирмена. Множественные сравнения были сделаны с помощью теста Крускала-Уоллиса. Все тесты были двусторонними, и величина разницы считалась значимой, если она соответствовала р < 0,05.
Уровни корреляции, согласно факторам Спирмена, классифицировались как очень слабая (от 0,00 до 0,19), слабая (от 0,20 до 0,39), умеренная (от 0,40 до 0,69), сильная (от 0,70 до 0,89) и очень сильная (от 0,90 до 1,00).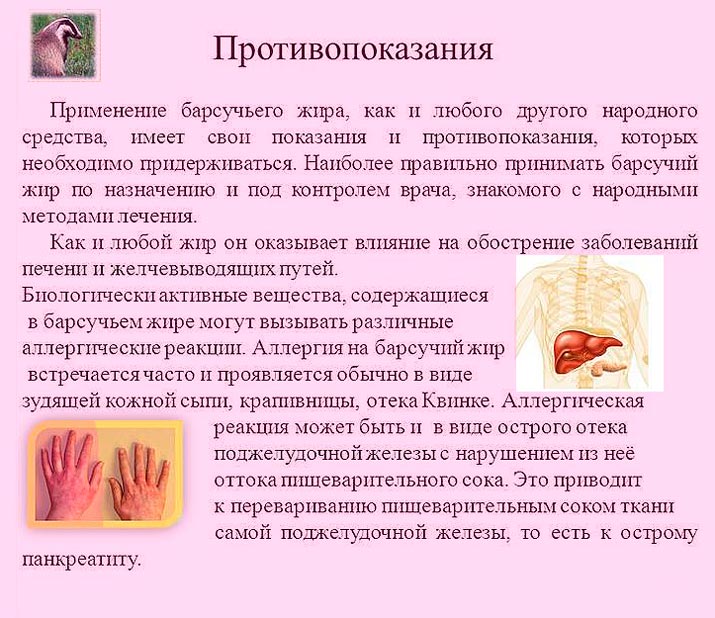 ) 45 . Фактор каппа оценивал соответствие между положительным результатом IgE и зарегистрированной аллергией и был классифицирован как слабый (κ ≤ 0,40), промежуточный (0,40 ≤ κ ≤ 0,75) и сильный (κ ≥ 0,75) 44 .
) 45 . Фактор каппа оценивал соответствие между положительным результатом IgE и зарегистрированной аллергией и был классифицирован как слабый (κ ≤ 0,40), промежуточный (0,40 ≤ κ ≤ 0,75) и сильный (κ ≥ 0,75) 44 .
Каталожные номера
Дженсен-Яролим, Э. и др. AllergoOncology – влияние аллергии на онкологию: документ с изложением позиции EAACI. Allergy 72 (6), 866–887 (2017).
Артикул КАС пабмед Google ученый
Ригони, А., Коломбо, М.П. и Пусильо, К. Тучные клетки, базофилы и эозинофилы: от аллергии к раку. Семин. Иммунол. 35 , 29–34 (2018).
Артикул КАС пабмед Google ученый
Палм, Н. В., Розенштейн, Р. К. и Меджитов, Р. Аллергическая защита хозяина.
 Природа 484 (7395), 465–472 (2012).
Природа 484 (7395), 465–472 (2012).Артикул КАС пабмед ОБЪЯВЛЕНИЯ Google ученый
Пулендран, Б. и Артис, Д. Новые парадигмы иммунитета 2 типа. Наука 337 (6093), 431–435 (2012).
Артикул КАС пабмед ПабМед Центральный ОБЪЯВЛЕНИЯ Google ученый
Hoste, E., Cipolat, S. & Watt, F.M. Понимание риска аллергии и рака: каковы барьеры?. Нац. Преподобный Рак. 15 (3), 131–132 (2015).
Артикул пабмед Google ученый
Козловска Р., Божек А. и Ярзаб Дж. Связь между раком и аллергией. Клиника Аллергической Астмы. Иммунол. 12 , 39 (2016).
Артикул пабмед ПабМед Центральный КАС Google ученый
«>Окерт Д., Шмитц М., Хэмпл М. и Рибер Э. П. Достижения в иммунотерапии рака. Иммунол. Сегодня. 20 (2), 63–65 (1999).
Артикул КАС пабмед Google ученый
Дженсен-Яролим, Э. и др. Аллергоонкология: роль IgE-опосредованной аллергии при раке. Аллергия 63 (10), 1255–1266 (2008).
Артикул КАС пабмед Google ученый
Jensen-Jarolim, E., Turner, M.C. & Karagiannis, S.N. Аллергоонкология: IgE- и IgG4-опосредованные иммунные механизмы, связывающие аллергию с раком, и их трансляционные последствия.
 J. Аллергическая клиника. Иммунол. 140 (4), 982–984 (2017).
J. Аллергическая клиника. Иммунол. 140 (4), 982–984 (2017).Артикул пабмед Google ученый
Нойкрист, К. и др. Распределение иммуноглобулинов при плоскоклеточном раке головы и шеи. Междунар. Арка Аллергия Иммунол. 104 (1), 97–100 (1994).
Артикул КАС пабмед Google ученый
Кумар, С., Сайни, Р. В. и Махиндроо, Н. Последние достижения в области иммунологии рака и противоопухолевой терапии на основе иммунологии. Биомед. Фармацевт. 96 , 1491–1500 (2017).
Артикул КАС пабмед Google ученый
Финн, О. Дж. Иммуноонкология: понимание функции и дисфункции иммунной системы при раке. Энн. Онкол. 23 (Приложение 8), 6–9 (2012).
Артикул Google ученый
«>Whiteside, T. L. Иммунная супрессия при раке: влияние на иммунные клетки, механизмы и будущее терапевтическое вмешательство. Семин. Рак биол. 16 (1), 3–15 (2006).
Артикул КАС пабмед Google ученый
Фельдман С. Х., Лю Дж., Фельдман С., Соломон Д. Х. и Ким С. С. Риск дисплазии шейки матки высокой степени и рака шейки матки у женщин с системной красной волчанкой, принимающих иммунодепрессанты. Волчанка 26 (7), 682–689 (2017).
Артикул КАС пабмед Google ученый
Гарритсен, Ф. М. и др.
 Риск немеланомного рака кожи у пациентов с атопическим дерматитом, принимающих пероральные иммунодепрессанты. Акта Дерм. Венереол. 97 (6), 724–730 (2017).
Риск немеланомного рака кожи у пациентов с атопическим дерматитом, принимающих пероральные иммунодепрессанты. Акта Дерм. Венереол. 97 (6), 724–730 (2017).Артикул КАС пабмед Google ученый
Дженсен-Яролим, Э. и Павелец, Г. Зарождающаяся область аллергоонкологии. Рак Иммунол. Иммунотер. 61 (9), 1355–1357 (2012).
Артикул КАС пабмед ПабМед Центральный Google ученый
Дженсен-Яролим, Э. и др. Аллергоонкология: противоположные результаты иммунной толерантности при аллергии и раке. Аллергия 73 (2), 328–340 (2018).
Артикул КАС пабмед Google ученый
Амириан Э. С. и др. Приближение к научному консенсусу в отношении связи между аллергией и риском глиомы: отчет о международном исследовании глиомы случай-контроль.
 Рак Эпидемиол. Биомарк. Пред. 25 (2), 282–290 (2016).
Рак Эпидемиол. Биомарк. Пред. 25 (2), 282–290 (2016).Артикул КАС Google ученый
Ван Ю. Ю. Многозадачность Т-хелперов. Иммунология 130 (2), 166–171 (2010).
Артикул КАС пабмед ПабМед Центральный Google ученый
O’Shea, J.J. & Paul, W.E. Механизмы, лежащие в основе приверженности линии и пластичности вспомогательных CD4+ T-клеток. Наука 327 (5969), 1098–1102 (2010).
Артикул КАС пабмед ПабМед Центральный ОБЪЯВЛЕНИЯ Google ученый
Cosmi, L., Maggi, L., Santarlasci, V., Liotta, F. & Annunziato, F. Пластичность Т-хелперных клеток при воспалении. Цитометрия А. 85 (1), 36–42 (2014).
Артикул пабмед КАС Google ученый
«>Gianchecchi, E. & Fierabracci, A. Ингибирующие рецепторы и пути лимфоцитов: роль PD-1 в развитии Treg и их участие в возникновении аутоиммунитета и прогрессировании рака. Фронт Иммунол. 9 , 2374 (2018).
Артикул пабмед ПабМед Центральный КАС Google ученый
Такеучи Ю. и Нишикава Х. Роль регуляторных Т-клеток в иммунитете против рака. Междунар. Иммунол. 28 (8), 401–409 (2016).
Артикул КАС пабмед ПабМед Центральный Google ученый
«>Нетеа, М. Г., ван де Вердонк, Ф. Л., ван дер Меер, Дж. В., Динарелло, К. А. и Йостен, Л. А. Независимая от воспаления регуляция цитокинов семейства IL-1. Анну. Преподобный Иммунол. 33 , 49–77 (2015).
Артикул КАС пабмед Google ученый
Лин, Р. Л. и Чжао, Л. Дж. Механистическая основа и клиническая значимость роли трансформирующего фактора роста-β в развитии рака. Рак Биол. Мед. 12 (4), 385–393 (2015).
КАС пабмед ПабМед Центральный Google ученый
«>Блоб, Г. К., Шиманн, В. П. и Лодиш, Х. Ф. Роль бета-трансформирующего фактора роста в заболевании человека. Н. англ. Дж. Мед. 342 (18), 1350–1358 (2000).
Артикул КАС пабмед Google ученый
Lippitz, B.E. Цитокиновые паттерны у больных раком: систематический обзор. Ланцет Онкол. 14 (6), e218-228 (2013).
Артикул КАС пабмед Google ученый
Карнейро, Б. Г. М. К., Петрояну, А., Резенде, В. и Альберти, Л.
 Р. Лечение рака, аллергии и иммуномедиадоров. Revista Médica de Minas Gerais. 27 (e-1877), 1–6 (2017).
Р. Лечение рака, аллергии и иммуномедиадоров. Revista Médica de Minas Gerais. 27 (e-1877), 1–6 (2017).Google ученый
Ляо Х.К. и др. Симптомы аллергии, общий иммуноглобулин Е в сыворотке и риск рака головы и шеи. Рак вызывает контроль. 27 (9), 1105–1115 (2016).
Артикул пабмед Google ученый
Божек А. и др. Может ли атопия оказывать защитное действие против рака?. PLoS ONE 15 (2), e0226950 (2020).
Артикул пабмед ПабМед Центральный КАС Google ученый
Джозефс Д. Х., Спайсер Дж. Ф., Корриган С. Дж., Гулд Х. Дж. и Карагианнис С. Н. Эпидемиологические ассоциации аллергии, IgE и рака. клин. Эксп. Аллергия. 43 (10), 1110–1123 (2013).

КАС пабмед Google ученый
Cui, Y. & Hill, A.W. Атопия и специфические локализации рака: обзор эпидемиологических исследований. клин. Преподобный Аллергия Иммунол. 51 (3), 338–352 (2016).
Артикул пабмед Google ученый
Millrud, C. R. и др. Обратные иммунологические реакции, вызванные аллергическим ринитом и плоскоклеточным раком головы и шеи. PLoS ONE 9 (1), e86796 (2014).
Артикул пабмед ПабМед Центральный ОБЪЯВЛЕНИЯ КАС Google ученый
Ковальчевская М.Е. и др. Анализ участия цитокинов в ассоциации аллергии и рака молочной железы. Контемп Онкол (Позн). 18 (6), 396–402 (2014).
ПабМед ПабМед Центральный Google ученый
«>Карнейро, Б. Г. М. К. и Петрояну, А. Связь между раком и аллергией. Заявл. Cancer Res.. 31 (4), 3 (2011).
Google ученый
Окен, М. М. и др. Критерии токсичности и ответа Восточной кооперативной онкологической группы. утра. Дж. Клин. Онкол. 5 (6), 649–655 (1982).
Артикул КАС пабмед Google ученый
Amid, ME Руководство по стадированию рака AJCC (Спрингер, 2017 г.).
Google ученый
«>Девор, Дж. Л. Вероятность и статистика для технических и естественных наук 8-е изд. (CengageLearning, 2011).
Google ученый
Логан Дж. и Сакер Д. Частота аллергических заболеваний при раке. NZ Med. J. 52 (289), 210–212 (1953).
КАС пабмед Google ученый
Wulaningsih, W. et al. Изучение связи между аллерген-специфическим иммуноглобулином Е, риском рака и выживаемостью. Онкоиммунология. 5 (6), e1154250 (2016).
Артикул пабмед ПабМед Центральный КАС Google ученый
«>Эль-Зейн, М. и др. История астмы или экземы и риск рака среди мужчин: популяционное исследование случай-контроль в Монреале, Квебек, Канада. Энн. Аллергия Астма Иммунол. 104 (5), 378–384 (2010).
Артикул пабмед Google ученый
Гусиас, К. и др. Частые нарушения иммунной системы при глиомах и корреляция с системой классификации злокачественных новообразований ВОЗ. J. Нейроиммунол. 226 (1–2), 136–142 (2010).
Артикул КАС пабмед Google ученый
«>Вимелс, Дж. Л. и др. Риск плоскоклеточного рака кожи в связи с IgE: вложенное исследование случай-контроль. Рак Эпидемиол. Биомарк. Пред. 20 (11), 2377–2383 (2011).
Артикул КАС Google ученый
Мосманн, Т. Р., Червински, Х., Бонд, М. В., Гидлин, М. А. и Коффман, Р. Л. Два типа мышиных хелперных Т-клеточных клонов. I. Определение по профилям активности лимфокинов и секретируемых белков. J. Иммунол. 136 (7), 2348–2357 (1986).
КАС пабмед Google ученый
Аббас А.К., Мерфи К.
 М. и Шер А. Функциональное разнообразие хелперных Т-лимфоцитов. Природа 383 (6603), 787–793 (1996).
М. и Шер А. Функциональное разнообразие хелперных Т-лимфоцитов. Природа 383 (6603), 787–793 (1996).Артикул КАС пабмед ОБЪЯВЛЕНИЯ Google ученый
Hirahara, K. & Nakayama, T. Субпопуляции CD4+ T-клеток при воспалительных заболеваниях: за пределами парадигмы Th2/Th3. Междунар. Иммунол. 28 (4), 163–171 (2016).
Артикул КАС пабмед ПабМед Центральный Google ученый
Лим А.И., Верриер Т., Восшенрих К.А. и Ди Санто Дж.П. Варианты развития и функциональная пластичность врожденных лимфоидных клеток. Курс. мнение Иммунол. 44 , 61–68 (2017).
Артикул КАС пабмед Google ученый
Гривенников С.И., Гретен Ф.Р. и Карин М. Иммунитет, воспаление и рак. Cell 140 (6), 883–899 (2010).

Артикул КАС пабмед ПабМед Центральный Google ученый
Горески, К. и др. Генерация патогенных клеток T(H)17 в отсутствие передачи сигналов TGF-β. Природа 467 (7318), 967–971 (2010).
Артикул КАС пабмед ПабМед Центральный ОБЪЯВЛЕНИЯ Google ученый
Сантарлаши, В. и др. TGF-бета косвенно способствует развитию клеток Th27 человека путем ингибирования клеток Th2. евро. Дж. Иммунол. 39 (1), 207–215 (2009).
Артикул КАС пабмед Google ученый
Шварцбаум, Дж. А. и др. Транскриптом аллергии и воспаления преимущественно отрицательно коррелирует с экспрессией CD133 при глиобластоме. Нейроонкол. 12 (4), 320–327 (2010).
Артикул КАС пабмед Google ученый
«>Петрояну, А., Босон, В.Л., Бэйл, А.Е., Фридман, Э. и Де Марко, Л. Мутационный анализ генов-кандидатов в плоскоклеточном раке человека. Ларингоскоп 109 , 661–663 (1999).
Артикул КАС пабмед Google ученый
Треллакис, С. и др. Нейтрофильные гранулоциты периферической крови пациентов с плоскоклеточным раком головы и шеи функционально отличаются от их аналогов у здоровых доноров. Междунар. Дж. Иммунопат. Фармакол. 24 (3), 683–693 (2011).
Артикул КАС пабмед Google ученый
Платцер, Б. и др. IgE/FcεRI-опосредованная перекрестная презентация антигена дендритными клетками усиливает противоопухолевый иммунный ответ. Cell Rep. 10 , 1487 (2015).
Артикул КАС пабмед ПабМед Центральный Google ученый
Ярчоан Р. и Улдрик Т. С. Рак, связанный с ВИЧ, и сопутствующие заболевания. Н. англ. Дж. Мед. 378 (11), 1029–1041 (2018).
Артикул пабмед ПабМед Центральный Google ученый
Хирахара К. и др. Механизмы, лежащие в основе пластичности хелперных Т-клеток: значение для иммуноопосредованного заболевания. J. Аллергическая клиника. Иммунол. 131 (5), 1276–1287 (2013).
Артикул КАС пабмед ПабМед Центральный Google ученый
Паломо, Дж., Дитрих, Д., Мартин, П., Палмер, Г. и Габай, С. Семейство цитокинов интерлейкина (IL)-1 – Баланс между агонистами и антагонистами при воспалительных заболеваниях. Цитокин 76 (1), 25–37 (2015).
Артикул КАС пабмед Google ученый
Тирадо-Родригес Б., Ортега Э., Сегура-Медина П. и Уэрта-Йепез С. TGF-β: важный медиатор аллергических заболеваний и молекула с двойной активностью в развитии рака. Дж. Иммунол. Рез. 2014 , 318481 (2014).
Артикул пабмед ПабМед Центральный КАС Google ученый
Петрояну А., Чавес Д. Н. и Де Оливейра О. Сравнительная частота аллергии при наличии или отсутствии рака. Дж. Междунар. Мед. Рез. 23 (5), 358–363 (1995).
Артикул КАС пабмед Google ученый
Wiemels, J. L. et al. Снижение уровня иммуноглобулина Е и аллергии у взрослых с глиомой по сравнению с контрольной группой. Рак Res. 64 (22), 8468–8473 (2004).
Артикул КАС пабмед Google ученый
Хсиао, Дж. Р. и др. Аллергии и риск рака головы и шеи: оригинальное исследование плюс метаанализ. PLoS ONE 8 (2), e55138 (2013 г.).
Артикул КАС пабмед ПабМед Центральный ОБЪЯВЛЕНИЯ Google ученый
Биггар, Р. Дж. и др. Уровни подкласса иммуноглобулина у пациентов с неходжкинской лимфомой. Междунар. Дж. Рак. 124 (11), 2616–2620 (2009).
Артикул КАС пабмед Google ученый
Франссон, М. и др. Активация Toll-подобных рецепторов 2, 3 и 4 при аллергическом рините. Респир. Рез. 6 , 100 (2005).
Артикул пабмед ПабМед Центральный КАС Google ученый
Ссылки на скачивание
Благодарности
Особая благодарность выражается всем пациентам и вовлеченным учреждениям и исследователям.
Финансирование
Эта работа была поддержана CNPq (Национальный совет по науке и технологиям) и FAPEMIG (Фонд поддержки исследований штата Минас-Жерайс).
Информация об авторе
Авторы и организации
Хирургический факультет медицинского факультета Федерального университета Минас-Жерайс, Белу-Оризонти, Бразилия
Энди Петрояну, Луис Роналдо Альберти, Вивиан Резенде и София Кандия Барриентос
Онкологическая служба больницы Альберто Кавальканти больничного фонда штата Минас-Жерайс, Руа-Рио-Кларо 235, ап 401, Белу-Оризонти, MG , 30411-235, Бразилия
Bruno Gustavo Muzzi Carvalho Carneiro
Больница Santa Casa of Belo Horizonte, Белу-Оризонти, Бразилия
José Augusto Nogueira Machado, Paula Martins Ferreira dos Silos & Fabiana Rocha da0003
Авторы
- Bruno Gustavo Muzzi Carvalho Carneiro
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Andy Petroianu
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- José Augusto Nogueira Machado
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Paula Martins Ferreira dos Anjos
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Fabiana Rocha da Silva
Просмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Luiz Ronaldo Alberti
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Вивиан Резенде
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Sofia Candia Barrientos
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Contributions
B. G.M.C.C., AP, J.A.N.M., L.R.A. и V.R. разработал эксперименты; B.G.M.C.C., P.M.F.A., F.R.S. и S.C.B. проводил опыты; B.G.M.C.C., A.P. и J.A.N.M. проанализировал данные и написал рукопись.
G.M.C.C., AP, J.A.N.M., L.R.A. и V.R. разработал эксперименты; B.G.M.C.C., P.M.F.A., F.R.S. и S.C.B. проводил опыты; B.G.M.C.C., A.P. и J.A.N.M. проанализировал данные и написал рукопись.
Автор, ответственный за переписку
Переписка с Бруно Густаво Муцци Карвалью Карнейро.
Заявление об этике
Конкурирующие интересы
Авторы не заявляют об отсутствии конкурирующих интересов.
Дополнительная информация
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Права и разрешения
Открытый доступ Эта статья находится под лицензией Creative Commons Attribution 4.0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или в любом формате при условии, что вы укажете первоначальных авторов и источник, ссылку на лицензию Creative Commons и указать, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons на статью, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/.
Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons на статью, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/.
Перепечатки и разрешения
Об этой статье
Исследование выявило связь между аллергией и повышенным риском рака крови у женщин
СИЭТЛ – 21 ноября 2013 г. обнаружили связь между наличием в анамнезе воздушно-капельных аллергий, в частности, на растения, траву и деревья, и риском развития рака крови у женщин.
Примечательно, что исследование не обнаружило такой же связи у мужчин, что предполагает возможную гендерно-специфическую роль в хронической стимуляции иммунной системы, которая может привести к развитию гематологического рака. Результаты опубликованы в Интернете в преддверии декабрьского печатного номера Американского журнала гематологии.
Результаты опубликованы в Интернете в преддверии декабрьского печатного номера Американского журнала гематологии.
«Насколько нам известно, наше исследование является первым, которое выявило важные гендерные различия в связи между аллергией и гематологическими злокачественными новообразованиями», — написал первый автор Мазьяр Шадман, доктор медицины, магистр здравоохранения, старший научный сотрудник отдела клинических исследований Фреда. Онкологический исследовательский центр Хатчинсона.
По словам Шадмана, руководившего исследованием, потенциальная роль иммунной системы в возникновении рака является предметом пристального научного интереса. «Если ваша иммунная система чрезмерно реактивна, у вас проблемы; если он недостаточно реактивен, у вас будут проблемы. Все больше данных указывает на то, что нарушение регуляции иммунной системы, такое как при аллергических и аутоиммунных заболеваниях, может повлиять на выживаемость клеток в развивающихся опухолях».
Для исследования Шадман, главный исследователь Эмили Уайт, доктор философии, из отдела наук о здравоохранении Фреда Хатча, и их коллеги использовали большую популяционную выборку мужчин и женщин из VITamins And Lifestyle (VITAL). ), в которую вошли люди в возрасте 50-76 лет из западного штата Вашингтон. Участники исследования ответили на 24-страничную анкету, в которой основное внимание уделялось трем основным областям: истории болезни и факторам риска рака, использованию лекарств и пищевых добавок, а также диете. Участники предоставили информацию о возрасте, расе / этнической принадлежности, образовании, курении, диете (употребление фруктов и овощей) и других характеристиках образа жизни, самооценке здоровья, истории болезни и семейной истории лейкемии или лимфомы.
), в которую вошли люди в возрасте 50-76 лет из западного штата Вашингтон. Участники исследования ответили на 24-страничную анкету, в которой основное внимание уделялось трем основным областям: истории болезни и факторам риска рака, использованию лекарств и пищевых добавок, а также диете. Участники предоставили информацию о возрасте, расе / этнической принадлежности, образовании, курении, диете (употребление фруктов и овощей) и других характеристиках образа жизни, самооценке здоровья, истории болезни и семейной истории лейкемии или лимфомы.
Также был взят анамнез на астму и аллергии, включая аллергии на растения, травы или деревья; плесень или пыль; кошки, собаки или другие животные; укусы или укусы насекомых; продукты питания; и лекарства.
Из 79 300 участников VITAL, заполнивших анкеты, было отобрано более 66 000 человек после исключения тех, у кого в анамнезе были злокачественные новообразования, отличные от немеланомного рака кожи, и отсутствовала информация об исходном анамнезе рака.
Участники наблюдались в среднем в течение восьми лет, пока они не выбыли из исследования, не уехали, у них не диагностировали рак, отличный от гематологического злокачественного новообразования или немеланомного рака кожи, или они не умерли. Заболеваемость гематологическими злокачественными новообразованиями и другими видами рака была выявлена с помощью онкологического регистра наблюдения, эпидемиологии и конечных результатов (SEER) западного штата Вашингтон.
Из участников 681 развили гематологическое злокачественное новообразование в течение периода наблюдения. Эти участники чаще были мужчинами, имели двух или более родственников первой степени родства с семейным анамнезом лейкемии или лимфомы, были менее активными и оценивали свое состояние здоровья как низкое. Наличие в анамнезе аллергии на переносимые по воздуху антигены было связано с более высоким риском гематологических злокачественных новообразований. Наиболее статистически значимая связь наблюдалась с аллергией на растения, траву и деревья.
Кроме того, в исследовании изучались связи между различными подтипами аллергии и гематологическими злокачественными новообразованиями и было обнаружено, что наличие в анамнезе аллергии на растения, траву и деревья в значительной степени связано со зрелыми В-клеточными новообразованиями, одной из четырех основных категорий лимфомы. Также был повышен риск новообразований плазматических клеток у участников, у которых в анамнезе была аллергия на кошек, собак или других животных. Плазмоклеточные новообразования — это состояния, как раковые, так и нераковые, при которых организм вырабатывает слишком много плазматических клеток.
При стратификации по полу заболеваемость раком крови в ответ на эти аллергены повышалась у женщин, но не у мужчин. Причина этого пока неизвестна.
«Заманчиво предположить, что дополнительный эффект аллергии может достигать статистической значимости у женщин из-за их более низкого исходного риска развития гематологических злокачественных новообразований по сравнению с мужчинами», — пишут авторы. «Однако гормональные эффекты на иммунную систему и взаимодействие с канцерогенезом могут предложить альтернативное биологическое объяснение, которое потребует дальнейших механических исследований, в частности, если наши результаты будут воспроизведены в независимой исследовательской группе».
«Однако гормональные эффекты на иммунную систему и взаимодействие с канцерогенезом могут предложить альтернативное биологическое объяснение, которое потребует дальнейших механических исследований, в частности, если наши результаты будут воспроизведены в независимой исследовательской группе».
При анализе данных учитывались потенциальные смешанные факторы, такие как пол, раса/этническая принадлежность, образование, история курения, потребление овощей и фруктов, уровень физической активности, семейный анамнез лейкемии/лимфомы и самооценка состояния здоровья. Типы лекарств от аллергии, используемые участниками, не контролировались. «Трудно исключить лечение аллергии как помеху, потому что почти все с аллергией принимают какие-то лекарства. Но ни одно из лекарств от аллергии, как известно, не вызывает рак», — сказал Шадман.
Авторы ссылаются на сильные стороны исследования, такие как большой размер популяции, исчерпывающие исходные данные о риске рака и заболеваниях, его перспективный дизайн и использование реестра SEER, отмеченной наградами программы регистрации рака, основанной на Fred Hutch. Между тем авторы признают ограничения исследования, а именно зависимость от самоотчетов об аллергии, ограничение получения ответов только о текущих аллергиях и, в частности, ограниченное количество гематологических раковых заболеваний для каждого подмножества типов аллергии.
Между тем авторы признают ограничения исследования, а именно зависимость от самоотчетов об аллергии, ограничение получения ответов только о текущих аллергиях и, в частности, ограниченное количество гематологических раковых заболеваний для каждого подмножества типов аллергии.
«Учитывая ограниченное количество случаев внутри каждого подтипа гематологического рака, оценки риска необходимо интерпретировать с осторожностью… и следует учитывать возможность случайного обнаружения в результате множественного тестирования», — написали Шадман и его коллеги.
Гранты Национального института рака и Национальных институтов здравоохранения финансировали исследование.
Примечание для СМИ: Чтобы получить копию статьи Американского журнала гематологии «Связь между аллергией и риском гематологических злокачественных новообразований: результаты когортного исследования витаминов и образа жизни», пожалуйста, свяжитесь с Кристен Вудворд по телефону 206-667-2210. или media@fredhutch.



 Am J Эпидемиол. 2003.
PMID: 12672680
Am J Эпидемиол. 2003.
PMID: 12672680 ; 131 (11): 2650-9. doi: 10.1002/ijc.27522. Epub 2012 2 апр.
Инт Джей Рак. 2012.
PMID: 22396152
; 131 (11): 2650-9. doi: 10.1002/ijc.27522. Epub 2012 2 апр.
Инт Джей Рак. 2012.
PMID: 22396152
 Природа 484 (7395), 465–472 (2012).
Природа 484 (7395), 465–472 (2012). J. Аллергическая клиника. Иммунол. 140 (4), 982–984 (2017).
J. Аллергическая клиника. Иммунол. 140 (4), 982–984 (2017). Риск немеланомного рака кожи у пациентов с атопическим дерматитом, принимающих пероральные иммунодепрессанты. Акта Дерм. Венереол. 97 (6), 724–730 (2017).
Риск немеланомного рака кожи у пациентов с атопическим дерматитом, принимающих пероральные иммунодепрессанты. Акта Дерм. Венереол. 97 (6), 724–730 (2017). Рак Эпидемиол. Биомарк. Пред. 25 (2), 282–290 (2016).
Рак Эпидемиол. Биомарк. Пред. 25 (2), 282–290 (2016). Р. Лечение рака, аллергии и иммуномедиадоров. Revista Médica de Minas Gerais. 27 (e-1877), 1–6 (2017).
Р. Лечение рака, аллергии и иммуномедиадоров. Revista Médica de Minas Gerais. 27 (e-1877), 1–6 (2017).
 М. и Шер А. Функциональное разнообразие хелперных Т-лимфоцитов. Природа 383 (6603), 787–793 (1996).
М. и Шер А. Функциональное разнообразие хелперных Т-лимфоцитов. Природа 383 (6603), 787–793 (1996).