Восстановление микрофлоры после антибиотиков: Микробиота после антибиотиков: как восстановить здоровье кишечника
Как восстановить микрофлору после антибиотиков
Светлана Белицкая
медицинский журналист
Профиль автора
Этот вопрос ученые решают уже много лет.
Антибиотики используют для лечения различных инфекционных заболеваний, и принимать их нужно только по рекомендации врача. При этом одни специалисты говорят, что вместе с курсом антибактериальных препаратов обязательно нужно принимать пробиотики, чтобы уберечь кишечник. Другие эксперты считают, что организм сам справится с последствиями лечения — помогать ему не нужно.
Правда в том, что антибиотики действительно могут нанести вред кишечному микробиому. Но в большинстве случаев он быстро возвращается в норму самостоятельно. Пока нет убедительных доказательств, что пробиотики эффективны при лечении диареи, спровоцированной антибиотиками, или могут ее предотвратить. Но при желании можно использовать препараты с бактериями Lactobacillus rhamnosus GG и Saccharomyces boulardii.
Сходите к врачу
Наши статьи написаны с любовью к доказательной медицине. Мы ссылаемся на авторитетные источники и ходим за комментариями к докторам с хорошей репутацией. Но помните: ответственность за ваше здоровье лежит на вас и на лечащем враче. Мы не выписываем рецептов, мы даем рекомендации. Полагаться на нашу точку зрения или нет — решать вам.
Мы ссылаемся на авторитетные источники и ходим за комментариями к докторам с хорошей репутацией. Но помните: ответственность за ваше здоровье лежит на вас и на лечащем враче. Мы не выписываем рецептов, мы даем рекомендации. Полагаться на нашу точку зрения или нет — решать вам.
Как возникла идея, что микрофлору надо восстанавливать после антибиотиков
Микробиотой, микробиомом или микрофлорой называют все микроорганизмы, которые живут на поверхности и внутри организма человека: бактерии, вирусы, простейшие и так далее. То, что внутри организма обитают микроорганизмы, обнаружил натуралист Антони ван Левенгук в конце 17 века. Он поместил образец собственного зубного налета под микроскоп, обнаружил в нем бактерии и дал им определение «анималькули» — «маленькие зверушки». А сам термин «микробиота» появился в начале 20 века, когда ученые поняли, что микробы играют большую роль в работе организма.
Микроскопические создания живут на коже, в ротовой полости, дыхательной и половой системе — везде. Но больше всего их в ЖКТ — там насчитывается более 3000 разных видов бактерий и других микроорганизмов. Вот какие функции они выполняют.
Но больше всего их в ЖКТ — там насчитывается более 3000 разных видов бактерий и других микроорганизмов. Вот какие функции они выполняют.
Человеческий микробиом — Обзоры питания
Пищеварительная. Если какие-то белки, жиры и углеводы не расщепились в тонкой кишке, кишечные микроорганизмы подвергают их ферментативному расщеплению. При этом некоторые вещества могут метаболизироваться только кишечной микрофлорой, потому что организм не вырабатывает нужные для этого ферменты.
Физиологическое значение кишечной микрофлоры — Consilium MedicumPDF, 304 КБ
Метаболическая. Кишечная микрофлора участвует в синтезе витаминов группы В и витамина К. Последний отвечает за доставку кальция и свертываемость крови. Он также участвует в обмене веществ в костной и соединительной тканях.
Микробиота кишечника как отдельная система организма — журнал «Доказательная гастроэнтерология»
Защитная. Кишечные бактерии могут синтезировать антибактериальные вещества бактериоцины, защищающие организм от заселения патогенными микроорганизмами. Например, короткоцепочечные жирные кислоты, в частности масляная кислота, оказывают противовоспалительный эффект на слизистую оболочку кишечника и снижают проницаемость кишечной стенки для чужеродных вредных микроорганизмов.
Например, короткоцепочечные жирные кислоты, в частности масляная кислота, оказывают противовоспалительный эффект на слизистую оболочку кишечника и снижают проницаемость кишечной стенки для чужеродных вредных микроорганизмов.
Предполагается, что изменения микрофлоры, которые по разным причинам происходят в течение жизни человека, могут быть вовлечены в развитие некоторых неинфекционных заболеваний, например неалкогольной жировой болезни печени.
Микробиота в здоровье и болезнях — журнал Nature
Считается, что раз антибиотики уничтожают бактерии без разбора, они могут стать причиной многих заболеваний, от которых спасает здоровый микробиом. Восстанавливать микробиом предлагают пробиотиками — препаратами с живыми полезными микроорганизмами. Например, с лакто- и бифидобактериями. Это красивая и стройная гипотеза, но у нее мало клинических доказательств.
Дело в том, что большинство обитателей микробиоты живут в кишечнике десятилетиями. Их численность меняется со временем, но в целом микробиом взрослого здорового человека довольно стабилен и может самостоятельно восстанавливаться — например, после болезни или приема лекарств. А различий состава микрофлоры у разных людей намного больше, чем ее изменений в течение жизни одного человека, в том числе после приема антибиотиков.
А различий состава микрофлоры у разных людей намного больше, чем ее изменений в течение жизни одного человека, в том числе после приема антибиотиков.
Устойчивость микробиоты кишечника — журнал Nature
К каким последствиям на самом деле могут приводить антибиотики
Сбой в работе кишечной микрофлоры из-за антибиотиков связывают с ожирением, диабетом, гипертонией и неинфекционными воспалительными заболеваниями кишечника. Но большинство исследований риска развития этих состояний на фоне приема антибиотиков проводились только на животных. Для людей достоверно установлен один побочный эффект антибиотиков, связанный с работой микробиоты, — диарея.
Антибиотик-ассоциированная диарея. Это диарея, которая возникает в связи с приемом антибиотиков и не имеет других причин. Она начинается либо прямо во время лечения, либо в течение восьми недель после окончания курса.
Диарея, связанная с антибиотиками — клиника Майо
Основной симптом диареи из-за антибиотиков — жидкий водянистый стул три или более раза в день. Расстройство обычно протекает в легкой форме и проходит в течение нескольких дней без лечения.
Расстройство обычно протекает в легкой форме и проходит в течение нескольких дней без лечения.
По разным оценкам от антибиотик-ассоциированной диареи страдают от 17,5 до 39% пациентов, принимающих антибиотики вне больницы. Это может быть побочный эффект самого препарата, но не обязательно. Антибиотики меняют состав бактериальной флоры кишечника, и это может приводить к нарушению метаболизма углеводов и желчных кислот.
Большинство углеводов всасывается в тонкой кишке, но некоторые из них ферментируются бактериями и превращаются в короткоцепочечные жирные кислоты. А когда антибиотик убивает бактерии, в кишечнике остается избыточное количество неиспользованных углеводов. Они притягивают к себе воду и разжижают стул — возникает осмотическая диарея. По мере того как микробиота самостоятельно восстанавливается, усвоение углеводов нормализуется.
Влияние антибиотиков на некротизирующий энтероколит и антибиотик-ассоциированную диарею — Europe PMCPDF, 246 КБ
Диарея после антибиотиков может возникнуть у любого человека, но риск выше у тех, кто:
- Ранее уже страдал от этого осложнения антибактериального лечения.

- Принимает антибиотики длительное время — больше одного курса.
- Лечится сразу несколькими антибактериальными препаратами.
Инфекция. Clostridium difficile — бактерия, выделяющая токсины. Она может не вызывать никаких симптомов, но иногда приводит к развитию псевдомембранозного колита — воспалительного заболевания толстой кишки.
Колит, вызванный Clostridioides (ранее Clostridium) difficile — справочник MSD
Как мы уже выяснили, антибиотики влияют на метаболическую функцию микрофлоры. В результате запускается цепная реакция: угнетение нормальной микробиоты снижает защитные способности бактерий, поэтому потенциально патогенные микроорганизмы получают карт-бланш. В этом случае увеличивается риск развития не осмотической диареи, а уже инфекционной, в том числе — из-за Clostridium difficile.
Вот главные признаки заражения инфекцией:
- диарея три и более раза в день, в тяжелых случаях — до 15 раз в день;
- боли и спазмы внизу живота;
- температура тела выше 38,3 °C;
- тошнота;
- обезвоживание;
- кровь или гной в стуле;
- потеря аппетита и снижение веса.

Инфекция Clostridioides difficile — клиника Майо
Симптомы инфекции бывают разной степени тяжести, они могут возникнуть во время антибактериальной терапии или через 5—10 дней после прекращения лечения, реже — через 10 недель после курса антибиотиков.
Антибиотик-ассоциированная диарея, вызванная Clostridioides difficile — Uptodate
В домашних условиях это осложнение возникает очень редко. Чаще с ним сталкиваются пациенты в стационаре, потому что C. difficile могут быть заражены прикроватные тумбочки, дверные ручки, раковины и другие предметы в больницах. Несоблюдение больными и медицинским персоналом правил гигиены повышает риск заражения.
При подозрении на инфекцию C. difficile назначают анализы. Если диагноз подтверждается, для лечения используют, как ни парадоксально, антибиотики ванкомицин или метронидазол.
Инфекция Clostridioides difficile иногда переходит в хроническую форму. В этом случае ее не удается полностью искоренить, поэтому выполняют восстановление микробиоты. Но не пробиотиками, а при помощи фекальной трансплантации.
Но не пробиотиками, а при помощи фекальной трансплантации.
Фекальная трансплантация — Университет Джона Хопкинса
Донорами здоровой микробиоты обычно выступают супруги, родители, братья и сестры, взрослые дети пожилых пациентов. Врачи берут у донора свежий образец стула, смешивают его с солевым раствором, пропускают полученную смесь через специальный фильтр и вводят в кишечник пациента при помощи колоноскопии или клизмы.
Какие антибиотики чаще всего вызывают диарею
Почти все антибиотики могут вызывать антибиотик-ассоциированную диарею. Чаще к осложнению приводят препараты из следующих групп:
- Макролиды, например кларитромицин.
- Цефалоспорины — цефдинир, цефподоксим.
- Фторхинолоны — ципрофлоксацин, левофлоксацин.
- Пенициллины — амоксициллин, ампициллин.
Чем более широкий спектр действия имеет антибиотик, тем выше вероятность, что его прием вызовет диарею.
/list/antibiotics-myths/
Как можно и нельзя принимать антибиотики: разбираем 9 мифов
Что говорят врачи и ученые о пользе пробиотиков
Некоторые клинические испытания показывают, что пробиотики действительно помогают при профилактике и лечении антибиотик-ассоциированной диареи. Но часто авторы этих исследований допускают серьезные методологические ошибки:
Но часто авторы этих исследований допускают серьезные методологические ошибки:
- В разных работах используют разные штаммы бактерий и в разной дозировке. Некоторые штаммы не задокументированы.
- Многие работы выполнены на госпитальных пациентах, но результаты таких экспериментов могут быть неактуальны для людей, которые лечатся дома. В стационарных и амбулаторных условиях врачи используют разные виды и дозировки антибиотиков.
- В некоторых работах нет группы контроля, вместо пробиотика принимающей плацебо.
- Нет исследований, которые отслеживали бы влияние антибиотиков и пробиотиков на представителей разных национальностей и жителей разных регионов, хотя доподлинно известно, что состав микробиоты зависит от пола, этнической принадлежности и места проживания.
Поэтому на основе результатов этих исследований нельзя сделать окончательный вывод о том, нужно ли использовать пробиотики для восстановления микрофлоры.
Например, ученые Университета Копенгагена провели систематический обзор и метаанализ исследований эффективности пробиотиков при диарее после курса антибиотиков и пришли к выводу, что пробиотики могут почти в два раза снижать частоту возникновения поноса. Но даже сами авторы обзора указывают, что полученным данным нельзя доверять полностью из-за высокого риска систематических ошибок.
Но даже сами авторы обзора указывают, что полученным данным нельзя доверять полностью из-за высокого риска систематических ошибок.
Метаанализ применения пробиотиков для профилактики диареи после антибиотиков — MDPI
В частности, два исследования, которые отслеживали влияние пробиотиков на состав микробиоты, показали разные результаты. В одном эксперименте пробиотики никак не повлияли на состав микрофлоры после приема антибиотика, а в другом исследователи обнаружили, что благодаря пробиотикам микрофлора после антибактериальной терапии восстанавливается быстрее.
Мнение официальных медицинских организаций о том, нужно ли принимать пробиотики параллельно с антибактериальными препаратами, тоже разошлись.
Российская гастроэнтерологическая ассоциация, РГА, включает некоторые типы пробиотиков в клинические рекомендации по профилактике антибиотик-ассоциированной диареи. Той же позиции придерживаются эксперты Всемирной гастроэнтерологической организации — WGO.
Американские гастроэнтерологи считают, что давать советы по восстановлению микробиома пробиотиками рано: нужны дополнительные исследования. А Европейское общество клинической микробиологии и инфекций, ESCMID, не рекомендует использовать пробиотики для лечения и профилактики антибиотик-ассоциированной диареи.
А Европейское общество клинической микробиологии и инфекций, ESCMID, не рекомендует использовать пробиотики для лечения и профилактики антибиотик-ассоциированной диареи.
Клинические рекомендации по применению пробиотиков — РГАPDF, 6249 КБ
Пробиотики и пребиотики — WGOPDF, 922 КБ
Как восстановить работу кишечника после приема антибиотиков
Если нет подозрения на инфекцию Clostridioides difficile, никакого специфического лечения при диарее на фоне приема антибиотиков не нужно. Достаточно выполнять общие рекомендации:
- Пить больше жидкостей, главное — не кофе, крепкий чай, сладкие газированные напитки и алкоголь.
- На время отказаться от молочных продуктов, жирной и острой пищи, которая усложняет пищеварительный процесс.
Сообщество 14.11.22
Можно ли совмещать антибиотики и алкоголь?
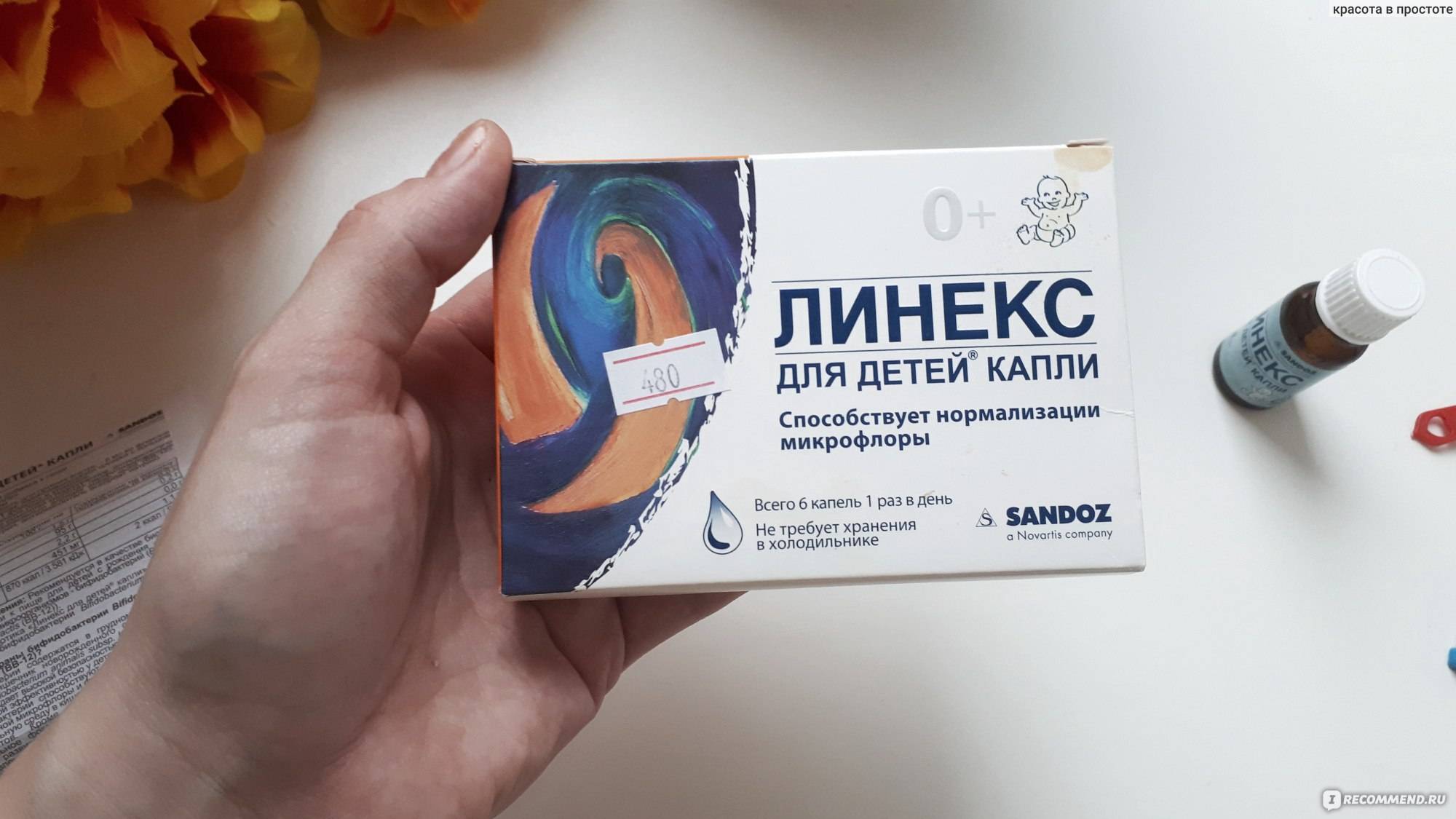
Если очень хочется, можно последовать рекомендациям Российской гастроэнтерологической ассоциации и принять пробиотики.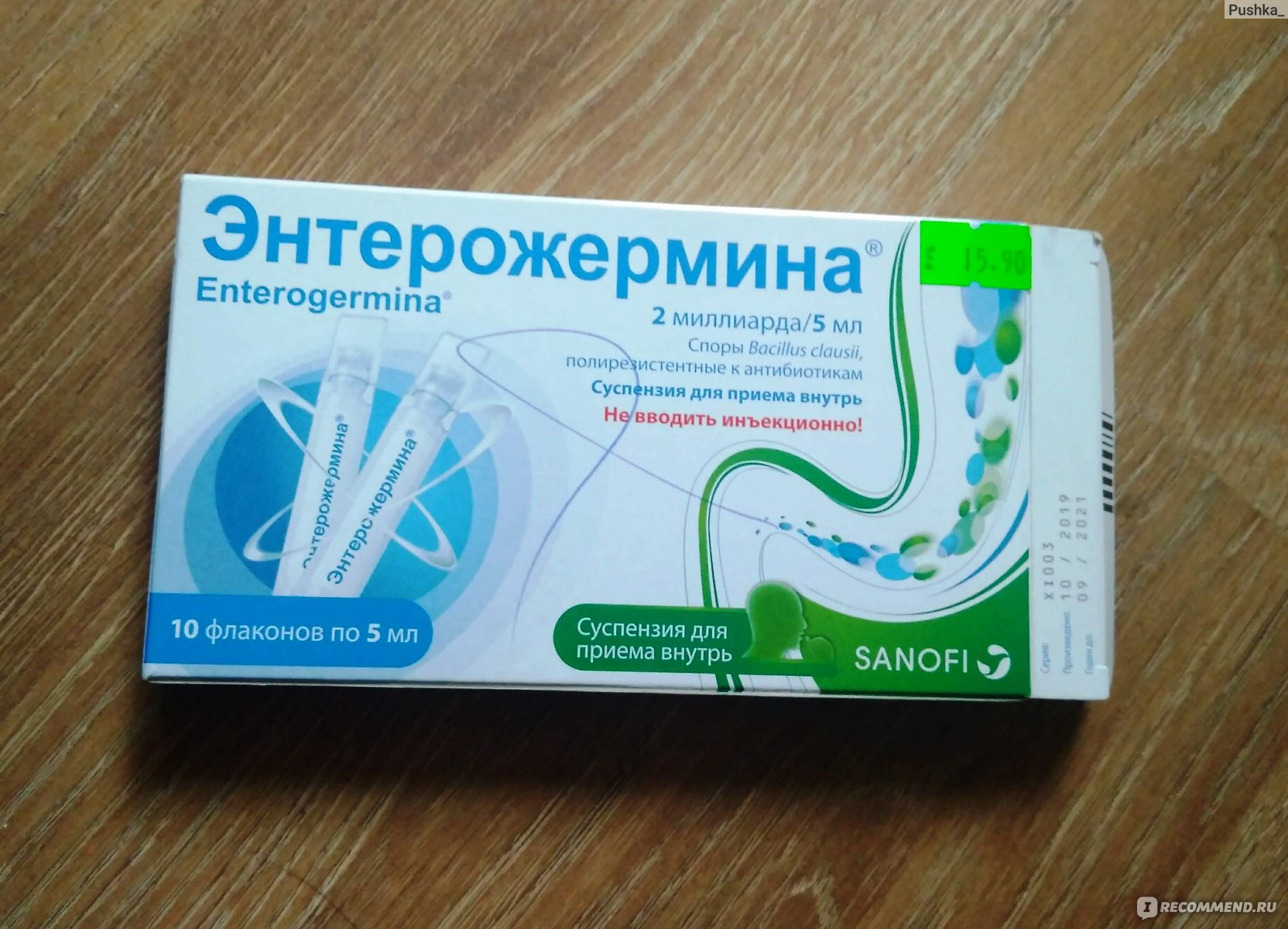 Сегодня научно доказана польза от бактерий Lactobacillus rhamnosus GG и Saccharomyces boulardii. Бактерии Lactobacillus rhamnosus GG содержатся в препаратах «Нормобакт L», «Комплинекс», а Saccharomyces boulardii — в «Энтероле».
Сегодня научно доказана польза от бактерий Lactobacillus rhamnosus GG и Saccharomyces boulardii. Бактерии Lactobacillus rhamnosus GG содержатся в препаратах «Нормобакт L», «Комплинекс», а Saccharomyces boulardii — в «Энтероле».
Влияние других микроорганизмов на профилактику и лечение антибиотик-ассоциированной диареи нужно дополнительно изучить. Абсолютно не доказана польза ферментированных продуктов с пробиотиками — например, кефира и йогурта.
«Нормобакт L» в порошке. Источник: eapteka.ru «Энтерол» в капсулах. Источник: eapteka.ruНовости о здоровье, интервью с врачами и инструкции для пациентов — в нашем телеграм-канале. Подписывайтесь, чтобы быть в курсе происходящего: @t_zdorov.
Восстановление микрофлоры после цистита
Восстановление микрофлоры после цистита
ЧТО ТАКОЕ ЦИСТИТ
Цистит — это инфекционно-воспалительный процесс, который локализуется в слизистой стенки мочевого пузыря. Ежегодно в России регистрируют до 36 миллионов случаев цистита. Женщины болеют циститом чаще, чем мужчины, из-за особенностей строения мочевыводящих путей. По статистике, обычно цистит развивается в возрасте 25–30 лет, а также у женщин в менопаузе (старше 55 лет). У каждой третьей женщины в течение года возникает рецидив заболевания, а у 10% оно переходит в хроническую рецидивирующую форму.
Ежегодно в России регистрируют до 36 миллионов случаев цистита. Женщины болеют циститом чаще, чем мужчины, из-за особенностей строения мочевыводящих путей. По статистике, обычно цистит развивается в возрасте 25–30 лет, а также у женщин в менопаузе (старше 55 лет). У каждой третьей женщины в течение года возникает рецидив заболевания, а у 10% оно переходит в хроническую рецидивирующую форму.
БАКТЕРИАЛЬНЫЙ ЦИСТИТ
В большинстве случаев бактериальный цистит вызывает уропатогенная бактерия — кишечная палочка, или Escherichia coli. Она входит в состав нормальной микрофлоры кишечника, но в определенных условиях (при переохлаждении, несоблюдении личной гигиены, частых простудных заболеваниях) большое количество этих бактерий скапливается на слизистой мочевого пузыря. У кишечной палочки есть специальное приспособление — фимбрии, помогающие бактерии проникать в клетки слизистой оболочки. Если местный иммунитет снижен и защитный слой эпителия мочевого пузыря нарушен, бактериям еще легче проникнуть внутрь клетки и вызвать воспаление.
ЛЕЧЕНИЕ БАКТЕРИАЛЬНОГО ЦИСТИТА
Всем пациентам с бактериальным циститом показано лечение антибиотиками.
Однако у такого лечения есть ряд недостатков:
может развиться резистентность, то есть невосприимчивость микроорганизма к антибиотикам;
антибиотики негативно влияют на микрофлору, что приводит к уничтожению полезных бактерий, снижению выработки витаминов, ослабеванию иммунитета.
ВОССТАНОВЛЕНИЕ МИКРОФЛОРЫ
Препараты на основе природных веществ, например, D-маннозы и экстракта клюквы, хорошо зарекомендовали себя для профилактики рецидива бактериального цистита и мобилизации защитных сил организма. Преимущество таких препаратов в том, что они не оказывают негативного влияния на микрофлору, в отличие от антибиотиков.
Восстановить слизистую мочевого пузыря поможет биологически активная добавка УРОЛАЙФ НЕКСТ, которая содержит лактобактерии, D-маннозу, экстракт клюквы, гиалуроновую кислоту и витамины:
Lactobacillus casei et rhamnosus препятствуют размножению Esherichia coli;
D-манноза связывает фимбрии Esherichia coli
экстракт клюквы усиливает действие D-маннозы и предотвращает обострение бактериального цистита;
гиалуроновая кислота входит в состав защитного слоя слизистой мочевого пузыря;
витамины С и D3 улучшают местный и системный иммунитет и создают неблагоприятные условия для жизни бактерий.
Такое сочетание компонентов наиболее эффективно для профилактики рецидивов хронического бактериального цистита: оно укрепляет иммунитет без негативного влияния на микрофлору.
ПРОФИЛАКТИКА ЦИСТИТА
Для профилактики цистита рекомендуется:
избегать переохлаждений;
соблюдать личную гигиену;
при наличии сопутствующих заболеваний строго следовать рекомендациям врача.
БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА, НЕ ЯВЛЯЕТСЯ ЛЕКАРСТВЕННЫМ СРЕДСТВОМ
Состав кишечных бактерий почти восстанавливается после антибиотиков — ScienceDaily
Новости науки
от исследовательских организаций
- Дата:
- 23 октября 2018 г.
- Источник:
- Университет Копенгагена Факультет здравоохранения и медицинских наук
- Резюме:
- Использование антибиотиков уже давно связывают с лишением кишечных бактерий.
 Теперь новое исследование показывает, что состав и функция кишечных бактерий могут восстанавливаться после лечения антибиотиками у здоровых людей. Но через шесть месяцев в кишечнике по-прежнему не хватает девяти распространенных видов полезных бактерий.
Теперь новое исследование показывает, что состав и функция кишечных бактерий могут восстанавливаться после лечения антибиотиками у здоровых людей. Но через шесть месяцев в кишечнике по-прежнему не хватает девяти распространенных видов полезных бактерий. Фейсбук Твиттер Пинтерест LinkedIN Электронная почта
ПОЛНАЯ ИСТОРИЯ
Триллионы бактерий в кишечнике человека влияют на наше здоровье различными способами, включая влияние на иммунные функции и обмен веществ. Считается, что богатая и разнообразная кишечная микробиота способствует укреплению здоровья, предоставляя человеку множество возможностей для предотвращения хронических заболеваний. Напротив, низкое разнообразие кишечной экосистемы является характерной чертой хронических заболеваний, включая ожирение, диабет, астму и воспалительные заболевания кишечника.
реклама
Из-за того, что антибиотики убивают бактерии, было высказано предположение, что повторное использование антибиотиков лишает людей богатой бактериальной средой кишечника и тем самым приводит к неблагоприятным последствиям для здоровья.
Международная группа исследователей под руководством Копенгагенского университета и Диабетического центра Стено в Копенгагене сообщает, что введение 3 антибиотиков молодым здоровым мужчинам в течение 4 дней привело к почти полному уничтожению кишечных бактерий с последующим постепенным восстановлением большинства видов бактерий в течение шести месяцев.
Однако по прошествии шести месяцев участники исследования по-прежнему отсутствовали девять из их обычных полезных бактерий, а несколько новых потенциально нежелательных бактерий колонизировали кишечник. Результаты опубликованы сегодня в Nature Microbiology .
«Мы показываем, что кишечные бактериальные сообщества здоровых взрослых устойчивы и способны восстанавливаться после кратковременного одновременного воздействия трех разных антибиотиков. Антибиотики могут быть благословением для сохранения здоровья человека, но их следует использовать только на основании четких доказательств бактериальной причины инфекции», — объясняет руководитель исследования профессор Олуф Педерсен из Центра фундаментальных исследований обмена веществ при Фонде Ново Нордиск.
Отсутствие полезных кишечных микробов в западном мире связано с чрезмерным использованием антибиотиков?
Исследование представляет собой четырехдневное вмешательство с тремя антибиотиками широкого спектра так называемого «крайнего средства» у 12 взрослых здоровых мужчин. Метод с коктейлем из трех антибиотиков был разработан, чтобы имитировать реальное лечение в отделениях интенсивной терапии.
Кишечник является резервуаром сотен различных видов бактерий с генами устойчивости к антибиотикам. Это было подтверждено в исследовании, поскольку эти бактериальные гены были инициирующей силой, которая привела к пополнению бактерий в кишечнике.
«В этом случае хорошо, что мы можем регенерировать микробиоту кишечника, которая важна для нашего общего здоровья. Однако проблема связана с потенциально безвозвратной потерей полезных бактерий после многократного воздействия антибиотиков в течение нашей жизни. доказательства того, что западное население имеет значительно более низкое разнообразие кишечной микробиоты, чем коренные жители, живущие в определенных частях Африки и Амазонии.
реклама
История Источник:
Материалы предоставлены Университет Копенгагена Факультет здравоохранения и медицинских наук . Примечание. Содержимое можно редактировать по стилю и длине.
Ссылка на журнал
- Альберт Пальеха, Кристиан Х. Миккельсен, София К. Форслунд, Алиреза Кашани, Кристин Х. Аллин, Трине Нильсен, Ту Х. Хансен, Суйша Лян, Цян Фэн, Ченчен Чжан, Пол Теодор Пыль, Луис Педро Коэльо, Хуанмин Ян, Цзянь Ван, Афанасиос Типас, Мортен Ф. Нильсен, Хенрик Бьорн Нильсен, Пир Борк, Джун Ван, Тина Вилсбёлль, Торбен Хансен, Филип К. Кноп, Маниможиян Арумугам, Олуф Педерсен. Восстановление микробиоты кишечника здоровых взрослых после воздействия антибиотиков . Природная микробиология , 2018; 3 (11): 1255 DOI: 10.
 1038/s41564-018-0257-9
1038/s41564-018-0257-9
Цитировать эту страницу :
- MLA
- АПА
- Чикаго
Университет Копенгагена Факультет здравоохранения и медицинских наук. «Состав кишечных бактерий почти восстанавливается после антибиотиков». ScienceDaily. ScienceDaily, 23 октября 2018 г.
Университет Копенгагена Факультет здравоохранения и медицинских наук. (2018, 23 октября). Состав кишечных бактерий практически восстанавливается после антибиотиков. ScienceDaily . Получено 3 апреля 2023 г. с сайта www.sciencedaily.com/releases/2018/10/181023110545.htm
Копенгагенский университет, факультет здравоохранения и медицинских наук. «Состав кишечных бактерий почти восстанавливается после антибиотиков». ScienceDaily. www.sciencedaily.com/releases/2018/10/181023110545.htm (по состоянию на 3 апреля 2023 г. ).
).
Сколько времени требуется для восстановления полезных бактерий после антибиотиков?
Хотя антибиотики часто играют важную роль в преодолении болезней, они также могут негативно влиять на микрофлору кишечника. Антибиотики не отличают хорошее от плохого, поэтому во время курса антибиотиков множество хороших бактерий в нашем кишечнике теряется вместе с плохими, что может привести к множеству проблем.
Зачем мне восстанавливать хорошие бактерии после антибиотиков?
Исследования подтверждает, что антибиотики могут уничтожать полезные бактерии и вызывать повреждение микробиома кишечника. Хотя это менее вероятно после одного курса антибиотиков (хотя и возможно), повторные курсы в течение определенного периода времени без восстановления здоровых кишечных бактерий могут негативно повлиять на здоровье кишечника в долгосрочной перспективе.
Нарушение здоровья кишечника может привести к ослаблению иммунной системы, проблемам с пищеварением, повышенной пищевой аллергии и повышенной чувствительности и многому другому. Хорошая новость заключается в том, что есть несколько простых способов восстановить полезные бактерии после антибиотиков.
Хорошая новость заключается в том, что есть несколько простых способов восстановить полезные бактерии после антибиотиков.
Как восстановить полезные бактерии?
Ниже вы найдете несколько быстрых и простых советов по восстановлению хороших бактерий. Для получения дополнительной информации о лучших стратегиях восстановления кишечной флоры,
- Принимайте высококачественную пробиотическую добавку, содержащую не менее 50 миллиардов КОЕ (колониеобразующих единиц) на дозу.
- Включите в свой ежедневный рацион ферментированные продукты. Подумайте о сырой квашеной капусте, кимчи, простом йогурте (если вы переносите молочные продукты), несладком чайном грибе и кефире (без добавления сахара).
- Обязательно ешьте много овощей и фруктов, особенно богатых пребиотиками, так как они необходимы для питания пробиотических бактерий в кишечнике. Отличными источниками пребиотиков являются такие продукты, как бананы, бананы, чеснок, лук, топинамбур и листовая зелень.

Сколько времени требуется для восстановления полезных бактерий после антибиотиков?
Многие люди хотят точно знать, сколько времени требуется для восстановления хороших бактерий после курса антибиотиков. Хотя это может варьироваться от человека к человеку, общая рекомендация — один курс пробиотиков за каждую неделю, когда вы принимали антибиотик. Как правило, полный пакет пробиотиков — это целая бутылка, которой может хватить на 1-2 недели.
3 совета по ускорению восстановления полезных бактерий
- Принимайте пробиотики во время приема антибиотиков. Распространенным заблуждением является то, что пробиотики будут потрачены впустую, если принимать их вместе с антибиотиками, но прием пробиотиков во время приема антибиотиков может действительно помочь. Пробиотики могут снизить pH (уровень кислотности) толстой кишки, делая ее менее пригодной для вредных бактерий и более благоприятной для полезных бактерий. может затруднить прикрепление вредных бактерий к слизистой оболочке пищеварительного тракта.



 Теперь новое исследование показывает, что состав и функция кишечных бактерий могут восстанавливаться после лечения антибиотиками у здоровых людей. Но через шесть месяцев в кишечнике по-прежнему не хватает девяти распространенных видов полезных бактерий.
Теперь новое исследование показывает, что состав и функция кишечных бактерий могут восстанавливаться после лечения антибиотиками у здоровых людей. Но через шесть месяцев в кишечнике по-прежнему не хватает девяти распространенных видов полезных бактерий. 1038/s41564-018-0257-9
1038/s41564-018-0257-9
