Атрезии пищевода – Атрезия пищевода — причины, симптомы, диагностика и лечение
Атрезия пищевода с трахеально-пищеводным свищом (Q39.1)
Специфической профилактики не существует.
Раняя перинатальная диагностика играет определенную роль в увеличении выживаемости. Она минимизирует риски, связанные с первым кормлением, и повышает готовность к ранней операционной коррекции.
По данным большинства авторов, перинатальная эхографическая диагностика атрезии пищевода основывается только на следующих косвенных признаках:
1. Многоводие, связанное со снижением оборота околоплодных вод вследствие непроходимости пищевода.
2. Отсутствие эхографического изображения желудка или маленькие его размеры при динамическом ультразвуковом наблюдении.
М. Stringer и соавторы установили, что положительное прогностическое значение этих маркеров составляет только 56%. По данным В. Chodirker и соавторов, чувствительность эхографии в диагностике атрезии пищевода при комбинированном использовании эхографических признаков (многоводие, отсутствие эхотени желудка) составляет только 42%.
При атрезии пищевода достаточно редко отмечается отсутствие эхотени желудка, так как частое наличие трахеально-пищеводной фистулы (ТПФ) или ТПСТПС — трахеопищеводный свищ
при этом пороке затрудняет диагностику.
Обычно ТПC располагается дистальнее места атрезии пищевода, что позволяет амниотической жидкости попадать из трахеи в пищевод, а затем в желудок. Только при изолированной атрезии пищевода или при ТПC, расположенной проксимальнее места обструкции, обычно отсутствует эхотень желудка. Это позволяет заподозрить атрезию пищевода с большей вероятностью.
Следует помнить, что изображение желудка может отсутствовать не только при атрезии пищевода, но и при врожденной микрогастрии, лицевых расщелинах, VACTERL синдроме, дистрессе плода и маловодий.
Эхотень желудка может отсутствовать в момент проведения УЗИ и при абсолютной норме, при динамическом эхографическом наблюдении эхотень желудка обнаруживается в типичном месте.
Принято считать, что атрезия пищевода относится к трудно диагностируемым врожденным порокам. Однако некоторым исследователям удалось определить дааный порок в 80% случаев благодаря прямой оценке пищевода в случаях обнаружения многоводия и микрогастрии или при отсутствии эхотени желудка.
Одними из первых сообщили о перинатальной диагностике атрезии пищевода американские специалисты J. Estroff и соавторы. Диагноз был поставлен на основании визуализации периодически наполняющегося и опустошающегося слепо заканчивающегося проксимального отдела пищевода, являющегося, по их мнению, специфическим признаком атрезии пищевода. Опираясь на этот признак, они смогли диагностировать 3 случая атрезии пищевода во II триместре беременности. Ранее считалось, что диагностика атрезии пищевода возможна в некоторых случаях только в конце II и в III триместре беременности.
По мнению некоторых авторов, наиболее действенной схемой диагностики атрезии пищевода является прямая визуализация пищевода плода в случаях обнаружения необъяснимого многоводия и микрогастрии или отсутствия эхотени желудка.
diseases.medelement.com
АТРЕЗИЯ ПИЩЕВОДА У ДЕТЕЙ. ВАЖНЕЙШИЕ АСПЕКТЫ В ДИАГНОСТИКЕ И ЛЕЧЕНИИ
Среди многочисленных аномалий развития пищевода особый интерес представляет врожденная непроходимость пищевода, обусловленная его атрезией. Данная патология нередко является причиной гибели новорожденного ребенка, поскольку диагностика данного заболевания, без определенной базы знаний, представляет собой некоторые трудности. Без срочного оперативного вмешательства атрезия пищевода является непосредственной угрозой для жизни ребенка в первые дни жизни.
Исторический очерк. Впервые такая аномалия развития пищевода была описана Thomas Gibson в 1696 году. Он очень четко и дотошно изложил клиническую и патологоанатомическую картину порока. Из его работ по сей день имеет огромную ценность фраза: «кажется, что ребенок очень хочет есть и с жадностью хватает ртом все, что дают ему, но когда собирается проглотить, то пища как будто наталкивается на препятствие и не проходит внутрь, а возвращается через рот и нос, при этом ребенок впадает в состояние, подобное судорожному припадку» [1, с. 282].
Спустя почти 150 лет, Thomas Hill (1839 г.) описывает случай непроходимости пищевода у новорожденного ребенка, который умер в течении первых часов жизни. Впервые в 1888 году лондонский хирург Charles Stiles внедрил метод хирургической коррекции по восстановлению проходимости пищевода при его атрезии, разобщив трахеопищеводный свищ [8, с. 25].
На протяжении долгого времени диагностика и хирургическое лечение атрезии пищевода являлись казуистическими, а исследования часто ограничивались лишь описанием отдельных примеров успешного лечения. Лишь в 1939 году Leven и Ladd, вне зависимости друг от друга, получили единичные успешные случаи прооперированных детей с врожденной непроходимостью пищевода, а в 1941 году Haight и Towsley впервые успешно прооперировали ребенка с АП радикально. С тех пор количество сообщений о благоприятном исходе хирургического лечения порока постепенно увеличивалось (Hofmann, 1960; Sanderung, 1960; Richardson, 1963 и др.). Впервые в нашей стране успешное разобщение трахеопищеводного свища произвел И.М. Раков в 1949 году [8, с. 26]
Этиология и патогенез. В норме после 19-го дня гестации происходит отделение дорсальной части кишки (пищевод) от вентральной (трахея) в области карины, распространяясь в головном направлении. Прерывание разделения пищевода и трахеи при несоответствии скорости роста или по каким-либо другим причинам, к 32 дню гестации образуется порок развития пищевода с формированием трахеопищеводного свища [5, с. 192]. Из-за нарушения пассажа пищи по пищеводу антенатально не формируются координированные перистальтические движения пищевода, вследствие чего нарушается развитие глотательного рефлекса. По мнению Grunewald и ряда других авторов, причиной развития атрезии пищевода является первоначально сформировавшийся трахеопищеводный свищ [1, с. 283]. Перерастяжение желудка воздухом, обусловленное наличием прямого сообщения между трахеей и пищеводом в дистальном отделе, имеет наиболее важное значение, так как оно непременно ведет к развитию ателектазов в базальных отделах легких из-за ограниченного движения диафрагмы. Такое состояние в свою очередь может осложниться аспирацией желудочного содержимого и развитием аспирационной бактериальной пневмонии.
Классификация. Атрезия пищевода и трахеопищеводный свищ могут встречаться как изолированные пороки развития, но наиболее часто наблюдается комбинированная аномалия.
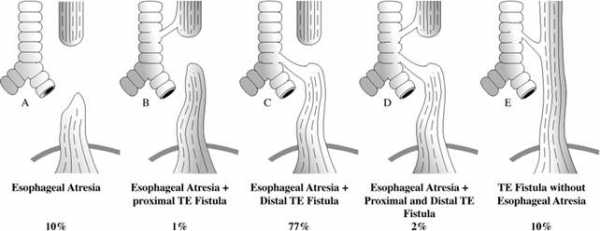
Рисунок 1. Виды атрезий пищевода [12, с. 818]
A) Изолированная атрезия пищевода (10 %) – характеризуется большим диастазом (> 1.5 см) между пищеводной трубкой и желудком, отсутствием трахеально-пищеводного свища;
B) Атрезия пищевода с проксимально расположенной трахеопищеводной фистулой (1%) – верхний сегмент пищевода образует трахеально-пищеводный свищ, а нижний заканчивается слепо;
C) Атрезия пищевода с дистально расположенной трахеопищеводной фистулой (77 %) – верхний сегмент пищевода заканчивается слепо, а нижний образует трахеально-пищеводный свищ;
D) Атрезия пищевода с проксимальной и дистальной трахеопищеводной фистулой (2 %) – верхний и нижний сегменты пищевода соединены с трахеей в двух отдельных местах;
E) Трахеопищеводный свищ без атрезии пищевода (10 %) – характеризуется наличием аномального соединения пищевода и трахеи, нарушения проходимости пищевода нет [7, с. 7-8].
Таким образом, можно выделить 3 основных формы порока:
— Атрезия пищевода без свища;
— Атрезия пищевода с трахеально-пищеводным свищем;
— Врожденный трахеально-пищеводный свищ без атрезии.
Клиническая картина и диагностика. Первый симптом, при котором врач должен насторожиться и предположить врожденную непроходимость пищевода, это обильное пенистое слюнотечение (симптом «мыльных пузырей») изо рта и носа, которое ребенок не может проглотить. К сожалению, даже в современном мире, в родильных домах не всегда придают должное внимание данному симптому. Если поставить диагноз до первого кормления ребенка, это значительно облегчит течение аспирационной пневмонии [3, с. 57]. Подозрение на атрезию пищевода должно усилиться, если при попытке отсасывания слизи последняя продолжает быстро накапливаться и выделяться изо рта и носа в большом количестве. При наличии трахеально-пищеводного свища аускультативно в легких выслушивается множество влажных разнокалиберных хрипов на различных уровнях. К концу 1-ого дня после рождения ребенка отчетливо выявляется характерная симптоматика нарушения дыхания (кашель, одышка, цианоз) [4, с. 51].
На сегодня наиболее достоверным признаком атрезии пищевода антенатально является дилатированный и гипертрофированный проксимальный сегмент пищевода при УЗ исследовании. Во время акта глотания околоплодной жидкости, который совершает эмбрион, визуализируется расширенный слепой мешковидный конец пищевода, который будет свидетельствовать о наличии порока.
После рождения диагноз уточняют при помощи катетеризации пищевода тонкой трубкой с атравматичным закругленным концом. Зонд вводят через нос на глубину 6-10 см. При атрезии пищевода дальнейшее введение зонда окажется невозможным. Не исключено заворачивание зонда и выход его конца через нос или рот. Проведение «пробы Элефанта» так же является необходимым для постановки диагноза. Для этого вводят катетер до упора в слепой конец пищевода и шприцем под давлением вводят воздух. При наличии атрезии он с шумом выходит из носоглотки.
У детей со свищевыми формами атрезии о длине диастаза между проксимальным и дистальным концами пищевода можно судить по боковой рентгенограмме. Использование для диагностики рентгенконтрастных веществ, в особенности бариевой смеси, крайне нежелательно из-за высокого риска развития аспирационной пневмонии. Некоторые хирурги считают, что бронхоскопия показана всем новорожденным с атрезией пищевода непосредственно на операционном столе перед хирургической коррекцией (для выявления проксимально расположенной трахеопищеводной фистулы и трахеомаляции).
Окончательный диагноз подтверждается рентгенологически. При введении рентгенконтрастного катетера до упора, на обзорной рентгенограмме будет отчетливо виден слепой расширенный мешковидный конец пищевода. Возможно обнаружение воздуха в желудке и кишечнике – это указывает на наличие дистально расположенного трахеопищеводного свища.
Стоит отметить, что немаловажным фактором является наличие почти у 60 % новорожденных детей с АП и ТПС сопутствующих аномалий развития, 6-10 % из которых носит генетический характер. Так, в 1973 году была описана ассоциация VACTERL+hydrocephalus (V = позвоночные аномалии, A = анальная атрезия, C = кардиальные пороки, T = трахеопищеводный свищ, E = атрезия пищевода, R = почечные аномалии, L = аномалии конечностей) [1, с. 285]. При наличии у ребенка одной из аномалий, входящих в данную ассоциацию, следует подозревать и искать другие пороки развития.
Лечение. Консервативное лечение исключено. Срочное хирургическое вмешательство должно проводиться в самые короткие сроки при стабильном кардиореспираторном статусе и нормализации диуреза. Длительность предоперационной подготовки может варьировать от нескольких часов до нескольких суток – в зависимости от степени выраженности аспирационной пневмонии. Новорожденным, масса тела которых менее 1500 гр., производят «нетипичную» многоэтапную операцию: отсроченный анастомоз с предварительной перевязкой трахеопищеводного свища [2, с. 22].
В настоящее время используется два способа хирургической коррекции атрезии пищевода: торакотомия (открытый способ) и торакоскопический.
Техника оперативного вмешательства при атрезии пищевода с трахеопищеводной фистулой сводится к следующим этапам:
- выделение и разобщение трахеопищеводной фистулы;
- мобилизация дистального и проксимального отделов пищевода;
- наложение первичного анастомоза (при диастазе <1.5 см)
При невозможности создания первичного анастомоза из-за наличия непреодолимого диастаза между дистальным и проксимальным отделами пищевода, операцию завершают разобщением и перевязкой ТПС и наложением гастростомы.
При «чистой» атрезии пищевода без ТПС со значительным диастазом оправдано выполнение этапной хирургической коррекции порока (наложением эзофаго- или гастростомы с последующим созданием отсроченного анастомоза).
При изолированном трахеопищеводном свище без атрезии пищевода операция заключается в мобилизации, перевязке и пересечении соустья. В зависимости от расположения фистулы операцию проводят правосторонним шейным доступом (при низком расположении ТПС), открытым или эндоскопическим способами.
На 6-7 сутки после оперативного вмешательства проводят рентгенологический контроль с водорастворимым контрастным веществом для исключения несостоятельности анастомоза. При благоприятном течении послеоперационного периода начинают кормление через рот и проводят терапию, направленную на лечение желудочно-пищеводного рефлюкса на 3-4 неделе. После оценивают функцию пищевода и диаметр анастомоза [6, с. 261].
Список литературы:
- Ашкрафт К. У., Холдер Т. М. Детская хирургия, том 1. – СПб., Хардфорд, 1996. – 384с.
- Бабляк Д. Е. Хирургическое лечение врожденной атрезии пищевода. Л., 1974. – 32с.
- Баиров Г. А. Срочная хирургия детей: руководство для врачей. – СПб.: Питер Пресс, 1997. – 464с.
- Биезинь А. П. Диагностика хирургических заболеваний органов грудной и брюшной полостей у детей, 1971. – 292с.
- Бычков В. А., Манжос П. И., Городова А. В. Основные вопросы хирургии детского возраста: Учебное пособие. – М.: из-во РУДН, 2011. – 329с.
- Исаков Ю. Ф., Дронов А. Ф. Детская хирургия: национальное руководство – М.: ГЭОТАР-Медиа, 2009. – 1168с.
- Клинические рекомендации. Атрезия пищевода у детей. // Российская ассоциация детских хирургов. 2016. – 36с.
- Новожилов В.А., Иванов В.О., Козлов Ю.А. и др. Использование эндоскопии для диагностики диастаза между отрезками пищевода при бессвищевой атрезии. // Современные проблемы педиатрии и детской хирургии: сб. науч. трудов. Иркутск, 2000. с. 161-164.
- Паршин В. Д., Русаков М. А., Паршин В. В. Хирургия трахеопищеводного свища под редакцией В. Д. Паршина. – М.: Альди-Принт, 2016. – 264с.
- Стручков В. И., Пугачев А. Г. М. Детская торакальная хирургия. «Медицина», 1975. – 560с.
- Bax N. M., Van der Zee, D.C. Thoracoscopic repair of esophageal atresia with distal fistula // Surg. Endosc. 2003. — Vol. 17, №7.-P. 1065-67.
- Dahnert, Wolfgang. Radiology Review Manual, 6th Edition, 2007. – 1135с.
- Levin, N.L. Congenital atresia of the esophagus with tracheoesophagea fistula / N.L. Levin // J. Thor. Cardiovasc. Surg. 1941. -Vol. 10.-P. 648-657.
- Pulmonary aspiration because of gastroesophageal reflux / B. Chernow et al. // Dig. Dis. Sci. 1979. — Vol. 24. — P. 839-844.
- Puri P., Hollwarth M.E. Pediatric Surgery. Springer, Berlin, Heidelberg, 2006. – P. 43-62.
- Two cases of congenital cardiac anomaly associated with esophageal atresia / Satoh Y. et al. // Japan J. Thorac. Surg. 1992. — Vol. 45, № 5. -P. 424-427.
- Usui, N. Anomalies of the tracheoobronchial tree in patients with esophageal atresia / N. Usui // J. Pediatr. Surg. 1996. — Vol. 31, № 2. — P. 258-263.
sibac.info
Атрезия пищевода
Атрезия пищевода — порок развития, при котором верхний и нижний сегменты пищевода разобщены за счет эмбриогенеза в раннем периоде, при этом один или оба сегмента (чаще нижний) могут иметь сообщение с трахеей.
Эпидемиология
Частота встречаемости составляет 1:3000-4000 новорожденных [4].
Патология
В основе патологии лежит нарушение дифференцировки первичной передней кишки в пищевод, трахею и легкие на 4й неделее эмбрионального развития.
Классификация Gross [1,4]
- Тип А
- изолированная («чистая») атрезия пищевода или атрезия пищевода с большим диастазом
- форма атрезии пищевода, которая характеризуется большим расстоянием между сегментами и отсутствием трахеопищеводной фистулы
- встречаемость 8%
- Тип В
- атрезия пищевода с проксимальной трахеопищеводной фистулой.
- верхний сегмент пищевода соединяется с трахеей, а нижний сегмент заканчивается слепо
- встречаемость 1%
- Тип С
- атрезия пищевода с дистальной трахеопищеводной фистулой
- нижний сегмент пищевода соединяется с трахеей, а верхний сегмент заканчивается слепо
- встречаемость 85%
- Тип D
- атрезия пищевода с проксимальной и дистальной трахеопищеводной фистулой.
- верхний и нижний сегмент пищевода соединяются с трахеей в двух отдельных местах
- встречаемость 1%
- Тип E
- трахеопищеводная фистула без атрезии пищевода, H –тип
- имеется аномальное соединение пищевода и трахеи, пищевод имеет нормальный просвет и хорошую функцию
- встречаемость 4%
Классификация Vogt [1]
- тип I
- агенезия, пищевод отсутствует практически полностью
- очень редкая аномалия пищевода
- не включенна в классификации Gross и Ladd
- тип II
- атрезия без фистулы трахеи
- встречаемость 7%
- тип III
- a: атрезия с фистулой между трахеей и проксимальним карманом пищевода, встречаемость 1%
- b: атрезия с фистулой между трахеей и дистальным карманом пищевода, встречаемость 87%
- c: атрезия с проксимальной и дистальной фистулами, встречаемость 2%
- тип IV — фистула пищевода, Н-образная фистула без атрезии, встречаемость 3%
Синдром VACTERL
Синдром VACTERL означает сочетание мальформаций
- V (vertebral — аномалии позвоночника)
- полупозвонок
- врожденный сколиоз
- каудальная регрессия
- spina bifida
- A (anorectal anomalies — пороки прямой кишки)
- атрезия ануса
- С (cardiac anomalies пороки сердца)
- дефект межпредсердной или межжелудочковой перегородки, аномалии дуги аорты
- ТЕ трахеоэзофагеальная фистула с или без атрезии пищевода
- R (renal) пороки развития почек
- L (limb) пороки развития конечностей
- полидактилия
- олигодактилия
Клиническая картина
- плод не заглатывает амниотическую жидкость, что приводит к развитию многоводия
- одышка и цианоз возникают при попадании секрета из проксимального кармана пищевода в трахею
- кашель, в особености во время кормления
- впалый живот при отсутствии дистальной фистулы, а вздутый живот при наличии дистальной фистулы
Диагностика
Рентгенография
Рентгенологическая картина зависит от типа атрезии. При отсутствии фистулы с дистальной частью пищевода газ в брюшной полости отсутствует. При наличии дистальной фистулы возникает патологический метеоризм. Дистальный карман пищевода может быть визуализирован при наличии рефлюкса из желудка. Дополнительными находками при рентгенографии могуть быть ателектаз, консолидации (пневмония) при аспирации, а также сопутствующие мальформации позвоночника и конечностей.
Скопия
Пищевод визуализируют при помощи водорастворимых контрастных веществ (около 0,5 мл), которые немедленно должны быть аспирированы сразу после проведения исследования. После аспирации секрета в проксимальную часть пищевода вводят 1-2 мл воздуха для визуализации расширенного, заполненного воздухом пищевода. Исследование может показать слепое окончание проксимального отдела пищевода и / или может указать на наличие о трахеоэзофагеальной фистулы. Скопия особенно полезна при демонстрации H-типа атрезии.
Антенатальное ультразвуковое исследование
- специфических признаков нет
- атрезия должна быть заподозрена при наличии любой VACTERL аномалии
- многоводие практически во всех случаях атрезии без фистулы
- задержка развития плода
- подтипы без трахео-эзофагеальной фистулы могут быть заподозрены по отсутствию визуализации желудка плода
Тактика
Лечение — хирургическое. Резекция фистулы с последующей реконструкцией пищевода (эзофагоколонопластика).
Осложнения
- аспирационная пневмония
- перфорация желудочным зондом
- стриктура пищевода
- нарушение сократимости пищевода
- гастроэзофагеальный рефлюкс
- рецидивирующая фистула
radiographia.info
Атрезия пищевода — Болезни детской хирургии
Атрезия пищевода — порок развития, при которой пищевод имеет вид двух мешкообразных образований, соединенных соответственно с глоткой и желудком.Распространенность атрезии пищевода
Атрезия пищевода встречается в популяции с частотой 3:10 000. Часто атрезия пищевода сочетается с другими пороками развития — врожденными пороками сердца, желудочно-кишечного тракта и т.д.Эмбриогенез атрезии пищевода
Пищевод и трахея возникают из одного зачатка — головного конца передней кишки.Разделение их происходит на 4-5-й неделе эмбриогенеза. При несоответствии направления и скорости роста пищевода и трахеи и возможно возникновение атрезии пищевода.Патогенез атрезии пищевода
Возможны следующие варианты атрезии пищевода:• Оба конца атрезированного пищевода слепые (а).
• Оральный конец пищевода сочетается с трахеей, абдоминальная конец — слепой (б).
• Оральный конец пищевода — слепой, абдоминальная конец открывается в трахею (в).
• Оральный и абдоминальная конце пищевода сочетаются с трахеей (г).
• Оба конца атрезированного пищевода слепые с большим диастазой между ними (д).
Клиника атрезии пищевода
Основным клиническим симптомом атрезии пищевода в первые часы после рождения ребенка являются пенистые выделения изо рта. После отсасывания содержимого ротоглотки они скоро появляются снова. При аспирации слизи у ребенка возникают приступы цианоза и удушья. В легких в следствии развития аспирационной пневмонии выслушиваются разнокалиберные хрипы.Диагностика атрезии пищевода
Диагностика атрезии пищевода у новорожденных начинается с родильного зала и основывается не только на клинической симптоматике, но и на диагностических приемах, к которым относятся:1. Катетеризация пищевода через нос тонким рентгеноконтрастных катетеров с закругленным концом. При атрезии пищевода — катетер, пройдя на глубину около 6 сантиметров, утыкается в слепой конец пищевода или, заворачиваясь, выходит через нос ребенка.
2. «Проба Элефанта» (англ. elephant — слон) — воздух, введенное через зонд в слепой конец пищевода, с шумом выходит из носа.
3. Обзорная рентгенография грудной клетки и органов брюшной полости:
а) бесконтрастная — при атрезии рентгеноконтрастный катетер отчетливо виден в слепом отрезке пищевода. Наличие воздуха в желудке и кишечнике указывает на свищ между трахеей и абдоминальным концом пищевода. При безсвищевыхевих формах — полное затмение брюшной полости;
b) контрастная (контрастирование введенного зонда водорастворимыми контрастными средствами) — при атрезии четко видно слепой конец пищевода, при наличии свищей — затекание контраста в трахею.
Лечение атрезии пищевода
Атрезия пищевода — безусловное показание к раннему оперативному лечению. Применяют следующие виды оперативного лечения:1. Разделение пищеводно-трахеальной свища и наложение прямого анастомоза между концами пищевода.
2. При большом диастаза концов пищевода — наложение эзофагостомы и гастростомы. Затем, в возрасте от 2-3 месяцев до 3 лет, — пластика пищевода толстокишечный трансплантатом.
vse-zabolevaniya.ru
Атрезия пищевода
Атрезия пищевода является тяжелым пороком развития, при котором верхний отрезок органа заканчивается слепо. Нижний отрезок пищевода чаще всего сообщается с трахеей. Возможный другие варианты атрезии пищевода (рис. 133), но они встречаются значительно реже. По статистическим данным, 1 ребенок из 3000—4000 рождается с атрезией пищевода.
Развитие порока связано с нарушениями в ранних стадиях эмбрионального периода. Пищевод и дыхательные пути возникают из одного зачатка — передней кишки (краниального отдела первичной кишки). Из ее центральной части образуется выпячивание, именуемое трахейным желобком. Оно идет параллельно дорсальной части перзичной кишки, из которой образуется пищевод. В самых ранних стадиях трахея широко сообщается с пищеводом. Разделение сообщения между ними происходит на 4—5-й неделе внутриутробного периода. Причину атрезий Р. И. Венгловский усматривает в неполной отшнуровке дыхательной трубки от пищевода и в нарушении его питания. По данным других авторов, возникновение порока связано с неправильным развитием эпителиальных слоев. В конце 2-го месяца эмбрионального развития отмечается усиленный рост эпителия; размер органа в это время очень мал, и просвет его заполнен массами эпителиальных клеток (Б. М. Пэттен). Вслед за этим начинается процесс постепенного рассасывания эпителиальных клеток, между ними образуются пустоты, вакуоли. Стадия вакуолизации приводит к восстановлению просвета пищевода, нарушение этого процесса может привести к атрезии или стенозу.
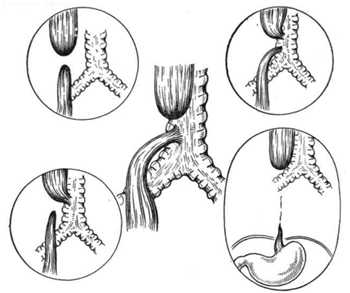
Рис. 133. Варианты атрезии и пищевода. В центре наиболее частая форма атрезии.
Клиническая картина. Атрезия пищевода выявляется вскоре после рождения ребенка. Одним из ведущих и ранних признаков являются пенистые выделения изо рта и носа, после отсасывая слизь быстро накапливается. Постепенно нарастают нарушения дыхания, появляется цианоз. В дальнейшем в клинической картине начинают преобладать симптомы дыхательной недостаточности, ооусловленные тяжелой аспирационной пневмонией Ребенок цианотичен, выражена одышка, в легких выслушивается
большое количество влажных разнокалиберных хрипов Пневмония связана не только с аспирацией слюны и молока, но и затеканием через трахеоэзофагеальный свищ желудочного содержимого в трахею и бронхи.
Диагностика. При наличии симптомов, вызывающих малейшее подозрение на атрезию пищевода, немедленно прибегают к дополнительным методам исследования. Простейшим среди них является зондирование пищевода резиновым катетером № 8-10 по шкале Шарьера, который вводят через рот или нос в пищевод
При атрезии катетер задерживается на уровне слепого мешка, а в норме свободно проходит. Учитывая огромную важность раннего выявления атрезии, до возникновения аспирационной пневмонии, зондирование пищевода целесообразно производить всем младенцам сразу после рождения. Этот прием даже при отсутствии атрезии может оказаться весьма полезным, так как обеспечивает эффективное удаление околоплодных вод и слизи из желудка, аспирация которых возможна и у здоровых детей.
При зондировании пищевода в сомнительных случаях проводят также пробу Элефанта: по катетеру, находящемуся в пищеводе, быстро вводят 20-граммовым шприцем воздух; при наличии атрезии он с шумом выходит через нос и рот ребенка.
Окончательный диагноз ставят при рентгенологическом исследовании. После введения катетера в пищевод делают обзорную рентгенограмму грудной клетки. При атрезии пищевода на рентгенограмме отчетливо видно, что катетер не проходит в желудок, а останавливается или заворачивается на уровне слепого конца пищевода (рис. 134). В сомнительных случаях возможно введение по катетеру 1—1,5 мл водорастворимого контрастного вещества или йодолипола с последующим его отсасыванием. Применение бариевой взвеси недопустимо ввиду опасности развития аспирационной пневмонии.
Рис. 134. Атрезия пищевода. Рентгенограмма. Катетер, введенный через, рот, заворачивается в слепом конце пищевода.
Рентгенологическое исследование не только окончательно подтверждает диагноз атрезии, но и позволяет установить ее уровень, наличие или отсутствие пищеводно-трахеального свища. Газ в желудке указывает на сообщение аборального конца пищевода с трахеей, отсутствие газа свидетельствует об атрезии пищевода без, свища. Если атрезию пищевода диагностируют поздно, дети умирают от тяжелой аспирационной пневмонии. Тяжесть пневмонии является фактором, во многом определяющим прогноз даже после успешной операции.
Лечение. Только раннее оперативное вмешательство может спасти жизнь ребенку с атрезией пищевода. Предоперационную подготовку начинают с момента установления диагноза. Она включает устранение дальнейшей аспирации, лечение аспирационной пневмонии, ликвидацию гипоксии и ацидоза, рациональные мероприятия по регидратации, парентеральное питание, симптоматическую медикаментозную терапию. Уже в родильном доме каждые 10—15 мин отсасывают слизь катетером из пищевода и носоглотки. Постоянно подают увлажненный кислород. Кормление через рот полностью исключают. Назначают антибиотики.
Предоперационная подготовка не может полностью ликвидировать явления пневмонии, так как продолжается аспирация из желудка через пищеводно-трахеальный свищ. По достижении более или менее выраженного улучшения приступают к операции.
Операция при атрезии пищевода преследует цель обеспечить возможность энтерального питания и ликвидировать сообщение дыхательных путей с пищеварительным трактом. Вмешательство выполняют под эндотрахеальным наркозом. Выделяют трахеопищеводный свищ, перевязывают и пересекают. Мобилизуют слепой конец пищевода. Наложение прямого анастомоза между концами пищевода возможно и целесообразно при диастазе не более 1,5 см.
После операции прямого анастомоза в послеоперационном периоде в первые дни в пищеводе оставляют катетер для кормления или накладывают гастростому.
Однако условия для наложения надежного прямого анастомоза при атрезии пищевода имеются не всегда из-за значительного диастаза между сегментами пищевода. В этих случаях прибегают к двухэтапной операции. Методики ее различны. В любом случае обязательными являются перевязка и пересечение пищеводно-трахеального свища. Далее дистальный отдел пищевода перевязывают или ушивают, производят мобилизацию проксимального слепого мешка пищевода. Путем разреза на шее выводят верхний отрезок пищевода и подшивают к коже — формируют эзофагостому, накладывают гастростому для кормления.
Пластику пищевода проводят в более старшем возрасте, после года.
Г. А. Баиров применяет двойную эзофагостомию. Отличие заключается в том, что гастростому не накладывают; ее роль выполняет дистальный отдел пищевода, который мобилизуют и выводят на переднюю поверхность брюшной стенки (нижняя эзофагостома). В дальнейшем выполняют операцию создания искусственного пищевода.
Успех операции во многом зависит от тщательного ухода и лечения в послеоперационном периоде. Необходим индивидуальный сестринский пост. В послеоперационном периоде продолжаются мероприятия по борьбе с пневмонией и гипоксией. В первые дни питание через катетер, гастростому или нижнюю эзофагостому должно быть минимальным (5—10 мл через 2 ч). Недостающее количество жидкости вводят парентерально. При благополучном течении постепенно переходят на кормление в соответствии с возрастом.
Результаты лечения при атрезии пищевода зависят от многих обстоятельств: ранней диагностики, успешной предоперационной подготовки, характера и объема оперативного вмешательства, течения послеоперационного периода.
Нередко прогноз ухудшается в связи с наличием недоношенности или сочетанных пороков развития, которые при данном заболевании встречаются довольно часто.
Исаков Ю. Ф. Детская хирургия, 1983 г.
extremed.ru
Операция при атрезии пищевода — «Медзаписки»
Атрезия пищевода представляет собой непроходимость пищевода с наличием или отсутствием трахеопищеводного свища (ТПС). Эта аномалия возникает в результате «поломки» на 4-й неделе гестации, когда в норме примитивная передняя кишка разделяется на пищевод и трахею. Известные семейные наблюдения атрезии пищевода наводят на мысль о возможной роли генетического фактора. Большинство случаев, однако, возникают спорадически, при отсутствии каких-либо определенных наследственных или тератогенных факторов. Частота атрезии пищевода составляет 1:4500 новорожденных с легким преобладанием патологии (59%) у мальчиков. Сочетанные пороки развития встречаются часто — в 40—60% случаев, а если проводить самое тщательное обследование скелетной системы, то этот показатель может подняться до 80%. Описаны, по меньшей мере, 18 различных синдромов, компонентом которых является атрезия пищевода. Наиболее хорошо известны VATER- или VACTERL-ассоциации аномалий (Vertebral-Anal-Cardiac-Tracheal-Esophageal-Renal- Limb)
Наиболее
ранний симптом атрезии пищевода — многоводие (выявляемое во второй
половине беременности) — является, однако, неспецифическим симптомом
нарушений глотания или пассажа жидкости через верхние отделы кишечного
тракта плода. При антенатальном УЗИ можно выявить движение жидкости,
поступающей в верхний сегмент пищевода и обратно, а при атрезии
пищевода без нижнего ТПС — отсутствие жидкости в желудке и тонкой
кишке. После рождения клинические проявления заключаются в выделении
слюны из ротоносоглотки и приступах цианоза. Если зонд для кормления №
12 не проходит в желудок, то диагноз атрезии пищевода становится
практически несомненным. Как только диагноз установлен, необходимо
ввести оро- или назоэзофагеальную трубку (Replogle) для постоянной или
периодической аспирации слюны с целью предотвращения аспирации. За
ребенком должен быть установлен тщательный сестринский уход, основная
цель которого — предупредить аспирацию желудочного содержимого в
дыхательные пути.
До операции необходимо установить вид порока. Воздух в желудочно-кишечном тракте на рентгенограммах (с обязательным захватом шеи, грудной клетки и брюшной полости) говорит о наличии нижнего трахеопищеводного свища. В большинстве подобных случаев (тип ЗЬ/С или Зс/О) возможно наложение первичного анастомоза. В противоположной ситуации, при отсутствии воздуха в ЖКТ, т.е. при изолированной форме атрезии пищевода без нижнего трахеопищеводного свища, можно с большой долей вероятности предполагать значительный диастаз между сегментами пищевода (тип 1/—, 2/А или За/В). Зонд, максимально продвинутый в верхний сегмент, позволяет определить его примерную длину.
Важно определить, нет ли сочетанных аномалий. Такие очевидные пороки, как атрезия ануса и аномалии развития конечностей, могут быть обнаружены при обычном первичном осмотре. Рентгенография ОГК и брюшной полости позволяет выявить сочетанную с атрезией пищевода непроходимость двенадцатиперстной кишки или других отделов кишечника, а также диафрагмальную грыжу и/или скелетные аномалии. Важно внимательно осмотреть клинически и рентгенологически позвоночник (в частности, сосчитать количество ребер и позвонков), чтобы не пропустить пороки его развития. Контрастное исследование редко бывает показанным. Кардиологическое обследование, включая эхокардиографию, играет важную роль, позволяя диагностировать сочетанные врожденные пороки сердца, которые могут повлиять на ведение наркоза, а обнаруженное при этом правостороннее расположение дуги аорты — на хирургическую тактику. Кроме того, необходимо провести УЗИ мочевых путей для выявления аномалий мочевыделительной системы.
Ребенок должен находиться в отделении реанимации новорожденных. Экстренная операция редко бывает показанной, поэтому все перечисленные методы обследования должны быть произведены шаг за шагом. При наличии респираторного дистресс-синдрома, тяжелой пневмонии или серьезных сочетанных аномалий, требующих респираторной терапии, показана интубация и ИВЛ. Эндотрахеальную трубку необходимо ввести ниже дистального трахеопищеводного свища, чтобы избежать инсуффляции воздуха в желудок, что таит в себе риск разрыва желудка, особенно в случае сочетания атрезии пищевода с атрезией кишечника.
Классификации атрезии пищевода обычно основаны на наличии свища и его виде. Чаще всего используются классификации Vogt (в ней вариант порока изображается в виде цифры и прописной буквы) и Gross(цифра и заглавная буква). Наиболее часто (85%) встречающийся вид атрезии пищевода (3bпо Vogt и С по Gross) — атрезия пищевода с нижним трахеопищеводным свищом. Самый редкий вариант по классификации Vogt, обозначаемый цифрой 1 и представляющий собой отсутствие пищевода на большом протяжении, в классификации Grossвообще отсутствует. Тип 2/А (7%) соответствует атрезии пищевода без свищей. При этом варианте обычно бывает большой диастаз между сегментами, как и при варианте За/В (2%) — с верхним ТПС. У детей с атрезией пищевода Зс/D(3%) имеются два свища — верхний и нижний. Некоторые авторы включают в классификацию изолированный ТПС без атрезии пищевода (Н-тип свища), обозначая этот вариант порока 4/Е (3%), хотя вряд ли это логично, поскольку при данном варианте нет собственно атрезии пищевода. В классификации Gross есть еще тип F— врожденный стеноз пищевода.
Ход операции
Операцию проводят под интубационным наркозом. Интубационную трубку вводят ближе к бифуркации трахеи и вентилируют мануально низким давлением на вдохе и небольшими объемами, что позволяет избежать гипервентиляции и раздувания желудка, а также стабилизировать трахею во время операции. В верхний сегмент вводят зонд, чтобы облегчить хирургу поиски верхнего сегмента. Обязательна профилактика антибиотиками широкого спектра действия при введении в наркоз. Мы традиционно начинаем вмешательство с трахеобронхоскопии жестким эндоскопом 3,5 мм. Осматриваем трахею и главные бронхи, находим отверстие трахеопищеводного свища, который обычно располагается на 5—7 мм выше карины.
В редких случаях свищ открывается непосредственно в карину или даже в правый главный бронх, что обычно является признаком наличия короткого нижнего сегмента и, соответственно, большого диастаза между сегментами. Следующая цель этого обследования — посмотреть, нет ли верхнего ТПС. Дорсальную (мембранозную) часть трахеальной стенки осматривают внимательно вверх до перстневидного хряща. Небольшой верхний свищ легко пропустить. Чтобы избежать этой ошибки, в трахею через бронхоскоп вводят уретеральный катетер ЗИ и его верхушкой слегка надавливают на дорсальную стенку в местах «неровностей». При наличии свища уретеральный катетер обычно попадает (проходит) в его отверстие.
Стандартный доступ при операции по поводу атрезии пищевода — правосторонняя заднебоковая торакотомия. Если до вмешательства выявлена правосторонняя дуга аорты, рекомендуется левосторонний доступ. Однако если правостороннее расположение нисходящей аорты обнаружено непосредственно во время операции, начатой из правостороннего доступа, обычно удается продолжить вмешательство из этого доступа с наложением анастомоза пищевода справа от дуги аорты.
Ребенка укладывают на операционном столе на левый бок, подкладывая валик и фиксируя новорожденного к столу лейкопластырем. Валик под левой половиной грудной клетки способствует улучшению доступа, особенно к глубоко расположенным структурам. Правую руку отводят вверх без излишнего натяжения. Легкий поворот руки кпереди позволяет снизить риск повреждения плечевого сплетения (в результате натяжения). Предплечье в локтевом суставе сгибают под углом 90°, при этом желательно фиксировать его мягкой повязкой к поперечной перекладине над головой ребенка. Важно обеспечить такое положение ребенка, чтобы ни одна часть тела, головы, конечностей не была сдавлена.
Мягкие прокладки должны быть помещены между коленями и под стопами, или конечности обвертывают теплыми шерстяными повязками, которые в то же время защищают от потери тепла.
Разрез производят слегка изогнутый, на 1 см ниже лопатки от среднеаксиллярной линии к углу лопатки. Некоторые хирурги предпочитают (по косметическим соображениям) вертикальный разрез по среднеаксиллярной линии. Большим преимуществом операций у новорожденных является возможность использовать щадящую технику разделения (разведения) мышц, что оказывается возможным, благодаря тому, что ткани мягкие, податливые и мобильные. Отслаивают лишь небольшие лоскуты кожи с подкожной клетчаткой (без широкой мобилизации). Широчайшую мышцу спины (m. Latissimus dorsi) мобилизуют, отсекая ее в зоне передних фасциальных пучков, и отводят кзади вместе с торакодорсальным нервом, который пересекает ее глубокую поверхность вдоль задней аксиллярной линии. После отведения m. Latissimus dorsi мобилизуют край передней зубчатой мышцы (m. Serratus anterior), отделяя ее от угла лопатки до VI ребра, и отводят вверх и вперед вместе с лопаткой.
Межреберные мышцы разделяют вдоль верхнего края V ребра. Париетальную плевру отделяют от грудной стенки маленьким тупфером. Как только становится возможно, осторожно вводят рано- расширитель, медленно, постепенно разводя его. Дальнейшее отделение плевры по направлению к заднему средостению производят двумя тупферами, одним из них хирург придерживает уже отделенную плевру, слегка на нее надавливая, другим продолжает отделение плевры. При случайном повреждении плевры отверстие можно ушить рассасывающейся мононитью 6/0.
Если непарная вена расположена непосредственно в зоне манипуляций и «мешает» выделению нижнего сегмента, ее мобилизуют, перевязывают двумя лигатурами (викрил 4/0) и рассекают между ними. В большинстве случаев удается ее сохранить. Находят правый блуждающий нерв, который идет вдоль латерального края верхнего сегмента и «сопровождает» ТПС в направлении нижнего сегмента пищевода, который обычно тонкий и гипопластичный, поэтому необходимо проявлять чрезвычайную осторожность, избегая любой травмы его нежных тканей. Всякое прикосновение руками и инструментами (пинцетом) к стенке пищевода должно быть сведено к минимуму. Важно также сохранение всех мельчайших волокон блуждающего нерва, сопровождающих нижний сегмент пищевода. «Обнажение» пищевода неизбежно ведет к значительным расстройствам двигательной активности и может вызвать тяжелый гастроэзофагеальный рефлюкс.
Изогнутым зажимом (правоугольным) под дистальный сегмент подводят сосудистую держалку и с ее помощью отводят сегмент от трахеи. Это помогает найти ТПС, который теперь освобождают от окружающих тканей.
Швы-держалки накладывают на трахеальный (один шов) и ээофагеальный (два шва) концы свища.
Свищ отсекают от трахеи, которую ушивают непрерывным швом рассасывающейся мононитью 6/0. Некоторые авторы предпочитают отдельные швы. Отсечение свища необходимо производить как можно ближе к трахее, но при этом таким образом, чтобы не сузить ее просвет. Поскольку в большинстве случаев свищ идет вверх в косом направлении, то на трахее часто остается небольшой резидуальный «карманчик». Герметичность ушивания трахеи проверяют, тщательно наблюдая за тем, не появятся ли пузырьки воздуха после наливания теплого физиологического раствора в рану на фоне гипервентиляции. На этой стадии желательно прекратить всякое сдавление легкого и добиться полного расправления всех спавшихся участков.
Верхний сегмент пищевода нередко сокращается и «уходит» на шею. Анестезиолог вводит в него зонд, чтобы продвинуть сегмент и облегчить его поиски. На верхний сегмент накладывают два тракционных шва, подтягивание за которые облегчает его мобилизацию. Наиболее сложный этап — отделение пищевода от трахеи, поскольку они бывают тесно связаны между собой соединительнотканными тяжами. Приходится использовать острые ножницы, стараясь при этом избежать малейшего повреждения как пищевода, так и трахеи. Спереди и латерально верхний сегмент легко отделяется тупфером. Если неожиданно обнаружен верхний свищ, его пересекают как можно ближе к пищеводу, после чего пищевод и трахею ушивают отдельными швами рассасывающейся мононитью 6/0. В отличие от нижнего сегмента, верхний имеет хорошее кровоснабжение, а потому при необходимости может быть выделен вплоть до его «входа» в грудную клетку. Соответственно, при большом диастазе предпочтительна интенсивная мобилизация верхнего, а не нижнего сегмента, ибо мобилизация последнего влечет за собой большой риск ишемии и последующего нарушения двигательной активности пищевода. После завершения мобилизации верхнего сегмента оба сегмента сближают и оценивают диастаз, решая вопрос о возможности наложения анастомоза конец-в-конец.
Рассекать верхний сегмент для наложения анастомоза необходимо строго в центре его верхушки, лучше всего точно над концом максимально продвинутого в сегмент зонда. Асимметричный разрез может быть причиной формирования несимметричного анастомоза, что потенциально ведет к образованию преанастомотического латерального кармана. Верхний сегмент вскрывают горизонтальным разрезом, в результате чего образуется отверстие, подобное «рыбьему рту», которое по размерам должно соответствовать диаметру нижнего сегмента.
Анастомоз конец-в-конец формируют отдельными рассасывающимися швами 6/0. Первые два шва накладывают по бокам, затем два или три дополнительных шва — на заднюю стенку. Необходима большая тщательность, чтобы захватить достаточно большие «кусочки» мышечного слоя вместе со слизистой. Слизистая оболочка имеет тенденцию сокращаться и уходить вверх, когда вскрывают верхний сегмент. После наложения всех швов (без завязывания) на заднюю полуокружность сегменты осторожно сближают и швы завязывают узелками внутрь просвета пищевода. Затем пластиковый зонд для питания 5Р со срезанным наружным концом подшивают этим концом к верхушке трубки, которую анестезиолог извлекает до тех пор, пока зонд для питания не выйдет изо рта. Дистальный конец зонда проводят в желудок. Зонд служит для послеоперационной декомпрессии желудка, раннего питания, а также для оттока слюны.
Переднюю полуокружность анастомоза создают так же, как и заднюю, накладывая 3-4 шва и завязывая нити снаружи стенки пищевода.
Описанная техника наложения анастомоза (без натяжения) может быть применена в большинстве случаев атрезии пищевода с нижним ТПС. Если же, несмотря на интенсивную «высокую» мобилизацию верхнего сегмента, диастаз остается значительным и сегменты не могут быть сопоставлены без натяжения, диастаз можно сократить путем применения циркулярной миотомии верхнего сегмента, что способствует удлинению верхнего сегмента и, соответственно, сокращению диастаза. Для этой цели в верхний сегмент через рот вводят баллонный катетер 8Р, который фиксируют мононитью-держалкой 4/0, прошивая стенку верхушки верхнего сегмента и сам катетер. Затем баллон раздувают до тех пор, пока он не заполнит просвет верхнего сегмента. Мышечный слой рассекают (циркулярно или спирально) над баллоном приблизительно на 1 см выше линии будущего анастомоза. Слизистая оболочка верхнего сегмента обычно довольно «толстая», поэтому при осторожных манипуляциях несложно избежать ее повреждения. При использовании этого метода можно достичь удлинения верхнего сегмента на 5—10 мм — этого обычно бывает достаточно, чтобы наложить анастомоз без натяжения. В литературе есть описания случаев образования псевдодивертикула (выбухание слизистой через созданный мышечный дефект) после циркулярной миотомии.
Другой путь уменьшения натяжения при большом диастазе — формирование мышечно-слизистого лоскута верхнего сегмента. На передней поверхности одной из половин верхнего сегмента делают прямоугольный разрез. Созданный лоскут поворачивают на 90° таким образом, чтобы вертикально рассеченный край «смотрел» вниз. Затем этот лоскут сворачивают в виде трубки. Однако такое удлинение приводит к уменьшению диаметра просвета.
Если после завершения формирования задней губы анастомоза возникают трудности (натяжение) при создании передней полуокружности, можно сформировать прямоугольный лоскут в соответствующей части верхнего сегмента (без тубуляризации), что позволяет уменьшить диастаз и создать более надежный анастомоз.
Операционную рану орошают физиологическим раствором. Мягкую дренажную трубку подводят к анастомозу, выводя наружу через отдельный прокол в межреберье. До ушивания грудной клетки необходимо расправить (с помощью усиленной вентиляции) все коллабированные участки легкого.
Ребра сближают двумя или тремя швами. М. latissimusdorsi и m. serratusanteriorвозвращают в нормальное положение и подшивают к месту их фасциального прикрепления одним или двумя (каждую мышцу) рассасывающимися швами 3/0. Подкожную клетчатку ушивают рассасывающимися швами 5/0. Подобная техника позволяет в большинстве случаев прекрасно сблизить кожные края, так что необходимость в кожных швах отпадает. Края разреза кожи просто сближают лейкопластырем. В тех случаях, когда сопоставление краев раны остается неудовлетворительным, применяют субэпидермальный непрерывный шов мононитью 5/0, который снимают через несколько дней.
Наличие при обследовании ребенка с атрезией пищевода «немого» живота на рентгенограммах должно вызывать подозрение на атрезию без нижнего свища (10%). Прямой первичный анастомоз в такой ситуации невозможен из-за большого диастаза.
Два основных варианта хирургической тактики применяют в этих случаях: сохранение собственного пищевода или пластика пищевода. Сохранение собственного пищевода с отсроченным анастомозом при атрезии без нижнего свища может быть осуществлено тремя путями. Во-первых, ожидание спонтанного роста, который характерен в основном для верхнего сегмента. Как подсказывает наш опыт, это занимает 8—12 нед., после чего относительно безопасно наложение отсроченного анастомоза. Во-вторых, можно попытаться удлинить верхний сегмент путем регулярного продольного его растяжения. В-третьих, сближение сегментов может быть достигнуто путем дополнительного бужирования нижнего сегмента. Последний способ мы считаем предпочтительным, поскольку он позволяет наложить анастомоз через 3—5 нед.
Первичная гастростомия для энтерального питания показана во всех случаях атрезии пищевода с большим диастазом. Кроме того, наличие гастростомы позволяет оценить величину диастаза, и, наконец, гастростома используется для манипуляций, направленных на удлинение нижнего сегмента.
Поперечный разрез делают в левой эпигастральной области на середине расстояния между пупком и реберной дугой. Мы предпочитаем гастростомию по Штамму (Stamm) с наложением по малой кривизне ближе к угловой вырезке (incisura angularis) двух кисетных швов рассасывающейся нитью 3/0. Желудок вскрывают в центре этих швов. Если не предполагается растяжение (удлинение) нижнего сегмента через гастростому, то соответствующую гастростомическую трубку вводят в желудок, кисетные швы завязывают и фиксируют изнутри в париетальной брюшине. Если предполагается бужирование как верхнего, так и нижнего сегмента, создают еюностому для питания, которую накладывают на первую петлю тощей кишки, выводя ее через отдельный разрез брюшной стенки ниже гастростомического. Еюностому формируют одним кисетным швом нитью 3/0, который фиксируют к внутренней поверхности брюшной стенки. Зонд для питания продвигают глубоко в тощую кишку. Энтеральное питание может быть начато через 24 ч после операции.
Если планируется механическое удлинение нижнего сегмента, то величина диастаза между сегментами оценивается следующим образом: зонд для питания 8Р—10Р обрезают в 10-13 см от его дистального конца и металлический изогнутый (под углом 70°) зонд вводят в зонд для питания до его верхушки. Этот «комплект» проводят в нижний сегмент пищевода через желудок. В это же время анестезиолог вводит рентгеноконтрастный зонд в верхний сегмент. Оба зонда под контролем экрана максимально сближают и измеряют расстояние между сегментами. Обычно расстояние соответствует высоте 4 или более тел позвонков. Зонд для питания с металлическим зондом внутри держат в желудке, и растяжение обоих сегментов проводят дважды в день в течение 3—5 мин под легкой седатацией. Растяжение нижнего сегмента производят очень деликатно, осторожно, в то время как растяжение верхнего сегмента можно производить с более значительным усилием. Важно, чтобы эти процедуры проводил один и тот же опытный хирург, тогда можно избежать такого осложнения, как перфорация пищевода. Динамику и эффективность удлинения оценивают еженедельно, проводя исследование под контролем экрана и фиксируя достигнутые результаты рентгенографически. Отчетливое захождение сегментов один за другой, которое необходимо для наложения анастомоза конец-в-конец без натяжения, обычно достигается за 3-5 нед.
На Н-тип трахеопищеводных свищей без атрезии пищевода приходится около 3% всех трахеопищеводных аномалий. Проявления такого варианта порока обычно не столь остры и длительны, а порой даже начинаются лишь после первого года жизни. Типичные симптомы — кратковременные эпизоды нарушения дыхания с цианозом во время кормления. Диагноз устанавливают с помощью эзофагографии с контрастом или трахеобронхоскопии. Если подтверждается наличие трахеопищеводного свища, во время бронхоскопии в свищ вводят уретеральный катетер. В большинстве случаев ТПС можно «достать» из шейного доступа, поскольку он обычно располагается на уровне второго грудного позвонка или даже выше. Если планируется шейный доступ, то ребенка укладывают на операционном столе на спину с головой, повернутой влево, и с валиком под плечами с переразогнутой шеей. В таком положении область шеи справа становится максимально доступной. Разрез производят по кожной складке, приблизительно на I см выше средней трети правой ключицы. После рассечения подкожной мышцы шеи медиальный край кивательной мышцы отводят кзади.
Разделение тканей продолжают медиально по направлению к сонной артерии, при этом иногда приходится перевязать и рассечь среднюю щитовидную вену и нижнюю щитовидную артерию, чтобы подойти к трахее и пищеводу, которые расположены медиально и кзади от долей щитовидной железы и ее перешейка. Пальпация трахеальных хрящей и желудочного зонда в пищеводе облегчает анатомическую ориентацию. Возвратный гортанный нерв, идущий кверху в желобе между трахеей и пищеводом, близко к свищу, должен быть четко идентифицирован, чтобы избежать его повреждения.
Поиски свища облегчаются благодаря уретеральному катетеру, проведенному в свищ. Изогнутый прямоугольный зажим используют для выделения свища, под который подводят небольшую сосудистую держалку Две нити-держалки накладывают на пищеводную часть свища, который пересекают после извлечения из него уретерального катетера.
Отверстие в трахее и пищеводе ушивают отдельными швами рассасывающейся мононитью 6/0. Рану ушивают послойно рассасывающимся материалом, заканчивая отдельными субэпидермальными рассасывающимися швами 6/0. В конце операции необходимо убедиться в подвижности голосовых связок.
ЗАКЛЮЧЕНИЕ
Первый успешный первичный анастомоз при атрезии пищевода был наложен Cameron Haight в 1941 г. В последующие десятилетия летальность при этом пороке была высокой. Результаты лечения определялись массой тела ребенка при рождении, тяжестью сопутствующих аномалий и аспирационной пневмонии, связанной с поздней диагностикой порока. В настоящее время диагноз атрезии пищевода в большинстве случаев устанавливается сразу после рождения, поэтому постоянная санация верхнего сегмента способствует профилактике пневмонии. Выживаемость недоношенных детей значительно возросла благодаря развитию неонатальной интенсивной терапии. Поэтому главным фактором, определяющим результаты, стали тяжелые сопутствующие аномалии. Принципы лечения наиболее частого варианта атрезии пищевода с нижним трахеопищеводным свищом общеприняты и особых дискуссий не вызывают, в то время как подходы к лечению порока при большом диастазе между сегментами остаются весьма противоречивыми. В некоторых клиниках, включая нашу, предпочитают сохранять собственный пищевод ребенка при малейших шансах, даже ценой тяжелого гастроэзофагеального рефлюкса, в то время как другие хирурги более широко ставят показания к пластике пищевода трансплантатом из толстой кишки или желудка.
Прогноз при лечении атрезии пищевода в общем хороший, однако в послеоперационном периоде остаются такие проблемы, как рецидивирующие эпизоды дисфагии, гастроэзофагеальный рефлюкс, рецидивирующая инфекция верхних дыхательных путей, которая может быть связана с повторными микроаспирациями во время сна. Нередко отмечается задержка опорожнения дистальных отделов пищевода, обусловленная нарушением его двигательной активности, которое, в свою очередь, может быть компонентом самой аномалии (атрезии пищевода), однако не исключена и ятрогенная природа, связанная с повреждением волокон блуждающего нерва во время интраоперационного выделения нижнего сегмента пищевода. Тем не менее, тяжелые нарушения глотания с дисфагией возникают редко. Задержка инородных тел над зоной анастомоза, чаще всего кусочков хлеба, мяса или фруктов, бывает отчасти связана с расстройствами двигательной активности пищевода.
Стеноз зоны анастомоза может быть результатом его наложения со значительным натяжением, несостоятельности или длительного воздействия кислого желудочного содержимого при гастроэзофагеальном рефлюксе. Задержка опорожнения пищевода от кислого желудочного содержимого, забрасывающегося в пищевод, скорее всего, в большей степени связана с высокой частотой гастро-эзофагеально-рефлюксной болезни, которая может развиваться более чем у 40% детей с атрезией пищевода.
Атипично изогнутые
хрящи трахеи и широкая межхрящевая мембрана в зоне бывшего свиша могут
быть причиной другого общеизвестного осложнения — трахеомаляции,
частота которой достигает 20%. При этом передне-задний диаметр просвета
трахеи уменьшается и стенки ее могут полностью спадаться, затрудняя как
вдох, так и выдох. Подобная аномалия редко вызывает серьезные проблемы и
обычно проходит с возрастом и ростом. Иногда, однако, развивается
тяжелый респираторный дистресс, что может потребовать хирургического
лечения, порой срочного. Наиболее часто применяемый в этом случае метод
— аортопексия под бронхоскопическим контролем. Это вмешательство
позволяет справиться с данной проблемой в большинстве случаев, если
только трахея поражена не на слишком большом протяжении. В последней
ситуации в настоящее время используется метод трахеосконической
стабилизации трахеи с помощью стента с баллоном, раздувающимся по всей
окружности или по полуокружности. Однако пока проводятся поиски
идеального стента. Кроме того, стентирование трахеи стали проводить
недавно, поэтому отдаленные результаты еще не могут быть оценены.
www.medzapiski.ru
Атрезия пищевода у новорожденных детей
Атрезия пищевода является тяжелейшим пороком в развитии, при котором верхний отрезок области пищевода завершается слепо. Очень часто представленное патологическое состояние сочетается с остальными заболеваниями: генетически приобретенными пороками сердечной мышцы, системы ЖКТ, а также мочеполовой системы. Примерно в 5% случаев атрезия формируется при хромосомных заболеваниях, одинаково часто патология проявляется у представителей мужского и женского пола.
Причины развития заболевания
 Говоря о причинах атрезии пищевода, настоятельно рекомендуется обратить внимание на целый перечень факторов. В частности, на дестабилизацию закладки пищевода на начальных этапах (с четвертой по 12 неделю) внутриутробного формирования плода. Далее, как известно, пищевод и трахея проявляются из единого общего зачатка, а именно краниального отдела первичной кишки. Во время начального эмбриогенеза (формирования плода в утробе матери) они сообщаются друг с другом.
Говоря о причинах атрезии пищевода, настоятельно рекомендуется обратить внимание на целый перечень факторов. В частности, на дестабилизацию закладки пищевода на начальных этапах (с четвертой по 12 неделю) внутриутробного формирования плода. Далее, как известно, пищевод и трахея проявляются из единого общего зачатка, а именно краниального отдела первичной кишки. Во время начального эмбриогенеза (формирования плода в утробе матери) они сообщаются друг с другом.
Поэтому необходимо учитывать, что атрезия пищевода может возникнуть в рамках их разделения при нарушении общего направления и скорости изменения не только трахеи, но и пищевода новорожденных. Еще одним фактором специалисты называют неполноценную отшнуровку респираторной трубки от пищевода, дестабилизацию его питания. Также заболевание вполне может развиться при некорректном процессе реканализации, через который проходят все структуры кишечной трубки.
Основные и дополнительные симптомы
Классическим признаком атрезии пищевода можно назвать постоянное выделение пенистой слюны в значительном количестве не только изо рта, но и из носа младенца (так называемая ложная гиперсаливация). По причине отсутствия нормального дыхания у ребенка части слизи в трахее нарастают и появляются симптомы нарушения дыхательного процесса, а именно:
- хрипы;
- приступы кашлевых позывов;
- тахипноэ – учащенное поверхностное дыхание;
- одышка;
- цианоз – изменение оттенка кожи и слизистых оболочек – приобретение синюшной окраски;
- асфиксия – удушье, продолжительное или кратковременное отсутствие нормальной возможности дышать.
После последующего выкачивания слизи из области носоглотки, а также трахеальной аспирации диагностируют непродолжительную нормализацию состояния. Однако в подавляющем большинстве случаев пенистые выделения образуются повторно. Уже при осуществлении первого кормления ребенка грудью после нескольких глотков идентифицируют регургитацию пищи. Речь идет о перманентном и немедленном срыгивании нествороженным молоком и даже о рвотных позывах.
Если атрезия пищевода будет комбинироваться с нижним трахеопищеводным свищом, то начнется заброс содержимого желудка в область респираторных путей.
В связи с этим любая попытка вскармливания провоцирует у ребенка поперхивание, продолжительный приступообразный кашель с возникновением не только цианоза, но и удушья. У определенной части детей с атрезией и трахеопищеводным свищом диагностируют вздутие брюшинной области. В особенности часто это затрагивает эпигастрий по причине проникновения воздуха посредством свища в пищевод и желудок. При отсутствии подобного канала у ребенка с атрезией пищевода, наоборот, идентифицируют запавший живот и даже непроходимость кишечника.
Повторяющиеся рвотные позывы при атрезии пищевода достаточно быстро приводят к дегидратации и даже истощению организма. К тому же вдыхание грудничком слизи и пищи часто влияет на образование аспирационного воспаления легких. Оно в свою очередь будет сопровождаться лихорадкой, прогрессированием признаков респираторной недостаточности и даже летальным исходом. Именно поэтому очень важно озаботиться своевременной и полноценной диагностикой, что позволит в будущем начать лечение.
Диагностика в случае атрезии
 Атрезия пищевода у детей нуждается в максимально быстрой диагностике. Осуществлять ее настоятельно рекомендуется буквально в первые 12—24 часа с момента рождения, чтобы предупредить возникновение аспирационного воспаления легких. При самых минимальных подозрениях на развитие патологического состояния новорожденных с симптомами респираторных расстройств проводят интраназальное зондирование пищевода с применением резинового катетера. Говоря о диагностике, не следует забывать еще и о том, что:
Атрезия пищевода у детей нуждается в максимально быстрой диагностике. Осуществлять ее настоятельно рекомендуется буквально в первые 12—24 часа с момента рождения, чтобы предупредить возникновение аспирационного воспаления легких. При самых минимальных подозрениях на развитие патологического состояния новорожденных с симптомами респираторных расстройств проводят интраназальное зондирование пищевода с применением резинового катетера. Говоря о диагностике, не следует забывать еще и о том, что:
- в сомнительных ситуациях осуществляют пробу Элефанта с внедрением в область пищевода посредством катетера определенной порции воздуха. При присоединении атрезии он будет с шумом выходить из носоглотки;
- в некоторых случаях имеет смысл проводить эзофагоскопию и бронхоскопию, потому что они дают возможность определить разновидность атрезии. К тому же именно представленные методики визуализируют слепой конец пищевода, длину его проксимального участка, присутствие свищевого канала с трахеей и бронхами;
- окончательное подтверждение диагноза возможно после проведения рентгенографии с внедрением в область пищевода рентгена и специального контрастного катетера.
На обзорной рентгенограмме органов грудины, а также брюшной полости при атрезии пищевода идентифицируется его слепой проксимальный отрезок. Следует учитывать, что применение в рамках диагностики патологического состояния бариевой взвеси является крайне нежелательным. Дело в том, что это ассоциируется с высокими рисками образования респираторных осложнений, а также с летальным исходом.
При атрезии пищевода настоятельно рекомендуется обеспечить дифференцирование бессвищевой формы от свищевой. Также специалисты обращают внимание на значимость исключения стеноза пищевода, эзофагоспазмов, врожденного пилоростеноза, расщелины гортани и других аномальных состояний. После такой подробной и полноценной диагностики можно говорить о начале восстановительного курса.
Лечение данной патологии
Нужно учитывать, что атрезия пищевода провоцирует гибель ребенка на самых ранних сроках, а потому спасти жизнь можно будет лишь при условии экстренной операции. Проводиться она должна не позднее 36 часов с момента рождения. В самом родильном отделении осуществляют комплексную предоперационную подготовку, которая заключается в придании малышу специфической позы. Представленные мероприятия позволяют устранить рефлюкс желудочного сока посредством дистального свища.
Кроме того, в родильном отделении обеспечивается исключение вскармливания посредством ротовой области. Настоятельно рекомендуется проводить частую аспирацию слюны и слизи изо рта, носоглотки, а также дыхательных путей. Еще одним условием специалисты называют постоянную ингаляцию кислорода, осуществление не только инфузионной или антибактериальной, но и симптоматической терапии. Далее необходимо учитывать, что:
- выбор конкретной методики хирургического вмешательства будет зависеть от особенностей атрезии пищевода, а также общего состояния ребенка;
- при высокой вероятности радикальной операции рассматривают вопрос о проведении гастростомы для улучшения состояния желудка;
- при патологическом состоянии с дистальным свищом и минимальном хирургическом риске проводят торакотомию с вскрытием свища, внедрением прямого оперативного вмешательства;
- может понадобиться двухэтапное хирургическое вмешательство, а именно образование гастростомы и шейной эзофагостомы. В дальнейшем допустимо проведение так называемой экстраплевральной корректировки атрезии с блокировкой свища или реконструктивной пластикой пищевода за счет участка толстой кишки, что обеспечивает полноценное заращение;
- в рамках периода после оперативного вмешательства рекомендуется продолжение проводившегося медикаментозного лечения.
В течение первой недели после операции детское вскармливание обеспечивается посредством зонда. Если будут отсутствовать осложнения, тогда ребенка начинают кормить обычным путем, применяя антирефлюксные смеси. Через несколько недель проводят контрольную фиброэзофагогастроскопию или рентгенологическое обследование области пищевода (такое решение должно обговариваться с несколькими специалистами). При рубцовом стенозе, который проявляется после хирургического вмешательства в 30—40% случаев, осуществляют эндоскопическое бужирование анастомоза, чтобы ребенок мог полноценно жить дальше.
Каков прогноз при заболевании?
При поздней диагностике патологического состояния дети погибают от усугубленного аспирационного воспаления легких. Прогноз при ранней операционной корректировке неусугубленных форм атрезии пищевода является благоприятным. При изолированной разновидности атрезии пищевода показатели выживаемости составляют от 90 до 100%. В том случае, когда речь идет о наличии существенных сочетанных пороков и даже недоношенности – 30—50%.
Необходимо учитывать еще и то, что даже при успешно проведенной хирургической корректировке атрезии пищевода и удовлетворительных результатах трансэзофагеального пассажа оптимальная моторика дистального участка пищевода полноценно не восстанавливается. Таким образом, появление атрезии пищевода у новорожденных требует скорейшего проведения восстановительного курса с целью исключения развития осложнений и критических последствий.
Важно!КАК ЗНАЧИТЕЛЬНО СНИЗИТЬ РИСК ЗАБОЛЕТЬ РАКОМ?
Лимит времени: 0
ПРОЙДИТЕ БЕСПЛАТНЫЙ ТЕСТ! Благодаря развернутым ответам на все вопросы в конце теста, вы сможете в РАЗЫ СОКРАТИТЬ вероятность заболевания!
Вы уже проходили тест ранее. Вы не можете запустить его снова.
Тест загружается…
Вы должны войти или зарегистрироваться для того, чтобы начать тест.
Вы должны закончить следующие тесты, чтобы начать этот:
Время вышло
1.Можно ли предотвратить рак?
Возникновение такого заболевания, как рак, зависит от многих факторов. Обеспечить себе полную безопасность не может ни один человек. Но существенно снизить шансы появления злокачественной опухоли может каждый.2.Как влияет курение на развитие рака?
Абсолютно, категорически запретите себе курить. Эта истина уже всем надоела. Но отказ от курения снижает риск развития всех видов рака. С курением связывают 30% смертей от онкологических заболеваний. В России опухоли лёгких убивают больше людей, чем опухоли всех других органов.
Исключение табака из своей жизни — лучшая профилактика. Даже если курить не пачку в день, а только половину, риск рака лёгких уже снижается на 27%, как выяснила Американская медицинская ассоциация.3.Влияет ли лишний вес на развитие рака?
Почаще смотрите на весы! Лишние килограммы скажутся не только на талии. Американский институт исследований рака обнаружил, что ожирение провоцирует развитие опухолей пищевода, почек и желчного пузыря. Дело в том, что жировая ткань служит не только для сохранения запасов энергии, у неё есть ещё и секреторная функция: жир вырабатывает белки, которые влияют на развитие хронического воспалительного процесса в организме. А онкологические заболевания как раз появляются на фоне воспалений. В России 26% всех случаев онкологических заболеваний ВОЗ связывает с ожирением.4.Способствуют ли занятия спортом снижению риска рака?
Уделите тренировкам хотя бы полчаса в неделю. Спорт стоит на одной ступени с правильным питанием, когда речь идёт о профилактике онкологии. В США треть всех смертельных случаев связывают с тем, что больные не соблюдали никакой диеты и не уделяли внимания физкультуре. Американское онкологическое общество рекомендует тренироваться 150 минут в неделю в умеренном темпе или в два раза меньше, но активнее. Однако исследование, опубликованное в журнале Nutrition and Cancer в 2010 году, доказывает, что даже 30 минут хватит, чтобы сократить риск рака молочной железы (которому подвержена каждая восьмая женщина в мире) на 35%.5.Как влияет алкоголь на клетки рака?
Поменьше алкоголя! Алкоголь обвиняют в возникновении опухолей полости рта, гортани, печени, прямой кишки и молочных желёз. Этиловый спирт распадается в организме до уксусного альдегида, который затем под действием ферментов переходит в уксусную кислоту. Ацетальдегид же является сильнейшим канцерогеном. Особенно же вреден алкоголь женщинам, так как он стимулирует выработку эстрогенов — гормонов, влияющих на рост тканей молочной железы. Избыток эстрогенов ведёт к образованию опухолей груди, а значит, каждый лишний глоток спиртного увеличивает риск заболеть.6.Какая капуста помогает бороться с раком?
Полюбите капусту брокколи. Овощи не только входят в здоровую диету, они ещё и помогают бороться с раком. В том числе поэтому рекомендации по здоровому питанию содержат правило: половину дневного рациона должны составлять овощи и фрукты. Особенно полезны овощи, относящиеся к крестоцветным, в которых содержатся глюкозинолаты — вещества, которые при переработке обретают противораковые свойства. К этим овощам относится капуста: обычная белокочанная, брюссельская и брокколи.7.На заболевание раком какого органа влияет красное мясо?
Чем больше едите овощей, тем меньше кладите в тарелку красного мяса. Исследования подтвердили, что у людей, съедающих больше 500 г красного мяса в неделю, выше риск заболеть раком прямой кишки.8.Какие средства из предложенных защищают от рака кожи?
Запаситесь солнцезащитными средствами! Женщины в возрасте 18–36 лет особенно подвержены меланоме, самой опасной из форм рака кожи. В России только за 10 лет заболеваемость меланомой выросла на 26%, мировая статистика показывает ещё больший прирост. В этом обвиняют и оборудование для искусственного загара, и солнечные лучи. Опасность можно свести к минимуму с помощью простого тюбика солнцезащитного средства. Исследование издания Journal of Clinical Oncology 2010 года подтвердило, что люди, регулярно наносящие специальный крем, болеют меланомой в два раза меньше, чем те, кто пренебрегает такой косметикой.
Крем нужно выбирать с фактором защиты SPF 15, наносить его даже зимой и даже в пасмурную погоду (процедура должна превратиться в такую же привычку, как чистка зубов), а также не подставляться под солнечные лучи с 10 до 16 часов.9.Как вы думаете, влияют ли стрессы на развитие рака?
Сам по себе стресс рака не вызывает, но он ослабляет весь организм и создаёт условия для развития этой болезни. Исследования показали, что постоянное беспокойство изменяет активность иммунных клеток, отвечающих за включение механизма «бей и беги». В результате в крови постоянно циркулирует большое количество кортизола, моноцитов и нейтрофилов, которые отвечают за воспалительные процессы. А как уже упоминалось, хронические воспалительные процессы могут привести к образованию раковых клеток.СПАСИБО ЗА УДЕЛЕННОЕ ВРЕМЯ! ЕСЛИ ИНФОРМАЦИЯ БЫЛА НУЖНОЙ, ВЫ МОЖЕТЕ ОСТАВИТЬ ОТЗЫВ В КОММЕНТАРИЯХ В КОНЦЕ СТАТЬИ! БУДЕМ ВАМ БЛАГОДАРНЫ!
- С ответом
- С отметкой о просмотре
Поделитесь с друзьями:
propishevarenie.ru
