Роландическая детская эпилепсия – причины заболевания, симптомы и признаки, методы лечения, особенности проявления у детей
причины заболевания, симптомы и признаки, методы лечения, особенности проявления у детей
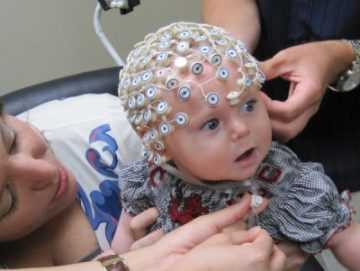
Роландическая эпилепсия (РЭ) относится к доброкачественному парциальному типу заболевания. Впервые характеристику патологии дал итальянский врач Л. Роланд.
Манифест болезни приходится на детский возраст от 3 до 13 лет. В 90% случаев недуг проходит по мере взросления.
Некоторые доктора склоняются к тому, что не необходимости лечить болезнь противосудорожными препаратами.
Суть патологии
Роландическая (височная) эпилепсия — это генетически обусловленное заболевание, связанное с гипервозбудимостью коры головного мозга в височной зоне.
Нейроны, находящиеся в этой области, производят нервные импульсы слишком часто, это приводит к возникновению эпиприступа.
Болезнь встречается в 15% из всех случаев эпилепсии, мальчики болеют в 1,5 раз чаще девочек. По МКБ 10 патология обозначается номером G40.9.
Лишь в очень редких случаях недуг трансформируется в другой тип эпилепсии и имеет неблагоприятный прогноз.
Причины болезни
 Точные причины возникновения роландической эпилепсии до сих пор не определены.
Точные причины возникновения роландической эпилепсии до сих пор не определены.
Врачи считают, что в основе развития РЭ лежит нарушение созревания мозговой коры в височной области.
Этому способствуют следующие обстоятельства:
- Наследственная предрасположенность. Наличие эпилепсии у родителей повышает вероятность развития болезни у ребенка.
- Внутриутробные аномалии развития головного мозга.
- Нейроинфекции (энцефалит, менингит).
- Травма головы.
- Неправильный режим дня с недостатком сна.
- Стресс.
По мере взросления ребенка нейроны мозга созревают, снижается их возбудимость, симптомы сходят на нет. Поэтому РЭ называется «возрастозависимой болезнью».
Зафиксированы случаи РЭ у взрослых как следствие заболеваний, перенесенных в детском возрасте. У малышей до 1 года болезнь не возникает.Клиническая картина и симптомы
Симптомы болезни возникают, в основном, в ночное время. Приступы носят парциальный характер, генерализованные припадки встречаются только у 20% заболевших.
Основные признаки роландического приступа:
- Появление ауры (предшественника приступа) в виде покалывания, онемения языка, губ.
- Судороги на одной половине лица.
- Выделение слюны.
- Закатывание глаз.
- «Булькающие» и «хрюкающие» звуки из горла.
- Заторможенность речи.
- Редко возникает рвота.
 Эти симптомы возникают ночью при засыпании или в конце сна.
Эти симптомы возникают ночью при засыпании или в конце сна.
Днем практически не встречаются. Припадки могут повторяться несколько раз за ночь с разной интенсивностью. Длительность приступа не превышает 5 минут.
В 20% развиваются генерализованные эпиприступы. Обычно они характерны для заболевания с ранним дебютом (до 3 лет).
Эти случаи имеют менее благоприятный прогноз и плохо поддаются лечению. У ребенка генерализованные припадки проявляются в следующем:
- Тонические судороги по всему телу.
- Мышечные спазмы.
- Потеря сознания.
- После окончания припадка ребенок не помнит, что с ним было, крепко засыпает, при пробуждении чувствует вялость и головную боль.
Таким образом, выделяют следующие особенности роландической эпилепсии:
- Нарастание эпилептической активности в фазе медленного сна.
- Появление предшественников приступа (ауры).
- Кратковременность приступов.
- Благоприятный исход болезни.
В медицине зафиксированы случаи (не более 5%) атипичного течения РЭ. У больных диагностирован эпилептический статус.
Приступы имели многократный ежедневный характер с потерей сознания и внезапными падениями больных. Однако, даже в этих случаях не отмечалось изменений в психическом развитии и поведении пациентов.Неврологический статус
 Неврологический статус больных РЭ изучен очень хорошо.
Неврологический статус больных РЭ изучен очень хорошо.
До недавнего времени считалось, что у таких пациентов нет органических поражений головного мозга.
Однако, при внедрении высокотехнологичных методов диагностики (МРТ, КТ) были выявлены случаи структурных изменений в мозге.
У 4% детей были диагностированы следующие патологии:
- ДЦП;
- задержка психического развития легкой формы;
- микроцефалия;
- мозжечковая недостаточность;
- нарушение речевого развития;
- синдром гиперактивности.
Наследственный фактор
Существует концепция влияния наследственного фактора на возникновение РЭ. Согласно проведенным исследованиям, около 70% заболевших имеют родственников, страдающих от разных форм эпилепсии.
При этом у родственников всех пациентов на ЭЭГ зафиксированы роландические спайки, а приступы возникали лишь у 40%.
Таким образом, РЭ относится к идиопатическому виду заболевания, наследуемому по доминантному признаку. Болезнь наследуется через поколения представителями одного пола.То есть, если болеет отец, то его дети будут здоровы, а внук, вероятно, унаследует патологию. Внучка же будет являться только субклиническим носителем гена эпилепсии.
Этот ген будет передаваться другим поколениям и невозможно предсказать, когда он себя проявит.
 Не у всех носителей данного гена в последствие разовьется эпилепсия.
Не у всех носителей данного гена в последствие разовьется эпилепсия.
Для активации болезни требуются сопутствующие условия в виде травмы, нейроинфекции, тяжелых родов.
Но почти у половины детей, больных РЭ, данные о провоцирующих факторах отсутствуют.
По этой причине исследования по выявлению генов, ответственных за возникновение эпилепсии, ведутся до сих пор.
Диагностика
Предварительный диагноз врач-эпилептолог ставит на основании жалоб ребенка и родителей. Основным и самым достоверным методом диагностики РЭ является электроэнцефаллография.
Она обнаруживает роландические спайки, фиксирует повышенную нейронную активность в лобно-височной доле головного мозга.
Поскольку приступы возникают в ночное время, это может осложнить диагностику. Поэтому дополнительно назначают ночную ЭЭГ (полисомнографию).Для дифференциации этого вида эпилепсии от других неврологических заболеваний (опухолей, кист) проводится МРТ или КТ головного мозга.
Лечение
До сих пор среди врачей не утихают споры по поводу необходимости лечения роландической эпилепсии противосудорожными препаратами.
Противники применения лекарств руководствуются возрастным характером болезни. В большинстве случаев болезнь проходит к 15-17 годам, не зависимо от приема препаратов.
Сторонники лекарственной терапии утверждают, что существует большая вероятность ошибочной постановки диагноза.
 Кроме того, есть риск перехода заболевания в атипичную или злокачественную форму.
Кроме того, есть риск перехода заболевания в атипичную или злокачественную форму.
Если приступы повторяются слишком часто, у ребенка развивается бессонница, что негативно сказывается на его психическом состоянии.
Поэтому противоэпилептические препараты обязательно назначаются при повторных приступах РЭ.
Первая помощь больному
Невыраженные эпиприступы часто остаются незамеченными родителями, так как возникают в ночное время.
При появлении судорог нужно приподнять ребенка, чтобы предотвратить западание языка и чтобы малыш не захлебнулся слюной.Больного следует уложить на мягкую поверзность, чтобы голова была чуть выше туловища. Нельзя сдерживать ребенка, фиксировать руки или ноги.
При длительном тяжелом приступе необходимо вызвать скорую.
Читайте о других формах эпилепсии:Особенности терапии у детей
Для лечния РЭ в детском возрасте используют монотерапию, то есть назначают только один из препаратов в минимальной дозировке. Обычно применяют препараты вальпроевой кислоты (Конвулекс, Конвульсофин). При отсутствии эффекта выписывают Топирамат или Кеппра.
Детям старше 7 лет при возникновении приступов только ночью, показан однократный прием Фенитоина в малых дозах перед сном. С помощью этого средства обычно достигается длительная ремиссия.
 Для лечения детей более старшего возраста в случаях генерализованных припадков назначается
Для лечения детей более старшего возраста в случаях генерализованных припадков назначается
Однако, следует быть осторожным с этим средством из-за большого количества побочных эффектов.
Барбитураты (Фенобарбитал) оказывают негативное влияние на интеллект ребенка, поэтому в терапии детской РЭ не используются.
Большинство врачей считают, что нецелесообразно использовать антиконвульсанты дольше двух лет. При раннем дебюте болезни терапия может быть продолжена до 10 лет.
Даже если на ЭЭГ фиксируется повышенная эпилептическая активность, но припадки не возвращаются длительное время, продолжать противосудорожную терапию не стоит.Прогноз
Роландическая эпилепсия отличается благоприятным прогнозом. У 95% детей приступы исчезают к 16 годам и больше не возвращаются.
Излечение зависит от возраста начала болезни и частоты припадков. Резистентность к терапии и ремиссия заболевания наблюдаются при раннем и позднем дебюте (младше 4 и старше 10 лет).
Вероятность рецидива во взрослом возрасте не превышает 4%. Это может произойти под влиянием экзогенных факторов: гормональной перестройки (беременность), стресса, тяжелой болезни или вследствие сохранения структурных изменений в мозге.
 Как таковой профилактики роландической эпилепсии не существует, принимая во внимание преимущественно наследственный характер возникновения.
Как таковой профилактики роландической эпилепсии не существует, принимая во внимание преимущественно наследственный характер возникновения.
РЭ относится к идиопатическим доброкачественным формам эпилепсии.
Дебют болезни приходится на детский возраст, у взрослых патология возникает очень редко.
Отличительной чертой недуга является возможность полного излечения по мере взросления пациента.
nerv.guru
Доброкачественная роландическая эпилепсия — причины, симптомы, диагностика и лечение
Общие сведения
В педиатрии доброкачественная роландическая эпилепсия является наиболее распространенной патологией из группы доброкачественных фокальных эпилепсий. На ее долю приходится 15% от всех случаев эпилепсии у детей в возрасте до 15 лет и около 20% случаев судорожного синдрома у детей. Доброкачественная роландическая эпилепсия встречается с частотой 21 случай на 100 тыс. детей. Доброкачественная роландическая эпилепсия может возникнуть в возрасте от 2 до 14 лет, но в 85% случаев она манифестирует в возрастном периоде от 4 до 10 лет. Доброкачественное течение классической роландической эпилепсии характеризуется отсутствием психо-неврологических изменений и полным исчезновением эпиприступов к 15-18 годам.
Доброкачественная роландическая эпилепсия
Причины возникновения доброкачественной роландической эпилепсии
Точные причины появления доброкачественной роландической эпилепсии пока не установлены. В некоторых случаях (по разным данным 20-60%) прослеживается наследственный характер заболевания, однако прямое аутосомно-рецессивное или аутосомно-доминантное наследование не наблюдается. Это послужило основанием для полигенной теории наследования доброкачественной роландической эпилепсии, согласно которой заболевание детерминируется двумя разными генами.
В современной неврологии и эпилептологии доминирующим является представление о том, что доброкачественная роландическая эпилепсия возникает вследствие нарушения созревания коры головного мозга в центрально-височной области. Доброкачественная роландическая эпилепсия является возраст-зависимым заболеванием и вероятно связана с повышенной возбудимостью мозга у детей. Последнее обусловлено целым рядом факторов: функциональными и структурными особенностями эпилептогенных областей (неокортекса, гиппокампа, амигдалы), превалированием возбуждающих нейротрансмиттеров, низким содержанием ГАМК, незрелостью ГАМК-рецепторов, увеличенным числом возбуждающих возвратных синапсов. По мере созревания головного мозга ребенка происходит снижение его возбудимости и постепенное исчезновение эпилептогенности очагов доброкачественной роландической эпилепсии. В результате наблюдается уменьшение числа эпилептических припадков и полное выздоровление пациентов при достижении ими пубертатного периода.
Симптомы доброкачественной роландической эпилепсии
Наиболее типичными для классической доброкачественной роландической эпилепсии являются простые парциальные эпиприступы, протекающие без утраты сознания. Как правило, приступу предшествует сенсорная аура в виде одностороннего чувства пощипывания, покалывания или онемения на лице, губах, деснах, языке и в глотке. Далее возникает моторный пароксизм, который может быть представлен как тоническими, так и клоническими мышечными сокращениями, а также их сочетанием. В зависимости от локализации судорог приступы доброкачественной роландической эпилепсии могут быть гемифациальными и фарингооральными. Гемифациальный приступ протекает с судорогами в мышцах половины лица. Фарингооральный приступ характеризуется односторонними судорогами в мышцах языка, губ, глотки и гортани. Он сопровождается гиперсаливацией и нарушением речи. Судорожные сокращения мышц гортани приводит к появлению характерных горловых звуков, напоминающих бульканье, полоскание горла или хрюканье. По мере развития доброкачественной роландической эпилепсии судорожные приступы могут «поменять» сторону.
80% эпиприступов, которыми сопровождается доброкачественная роландическая эпилепсия, возникают в ночное время и тесно связаны с периодами засыпания и пробуждения. Гораздо реже наблюдается сочетание ночных приступов с припадками, происходящими в дневное время. В 20% случаев доброкачественная роландическая эпилепсия протекает с брахиофациальными приступами, во время которых судороги лицевой области распространяются на гомолатеральную руку. В 8% случаев наблюдается вовлечение гомолатеральной нижней конечности. В некоторых случаях доброкачественная роландическая эпилепсия сопровождается сложными парциальными эпиприступами, для которых типична кратковременная потеря сознания. Примерно у 20% больных возникают вторично-генерализованные эпиприступы, во время которых судороги захватывают все мышцы тела. Такие приступы протекают с полной потерей сознания.
Течение доброкачественной роландической эпилепсии
Доброкачественная роландическая эпилепсия характеризуется малой продолжительностью эпиприступов (до 2-3 минут) и их небольшой частотой. Приступы бывают единичными или наблюдаются несколько раз в году. Иногда в начале заболевания приступы могут быть более частыми, однако по мере взросления ребенка наблюдается их урежение.
В отличие от эпилепсии, описанной Джексоном, классическая доброкачественная роландическая эпилепсия не сопровождается задержкой психо-моторного развития ребенка и не приводит к олигофрении. Однако нельзя сказать об абсолютном отсутствии неврологических нарушений, поскольку примерно у 3% больных после приступов возникает преходящий гемипарез.
Диагностика доброкачественной роландической эпилепсии
Основным способом диагностики доброкачественной роландической эпилепсии является ЭЭГ. Поскольку у некоторых больных изменения ЭЭГ наблюдаются лишь в период сна, при нормальной дневной ЭЭГ дополнительно необходимо проведение ночного ЭЭГ-мониторинга или полисомнографии.
Патогномоничным признаком доброкачественной роландической эпилепсии считается обнаружение на фоне нормальной основной активности высокоамплитудных острых волн или пиков, расположенных в центрально-височных отведениях. Зачастую после пика следуют медленные волны, вместе с пиком они составляют так называемый «роландический комплекс» длительностью до 30мс. Визуально такие комплексы напоминают комплексы QRST на электрокардиограмме. Обычно «роландические комплексы» локализуются на стороне, противоположной судорожным приступам, но могут иметь и двусторонний характер. К особенностям ЭЭГ-паттернов доброкачественной роландической эпилепсии относится их изменчивость от одной записи ЭЭГ к другой.
Дифференциальная диагностика доброкачественной роландической эпилепсии
В первую очередь доброкачественная роландическая эпилепсия нуждается в дифференцировке от симптоматических эпилепсий, возникающих при внутримозговых опухолях, черепно-мозговых травмах, воспалительных поражениях головного мозга (абсцессе, энцефалите, гнойном менингите). В подтверждение роландической эпилепсии говорит отсутствие патологических изменений в неврологическом статусе и расстройств поведения, сохранность интеллекта, анамнестические данные, нормальная основная активность на ЭЭГ. В некоторых случаях для уточнения диагноза проводится МРТ головного мозга.
Большие сложности представляет дифференциальная диагностика доброкачественной роландической эпилепсии и ночной эпилепсии со сложными парциальными эпиприступами. Это связано с тем, что типичные для приступа доброкачественной роландической эпилепсии нарушения речи могут интерпретироваться как нарушения сознания. С другой стороны достаточно трудно адекватно диагностировать ночные расстройства сознания. В таких случаях в постановке диагноза решающую роль играют данные ЭЭГ, которые при лобной и височной эпилепсии демонстрируют очаговые изменения активности головного мозга в соответствующих отведениях.
Определенные затруднения вызывает дифференцировка классической доброкачественной роландической эпилепсии от синдрома псевдоленнокса, который наблюдается у 5% больных с симптомами роландической эпилепсии. Сочетание типичных роландических эпиприступов с атипичными абсансами, миоклоническими и астеническими приступами, интеллектуально-мнестическими нарушениями, а также выявление на ЭЭГ диффузной пиковой активности или медленных комплексов, характерных для синдрома Леннокса — Гасто, свидетельствуют в пользу синдрома псевдоленнокса.
Лечение доброкачественной роландической эпилепсии
Для детских неврологов и эпилептологов вопрос целесообразности лечения доброкачественной роландической эпилепсии является весьма дискутабельным. Поскольку даже без проведения лечения доброкачественная роландическая эпилепсия заканчивается выздоровлением, то, по мнению некоторых авторов, она не является показанием к назначению антиэпилептической терапии. Другие неврологи, указывая на вероятность диагностической ошибки при постановке диагноза «доброкачественная роландическая эпилепсия» и учитывая возможность ее перехода в синдром псевдоленнокса, рекомендуют проводить антиэпилептическую терапию при повторных эпиприступах.
В лечении детей с доброкачественной роландической эпилепсией всегда используется только 1 противоэпилептический препарат (монотерапия). Лечение обычно начинают назначением одного из препаратов вальпроевой кислоты. При его непереносимости или неэффективности, как правило, переходят на прием топирамата или леветирацетама. У детей старше 7 лет возможно применение карбомазепина, однако следует помнить, что в некоторых случаях он может привести к феномену аггравации, т. е. к учащению приступов.
www.krasotaimedicina.ru
Роландическая эпилепсия, полезные статьи медицинской клиники Невро-Мед
К.Ю. Мухин, П.А. Темин, Е.А. Рыкова
Луиджо Роландо (1773-1831 г.), итальянский врач и анатом, дал классическое топографическое описание центральной борозды коры головного мозга. При идиопатической парциальной эпилепсии детского возраста, характеризующейся короткими гемифациальными моторными ночными приступами, часто с предшествующей соматосенсорной аурой и типичными изменениями ЭЭГ (полифазные спайки с локализацией в центральной и срединной височной областях) [14], эпилептогенной зоной являются нижние отделы роландической борозды. Изучение этой разновидности идиопатической парциальной эпилепсии начато более 40 лет назад. Первоначально были описаны специфические изменения ЭЭГ у определенной группы детей. В 1952 г. H.Gastaut [25] впервые обратил внимание на особые эпилептические изменения ЭЭГ у некоторых детей: полифазные спайки со строгой локализацией в перироландической области. Первое клиническое описание симптомов эпилепсии с роландическими спайками (1958 г.) принадлежит Р.Nayras и М.Веаussart [40]. В последующем Е.Gibbs и F.Gibbs [27], С.Lombroso [36], Р.Loisea и соавт. [35] провели клинический анализ симптомов при эпилепсии с роландическими спайками и предложили называть данную форму эпилепсии роландической. Авторы отметили ее благоприятный прогноз и отсутствие симптомов органического поражения центральной нервной системы.
Частота
Роландическая эпилепсия (РЭ) — одна из наиболее частых форм эпилепсии детского возраста. Распространенность ее составляет 21 на 100 тыс. здорового детского населения [29]. Частота РЭ среди всех форм эпилепсии с дебютом до 13 лет варьирует по разным данным от 11,5% [15] до 25% [5]. Из 360больных эпилепсией детей, наблюдавшихся Р.Lerman [34],у 14,4% была диагностирована роландическая эпилепсия. Для сравнения заметим, что одна из наиболее частых форм эпилепсии детского возраста — пикнолепсия — была диагностирована лишь у 10,5% пациентов. Не исключено, что истинная частота роландической эпилепсии в популяции значительно выше, так как у многих больных отмечаются единичные ночные приступы, часто остающиеся без внимания родителей и врачей [34].
Большинство авторов отмечают преобладание мальчиков среди больных роландической эпилепсии [3]. Соотношение мальчиков и девочек в среднем составляет 6:4 [11].Среди 100 бальных, наблюдавшихся Р.Lerman [34], было 62 мальчика и 38 девочек.
Клиника
Дебют роландической эпилепсии варьирует в возрастном интервале 2 — 14 лет. В 83% случаев РЭ дебютирует в возрасте 4 — 10 лет[5]. У подавляющего большинства пациентов приступы начинаются между 5-м и 10-м годом жизни с максимумом в возрасте 9 лет [9]. Средний возраст появления приступов — 9,9 года [33]. Начало заболевания в возрасте до 2 лет отмечается не чаще чем в 8% случаев [15]. Имеются единичные описания начала РЭ на 1-м году жизни [17], однако отнесение данных случаев к РЭ дискутируется [21].Начало заболевания после 11 лет также является редкостью, а после 14 лет такие случаи не наблюдаются [9].
Клиническая симптоматика приступов при роландической эпилепсии, как правило, типична. Наблюдаются простые парциальные (моторные, сенсорные, вегетативные), сложные парциальные (моторные) и вторично генерализованныс приступы. Наиболее типичны простые парциальные моторные и/или сенсорные пароксизмы [2].
Простые парциальные приступы составляют «ядро» роландической эпилепсии и наблюдаются у 70 — 80% больных. Наиболее типично начало приступа с соматосенсорной ауры: ощущение покалывания, онемения, «прохождения электрического тока» унилатерально в области глотки, языка, десны. Вслед за аурой развивается парциальный приступ. Возможны следующие варианты: гемифациальные приступы; унилатеральные тонические, клонические или тонико-клонические судороги мышц лица; фарингооральные приступы; унилатеральные судороги губы, языка, глотки, гортани, часто сочетающиеся с анартрией и гиперсаливацией. Гемифациальные приступы имеютместо у 37% больных, фарингооральные — у 53% [91. Часто во сне больные издают своеобразные горловыезвуки типа «бульканья», «хрюканья», «полоскания горла». Истинную частоту соматосенсорных приступов (щечная парестезия по терминологии J.Aicardi [5]) определить сложно, так как дети, особенно маленькие, затрудняются описать свои ощущения во время приступов.
У 20% больных судороги могут распространяться с мышц лица на гомолатеральную руку (брахиофациальные приступы) и примерно в 8%случаев вовлекать и ногу (унилатеральные приступы). По мере развития заболевания приступы могут менять сторонность. Вторично генерализованные судорожные приступы отмечаются у 20-25% больных роландической эпилепсии. Они наиболее характерны для младших детей, и возникновение генeрализованных приступов «жестко» приурочено ко сну. Наличие у пациентов длительное время только генерализованных судорожных приступов нехарактерно для РЭ, как и наличие абсансов, психомоторных приступов и приступов с психическими симптомами [5].
Продолжительность приступов при роландической эпилепсии, как правило, небольшая [5] от нескольких-секунд до 2-3мин. У 11% [16] — 22% [5] больных продолжительность пароксизмов превышает 10-15 мин, у 16% [5] отмечаются тяжелые продолжительные приступы ,заканчивающиеся постприступным гемипарезом (паралич Тодда). Частота приступов при РЭ обычно невысока — в среднем 2 в год [5]. В первые 1-2 года с момента дебюта заболевания приступы могут быть более частыми, однако с течением времени они возникают все реже. После 13-16 лет возможно полное исчезновение приступов. У 10-40% детей наблюдается единичный приступ за все время болезни, даже если они не получают антиконвульсантов [41].Еженедельные и более частые, ежедневные приступы наблюдаются лишь в 6% [35] — 20% [34] случаев. Серийные приступы и повторные в течение одной ночи редки и наблюдались в 3% случаев, описанных Т . Deonna и со авт.[17].
В редких публикациях [15,16,23,34] сообщается о развитии эпилептического статуса при РЭ. Часто та его при РЭ составляет около 11% [16]. Подробное описание эпилептического статуса у больных РЭ представлено в работе N . Fejerman и А.Di Blasi [23]. Авторы наблюдали 2 мальчиков 8 лет с дебютом РЭ в 3 года, у которых возник длительный статус гемифациальных приступов. Сознание было сохранено, однако констатировались анартрия и выраженное слюнотечение. Пероральное назначение антиконвульсантов в высоких дозах, как и парентеральное введение диазепама или лоразепама, не оказало влияния на эпилептический статус. Лишь назначение гормональных препаратов(дексаметазон) полностью купировало судороги.Вызывает сомнение, однако, отнесение данныхслучаев к роландической эпилепсии. У одного из этих пациентов наблюдались типичные абсансы, у другого -приступы с джексоновским маршем; у обоих приступы были резистeнтны к антиконвульсантам . Возможно, данные случаи представляют собой атипичную форму РЭ. Е.Roulet и соавт. [42] описал иэпилептический статус у мальчика 6 лет с роландической эпилепсии. Единственным его проявлением было длительное слюнотечение в сочетании с оролингвомоторной диспраксией. На ЭЭГ во время слюнотечения регистрировались спайк-волновые комплексы ,включая роландические. При увеличении дозы карбамазепина слюнотечение прекратилось. По мнению авторов, длительное перманентное слюнотечение у больных роландической эпилепсии может быть единственным симптомом эпилептического статуса.
Пароксизмы РЭ связаны с ритмом сон -бодрствование. Наиболее типичны ночные приступы ,возникающие преимущественно при засыпании и пробуждении. При ночных приступах пароксизмы возникают в период пробуждения (35%), реже — все редине ночи (25%) и при засыпании (20%). У 25-30%больных приступы наблюдаются как во сне, так и всостоянии бодрствования [5]. Лишь у 5-25% пациентов они возникают исключительно со время бодрствования [5,34]. Имеется некоторое различие картины приступов в зависимости от ритма сон — бодрствование. Дневные приступы практически всегда простые парциальные, чаще гемифациальные ,короткие, ночные, как правило, более тяжелые, продолжительные, обычно унилатеральные или вторично генерализованные. Провести оценку сознания у пациентов с ночными приступами сложно; феномен анартрии часто симулируетклинику выключения сознания. Сложные парциальные приступы при роландической эпилепсии редки и составляют лишь около 5% всех случаев [15]. Возможно, на протяжении приступа у некоторых больных имеет место «флюктуация» уровня нарушения со знания.
J.Aicatdi и J.Сhevrie [4] была выделена группа больных сосвоеобразным эпилептическим синдромом ,клиническая симптоматика которого была схожа с роландической эпилепсией. У больных отмечались простые парциальные гемифациальные и гемиклонические приступы,однако в сочетании с миоклонически-астатическими, атоническими приступами и в ряде случаев с абсансами. Данная группа наблюдений классифицирована какатипичный вариант РЭ. Частота его, согласно Т.Deonnaи соавт. [16], составляет 5% среди всех больных РЭ.Таксономическое положение данного синдрома спорно. По мнению J.Aicatdi и J.Сhevrie [5], данная форма эпилепсии является нозологически самостоятельным синдромом с четко очерченными клиникой, изменениями ЭЭГ и прогнозом. Другие авторы предполагают наличие атипичного варианта в рамках РЭ [17]. Подробное описание данного синдрома представлено Т.Deonna и соавт. [16] на примере 6 пациентов. Среди обследованных больных преобладали мальчики. Приступы дебютировали в возрастном интервале от 2 до 7 лет у неврологически нормальных детей с сохранным интеллектом. Клинические симптомы включали различные виды приступов. Характерными были ночные простые парциальные приступы, подобные таковым при РЭ, миоклонически-астатические и атонические приступы. У ряда больных отмечались атипичные абсансы. Приступы во всех случаях были частыми, ежедневными и приводили к многократным падениям пациентов и тяжелым ушибам. На ЭЭГ типичные роландические спайки сочетались с медленными комплексами пик-волна, характерными для синдрома Леннокса — Гасто. Отмечалось нарастание эпилептической активности в фазе медленного сна.
Клиническая симптоматика атипичной роландической эпилепсии носит черты целого ряда эпилептических синдромов: РЭ (простые парциальные ночные приступы в сочетаниис типичными роландическими спайками), синдрома Леннокса — Гасто (частые атонически-астатические приступы, атипичные абсансы в сочетании с медленными комплексами пик-волна) и эпилепсии смиоклонически-астатическими приступами,описанной Н.Doose [19]. Однако кардинальным отличием атипичной роландической эпилепсии от синдрома Леннокса — Гасто и эпилепсии с миоклоничeски-астатическими приступами являются отсутствие у пациентов нарушений интеллекта и хороший прогноз. Р.Loisea и соавт. [35] провели катамнестическое исследование13 пациентов с атипичной РЭ в течение не менее 9лет. Спустя разный промежуток времени во всех случаях была достигнута полная ремиссия, при этом большая часть пациентов (10) не применяли регулярной противоэпилептической терапии. Авторы не отметили ни отставания в психическом развитии, ни серьезных нарушений поведения как в наиболее активный период заболевания, так и в период ремиссии, что сближает данные случаи с типичной РЭ. По мнению авторов, при данном синдроме следует избегать «агрессивной» противоэпилептической терапии ввиду хорошего прогноза.
O.Dulac и соавт. [21] проанализировали случаи парциальной эпилепсии с ранним дебютом — между 8днями и 3 годами жизни. Среди 442 больных выявлено 17с парциальной эпилепсией с ранним дебютом .Приступы характеризовались как простые парциальные с частой вторичной генерализацией. По мнению авторов, данные случаи являются переходной формой между доброкачественной эпилепсией новорожденных и РЭ. В отличие от двух указанных синдромов прогноз был неблагоприятными приступы не поддавались медикаментозной терапии. Последующие исследования покажут, являются ли случаи парциальной эпилепсии с дебютом в первые 3 года жизни нозологически самостоятельным синдромом или еще одним» атипичным вариантом» РЭ.
Неврологический статус
Неврологический статус у детей, страдающих роландической эпилепсии, изучен достаточно подробно. Роландическая эпилепсия относится к идиопатическим формам эпилепсии, при которых отсутствуют признаки органического поражения головного мозга, что подтверждается большинством публикаций. Более того, по мнению А. Веаumanoir и соавт. [8] наличие таких симптомов противоречит критериям диагноза роландической эпилепсии. Однако в последние годы благодаря внедрению в клиническую практику высокоэффективных нейрорадиологических методов исследования(компьютерная томография, ядерно-магнитный резонанс, позитронная эмиссионная томография) появились единичные сообщения об обнаружении структурных изменений в головном мозге у больных РЭ.
Из 100 больных, наблюдавшихся Р.Lerman и S.Kivity [33], у 4 констатированы симптомы органического поражения центральной нервной системы: детский церебральный паралич (гемипаретическая и тетраплегическая формы), микроцефалия, умеренная задержка умственного развития. Во всех этих случаях диагноз РЭ не вызывал сомнения и был подтвержден как клинически, так и нейрофизиологически. Пневмоэнцефалография не выявила нарушений у данных больных. S.Blom и J.Heijbet [11]в 3 (7,5%) из 40 случаев РЭ обнаружили у больных центральный гемипарез. E.Roulet и соавт. [42] отметили проявления оролингвомоторной диспраксии у больного РЭ. Такие симптомы, как микроцефалия, косоглазие, мозжечковая недостаточность, задержка психического и речевого развития, констатировали у ряда больных РЭ Р.Santanelli и соавт.[43]. Синдром гиперактивности был обнаружен у 16,7%больных РЭ [34].
Генетика
Р.Вrау и W.Wiser [13] первыми констатировали наличие семейных случаев роландической эпилепсии и предположили аутосомно-доминантную модель наследования с неполной пенетрантностью и возрастной зависимостью. В последние десятилетия проведены многочисленные клинико-генеалогические исследования при роландической эпилепсии, подтверждающие правомерность данной концепции. Согласно обобщенным данным литературы, 8,9% [35] — 68% [29]больных РЭ имеют родственников, страдающих эпилепсией или имеющих приступы в анамнезе, и до 30% [13] — родственников с наличием на ЭЭГ роландических спайков при отсутствии приступов. Частота обнаружения спайков у сибсов пробандов и детей, родители которых страдали РЭ, составляет25-36% (в популяции здорового населения — 1,4-5% [З7]).Однако лишь у малой части из них (12% в исследовании Р.Вrау и W.Wiser [13]) отмечались приступы: остальные были клинически здоровы. Характер приступов у родственников больных роландической эпилепсии может быть различным. Типичные приступы, характерные для РЭ, констатируются у 13%родственников, абсансная эпилепсия — у 10%, гснсрализованные судорожные приступы — у 3%,фокальная эпилепсия — у 1% [9].
В ряде исследований изучена конкордантность монозиготных близнецов по РЭ. Обнаружена высочайшая конкордантность по наличию на ЭЭГ роландических спайков, но не по развитию самой РЭ. T.Kajitani и соавт. [30] изучили 3 пары монозиготных близнецов в возрасте 5-11 лет, в которых один из сибсов страдал РЭ. Во всех случаях констатирована типичная роландическая эпилептическая активность на ЭЭГ, но ни у одного из здоровых сибсов не было никаких проявлений РЭ.
В последние годы была выдвинута гипотеза о мультифакторном наследовании роландической эпилепсии [29]. Она основывается на том факте, что лишь у небольшой части детей, имеющих на ЭЭГ роландические спайки, в дальнейшем развивается РЭ. Предполагается, что роландические спайки и развитие РЭ детерминированы двумя различными, но сцепленными генами. В 1982 г. O.Eeg-Olofsson и соавт. [22] обнаружили, что у родителей, сибсов и других родственников детей, больных РЭ, низкая встречаемость гаплотипа А1В8 антигенов лейкоцитарной гистосовместимости. Частота его в общей популяции крайне высока [22]- Возможно, что данный гаплотип играет роль протектора или ингибирующего фактора, препятствующего развитию РЭ.
Интересны исследования, раскрывающие взаимосвязь РЭ с фебрильными судорогами. E.Frantzen и соавт. [24] сообщили, что у 20% детей с фебрильными судорогами в дальнейшем на ЭЭГ появляется фокальная эпилептическая активность, идентичная роландическим спайкам. Ни у одного из этих пациентов не отмечалось в дальнейшем эпилептических приступов. Исследования на монозиготных близнецах также показали возможное генетическое сцепление между РЭ и фебрильными судорогами. M.Lennox-Buchthul [32] изучила 24 пары монозиготных близнецов, в которых по крайней мере у 1 из пары имелись фебрильные судороги, и выявила, что 20% их сибсов имели редкие ночные приступы. У 2 из 24 обнаружено сочетание ночных приступов с фебрильными судорогами. К сожалению, автор не идентифицировала данные ночные приступы, однако по характеру их течения и возрасту дебюта можно предположить, что это случаи РЭ. В исследовании T.Kajitani и соавт. [31] среди 3 пар монозиготных близнецов 3 имели РЭ и 5 — фебрильные судороги. Данные работы могут свидетельствовать о генетическом сцеплении РЭ и фебрильных судорог. Подтверждением этой гипотезы служит и клиническая схожесть двух данных синдромов: высокая генетическая детерминированность, «жесткий» возрастзависимый дебют, доброкачественный прогноз [1] .
Остается неясной роль экзогенных, средовых факторов в развитии роландической эпилепсии. H.Doose и W.Baier [18] предположили, что генетические факторы при РЭ детерминируют низкий порог судорожной готовности головного мозга. При этом здоровых детей, имеющих на ЭЭГ роландические спайки, они расценили как субклинических носителей с низким судорожным порогом. По мнению авторов, воздействие различных экзогенных факторов в онтогенезе, а также сцепление с другими генами может способствовать у таких пациентов клинической манифестации заболевания и оказывать некоторое влияние на его течение. Т.Каjitani и соавт. [30] описали 3 родных сибсов, у каждого из которых на ЭЭГ имелись типичные роландические спайки. У одного из сибсов РЭ дебютировала в 4 года во время лихорадочного заболевания, у другого отмечался единственный приступ в возрасте 10 лет при просмотре телепередач, третий миновал «критический период» для дебюта и был здоров. Данное наблюдение иллюстрирует полиморфизм клинических проявлений заболевания, что может зависеть от различных экзогенных воздействий.
Факторами, трансформирующими субклиническое носительство в РЭ, могут быть патология беременности и родов, травмы головы, нейроинфекции и пр. [5]. Однако более чем у половины детей, страдающих РЭ, указание на наличие данных факторов в анамнезе отсутствует[15].
Электроэнцефалография
Необходимым исследованием для объективизации диагноза РЭ является электроэнцефалография [14].На ЭЭГ в межприступном периоде при РЭ обнаруживаются характерные, типичные «роландические» или «центровисочные» комплексы при обязательно сохранной основной активности. Эти комплексы представляют собой медленные дифазные высокоамплитудные пики или острые волны (100 — 300 мВ), нередко с последующими медленными волнами, общей продолжительностью около 30 мс (см. рисунок). Они имеют тенденцию к возникновению группами. Данные комплексы напоминают зубцы QRST ЭКГ. Роландические комплексы «жестко» локализованы: центральная и центровисочная области. Роландические комплексы могут наблюдаться как унилатерально (обычно контралатерально гемифациальным приступам) — 60% больных, так и билатерально — 40% [29].Эпилептические комплексы, как правило, независимы друг от друга, лишь в редких случаях наблюдается их билатерально-синхронное распространение с амплитудным преобладанием с одной стороны [26,34].
D.Gregory и Р.Wong [28] провели изучение точной локализации роландических спайков, используя метод компьютеризированного топографического картирования. Авторы обнаружили, что максимум «позитивности» электрического диполя при РЭ находится в центрально-височной области, а максимум «негативности» — в лобной. Предположено, что специфические ЭЭГ-паттерны при РЭ исходят из зоны, расположенной в нижних отделах роландической борозды, на границе с сильвиевой бороздой. Типичной особенностью изменений ЭЭГ при РЭ является нестойкость паттернов, их вариабельность от одной записи к другой. Роландические спайки могут исчезать, а затем появляться вновь, менять стройность, конфигурацию даже при двух последующих записях ЭЭГ через короткий промежуток времени. Нестойкость ЭЭГ-паттернов при РЭ свидетельствует, по мнению J.Aicardi [5], об отсутствии органических изменений в головном мозге при РЭ. В связи с этим отсутствие роландических спайков при однократном злектроэнцефалографическом исследовании не может считаться убедительным аргументом для исключения диагноза РЭ при наличии типичной картины приступов [15]. Крайне важным для подтверждения диагноза РЭ является исследование ЭЭГ во время сна. Около 30% детей, страдающих РЭ, имеют роландические спайки исключительно во время сна [29]. Во время дремоты и на всех стадиях сна отмечается тенденция к переходу унилатеральных роландических комплексов в билатеральные [34].
Интересной находкой при РЭ является обнаружение на ЭЭГ наряду с типичными роландическими комплексами и других эпилептических паттернов. От 10 до 20% детей с РЭ имеют на ЭЭГ пик-волновые комплексы в других зонах коры, главным образом в затылочной области [41]. Морфология «затылочных комплексов «близка к роландическим и к наблюдаемым при доброкачественной фокальной эпилепсии с затылочными пароксизмами [10]. По мнению J.Aicardi [5],частота «затылочных комплексов» при Рэо братно пропорциональна возрасту ребенка и является нередкой у больных до 3 лет жизни. От 7% [34]до 20% [5] пациентов с РЭ демонстрируют на ЭЭГ типичную генерализованную пик-волновую активность с частотой 3-4 Гц, нередко возникающую при гипервентиляции. У отдельных больных возможно появление медленных пик-волновых комплексов. Большинство авторов придерживаются однозначного мнения об отсутствии корреляции между частотой и выраженностью пик- волновыхкомплексов на ЭЭГ и особенностями течения заболевания.
Исследование ЭЭГ во время приступа представляется довольно сложным ввиду низкой частоты приступов при РЭ. B.Dalla-Bernardina и соавт. [15]описали во время ночного приступа появление на ЭЭГ низкоамплитудной быстрой активности в центрально-височной области, переходящей в роландические комплексы с распространением на всю гемисферу и с последующим охватом всего полушария.
Нейрорадиологическое исследование
Сведения о нeйрорадиологическом исследовании у больных РЭ единичны. H.Gastaut [25] одним из первых изучил данные компьютерной томографии у 15 больных РЭ и не нашел патологических изменений ни в одном случае. В последующем при нейрорадиологическом исследовании у больных РЭ были обнаружены некоторые структурные изменения в головном мозге: расширение сильвиевой щели, наличие полости прозрачной перегородки (2 из 13случаев) [39], вентрикуломегалия, арахноидальные кисты (3 из 17 случаев) [38]. Р.Santanelli и соавт. [43] представили подробное клиническое и нейрорадиологическое описание 3 случаев РЭ, сочетающейся со структурными изменениями головного мозга. У одного больного была выявлена липома мозолистого тела, у другого (соспондилоторакальной дисплазией) — агенезия мозолистого тела с вентрикуломегалией, у третьего — множество церебральных, преимущественно перивентрикулярных, кальцификатов (врожденный токсоплазмоз). У всех этих больных наблюдались типичная клиническая картина РЭ и роландические спайки на ЭЭГ.
Обнаруженные при нейрорадиологическом исследовании у единичных больных РЭ органические симптомы поражения головного мозга трудно интерпретировать однозначно. Не исключено, что эти нарушения не имеют непосредственной причинно-следственной связи с РЭ и могут быть вызваны сочетанием РЭ с другими заболеваниями — детским церебральным параличом, микроцефалией, токсоплазмозом, эктомезодермальными дисплазиями. Как и в популяции в целом, у больных РЭ могут наблюдаться перинатальное поражение центральной нервной системы, постнатальные черепно-мозговые травмы. Частота перинатальных поражений центральной нервной системы среди больных РЭ составляет 6% [16]- 13% [34], сотрясения головного мозга — 4 — 5% [34], что не превышает статистических данных в популяции здоровых детей. Принципиально важный и до конца не решенный вопрос — влияют ли данные экзогенные факторы на возникновение и течение РЭ. По мнению J.Aicardi [5], нарушения, обнаруженные в головном мозге у больных РЭ, не могут быть причиной эпилепсии, а являются случайными находками. С другой стороны, нельзя игнорировать тот факт, что у ряда больных РЭ структурные изменения с головном мозге локализуются в нижних отделах роландической борозды [43], а это не исключает полностью возможность существования «симптоматической» формы эпилепсии.
Лечение
За последние годы в лечении РЭ апробирован целый ряд противоэпилептических препаратов. Большинство авторов рекомендуют применять препараты, преимущественно воздействующие на парциальные формы эпилепсии: карбамазепин (финлепсин, тегретол) и дифенин (фенитоин). При лечении РЭ необходимо избегать политерапии, а также на значения противосудорожных препаратов в высоких дозах. Доброкачественное течение РЭ, отсутствие интеллектуально-мнестических нарушений у пациентов не дают оснований рекомендовать «агрессивную» антиконвульсантную политерапию для лечения данной формы эпилепсии ввиду возможности развития тяжелых побочных эффектов.
По мнению P.Lerman [34], а также В. Dalla-Bermardina и соавт.[15], одним из препаратов выбора влечении РЭ является фенитоин в низких и средних дозах. При возникновении приступов исключительно в ночное время или в период пробуждения рекомендован однократный прием фенитоина на ночь. Во всех наблюдавшихся авторами случаях применение средних терапевтических доз фенитоина приводило к полной клинической ремиссии приступов. Согласно данным P.Lerman и S.Kivity [33], эффективность фенитоина в лечении РЭ превышает таковую карбамазепина и фенобарбитала.
Карбамазепин также высокоэффективен в лечении РЭ [41] и отличается от дифенина минимальной выраженностью побочных эффектов терапии.
Сультиам (осполот) эффективен и хорошо переносится больными РЭ [19]. Применение барбитуратов (фенобарбитал, бензонал) лимитировано частым и тяжелым побочным влиянием на интеллектуально-мнестическис функции и поведение детей [5] и не может быть рекомендовано для лечения РЭ.
В последние годы появились публикации, свидетельствующие об эффективности препаратов вальпроевой кислоты (депакин, конувулекс) при РЭ[6,15,29]. Важной особенностью их является позитивное влияние на интеллектуально-мнестические функции пациентов и хорошая переносимость [12]. Однако, катамнестические исследования эффективности применения вальпроатов при РЭ отсутствуют.
Большинство авторов считают, что продолжительность применения антиконвульсантов при РЭ не должна превышать 2 лет с момента последнего приступа [35]. В среднем продолжительность медикаментозного лечения при РЭ составляет 3,2 года [33]. Однако в случае раннего дебюта приступов (2-3 года) лечение должно быть продолжено до 10-летнего возраста, независимо от длительности ремиссии [4]. Лечение рекомендуется назначать только после повторного приступа. Сохранение на ЭЭГ типичной эпилептической активности не может являться причиной продолжения антиконвульсантной терапии, если у больного имеется длительная ремиссия.
Прогноз
Особенностью РЭ является хороший прогноз заболевания [20]. По данным P.Loisea и соавт. [35], после 13лет приступы РЭ исчезли у 93,5% из 168 обследованных больных, а после 16 лет — у 98,8%. P.Loisea и соавт. [35] подробно исследовали влияние отдельных клинических симптомов РЭ на прогноз заболевания. В качестве возможных факторов, влияющих на прогноз, были проанализированы пол пациентов, возраст дебюта эпилепсии, частота и характер приступов, их суточное распределение, особенности неврологического статуса. У всех 168 пациентов с РЭ прослежен катамнез в течение не менее 4 лет с момента последнего приступа. Выделены факторы, влияющие на прогноз РЭ: возраст дебюта и частота приступов. Обнаружено, что лишь возраст дебюта эпилепсии статистически достоверно коррелирует с прогнозом РЭ. Установлено, что продолжительность заболевания и резистентность к терапии увеличиваются при раннем (до 4 лет) и позднем (после 10 лет) дебюте эпилепсии. Все остальные факторы существенно не влияют на прогноз РЭ.
Длительное наблюдение больных в катамнезе обнаружило возможность рецидивов приступов при РЭ после продолжительной ремиссии. Частота рецидивов приступов во взрослом возрасте при РЭ невысока — от 1,8% [35] до 4% [34]. Рецидив приступов чаще наблюдается у женщин в период гормональной перестройки, через 3 — 10 лет с момента наступления ремиссии, и не связан с приемом антиконвульсантов [35]. В большинстве случаев появляются генерализованные судорожные приступы, единичные или редкие. Важной особенностью является отсутствие на ЭЭГ типичных роландических спайков; по мнению P.Loisea и соавт. [35], ЭЭГ у данных пациентов обычно в пределах нормы.
Учитывая генерализованный характер приступов, появление их спустя длительное время после наступления ремиссии, отсутствие роландических спайков на ЭЭГ, P.Lerman [34] предположил, что данные случаи не имеют отношения к РЭ и представляют собой возникновение эпилепсии de novo. Противоречит данной концепции тот факт, что частота рецидивов при РЭ (2-4%) значительно превышает популяционную частоту эпилепсии (0,8%). Возможно, в возникновении приступов во взрослом возрасте при РЭ играет роль взаимодействие экзогенных факторов с генетически детерминированным снижением порога судорожной готовности. Одним из «разрешающих» факторов может явиться нарушение гормонального баланса в организме.
Другой возможной причиной рецидивов приступов может быть существование стойких структурных изменений в головном мозге с локализацией в нижних отделах роландической или сильвиевой борозды. G.Ambrosetto и соавт. [6] описали рецидив типичных «роландических» приступов у больного в возрасте 21 года. Пациент страдал РЭ с 10 лет: ночные простые парциальные и вторичногенерализованные приступы. С 13 лет наступила ремиссия, с 16 детой прекратил прием антиконвульсантов. В 21 год без видимой причины у больного развились точно такие же парциальные и вторично генерализованные приступы в ночное время с частотой 1-4 в месяц. При компьютернойтомографии патологии не выявлено. На ЭЭГ в 21 год ив 30 лет (в динамике) — правосторонний фокустипичной роландической активности. Уникальностьданного наблюдения состоит в том, что у больного РЭ приступы вновь возникли спустя 8 лет после наступления ремиссии и носили типичный для РЭ характер, являясь, однако, резистентными к антиконвульсантам. По мнению авторов, в данном случае имеется высокая вероятность наличия у больного структурных изменений в роландической области, что может быть выявлено при более тщательном нейрорадиологическом обследовании (ядерно-магнитный резонанс, позитронная эмиссионная томография).
Дальнейшие исследования покажут соотношение генетических и экзогенных факторов в детерминации РЭ и возможность существования «симптоматических» форм РЭ, обусловленных структурными изменениями, локализованными в роландической области. Необходимо также проведение молекулярно-генетических исследований с целью поиска генов, ответственных за развитие РЭ. Это позволит определить взаимосвязь РЭ с другими формами идиопатической эпилепсии, такими как доброкачественная затылочная эпилепсия Гасто, детская абсанс-эпилепсия и др.
ЛИТЕРАТУРА
I. Бадалян Л.О., Темин П.А., Мухин К.Ю. Фебрильныесудороги. Методические рекомендации. М. 1987; 24.
2. Карлов В.А. Эпилепсия. М. 1990; 219 — 223.
3. Сараджишвили П.М., Геладзе Т.Ш. Там же 1977, 148 — 149.
4. Aicardi .J., Chevrie J.-J. Dev Med Child Neurol 1982, 24: 281 — 292.
5. Aicardi J. Epilepsy in children 1986; 4.
6. Ambrosetto G., Tenuper P., Baruzzi A. J Neural Neurosurg Psychiat 1985; 48: 90.
7. Bancaund J., Collomb D., Dell M.B. Rev Neurol 1958; 99: 206 — 209.
8. Beaumanoir A., BallisT.,Varfis G., Ansai K. Epilepsia l974; 15: 301 — 315.
9. Beaussart M., Favou R. Ibid 1978; 19: 337 — 342.
10. Beydoun A»index.html» Garofalo E.A»index.html» Drury I. Ibid 1992; 33: 1091 — 1096.
11. Blom S., Heijbel J. Ibid 1982: 23: 629 — 631.
12. Bourgeois B.F.D. Ibid 1994. 35: 2: 18 — 23.
13. Bray P.P., Wiser W.C. Pediatrics 1965; 36: 207 — 211.
14. Comissionon Classification and Terminology of the ILAE. Epilepsia 1989; 30: 389 -399.
15. Dalla-Bermardina В., Sgro V., Fontana E. Epileptic syndromes in infancy, childhoodand adolescence. Paris 1992; 173 — 186.
16. DeonnaTh., ZieglevA-L., Despland P.-A. Neuropediatrics 1986; 17: 144 — 151.
17. Deonna Th., Zieglev A.-L., Despland P.-A. Guyvan Меllе. Epilepsia 1986; 27: 241- 247.
18. Doose Н., Baier W.K. Еuгор J Pediatr 1989; 149: 152 — 158.
19. Doose H. Epileptic syndromes in enfancy, childhood and adolescence. Paris 1992; 103- 114.
20. Dreifuss F.E. Epilepsia 1994; 35: 2: 30 — 34.
21. Dulac O., Cusmai R., Olivera K.de. Ibid 1989; 30: 798 — 801.
22. Eeg-Olofsson O., Safwenbery J., Wigrtz A. Ibid 1982; 23: 27 — 34.
23. Fejerman N., Di Blasi A.M. Ibid 1987; 28: 351 — 355.
24. Frantzen E., Lennox-Buchthal M., Nygaakt A. Electroen-cephalogr Clin Neurophysiol1968; 24: 197 — 212.
25. Gastaut H. Rev Neurol 1952; 87: 488 — 490.
26. Gastaut H., Gastaut J.L. Epilepsia 1976; 17: 325 — 326.
27. Gibbs E.L., Gibbs F.A. Ibid 1960; 1: 448 — 453.
28. Gregory D.L., Wong P.K. Ibid 1984, 25: 705 — 711.
29. Heijbel J. Pediatric Epilepsy. Helsinky 1989.
30. Kajitani Т., Nakaltmra M., Llcaka K., Kobuchi S. Advances in Epileptology 1980; 4:171 — 175.
31. Kajitani Т., Kimura Т., Sumita M., Kaneco M. Brain Dev 1992; 14: 230 — 234.
32. Lennox-Buchthul M. Epilepsia 1971, 12: 197 — 212. 33. Lerman P., Kivity S. ArchNeural 1975; 32: 261 — 264.
34. Lerman P. Epileptic syndromes in infancy, childhood and adolescence. Paris 1992;173 — 186.
35. Loisea P., Duche В., Cordova S. et al. Epilepsia 1988; 29: 229 — 235.
36. Lombroso C.T. Arch Neurol 1967; 17: 52 — 59.
37. Luders Н.O., Lesser R.P., Dinner D.S., Morris H.H. Epilepsy — electroclinicalsyndromes. Berlin 1987; 303 — 346.
38. Mambelli M., Moscano F., Maroni P. et al. Bulll. Liga Int. Epilepsy 1985; 51/52: 79- 80.
39. Morikawa Т., Osawa Т., Ishihara O., Seino M. Brain Dev 1979; 1: 303 — 346.
40. Nayrac P., Beaussart M. Rev Neurol 1958; 99: 201 — 206.
41. Panayiotopoulos С.Р. J Neurol Neurosurg Psychiat 1993; 56: 2 — 5.
42. Roulet E., Deonna Th., Despland P.A. Epilepsia 1989; 30. 564 — 568.
43. Santanelli P., Вureau M., Magaudda A. et al. Ibid 1989; 30: 182 — 188.
www.nevromed.ru
Доброкачественная детская эпилепсия (роландическая эпилепсия)
Русский Медицинский Сервер / Лечение эпилепсии / Доброкачественная детская эпилепсия (роландическая эпилепсия)
Доброкачественная детская эпилепсия — одна из форм эпилепсии. Характерной особенностью этой формы болезни является то, что судороги затрагивают лицо и иногда тело. Другое название этого вида эпилепсии — доброкачественная эпилепсия с центрально-височными пиками. Термин «доброкачественная» в названии заболевания указывает на благоприятный прогноз течения этой формы эпилепсии, так как у большинства пациентов заболевание проходит подростковом возрасте.
Термин «роландическая» в названии этой болезни указывает на то, что эпилептический очаг возникает в роландовой области головного мозга. Подобные приступы относятся к парциальным, так как их природа связана только с данной областью головного мозга.
Кто страдает доброкачественной роландической эпилепсией?
Доброкачественная роландическая эпилепсия встречается у 15% детей, страдающих эпилепсией. В среднем, первые приступы роландической эпилепсии встречаются в возрасте от 6 до 8 лет. У взрослых данная форма эпилепсии не встречается.
Какова причина доброкачественной роландической эпилепсии?
Причины возникновения роландической эпилепсии неизвестны. У детей, чьи близкие родственники страдают эпилепсией, риск развития роландической эпилепсии чуть выше.
Проявления доброкачественной роландической эпилепсии
Как и все формы эпилепсии, для доброкачественной роландической эпилепсии характерны приступы. Обычно они носят умеренный характер. Чаще всего при этом затрагивается лицо:
- Подергивание лица или щеки
- Покалывание или необычные ощущения в области лица или языка
- Затруднение речи
- Слюнотечение ввиду нарушения контроля мышц рта
Примерно у каждого второго ребенка с доброкачественной роландической эпилепсией патологический очаг с роландической области переходит на остальные области мозга. В таком случае говорят о вторично генерализованных приступах. Они также называются тонико-клоническими. Проявление этих судорог следующее:
- Пациент застывает, не отвечает на вопросы
- Сжимание мышц всего тела на короткий период
- Ритмические судороги всего тела
- Спутанность и дезориентация после того, как сознание вернулось
Обычно при доброкачественной роландической эпилепсии приступы начинаются во время сна. Поэтому они могут оставаться незамеченными другими. Часто родители узнают о приступе эпилепсии из-за ночного шума в комнате ребенка.
У некоторых детей с доброкачественной роландической эпилепсией могут также отмечаться затруднения в обучаемости и нарушения в поведении. Таким детям требуется дополнительное внимание и лечение. Однако, в большинстве случаев дети хорошо справляются со школьными заданиями.
Диагностика доброкачественной роландической эпилепсии
При легкой степени проявлений приступов, и если они появляются только в ночное время, диагноз доброкачественной роландической эпилепсии может быть легко нераспознан. Зачастую родители приводят ребенка к врачу после тонико-клонических судорог во время сна.
Диагностика доброкачественной роландической эпилепсии основана на типе приступов. Также применяются инструментальные методы исследований: ЭЭГ, МРТ, неврологические тесты.
Лечение доброкачественной роландической эпилепсии
Зачастую при доброкачественной роландической эпилепсии не требуется никакого лечения. Приступы при этой форме болезни обычно легкие и нечастые. Фактически, ребенок может сам вырасти из болезни.
Лечение может назначаться в случае, если доброкачественная роландическая эпилепсия сопровождается затруднением учебы в школе, нарушениями мышления или внимания, поведенческими расстройствами, дневными приступами или частыми судорогами. Лечение обычно медикаментозное.
Чаще всего приступы данной формы эпилепсии контролируются такими противоэпилептическими препаратами, как карбамазепин, ламотриджин или вальпроат натрия. Их принимают ежедневно, а курс лечения длится в среднем два года.
+7 (925) 50 254 50 – Лечение эпилепсии
ЗАПРОС в КЛИНИКУ
www.rusmedserv.com
Роландическая эпилепсия у детей
Эпилепсия – патологическое состояние, сопровождаемое единичными или повторными приступами. Структура болезни разнообразна. Существует целый ряд форм, выделяемых в отдельные заболевания, имеющие свое место в классификации.
Что такое роландическая эпилепсия?
Само название «роландическая эпилепсия» (РЭ) говорит о том, что очаг патологической импульсации формируется в области роландовой борозды, отделяющей лобные доли больших полушарий от теменных. Симптомы появляются на стороне, противоположной очагу. Это один из типичных эписиндромов детского возраста. К счастью, эта форма болезни является доброкачественной и к окончанию подросткового периода ребенок обычно перерастает эти состояния. РЭ составляет приблизительно шестую часть всех детских эпилепсий. Взрослые не подвержены этому заболеванию.
Симптомы и признаки роландической эпилепсии у детей

Приступы появляются в разном возрасте, обычно в промежутке от 3 до 12 лет, но чаще в 7 – 8 лет. Приступы редкие, обычно 1 – 2 раза в год. Бывает, что у ребенка регистрируется один эпиприпадок в жизни.
Типичный роландический приступ имеет некоторые особенности, позволяющие без труда поставить предварительный диагноз:
- Приступу предшествует своеобразная чувствительная аура. Внезапно в области лица с одной стороны появляются ощущения онемения, покалывания или ползания мурашек на щеке, во рту или языке.
- После ауры развивается типичный приступ: судорожные подергивания в тех же участках тела, где ощущались предвестники. Родители замечают перекос рта, из которого сочится слюна.
- Припадки сопровождаются нарушением речи, слюнотечением. Ребенок остается в сознании.
- Время, характерное для приступа — когда ребенок засыпает или просыпается. Часто это ночь, поэтому приступ может остаться незамеченным.
- Ребенок отлично помнит приступ. Амнезия в данном случае не характерна.
- Длительность эпизода 1 – 2 минуты.
- Возможна вторичная генерализация, то есть распространение очага возбуждения на другие области мозга и развитие общего тонико-клонического припадка, который большинство людей представляет себе, когда речь идет об эпилепсии.
Причины роландической эпилепсии у детей
Причина развития РЭ неизвестна. Вероятность заболеть однозначно выше у пациентов, чьи родители или близкие родственники страдают этой патологией. Возможно, определенную роль в провокации клинических проявлений играют родовые травмы и хроническая гипоксия плода во время беременности.
Диагностика роландической эпилепсии

Для РЭ характерны специфические жалобы. Врач тщательно расспрашивает родителей ребенка, пытаясь воссоздать картину болезни. При осмотре с молоточком никаких отклонений обычно не выявляется.
Как при любом состоянии, сопровождающимся приступообразными эпизодами, выполняется электроэнцефалография, которая подтверждает или опровергает судорожные состояния. Это основной метод диагностики патологии. После проведения данного исследования для специалиста электрофизиолога будет несложно установить точный диагноз.
В рамках обследования вашему ребенку будут назначены общие анализы крови и мочи, биохимическое исследование крови. Обязательно будет предложена магнитно-резонансная томография. При РЭ структурных изменений в полушариях мозга не обнаруживается.
Особенности развития детей с роландической эпилепсией

Обычно интеллект при такой форме заболевания не страдает. Дети посещают общеобразовательную школу, кружки, хотя могут быть ограничения в отношении некоторых видов спортивных секций. Несмотря на это, иногда отмечаются некоторые затруднения познавательной деятельности, нарушение концентрации внимания, быстрая утомляемость.
Лечение роландической эпилепсии у детей
Для успешного результата необходим позитивный настрой не только врача, но и родителей малыша. Мастерство специалиста выражается в умении разъяснить суть болезни и дать установку на благополучный исход болезни.
Основные препараты, назначаемые при РЭ:
- конвулекс;
- сультиам;
- универсальное производное вальпроевой кислоты – депакин.
Если у ребенка фиксируются редкие единичные приступы, то в таком случае ставится вопрос только о наблюдении, хотя отечественные эпилептологи все-таки рекомендуют назначение возрастных доз препаратов под контролем ЭЭГ, особенно если маленький пациент испытывает затруднения в учебе. Карбамазепин противопоказан — его ошибочное назначение может привести к появлению абсансов и видоизменению роландических приступов. Лечение длится около двух лет.
С учетом вышеизложенных особенностей психического развития, возникает необходимость подбора мягкого препарата, стимулирующего умственную деятельность, имеющего седативный эффект и не учащающий приступы. Обычно это широко распространенная в детской практике гопантеновая кислота или Пантогам — она улучшает поглощение головным мозгом глюкозы, уменьшает кислородное голодание тканей.
Оксана Коленко, врач-невролог, к.м.н., специально для сайта Mirmam.pro
Полезное видео:
mirmam.pro
Роландическая эпилепсия у детей: симптомы и лечение
Роландическая эпилепсия у детей является наиболее распространенной формой этого заболевания. Вместе с тем болезнь переносится относительно легко, частота приступов небольшая. В некоторых случаях для коррекции состояния ребенка даже не требуется назначения противоэпилептических лекарственных препаратов.

Роландическая эпилепсия у детей
Причины и патогенез заболевания
Название болезни пошло от имени итальянского медика Л. Роланда, который впервые и дал описание этой зоны головного мозга. Приступы при роландической эпилепсии обусловлены формированием патологического очага в центрально-височной области. То есть определенная часть располагающихся там нейронов вырабатывает нервные импульсы со слишком высокой частотой. Этот процесс рано или поздно приводит к развитию эпилептического припадка.
Роландическую эпилепсию относят к группе так доброкачественных идиопатических эпилепсий детского возраста. Основной причиной патологии является наследственную предрасположенность по аутосомно-доминантному типу. То есть, если у одного из родителей в детстве наблюдались симптомы эпилептических припадков, то существует приблизительно 10% вероятность того, что у ребенка также диагностируют роландическую эпилепсию.
Однако в некоторых случаях нарушения в центрально-височной доле могут не давать явной симптоматики. Кроме того, они не сопровождаются структурными изменениями в головном мозге, и вероятность их обнаружения очень мала. Поэтому человек может не подозревать о своем состоянии, а опасность наследования патологии сохраняется.
Интересные статьи
Согласно недавно проведенным клиническим исследованиям, при наличии предпосылок к развитию роландической эпилепсии первый приступ может начаться под влиянием таких факторов:
- Быстрая смена изображения на экране телевизора, монитора или планшета.
- Переутомление.
- Мелькание вспышек света.
- Сильный стресс.
Болезнь проявляет себя у детей в возрасте 2 — 14 лет, но больше половины случаев отмечается в период от 4 до 10 лет. Мальчики страдают от роландической эпилепсии приблизительно в полтора раза чаще, чем девочки.
Клиническая картина болезни
Как и любая другая очаговая форма подобной патологии нервной системы роландическая эпилепсия протекает в виде простых и сложных парциальных припадков. Характерной особенностью заболевания является низкая частота обострений – обычно не более 1 – 2 в течение года. Почти во всех случаях эпилептические приступы возникают во время сна или же в первые часы после пробуждения.
За несколько минут или секунд до появления сложного парциального припадка характерно появление предчувствия, которое в медицинской литературе также называют аурой. Для каждого больного она индивидуальна, но при роландической эпилепсии у детей чаще всего отмечаются такие симптомы:
- Чувство покалывания в области глотки.
- Онемение горла.
- Нечувствительность языка и десен.
- Появление постороннего привкуса во рту.
Затем начинаются судорожные сокращения мышц гортани, которые сопровождаются характерными звуками, напоминающими полоскание или бульканье. Потом судороги распространяются на мимическую мускулатуру, губы и язык. Они могут носить клонический либо тонический характер. При клонических сокращениях наблюдаются ритмические быстрые подергивания половины лица, при тонических, наоборот, — неподвижность. Эти симптомы сопровождаются нарушениями речи, усилением секреции слюны.
Приблизительно у 20% детей кроме лица судороги охватывают руку и ногу с одной стороны. При тяжелом течении роландической эпилепсии существует вероятность перехода сложного парциального припадка во вторичный генерализованный, который охватывает все тело.
Эпилепсия. Результат лечения эписиндрома у ребенка. Отзыв мамы
Эпилепсия у детей. Признаки эпилепсии. Лечение, симптомы. Детская эпилепсия
приступ у ребенка из п. Березовка
Причины эпилепсии у детей, лечение. Эписиндром. Отзыв мамы.
подергивания во сне
Приступ протекает с полной или частичной потерей ориентации, его длительность не превышает 2 – 3 минут. Он проходит самостоятельно без посторонней помощи. Развитие эпилептического статуса или синдрома, при которых припадки следуют один за другим через короткие промежутки времени, для роландической эпилепсии нехарактерно.
Диагностика
Основным способом определения участков патологической активности в головном мозге является электроэнцефалограмма. Современные компьютерные программы для обработки результатов обследования позволяют установить точную локализацию эпилептического очага.
При роландической эпилепсии изменение частоты импульсов в центрально-височной зоне отмечается в виде характерных пиков не только во время приступов, но и в промежуток времени между ними, особенно в ночное время.
Очень важна дифференциальная диагностика с другими, более серьезными формами эпилепсии. Для исключения структурных изменений, опухолей, кист и абсцессов в головном мозге рекомендуется сделать магнитно-резонансную томографию. КТ для детей менее предпочтительна из-за определенной лучевой нагрузки.
Лечение
На сегодняшний день для терапии эпилепсии доступно несколько десятков различных препаратов. В педиатрической практике к выбору медикаментов для купирования эпилептических припадков подходят с особой тщательностью. Дело в том, что некоторые средства могут привести к задержке интеллектуального развития и другим серьезным побочным эффектам. Лечение назначается только после второго приступа и постановки точного диагноза.
Лекарствами первой очереди для лечения роландической эпилепсии являются вальпроаты (Депакин, Конвусольфин, Конвулекс). Дозировка препарата рассчитывается индивидуально для каждого пациента с учетом возраста и состояния ребенка. Прием таблеток начинают с минимально возможной дозы, которую при отсутствии эффекта постепенно увеличивают до 15 – 30 мг/кг в сутки.
В случае индивидуальной непереносимости вальпроатов прописывают:
- Топирамакс (Топамакс) в количестве 3 – 5 мг/кг.
- Карбамазепин или его более современные аналоги Тегретол, Финлепсин (15 – 20 мг/кг). Однако в некоторых случаях у детей под влиянием Карбамазепина было отмечено учащение приступов и ухудшение состояния. Поэтому этот препарат применяется только при неэффективности других средств. Также он противопоказан для детей до 7 лет.
При лечении других форм заболевания назначаются комбинации двух или трех противоэпилептических препаратов. Однако подобная тактика во время терапии роландической эпилепсии не оправдана. С одной стороны, это обусловлено слишком высоким риском разнообразных побочных эффектов, что особенно опасно в детском возрасте. С другой – легким течением болезни и невысокой частотой припадков.
Лекарственные средства из группы барбитуратов (например, фенобарбитал) также не назначаются из-за вероятности развития выраженной задержки развития ребенка.
При лечении вальпроатами, Топамаксом или Карбамазепином у детей могут наблюдаться такие осложнения:
- Нарушение координации движений.
- Спутанность сознания.
- Расстройства мышления, памяти, интеллектуальной деятельности.
- Головная боль, повышенная утомляемость.
- Тошнота, рвота.
Также при клиническом исследовании крови отмечается уменьшение количества эритроцитов и лейкоцитов. Однако практически все перечисленные эффекты проходят через некоторое время после отмены препарата. Кроме того, необходимо регулярно сдавать анализы на определение концентрации действующего вещества препарата в крови.
Лечение достаточно длительное. Даже после полного прекращения приступов прием лекарств необходимо продолжать еще 1 – 2 года.
Прогноз заболевания
По наблюдениям врачей при роландической эпилепсии через 1 – 2 года после первого приступа их частота снижается (иногда даже без соответствующей терапии), а к 14 – 16 годам в большинстве случаев они полностью прекращаются. Лишь у крайне незначительного числа больных болезнь прогрессирует.
В лечении роландической эпилепсии у детей помимо регулярного приема медикаментов большую роль играют такие факторы:
- Строгое соблюдение режима дня. Нельзя допускать недосыпания, резкого пробуждения, стрессов.
- Правильное питание. Из рациона необходимо исключить напитки, возбуждающие центральную нервную систему (кока-колу, пепси).
- Ограничение игр на компьютере, приставке или планшете.
- Обязательная физическая нагрузка. О том, каких видов спорта лучше избегать, нужно посоветоваться с неврологом. Обычно врачи советуют плавание, регулярную общую гимнастику.
Роландическая эпилепсия не приводит к отклонениям в умственном, психическом и физическом развитии ребенка. Подобные нарушения возможны лишь при присоединении вторичных генерализованных приступов. Но даже в таком случае это корректируется своевременным и адекватным лечением.
Для улучшения социальной адаптации, учителей в школе и воспитателей в саду нужно в обязательном порядке проинформировать о болезни и о том, что нужно делать во время припадка, но в то же время не акцентировать внимание окружающих на особенностях состояния здоровья ребенка.
kakiebolezni.ru
Роландическая эпилепсия | www.doctor.nevromed.ru
К.Ю. Мухин, П.А. Темин, Е.А. Рыкова
Луиджо Роландо (1773-1831 г.), итальянский врач и анатом, дал классическое топографическое описание центральной борозды коры головного мозга. При идиопатической парциальной эпилепсии детского возраста, характеризующейся короткими гемифациальными моторными ночными приступами, часто с предшествующей соматосенсорной аурой и типичными изменениями ЭЭГ (полифазные спайки с локализацией в центральной и срединной височной областях) [14], эпилептогенной зоной являются нижние отделы роландической борозды. Изучение этой разновидности идиопатической парциальной эпилепсии начато более 40 лет назад. Первоначально были описаны специфические изменения ЭЭГ у определенной группы детей. В 1952 г. H.Gastaut [25] впервые обратил внимание на особые эпилептические изменения ЭЭГ у некоторых детей: полифазные спайки со строгой локализацией в перироландической области. Первое клиническое описание симптомов эпилепсии с роландическими спайками (1958 г.) принадлежит Р.Nayras и М.Веаussart [40]. В последующем Е.Gibbs и F.Gibbs [27], С.Lombroso [36], Р.Loisea и соавт. [35] провели клинический анализ симптомов при эпилепсии с роландическими спайками и предложили называть данную форму эпилепсии роландической. Авторы отметили ее благоприятный прогноз и отсутствие симптомов органического поражения центральной нервной системы.
Частота
Роландическая эпилепсия (РЭ) — одна из наиболее частых форм эпилепсии детского возраста. Распространенность ее составляет 21 на 100 тыс. здорового детского населения [29]. Частота РЭ среди всех форм эпилепсии с дебютом до 13 лет варьирует по разным данным от 11,5% [15] до 25% [5]. Из 360больных эпилепсией детей, наблюдавшихся Р.Lerman [34],у 14,4% была диагностирована роландическая эпилепсия. Для сравнения заметим, что одна из наиболее частых форм эпилепсии детского возраста — пикнолепсия — была диагностирована лишь у 10,5% пациентов. Не исключено, что истинная частота роландической эпилепсии в популяции значительно выше, так как у многих больных отмечаются единичные ночные приступы, часто остающиеся без внимания родителей и врачей [34].
Большинство авторов отмечают преобладание мальчиков среди больных роландической эпилепсии [3]. Соотношение мальчиков и девочек в среднем составляет 6:4 [11].Среди 100 бальных, наблюдавшихся Р.Lerman [34], было 62 мальчика и 38 девочек.
Клиника
Дебют роландической эпилепсии варьирует в возрастном интервале 2 — 14 лет. В 83% случаев РЭ дебютирует в возрасте 4 — 10 лет[5]. У подавляющего большинства пациентов приступы начинаются между 5-м и 10-м годом жизни с максимумом в возрасте 9 лет [9]. Средний возраст появления приступов — 9,9 года [33]. Начало заболевания в возрасте до 2 лет отмечается не чаще чем в 8% случаев [15]. Имеются единичные описания начала РЭ на 1-м году жизни [17], однако отнесение данных случаев к РЭ дискутируется [21].Начало заболевания после 11 лет также является редкостью, а после 14 лет такие случаи не наблюдаются [9].
Клиническая симптоматика приступов при роландической эпилепсии, как правило, типична. Наблюдаются простые парциальные (моторные, сенсорные, вегетативные), сложные парциальные (моторные) и вторично генерализованныс приступы. Наиболее типичны простые парциальные моторные и/или сенсорные пароксизмы [2].
Простые парциальные приступы составляют «ядро» роландической эпилепсии и наблюдаются у 70 — 80% больных. Наиболее типично начало приступа с соматосенсорной ауры: ощущение покалывания, онемения, «прохождения электрического тока» унилатерально в области глотки, языка, десны. Вслед за аурой развивается парциальный приступ. Возможны следующие варианты: гемифациальные приступы; унилатеральные тонические, клонические или тонико-клонические судороги мышц лица; фарингооральные приступы; унилатеральные судороги губы, языка, глотки, гортани, часто сочетающиеся с анартрией и гиперсаливацией. Гемифациальные приступы имеютместо у 37% больных, фарингооральные — у 53% [91. Часто во сне больные издают своеобразные горловыезвуки типа «бульканья», «хрюканья», «полоскания горла». Истинную частоту соматосенсорных приступов (щечная парестезия по терминологии J.Aicardi [5]) определить сложно, так как дети, особенно маленькие, затрудняются описать свои ощущения во время приступов.
У 20% больных судороги могут распространяться с мышц лица на гомолатеральную руку (брахиофациальные приступы) и примерно в 8%случаев вовлекать и ногу (унилатеральные приступы). По мере развития заболевания приступы могут менять сторонность. Вторично генерализованные судорожные приступы отмечаются у 20-25% больных роландической эпилепсии. Они наиболее характерны для младших детей, и возникновение генeрализованных приступов «жестко» приурочено ко сну. Наличие у пациентов длительное время только генерализованных судорожных приступов нехарактерно для РЭ, как и наличие абсансов, психомоторных приступов и приступов с психическими симптомами [5].
Продолжительность приступов при роландической эпилепсии, как правило, небольшая [5] от нескольких-секунд до 2-3мин. У 11% [16] — 22% [5] больных продолжительность пароксизмов превышает 10-15 мин, у 16% [5] отмечаются тяжелые продолжительные приступы ,заканчивающиеся постприступным гемипарезом (паралич Тодда). Частота приступов при РЭ обычно невысока — в среднем 2 в год [5]. В первые 1-2 года с момента дебюта заболевания приступы могут быть более частыми, однако с течением времени они возникают все реже. После 13-16 лет возможно полное исчезновение приступов. У 10-40% детей наблюдается единичный приступ за все время болезни, даже если они не получают антиконвульсантов [41].Еженедельные и более частые, ежедневные приступы наблюдаются лишь в 6% [35] — 20% [34] случаев. Серийные приступы и повторные в течение одной ночи редки и наблюдались в 3% случаев, описанных Т . Deonna и со авт.[17].
В редких публикациях [15,16,23,34] сообщается о развитии эпилептического статуса при РЭ. Часто та его при РЭ составляет около 11% [16]. Подробное описание эпилептического статуса у больных РЭ представлено в работе N . Fejerman и А.Di Blasi [23]. Авторы наблюдали 2 мальчиков 8 лет с дебютом РЭ в 3 года, у которых возник длительный статус гемифациальных приступов. Сознание было сохранено, однако констатировались анартрия и выраженное слюнотечение. Пероральное назначение антиконвульсантов в высоких дозах, как и парентеральное введение диазепама или лоразепама, не оказало влияния на эпилептический статус. Лишь назначение гормональных препаратов(дексаметазон) полностью купировало судороги.Вызывает сомнение, однако, отнесение данныхслучаев к роландической эпилепсии. У одного из этих пациентов наблюдались типичные абсансы, у другого -приступы с джексоновским маршем; у обоих приступы были резистeнтны к антиконвульсантам . Возможно, данные случаи представляют собой атипичную форму РЭ. Е.Roulet и соавт. [42] описал иэпилептический статус у мальчика 6 лет с роландической эпилепсии. Единственным его проявлением было длительное слюнотечение в сочетании с оролингвомоторной диспраксией. На ЭЭГ во время слюнотечения регистрировались спайк-волновые комплексы ,включая роландические. При увеличении дозы карбамазепина слюнотечение прекратилось. По мнению авторов, длительное перманентное слюнотечение у больных роландической эпилепсии может быть единственным симптомом эпилептического статуса.
Пароксизмы РЭ связаны с ритмом сон -бодрствование. Наиболее типичны ночные приступы ,возникающие преимущественно при засыпании и пробуждении. При ночных приступах пароксизмы возникают в период пробуждения (35%), реже — все редине ночи (25%) и при засыпании (20%). У 25-30%больных приступы наблюдаются как во сне, так и всостоянии бодрствования [5]. Лишь у 5-25% пациентов они возникают исключительно со время бодрствования [5,34]. Имеется некоторое различие картины приступов в зависимости от ритма сон — бодрствование. Дневные приступы практически всегда простые парциальные, чаще гемифациальные ,короткие, ночные, как правило, более тяжелые, продолжительные, обычно унилатеральные или вторично генерализованные. Провести оценку сознания у пациентов с ночными приступами сложно; феномен анартрии часто симулируетклинику выключения сознания. Сложные парциальные приступы при роландической эпилепсии редки и составляют лишь около 5% всех случаев [15]. Возможно, на протяжении приступа у некоторых больных имеет место «флюктуация» уровня нарушения со знания.
J.Aicatdi и J.Сhevrie [4] была выделена группа больных сосвоеобразным эпилептическим синдромом ,клиническая симптоматика которого была схожа с роландической эпилепсией. У больных отмечались простые парциальные гемифациальные и гемиклонические приступы,однако в сочетании с миоклонически-астатическими, атоническими приступами и в ряде случаев с абсансами. Данная группа наблюдений классифицирована какатипичный вариант РЭ. Частота его, согласно Т.Deonnaи соавт. [16], составляет 5% среди всех больных РЭ.Таксономическое положение данного синдрома спорно. По мнению J.Aicatdi и J.Сhevrie [5], данная форма эпилепсии является нозологически самостоятельным синдромом с четко очерченными клиникой, изменениями ЭЭГ и прогнозом. Другие авторы предполагают наличие атипичного варианта в рамках РЭ [17]. Подробное описание данного синдрома представлено Т.Deonna и соавт. [16] на примере 6 пациентов. Среди обследованных больных преобладали мальчики. Приступы дебютировали в возрастном интервале от 2 до 7 лет у неврологически нормальных детей с сохранным интеллектом. Клинические симптомы включали различные виды приступов. Характерными были ночные простые парциальные приступы, подобные таковым при РЭ, миоклонически-астатические и атонические приступы. У ряда больных отмечались атипичные абсансы. Приступы во всех случаях были частыми, ежедневными и приводили к многократным падениям пациентов и тяжелым ушибам. На ЭЭГ типичные роландические спайки сочетались с медленными комплексами пик-волна, характерными для синдрома Леннокса — Гасто. Отмечалось нарастание эпилептической активности в фазе медленного сна.
Клиническая симптоматика атипичной роландической эпилепсии носит черты целого ряда эпилептических синдромов: РЭ (простые парциальные ночные приступы в сочетаниис типичными роландическими спайками), синдрома Леннокса — Гасто (частые атонически-астатические приступы, атипичные абсансы в сочетании с медленными комплексами пик-волна) и эпилепсии смиоклонически-астатическими приступами,описанной Н.Doose [19]. Однако кардинальным отличием атипичной роландической эпилепсии от синдрома Леннокса — Гасто и эпилепсии с миоклоничeски-астатическими приступами являются отсутствие у пациентов нарушений интеллекта и хороший прогноз. Р.Loisea и соавт. [35] провели катамнестическое исследование13 пациентов с атипичной РЭ в течение не менее 9лет. Спустя разный промежуток времени во всех случаях была достигнута полная ремиссия, при этом большая часть пациентов (10) не применяли регулярной противоэпилептической терапии. Авторы не отметили ни отставания в психическом развитии, ни серьезных нарушений поведения как в наиболее активный период заболевания, так и в период ремиссии, что сближает данные случаи с типичной РЭ. По мнению авторов, при данном синдроме следует избегать «агрессивной» противоэпилептической терапии ввиду хорошего прогноза.
O.Dulac и соавт. [21] проанализировали случаи парциальной эпилепсии с ранним дебютом — между 8днями и 3 годами жизни. Среди 442 больных выявлено 17с парциальной эпилепсией с ранним дебютом .Приступы характеризовались как простые парциальные с частой вторичной генерализацией. По мнению авторов, данные случаи являются переходной формой между доброкачественной эпилепсией новорожденных и РЭ. В отличие от двух указанных синдромов прогноз был неблагоприятными приступы не поддавались медикаментозной терапии. Последующие исследования покажут, являются ли случаи парциальной эпилепсии с дебютом в первые 3 года жизни нозологически самостоятельным синдромом или еще одним» атипичным вариантом» РЭ.
Неврологический статус
Неврологический статус у детей, страдающих роландической эпилепсии, изучен достаточно подробно. Роландическая эпилепсия относится к идиопатическим формам эпилепсии, при которых отсутствуют признаки органического поражения головного мозга, что подтверждается большинством публикаций. Более того, по мнению А. Веаumanoir и соавт. [8] наличие таких симптомов противоречит критериям диагноза роландической эпилепсии. Однако в последние годы благодаря внедрению в клиническую практику высокоэффективных нейрорадиологических методов исследования(компьютерная томография, ядерно-магнитный резонанс, позитронная эмиссионная томография) появились единичные сообщения об обнаружении структурных изменений в головном мозге у больных РЭ.
Из 100 больных, наблюдавшихся Р.Lerman и S.Kivity [33], у 4 констатированы симптомы органического поражения центральной нервной системы: детский церебральный паралич (гемипаретическая и тетраплегическая формы), микроцефалия, умеренная задержка умственного развития. Во всех этих случаях диагноз РЭ не вызывал сомнения и был подтвержден как клинически, так и нейрофизиологически. Пневмоэнцефалография не выявила нарушений у данных больных. S.Blom и J.Heijbet [11]в 3 (7,5%) из 40 случаев РЭ обнаружили у больных центральный гемипарез. E.Roulet и соавт. [42] отметили проявления оролингвомоторной диспраксии у больного РЭ. Такие симптомы, как микроцефалия, косоглазие, мозжечковая недостаточность, задержка психического и речевого развития, констатировали у ряда больных РЭ Р.Santanelli и соавт.[43]. Синдром гиперактивности был обнаружен у 16,7%больных РЭ [34].
Генетика
Р.Вrау и W.Wiser [13] первыми констатировали наличие семейных случаев роландической эпилепсии и предположили аутосомно-доминантную модель наследования с неполной пенетрантностью и возрастной зависимостью. В последние десятилетия проведены многочисленные клинико-генеалогические исследования при роландической эпилепсии, подтверждающие правомерность данной концепции. Согласно обобщенным данным литературы, 8,9% [35] — 68% [29]больных РЭ имеют родственников, страдающих эпилепсией или имеющих приступы в анамнезе, и до 30% [13] — родственников с наличием на ЭЭГ роландических спайков при отсутствии приступов. Частота обнаружения спайков у сибсов пробандов и детей, родители которых страдали РЭ, составляет25-36% (в популяции здорового населения — 1,4-5% [З7]).Однако лишь у малой части из них (12% в исследовании Р.Вrау и W.Wiser [13]) отмечались приступы: остальные были клинически здоровы. Характер приступов у родственников больных роландической эпилепсии может быть различным. Типичные приступы, характерные для РЭ, констатируются у 13%родственников, абсансная эпилепсия — у 10%, гснсрализованные судорожные приступы — у 3%,фокальная эпилепсия — у 1% [9].
В ряде исследований изучена конкордантность монозиготных близнецов по РЭ. Обнаружена высочайшая конкордантность по наличию на ЭЭГ роландических спайков, но не по развитию самой РЭ. T.Kajitani и соавт. [30] изучили 3 пары монозиготных близнецов в возрасте 5-11 лет, в которых один из сибсов страдал РЭ. Во всех случаях констатирована типичная роландическая эпилептическая активность на ЭЭГ, но ни у одного из здоровых сибсов не было никаких проявлений РЭ.
В последние годы была выдвинута гипотеза о мультифакторном наследовании роландической эпилепсии [29]. Она основывается на том факте, что лишь у небольшой части детей, имеющих на ЭЭГ роландические спайки, в дальнейшем развивается РЭ. Предполагается, что роландические спайки и развитие РЭ детерминированы двумя различными, но сцепленными генами. В 1982 г. O.Eeg-Olofsson и соавт. [22] обнаружили, что у родителей, сибсов и других родственников детей, больных РЭ, низкая встречаемость гаплотипа А1В8 антигенов лейкоцитарной гистосовместимости. Частота его в общей популяции крайне высока [22]- Возможно, что данный гаплотип играет роль протектора или ингибирующего фактора, препятствующего развитию РЭ.
Интересны исследования, раскрывающие взаимосвязь РЭ с фебрильными судорогами. E.Frantzen и соавт. [24] сообщили, что у 20% детей с фебрильными судорогами в дальнейшем на ЭЭГ появляется фокальная эпилептическая активность, идентичная роландическим спайкам. Ни у одного из этих пациентов не отмечалось в дальнейшем эпилептических приступов. Исследования на монозиготных близнецах также показали возможное генетическое сцепление между РЭ и фебрильными судорогами. M.Lennox-Buchthul [32] изучила 24 пары монозиготных близнецов, в которых по крайней мере у 1 из пары имелись фебрильные судороги, и выявила, что 20% их сибсов имели редкие ночные приступы. У 2 из 24 обнаружено сочетание ночных приступов с фебрильными судорогами. К сожалению, автор не идентифицировала данные ночные приступы, однако по характеру их течения и возрасту дебюта можно предположить, что это случаи РЭ. В исследовании T.Kajitani и соавт. [31] среди 3 пар монозиготных близнецов 3 имели РЭ и 5 — фебрильные судороги. Данные работы могут свидетельствовать о генетическом сцеплении РЭ и фебрильных судорог. Подтверждением этой гипотезы служит и клиническая схожесть двух данных синдромов: высокая генетическая детерминированность, «жесткий» возрастзависимый дебют, доброкачественный прогноз [1] .
Остается неясной роль экзогенных, средовых факторов в развитии роландической эпилепсии. H.Doose и W.Baier [18] предположили, что генетические факторы при РЭ детерминируют низкий порог судорожной готовности головного мозга. При этом здоровых детей, имеющих на ЭЭГ роландические спайки, они расценили как субклинических носителей с низким судорожным порогом. По мнению авторов, воздействие различных экзогенных факторов в онтогенезе, а также сцепление с другими генами может способствовать у таких пациентов клинической манифестации заболевания и оказывать некоторое влияние на его течение. Т.Каjitani и соавт. [30] описали 3 родных сибсов, у каждого из которых на ЭЭГ имелись типичные роландические спайки. У одного из сибсов РЭ дебютировала в 4 года во время лихорадочного заболевания, у другого отмечался единственный приступ в возрасте 10 лет при просмотре телепередач, третий миновал «критический период» для дебюта и был здоров. Данное наблюдение иллюстрирует полиморфизм клинических проявлений заболевания, что может зависеть от различных экзогенных воздействий.
Факторами, трансформирующими субклиническое носительство в РЭ, могут быть патология беременности и родов, травмы головы, нейроинфекции и пр. [5]. Однако более чем у половины детей, страдающих РЭ, указание на наличие данных факторов в анамнезе отсутствует[15].
Электроэнцефалография
Необходимым исследованием для объективизации диагноза РЭ является электроэнцефалография [14].На ЭЭГ в межприступном периоде при РЭ обнаруживаются характерные, типичные «роландические» или «центровисочные» комплексы при обязательно сохранной основной активности. Эти комплексы представляют собой медленные дифазные высокоамплитудные пики или острые волны (100 — 300 мВ), нередко с последующими медленными волнами, общей продолжительностью около 30 мс (см. рисунок). Они имеют тенденцию к возникновению группами. Данные комплексы напоминают зубцы QRST ЭКГ. Роландические комплексы «жестко» локализованы: центральная и центровисочная области. Роландические комплексы могут наблюдаться как унилатерально (обычно контралатерально гемифациальным приступам) — 60% больных, так и билатерально — 40% [29].Эпилептические комплексы, как правило, независимы друг от друга, лишь в редких случаях наблюдается их билатерально-синхронное распространение с амплитудным преобладанием с одной стороны [26,34].
D.Gregory и Р.Wong [28] провели изучение точной локализации роландических спайков, используя метод компьютеризированного топографического картирования. Авторы обнаружили, что максимум «позитивности» электрического диполя при РЭ находится в центрально-височной области, а максимум «негативности» — в лобной. Предположено, что специфические ЭЭГ-паттерны при РЭ исходят из зоны, расположенной в нижних отделах роландической борозды, на границе с сильвиевой бороздой. Типичной особенностью изменений ЭЭГ при РЭ является нестойкость паттернов, их вариабельность от одной записи к другой. Роландические спайки могут исчезать, а затем появляться вновь, менять стройность, конфигурацию даже при двух последующих записях ЭЭГ через короткий промежуток времени. Нестойкость ЭЭГ-паттернов при РЭ свидетельствует, по мнению J.Aicardi [5], об отсутствии органических изменений в головном мозге при РЭ. В связи с этим отсутствие роландических спайков при однократном злектроэнцефалографическом исследовании не может считаться убедительным аргументом для исключения диагноза РЭ при наличии типичной картины приступов [15]. Крайне важным для подтверждения диагноза РЭ является исследование ЭЭГ во время сна. Около 30% детей, страдающих РЭ, имеют роландические спайки исключительно во время сна [29]. Во время дремоты и на всех стадиях сна отмечается тенденция к переходу унилатеральных роландических комплексов в билатеральные [34].
Интересной находкой при РЭ является обнаружение на ЭЭГ наряду с типичными роландическими комплексами и других эпилептических паттернов. От 10 до 20% детей с РЭ имеют на ЭЭГ пик-волновые комплексы в других зонах коры, главным образом в затылочной области [41]. Морфология «затылочных комплексов «близка к роландическим и к наблюдаемым при доброкачественной фокальной эпилепсии с затылочными пароксизмами [10]. По мнению J.Aicardi [5],частота «затылочных комплексов» при Рэо братно пропорциональна возрасту ребенка и является нередкой у больных до 3 лет жизни. От 7% [34]до 20% [5] пациентов с РЭ демонстрируют на ЭЭГ типичную генерализованную пик-волновую активность с частотой 3-4 Гц, нередко возникающую при гипервентиляции. У отдельных больных возможно появление медленных пик-волновых комплексов. Большинство авторов придерживаются однозначного мнения об отсутствии корреляции между частотой и выраженностью пик- волновыхкомплексов на ЭЭГ и особенностями течения заболевания.
Исследование ЭЭГ во время приступа представляется довольно сложным ввиду низкой частоты приступов при РЭ. B.Dalla-Bernardina и соавт. [15]описали во время ночного приступа появление на ЭЭГ низкоамплитудной быстрой активности в центрально-височной области, переходящей в роландические комплексы с распространением на всю гемисферу и с последующим охватом всего полушария.
Нейрорадиологическое исследование
Сведения о нeйрорадиологическом исследовании у больных РЭ единичны. H.Gastaut [25] одним из первых изучил данные компьютерной томографии у 15 больных РЭ и не нашел патологических изменений ни в одном случае. В последующем при нейрорадиологическом исследовании у больных РЭ были обнаружены некоторые структурные изменения в головном мозге: расширение сильвиевой щели, наличие полости прозрачной перегородки (2 из 13случаев) [39], вентрикуломегалия, арахноидальные кисты (3 из 17 случаев) [38]. Р.Santanelli и соавт. [43] представили подробное клиническое и нейрорадиологическое описание 3 случаев РЭ, сочетающейся со структурными изменениями головного мозга. У одного больного была выявлена липома мозолистого тела, у другого (соспондилоторакальной дисплазией) — агенезия мозолистого тела с вентрикуломегалией, у третьего — множество церебральных, преимущественно перивентрикулярных, кальцификатов (врожденный токсоплазмоз). У всех этих больных наблюдались типичная клиническая картина РЭ и роландические спайки на ЭЭГ.
Обнаруженные при нейрорадиологическом исследовании у единичных больных РЭ органические симптомы поражения головного мозга трудно интерпретировать однозначно. Не исключено, что эти нарушения не имеют непосредственной причинно-следственной связи с РЭ и могут быть вызваны сочетанием РЭ с другими заболеваниями — детским церебральным параличом, микроцефалией, токсоплазмозом, эктомезодермальными дисплазиями. Как и в популяции в целом, у больных РЭ могут наблюдаться перинатальное поражение центральной нервной системы, постнатальные черепно-мозговые травмы. Частота перинатальных поражений центральной нервной системы среди больных РЭ составляет 6% [16]- 13% [34], сотрясения головного мозга — 4 — 5% [34], что не превышает статистических данных в популяции здоровых детей. Принципиально важный и до конца не решенный вопрос — влияют ли данные экзогенные факторы на возникновение и течение РЭ. По мнению J.Aicardi [5], нарушения, обнаруженные в головном мозге у больных РЭ, не могут быть причиной эпилепсии, а являются случайными находками. С другой стороны, нельзя игнорировать тот факт, что у ряда больных РЭ структурные изменения с головном мозге локализуются в нижних отделах роландической борозды [43], а это не исключает полностью возможность существования «симптоматической» формы эпилепсии.
Лечение
За последние годы в лечении РЭ апробирован целый ряд противоэпилептических препаратов. Большинство авторов рекомендуют применять препараты, преимущественно воздействующие на парциальные формы эпилепсии: карбамазепин (финлепсин, тегретол) и дифенин (фенитоин). При лечении РЭ необходимо избегать политерапии, а также на значения противосудорожных препаратов в высоких дозах. Доброкачественное течение РЭ, отсутствие интеллектуально-мнестических нарушений у пациентов не дают оснований рекомендовать «агрессивную» антиконвульсантную политерапию для лечения данной формы эпилепсии ввиду возможности развития тяжелых побочных эффектов.
По мнению P.Lerman [34], а также В. Dalla-Bermardina и соавт.[15], одним из препаратов выбора влечении РЭ является фенитоин в низких и средних дозах. При возникновении приступов исключительно в ночное время или в период пробуждения рекомендован однократный прием фенитоина на ночь. Во всех наблюдавшихся авторами случаях применение средних терапевтических доз фенитоина приводило к полной клинической ремиссии приступов. Согласно данным P.Lerman и S.Kivity [33], эффективность фенитоина в лечении РЭ превышает таковую карбамазепина и фенобарбитала.
Карбамазепин также высокоэффективен в лечении РЭ [41] и отличается от дифенина минимальной выраженностью побочных эффектов терапии.
Сультиам (осполот) эффективен и хорошо переносится больными РЭ [19]. Применение барбитуратов (фенобарбитал, бензонал) лимитировано частым и тяжелым побочным влиянием на интеллектуально-мнестическис функции и поведение детей [5] и не может быть рекомендовано для лечения РЭ.
В последние годы появились публикации, свидетельствующие об эффективности препаратов вальпроевой кислоты (депакин, конувулекс) при РЭ[6,15,29]. Важной особенностью их является позитивное влияние на интеллектуально-мнестические функции пациентов и хорошая переносимость [12]. Однако, катамнестические исследования эффективности применения вальпроатов при РЭ отсутствуют.
Большинство авторов считают, что продолжительность применения антиконвульсантов при РЭ не должна превышать 2 лет с момента последнего приступа [35]. В среднем продолжительность медикаментозного лечения при РЭ составляет 3,2 года [33]. Однако в случае раннего дебюта приступов (2-3 года) лечение должно быть продолжено до 10-летнего возраста, независимо от длительности ремиссии [4]. Лечение рекомендуется назначать только после повторного приступа. Сохранение на ЭЭГ типичной эпилептической активности не может являться причиной продолжения антиконвульсантной терапии, если у больного имеется длительная ремиссия.
Прогноз
Особенностью РЭ является хороший прогноз заболевания [20]. По данным P.Loisea и соавт. [35], после 13лет приступы РЭ исчезли у 93,5% из 168 обследованных больных, а после 16 лет — у 98,8%. P.Loisea и соавт. [35] подробно исследовали влияние отдельных клинических симптомов РЭ на прогноз заболевания. В качестве возможных факторов, влияющих на прогноз, были проанализированы пол пациентов, возраст дебюта эпилепсии, частота и характер приступов, их суточное распределение, особенности неврологического статуса. У всех 168 пациентов с РЭ прослежен катамнез в течение не менее 4 лет с момента последнего приступа. Выделены факторы, влияющие на прогноз РЭ: возраст дебюта и частота приступов. Обнаружено, что лишь возраст дебюта эпилепсии статистически достоверно коррелирует с прогнозом РЭ. Установлено, что продолжительность заболевания и резистентность к терапии увеличиваются при раннем (до 4 лет) и позднем (после 10 лет) дебюте эпилепсии. Все остальные факторы существенно не влияют на прогноз РЭ.
Длительное наблюдение больных в катамнезе обнаружило возможность рецидивов приступов при РЭ после продолжительной ремиссии. Частота рецидивов приступов во взрослом возрасте при РЭ невысока — от 1,8% [35] до 4% [34]. Рецидив приступов чаще наблюдается у женщин в период гормональной перестройки, через 3 — 10 лет с момента наступления ремиссии, и не связан с приемом антиконвульсантов [35]. В большинстве случаев появляются генерализованные судорожные приступы, единичные или редкие. Важной особенностью является отсутствие на ЭЭГ типичных роландических спайков; по мнению P.Loisea и соавт. [35], ЭЭГ у данных пациентов обычно в пределах нормы.
Учитывая генерализованный характер приступов, появление их спустя длительное время после наступления ремиссии, отсутствие роландических спайков на ЭЭГ, P.Lerman [34] предположил, что данные случаи не имеют отношения к РЭ и представляют собой возникновение эпилепсии de novo. Противоречит данной концепции тот факт, что частота рецидивов при РЭ (2-4%) значительно превышает популяционную частоту эпилепсии (0,8%). Возможно, в возникновении приступов во взрослом возрасте при РЭ играет роль взаимодействие экзогенных факторов с генетически детерминированным снижением порога судорожной готовности. Одним из «разрешающих» факторов может явиться нарушение гормонального баланса в организме.
Другой возможной причиной рецидивов приступов может быть существование стойких структурных изменений в головном мозге с локализацией в нижних отделах роландической или сильвиевой борозды. G.Ambrosetto и соавт. [6] описали рецидив типичных «роландических» приступов у больного в возрасте 21 года. Пациент страдал РЭ с 10 лет: ночные простые парциальные и вторичногенерализованные приступы. С 13 лет наступила ремиссия, с 16 детой прекратил прием антиконвульсантов. В 21 год без видимой причины у больного развились точно такие же парциальные и вторично генерализованные приступы в ночное время с частотой 1-4 в месяц. При компьютернойтомографии патологии не выявлено. На ЭЭГ в 21 год ив 30 лет (в динамике) — правосторонний фокустипичной роландической активности. Уникальностьданного наблюдения состоит в том, что у больного РЭ приступы вновь возникли спустя 8 лет после наступления ремиссии и носили типичный для РЭ характер, являясь, однако, резистентными к антиконвульсантам. По мнению авторов, в данном случае имеется высокая вероятность наличия у больного структурных изменений в роландической области, что может быть выявлено при более тщательном нейрорадиологическом обследовании (ядерно-магнитный резонанс, позитронная эмиссионная томография).
Дальнейшие исследования покажут соотношение генетических и экзогенных факторов в детерминации РЭ и возможность существования «симптоматических» форм РЭ, обусловленных структурными изменениями, локализованными в роландической области. Необходимо также проведение молекулярно-генетических исследований с целью поиска генов, ответственных за развитие РЭ. Это позволит определить взаимосвязь РЭ с другими формами идиопатической эпилепсии, такими как доброкачественная затылочная эпилепсия Гасто, детская абсанс-эпилепсия и др.
ЛИТЕРАТУРА
I. Бадалян Л.О., Темин П.А., Мухин К.Ю. Фебрильныесудороги. Методические рекомендации. М. 1987; 24.
2. Карлов В.А. Эпилепсия. М. 1990; 219 — 223.
3. Сараджишвили П.М., Геладзе Т.Ш. Там же 1977, 148 — 149.
4. Aicardi .J., Chevrie J.-J. Dev Med Child Neurol 1982, 24: 281 — 292.
5. Aicardi J. Epilepsy in children 1986; 4.
6. Ambrosetto G., Tenuper P., Baruzzi A. J Neural Neurosurg Psychiat 1985; 48: 90.
7. Bancaund J., Collomb D., Dell M.B. Rev Neurol 1958; 99: 206 — 209.
8. Beaumanoir A., BallisT.,Varfis G., Ansai K. Epilepsia l974; 15: 301 — 315.
9. Beaussart M., Favou R. Ibid 1978; 19: 337 — 342.
10. Beydoun A»index.html» Garofalo E.A»index.html» Drury I. Ibid 1992; 33: 1091 — 1096.
11. Blom S., Heijbel J. Ibid 1982: 23: 629 — 631.
12. Bourgeois B.F.D. Ibid 1994. 35: 2: 18 — 23.
13. Bray P.P., Wiser W.C. Pediatrics 1965; 36: 207 — 211.
14. Comissionon Classification and Terminology of the ILAE. Epilepsia 1989; 30: 389 -399.
15. Dalla-Bermardina В., Sgro V., Fontana E. Epileptic syndromes in infancy, childhoodand adolescence. Paris 1992; 173 — 186.
16. DeonnaTh., ZieglevA-L., Despland P.-A. Neuropediatrics 1986; 17: 144 — 151.
17. Deonna Th., Zieglev A.-L., Despland P.-A. Guyvan Меllе. Epilepsia 1986; 27: 241- 247.
18. Doose Н., Baier W.K. Еuгор J Pediatr 1989; 149: 152 — 158.
19. Doose H. Epileptic syndromes in enfancy, childhood and adolescence. Paris 1992; 103- 114.
20. Dreifuss F.E. Epilepsia 1994; 35: 2: 30 — 34.
21. Dulac O., Cusmai R., Olivera K.de. Ibid 1989; 30: 798 — 801.
22. Eeg-Olofsson O., Safwenbery J., Wigrtz A. Ibid 1982; 23: 27 — 34.
23. Fejerman N., Di Blasi A.M. Ibid 1987; 28: 351 — 355.
24. Frantzen E., Lennox-Buchthal M., Nygaakt A. Electroen-cephalogr Clin Neurophysiol1968; 24: 197 — 212.
25. Gastaut H. Rev Neurol 1952; 87: 488 — 490.
26. Gastaut H., Gastaut J.L. Epilepsia 1976; 17: 325 — 326.
27. Gibbs E.L., Gibbs F.A. Ibid 1960; 1: 448 — 453.
28. Gregory D.L., Wong P.K. Ibid 1984, 25: 705 — 711.
29. Heijbel J. Pediatric Epilepsy. Helsinky 1989.
30. Kajitani Т., Nakaltmra M., Llcaka K., Kobuchi S. Advances in Epileptology 1980; 4:171 — 175.
31. Kajitani Т., Kimura Т., Sumita M., Kaneco M. Brain Dev 1992; 14: 230 — 234.
32. Lennox-Buchthul M. Epilepsia 1971, 12: 197 — 212. 33. Lerman P., Kivity S. ArchNeural 1975; 32: 261 — 264.
34. Lerman P. Epileptic syndromes in infancy, childhood and adolescence. Paris 1992;173 — 186.
35. Loisea P., Duche В., Cordova S. et al. Epilepsia 1988; 29: 229 — 235.
36. Lombroso C.T. Arch Neurol 1967; 17: 52 — 59.
37. Luders Н.O., Lesser R.P., Dinner D.S., Morris H.H. Epilepsy — electroclinicalsyndromes. Berlin 1987; 303 — 346.
38. Mambelli M., Moscano F., Maroni P. et al. Bulll. Liga Int. Epilepsy 1985; 51/52: 79- 80.
39. Morikawa Т., Osawa Т., Ishihara O., Seino M. Brain Dev 1979; 1: 303 — 346.
40. Nayrac P., Beaussart M. Rev Neurol 1958; 99: 201 — 206.
41. Panayiotopoulos С.Р. J Neurol Neurosurg Psychiat 1993; 56: 2 — 5.
42. Roulet E., Deonna Th., Despland P.A. Epilepsia 1989; 30. 564 — 568.
43. Santanelli P., Вureau M., Magaudda A. et al. Ibid 1989; 30: 182 — 188.
www.doctor.nevromed.ru
