Эритроплазия кейра у женщин фото: Эритроплазия Кейра: причины, симптомы, лечение
Рентгенотерапия в лечении распространённой формы эритроплазии Кейра | Джабаров
Введение
Эритроплазия Кейра (ЭК) (син.: папиллярная эпителиома Дарье, эпителиома бархатистая) плоскоклеточный рак in situ — достаточно редкое онкологическое заболевание, сопровождающиеся появлением поверхностной внутриэпителиальной опухоли на головке или внутреннем листке крайней плоти полового члена. Данная патология по своим симптомам и гистологическому строению во многом напоминает болезнь Боуэна (или Бовена), хотя имеет ряд характерных клинических признаков, что и даёт возможность рассматривать это заболевание как самостоятельное. Впервые заболевание было описано L. Queyrat в 1911 году как «erytthroplasie du gland»» [1][2]. По материалам Всемирной организации здравоохранения (1980), рекомендуется считать ЭК и болезнь Боуэна отдельными нозологическими единицами, так как при ЭК вероятность инфильтративного роста значительно выше: риск злокачественной трансформации чётко не определен, но, как сообщается, составляет до 30% в случае отсутствия специализированной терапии [3][4].
К факторам риска развития ЭК относятся необрезанная крайняя плоть, токсическое влияние смегмы на кожу головки полового члена и внутреннего листка крайней плоти при недостаточной гигиене, фимозе, хроническое механическое повреждение и травматизация кожи полового члена, рецидивирующий генитальный вирус простого герпеса, инфицирование вирусом папилломы человека 16-го и 18-го типов, хронические воспалительные процессы, частая смена сексуальных партнёров, иммуносупрессивные состояния (ВИЧ-инфекция), курение [5].
Инфицирование вирусом папилломы человека (ВПЧ) является одним из наиболее важных и широко изученных факторов риска развития рака полового члена, при этом ДНК ВПЧ обнаруживается примерно в 50% всех ЭК и плоскоклеточных карцином полового члена [6].
Предраковые поражения полового члена можно в общих чертах разделить на те, которые связаны с инфекцией ВПЧ, и те, которые не связаны с ВПЧ, но вызваны хроническим воспалением. Поражения, ассоциированные с ВПЧ, включают болезнь Боуэна, ЭК и бовеноидный папулёз, которые связаны с типами ВПЧ 16 и 18 «высокого риска». ВПЧ типов 6 и 11 низкого риска связаны с другими предраковыми поражениями, такими как гигантские остроконечные кондиломы или опухоли Бушке-Левенштейна. ЭК представляет собой ярко-красную бляшку с чёткими конурами, гладкую на ощупь, без уплотнения подлежащих тканей, бархатистую на вид, без глянцевого блеска. В редких случаях на поверхности бляшки могут иметься эрозированные участки. Поражения наиболее часто локализуются на слизистых поверхностях гениталий, таких как внутренняя крайняя плоть и головка полового члена, в большинстве случаев встречается у мужчин с фимозной крайней плотью.
ВПЧ типов 6 и 11 низкого риска связаны с другими предраковыми поражениями, такими как гигантские остроконечные кондиломы или опухоли Бушке-Левенштейна. ЭК представляет собой ярко-красную бляшку с чёткими конурами, гладкую на ощупь, без уплотнения подлежащих тканей, бархатистую на вид, без глянцевого блеска. В редких случаях на поверхности бляшки могут иметься эрозированные участки. Поражения наиболее часто локализуются на слизистых поверхностях гениталий, таких как внутренняя крайняя плоть и головка полового члена, в большинстве случаев встречается у мужчин с фимозной крайней плотью.
Предраковые поражения составляют примерно 10% всех злокачественных новообразований полового члена при первичной диагностике, причём подавляющее большинство из них возникает на головке полового члена [7][8]. Неинвазивный характер предраковых поражений предопределяет лечение с сохранением полового члена. В зависимости от размера, локализации и типа поражения можно использовать ряд различных подходов.
Описание клинического случая
Пациент М. 1952 года рождения. Впервые диагноз плоскоклеточный рак in situ (эритроплазия Кейра) установлен в 2014 году. В течение двух лет до установления диагноза проходил лечение у дерматолога по месту жительства. Однако эффекта получено не было. Направлен на консультацию к онкологу. Взята биопсия — плоскоклеточный рак in situ. Проведена криотерапия жидким азотом. В течение года пациент не наблюдался. При явке отмечен рецидив на головке полового члена. В проекции изменённых после криотерапии тканей имеется ярко алое образование с чёткими ровными краями и бархатистой поверхностью (рис. 1). Общесоматическая патология не выявлена.
Рисунок 1. Внешний вид головки полового члена на момент консультации
Figure 1. The initial appearance of the glans penis
Рисунок 2. Внешний вид головки полового члена после окончания лечения
Figure 2. The appearance of the glans penis after the treatment course
The appearance of the glans penis after the treatment course
Рисунок 3. Внешний вид головки полового члена спустя полгода после завершения лечения
Figure 3. The appearance of the glans penis six months after the treatment course
Учитывая рецидивирующее течение, после консультации радиотерапевта рекомендован курс рентгенотерапии. Учитывая собственный опыт о высоком лечебном эффекте и отсутствии постлучевых рубцовых изменений кожи после мультифракционного курса рентгенотерапии, проведён курс мультифракционной лучевой терапии — РОД 2,0 + 2,0 Гр до СОД = 60,0 Гр. Тубус — 3,5 см 1,8 Al. На момент окончания лечения отмечена выраженная гиперемия и радиоэпителиит второй степени выраженности. На фоне симптоматической терапии в течение 6 недель проявления острой лучевой реакции купированы.
Пациент наблюдался в течение 4-х лет после завершения курса лучевой терапии. Признаков рецидива не отмечено.
Обсуждение
Существуют различные варианты лечения плоскоклеточного рак in situ полового члена. Выбор метода лечения должен быть адаптирован к типу и месту поражения, принимая во внимание предпочтения пациента и вероятное соблюдение режимов лечения, а также необходимость тщательного наблюдения с использованием минимально инвазивных методов. Наиболее широко используются следующие методики: местная химиотерапия / иммунотерапия (5-фторурацил / имиквимод), лазеротерапия, криотерапия, фотодинамическая терапия, хирургическое удаление: шлифовка головки полового члена (частичная / полная), обрезание, микрографическая хирургия Мооса, близкофокусная рентгенотерапия.
Выбор метода лечения должен быть адаптирован к типу и месту поражения, принимая во внимание предпочтения пациента и вероятное соблюдение режимов лечения, а также необходимость тщательного наблюдения с использованием минимально инвазивных методов. Наиболее широко используются следующие методики: местная химиотерапия / иммунотерапия (5-фторурацил / имиквимод), лазеротерапия, криотерапия, фотодинамическая терапия, хирургическое удаление: шлифовка головки полового члена (частичная / полная), обрезание, микрографическая хирургия Мооса, близкофокусная рентгенотерапия.
Местная химиотерапия 5% 5-фторурацилом (5-ФУ) является одним из наиболее часто используемых методов лечением. Наиболее эффективен он у иммунокомпетентных пациентов с чётко выраженными одиночными поражениями небольшого размера, но имеет низкую эффективность у пациентов с ослабленным иммунитетом или пациентов с широко распространённым поражением. Протоколы применения 5-ФУ различаются. Обычно его используют местно на срок от 4 до 6 недель через день.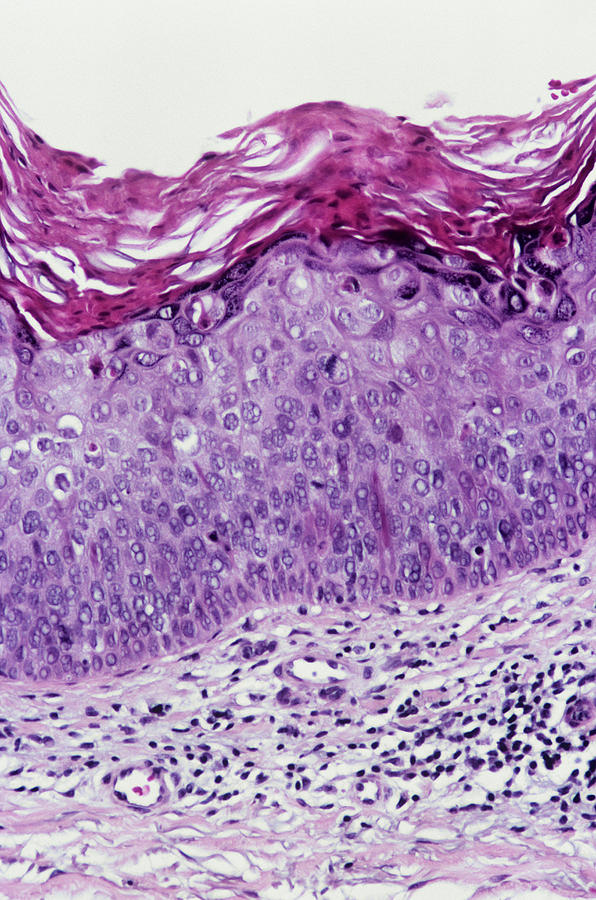 Во всех исследованиях отмечают, что обработанный участок часто покрывается коркой и воспаляется в период лечения. Дополнительное применение стероидов снижает остроту местных реакций, но увеличивает длительность клинических проявлений. Для заживления реактивных изменений может потребоваться от 4 до 8 недель.
Во всех исследованиях отмечают, что обработанный участок часто покрывается коркой и воспаляется в период лечения. Дополнительное применение стероидов снижает остроту местных реакций, но увеличивает длительность клинических проявлений. Для заживления реактивных изменений может потребоваться от 4 до 8 недель.
Лазеротерапия может использоваться для лечения более обширных очагов поражения. Лазер проникает в ткань на 3 — 5 мм, и вызывает коагуляцию ткани, препятствуя гистологической диагностике, и создаёт риск занижения стадии заболевания. Для заживления участков, подвергшихся абляции может потребоваться до 2 — 3 месяцев. Лечение лазером обычно хорошо переносится, но имеются и осложнения, включающие выраженный болевой синдром и кровоточивость в местах лечения [9]. Пациенты, подвергнутые лазеротерапии, имеет более высокую частоту развития рецидивов и риск прогрессирования по сравнению с другими методами лечения. В исследовании B.P. van Bezooijen et al. из 19 пациентов, получавших лазерную терапию, у 5 (26,3%) был верифицирован рецидив ЭК, им потребовалось повторное вмешательство. Средний период наблюдения составил 32 месяца, а у одного пациента (5,2%) при явке был диагностирован инвазивный плоскоклеточный рак головки полового члена [10]. В другом исследовании рецидив заболевания после лазеротерапии диагностирован в 23% случаев. [11].
Средний период наблюдения составил 32 месяца, а у одного пациента (5,2%) при явке был диагностирован инвазивный плоскоклеточный рак головки полового члена [10]. В другом исследовании рецидив заболевания после лазеротерапии диагностирован в 23% случаев. [11].
При криотерапии используют жидкий азот для создания циклов быстрого замораживания и медленного опаивания для достижения температуры от -20 °с до -50 °C, чтобы вызвать повреждение тканей за счёт образования кристаллов льда, что приводит к разрушению клеточных мембран и гибели клеток. Обобщённые данные о применении криотерапии у пациентов с плоскоклеточным раком in situ, говорят о достаточном высоком проценте развития рецидивов заболевания (до 20%) [12].
Фотодинамическая терапия (ФДТ) предраковых поражений полового члена всё ещё находится в стадии изучения. Этот метод включает покрытие поражённой области фотосенсибилизирующим кремом для местного применения, содержащим химические вещества, такие как дельта-5-аминолевулиновая кислота, в течение примерно 3 часов, которые предпочтительно поглощаются и задерживаются злокачественными клетками. Затем зона поражение подвергается воздействию некогерентного света от лампы PDT, что приводит к фотоселективной гибели сенсибилизированных клеток. В исследовании j. Paoli et al. с участием 10 пациентов только 40% имели полный ответ при среднем периоде наблюдения в течение 35 месяцев, при этом было проведено в среднем четыре сеанса лечения [13]. Учитывая высокую эффективность данного метода при лечении аналогичных опухолей экстрагенитальной локализации, сохраняется перспектива более широкого применения фотодинамической терапии при ЭК.
Затем зона поражение подвергается воздействию некогерентного света от лампы PDT, что приводит к фотоселективной гибели сенсибилизированных клеток. В исследовании j. Paoli et al. с участием 10 пациентов только 40% имели полный ответ при среднем периоде наблюдения в течение 35 месяцев, при этом было проведено в среднем четыре сеанса лечения [13]. Учитывая высокую эффективность данного метода при лечении аналогичных опухолей экстрагенитальной локализации, сохраняется перспектива более широкого применения фотодинамической терапии при ЭК.
Все предраковые поражения можно лечить хирургическим путём. Первичное хирургическое иссечение рекомендуется пациентам с обширным изменением головки полового члена, а также тем, кто не соблюдает строгие протоколы лечения и наблюдения. Хирургическое лечение является практически безальтернативным при рецидиве заболевания после других консервативных методов лечения, когда повторное местное лечение приводит к появлению грубых рубцов и обнажённой головки, что может затруднить клинический мониторинг.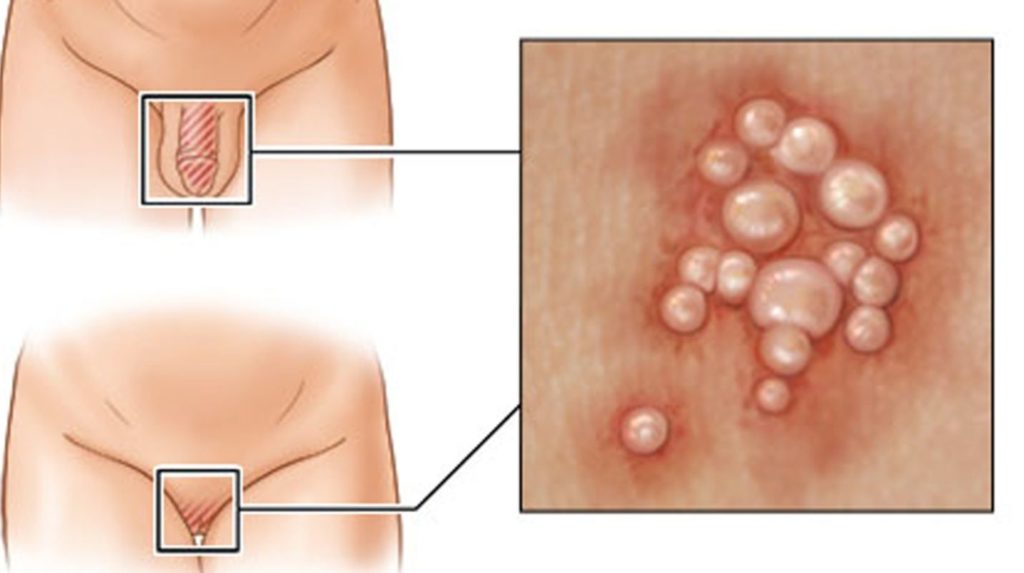
Процедура тотальной шлифовки головки полового члена (TGR) обеспечивает наиболее эффективный хирургический подход к лечению: иссечение поражённого участка с адекватным краем с последующей пересадкой кожи. Методика была впервые описана A. Bracka для лечения тяжёлой формы лейкоплакии, но был адаптирована и для стадий Tis / T1 [14]. Частичная шлифовка головки полового члена (PGR) также используется в качестве основного хирургического подхода для лечения ЭК на головке. Этот метод основан на тех же принципах, что и TGR, но используется в случаях одиночных локализованных очагов, поражающих менее 50% головки.
Альтернативным подходом является иссечение с использованием микрографической хирургии Мооса, что включает удаление всего очага поражения тонкими срезами с одновременным гистологическим исследованием, чтобы под микроскопом убедиться в интактности краёв резекции. Хотя методика позволяет максимально сохранить нормальную ткань полового члена, она сложна и требует много времени, требуя обучения ей как хирурга, так и патологоанатома для обеспечения адекватной абластики. В обзоре этой методики сообщается о высокой (32%) частоте рецидивов [15], а распространение и использование её во всем мире весьма ограничено.
В обзоре этой методики сообщается о высокой (32%) частоте рецидивов [15], а распространение и использование её во всем мире весьма ограничено.
Близкофокусная рентгенотерапия (БФРГ) является наиболее широко распространённым методом лучевого лечения ЭК. С течением времени частота её применения несколько снизилась в связи расширением арсенала методик лечения, однако полностью отказываться от данной высокоэффективной методики, в настоящее время несколько преждевременно. По данным исследований, эффективность БФРТ составляет около 100% при длительности наблюдения до 60-ти месяцев. Также необходимо отметить, что БФРТ является чуть ли не единственным эффективным лечением рецидивов ЭК, возникших после использования других методов лечения [16][17]. Из недостатков — развитие склероза и рубцовой деформации головки полового члена.
Заключение
Данное клиническое наблюдение свидетельствует о излечивающем эффекте рентгенотерапии при рецидиве ЭК. Режим мультифракционирования суточной дозы позволяет минимизировать рубцовые изменения и косметические дефекты в проекции поля облучения. Гетерогенный характер популяции больных диктует необходимость определения персонализированного индивидуального подхода при проведении лечения в каждой конкретной клинической ситуации.
Гетерогенный характер популяции больных диктует необходимость определения персонализированного индивидуального подхода при проведении лечения в каждой конкретной клинической ситуации.
1. Schulze K, Schwartz RA, Lambert WC. Erythroplasia of Quey-rat. Am Fam Physician. 1984;29(4):185-6. PMID: 6720494
2. Kaye V, Zhang G, Dehner LP, Fraley EE. Carcinoma in situ of penis. Is distinction between erythroplasia of Queyrat and Bowen’s disease relevant? Urology. 1990;36(6):479-82. DOI: 10.1016/0090-4295(90)80181-l
3. Wieland U, Jurk S, Weissenborn S, Krieg T, Pfister H, Ritzkowsky A. Erythroplasia of queyrat: coinfection with cutaneous carcinogenic human papillomavirus type 8 and genital papillomaviruses in a carcinoma in situ. J Invest Dermatol. 2000;115(3):396-401. DOI: 10.1046/j.1523-1747.2000.00069.x
4. Mikhail GR. Cancers, precancers, and pseudocancers on the male genitalia. A review of clinical appearances, histopatholo-gy, and management. J DermatolSurg Oncol. 1980;6(12):1027-35. DOI: 10.1111/j.1524-4725.1980.tb01026.x
DOI: 10.1111/j.1524-4725.1980.tb01026.x
5. Gerber GS. Carcinoma in situ of the penis. J Urol. 1994;151(4):829-33. DOI: 10.1016/s0022-5347(17)35099-1
6. Backes DM, Kurman RJ, Pimenta JM, Smith JS. Systematic review of human papillomavirus prevalence in invasive penile cancer. Cancer Causes Control. 2009;20(4):449-57. DOI: 10.1007/s10552-008-9276-
7. Brown CT, Minhas S, Ralph DJ. Conservative surgery for penile cancer: subtotal glans excision without grafting. BJU Int. 2005;96(6):911-2. DOI: 10.1m/j.1464-410X.2005.05751.x
8. Trecedor J, Lopez Hernandez B. Human papillomavirus and mucocutaneous squamous cell carcinoma. Piel. 1991;6:470-471.
9. Tietjen DN, Malek RS. Laser therapy of squamous cell dysplasia and carcinoma of the penis. Urology. 1998;52(4):559-65. DOI: 10.1016/s0090-4295(98)00308-2
10. van Bezooijen BP, Horenblas S, Meinhardt W, Newling DW. Laser therapy for carcinoma in situ of the penis. J Urol. 2001;166(5):1670-1. DOI: 10.1097/00005392-200111000-00013
11. Windahl T, Andersson SO. Combined laser treatment for penile carcinoma: results after long-term followup. J Urol. 2003;169(6):2118-21. DOI: 10.1097/01. ju.0000067361.81295.a2
Windahl T, Andersson SO. Combined laser treatment for penile carcinoma: results after long-term followup. J Urol. 2003;169(6):2118-21. DOI: 10.1097/01. ju.0000067361.81295.a2
12. Hansen JP, Drake AL, Walling HW. Bowen’s Disease: a four-year retrospective review of epidemiology and treatment at a university center. Dermatol Surg. 2008;34(7):878-83. DOI: 10.1111/j.1524-4725.2008.34172.x
13. Paoli J, Ternesten Bratel A, Lowhagen GB, Stenquist B, Forslund O, Wennberg AM. Penile intraepithelial neoplasia: results of photodynamic therapy. Acta Derm Venereol. 2006;86(5):418-21. DOI: 10.2340/00015555-0130
14. Depasquale I, Park AJ, Bracka A. The treatment of balanitis xerotica obliterans. BJU Int. 2000;86(4):459-65. DOI: 10.1046/j.1464-410x.2000.00772.x
15. Shindel AW, Mann MW, Lev RY, Sengelmann R, Petersen J, Hruza GJ, Brandes SB. Mohs micrographic surgery for penile cancer: management and long-term followup. J Urol. 2007;178(5):1980-5. DOI: 10.1016/j.juro.2007.07.039
16. Бровкина А.Ф. Вайнштейн Е.С. Воробьев Ю.И. Клиническая рентгенрадиология. Москва: Издательство «Медицина»; 1985.
Бровкина А.Ф. Вайнштейн Е.С. Воробьев Ю.И. Клиническая рентгенрадиология. Москва: Издательство «Медицина»; 1985.
17. Агеева Н.А., Джабаров Ф.Р., Толмачев В.Г. Критерии эффективности режимов фракционирования близкофокусной рентгенотерапии базальноклеточного рака кожи лица. В сборнике: Наука сегодня: глобальные вызовы и механизмы развития Материалы международной научно-практической конференции: в 2 ч. Вологда: Научный центр «Диспут»; 2017.
Болезнь Кейра (эритроплазия)
Стадии
- инвазивная;
- неинвазивная.
Каждая из стадий имеет свои особенности.
Причины
Определить причины возникновения, способствующие развитию недуга не представляется возможным. Провоцирующими факторами являются:
- хронический баланопостит;
- неблагоприятные условия смегмы на слизистой головки полового члена;
- генитальный герпес;
- травмирование кожи на мужском половом органе.
- вирус папилломы;
Также к образованию патологии приводит несоблюдение правил гигиены.
Симптомы
Главным признак – появление единого очага, находящегося на слизистой. В большинстве случаев он располагается на головке органа, а у женщин – вокруг вульвы. При этом его границы выглядят равномерно и имеют круглую форму. В зоне поражения ощущается дискомфорт и небольшая инфильтрация. Очаг имеет ярок-красный или коричневый оттенок, его поверхность блестящая и гладкая. При прогрессировании происходит усиление инфильтрации, из-за этого возможно образование эрозий. Когда к заболеванию присоединяется инфекция, место очага становится желтым и появляется гной.
Обычно при эритроплазии очаг всего один, с фестончатыми краями. Через определенное время его поверхность покрывается корочками и начинает кровоточить. Рост эрозий свидетельствует о развитии инвазии патологических клеток.
Если болезнь перешла в ротовую полость, очаги локализуются на слизистой губ и языке. Поражающие элементы приобретают бархатную структуру с видимыми границами ярко-красного цвета. Структура новообразования обычно покрыта эрозиями. Пациенты с этой патологией нередко страдают от жжения в области опухоли.
Пациенты с этой патологией нередко страдают от жжения в области опухоли.
Эритроплазия зачастую появляется после 50 лет, преимущественно у представителей сильного пола, не подвергшихся обрезанию. При несвоевременном лечении опухоль трансформируется в плоскоклеточный рак.
При появлении одного из перечисленных проявлений нужна консультация врача уролога-андролога.
Диагностика
Перед началом обследования полагается осмотр у уролога-андролога. На приеме доктор изучает историю болезни и выслушивает жалобы пациента, после этого назначает диагностику, основой которой является изучение клинических симптомов и проведение гистологического и цитологического анализа.
Для диагностирования заболевания используют тест, предусматривающий наложение на зону поражения компресса
с раствором толуидинового синего (1%), из-за этого область эритроплазии окрашивается в синий цвет.
Дифференциальный диагноз устанавливается исходя из результатов цитологического и гистологического анализа.
Данные процедуры помогают отличить недуг от других схожих по клиническим проявлениям заболеваний.
Лечение
При этом недуге применяется комплексная терапия. Как правило, применяется лучевая, химиотерапия и различные медикаменты. Выбор методики зависит о распространенности процесса. Если наблюдается инвазивная форма, назначается блеомицин. Лекарство вводится внутримышечно или внутривенно. Очень важно, чтобы оно не попало на кожу, поскольку это может привести к некрозу. Раствор блеомицина – 15 мг вводят через день. Если потребуется – курс повторяют.
Наружное лечение прописывается исходя из локализации новообразования. Если инфекция находится на головке органа, используют жидкий азот. Перед криолечением применяют обезболивающие. Процедуру проводят два раза в неделю, курс составляет от 4 до 5 процедур.
Также очень часто применяют фторофуровую мазь. Ее необходимо накладывать на поврежденное место на протяжении двадцати дней.
Если болезнь затронула лимфатические узлы, показано их хирургическое удаление.
Профилактика
Профилактические меры направлены на ранее выявление патологии и адекватное лечение. Также следует уделять внимание личной гигиене.
Эритроплазия Кейра: причины, симптомы, диагностика, лечение
Эритроплазия Кейра (син.: эпителиома бархатистая, эпителиома бархатистая) — рак in situ, по сравнению с болезнью Боуэна, он чаще метастазирует, что может быть связано с особенностями локализации. Появляется на головке полового члена, женских половых органах, в перианальной области или (редко) на слизистой оболочке полости рта. Онкогенный вирус папилломы человека 16 или 33 типа выявляется в 70% случаев.
Причины и патогенез эритроплазии. Эритроплазия Кейра считается внутриэпидермальным раком и относится к группе карцином in situ. В развитии заболевания большое значение имеет несоблюдение личной гигиены. Многие дерматологи считают, что эритроплазия Кейры — это вариант слизисто-полупрозрачной болезни Боуэна.
Симптомы эритроплазии Кейра. Эритроплазия Кейра встречается значительно чаще у мужчин, как правило, старше 50 лет, не подвергавшихся обрезанию. В большинстве случаев на половых органах (у мужчин — на головке полового члена, крайней плоти, у женщин — в области вульвы) появляется единичный, слегка отечный очаг, имеющий резко очерченные неровные границы, округлую или овальную форму. Отмечаются незначительная инфильтрация в очаге и болезненность. Его поверхность характеризуется насыщенным красным цветом, часто с коричневатым оттенком, влажная, блестящая, глянцевая, как бы бархатистая. Со временем наблюдается нарастание инфильтрата, иногда эрозии очага. При вторичном инфицировании отмечают гнойное отделяемое, а очаг покрывается желтоватым налетом.
Эритроплазия Кейра встречается значительно чаще у мужчин, как правило, старше 50 лет, не подвергавшихся обрезанию. В большинстве случаев на половых органах (у мужчин — на головке полового члена, крайней плоти, у женщин — в области вульвы) появляется единичный, слегка отечный очаг, имеющий резко очерченные неровные границы, округлую или овальную форму. Отмечаются незначительная инфильтрация в очаге и болезненность. Его поверхность характеризуется насыщенным красным цветом, часто с коричневатым оттенком, влажная, блестящая, глянцевая, как бы бархатистая. Со временем наблюдается нарастание инфильтрата, иногда эрозии очага. При вторичном инфицировании отмечают гнойное отделяемое, а очаг покрывается желтоватым налетом.
Очаг обычно одиночный, резко очерченный, овальной или округлой формы, часто с фестончатыми краями. Поверхность его насыщенно-красного цвета, с коричневым оттенком, влажная, блестящая, бархатистая. По мере развития процесса инфильтрация становится более выраженной, поверхность может покрываться корками, легко кровоточить, иногда становится вегетативной, эрозированной, что может служить признаком развития инвазии.
Описана локализация эритроплазии Кейра и других участков кожи и слизистых оболочек. Заболевание чаще всего трансформируется в плоскоклеточный рак.
Гистопатология. Изменения аналогичны гистологической картине болезни Боуэна. Наблюдаются неравномерный акантоз, очаговый гипер- и паракератоз. В результате нарушения дифференцировки клеток появляются атипичные клетки. В дерме отмечается инфильтрат, состоящий в основном из лимфоцитов и небольшого количества плазматических клеток.
Патоморфология. Во всей толще эпидермиса выявляются мелкие, неправильно расположенные, соединенные между собой тяжи атипичных клеток. В отличие от классической картины болезни Боуэна дискератоз отсутствует. В остальном гистологическая картина соответствует базалоидно-буоноидному типу пролиферации эпидермальных тяжей.
Дифференциальная диагностика. Дифференцируют кериловую эритроплазию от баланопостита (вульвита), крауроза, плазмоцеллюлярного ограниченного баланопостита Зоона, ограниченного псориаза, экземы, фиксированной эритемы, красного плоского лишая, спиналомы, педжетоидной эпителиомы, болезни Педжета, сифилиса. Эритроплазию Каира дифференцируют также с бовеноидным папулезом, генитальной формой красного плоского лишая, фиксированной лекарственной эритемой, ограниченным плазмоцеллюлярным баланитом Зоона, при котором эпителий обычно истончен, а в дерме имеется плотный воспалительный инфильтрат с большим количеством плазмоцитов. Капилляры обычно расширены, могут появиться отложения гемосидерина. Атипичных разрастаний эпителия не выявляют. Ввиду большого клинического сходства этих заболеваний окончательный диагноз ставят на основании данных гистологического исследования.
Эритроплазию Каира дифференцируют также с бовеноидным папулезом, генитальной формой красного плоского лишая, фиксированной лекарственной эритемой, ограниченным плазмоцеллюлярным баланитом Зоона, при котором эпителий обычно истончен, а в дерме имеется плотный воспалительный инфильтрат с большим количеством плазмоцитов. Капилляры обычно расширены, могут появиться отложения гемосидерина. Атипичных разрастаний эпителия не выявляют. Ввиду большого клинического сходства этих заболеваний окончательный диагноз ставят на основании данных гистологического исследования.
Лечение эритроплазии Кейра. Назначают блеомицин, лучевую терапию, хирургическое иссечение и наружно — цитостатические мази.
[1], [2], [3], [4], [5], [6], [7], [8], [9]
Причины, симптомы, диагностика и особенности лечения
Мужчины в несколько раз чаще обращаются к врачу с симптомами нарушения работы мочеполовой системы, чем представительницы прекрасного пола. Наибольшую опасность представляют предраковые состояния и злокачественные образования. К первой группе патологий относится эритроплазия Кейра. Что это?
К первой группе патологий относится эритроплазия Кейра. Что это?
Описание болезни
Под эритроплазией Кейра понимают предраковое поражение слизистых оболочек. В медицинской практике можно встретить и другое название этой патологии – эпителий бархатистый. В большинстве случаев заболевание поражает головку полового члена. Редко эритроплазию диагностируют у представительниц прекрасного пола. При этом очагами патологического процесса являются слизистые оболочки половых органов, полости рта и перианальной области.
Эритроплазия Кейра и болезнь Боуэна имеют много общих признаков, но ряд специфических признаков позволяет выделить первую как самостоятельную форму опухоли. Обычно его диагностируют у мужчин в пожилом возрасте. Для этого заболевания характерна склонность к перерождению в плоскоклеточный рак (30% всех случаев). У каждого пятого больного имеются метастазы, что свидетельствует о неблагоприятном прогнозе.
Этиология заболевания
Представители сильного пола старше 55 лет чаще всего страдают проявлением такой патологии, как эритроплазия Кейра. Причины его развития до сих пор неизвестны. Медики выделяют целую группу факторов, способствующих появлению симптомов заболевания. Среди них можно отметить:
Причины его развития до сих пор неизвестны. Медики выделяют целую группу факторов, способствующих появлению симптомов заболевания. Среди них можно отметить:
- Хронический баланопостит;
- Заражение вирусом папилломы;
- генитальный герпес;
- Периодические травмы тканей полового органа;
- Несоблюдение элементарных правил личной гигиены.
Под влиянием одного или одновременно нескольких факторов развивается эритроплазия Кейры.
Симптомы и первые признаки недуга
Основным признаком заболевания является появление единичного очага на слизистой оболочке. У мужчин она располагается на головке полового члена, у женщин — в области вульвы. Очаг поражения имеет ровные края, красноватый или коричневатый оттенок. Его поверхность блестящая, слегка бархатистая. При пальпации возможна болезненность. По мере развития патологического процесса на этом месте возникают мелкие эрозии. При инфицировании поверхность очага становится желтой, появляется гнойный секрет.
Эритроплазия Кейра в полости рта характеризуется специфической клинической картиной. Высыпания локализуются на поверхности языка и слизистых губ. Они имеют красноватый оттенок, четкие границы. Консистенция образований в основном мягкая, не исключены мелкие эрозии.
Методы диагностики
При подозрении на эритроплазию врач сначала изучает клинические проявления патологии, затем приступает к гистологическим исследованиям. В основе диагностики лежит простая проба, во время которой на место поражения наносится аппликация или раствор толуидинового синего. Участок эритроплазии окрашивается в синий цвет, при этом обычный оттенок эритемы не изменяется.
Еще одним диагностическим признаком заболевания является четкое обрамление очага. При воспалительных процессах они имеют менее выраженные контуры, а применение кортикостероидов сопровождается быстрым регрессом высыпаний.
Важным этапом обследования больного является дифференциальная диагностика. Симптоматика заболевания во многом схожа с проявлениями баланита Зун. Поэтому поставить окончательный диагноз, основываясь только на клинических признаках, невозможно. В этом случае необходимо прибегнуть к помощи гистологического/цитологического исследования. Возникающая картина, как правило, похожа на болезнь Боуэна. На взятом образце небольшое количество атипичных клеток, очаговый гиперкератоз.
Поэтому поставить окончательный диагноз, основываясь только на клинических признаках, невозможно. В этом случае необходимо прибегнуть к помощи гистологического/цитологического исследования. Возникающая картина, как правило, похожа на болезнь Боуэна. На взятом образце небольшое количество атипичных клеток, очаговый гиперкератоз.
Основное отличие от сифилитического шанкра — отсутствие утолщения и регионарного склераденитита. Однако на стадии трансформации в плоскоклеточный рак эритроплазии Кейра сопровождается уплотнением тканей. Последующим метастазированием в паховые лимфатические узлы является их увеличение. Для уточнения диагноза иногда требуется цитологическое исследование. Если в отпечатке отделяемого отсутствуют бледные трепонемы, но опухолевые клетки четко различаются, также подтверждается эритроплазия.
Принципы лечения
Заболевание эритроплазия Кейра предполагает комплексный подход к лечению, который состоит из химиотерапии и применения наружных средств. Применение конкретных препаратов зависит от стадии патологического процесса, определяемой на основании результатов гистологического исследования.
Применение конкретных препаратов зависит от стадии патологического процесса, определяемой на основании результатов гистологического исследования.
При инвазивной форме заболевания назначают химиотерапевтические препараты. Среди них самым эффективным является «Блумицин». Препарат вводят внутримышечно или внутривенно, соблюдая меры предосторожности и избегая попадания на поверхность кожи. Разовая доза составляет 15 мг. Для инъекций каждый раз, когда готовят новый раствор, их необходимо повторять через день. Учитывая состояние больного, может быть назначена повторная доза препарата. Временной интервал между курсами лечения составляет не менее двух месяцев.
Наружное лечение заболевания подбирается в зависимости от локализации очага. Например, поражение головки полового органа предполагает применение жидкого азота. Перед началом криотерапии применяют анестетики. Процедуры повторяются два раза в неделю, а весь курс состоит из пяти сеансов. Фторофуриновая или фторурациловая мазь применяется также при болезни эритроплазии Кейра. Его наносят непосредственно на очаг поражения. Курс лечения 20 дней.
Его наносят непосредственно на очаг поражения. Курс лечения 20 дней.
При инвазивной форме, когда имеется выраженная реакция со стороны паховых лимфатических узлов, рекомендуется проведение рентгенотерапии. Развитие патологии на половых органах часто требует оперативного вмешательства. Операция предполагает удаление крайней плоти, что приводит к замедлению или регрессу заболевания. Основным показанием к оперативному вмешательству является осложненная эритроплазия Кейра.
Лечение народными средствами
Перед применением рецептов народной медицины необходимо проконсультироваться со специалистом. Самолечение предраковых состояний может не только не дать должного эффекта, но и усугубить течение болезни.
- При этом заболевании народные знахари советуют употреблять траву заячьей капусты. Его следует разбавить, а затем нанести на пораженные участки.
- Можно использовать свежий сок травы тысячелистника (50 мл) и болиголова (25 мл). В полученную смесь добавить 100 мл морковного сока.

