Фосфатаза щелочная повышена лечение: Щелочная фосфатаза в крови норма и причины отклонения от нормы
Что такое щелочная фосфатаза в биохимическом анализе крови
Особо важную роль в организме человека имеет фосфорно- кальциевый обмен. Правильная работа этого обмена влияет на работу почти всех жизненно важных систем организма человека — от костно-мышечной ткани, до печени. Для нормального обмена веществ необходима работа ферментов. Эти ферменты имеют название — фосфатаза щелочная (ЩФ). Для диагностики заболеваний пациенты сдают анализ крови, где определяется норма ЩФ.
Что такое щелочная фосфатаза в анализе? В биохимическом анализе крови щелочная фосфатаза помогает своевременно определить не только тяжелые заболевания систем жизнедеятельности человека, но и онкологические опухоли. Для того, чтобы провести исследование, пациенту необходимо сдать кровь на общий анализ и биохимию. Анализ крови покажет в какой концентрации находиться фермент.
Как работают ферменты
С различными продуктами питания, в организм человека поступает фосфорная кислота. В полном составе она не усваивается организмом. В действие вступают ферменты ЩФ. Они отделяют фосфорную кислоту от других элементов, и расщепляют ее.
В действие вступают ферменты ЩФ. Они отделяют фосфорную кислоту от других элементов, и расщепляют ее.
Затем, ЩФ в крови, выступает в роли катализатора. Ферменты доставляют фосфор в ткани всех внутренних систем организма. Фосфор обеспечивает клеткам необходимый уровень метаболизма.
Если в тканях появляется патология или новообразования, процесс усвоения фосфора замедляется. Уровень ферментов отклоняется от нормы, и происходит нарушение обмена веществ. Анализ крови в этот момент показывает скачок уровня ЩФ. Биохимия позволяет точно определить патологию внутренних органов человека.
Что показывает анализ крови
Чаще всего биохимический анализ крови на щелочную фосфатазу и его норму, применяют в комплексном исследовании, совместно с определением других веществ. Биохимия крови помогает диагностировать:
- Нарушение обменных процессов в период беременности.
- Появление камней в желчном пузыре.
- Поражение косной ткани.
- Онкологическое заболевание.

- Развитие инфекционного мононуклеоза.
- Появление патологии печение и почек.
Отклонение в нормальных показателях щелочной фосфатазы может показать эффективность проводимой терапии. Чаще всего этот анализ назначают перед сложной операцией. На него будет напрямую влиять прием тех или иных лекарственных препаратов. Например: Фенобарбитал, Ранитидин, Папаверин, Фуросемид и другие.
ЩФ в биохимическом анализе может иметь значение выше нормы даже в анализе здорового человека. Это может означать, что в организме пациента высокий уровень метаболизма. Повышена щелочная фосфатаза обычно бывает:
- У спортсменов, в период высоких спортивных нагрузок.
- У будущих мам, и у женщин в период лактации.
- У ребенка в период развития и формирования костей
- У взрослых людей в период обильного приема пищи.
Ситуаций значительно хуже, если щелочная фосфатаза в крови имеет показатель ниже нормы. Это значит, что в организме происходят патологические процессы:
- Нарушение в работе щитовидной железы.

- Дисбаланс в микроэлементах.
- Переизбыток витамина D в тканях.
- Авитаминоз, с дефицитом витаминов В и С.
Низкий уровень щелочной фосфатазы может быть обусловлен приемам лекарственных препаратов, в состав которых входят статины и сульфаниломиды.
Как правильно сдать анализ
Для получения точных результатов, необходимо обеспечить качественный ход анализа. Забор крови делается из вены. Сдавать анализ нужно утром, натощак. Лучше всего, не употреблять пищу минимум за 10-12 часов до анализа.
Перед анализом потребуется исключить тяжелые физические нагрузки. Минимум за 2 суток рекомендуется отказаться от активного образа жизни и физического труда. Щелочная фосфатаза повышена в период занятия спортом. Поэтому, любая физическая активность, будет искажать результат анализа. Дети особенно активно себя ведут на прогулках.
Поэтому, нужно исключить подвижные игры за сутки до забора крови.
При подготовке к анализу следует полностью отказаться от употребления любых алкогольных напитков. Прием лекарств, необходимо ограничить, если они не несут жизненно — важную функцию. Перед проведение анализа лучше не проходить физиотерапевтические процедуры и аппаратные исследования (рентген, флюорография и т.д.).
Прием лекарств, необходимо ограничить, если они не несут жизненно — важную функцию. Перед проведение анализа лучше не проходить физиотерапевтические процедуры и аппаратные исследования (рентген, флюорография и т.д.).
Как оценить результат анализа
Норма щелочной фосфатазы в крови варьируется в зависимости возраста человека и его пола. Незначительные отклонения от нормы бывают естественной погрешностью анализа. Какое отклонение считать незначительным? На этот вопрос может ответить только лечащий врач.Чтобы ориентироваться в вопросе, достаточно знать ориентировочные нормы щелочной фосфатазы:
- У взрослых мужчин норма ЩФ от 30 до 130 ед/л.
- У взрослых женщин норма в крови ЩФ от 30 до 120 ед/л.
- У детей в подростковом возрасте норма содержания от 150 до 280 ед/л.
- У детей новорожденных, и у детей до 9 лет норма содержания от 250 до 350 ед/л.
В некоторых лабораториях результат может расчитываться в мкмоль/л. Если у вас в анализе крови написано мкмоль, привести результат к общепринятым еденицам может только врач. Высокий показатель ЩФ в крови детей должен отвечать особенностями возраста. В детском возрасте в организме человека происходит развитие костной ткани, рост внутренних органов, и высокая двигательная активность. Для этих процессов жизненно необходима высокая концентрация ферментов, отвечающих за метаболизм.
Высокий показатель ЩФ в крови детей должен отвечать особенностями возраста. В детском возрасте в организме человека происходит развитие костной ткани, рост внутренних органов, и высокая двигательная активность. Для этих процессов жизненно необходима высокая концентрация ферментов, отвечающих за метаболизм.
Почему уровень ЩФ бывает повышенный
Такой результат анализа на ЩФ бывает значительно чаще, чем пониженный уровень щелочной фосфатазы. Если можно исключить, что повышение уровня возникло в следствие занятия спортом или после приема тяжелой пищи, то расшифровка может говорить о наличии серьезных заболеваний.
Наиболее вероятными причинами повышенной ЩФ в крови будут болезни печени:
- Обструктивный панкреатит.
- Гепатит С.
- Мононуклеоз.
- Жировая дистрофия печени.
- Холестаз.
- Злокачественная опухоль.
- Бактериальные и вирусные инфекции.
Еще одной группой заболеваний, которые диагностируются при повышенном уровне ЩФ, являются патологии костной ткани:
- Рахит.

- Болезнь Педжета.
- Акромегалии.
- Миелофиброз.
- Лейкемия.
- Миелома.
Изменения гормонального фона, тоже приводят к нарушению работы внутренних органов и развитию опасных заболеваний. В следствии развития болезней, обусловленных гормонами, так же повышается уровень ферментной концентрации. Поэтому результат анализа, значительно превышающий норму, может свидетельствовать о наличии заболеваний:
- Гипертиреоз, гиперпаратиреоз.
- Остеомаляция.
- Рахит.
- Остеогенная саркома.
- Опоясывающий лишай.
- Гиперфункция надпочечников.
Прием противозачаточных препаратов на постоянном уровне, может повлечь за собой обострение заболеваний печени. Если прием препаратов длительный (более 3 лет), то анализ на определение уровня ферментов будет завышенным.
Высокий показатель щелочной фосфатазы может быть после перелома костей. В этот период идет активное срастание костной ткани, и заживление ран.
Поэтому результат выше нормы будет естественным явлением.
Крайне высокий показатель уровня ферментов при обследовании абсолютно точно свидетельствует о наличии онкологического заболевания костей. Но такой результат требует расширения анализа, чтобы точно диагностировать очаг поражения и степень развития рака.
Длительный прием алкогольных напитков при алкоголизме способствует разрушению клеток печени. Любые анализы ферментов у таких пациентов будут повышены.
Почему уровень ЩФ бывает пониженный
Пониженный уровень щелочной фосфатазы в биохимическом анализе крови бывает обусловлен недостатком питания. Если рацион человека не сбалансирован, или количество еды недостаточно, это приводит к замедлению процесса метаболизма. Клетки и ткани перестают функционировать в стабильном режиме. Во внутренних органах начинаются необратимые последствия, и появляются очаги заболеваний. Такие последствия трудно поддаются медикаментозному лечению.
Если пациент не жалуется на недостаток пищи, то низкий уровень щелочной фосфатазы нередко, демонстрирует наличие серьезных заболеваний:
- Гипофосфатазия (нехватка фосфора в организме).
- Низкое содержание белка.
- Дисфункция паращитовидных желез.
- Злокачественная анемия.
- Дефицит витаминов и микроэлементов.
Низки уровень ферментов бывает у доноров в период сдачи больших объемов крови. При этом для поддержки нормального функционирования организма донора назначают прием витаминов и биологически активных добавок.
Во время менопаузы у женщин как правило наблюдается замедление всех процессов в организме. В том числе замедляется и метаболизм. Поэтому немного понижена ферментная активность. Это считается нормальным.
Прочтение этого текста требует наличия некоторой медицинской подготовки.
Разработка нормальных границ любого биохимического показателя по определению подразумевает, что 2,5% здоровых людей не уложатся в условно нормальные рамки. Чем больше тестов используется одновременно, тем больше получаем отклонений. Во всех случаях полагается дать оценку факту, т. е. заключить, является это отклонение клинически значимым или незначимым. Естественно, сделать это можно лишь с учетом всего индивидуального клинического контекста. В последнее время эту оценку полагается излагать в медицинском документе; это давно уже принято за правило при клинических испытаниях лекарств.
Чем больше тестов используется одновременно, тем больше получаем отклонений. Во всех случаях полагается дать оценку факту, т. е. заключить, является это отклонение клинически значимым или незначимым. Естественно, сделать это можно лишь с учетом всего индивидуального клинического контекста. В последнее время эту оценку полагается излагать в медицинском документе; это давно уже принято за правило при клинических испытаниях лекарств.
В отношении конкретно печеночных тестов известно, что повышенные значения их встречаются чаще, а именно у 5% людей, не имеющих симптомов патологии печени. Играют роль такие факторы, как возраст, пол, группа крови и др.; физиологические состояния, например беременность. Отметим, и то, что синдром Жильбера (доброкачественная гипербилирубинемия) имеет место у 5% популяции.
Наибольшие трудности возникают у бессимптомных, точнее малосимптомных пациентов. Тесты классифицированы в таблице 1.
Таблица 1. Диагностический минимум биохимических печеночных тестов
| Аланинаминотрансфераза, АЛТ (≤45) | ↑ — Повреждение гепатоцитов |
| Аспартатаминотрансфераза, АСТ (≤35) | ↑ — Повреждение гепатоцитов |
| Билирубин (2-17) | ↑ — Холестаз, билиарная обструкция или нарушение конъюгации |
| Щелочная фосфатаза, ЩФ (норма зависит от метода) | |
| 5’- Нуклеотидаза, 5-НТ (норма зависит от метода) | ↑ — Холестаз или билиарная обструкция |
| γ — Глютамилтрансфераза, ГГТП (≤ 30) | ↑ — Холестаз или билиарная обструкция |
| Лактатдегидрогеназа, ЛДГ (≤ 450) | ↑ — Неспецифическое для болезней печени повреждение гепатоцитов |
| Альбумин (40-60) | ↓ — Снижение синтетической функции |
Протромбиновое время (ПВ): 10. 9-12.5 сек (и МНО) 9-12.5 сек (и МНО) | ↑ — Снижение синтетической функции |
Если подозревается лабораторная ошибка, измененный тест обычно повторяют. Однако получение результата нормального не исключает того, что прежнее отклонение было истинным, это может отражать естественные колебания при болезни. Например при гепатите С АЛТ может стать нормальной, но это не коррелирует с тканевыми изменениями. Нормальный результат, к сожалению, не исключает болезни печени. Необходимо учитывать и факт, что чувствительность и специфичность определения активности ферментов ограничены.
ЛДГ содержится в сердце и скелетных мышцах, в печени, легких, клетках крови. В печени — изофермент ЛДГ5.
Печень синтезирует 10-12 г альбумина в сутки. Содержание альбумина менее 30 г/л свидетельствует о хронизации болезни печени.
ПВ отражает скорость превращения протромбина в тромбин. Оно связано с факторами I, II, V, VII, X свертывания крови, с уровнями фибриногена и протромбина. В печени синтезируются все факторы кроме VIII.
Период полужизни сывороточного альбумина 20 дней, а факторов коагуляции — менее суток. Если гипоальбуминемия отражает хронизацию, то увеличение протромбинового времени может служить маркером тяжести острой дисфункции печени. Например, при остром вирусном гепатите увеличение ПВ на 5-6 сек говорит о возможности молниеносного некроза. Его выявление возможно благодаря короткому периоду полураспада (ключевого) фактора VII коагуляции.
БИЛИРУБИН
Билирубин формируется из гема в ретикуло-эндотелиальной системе. Фракции прямого и непрямого билирубина определяют с 20-х годов прошлого столетия. Но только в 60-х годах было констатировано, что непрямой Б соответствует его неконъюгированной форме, а прямой Б — это комбинация моно- и диглюкуронидов Б, т. е. связанный Б). Термины «прямой/непрямой» используются все реже.
Содержание неконъюгированного Б в сыворотке отражает баланс между его продукцией и гепатобилиарной экскрецией. Неконъюгированная ГБ сама по себе не опасна, но повышает риск образования пигментных желчных камней.
Конъюгированная ГБ отражает болезни паренхимы печени или билиарную обструкцию. При конъюгированной ГБ значимые количества Б попадают в мочу. Холестаз бывает вне- и внутрипеченочный, при этом ГБ может быть без одновременного отклонения активности ферментов.
Колебания показателя билирубина ото дня ко дню составляют 15-30%; цифра возрастает в 1,5-2 раза после длительного голодания, снижается на 15% при приеме противозачаточных таблеток, снижается на 33% во втором триместре беременности, повышается на 50% после физической нагрузки у мужчин; лабораторные ошибки — гемолиз крови — меняет показатели, пребывание образца крови на свету в течение часа снижает показатель на 50%.
Таблица 2. Основные причины гипербилирубинемии (ГБ)
| Синдром Жильбера Неэффективный эритропоэз (В12-дефицит и др.) Гемолиз (в т. ч. при гематрансфузии) Рассасывание обширной гематомы |
| Билиарная обструкция Гепатиты Цирроз Лекарства / токсины Первичный билиарный цирроз Первичный склерозирующий холангит Внутрипеченочный холестаз беременных Доброкачественный рекуррентный холестаз |
АМИНОТРАНСФЕРАЗЫ
Аминотрансферазы — ферменты глюконеогенеза. АСТ (АсАТ) имеет цитозольный и митохондриальный изоэнзимы. АЛТ (АлАТ) — цитозольный фермент. Ферменты АСТ и АЛТ применяются в диагностике болезней печени с 1955 года. Они встречаются в клетках различных тканей, причем наибольшая активность АСТ — в печени, в сердце и скелетной мускулатуре, в почках. АЛТ находится в основном в цитоплазме клеток печени и, в меньшей степени, в мышечных клетках. Следовательно, повышение м. б. при эндокардитах, инфаркте сердца, мышечно-скелетных травмах. Наибольшее повышение наблюдается при гепатитах любых, в т. ч. ишемическом. Степень пропорциональна выраженности острого повреждения печени.
АСТ (АсАТ) имеет цитозольный и митохондриальный изоэнзимы. АЛТ (АлАТ) — цитозольный фермент. Ферменты АСТ и АЛТ применяются в диагностике болезней печени с 1955 года. Они встречаются в клетках различных тканей, причем наибольшая активность АСТ — в печени, в сердце и скелетной мускулатуре, в почках. АЛТ находится в основном в цитоплазме клеток печени и, в меньшей степени, в мышечных клетках. Следовательно, повышение м. б. при эндокардитах, инфаркте сердца, мышечно-скелетных травмах. Наибольшее повышение наблюдается при гепатитах любых, в т. ч. ишемическом. Степень пропорциональна выраженности острого повреждения печени.
Как отдельную категорию рассматривают лиц с повышением АЛТ и АСТ выше в 1.5 и не более чем в 5 раз. Это — самая актуальная группа. Хроническим подъемом АЛТ или АСТ условно считают сохранение отклонений на протяжении полугода. Повреждение печени вовсе необязательно означает некроз, это может быть обратимое состояние в виде повышения проницаемости клеточных мембран. Одновременное повышение АЛТ и АСТ обычно исключает лабораторную ошибку и говорит о печеночном генезе.
Для алкогольного поражения печени считают характерным соотношение АСТ/АЛТ 2:1 и более + двойное повышение уровня ГГТП. Резкое повышение энзимов редко бывает при хронической АБП. Это происходит при присоединении вирусного гепатита или приема парацетамола. Более высокие трансферазы наблюдают при ишемическом гепатите и других перечисленных в таблице 3 состояниях, включая иногда и холедохолитиаз.
Таблица 3. Основные причины умеренной гипертрансаминаземии (
| Гемолиз | |
| Хронические гепатиты В, С | Миопатии (в т.ч. от статинов) |
| Острые вирусные гепатиты (А-Е, ВЭБ, ЦМВ) | ХСН и ишемический гепатит |
| Стеатоз/стеатогепатит | Гипотиреоз |
| Гемохроматоз | Чрезмерная физ. нагрузка |
| Лекарства/токсины | Синдром макро-АСТ (редко) |
| Аутоиммунный гепатит | |
| Дефицит α1-антитрипсина | |
| Болезнь Вильсона | |
| Алкогольное повреждение печени | |
| Стеатоз/стеатогепатит | |
| Цирроз |
Частая серьезная причина — гепатит С, гепатит В теперь будет встречаться реже (результаты вакцинации). В США инфицированы вирусом гепатита С примерно 4 млн человек, у нас, вероятно, примерно столько же. Антитела к вирусу гепатита С не протективны, четко означают наличие инфекции, но появляются гораздо позже инфицирования. Нужно принимать во внимание, что и HbsAg становится положительным только через 2-8 недель после сдвига печеночных тестов.
В США инфицированы вирусом гепатита С примерно 4 млн человек, у нас, вероятно, примерно столько же. Антитела к вирусу гепатита С не протективны, четко означают наличие инфекции, но появляются гораздо позже инфицирования. Нужно принимать во внимание, что и HbsAg становится положительным только через 2-8 недель после сдвига печеночных тестов.
Относительно новая причина — жировая инфильтрация печени с воспалением или без него (стеатогепатит и гепатоз). Этот диагноз-причину при хронических сдвигах ферментов обычно приходится ставить методом исключения. При неалкогольном стеатозе соотношение АСТ/АЛТ обычно ниже 1:1, а билирубин и альбумин нормальны.
Наследственный гемохроматоз (ГХ) — одна из самых частых генетических болезней с разной выраженностью клиники. Может первично проявляться подъемом трансаминаз. В семейном анамнезе абдоминальные боли, артралгии, импотенция, общая слабость и усталость. Есть и не наследственные формы ГХ.
Аутоиммунный гепатит, болезнь Вильсона и дефицит α-1-антитрипсина встречаются каждое с частотой в популяции примерно 1:6000. При ХАГ более 80% пациентов имеют гипергаммаглобулинемию при электрофорезе. Различают три типа ХАГ.
При ХАГ более 80% пациентов имеют гипергаммаглобулинемию при электрофорезе. Различают три типа ХАГ.
АЛТ: колебания ото дня ко дню составляют 10-30%, в течение суток — до 45% (самый высокий результат днем), физическая нагрузка снижает показатель на 20%. АСТ: колебания ото дня ко дню составляют 5-10%, хорошая физическая нагрузка повышает показатель почти в три раза. На активность обоих ферментов — АЛТ, АСТ — прием пищи не влияет; оба показателя возрастают на 4-50% при ожирении.
НОВЫЕ ЛЕКАРСТВА — СТАРЫЕ ОПАСНОСТИ
У большинства людей с изолированным умеренным подъемом АЛТ болезни печени нет. При подозрении на лекарственное средство (ЛС) как на причину, его можно заменить на другое лекарство. Важно представлять, какие ЛС повреждают печень и при применении каких подъем трансаминаз имеет внепеченочные причины, ведь приходится решать вопрос о целесообразности отмены ЛС или продолжении терапии. Наиболее актуальны сейчас ситуации, связанные с приемом статинов. Также ¾ получающих противосудорожную терапию имеют аномалии печеночных тестов. Условно неблагоприятные печеночные реакции на ЛС разделяют на: ненормальные тесты — когда показатель одного из ферментов не превышает двух норм, и поражение печени — когда один из показателей (не только трансаминаз) в два раза или более превышает верхнюю границу нормы. Риск лекарственных поражений печени более высок при полипрагмазии, особенно в пожилом возрасте. Функциональные нарушения печени обычно исчезают через 4-6 недель после отмены ЛС.
Условно неблагоприятные печеночные реакции на ЛС разделяют на: ненормальные тесты — когда показатель одного из ферментов не превышает двух норм, и поражение печени — когда один из показателей (не только трансаминаз) в два раза или более превышает верхнюю границу нормы. Риск лекарственных поражений печени более высок при полипрагмазии, особенно в пожилом возрасте. Функциональные нарушения печени обычно исчезают через 4-6 недель после отмены ЛС.
Понятие гепатотоксичности включает истинную, связанную с ЛС, токсичность, зависящую от дозы (парацетамол), и идиосинкразию. Вторая — следствие индивидуальной предрасположенности. Гораздо чаще имеем дело с более мягкими состояниями, обусловленными идиосинкразией. Известно более 50 микросомальных изоферментов в печеночной системе детоксикации цитохрома Р450, структура которых кодируется отдельными генами. Генетические различия каталитической активности ферментов объясняют причину развития реакций идиосинкразии к отдельным ЛС. Но и чрезмерное повышение активности ферментов системы цитохрома Р-450 в результате их индукции (например, на фоне алкогольной интоксикации) может сопровождаться резким повышением выработки токсичных метаболитов.
Допегит, Никотиновая кислота, Кетоконазол и Флуконазол провоцируют острый лекарственный гепатит.
Парацетамол — некроз гепатоцитов перицентральной зоны печеночной дольки.
Диклофенак, Финлепсин, Пропилтиоурацил — поражение печени по типу реакции гиперчувствительности. Реакция обычно развивается через 2-4 недели лечения, в особенности при повторном назначении «виновного» ЛС. Клинически отмечается большая вариабельность проявлений: от изолированного острого гепатита умеренной активности до активного гепатита с системными поражениями. Из известных нам НПВС диклофенак значимо чаще дает серьезные печеночные нарушения по сравнению с плацебо. При развитии реакции по механизму гиперчувствительности, когда ЛС выступает в роли гаптена, симптомы могут сохраняться даже спустя много месяцев после отмены ЛС.
Амиодарон — развитие лекарственного стеатогепатита. Он угнетает процесс окисления жирных кислот в митохондриях и нарушает процесс переноса электронов в дыхательной цепи, что способствует активации перекисного окисления липидов. Происходит и подавление катаболизма фосфолипидов в лизосомах, что приводит к развитию фосфолипидоза.
Происходит и подавление катаболизма фосфолипидов в лизосомах, что приводит к развитию фосфолипидоза.
Депакин — поражение печени по типу митохондриальной цитопатии. Механизм данного типа поражения обусловлен блокадой ферментов дыхательной цепи митохондрий, прямым угнетением ферментов метаболитом вальпроата (2-пропилпентаноевой кислотой).
Амоксициллин, Манинил, Сульфонамиды — паренхиматозно-канальцевый холестаз. В патогенезе расстройства, по-видимому, преобладают иммунные механизмы.
Первым шагом в лечении должна быть отмена лекарственного средства. В большинстве случаев отмена «виновного» ЛС относительно быстро приводит к существенному улучшению клинико-лабораторных данных. Но следует учитывать, что необходимо продолжать длительное наблюдение больных, в особенности тех, которые получали препараты с большим периодом полувыведения (например, амиодарон).
Таблица 4. Лекарства, м. б. причиной гипертрансаминаземии
| Метилдофа (Альдомет, Допегит) |
| Никотиновая кислота в высоких дозах |
| Кетоконазол (Низорал) |
| Флуконазол (Дифлюкан) |
| Парацетамол в высоких дозах |
| Диклофенак |
| Карбамазепин (Финлепсин) |
| Пропилтиоурацил |
| Амиодарон (Кордарон) |
| Вальпроевая к-та (Конвулекс, Депакин) |
| Амоксициллин + клавулановая к-та (Амоксиклав) |
| Глибенкламид (Манинил) |
| Сульфаниламиды |
| Гепарин |
| Зафирлукаст (Аколат) |
| Ингибиторы протеиназ (Гордокс, Контрикал) |
| Статины |
| Фенилбутазон (Бутадион) |
ЩЕЛОЧНАЯ ФОСФАТАЗА
ЩФ принадлежит к семейству цинк-содержащих металлоферментов. Содержится преимущественно в печени и костях, 20% находится в стенке кишечника. ЩФ растет, когда в соответствующих тканях имеется метаболическая стимуляция. Так, у подростков возрастает в 2 раза по сравнению с взрослой нормой за счет костного изофермента. При беременности в первом триместре может повыситься в два раза за счет плацентарных изоферментов и более значительно — в предродовом периоде.
Содержится преимущественно в печени и костях, 20% находится в стенке кишечника. ЩФ растет, когда в соответствующих тканях имеется метаболическая стимуляция. Так, у подростков возрастает в 2 раза по сравнению с взрослой нормой за счет костного изофермента. При беременности в первом триместре может повыситься в два раза за счет плацентарных изоферментов и более значительно — в предродовом периоде.
Период полужизни ЩФ составляет неделю, поэтому она начинает расти через 1-2 дня после наступления билиарной обструкции и сохраняется повышенной несколько дней после ее разрешения.
Изолированное повышение ЩФ м. б. единственной аномалией при первичном билиарном циррозе и других холестатических болезнях. Подъем ЩФ при нормальных или слегка повышенных уровнях других показателей может также указывать на инфильтративный (опухолевый) процесс.
Каждый раз приходится разбираться с ЩФ — печеночное или костное она имеет происхождение. Известно также, что ЩФ может повышаться при раках без поражения печени или костей за счет одного изофермента, который теперь называют изоэнзимом (президента) Рейгана. Фракционное определение изоферментов ЩФ позволяет установить источник повышения ее активности. Более специфичным тестом, чем ЩФ, является определение 5′-нуклеотидазы, также из семейства фосфатаз, она существенно повышается только при болезнях печени с холестазом. Она также содержится и в других органах, но не в костях. Другим способом оценки источника служит определение ГГТП.
Фракционное определение изоферментов ЩФ позволяет установить источник повышения ее активности. Более специфичным тестом, чем ЩФ, является определение 5′-нуклеотидазы, также из семейства фосфатаз, она существенно повышается только при болезнях печени с холестазом. Она также содержится и в других органах, но не в костях. Другим способом оценки источника служит определение ГГТП.
Колебания уровня ЩФ ото дня ко дню составляют 5-10%; цифра возрастает в 2-3 раза в третьем триместре беременности, снижается на 20% при приеме противозачаточных таблеток, на 10% выше у курильщиков, на 25% выше при ожирении; физическая нагрузка заметно не влияет; прием пищи меняет показатель у лиц с определенной группой крови.
Таблица 5. Причины подъема щелочной фосфатазы
| Билиарная обструкция |
| Первичный билиарный цирроз |
| Лекарства |
| Инфильтративные болезни печени |
| Метастазы в печень |
| Гепатиты |
| Цирроз |
| Дисфункции билиарных сфинктеров |
| Доброкачественный рекуррентный холестаз |
| Инфекция / воспаление |
| Болезни костей |
| Застойная сердечная недостаточность |
| ХПН (хроническая почечная недостаточность) |
Лимфома и др. злокач. процессы злокач. процессы |
| Ростовой скачок у подростков |
| Беременность (III триместр) |
ГАММАГЛЮТАМИЛТРАНСПЕПТИДАЗА
Этот фермент локализован на каналикулярной мембране гепатоцита, обращенной в желчный капилляр. ГГТП также обнаруживается в почках, в поджелудочной железе, кишечнике и, в меньшей степени, в сердечной мышце. В костях этот фермент отсутствует. Таким образом, подъем ГГТП подтверждает печеночный генез подъема ЩФ.
Вообще же ГГТП повышается при многих ситуациях, например у алкоголиков. Изолированное повышение ГГТП может наблюдаться и после эпизодического приема алкоголя на фоне противосудорожной терапии или приема варфарина. Кстати говоря, присоединение к варфарину диклофенака повышает риск желудочного кровотечения в 3-6 раз.
Таблица 6. Причины повышения ГГТП
| Гепатобилиарные болезни (обычно одноврем. с аномалиями других ферментов) |
| Болезни поджелудочной железы |
| Алкогольная интоксикация |
| ХОБЛ (хроническая обструктивная болезнь легких, хронический обструктивный бронхит) |
| Диабет |
| Острый инфаркт миокарда |
Лекарства (напр. , противосудорожные) , противосудорожные) |
Амоксиклав, Хлорпропамид, Перитол могут провоцировать паренхиматозно-канальцевый холестаз.
Дилтиазем, Бисептол — лекарственный стеатогепатит.
Эстрогены — стеатогепатит и канальцевый холестаз. Развитие холестаза обусловлено подавлением транспорта желчи, не зависящего от желчных кислот.
Противовирусные средства — поражение печени по типу митохондриальной цитопатии.
Финлепсин, Хинидин — поражение печени по типу реакции гиперчувствительности.
Каптоприл — острый лекарственный гепатит.
Таблица 7. Лекарства, могущие спровоцировать подъем билирубина или ЩФ
| Амоксиклав |
| Хлорпропамид |
| Ципрогептадин (Перитол) |
| Дилтиазем |
| Ко-сульфаметоксазол (Бисептол) |
| Эстрогены |
| Противовирусные (Вирамун, Криксиван) |
| Карбамазепин (Финлепсин) |
| Хинидин |
| Каптоприл (Капотен) |
| Аллопуринол |
| Имипрамин (Мелипрамин) |
| Эритромицин |
В стране, где считают деньги, дают следующую оценку слагающимся ситуациям. Повторение анализа трансаминаз стоит 30 долл, обычное клиническое уточняющее обследование (серология вирусных гепатитов, железо сыворотки и т. п.) — уже 350 долл, а расширенное, включающее дополнительную серологию и биопсию печени — 3000 долл. Т. е. своевременное заключение дипломированного специалиста о состоянии здоровья пациента позволяет сэкономить пару тысяч долларов.
Повторение анализа трансаминаз стоит 30 долл, обычное клиническое уточняющее обследование (серология вирусных гепатитов, железо сыворотки и т. п.) — уже 350 долл, а расширенное, включающее дополнительную серологию и биопсию печени — 3000 долл. Т. е. своевременное заключение дипломированного специалиста о состоянии здоровья пациента позволяет сэкономить пару тысяч долларов.
Плохая экология, вредные привычки, несбалансированное питание — все эти факторы негативно влияют на наше здоровье, и первой под удар попадает печень. Провести объективную оценку базовых функций органа можно при помощи такого специфического анализа, как печеночные пробы. В этой статье мы расскажем про основные показатели исследования и какие нарушения оно позволяет определить.
Для чего проводится исследование?
Печень — самый крупный орган в человеческом организме, который выполняет много важных функций:
- участвует в процессе пищеварения. Печень вырабатывает желчь, которая обеспечивает смену желудочного пищеварения на кишечное,
- нейтрализует действие аллергенов, токсических веществ;
- регулирует углеводный, липидный, белковый обмен;
- удаляет из организма избыток гормонов, витаминов;
- синтезирует иммуноглобулины, антитела;
- хранит, распределяет глюкозу и гликоген;
- пополняет запас некоторых витаминов.

Однако полноценно выполнять эти функции печень способна только при отсутствии патологий. Оценить состояние органа позволяют печеночные пробы — биохимическое исследование крови, состоящее из множества лабораторных тестов.
Исследование редко проводится в качестве профилактической меры. Чаще всего тесты назначаются, если у врача есть подозрение на наличие у пациента нарушений работы печени. Например, направление на исследование может быть выдано тем, у кого наблюдается симптоматика, характерная для патологий печени — желтушность кожных покровов и склер, болевой синдром в правом подреберье, резкое снижение веса, тошнота, рвота, появление кисло-горького вкуса во рту. Кроме этого, исследование используется для отслеживания результатов лечения патологий печени.
Показатели, входящие в печеночные пробы, отражают не только работу печени, но и других органов и систем — сердца, почек, кишечника, щитовидной железы, скелетной мускулатуры. Поэтому в ходе исследования также могут быть выявлены нарушения, не связанные с работой печени.
Поэтому в ходе исследования также могут быть выявлены нарушения, не связанные с работой печени.
Врач терапевт Ханова Ирина Ивановна расшифрует ваши анализы в режиме онлайн звонка в приложении Zoom или WhatsApp.
- подробное пояснение врача терапевта.
- альтернативное мнение компетентного специалиста по расшифровке анализов.
- возможность задать вопросы врачу, касающиеся результатов анализов.
Как подготовиться к исследованию?
Подготовка к исследованию заключается в следующем:
- за сутки до сдачи анализа нужно отказаться от алкоголя, избыточной физической активности;
- последний прием пищи должен быть не позже чем за 12 часов до исследования;
- за один час до анализа необходимо исключить курение.
Забор крови выполняется утром натощак. Перед анализом можно употреблять только воду.
Основные показатели печеночных проб
Рассмотрим основные показатели печеночных проб, а также их нормы и причины отклонения от референсных значений.
Аланинаминотрансфераза (АЛТ) и аспартатаминотрансфераза (АСТ)
АЛТ и АСТ — ферменты, которые синтезируются внутриклеточно, принимают участие в углеводном, белковом обмене, поддерживают функционирование многих органов, играют ключевую роль в метаболизме одних из важнейших аминокислот — аланина и аспарагиновой кислоты. При отсутствии патологий ферменты присутствуют в крови лишь в незначительном количестве ⇓⇓⇓
5 дней-6 месяцев
12-17 лет (девочки)
12-17 лет (мальчики)
старше 17 лет (женщины)
старше 17 лет (мужчины)
Несмотря на некоторое сходство, АЛТ и АСТ имеют и отличия:
- АЛТ в большей степени вырабатывается в печени, в меньшей — в мышцах, сердце, поджелудочной железе, почках и других органах. В связи с этим высокий уровень фермента в первую очередь указывает на заболевания печени.
- АСТ содержится в тех же клетках, что и АЛТ, но в миокарде его концентрация значительно выше. Именно поэтому основными причинами повышения АСТ являются не только патологии печени, но и сердечные заболевания.

К основным причинам повышения АЛТ относятся:
- гибель гепатоцитов (клеток паренхимы печени), вызванная вирусным гепатитом, воздействием токсических веществ;
- цирроз печени — хроническая патология, при которой здоровая ткань органа замещается соединительной тканью или стромой;
- внутрипеченочный холестаз — недостаточное выделение желчи, обусловленное нарушением ее выработки клетками печени;
- жировой гепатоз — синдром, сопровождающийся накоплением жира в ткани печени;
- онкология печени.
Менее распространенные причины высоких значений АЛТ:
- сердечная недостаточность;
- инфаркт миокарда;
- воспаление сердечной мышцы;
- воспаление скелетной мускулатуры;
- тяжелые ожоги;
- шок;
- алкоголизм.
Также значение АЛТ может быть повышено при приеме гепатотоксических лекарственных средств, к которым относятся некоторые антибактериальные, анаболические, противозачаточные средства, препараты с содержанием салициловой кислоты. Как правило, повышение АЛТ в этом случае носит временный характер.
Как правило, повышение АЛТ в этом случае носит временный характер.
Повышение АСТ вызывают те же факторы, что и повышение АЛТ. Однако сильный рост АСТ позволяет заподозрить инфаркта миокарда. При некрозе сердечной мышцы уровень аспартатаминотрансферазы может повышаться в 2-20 раз. При этом высокая концентрация фермента обнаруживается еще до появления клинических симптомов заболевания. Нарастание активности фермента АСТ в динамике заболевания может указывать на вовлечение в патологический процесс печени и других органов
Так как концентрация АСТ и АЛТ в крови может повышаться из-за многих факторов, то поставить точный диагноз бывает сложно. Для облегчения дифференциальной диагностики применяется коэффициента Ритиса, который показывает соотношение сывороточных АСТ и АЛТ.
Допустимые значения коэффициента — от 0,9 до 1,7. Отклонение показателя в большую сторону указывает на патологии сердца, в меньшую — на заболевания печени.
Гамма-глютамилтранспептидаза (гамма-ГТП)
Фермент, основным источником которого является гепатобилиарная система, состоящая из печени, желчного пузыря, желчных протоков. Также фермент присутствует в поджелудочной железе, почечных канальцах, кишечнике.
Гамма-ГТП — маркер застоя желчи. При обструкции желчных протоков содержание фермента в крови может повышаться в несколько десятков раз. Гамма-глютамилтранспептидаза является более чувствительным показателем патологий печени, чем АЛТ и АСТ.
При отсутствии нарушений концентрация фермента в крови у женщин составляет 5-39 ед/л, у мужчин — 10-66 ед/л.
Высокие значения показателя могут вызывать следующие патологии печени:
- внутри- и внепеченочный холестазы;
- острый вирусный, хронический гепатиты;
- алкогольный цирроз;
- поражение печени токсическими веществами, лекарственные интоксикации;
- жировое перерождение печени;
- онкологические заболевания печени.

Причины высоких показателей, не связанных с нарушением работы печени:
- воспалительные процессы поджелудочной железы;
- онкология поджелудочной железы, предстательной железы;
- почечные патологии — пиелонефрит, гломерулонефрит, диабетический кетоацидоз и другие.
ГГТП — индикатор заболеваний печени, вызванных алкоголем, так как высокий уровень фермента в сыворотке крови наблюдается у пациентов с алкогольным циррозом и у большинства людей, злоупотребляющих алкоголем.
Щелочная фосфатаза
Фермент, ускоряющий расщепление фосфорной кислоты при рН 8,6-10,1. Содержится практически во всех тканях организма, наиболее высокая концентрация щелочной фосфатазы в клетках костной ткани, печени, почек, слизистой кишечника, плаценте. Референсные значения содержания фермента в крови представлены в таблице⇓⇓⇓
Щелочная фосфатаза – это определенный фермент, относящийся к группе гидролаз. Необходим он для того, чтобы в организме с успехом проходили реакции дефосфорилирования, а именно: отщепление фосфата от органических веществ, которое происходит на молекулярном уровне. Пронося фосфор через мембрану клеток, фосфатаза имеет некоторую постоянную концентрацию в крови и является показателем нормы фосфорно-кальциевого обмена. Название «щелочная» фермент получил за то, что наибольшую активность он проявляет при наличии pH среды в диапазоне от 8,6 до 10,1.
Пронося фосфор через мембрану клеток, фосфатаза имеет некоторую постоянную концентрацию в крови и является показателем нормы фосфорно-кальциевого обмена. Название «щелочная» фермент получил за то, что наибольшую активность он проявляет при наличии pH среды в диапазоне от 8,6 до 10,1.
Несмотря на то что щелочная фосфатаза относится к наиболее часто встречающимся ферментам, до конца механизм её действия не изучен. Стоит отметить, что в организме человека она присутствует практически везде, во всех тканях, но при этом представлена в нескольких разновидностях: почечная, кишечная, плацентарная, печеночная и костная. Что касается сыворотки крови, то у взрослых людей фосфатаза представлена двумя последними изоферментами, в относительно одинаковых количествах. В костях фермент образуется в остеобластах, а в печени в гепатоцитах. Чем выше активность тех или иных клеток, например, при переломах костей или при разрушении клеток печени, тем и уровень фосфатазы в крови становится больше.
Норма щелочной фосфатазы в крови
Что касается нормального уровня содержания щелочной фосфатазы в крови, то эти показания колеблются в довольно широких диапазонах, могут составлять от 44 до 147 МЕ/л. При этом стоит обращать внимание на пол человека, у которого была взята кровь для исследования, а также на его возраст. У беременных женщин этот показатель может быть слегка завышен, также, как и у подростков, находящихся в стадии полового созревания, но не будет указывать на какие-либо отклонения в их организме. Просто это связано с перестройкой некоторых систем жизнеобеспечения, а также с ростом костной ткани или плаценты.
При этом стоит обращать внимание на пол человека, у которого была взята кровь для исследования, а также на его возраст. У беременных женщин этот показатель может быть слегка завышен, также, как и у подростков, находящихся в стадии полового созревания, но не будет указывать на какие-либо отклонения в их организме. Просто это связано с перестройкой некоторых систем жизнеобеспечения, а также с ростом костной ткани или плаценты.
К тому же показатели нормы могут варьироваться и в зависимости от реагентов, применяемых для её исследования в различных лабораториях, так как стандартизированная методика на данный момент времени отсутствует. Конкретные цифры меняются, но диапазон их колебаний, тем не менее, остается незначительным, поэтому при определении нормы можно опираться на следующие усредненные показатели:
для детей до 10 лет — от 150 до 350
для детей от 10 до 19 – от 155 до 500
для взрослых в возрасте до 50 лет – от 30 до 120
для возрастной категории от 50 до 75 – от 110 до 135
для людей старше 75 лет – от 165 до 190
Эти референсные значения указаны в расчете международные единицы на литр.
Щелочная фосфатаза повышена
Исследование повышения или понижения уровня фосфатазы в крови проводят по некоторым показаниям. Это может быть подготовка к хирургическому вмешательству, а также плановый осмотр пациента. Берут кровь на выявление уровня данного фермента и при проведении «печеночных проб», для оценки функциональной способности органа.
Нередко при жалобах пациентов на усталость, потерю аппетита, тошноту или боли в правом подреберье изучают уровень щелочной фосфатазы в крови. Показательным результат является и для диагностики различных поражений костей и костной ткани.
Когда щелочная фосфатаза повышена, это почти всегда означает либо поражение, либо вовлечение в какой-либо патологический процесс или костей, или печени, или желчевыводящих путей. Разграничить и уточнить результаты помогают дополнительные исследования, так, если наряду с данным ферментом имеется завышение уровня АЛТ и АСТ, то это однозначно говорит о болезни печени. Если же в совокупности с щелочной фосфатазой повышен уровень кальция и фосфора, то повреждение костной ткани налицо.
Причины повышения щелочной фосфатазы
В качестве тех или иных причин можно выделить четыре основные подгруппы, которые приводят к повышению в крови уровня данного фермента:
Первая группа – это нарушения, связанные с изменениями или болезнями печени. Это может быть механическая желтуха, которая вызвана непроходимостью желчевыводящих путей, камни, расположенные в желчных протоках, а также возникновение в них рубцов после операций. Рак либо головки поджелудочной железы, либо желудка, либо печени с метастазами. При гепатите любого происхождения наблюдается повышение фосфатазы, так же, как и при циррозе. Ещё одна вирусная инфекция, а именно инфекционный мононуклеоз может стать причиной нарушения работы печени, а как следствие увеличения в крови данного фермента.
Вторая группа – это нарушения, связанные с изменением в костной ткани. Сюда входят такие заболевания, как остеомаляция (размягчение костной ткани из-за дефицита кальция), остеосаркома, метастазы, затрагивающие костную ткань, болезнь Педжета (патологический рост костей с изменением их структуры), переломы, рахит и миеломная болезнь.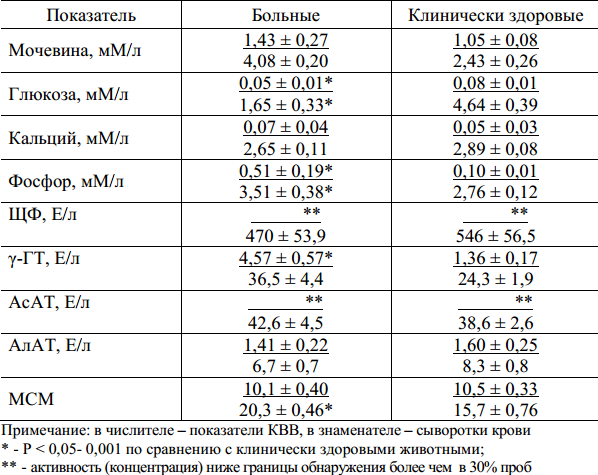
Третья группа – это иные причины. Скачок в показателях уровня щелочной фосфатазы может быть связан с инфарктом миокарда, с язвенным колитом и перфорацией кишечника, а также с гиперпаратиреозом (гормональное заболевание, характеризующееся вымыванием кальция из костей).
Четвертая группа – это состояния, не связанные с болезнями, но обусловленные рядом факторов. Сюда относится беременность, подростковый возраст, здоровые женщины до 20 лет и здоровые мужчины до 30 лет, а также приём антибиотиков и гормональных препаратов с целью контрацепции и ряда других лекарственных средств, входящих в довольно обширный список и содержащий до 250 наименований. Также, если кровь была охлаждена после её забора на изучение, уровень щелочной фосфатазы будет завышен.
Следует отметить, что повышение уровня данного фермента не во всех без исключения случаях является показателем той или иной болезни. Иногда он может превышать норму даже у абсолютно здоровых людей. Поэтому чтобы судить о наличии того или иного патологического процесса, необходимо проводить дополнительные исследования и изучать полученные результаты в комплексе.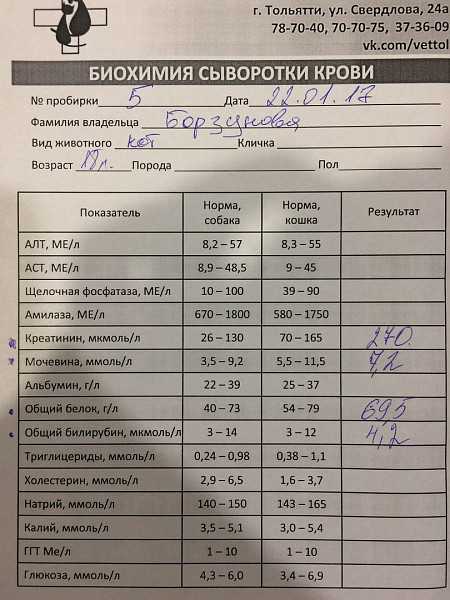
Щелочная фосфатаза понижена
На понижения данного фермента в крови следует обращать внимание, так как подобный показатель может служить признаками ряда заболеваний, не менее опасных, чем и при повышении уровня фосфатазы.
Возможные причины, которые приводят к понижению уровня фермента:
Переливания крови в значительном объеме.
Снижение функциональных возможностей щитовидной железы.
Анемия тяжелой степени тяжести.
Недостаток в организме таких элементов, как магний и цинк.
Редкое заболевание – гипофосфатазия, является врожденным и приводит к тому, что костная ткань размягчается.
У беременных снижение щелочной фосфатазы может стать признаком недостаточности плаценты.
Итак, для того, чтобы качественно оценить результат повышения или понижения уровня щелочной фосфатазы в крови любому специалисту потребуется проведение дополнительных исследований. Стоит помнить, что границы, в которых могут находиться нормальные значения фосфатазы довольно обширные и значительно зависят от возраста испытуемого. Поэтому точно диагностировать наличие того или иного заболевания лишь при повышении уровня данного фермента не может даже врач. Тем не менее этот показатель в совокупности с дополнительными исследованиями может дать полную картину болезни.
Поэтому точно диагностировать наличие того или иного заболевания лишь при повышении уровня данного фермента не может даже врач. Тем не менее этот показатель в совокупности с дополнительными исследованиями может дать полную картину болезни.
Автор статьи: Мочалов Павел Александрович | д. м. н. терапевт
Образование: Московский медицинский институт им. И. М. Сеченова, специальность — «Лечебное дело» в 1991 году, в 1993 году «Профессиональные болезни», в 1996 году «Терапия».
Наши авторы
«Щелочная фосфатаза повышена у ребенка-причины,норма у детей» — Яндекс Кью
В статье рассматривается щелочная фосфатаза,ее норма у детей и причины,по которым она бывает повышена у ребенка в крови.
Содержание
- 1 Что это такое: ЩФ анализ крови?
- 2 Щелочная фосфатаза– норма у детей
- 3 Если щелочная фосфатаза повышена у ребенка – что это значит?
- 3.
 1 Рахит
1 Рахит - 3.2 Лимфобластоз
- 3.3 Другие причины
- 3.
- 4 Выводы
Повышена у ребенка щелочная фосфатаза, как правило, на фоне развивающихся заболеваний печени или костной ткани. Что в результате может стать причиной неправильного формирования опорно-двигательного аппарата или развития патологий печени.
Для исследования показателя у маленького пациента собирается венозная или капиллярная кровь. С целью получения точных результатов необходимо сдавать биоматериал натощак. Для грудничков перерыв с последнего кормления должен быть минимум 2-3 часа. Для остальных детей – минимум 6 часов.
Реклама
Что это такое: ЩФ анализ крови?
Щелочная фосфатаза – это белковый фермент, принимающий участие в обменных реакциях фосфорной кислоты. Именно ЩФ способствует отсоединению молекул фосфатов от белков, нуклеотидов и других молекул. Повышенную активность ЩФ проявляет в рН от 8,6 до 10 (щелочная среда). Наибольшее содержание вещества обнаруживается в молодых клетках костной и печёночной ткани, а также в слизистой оболочке кишечника человека и плаценте.
Повышенную активность ЩФ проявляет в рН от 8,6 до 10 (щелочная среда). Наибольшее содержание вещества обнаруживается в молодых клетках костной и печёночной ткани, а также в слизистой оболочке кишечника человека и плаценте.
У маленьких пациентов щелочная фосфатаза проявляет большую активность, чем у взрослых. Поскольку для них характерен активный рост костей, в которых и содержится фермент.
Исследование назначается педиатром при плановых осмотрах в рамках стандартных лабораторных анализов. При необходимости уточнения наличия заболеваний печени также определяется уровень ЩФ в крови.
Симптомы, при которых необходимо сдать анализ на фермент:
- необъяснимое снижение аппетита у малыша;
- расстройство пищеварения: тошнота или рвота;
- изменение окраски мочи или кала;
- жалобы ребёнка на боли в животе;
- общая слабость малыша, отсутствие активности и сонливость.
При подозрении или установленном факте патологии костей ребёнку также проводится анализ на ЩФ./10_m2.jpg)
Реклама
Щелочная фосфатаза– норма у детей
Поскольку активность фермента отличается у разных возрастов, то и показатели нормы следует подбирать исходя из этого факта. После наступления пубертатного периода следует также учитывать половые различия пациентов. Рассмотрим подробнее значения нормы ЩФ для разных возрастных категорий пациентов.
У новорождённых малышей в первые две недели жизни нормальные значения варьируют от 80 до 250 Ед/л.
Максимальные концентрации вещества характерны для первого года жизни малыша. Так, со второй недели и до 1 года допустимая норма ЩФ от 125 до 173 Ед/л. Именно в этот период отмечается усиленный рост ребёнка, особенно костной ткани. Образуется большое количество молодых клеток костей, которые необходимы для правильного развития организма.
От 1 года до 10 лет референсные значения рассматриваемого показателя находятся в интервале от 137 до 331 Ед/л. А с 10 до 13 лет: от 130 до 415 Ед/л.
После наступления полового созревания, в возрасте от 13 до 15 лет, норма для мальчиков составляет 111- 457 Ед/л, для девочек — 55 – 257 Ед/л.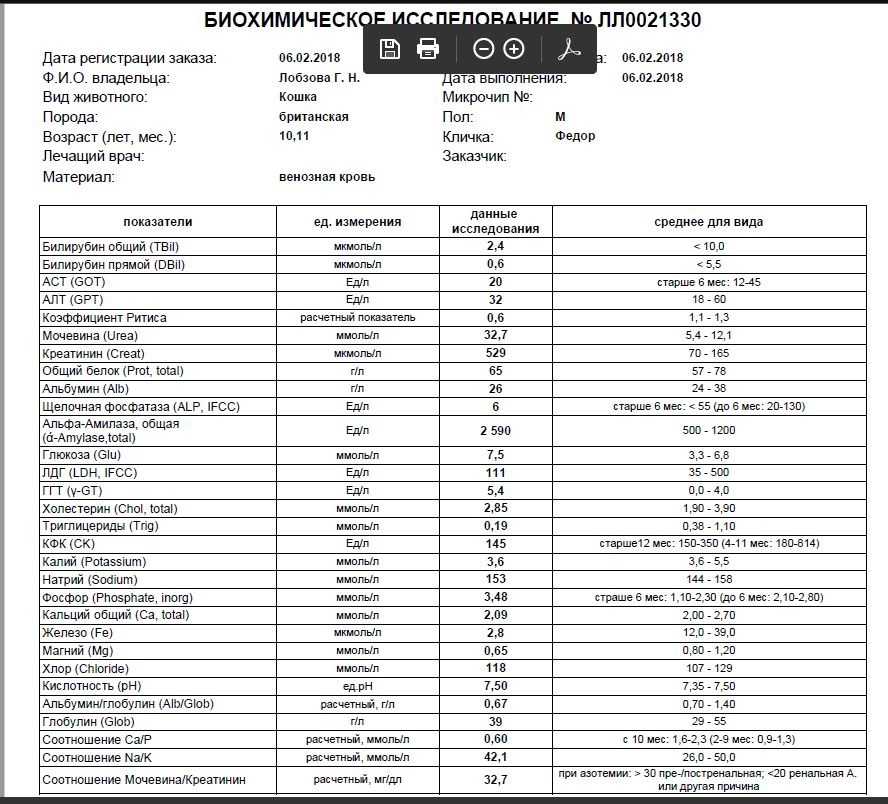 Столь заметные различия между юношами и девушками объясняются более выраженным процессом роста костной и мышечной ткани у парней.
Столь заметные различия между юношами и девушками объясняются более выраженным процессом роста костной и мышечной ткани у парней.
С 15 до 19 лет норма для юношей от 80 до 300 Ед/л, для девушек – от 51 до 114 Ед/л. В дальнейшем показатели идентичны для всех возрастов, и составляют 35 – 111 и 39 — 134 Ед/л для женщин и мужчин соответственно.
Если щелочная фосфатаза повышена у ребенка – что это значит?
2 основные причины повышенной щелочной фосфатазы у ребёнка: патологии печени или костей. Для более точного понимания необходимо провести дополнительное обследование с изучением биохимических лабораторных показателей.
Если отмечается сочетанное отклонение от нормы ЩФ и билирубина, аланинаминотрансферазы и аспартатаминотрансферазы, то возможная причина – заболевания печени. О патологиях костной ткани свидетельствуют изменения уровня кальция и фосфора в крови, а также повышение щелочной фосфатазы у детей. Рассмотрим подробнее каждую из патологий.
Реклама
Рахит
Одна из наиболее часто встречающихся причин – это рахит. Болезнь поражает новорождённых и малышей раннего детского возраста. Характеризуется неправильным процессом образования костей и неполноценной их минерализацией. Рахит развивается из-за нехватки витамина D и его метаболитов в результате недостаточного получения ребёнком солнечных лучей. Заболевание также поражает недоношенных детей, не исключена наследственная предрасположенность. Важно правильно составить рацион питания ребёнка, поскольку молочные смеси без добавок витамина D способствуют манифестации заболевания.
В осенне-зимний период болезнь возникает чаще и протекает тяжелее, чем в летний. Поскольку дети даже если гуляют на улице, то всё тело спрятано от прямого попадания солнечных лучей. Отмечено, что дети, которые получают грудное молоко матери, болеют рахитом реже.
Методы лечения определяются с учётом стадии заболевания. Дозировку и длительность приёма витамина D подбирает лечащий врач ребёнка.
Реклама
Важно наладить режим дня для маленького пациента. Организовать достаточное количество времени для прогулок, массажа и лечебной гимнастики. Необходимо пересмотреть рацион ребёнка, включив в него продукты богатые кальцием, фосфором и витамином D.
Прогнозируемый исход благоприятный. Необратимые изменения костной ткани и деформации возникают при несоблюдении рекомендаций врача и отсутствии грамотной тактики лечения.
Лимфобластоз
Заболевание, которое вызывает вирус Эпштейна-Барра. Проявляется сочетанными поражениями печени, селезёнки, лимфоузлов и нарушениями состава крови. У 95% пациентов вирусная инфекция сопровождается нарушением нормальной работы печени. Наблюдается повышенная щелочная фосфата в крови у ребёнка наряду с увеличением концентрации ферментов печени (АЛАТ и АСАТ).
В настоящее время не разработана единая тактика лечения инфекции. Поэтому детям проводят симптоматическую терапию.
Следует подчеркнуть, что кишечные инфекции также могут приводить к схожим проявлениям и отклонению ЩФ от нормы. Важно идентифицировать возбудителя инфекции и подобрать соответствующее лечение.
Важно идентифицировать возбудителя инфекции и подобрать соответствующее лечение.
Реклама
Другие причины
При отклонении показателя от нормы следует проводить комплексную диагностику для установления точной причины. К повышению уровня ЩФ также приводят:
- желтуха, возникающая из-за закупорки желчевыводящих протоков;
- остеомаляция – патологическое размягчение костей;
- заболевания эндокринной системы, например, гиперпаратиреоз. В организме секретируется избыточное количество гормонов околощитовидных желёз. В результате усиливаются процессы вымывания ионов кальция из костной ткани;
- гепатит различной этиологии. В этом случае рассматриваемый показатель повышается в 3 раза;
- онкологические заболевания печени или костной ткани, а также метастазы в другие органы.
Выводы
Подводя итог, случает подчеркнуть:
- максимальная активность щелочной фосфатазы наблюдается в первые годы жизни малышей и в период полового созревания.
 В этих периодах отмечается усиленный рост костей;
В этих периодах отмечается усиленный рост костей; - при интерпретации результатов необходимо учитывать данные комплексного обследования. Подбор референсных показателей осуществляется с учётом возраста и пола пациентов;
- сочетанное отклонение от нормы ЩФ и ферментов печени указывают на патологию данного органа;
- о нарушении нормального развития костной ткани свидетельствуют нехватка кальция и фосфора, наряду с повышенной ЩФ;
- неправильное хранение биоматериала может привести к ложноположительным результатам исследования. Недопустимо охлаждение при хранении и транспортировке взятой крови.
Материал предоставлен medseen.ru
Повышена щелочная фосфатаза у собаки: причины, что означает
Содержание статьи
- Причины
- Основные симптомы
- Диагностика в ветклинике
- Методика лечения и прогноз
- Что делать в домашних условиях
- Меры профилактики
Щелочной фосфатазой называется фермент, участвующий в обмене фосфорно-кальциевого обмена и обеспечивающий гидролиз сложных эфиров. Концентрация щелочной фосфатазы наблюдается в слизистой кишечника, почечных и желчных каналах, клетках костной ткани и печени. Нормальные показатели фермента у взрослых собак — до 100 ед./л.
Концентрация щелочной фосфатазы наблюдается в слизистой кишечника, почечных и желчных каналах, клетках костной ткани и печени. Нормальные показатели фермента у взрослых собак — до 100 ед./л.
Причины
При патологическом процессе в организме увеличивается проницаемость клеточных мембран, в результате чего клетки разрушаются. Так щелочная фосфатаза, точнее, ее избыток, проникает в кровь. Подтвердить это может результат биохимического анализа крови.
Это не всегда означает развитие серьезных патологий в организме. Например, у щенков и молодых особей увеличение уровня ферментов может повышаться за счет интенсивного развития скелета и костной ткани.
Не является отклонением от нормы повышение фосфатазы у животных после переломов, а также у сук во время беременности.
Еще одной распространенной причиной повышения ферментов является прием определенных медикаментозных препаратов, таких, как стероидные гормоны, противосудорожные средства, нестероидные противовоспалительные лекарства.
Увеличение фосфатазы может возникнуть при дефиците кальция и употреблении жирной пищи, а также при развитии в организме собаки серьезных патологий: цирроза печени, синдром Кушинга у собаки, онкологии молочных желез, костной ткани, желчевыводящих путей, панкреатите.
И это далеко не полный список опасных для жизни заболеваний. Вот почему при обнаружении подозрительных признаков так важно своевременно обратиться к ветеринару.
Основные симптомы
Процесс повышения показателей щелочной фосфатазы не имеет определенных клинических признаков. Владельца собаки должны насторожить следующие признаки:
- темный цвет урины;
- светлый оттенок каловых масс;
- отсутствие аппетита;
- тошнота, рвота;
- вялость, малая подвижность, усталость домашнего питомца.
Подтвердить или опровергнуть увеличение ферментов могут только диагностические исследования.
Диагностика в ветклинике
Чтобы поставить точный диагноз, ветеринару необходимо собрать анамнез и провести ряд манипуляций (визуальный осмотр, в том числе и состояние шерстяного покрова, пальпация живота). К необходимым диагностическим исследованиям относятся УЗИ почек и печени, рентген (при наличии определенных показателей).
К необходимым диагностическим исследованиям относятся УЗИ почек и печени, рентген (при наличии определенных показателей).
Биохимический анализ сдается после необходимой подготовки. Перед его проведением собаку нельзя кормить, последний прием пищи должен быть не позднее, чем за 8 часов до сдачи анализа.
Владелец пса должен рассказать ветеринару, сколько раз в день питается домашний питомец, какой пище отдается предпочтение — натуральной или промышленным кормам. Если в данный момент животное принимает какие-либо медикаменты, об этом ветеринара также нужно поставить в известность.
За несколько дней до процедуры животное не следует подвергать сильным физическим нагрузкам и стрессам. Целесообразно пригласить специалиста домой, чтобы он взял кровь в привычных и комфортных для собаки условиях, а хозяин находился рядом.
Результат готов на следующий день, однако если возникает сомнение в его точности и информативности, назначается повторное исследование крови.
Методика лечения и прогноз
Как правило, собаке назначается курсовой прием препаратов, направленных на устранение основного заболевания, вызвавшего увеличение ферментов. Так, если процесс развился на фоне печеночной патологии, назначается препарат Эссенциале, стабилизирующий работу печени. Дозировка устанавливается ветеринаром.
По окончанию лечения биохимический анализ крови делается повторно. Показатели ферментов на прежнем уровне или их увеличение говорит о том, что лечение оказалось неэффективным. В таком случае возникает необходимость в проведении операции по удалению пораженного органа.
В послеоперационной период уровень фосфатазы также повышен, но это не считается патологией. Со временем он нормализуется.
В процессе лечения и послеоперационного периода хозяин должен неукоснительно выполнять рекомендации специалиста. Ни в коем случае нельзя заниматься самолечением и назначать препараты без консультации с ветеринаром.
Что касается прогноза, то все зависит от того, насколько своевременно и грамотно было проведено лечение (операция). Развитие патологии приводит к хроническим заболеваниям органов.
Развитие патологии приводит к хроническим заболеваниям органов.
Что делать в домашних условиях
В послеоперационный период огромное значение придается кормлению. Не стоит резко менять рацион и переводить домашнего питомца с привычной натуральной пищи на готовые корма от известных производителей. Еда должна быть диетической, предпочтение нужно отдавать отварным блюдам, например, курице.
Допускается использование небольшого количества риса. Порции употребляемой пищи, независимо от того, «натуралка» это или готовый корм, следует уменьшить.
В период реабилитации не рекомендуется перевозить собаку на новое место жительство, посещать шумные места, допускать контакт с бродячими животными. Любой стресс может негативно отразиться на состоянии питомца и провоцировать рецидив.
Меры профилактики
К профилактическим мероприятиям в данном случае можно отнести, прежде всего, кормление собаки сбалансированными нежирными кормами. Давать ежу следует небольшими порциями, чтобы пес не переедал.
Своевременные осмотры в ветеринарной клинике помогут избежать многих проблем, в том числе и повышения щелочной фосфатазы у собаки.
Авторы статей: коллектив клиники Беланта
Феномен обострения щелочной фосфатазы: транзиторное значительное повышение концентрации щелочной фосфатазы у пациента с раком простаты после начала лечения агонистом ГнРГ — Полный текст — Отчеты о клинических случаях в онкологии 2021, Vol. 14, № 1
Мужчина 78 лет с метастатическим раком предстательной железы поступил в стационар через 5 недель после начала системной терапии гозерелином (агонистом ГнРГ) в связи со значительным повышением концентрации щелочной фосфатазы (ЩФ), несмотря на клиническое улучшение. Дальнейшее обследование выявило снижение уровня простатспецифического антигена и отсутствие рентгенологических признаков прогрессирования заболевания. Впоследствии ЩФ самопроизвольно снизилась. Этот клинический случай является примером раннего обострения ЩФ после начала эндокринной терапии у пациентов с метастазами в кости, что согласуется с ответом на лечение. Клиницисты должны быть знакомы с феноменом обострения ЩФ в этих условиях, который не отражает прогрессирования заболевания или неэффективности лечения, чтобы предотвратить ненужные обследования, госпитализации или даже ошибочное прекращение успешной терапии.
Клиницисты должны быть знакомы с феноменом обострения ЩФ в этих условиях, который не отражает прогрессирования заболевания или неэффективности лечения, чтобы предотвратить ненужные обследования, госпитализации или даже ошибочное прекращение успешной терапии.
Введение
Щелочная фосфатаза (ЩФ) представляет собой фермент, экспрессируемый на поверхности остеобластов [1] и способствующий минерализации костей. Следовательно, он используется в качестве маркера активности остеобластов. Однако поверхностная экспрессия также была продемонстрирована в клетках метастатического рака предстательной железы (РПЖ) [2, 3]. У мужчин с распространенным РПЖ скелет является наиболее частым местом метастазирования [4]. В кости клетки РПЖ могут способствовать повышению уровня ЩФ двумя путями: активируя остеобласты и экспрессируя ЩФ опухолевого происхождения. Следовательно, измерение ЩФ может быть использовано для диагностики метастазов в кости и мониторинга ответа на лечение. Более высокие уровни ЩФ связаны с прогрессированием заболевания и ранней смертью [5]. Однако повышение метаболизма и восстановления костной ткани может также отражаться повышением концентрации ЩФ. Есть несколько других заболеваний и состояний, связанных с повышением уровня ЩФ, таких как холестатические заболевания печени, заболевания костей и токсичность лекарств. В связи с этим костно-специфическая ЩФ может быть использована для дифференциации повышения ЩФ, вторичного по отношению к костным заболеваниям, от повышения, вызванного заболеваниями печени [6]. Мониторинг концентрации ЩФ может быть выгодным, поскольку это широко доступный и недорогой, чувствительный и неинвазивный метод обнаружения метастатического рака в костях по сравнению с компьютерной томографией (КТ) или сканированием костей. В процессе лечения динамические изменения ЩФ проявляются даже раньше, чем изменения простатспецифического антигена (ПСА) [7].
Однако повышение метаболизма и восстановления костной ткани может также отражаться повышением концентрации ЩФ. Есть несколько других заболеваний и состояний, связанных с повышением уровня ЩФ, таких как холестатические заболевания печени, заболевания костей и токсичность лекарств. В связи с этим костно-специфическая ЩФ может быть использована для дифференциации повышения ЩФ, вторичного по отношению к костным заболеваниям, от повышения, вызванного заболеваниями печени [6]. Мониторинг концентрации ЩФ может быть выгодным, поскольку это широко доступный и недорогой, чувствительный и неинвазивный метод обнаружения метастатического рака в костях по сравнению с компьютерной томографией (КТ) или сканированием костей. В процессе лечения динамические изменения ЩФ проявляются даже раньше, чем изменения простатспецифического антигена (ПСА) [7].
Преходящее повышение концентрации ЩФ через 4–6 недель после начала системного лечения может наблюдаться у пациентов с метастазами в кости различных злокачественных новообразований. Это явление называется вспышкой ЩФ, которое может быть определено как временное повышение уровня ЩФ в сыворотке до 120% и более от значения до лечения с последующим снижением [8]. В предыдущих исследованиях сообщалось о замечательном разнообразии длительности и интенсивности вспышек ALP, что, возможно, связано с отсутствием общепринятого определения этого явления [5, 8-10]. Преходящее повышение ЩФ наблюдалось у пациентов после начала лечения ингибитором рецептора эпидермального фактора роста-тирозинкиназы при немелкоклеточном раке легкого, а также после начала системной терапии у пациентов с распространенным раком молочной железы и РПЖ с метастазами в кости. [9, 11]. Эти явления следует интерпретировать не как признак неэффективности лечения, а скорее как ответ на лечение, и следует продолжать противораковую терапию [8, 11, 12].
Это явление называется вспышкой ЩФ, которое может быть определено как временное повышение уровня ЩФ в сыворотке до 120% и более от значения до лечения с последующим снижением [8]. В предыдущих исследованиях сообщалось о замечательном разнообразии длительности и интенсивности вспышек ALP, что, возможно, связано с отсутствием общепринятого определения этого явления [5, 8-10]. Преходящее повышение ЩФ наблюдалось у пациентов после начала лечения ингибитором рецептора эпидермального фактора роста-тирозинкиназы при немелкоклеточном раке легкого, а также после начала системной терапии у пациентов с распространенным раком молочной железы и РПЖ с метастазами в кости. [9, 11]. Эти явления следует интерпретировать не как признак неэффективности лечения, а скорее как ответ на лечение, и следует продолжать противораковую терапию [8, 11, 12].
Отчет о болезни
78-летний мужчина был направлен в нашу больницу лечащим врачом из-за заметного повышения ЩФ. У пациента был диагностирован метастатический РПЖ (7 баллов по шкале Глисона, лимфатические узлы и кости) во время предыдущей госпитализации 5 недель назад. Было начато лечение агонистом рецептора ГнРГ гозерелином и антиандрогенным бикалутамидом (кратковременное лечение в течение 2 недель для предотвращения всплеска тестостерона).
Было начато лечение агонистом рецептора ГнРГ гозерелином и антиандрогенным бикалутамидом (кратковременное лечение в течение 2 недель для предотвращения всплеска тестостерона).
При поступлении пациент сообщил, что чувствует себя намного лучше, чем до начала терапии, и его пройденное расстояние заметно улучшилось. Физический осмотр не изменился по сравнению с предыдущей госпитализацией, как и его список лекарств. Лабораторные результаты были значимыми для 8,4-кратного увеличения концентрации ЩФ с 437 до 3688 ЕД/л (нормальный диапазон 40–130 ЕД/л) (рис. 1) при отсутствии изменений в других функциональных пробах печени. Напротив, его уровень ПСА значительно снизился с 17,4 до 0,17 мкг/л (нормальный диапазон <4,1 мкг/л). При компьютерной томографии брюшной полости выявлено стабильное метастатическое заболевание без признаков прогрессирования. Уровни костно-специфической ЩФ были заметно повышены (1060 мкг/л, нормальный диапазон 5,5–24,6 мкг/л), а показатель С-концевого телопептида (бета-CrossLaps), маркер ремоделирования кости, значительно увеличился с 0,7 при первом поступлении до 3,1 нг/л. мл (нормальный диапазон 0,13–0,46 нг/мл). Эти результаты исключали холестатическую болезнь печени или гепатит, связанный с лекарственными препаратами, как причину повышения ЩФ. С учетом клинического улучшения и снижения уровня ПСА был диагностирован обострение ЩФ как следствие эндокринной терапии, продолжено лечение гозерелином, и больной был немедленно выписан. В дальнейшем концентрации ЩФ и ПСА спонтанно снижались (минимальные концентрации ЩФ и ПСА 206 ЕД/л и 0,14 мкг/л соответственно).
мл (нормальный диапазон 0,13–0,46 нг/мл). Эти результаты исключали холестатическую болезнь печени или гепатит, связанный с лекарственными препаратами, как причину повышения ЩФ. С учетом клинического улучшения и снижения уровня ПСА был диагностирован обострение ЩФ как следствие эндокринной терапии, продолжено лечение гозерелином, и больной был немедленно выписан. В дальнейшем концентрации ЩФ и ПСА спонтанно снижались (минимальные концентрации ЩФ и ПСА 206 ЕД/л и 0,14 мкг/л соответственно).
Рис. 1.
Течение ЩФ и ПСА с момента начала андрогендепривационной терапии гозерелином (агонистом ГнРГ). ALP, щелочная фосфатаза; ПСА, простатоспецифический антиген.
Через восемь месяцев пациент снова госпитализирован из-за головокружения и слабости с последующим падением дома во время продолжения терапии гозерелином. Он не сообщал о какой-либо боли, и физикальное обследование было без изменений. Лабораторные результаты свидетельствовали о повышении концентрации ЩФ (980 ЕД/л) с умеренным, но значительным повышением концентрации ПСА (1,32 мкг/л). Прогрессирование метастазов в кости и лимфатические узлы было очевидно при КТ брюшной полости и сканировании костей. После обсуждения терапевтических возможностей с пациенткой была начата паллиативная химиотерапия доцетакселом и низкими дозами дексаметазона. Он сообщил о значительном уменьшении головокружения и усталости после начала химиотерапии. Через 2 месяца химиотерапии (примерно через 1 год после начала андрогенной депривации) ответ на терапию был подтвержден данными КТ и сканирования костей с сопутствующим снижением уровня ПСА и ЩФ (ЩФ 176 ЕД/л, ПСА 0,06 мкг/л). л).
Прогрессирование метастазов в кости и лимфатические узлы было очевидно при КТ брюшной полости и сканировании костей. После обсуждения терапевтических возможностей с пациенткой была начата паллиативная химиотерапия доцетакселом и низкими дозами дексаметазона. Он сообщил о значительном уменьшении головокружения и усталости после начала химиотерапии. Через 2 месяца химиотерапии (примерно через 1 год после начала андрогенной депривации) ответ на терапию был подтвержден данными КТ и сканирования костей с сопутствующим снижением уровня ПСА и ЩФ (ЩФ 176 ЕД/л, ПСА 0,06 мкг/л). л).
Обсуждение
У пациентов с РПЖ через 4–6 недель после начала эндокринной терапии иногда наблюдается транзиторное повышение концентрации ЩФ («вспышка»), особенно при наличии метастатического заболевания и более высоких уровнях ПСА [8]. Хотя точный механизм еще предстоит выяснить, наблюдаемое повышение ЩФ, вероятно, отражает повышенную активность остеобластов («восстановление кости») в ответ на эффективное лечение./6.jpg) Тем не менее, распознавание этого явления важно, чтобы избежать прекращения полезного лечения из-за неправильной интерпретации обострения как признака прогрессирования заболевания или побочных эффектов лекарств. Верно, скорее, обратное, поскольку обострение ЩФ является признаком ответа на лечение [13]. Поскольку заболевание печени или лекарственная токсичность могут способствовать повышению уровня ЩФ, измерение костно-специфического ЩФ может помочь отличить обострение ЩФ от других заболеваний [3, 6]. Это имеет особое значение при наличии противоречивых клинических и лабораторных данных, как показано в данном случае. Несмотря на улучшение общего состояния здоровья и самочувствия, пациент был госпитализирован из-за беспокойства о прогрессировании заболевания и отсутствия знаний об этом явлении.
Тем не менее, распознавание этого явления важно, чтобы избежать прекращения полезного лечения из-за неправильной интерпретации обострения как признака прогрессирования заболевания или побочных эффектов лекарств. Верно, скорее, обратное, поскольку обострение ЩФ является признаком ответа на лечение [13]. Поскольку заболевание печени или лекарственная токсичность могут способствовать повышению уровня ЩФ, измерение костно-специфического ЩФ может помочь отличить обострение ЩФ от других заболеваний [3, 6]. Это имеет особое значение при наличии противоречивых клинических и лабораторных данных, как показано в данном случае. Несмотря на улучшение общего состояния здоровья и самочувствия, пациент был госпитализирован из-за беспокойства о прогрессировании заболевания и отсутствия знаний об этом явлении.
Феномен вспышки ALP хорошо описан в литературе, в частности, при распространенном РПЖ [5, 8, 13]. По сравнению с исследованием III фазы агониста рецепторов ГнРГ леупролидом в сравнении с блокатором рецепторов ГнРГ дегареликсом, проведенным Schröder et al. [14], повышение ЩФ в нашем случае было более выраженным (3600 ЕД/л против в среднем около 350 МЕ/л в группе пациентов с метастазами и уровнем гемоглобина <13 г/дл) через 6–8 недели. Вероятно, это объясняется высокой опухолевой массой в начале эндокринной терапии в данном случае.
[14], повышение ЩФ в нашем случае было более выраженным (3600 ЕД/л против в среднем около 350 МЕ/л в группе пациентов с метастазами и уровнем гемоглобина <13 г/дл) через 6–8 недели. Вероятно, это объясняется высокой опухолевой массой в начале эндокринной терапии в данном случае.
Суммарный балл по шкале Глисона ранее считался прогностическим фактором прогрессирования андрогеннезависимого РПЖ [15]. В свою очередь, необычайное повышение ЩФ у нашего пациента с умеренным баллом по шкале Глисона 7 было связано с ранним прогрессированием заболевания, что согласуется с предыдущими исследованиями, в которых раннее обострение ЩФ было определено как отрицательный прогностический маркер как после орхиэктомии, так и после лечения агонистами рецепторов ГнРГ [5]. , 8]. Интересно, что в недавнем ретроспективном исследовании пациентов с РПЖ со скелетными метастазами, получавших лечение абиратероном, начальное повышение ЩФ в течение 4 недель с последующим быстрым снижением до исходного уровня в течение 8 недель было связано со сниженным риском прогрессирования заболевания через 12 недель после начала лечения. лечение абиратероном [7]. Однако при многофакторном анализе только отсутствие >50% снижения уровня ПСА через 12 недель ассоциировалось с прогрессированием заболевания и общей выживаемостью. Возможно, это объясняется небольшим числом пациентов, что ограничивает возможность показать разницу в многомерном анализе для обеих переменных. Кроме того, исследование показало, что повышение ЩФ появляется раньше, чем снижение ПСА, и должно привести к продолжению приема абиратерона.
лечение абиратероном [7]. Однако при многофакторном анализе только отсутствие >50% снижения уровня ПСА через 12 недель ассоциировалось с прогрессированием заболевания и общей выживаемостью. Возможно, это объясняется небольшим числом пациентов, что ограничивает возможность показать разницу в многомерном анализе для обеих переменных. Кроме того, исследование показало, что повышение ЩФ появляется раньше, чем снижение ПСА, и должно привести к продолжению приема абиратерона.
Учитывая связь обострения ЩФ в ранние сроки после начала андрогенной депривационной терапии с более короткой выживаемостью без прогрессирования при РПЖ [8], у этих пациентов можно рассмотреть вопрос о тщательном наблюдении или интенсификации лечения. Интересно, что в ретроспективном анализе значительное увеличение выживаемости без прогрессирования было продемонстрировано только у пациентов с обострением ЩФ в течение 4 недель после орхиэктомии, получавших дополнительную химиотерапию, по сравнению с пациентами с орхиэктомией, но без химиотерапии [10]. При условии, что механизм обострения ЩФ после орхиэктомии подобен механизму обострения ЩФ после начала эндокринной терапии, будущие исследования должны оценить, можно ли его появление использовать в качестве маркера для ранней дополнительной химиотерапии у пациентов с РПЖ.
При условии, что механизм обострения ЩФ после орхиэктомии подобен механизму обострения ЩФ после начала эндокринной терапии, будущие исследования должны оценить, можно ли его появление использовать в качестве маркера для ранней дополнительной химиотерапии у пациентов с РПЖ.
Заключение
Как показано в этом клиническом случае, мониторинг концентрации ЩФ после начала эндокринной терапии может помочь в выявлении пациентов с высоким риском раннего прогрессирования заболевания и может использоваться для индивидуализации последующего наблюдения и подбора лечения в будущем. . Тем не менее, пороговое значение для значительного обострения ЩФ, связанного с ранним прогрессированием заболевания, еще предстоит определить, и необходимы клинические испытания, в которых оцениваются решения о лечении на основе наличия или отсутствия значительного обострения ЩФ. Клиницисты должны быть знакомы с феноменом обострения ЩФ, который может возникать у пациентов с метастазами в костях после начала лечения и не отражает прогрессирования заболевания или неэффективности лечения, чтобы предотвратить ненужные обследования или даже госпитализацию.
Заявление об этике
Пациент дал письменное информированное согласие на публикацию своего случая.
Заявление о конфликте интересов
У авторов нет конфликта интересов, о котором следует заявить.
Источники финансирования
У авторов нет источников финансирования для объявления.
Вклад авторов
П. Мерло и М. Остхофф собрали данные, провели исследование литературы и написали первый черновик рукописи. К. Рохлиц помогал в написании и редактировании рукописи. Все авторы принимали участие в уходе за пациентом и одобрили окончательный вариант рукописи.
Эта статья находится под лицензией Creative Commons Attribution-NonCommercial 4.0 International License (CC BY-NC). Использование и распространение в коммерческих целях требует письменного разрешения. Дозировка препарата: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор препарата и дозировка, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации. Тем не менее, в связи с продолжающимися исследованиями, изменениями в правительственных постановлениях и постоянным потоком информации, касающейся лекарственной терапии и реакций на лекарства, читателю настоятельно рекомендуется проверять вкладыш в упаковке для каждого лекарства на предмет любых изменений в показаниях и дозировке, а также для дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендуемый агент является новым и/или редко используемым лекарственным средством. Отказ от ответственности: заявления, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и участникам, а не издателям и редакторам. Появление рекламы и/или ссылок на продукты в публикации не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор(ы) отказываются от ответственности за любой ущерб, нанесенный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в содержании или рекламе.
Тем не менее, в связи с продолжающимися исследованиями, изменениями в правительственных постановлениях и постоянным потоком информации, касающейся лекарственной терапии и реакций на лекарства, читателю настоятельно рекомендуется проверять вкладыш в упаковке для каждого лекарства на предмет любых изменений в показаниях и дозировке, а также для дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендуемый агент является новым и/или редко используемым лекарственным средством. Отказ от ответственности: заявления, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и участникам, а не издателям и редакторам. Появление рекламы и/или ссылок на продукты в публикации не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор(ы) отказываются от ответственности за любой ущерб, нанесенный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в содержании или рекламе.
Высокая сывороточная щелочная фосфатаза вспышка после первой линии андрогенной депривационной терапии предсказывает плохой прогноз у пациентов с метастатическим раком предстательной железы, получавших терапию андрогенов второго поколения
. . Определить, связано ли повышение уровня щелочной фосфатазы (ЩФ) после андрогенной депривационной терапии (АДТ) с реакцией на лечение при кастрационно-резистентном раке предстательной железы (КРРПЖ) и предсказать прогноз пациентов с метастатическим раком предстательной железы (РПЖ). Методы . Ретроспективно обследовано 119 пациентов с диагнозом метастатический РПЖ в период с 2008 по 2017 год. Коэффициент усиления ЩФ рассчитывали как отношение уровней ЩФ через 1 месяц после начала ГТ к уровням ЩФ при постановке диагноза. Была исследована связь коэффициента вспышки ЩФ с реакцией простатспецифического антигена (ПСА) на лечение КРРПЖ (таргетная терапия андрогенных рецепторов (АРТ) второго поколения или доцетаксел), временем до КРРПЖ и общей выживаемостью (ОВ). Результаты . Время до КРРПЖ и ОВ было значительно больше у пациентов с коэффициентом вспышки ЩФ менее 1,33 по сравнению с коэффициентом более 1,33. Никакой разницы в ответе ПСА не наблюдалось в отношении коэффициента резкого обострения ЩФ как при АРТ, так и при лечении доцетакселом. У пациентов, получавших АРТ второго поколения, с низким коэффициентом обострения ЩФ наблюдалась более длительная ОВ, чем у пациентов с более высоким коэффициентом обострения ЩФ (12). Тем не менее, не было замечено никакой разницы между высоким и низким коэффициентом обострения ALP () у пациентов, получавших доцетаксел. Коэффициент вспышки ALP был наиболее значимым прогностическим фактором для ОС (). Выводы . Более высокий коэффициент обострения ЩФ после ГТ первой линии был значимым прогностическим фактором при метастатическом РПЖ, особенно у пациентов, получавших АРТ второго поколения по поводу КРРПЖ. Химиотерапия для пациентов с более высоким коэффициентом обострения ALP через 1 месяц после индукции ADT может быть клинически значимым решением.
Результаты . Время до КРРПЖ и ОВ было значительно больше у пациентов с коэффициентом вспышки ЩФ менее 1,33 по сравнению с коэффициентом более 1,33. Никакой разницы в ответе ПСА не наблюдалось в отношении коэффициента резкого обострения ЩФ как при АРТ, так и при лечении доцетакселом. У пациентов, получавших АРТ второго поколения, с низким коэффициентом обострения ЩФ наблюдалась более длительная ОВ, чем у пациентов с более высоким коэффициентом обострения ЩФ (12). Тем не менее, не было замечено никакой разницы между высоким и низким коэффициентом обострения ALP () у пациентов, получавших доцетаксел. Коэффициент вспышки ALP был наиболее значимым прогностическим фактором для ОС (). Выводы . Более высокий коэффициент обострения ЩФ после ГТ первой линии был значимым прогностическим фактором при метастатическом РПЖ, особенно у пациентов, получавших АРТ второго поколения по поводу КРРПЖ. Химиотерапия для пациентов с более высоким коэффициентом обострения ALP через 1 месяц после индукции ADT может быть клинически значимым решением.
1. Введение
Рак предстательной железы (РПЖ) является второй ведущей причиной смерти от рака у мужчин в западных странах [1]. Широко используемый скрининг на простат-специфический антиген (ПСА) уменьшил число de novo случая метастатического РПЖ при постановке диагноза, но некоторые пациенты с метастатическим РПЖ все еще выявляются [2]. Андрогенная депривационная терапия (АДТ) является эффективным методом лечения большинства пациентов с РПЖ; однако у этих пациентов в конечном итоге развивается кастрационно-резистентный рак предстательной железы (КРРПЖ). Медиана общей выживаемости (ОВ) больных метастатическим РПЖ составляет примерно 3–6 лет в зависимости от объема опухоли, висцерального метастазирования и других прогностических факторов [2, 3]. Доцетаксел и таргетная терапия андрогенных рецепторов (АРТ) второго поколения являются эффективными методами лечения не только КРРПЖ, но и метастатического гормоночувствительного РПЖ (ГСРП) [4–7]. Какие пациенты выиграют от химиотерапии, поскольку начальное лечение не ясно.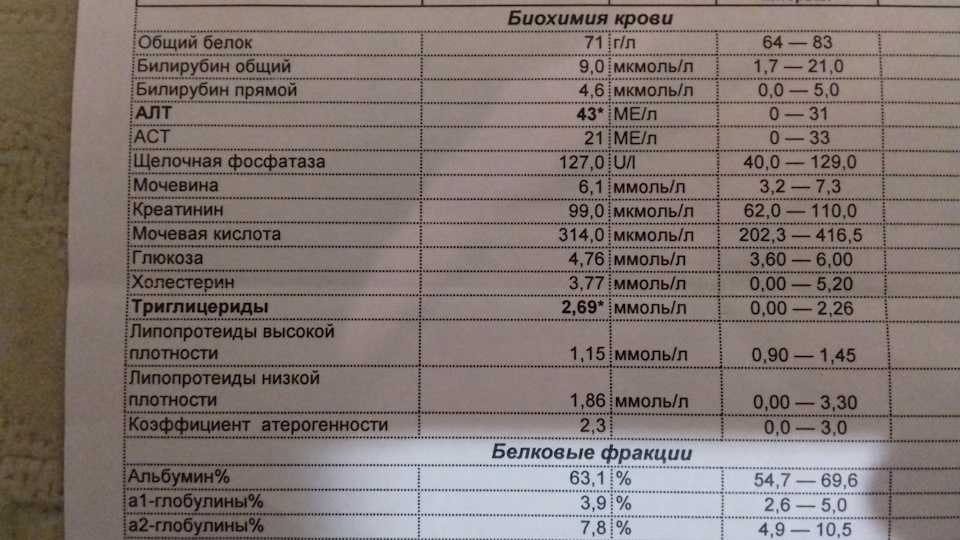 Чтобы предсказать ответ или прогноз HSPC, необходим надежный прогностический маркер. Время до КРРПЖ менее 12 мес и надир уровня ПСА (<0,2 нг/мл) через 6 мес после индукции ГТ являются хорошо известными прогностическими предикторами [3, 8]. Пациенты с метастатическим РПЖ с большим объемом заболевания имеют плохой прогноз, но мы часто видим пациентов, которые живут дольше, чем сообщается в литературе. Необходима стратификация пациентов с метастатическим РПЖ для выявления пациентов с РПЖ высокого риска, которым следует проводить агрессивное лечение.
Чтобы предсказать ответ или прогноз HSPC, необходим надежный прогностический маркер. Время до КРРПЖ менее 12 мес и надир уровня ПСА (<0,2 нг/мл) через 6 мес после индукции ГТ являются хорошо известными прогностическими предикторами [3, 8]. Пациенты с метастатическим РПЖ с большим объемом заболевания имеют плохой прогноз, но мы часто видим пациентов, которые живут дольше, чем сообщается в литературе. Необходима стратификация пациентов с метастатическим РПЖ для выявления пациентов с РПЖ высокого риска, которым следует проводить агрессивное лечение.
Уровень щелочного фосфата в сыворотке (ЩФ) является важным прогностическим фактором при метастатическом РПЖ. Вспышка ALP впервые была зарегистрирована в 1996 г. [9] и может быть полезна для ранней диагностики пациентов, у которых заболевание может быстро прогрессировать и которым потенциально может помочь агрессивное лечение. Это исследование было сосредоточено на пациентах с de novo метастатическим РПЖ в костях, которые прогрессировали до КРРПЖ, и определялось, является ли соотношение обострений ЩФ (ЩФ через 1 месяц после ГТ/начальное значение ЩФ) прогнозирующим их ОВ. Если бы можно было идентифицировать пациентов с метастатическим заболеванием с высокой степенью злокачественности, более агрессивное лечение могло бы быть предоставлено пациентам, которые, скорее всего, получат пользу.
Если бы можно было идентифицировать пациентов с метастатическим заболеванием с высокой степенью злокачественности, более агрессивное лечение могло бы быть предоставлено пациентам, которые, скорее всего, получат пользу.
2. Материалы и методы
Сто семьдесят два пациента с метастатическим РПЖ поступили в Медицинский центр Тиба Университета Тейкё в период с 2008 по 2017 год, и у 162 пациентов были диагностированы метастазы в кости. Мы могли бы ретроспективно оценить уровни ЩФ у 119 пациентов до и через 1 и 3 месяца от начала ГТ. Клиническую стадию оценивали в соответствии с классификацией TNM 2017 года. Мы использовали критерии PCWG2/3 для определения CRPC. Всем пациентам была проведена трансректальная пункционная биопсия для патологической диагностики РПЖ и была определена оценка по шкале Глисона. Все пациенты получали ГТ, включая хирургическую кастрацию и агонисты или антагонисты рилизинг-гормона лютеинизирующего гормона с антиандрогенным бикалутамидом или без него (80 мг в день). Пятьдесят два пациента с прогрессированием КРРПЖ получали АРТ нового поколения (абиратерона ацетат или энзалутамид) или доцетаксел (таблица 1). Письменное согласие на определение биомаркера РПЖ было получено от каждого пациента (наблюдательный совет Университета Тейкё № 14-016).
Пятьдесят два пациента с прогрессированием КРРПЖ получали АРТ нового поколения (абиратерона ацетат или энзалутамид) или доцетаксел (таблица 1). Письменное согласие на определение биомаркера РПЖ было получено от каждого пациента (наблюдательный совет Университета Тейкё № 14-016).
Сывороточные уровни ПСА, ЩФ (нормальный диапазон 87-304 ЕД/л), гемоглобина и лактатдегидрогеназы (ЛДГ) при постановке диагноза; ЩФ через 1 и 3 мес после начала ГТ; и был измерен надир ПСА. Обострение ЩФ определяли как любое повышение ЩФ в сыворотке выше исходного уровня через 1 месяц после ГТ. Время до КРРПЖ определяли как время от начала ГТ до клинического прогрессирования или прогрессирования ПСА (≥2,0 нг/мл). ОВ определяли как время от начала ГТ до смерти от РПЖ или любой другой причины.
Одномерные сравнения между пациентами, получавшими АРТ и получавшими доцетаксел, оценивались с использованием критерия хи-квадрат или критерия Вилкоксона. Время до КРРПЖ и ОС анализировали с использованием метода Каплана-Мейера и критерия логарифмического ранга. Одномерный и многомерный регрессионный анализ Кокса доступных прогностических переменных (возраст, оценка по шкале Глисона, ПСА, надир ПСА, исходный уровень ЩФ, значение повышения ЩФ через 1 месяц после ГТ, уровни ЛДГ, гемоглобина и тестостерона) были проведены для выявления значимых прогностических факторов. факторы. Статистический анализ проводили с использованием программного обеспечения JMP версии 11 для Windows (SAS Institute, Inc., Кэри, Северная Каролина). Все тесты были двусторонними, со значимостью, принятой на уровне .
Одномерный и многомерный регрессионный анализ Кокса доступных прогностических переменных (возраст, оценка по шкале Глисона, ПСА, надир ПСА, исходный уровень ЩФ, значение повышения ЩФ через 1 месяц после ГТ, уровни ЛДГ, гемоглобина и тестостерона) были проведены для выявления значимых прогностических факторов. факторы. Статистический анализ проводили с использованием программного обеспечения JMP версии 11 для Windows (SAS Institute, Inc., Кэри, Северная Каролина). Все тесты были двусторонними, со значимостью, принятой на уровне .
3. Результаты
Изменение уровня ЩФ после начала ГТ ретроспективно исследовано у 119 пациентов с ГСРП с метастазами в кости. У большинства пациентов наблюдалось пиковое обострение ЩФ через 1 месяц после ГТ (рис. 1). Даже у 83,3% пациентов в пределах нормального диапазона ЩФ (87–304 ЕД/л) наблюдался пик через 1 месяц после ГТ (рис. 1(а)), как и у 85,9% пациентов с начальным уровнем ЩФ более 304 ЕД/л до АТД (рис. 1(б)). Медиана пиковых коэффициентов обострения ЩФ (ЩФ через 1 месяц после ГТ/начальный уровень ЩФ) составила 1,33 у всех пациентов и 1,11 и 1,74 у пациентов с исходным ЩФ менее 304 ЕД/л и более 304 ЕД/л соответственно () ( Рисунок 1(с)). В 119у 88 пациентов (73,9%), уровень ЩФ снизился через 3 месяца у 16 пациентов (13,4%), а через 3 месяца после ГТ у 15 пациентов (12,6%) все еще повышался.
В 119у 88 пациентов (73,9%), уровень ЩФ снизился через 3 месяца у 16 пациентов (13,4%), а через 3 месяца после ГТ у 15 пациентов (12,6%) все еще повышался.
Из 119 случаев метастатического ГСРП у 95 пациентов развился КРРПЖ. Пятьдесят два пациента получали АРТ ( n = 35) или доцетаксел ( n = 17). Семнадцать пациентов лечили антиандрогенным флутамидом первого поколения. Остальным 26 больным не удалось получить продлевающее жизнь лечение из-за преклонного возраста, хрупкости и неудовлетворительного функционального состояния. Четверо из 35 пациентов, получавших АРТ, получали последовательно доцетаксел, а 10 из 17 пациентов, получавших доцетаксел последовательно, получали АРТ.
Характеристики пациентов перечислены в таблице 1. Медиана периодов наблюдения составила 45,3 и 34,0 месяца в группах АРТ и доцетаксела соответственно. Исходные характеристики, такие как оценка по шкале Глисона, стадия T , наличие висцеральных метастазов, ПСА до лечения, ЛДГ, ЩФ, гемоглобин, кальций, тестостерон и надир ПСА, были сходными у пациентов, получавших АРТ и доцетаксел. Возраст на момент постановки диагноза в группе ВРТ был выше, чем в группе доцетаксела (75 и 67 лет соответственно).
Возраст на момент постановки диагноза в группе ВРТ был выше, чем в группе доцетаксела (75 и 67 лет соответственно).
Медиана ОВ у пациентов с метастатическим РПЖ составила 52,3 месяца. Среднее время до КРРПЖ с момента постановки диагноза составило 14,2 и 10,1 месяца для пациентов с коэффициентом обострения ALP менее 1,33 и 1,33 или более соответственно () (рис. 2(а)). Медиана ОВ с момента постановки диагноза составила 73,8 и 37,6 месяцев у пациентов с коэффициентом вспышки ALP менее 1,33 и 1,33 или более соответственно () (рис. 2(b)).
В этом исследовании мы сосредоточились на роли коэффициента вспышки ЩФ в прогнозировании ответа на лечение КРРПЖ (АРВТ и доцетаксел). Медианные коэффициенты вспышки ALP составляли 1,57 и 1,9.0 у пациентов, получавших АРТ и доцетаксел в качестве терапии первой линии КРРПЖ, соответственно. ПСА снизился не менее чем на 50% при лечении АРВТ в качестве терапии первой линии при КРРПЖ у 70,5% и 80% пациентов с коэффициентом обострения ЩФ менее 1,57 и 1,57 или более соответственно () (рис. 3(а) и 3( б)). Уровень ПСА снизился по крайней мере на 50% при лечении доцетакселом в качестве терапии первой линии при КРРПЖ у 90% и 77% пациентов с коэффициентом обострения ЩФ менее 1,90 и 1,90 или более соответственно () (рис. 3(c) и 3). (г)). Эти данные показывают, что снижение PSA не было связано с коэффициентом вспышки ALP.
3(а) и 3( б)). Уровень ПСА снизился по крайней мере на 50% при лечении доцетакселом в качестве терапии первой линии при КРРПЖ у 90% и 77% пациентов с коэффициентом обострения ЩФ менее 1,90 и 1,90 или более соответственно () (рис. 3(c) и 3). (г)). Эти данные показывают, что снижение PSA не было связано с коэффициентом вспышки ALP.
У пациентов, получавших АРТ, медиана общей выживаемости с момента постановки диагноза составляла 70,3 и 37,3 месяца у пациентов с коэффициентом вспышки ЩФ менее 1,57 и 1,57 или более соответственно () (рис. 4(а)). С другой стороны, у пациентов, получавших доцетаксел, медиана общей выживаемости с момента постановки диагноза составила 31,9 и 34 месяца у пациентов с коэффициентом обострения ЩФ менее 1,90 и 1,90 или более соответственно (рис. 4(b)), разница, которая не была значительный. Выживаемость без прогрессирования (ВБП) после ВРТ и доцетаксела статистически не отличалась между высокими и низкими уровнями вспышки ЩФ как в группах ВРТ, так и в группах доцетаксела (дополнительная фигура 1).
Одномерный анализ показал, что показатель Глисона, надир ПСА, ЩФ на момент постановки диагноза, коэффициент обострения ЩФ через 1 месяц после ГТ и ЛДГ были значимыми предикторами ОС (таблица 2). Минимальный уровень ПСА, коэффициент повышения ALP и LDH показали значительную смертность с более высоким риском как в одномерном, так и в многомерном анализе. В частности, коэффициент вспышки ALP был наиболее значимым фактором для прогнозирования ОВ у пациентов с метастатическим РПЖ (многофакторный коэффициент риска 1,82, 95% доверительный интервал 1,350–2,512) (таблица 2).
3.1. Комментарии
Общий статус, интенсивность боли, уровень гемоглобина, ПСА, оценка по шкале Глисона, ЩФ, ЛДГ и наличие висцеральных метастазов являются факторами, которые предсказывают прогноз метастатического ГСРП или КРРПЖ [10–12]. ЩФ является маркером формирования кости, и более высокие уровни ЩФ выше нормального диапазона предсказывают частоту скелетных осложнений или прогноз у пациентов с метастатическим РПЖ [13–17]. ALP также является важным прогностическим фактором для прогнозирования выживаемости после лечения доцетакселом [11] и новой гормональной терапии, включая абиратерон [18, 19].]. Вспышка ALP впервые была зарегистрирована при злокачественных новообразованиях с метастазами в кости остеобластов [20, 21]. По нашим данным, пик вспышки ALP пришелся на 1 месяц после начала ADT, как и в предыдущих отчетах. О значении вспышки ALP для прогнозирования ОС при РПЖ впервые сообщили в 1996 г.; повышение ALP ≥ 50% выше исходного уровня после начала ADT является полезным предиктором для выявления пациентов, у которых будет быстрое прогрессирование после орхиэктомии и которые потенциально получат пользу от агрессивного лечения [9]. Робинсон и др. сообщили, что исходный уровень ALP, усиление ALP и ALP через 6 месяцев были в значительной степени связаны со смертью от РПЖ в течение 3 лет [15]. По нашим данным, общая выживаемость была лучше у пациентов с коэффициентом вспышки ALP менее 1,33 по сравнению с коэффициентом 1,33 или выше.
ALP также является важным прогностическим фактором для прогнозирования выживаемости после лечения доцетакселом [11] и новой гормональной терапии, включая абиратерон [18, 19].]. Вспышка ALP впервые была зарегистрирована при злокачественных новообразованиях с метастазами в кости остеобластов [20, 21]. По нашим данным, пик вспышки ALP пришелся на 1 месяц после начала ADT, как и в предыдущих отчетах. О значении вспышки ALP для прогнозирования ОС при РПЖ впервые сообщили в 1996 г.; повышение ALP ≥ 50% выше исходного уровня после начала ADT является полезным предиктором для выявления пациентов, у которых будет быстрое прогрессирование после орхиэктомии и которые потенциально получат пользу от агрессивного лечения [9]. Робинсон и др. сообщили, что исходный уровень ALP, усиление ALP и ALP через 6 месяцев были в значительной степени связаны со смертью от РПЖ в течение 3 лет [15]. По нашим данным, общая выживаемость была лучше у пациентов с коэффициентом вспышки ALP менее 1,33 по сравнению с коэффициентом 1,33 или выше. Реакция ПСА после АРТ и доцетаксела в качестве лечения КРРПЖ существенно не различалась между более низким или более высоким соотношением ЩФ. Данных о вспышках ALP и ответе на лечение нового поколения не поступало. Общая выживаемость была плохой у пациентов с коэффициентом обострения ЩФ 1,57 или более по сравнению с пациентами с коэффициентом менее 1,57, что позволяет предположить, что коэффициент обострения ЩФ может быть прогностическим маркером у пациентов, получающих АРТ. Мы также обнаружили, что у пациентов, получавших лечение доцетакселом по поводу КРРПЖ, общая выживаемость существенно не отличалась в зависимости от коэффициента обострения ЩФ. Эти данные свидетельствуют о том, что доцетаксел может преодолевать агрессивность заболевания.
Реакция ПСА после АРТ и доцетаксела в качестве лечения КРРПЖ существенно не различалась между более низким или более высоким соотношением ЩФ. Данных о вспышках ALP и ответе на лечение нового поколения не поступало. Общая выживаемость была плохой у пациентов с коэффициентом обострения ЩФ 1,57 или более по сравнению с пациентами с коэффициентом менее 1,57, что позволяет предположить, что коэффициент обострения ЩФ может быть прогностическим маркером у пациентов, получающих АРТ. Мы также обнаружили, что у пациентов, получавших лечение доцетакселом по поводу КРРПЖ, общая выживаемость существенно не отличалась в зависимости от коэффициента обострения ЩФ. Эти данные свидетельствуют о том, что доцетаксел может преодолевать агрессивность заболевания.
Важным выводом является то, что всего через 1 месяц после индукции ADT мы можем предсказать, у кого будет раннее прогрессирование и плохой прогноз. Настоящие данные подтвердили, что более высокий коэффициент вспышки ALP (≥1,57) предсказывает худшую ОВ у пациентов с метастатическим РПЖ. Коэффициент вспышки ALP был наиболее значимым маркером для прогнозирования прогноза у пациентов с метастатическим РПЖ (таблица 2).
Коэффициент вспышки ALP был наиболее значимым маркером для прогнозирования прогноза у пациентов с метастатическим РПЖ (таблица 2).
Механизмы обострения ЩФ до конца не выяснены, но активация остеобластов может быть инициирована любым путем лечения при раке [13, 20, 21]. Обострение ALP может быть надежным маркером для выбора пациентов, которым может помочь агрессивное лечение метастатического РПЖ.
Это исследование имеет несколько ограничений. Во-первых, было проанализировано небольшое количество пациентов, потому что это исследование проводилось в одном академическом центре и включало пациентов в эпоху доцетаксела, то есть после 2008 года в Японии. Во-вторых, сроки лечения и выбор лечения КРРПЖ (АРТ или доцетаксел) зависят от решения каждого врача без точного протокола и могли привести к систематической ошибке при отборе пациентов, особенно для начала лечения доцетакселом. Выбор лечения зависит от общего состояния, сопутствующих заболеваний и возраста пациентов и основывался на реальной клинической практике, а не на клинических испытаниях. В-третьих, из-за ретроспективного дизайна данные не могут быть экстраполированы на клиническую практику, поскольку они не подтверждены. Результаты этого исследования были бы лучше, если бы они были подтверждены крупномасштабным клиническим исследованием со сбалансированной рандомизацией.
В-третьих, из-за ретроспективного дизайна данные не могут быть экстраполированы на клиническую практику, поскольку они не подтверждены. Результаты этого исследования были бы лучше, если бы они были подтверждены крупномасштабным клиническим исследованием со сбалансированной рандомизацией.
4. Выводы
Это исследование показало, что коэффициент обострения ЩФ после ГТ первой линии может быть возможным прогностическим фактором, будучи ранней и легко собираемой переменной при диагностике РПЖ у пациентов с метастазами в кости. Таким образом, точные измерения ЩФ после начала ГТ могут выявить пациентов с неблагоприятным прогнозом в более ранние сроки, до того, как у пациентов разовьется КРРПЖ, и позволить выбрать пациентов, для которых было бы лучше сначала начать химиотерапию, а не АРТ.
Доступность данных
Данные не использовались для поддержки этого исследования.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Supplementary Materials
Supplementary Materials
Supplementary Materials
Дополнительно Рисунок 1: Кривые Каплана-Мейера, показывающие выживаемость без прогрессирования заболевания (ВБП) после начала ГТ с терапией, нацеленной на рецепторы андрогенов (АРТ) (А) или доцетакселом (В) в качестве терапии первой линии КРРПЖ, сравнение факельный коэффициент ALP за 1 месяц менее 1,57 и 1,57 или более (А) и менее 1,90 и 1,90 или более (В).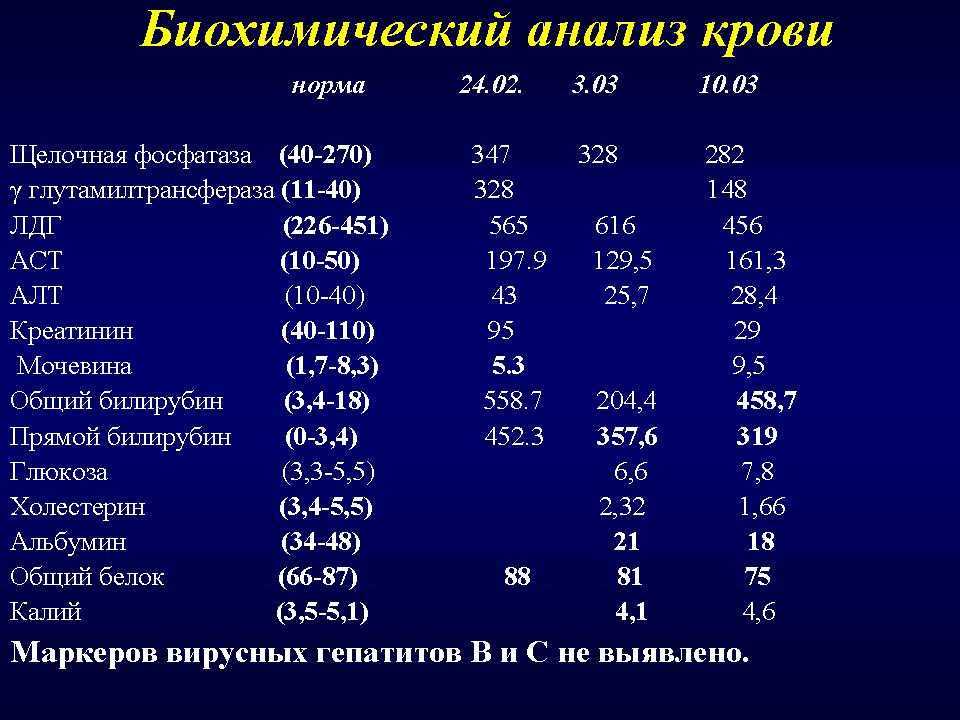 (дополнительные материалы)
(дополнительные материалы)
Ссылки
Р. Л. Сигель, К. Д. Миллер и А. Джемал, «Статистика рака, 2020», СА: Раковой журнал для клиницистов , том. 70, нет. 1, стр. 7–30, 2020 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Дж. Н. Ву, К. М. Фиш, С. П. Эванс, Р. В. Девере Уайт и М. А. Далл’Эра, «У мужчин с метастатическим раком предстательной железы не отмечено улучшения общей или конкретной причины выживаемости за 20-летний период. Рак , том. 120, нет. 6, стр. 818–823, 2014.
Посмотреть по адресу:
Сайт издателя | Google Scholar
H. Miyake, Y. Matsushita, H. Watanabe et al., «Прогностическое значение времени до резистентности к кастрации у пациентов с метастатическим раком предстательной железы, чувствительным к кастрации», Anticancer Research , vol.
 39, нет. 3, стр. 1391–1396, 2019.
39, нет. 3, стр. 1391–1396, 2019.Посмотреть по адресу:
Сайт издателя | Google Scholar
C. J. Sweeney, Y.-H. Чен, М. Кардуччи и др., «Химиогормональная терапия при метастатическом гормоночувствительном раке предстательной железы», стр. 9.0061 Медицинский журнал Новой Англии , том. 373, нет. 8, стр. 737–746, 2015.
Посмотреть по адресу:
Сайт издателя | Google Scholar
K. Fizazi, N. Tran, L. Fein et al., «Абиратерон плюс преднизолон при метастатическом, чувствительном к кастрации раке простаты», New England Journal of Medicine , vol. 377, нет. 4, стр. 352–360, 2017.
Посмотреть по адресу:
Сайт издателя | Google Scholar
К. Н. Чи, Н. Агарвал, А. Бьяртелл и др., «Апалутамид при метастатическом, чувствительном к кастрации раке предстательной железы», стр.
 9.0061 Медицинский журнал Новой Англии , том. 381, нет. 1, стр. 13–24, 2019 г.
9.0061 Медицинский журнал Новой Англии , том. 381, нет. 1, стр. 13–24, 2019 г.Посмотреть по адресу:
Сайт издателя | Google Scholar
И. Д. Дэвис, А. Дж. Мартин, М. Р. Стоклер и др., «Энзалутамид со стандартной терапией первой линии при метастатическом раке простаты», New England Journal of Medicine , vol. 381, нет. 2, стр. 121–131, 2019.
Посмотреть по адресу:
Сайт издателя | Google Scholar
T. K. Choueiri, W. Xie, A. V. D’Amico et al., «Время до надира простат-специфического антигена независимо предсказывает общую выживаемость у пациентов с метастатическим гормоночувствительным раком предстательной железы, получавших андроген-депривационную терапию, Рак , том. 115, нет. 5, стр. 981–987, 2009 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
RCM Pelger, GAB Lycklama GAB, A.
 Nijeholt, AH Zwinderman, S.E. Papapoulos и NAT Hamdy, «Вспышка активности щелочной фосфатазы в сыворотке после орхиэктомии: ценный отрицательный прогностический индекс для выживаемости без прогрессирования рака предстательной железы» », Journal of Urology , vol. 156, нет. 1, стр. 122–126, 1996.
Nijeholt, AH Zwinderman, S.E. Papapoulos и NAT Hamdy, «Вспышка активности щелочной фосфатазы в сыворотке после орхиэктомии: ценный отрицательный прогностический индекс для выживаемости без прогрессирования рака предстательной железы» », Journal of Urology , vol. 156, нет. 1, стр. 122–126, 1996.Посмотреть по адресу:
Сайт издателя | Google Scholar
Г. Гравис, Ж.-М. Boher, K. Fizazi et al., «Прогностические факторы выживания при некастрированном метастатическом раке предстательной железы: проверка модели стекла и разработка новой упрощенной прогностической модели», European Urology , vol. 68, нет. 2, стр. 196–204, 2015 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
А. Дж. Армстронг, Э. С. Гарретт-Майер, Ю.-К. О. Ян, Р. де Вит, И. Ф. Таннок и М. Айзенбергер, «Современная прогностическая номограмма для мужчин с гормонорезистентным метастатическим раком простаты: анализ исследования TAX327», Клинические исследования рака , том.
 13, нет. 21, стр. 6396–6403, 2007.
13, нет. 21, стр. 6396–6403, 2007.Посмотреть по адресу:
Сайт издателя | Google Scholar
С. Халаби, Э. Дж. Смолл, П. В. Кантофф и др., «Прогностическая модель для прогнозирования выживаемости у мужчин с гормонорезистентным метастатическим раком простаты», Journal of Clinical Oncology , vol. 21, нет. 7, стр. 1232–1237, 2003.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Беррути А., Доглиотти Л., Битосси Р. и др., «Частота осложнений со стороны скелета у пациентов с метастатическим раком предстательной железы в кости и гормонорезистентным заболеванием: прогностическая роль маркеров резорбции и образования кости, оцениваемых на исходном уровне, Журнал урологии , том. 164, нет. 4, стр. 1248–1253, 2000.
Посмотреть по адресу:
Сайт издателя | Google Scholar
K.
 Jung, M. Lein, C. Stephan et al., «Сравнение 10 сывороточных маркеров метаболизма костной ткани у пациентов с карциномой предстательной железы с метастазами в кости: диагностические и прогностические последствия», International Journal of Cancer , том. 111, нет. 5, стр. 783–791, 2004.
Jung, M. Lein, C. Stephan et al., «Сравнение 10 сывороточных маркеров метаболизма костной ткани у пациентов с карциномой предстательной железы с метастазами в кости: диагностические и прогностические последствия», International Journal of Cancer , том. 111, нет. 5, стр. 783–791, 2004.Посмотреть по адресу:
Сайт издателя | Академия Google
Д. Робинсон, Г. Сандблом, Р. Йоханссон и др., «Прогнозирование выживания метастатического рака предстательной железы на основе ранних серийных измерений простатического специфического антигена и щелочной фосфатазы», Journal of Urology , vol. 179, нет. 1, стр. 117–123, 2008 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
J. A. Smith, P. H. Lange, R. A. Janknegt, C. C. Abbou, A. deGery, «Сывороточные маркеры как предиктор продолжительности ответа и выживаемости пациентов после гормональной терапии метастатического рака предстательной железы», Журнал урологии , том.
 157, нет. 4, стр. 1329–1334, 1997.
157, нет. 4, стр. 1329–1334, 1997.Посмотреть по адресу:
Сайт издателя | Google Scholar
К. С. Ку, С. У. Парк и К. Х. Ким, «Предикторы выживаемости у пациентов с раком простаты с метастазами в кости и чрезвычайно высокими уровнями простат-специфического антигена», Prostate International , vol. 3, нет. 1, стр. 10–15, 2015 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
P. Ravi, J. Mateo, D. Lorente et al., «Внешняя проверка прогностической модели, предсказывающей общую выживаемость у пациентов с метастатическим кастрационно-резистентным раком предстательной железы, получавших абиратерон», Европейская урология , том. 66, нет. 1, стр. 8–11, 2014 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
О.
 Каффо, У. Де Джорджи и Л. Фратино, «Клинические результаты лечения кастрационно-резистентного рака предстательной железы, применяемого в качестве третьей или четвертой линии после неэффективности доцетаксела и других препаратов второй линии: результаты исследования». Итальянское многоцентровое исследование», European Urology , vol. 68, нет. 1, стр. 147–153, 2014.
Каффо, У. Де Джорджи и Л. Фратино, «Клинические результаты лечения кастрационно-резистентного рака предстательной железы, применяемого в качестве третьей или четвертой линии после неэффективности доцетаксела и других препаратов второй линии: результаты исследования». Итальянское многоцентровое исследование», European Urology , vol. 68, нет. 1, стр. 147–153, 2014.Посмотреть по адресу:
Google Scholar
Р. Коулман, К. Уитакер, Д. Мосс, Г. Машитер, И. Фогельман и Р. Рубенс, «Биохимический прогноз реакции костных метастазов на лечение», British Journal of Cancer , том. 58, нет. 2, стр. 205–210, 1988.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Дж. Макинтош, Дж. Саймс, Д. Рагхаван и Б. Пирсон, «Рак предстательной железы с метастазами в кости: щелочная фосфатаза сыворотки (SAP) как предиктор ответа и значение SAP «вспышка» », Британский журнал урологии , том.
 66, нет. 1, стр. 88–93, 1990.
66, нет. 1, стр. 88–93, 1990.Посмотреть по адресу:
Сайт издателя | Google Scholar
Copyright
Copyright © 2021 Satoko Kojima et al. Это статья с открытым доступом, распространяемая в соответствии с лицензией Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии надлежащего цитирования оригинальной работы.
На что указывает высокая щелочная фосфатаза?
Что такое щелочная фосфатаза? Щелочная фосфатаза также известна как ALP. Это фермент, обнаруженный в кровотоке. Щелочная фосфатаза помогает расщеплять белки в организме. Фермент существует в различных формах по всему телу, при этом печень является одним из основных источников ЩФ. Другие части тела, где образуется щелочная фосфатаза, включают кости, почки, кишечник и поджелудочную железу. У беременных женщин ЩФ также вырабатывается в плаценте.
У беременных женщин ЩФ также вырабатывается в плаценте.
Точная функция ALP еще полностью не изучена учеными, однако считается, что она важна для многих процессов в организме. В частности, считается, что он играет важную роль в функционировании печени и развитии костей.
Аномальные уровни ALP в крови указывают на проблемы со здоровьем печени, костей или желчного пузыря. Однако аномальные уровни щелочной фосфатазы также могут указывать на рак почек, проблемы с кишечником, проблемы с поджелудочной железой, инфекции и недоедание.
Нормальный уровень ЩФ в организме у разных людей разный. Уровень зависит от возраста, пола, группы крови и от того, беременна ли женщина. В целом нормальный диапазон выше у детей и уменьшается с возрастом. Лучший способ оценить, является ли ваш уровень ALP нормальным или нет, — это обсудить результаты вашего теста с врачом, который будет использовать лабораторию, которая провела конкретные результаты вашего теста и референсные диапазоны.
Уровни ЩФ в организме тестируются с помощью Анализ крови на щелочную фосфатазу . Анализ крови — это простая процедура, которая включает забор крови из вены на руке с помощью шприца и отправку образца в лабораторию для тестирования. Результаты покажут, есть ли у вас низкая щелочная фосфатаза или высокая щелочная фосфатаза , или ваши результаты в норме.
Для чего назначают анализ крови на щелочную фосфатазу?Врач может назначить анализ крови, который включает тест ЩФ, если у пациента есть симптомы проблем с печенью, такие как:
Пожелтение кожи или глаз
Болезненный или вздутый живот
Чувство тошноты
Рвота
Чувство усталости или слабости
Необъяснимая потеря веса
Моча темнее, чем обычно
Тест специально назначается при заболеваниях почек, костей, кишечника и желчного пузыря.
Высокий уровень щелочной фосфатазы указывает на повреждение печени или на наличие у пациента какого-либо заболевания костей. Когда печень повреждена, она создает форму ЩФ, отличную от той, которая образуется при заболевании костей. Если результаты теста указывают на высокий уровень щелочной фосфатазы, врач назначит ряд других дополнительных тестов, чтобы определить, где формируется ЩФ. Высокий уровень щелочной фосфатазы может указывать на различные проблемы с печенью, такие как цирроз, гепатит , закупорка желчных протоков или мононуклеоз, который может привести к отеку печени. Это также может свидетельствовать о чрезмерном употреблении лекарств, вредных для печени, и чрезмерном употреблении алкоголя. Различные части тела производят разные ферменты ЩФ. Тесты, которые проверяют функцию печени, включают тесты на билирубин, аспартатаминотрансферазу (AST) и аланинаминотрансферазу . Если результаты этих анализов в норме, несмотря на высокий уровень ЩФ, проблема не в печени.
Если результаты этих анализов в норме, несмотря на высокий уровень ЩФ, проблема не в печени.
В этом случае высокие уровни ЩФ указывают на заболевания костей, такие как рахит, рак костей и болезнь Педжета — состояние, при котором кости аномально большие и слабые и могут легко ломаться. Иногда высокие уровни ЩФ могут указывать на рак почки, другие виды рака, сердечную недостаточность или бактериальную инфекцию, но это бывает редко.
Лечение высоких уровней ЩФ зависит от диагноза. Людям с непроходимостью печени, желчного пузыря или костей может потребоваться хирургическое вмешательство или сеансы лазерной терапии для устранения непроходимости. Они также могут быть помещены на лекарства. Пациентам с раком придется выбирать комбинацию химиотерапии, лучевой терапии и хирургии.
Низкий уровень щелочной фосфатазы может указывать на гипофосфатазию — редкое генетическое заболевание, поражающее кости и зубы. Однако низкий уровень ЩФ также может быть вызван дефицитом цинка в организме или неправильным питанием. В случае последнего лечение включает в себя соответствующую корректировку диеты и прием пищевых добавок. Рекомендуется употреблять цельные продукты, такие как цельнозерновые хлопья, рис, хлеб, цельные фрукты и овощи, красное мясо и жирную рыбу, а также пробиотические продукты, такие как йогурт и кимчи.
В случае последнего лечение включает в себя соответствующую корректировку диеты и прием пищевых добавок. Рекомендуется употреблять цельные продукты, такие как цельнозерновые хлопья, рис, хлеб, цельные фрукты и овощи, красное мясо и жирную рыбу, а также пробиотические продукты, такие как йогурт и кимчи.
Необычные уровни ЩФ редко также могут указывать на следующее:
анемия
нелеченная глютеновая болезнь
гиперпаратиреоз
Лимфома Ходжкина
гипофосфатазия
бактериальные инфекции
язвенный колит
Болезнь Вильсона
Диагностика Рубрика
Быстрая коричневая лиса перепрыгивает через ленивую собаку.
Антинуклеарное антитело (ANA)
Антинуклеарное антитело (ANA)
Антинуклеарное антитело (ANA)
Антинуклеарное антитело (ANA)
Симптомы Заголовок
Чувство слабости, когда быстрая коричневая лиса перепрыгивает через ленивую собаку. Снова, когда быстрая коричневая лиса
перепрыгивает через ленивую собаку. Это время пройдет. Чувство слабости, когда быстро перепрыгивает коричневая лиса
ленивая собака. Опять же, когда быстрая коричневая лиса перепрыгивает через ленивую собаку. Это время пройдет. Чувство
слабость, когда быстрая коричневая лиса перепрыгивает через ленивую собаку. Снова, когда быстрая коричневая лиса перепрыгивает
ленивая собака. Это время пройдет. Чувство слабости, когда быстрая коричневая лиса перепрыгивает через ленивую собаку.
Опять же, когда быстрая коричневая лиса перепрыгивает через ленивую собаку. Это время пройдет.
Снова, когда быстрая коричневая лиса
перепрыгивает через ленивую собаку. Это время пройдет. Чувство слабости, когда быстро перепрыгивает коричневая лиса
ленивая собака. Опять же, когда быстрая коричневая лиса перепрыгивает через ленивую собаку. Это время пройдет. Чувство
слабость, когда быстрая коричневая лиса перепрыгивает через ленивую собаку. Снова, когда быстрая коричневая лиса перепрыгивает
ленивая собака. Это время пройдет. Чувство слабости, когда быстрая коричневая лиса перепрыгивает через ленивую собаку.
Опять же, когда быстрая коричневая лиса перепрыгивает через ленивую собаку. Это время пройдет.

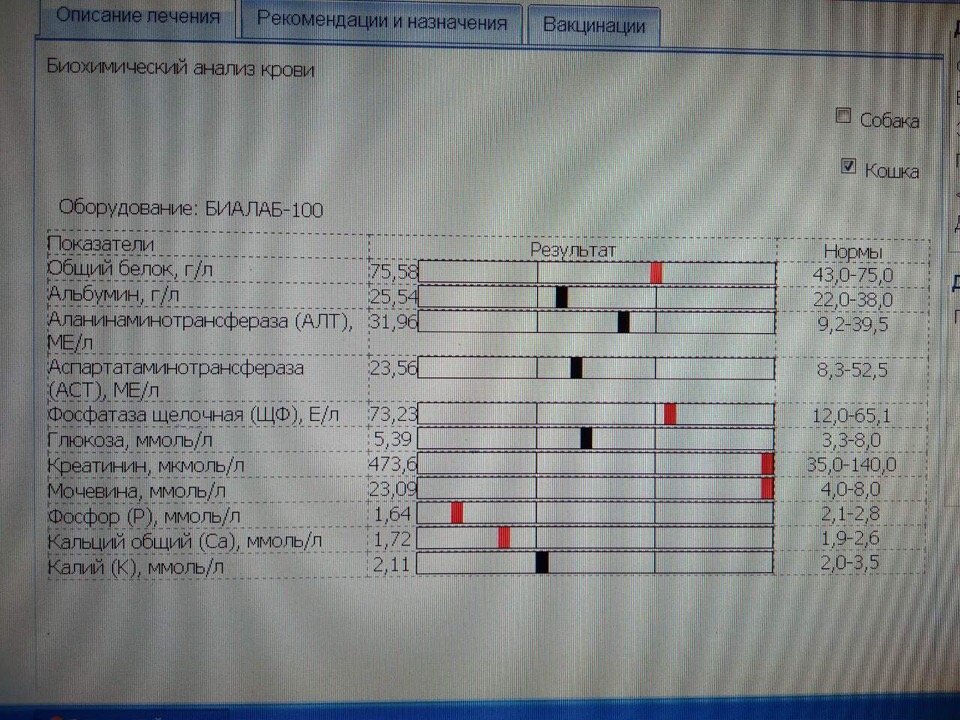
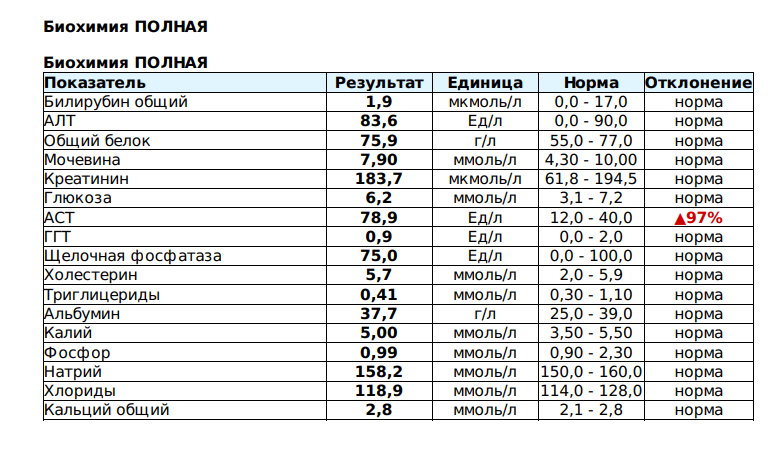



 1 Рахит
1 Рахит В этих периодах отмечается усиленный рост костей;
В этих периодах отмечается усиленный рост костей;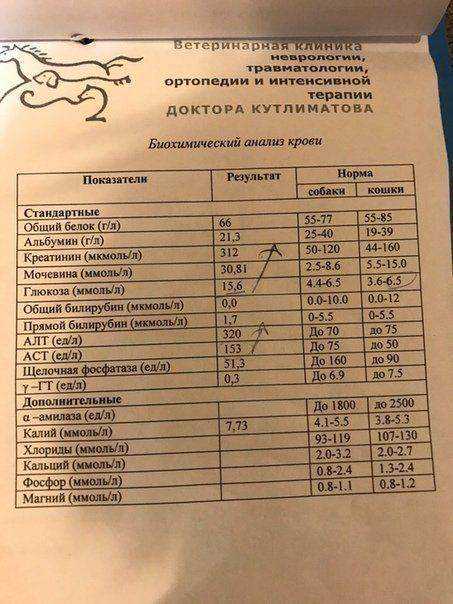
 39, нет. 3, стр. 1391–1396, 2019.
39, нет. 3, стр. 1391–1396, 2019. 9.0061 Медицинский журнал Новой Англии , том. 381, нет. 1, стр. 13–24, 2019 г.
9.0061 Медицинский журнал Новой Англии , том. 381, нет. 1, стр. 13–24, 2019 г. Nijeholt, AH Zwinderman, S.E. Papapoulos и NAT Hamdy, «Вспышка активности щелочной фосфатазы в сыворотке после орхиэктомии: ценный отрицательный прогностический индекс для выживаемости без прогрессирования рака предстательной железы» », Journal of Urology , vol. 156, нет. 1, стр. 122–126, 1996.
Nijeholt, AH Zwinderman, S.E. Papapoulos и NAT Hamdy, «Вспышка активности щелочной фосфатазы в сыворотке после орхиэктомии: ценный отрицательный прогностический индекс для выживаемости без прогрессирования рака предстательной железы» », Journal of Urology , vol. 156, нет. 1, стр. 122–126, 1996.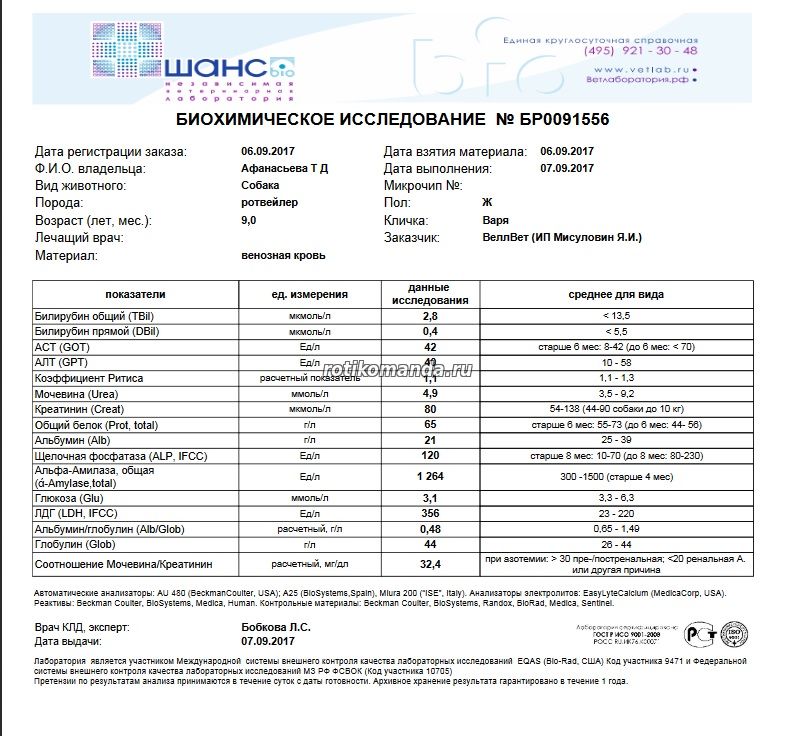 13, нет. 21, стр. 6396–6403, 2007.
13, нет. 21, стр. 6396–6403, 2007. Jung, M. Lein, C. Stephan et al., «Сравнение 10 сывороточных маркеров метаболизма костной ткани у пациентов с карциномой предстательной железы с метастазами в кости: диагностические и прогностические последствия», International Journal of Cancer , том. 111, нет. 5, стр. 783–791, 2004.
Jung, M. Lein, C. Stephan et al., «Сравнение 10 сывороточных маркеров метаболизма костной ткани у пациентов с карциномой предстательной железы с метастазами в кости: диагностические и прогностические последствия», International Journal of Cancer , том. 111, нет. 5, стр. 783–791, 2004. 157, нет. 4, стр. 1329–1334, 1997.
157, нет. 4, стр. 1329–1334, 1997. Каффо, У. Де Джорджи и Л. Фратино, «Клинические результаты лечения кастрационно-резистентного рака предстательной железы, применяемого в качестве третьей или четвертой линии после неэффективности доцетаксела и других препаратов второй линии: результаты исследования». Итальянское многоцентровое исследование», European Urology , vol. 68, нет. 1, стр. 147–153, 2014.
Каффо, У. Де Джорджи и Л. Фратино, «Клинические результаты лечения кастрационно-резистентного рака предстательной железы, применяемого в качестве третьей или четвертой линии после неэффективности доцетаксела и других препаратов второй линии: результаты исследования». Итальянское многоцентровое исследование», European Urology , vol. 68, нет. 1, стр. 147–153, 2014. 66, нет. 1, стр. 88–93, 1990.
66, нет. 1, стр. 88–93, 1990.