Гемоторакс степени: причины, симптомы, диагностика и лечение
причины, симптомы, диагностика и лечение
Гемоторакс – это кровотечение в полость плевры, скопление крови между ее листками, приводящее к сдавлению легкого и смещению органов средостения в противоположную сторону. При гемотораксе отмечается боль в грудной клетке, затруднение дыхания, развиваются признаки острой кровопотери (головокружение, бледность кожных покровов, тахикардия, гипотония, холодный липкий пот, обмороки). Диагностика гемоторакса основана на физикальных данных, результатах рентгеноскопии и рентгенографии грудной клетки, КТ, диагностической плевральной пункции. Лечение гемотракса включает гемостатическую, антибактериальную, симптоматическую терапию; аспирацию скопившейся крови (пункции, дренирование плевральной полости), при необходимости – открытое или видеоторакоскопическое удаление свернувшегося гемоторакса, остановку продолжающегося кровотечения.
Общие сведения
Гемоторакс является вторым по частоте (после пневмоторакса) осложнением травм грудной клетки и встречается у 25 % больных с торакальной травмой.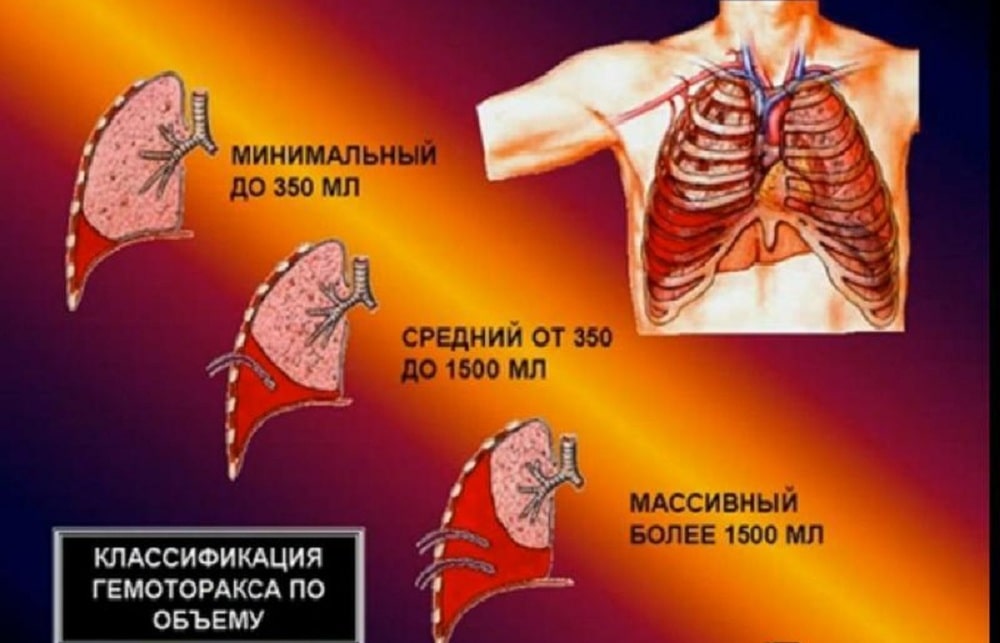 Довольно часто в клинической практике наблюдается комбинированная патология — гемопневмоторакс. Опасность гемоторакса заключается как в нарастающей дыхательной недостаточности, обусловленной сдавлением легкого, так и в развитии геморрагического шока вследствие острого внутреннего кровотечения. В пульмонологии и торакальной хирургии гемотракс расценивается как неотложное состояние, требующее оказания экстренной специализированной помощи.
Довольно часто в клинической практике наблюдается комбинированная патология — гемопневмоторакс. Опасность гемоторакса заключается как в нарастающей дыхательной недостаточности, обусловленной сдавлением легкого, так и в развитии геморрагического шока вследствие острого внутреннего кровотечения. В пульмонологии и торакальной хирургии гемотракс расценивается как неотложное состояние, требующее оказания экстренной специализированной помощи.
Гемоторакс
Причины гемоторакса
Выделяют три группы причин, наиболее часто приводящих к развитию гемоторакса: травматические, патологические и ятрогенные.
- Под травматическими причинами понимают проникающие ранения или закрытые повреждения грудной клетки. К торакальной травме, сопровождающейся развитием гемоторакса, относятся ДТП, огнестрельные и ножевые ранения грудной клетки, переломы ребер, падения с высоты и др. При подобных травмах довольно часто происходит повреждение органов грудной полости (сердца, легких, диафрагмы), органов брюшной полости (травмы печени, селезенки), межреберных сосудов, внутренней грудной артерии, внутригрудных ветвей аорты, кровь из которых изливается в плевральную полость.

- К причинам гемоторакса патологического характера причисляют различные заболевания: рак легкого или плевры, аневризму аорты, туберкулез легких, абсцесс легкого, новообразования средостения и грудной стенки, геморрагический диатез, коагулопатии и др.
- Ятрогенными факторами, приводящими к развитию гемоторакса, выступают осложнения операций на легких и плевре, торакоцентеза, дренирования плевральной полости, катетеризации центральных вен.
Патогенез
Скопление крови в полости плевры вызывает компрессию легкого на стороне поражения и смещение органов средостения в противоположную сторону. Это сопровождается уменьшением дыхательной поверхности легкого, возникновением расстройств дыхания и гемодинамики. Поэтому при гемотраксе нередко развивается клиника геморрагического и кардио-пульмонального шока с острой дыхательной и сердечной недостаточностью.
Уже в ближайшие часы после попадания крови в плевральную полость развивается асептическое воспаление плевры — гемоплеврит, обусловленный реакцией плевральных листков.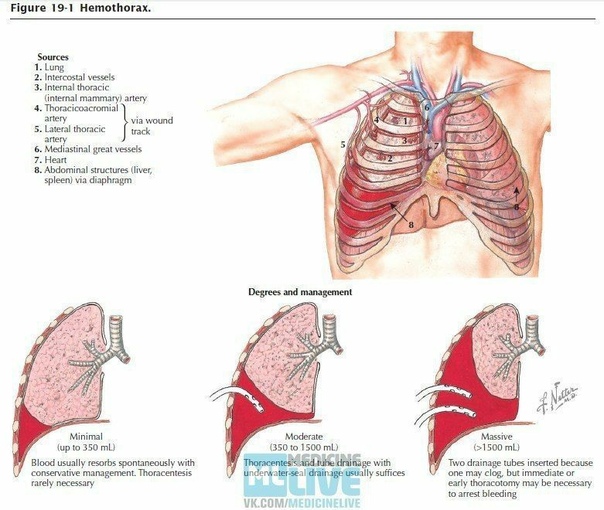 При гемотораксе возникает отек и умеренная лейкоцитарная инфильтрация плевры, набухание и слущивание клеток мезотелия. В начальном периоде излившаяся в плевральную полость кровь практически не отличается по составу от периферической крови. В дальнейшем в ней происходит снижение гемоглобина, уменьшение эритроцитарно-лейкоцитарного индекса.
При гемотораксе возникает отек и умеренная лейкоцитарная инфильтрация плевры, набухание и слущивание клеток мезотелия. В начальном периоде излившаяся в плевральную полость кровь практически не отличается по составу от периферической крови. В дальнейшем в ней происходит снижение гемоглобина, уменьшение эритроцитарно-лейкоцитарного индекса.
Попадая в плевральную полость, кровь вначале сворачивается. Однако затем вскоре наступает процесс фибринолиза, и происходит повторное разжижение крови. Этому способствуют антикоагулянтные факторы, содержащиеся в самой крови и плевральной жидкости, а также механическое дефибринирование крови за счет дыхательной экскурсии грудной клетки. По мере истощения механизмов антикоагуляции происходит свертывание крови и формирование свернувшегося гемоторакса. В случае присоединения микробного инфицирования на фоне гемоторакса довольно быстро может возникать эмпиема плевры.
Классификация
В соответствии с этиологией различают травматический, патологический и ятрогенный гемоторакс. С учетом величины внутриплеврального кровотечения гемоторакс может быть:
С учетом величины внутриплеврального кровотечения гемоторакс может быть:
- малый — объем кровопотери до 500 мл, скопление крови в синусе;
- средний — объем до 1,5 л, уровень крови до нижнего края IV ребра;
- субтотальный — объем кровопотери до 2 л, уровень крови до нижнего края II ребра;
- тотальный — объем кровопотери свыше 2 л, рентгенологически характеризуется тотальным затемнением плевральной полости на стороне поражения.
Кроме этого, также выделяют ограниченный (обычно малый по объему) гемоторакс, при котором излившаяся кровь скапливается между плевральными спайками, на изолированном участке полости плевры. С учетом локализации ограниченный гемоторакс бывает верхушечным, междолевым, паракостальным, наддиафрагмальным, парамедиастинальным.
С учетом локализации ограниченный гемоторакс бывает верхушечным, междолевым, паракостальным, наддиафрагмальным, парамедиастинальным.
В случае продолжающегося внутриплеврального кровотечения говорят о нарастающем гемотораксе, в случае прекращения кровотечения – о ненарастающем (стабильном). К осложненным видам относят свернувшийся и инфицированный гемоторакс (пиогемоторакс). При одновременном попадании в полость плевры воздуха и крови, говорят о гемопневмотораксе.
Симптомы гемоторакса
Клиническая симптоматика гемоторакса зависит от степени кровотечения, сдавления легочной ткани и смещения органов средостения. При малом гемотораксе клинические проявления выражены минимально или отсутствуют. Основными жалобами служат боли в грудной клетке, усиливающиеся при кашле, умеренная одышка.
При гемотораксе среднего или большого размера развиваются дыхательные и сердечно-сосудистые расстройства, выраженные в различной степени. Характерна резкая боль в груди, иррадиирующая в плечо и спину при дыхании и кашле; общая слабость, тахипноэ, снижение АД. Даже при незначительной физической нагрузке происходит усиление симптоматики. Больной обычно принимает вынужденное сидячее или полусидячее положение.
Характерна резкая боль в груди, иррадиирующая в плечо и спину при дыхании и кашле; общая слабость, тахипноэ, снижение АД. Даже при незначительной физической нагрузке происходит усиление симптоматики. Больной обычно принимает вынужденное сидячее или полусидячее положение.
При тяжелом гемотораксе на первый план выступает клиника внутриплеврального кровотечения: слабость и головокружение, холодный липкий пот, тахикардия и гипотония, бледность кожных покровов с цианотичным оттенком, мелькание мушек перед глазами, обмороки.
Гемоторакс, сопряженный с переломом ребер, как правило, сопровождается подкожной эмфиземой, гематомами мягких тканей, деформацией, патологической подвижностью и крепитацией отломков ребер. При гемотораксе, протекающем с разрывом легочной паренхимы, может возникать кровохарканье.
В 3-12% случаев формируется свернувшийся гемоторакс, при котором в полости плевры образуются кровяные сгустки, фибринные наслоения и шварты, ограничивающие дыхательную функцию легкого, вызывая развитие склеротических процессов в легочной ткани. Клиника свернувшегося гемоторакса характеризуется тяжестью и болью в грудной клетке, одышкой. При инфицированном гемотораксе (эмпиеме плевры) на первый план выходят признаки тяжелого воспаления и интоксикации: лихорадка, ознобы, вялость и др.
Клиника свернувшегося гемоторакса характеризуется тяжестью и болью в грудной клетке, одышкой. При инфицированном гемотораксе (эмпиеме плевры) на первый план выходят признаки тяжелого воспаления и интоксикации: лихорадка, ознобы, вялость и др.
Диагностика
Для постановки диагноза уточняются подробности истории заболевания, проводится физикальное, инструментальное и лабораторное обследование. При гемотораксе определяется отставание пораженной стороны грудной клетки при дыхании, притупление перкуторного звука над уровнем жидкости, ослабление дыхания и голосового дрожания. При рентгеноскопии и обзорной рентгенографии легких выявляется коллабирование легкого, наличие горизонтального уровня жидкости или сгустков в полости плевры, флотация (смещение) тени средостения в здоровую сторону.
С диагностической целью выполняется пункция плевральной полости: получение крови достоверно свидетельствует о гемотораксе. Для дифференциации стерильного и инфицированного гемоторакса проводят пробы Петрова и Эфендиева с оценкой прозрачности и осадка аспирата. С целью суждения о прекращении или продолжении внутриплеврального кровотечения выполняют пробу Рувилуа-Грегуара: свертывание полученной крови в пробирке или шприце свидетельствует о продолжающемся кровотечении, отсутствие коагуляции говорит о прекращении кровотечения. Образцы пунктата направляют в лабораторию для определения гемоглобина и проведения бактериологического исследования.
С целью суждения о прекращении или продолжении внутриплеврального кровотечения выполняют пробу Рувилуа-Грегуара: свертывание полученной крови в пробирке или шприце свидетельствует о продолжающемся кровотечении, отсутствие коагуляции говорит о прекращении кровотечения. Образцы пунктата направляют в лабораторию для определения гемоглобина и проведения бактериологического исследования.
При банальном и свернувшемся гемотораксе прибегают к лабораторному определению Нb, количества эритроцитов, тромбоцитов, исследованию коагулограммы. Дополнительная инструментальная диагностика при гемотораксе может включать УЗИ плевральной полости, рентгенографию ребер, КТ грудной клетки, диагностическую торакоскопию.
Лечение гемоторакса
Пациенты с гемотораксом госпитализируются в специализированные хирургические отделения и находятся под наблюдением торакального хирурга. С лечебной целью для аспирации/эвакуации крови производится дренирование плевральной полости с введением в дренаж антибиотиков и антисептиков (для профилактики инфицирования и санации), протеолитических ферментов (для растворения сгустков). Консервативное лечение гемоторакса включает проведение гемостатической, дезагрегантной, симптоматической, иммунокорригирующей, гемотрансфузионной терапии, общей антибиотикотерапии, оксигенотерапии.
Консервативное лечение гемоторакса включает проведение гемостатической, дезагрегантной, симптоматической, иммунокорригирующей, гемотрансфузионной терапии, общей антибиотикотерапии, оксигенотерапии.
Малый гемоторакс в большинстве случаев может быть ликвидирован консервативным путем. Хирургическое лечение гемоторакса показано в случае продолжающегося внутриплеврального кровотечения; при свернувшемся гемотораксе, препятствующем расправлению легкого; повреждении жизненно важных органов.
В случае ранения крупных сосудов или органов грудной полости производится экстренная торакотомия, перевязка сосуда, ушивание раны легкого или перикарда, удаление излившейся в плевральную полость крови. Свернувшийся гемоторакс является показанием к плановому выполнению видеоторакоскопии или открытой торакотомии для удаления сгустков крови и санации плевральной полости. При нагноении гемоторакса лечение проводится по правилам ведения гнойного плеврита.
Прогноз и профилактика
Успешность лечения гемоторакса определяется характером травмы или заболевания, интенсивностью кровопотери и своевременностью хирургической помощи. Прогноз наиболее благоприятен при малом и среднем неинфицированном гемотораксе. Свернувшийся гемоторакс повышает вероятность развития эмпиемы плевры. Продолжающееся внутриплевральное кровотечение или одномоментная большая кровопотеря могут привести к гибели пациента.
Прогноз наиболее благоприятен при малом и среднем неинфицированном гемотораксе. Свернувшийся гемоторакс повышает вероятность развития эмпиемы плевры. Продолжающееся внутриплевральное кровотечение или одномоментная большая кровопотеря могут привести к гибели пациента.
Исходом гемоторакса может являться образование массивных плевральных сращений, ограничивающих подвижность купола диафрагмы. Поэтому в период реабилитации пациентам, перенесшим гемоторакс, рекомендуются занятия плаванием и дыхательной гимнастикой. Профилактика гемоторакса заключается в предупреждении травматизма, обязательной консультации пациентов с торакоабдоминальной травмой хирургом, контроле гемостаза при операциях на легких и средостении, осторожном выполнении инвазивных манипуляций.
причины, симптомы, диагностика, лечение, профилактика
Это внутриплевральное кровотечение, которое сопровождается скоплением крови в плевральной полости, что вызывает сдавление легкого и смещение органов средостения в другую сторону.
Чаще всего развитие гемоторакса вызывают травмы, аномалии развития и ятрогенные причины. Под травматическим повреждением понимают проникающие раны или закрытые повреждения грудной клетки. Торокальные травмы, которые сопровождаются гемотораксом, возникают при дорожно-транспортных происшествиях, огнестрельных и ножевых ранениях грудной клетки, а также переломах ребер и падения с высоты. Чаще всего такие травмы сопровождаются нарушением целостности органов грудной клетки, брюшной полости, межреберных сосудов, внутренней грудной артерии, внутригрудных ветвей аорты, что вызывает истечением крови в полость плевры.
К патологическим причинам способным вызвать гемоторакс относятся такие заболевания, как аневризма аорты, туберкулезное поражение легких, рак легкого либо плевры, абсцесс легкого, опухолевые поражения средостения и грудной стенки, геморрагический диатез, коагулопатия.
Ятрогенными причинами гемоторакса, являются осложнения хирургического вмешательства на легких и плевре, торакоцентез, дренирование плевральной полости, катетеризация центральных вен.
Клиническая картина гемоторакса зависит от интенсивности кровотечения, степени сдавления легкого и выраженности смещения органов средостения. В случае развития малого гемоторакса симптомы отсутствуют либо слабо выражены. Основными симптомами недуга является боль в груди, усиливающаяся при кашле, и легкая одышка.
При тяжелом гемотораксе наблюдается развитие сердечнососудистых и дыхательных расстройств, которые проявляются в различной степени. При тяжелой степени заболевания в больных наблюдается резкая боль в грудной клетке, которая может иррадиировать в спину и плечо и усиливается при кашле и дыхании. Также у таких больных может возникать тахипноэ, слабость, снижение артериального давления. Усиление выраженности симптомов наблюдается даже при незначительных физических нагрузках. Такие больные, как правило, принимают вынужденное полусидящее положение.
При тяжелой форме гемоторакса наблюдается развитие симптомов внутриплеврального кровотечения, таких как слабость, головокружение, холодный липкий пот, учащение сердцебиения, снижение артериального давления, выраженная бледность кожи, появление цианотичного оттенка кожи, мелькание мушек перед глазами, потеря сознания.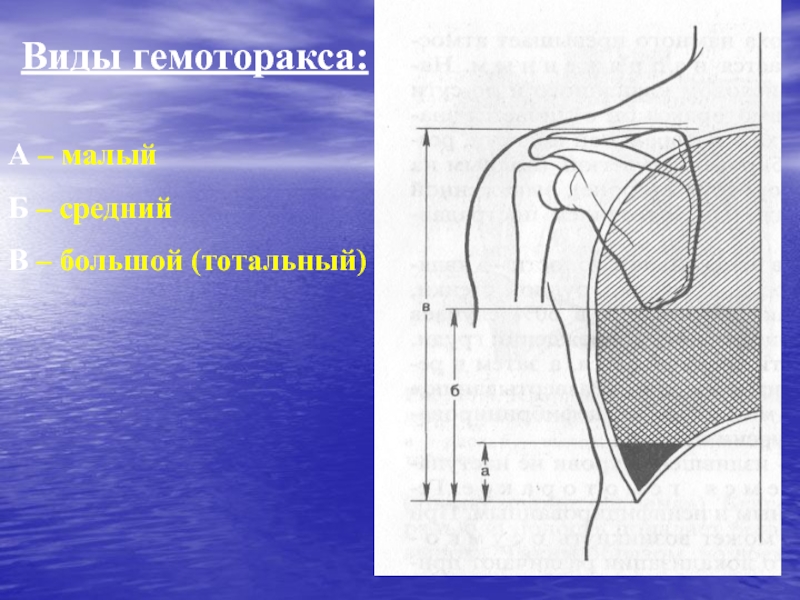
При постановке диагноза обязательно уточняется история заболевания, проводится физикальный осмотр пациента, а также назначаются необходимые инструментально-лабораторные методы исследования.
При гемотораксе у пациента может наблюдаться отставание в дыхании, притупление перкуторного звука в области скопления жидкости, ослабление дыхания и голосовое дрожание. Таким больным назначается проведение рентгеноскопии и обзорной рентгенографии легких, с диагностической целью может потребоваться проведение пункции плевральной полости.
ЛечениеЛечением гемоторакса занимается торакальный хирург. Для удаления крови из плевральной полости больному назначают торакоцентез или дренирование плевральной полости с введением в дренаж антибиотиков и антисептиков. Консервативное лечение гемоторакса включает проведение гемостатической, дезагрегантной, симптоматической, иммунокорригирующей, гемотрансфузионной терапии, общей антибиотикотерапии, оксигенотерапии.
Предупреждение гемоторакса основано на предупреждении травм грудной клетки либо своевременном лечении любых заболеваний, травм и инвазивных манипуляций, способных вызвать возникновение заболевания.
Гемоторакс — симптомы и лечение, причины
Общие сведения
Чаще всего образуется как осложнение после травм грудного отдела. Связано это состояние с повреждением сосудов составными элементами грудной клетки, находящимися в непосредственной близости к сердечно-легочному комплексу. Объем теряемой крови может варьироваться от степени повреждения плевры.
При повреждении межреберных артерий происходит массивное кровоизлияние, такой гемоторакс называют обширным. Данное состояние считается неотложным из-за нарастания механического сдавления легочного ствола, большого количества теряемой крови и требует срочного оперативного вмешательства. В таком случае выражен синдром легочной недостаточности.
Причины
 К ним относятся:
К ним относятся: - Механическое повреждение груди после огнестрельного или ножевого ранения.
- Травматизация грудной клетки.
- Переломы костного скелета торакальной области.
- Переломы компрессионного генеза.
- Изменение стенки аорты.
- Разрыв туберкулезной буллы.
- Злокачественные и доброкачественные новообразования трахеи, легких.
- Последствия хронической обструктивной болезни легких.
- Исходы хронических заболеваний со стороны крови.
- Осложнения после хирургических вмешательств в грудной клетке.
- Постановка центральных катетеров.
- Разрушение стенок бронхиального дерева.
Классификация
Классифицируют гемоторакс по степени кровотечения, течению, стороне процесса и присоединению инфекционного агента.
В зависимости от степени выделяют малую, среднюю, субтотальную и тотальную степень кровотечения.
- При малой степени кровотечения объем кровопотери составляет не более 500 мл, на рентгеновском снимке отмечается скопление экссудата в синусе.
- Средняя степень характеризуется потерей крови в пределах от 500 до 1500 мл. На рентгенограмме уровень крови определяется на уровне 4 межреберья.
- При субтотальной степени кровопотеря достигает 2000 мл, уровень жидкости на рентгенограмме поднимается до нижнего края второго ребра.
- Тотальная степень характеризуется массивной кровопотерей более двух литров. На рентгеновском снимке наблюдается полное затемнение пораженной стороны.
По течению гемоторакс делится на свернувшийся, спонтанный, пневмогемоторакс, травматический гемоторакс
- Свернувшийся гемоторакс характеризуется наличием сгустков крови в плевральной полости, которые образуются после проводимого ранее коагуляционного лечения. Чаще всего возникает после хирургических вмешательств.
- При произвольном кровотечении в плевральную полость образуется спонтанный гемоторакс.
 Такой вид заболевания встречается крайне редко.
Такой вид заболевания встречается крайне редко.
- Пневмогемоторакс характеризуется смешанностью своего происхождения. При этой патологии в плевральной полости одновременно находится воздух и кровь. Наиболее частой причиной становится прорвавшаяся туберкулезная булла.
- У больного с травматическим гемотораксом будет присутствовать в анамнезе травма или проникающее ранение грудной клетки. Немаловажным фактором повреждения плевры будет разрыв стенки поврежденными ребрами.
По стороне поражения делится на левосторонний и правосторонний гемоторакс.
Если очаг поражения находится в левой доле легкого, то принято называть левосторонним гемотораксом. При поражении правой доли легкого, соответственно, правосторонний гемоторакс. Стоит отметить, что при правостороннем гемотораксе риск возникновения тяжелых последствий для пациента выше, чем при левостороннем поражении. Это происходит из-за быстрого нарастания дыхательной недостаточности. При двухстороннем гемотораксе поражаются обе доли легких. Это состояние является неотложным. Принятие мер должно быть произведено в течение одной минуты.
Это состояние является неотложным. Принятие мер должно быть произведено в течение одной минуты.
К развитию заболевания в первые часы может присоединяться инфекционный агент. Гемоторакс разделяют на инфицированный и неинфицированный.
В динамике подразделяют на стабильное и нарастающее течение.
Симптомы
При невыраженном течении заболевание может протекать бессимптомно. Перкуторно наблюдается укорочение получаемого звука по задней подмышечной линии. Аускультативно — снижение экскурсии легких над нижними отделами легких.
При тяжелой степени гемоторакса проявляются симптомы, характерные для внутреннего кровотечения: нарастает тахикардия, виден цианоз кожного покрова, холодный пот, побледнение кожи, низкое артериальное давление. Пациент отмечает появление боли в боку, одышку.
При прогрессировании заболевания возникает дыхательная недостаточность. Перкуторно выслушивается тупое звучание преимущественно над нижними отделами легких. Аускультативно — ослабление легочного звука.
Аускультативно — ослабление легочного звука.
Диагностика
Определить наличие гемоторакса можно с помощью:
- рентгена;
- ультразвука;
- КТ;
- МРТ;
- бронхоскопического исследования, которое сопровождается биопсией;
- цитологического исследования мокроты;
- проведения торакоцентеза по пробам Петрова или Ривилуа-Грегуара.
Кроме того, эффективным методом диагностики является плевральная пункция, которая одновременно является лечебной процедурой. Для проведения этого исследования делается прокол в грудной стенке, который должен достать до плевры. Затем через это отверстие с помощью шприца и отсоса из плевральной полости удаляют экссудат (содержимое). Процедура из диагностической превращается в лечебную, ведь вся нежелательная жидкость, затрудняющая дыхание, удаляется. Также дополнительно через прокол можно промыть полость, ввести антибиотики и произвести дренирование.
Но самой точным диагностическим исследованием считается эндоскопическая процедура – торакоскопия.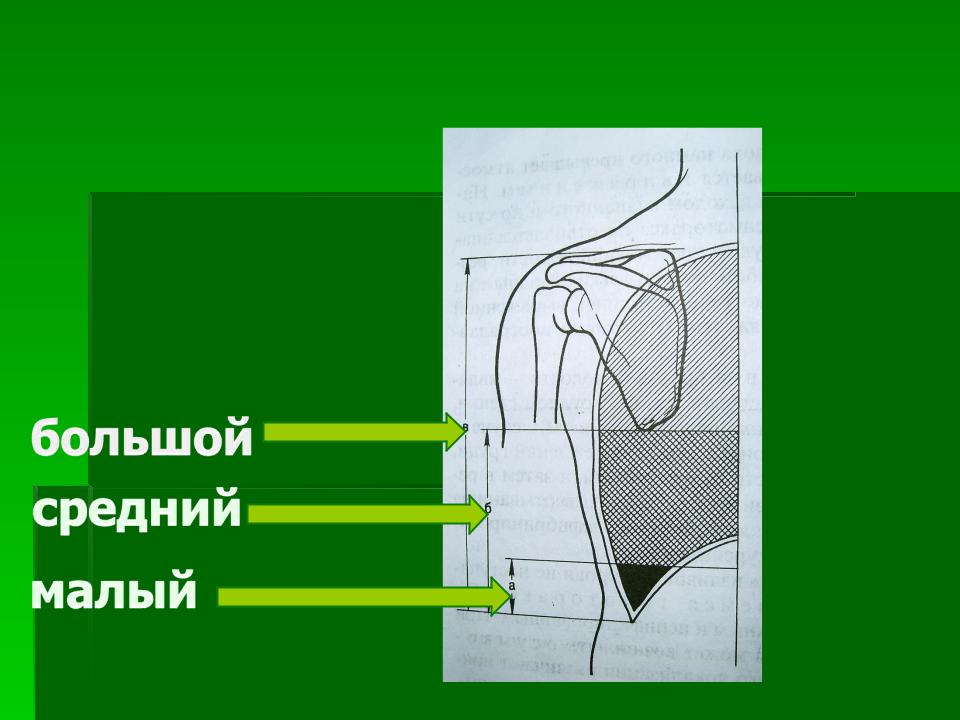 Этот метод дает возможность увидеть внутреннюю поверхность плевральной полости.
Этот метод дает возможность увидеть внутреннюю поверхность плевральной полости.
Лечение
При подозрении на возникновение гемоторакса больному необходимо сразу же вызвать скорую помощь. Ведь оказать квалифицированную помощь при этом поражении неспециалист не сможет. Врачи наложат тугую повязку и попытаются остановить кровотечение, а также смягчить последствия от падения уровня крови с помощью инфузионных растворов. Под контролем специалистов и постоянным наблюдением за гемодинамикой больного госпитализируют в торакальное хирургическое отделение.
Дальнейший ход лечения определит торакальный хирург или пульмонолог. Обычно для устранения возможных осложнений необходим прокол грудной клетки для исследования и устранения экссудата. При этом ставится дренаж (пассивный или активный), через который происходит введение необходимых лекарственных препаратов протеолитического и бактериального действия.
Терапия не обходится без кровезаменителей, дезагрегантов, иммунокорректоров, гемостатических и антибактериальных средств.
Если все перечисленные меры не приводят к улучшению состояния, необходимы хирургические манипуляции — видеоторакоскопия и открытая торакотомия.
Осложнения
У гемоторакса существует ряд осложнений, к которым относят следующие:
- Вследствие удаления крови из зоны плевральной полости возможен отек легких. Это осложнение встречается редко. На фоне с ним может развиться гиповолемия.
- В случае вторичного инфицирования сгустка крови может развиться эмпиема. Это случается в результате сочетанных ранений легких. Также возможно при повреждениях внешними источниками (любыми проникающими объектами, которые стали изначальной причиной травмы).
- Фиброторакс и сдавливание легких развивается в случае, когда в запекшейся массе крови происходит осаждение фибрина. Это может стать причиной постоянного ателектаза и понижения легочной функции. Для уменьшения рисков возникновения эпидемии, а также исправления ситуации с расширенными легкими проводится процедура декортикации.

Также при гемотораксе диагностируются:
Профилактика
Основой профилактики в данном случае является предупреждение получение травмы. Если имели место травмы живота или области груди, необходимо пройти консультацию торакального хирурга. Если пришлось прибегнуть к оперативному вмешательству, пациент нуждается в дальнейшем постоянном контроле состояния.
Прогноз
Прогноз гемоторакса зависит от нескольких факторов, таких как:
- сложность поражения грудной клетки и ближайших органов пострадавшего;
- объемы кровопотери;
- правильность и своевременность действий при оказании первой неотложной помощи.
К тому же на результативность лечения непосредственно влияет сам характер повреждений, в частности то, задело кровоизлияние одну сторону или две.
Более оптимистичный прогноз при малой или средней степени патологии. Если же речь идет о свернувшейся форме, вероятность возникновения эмпиемы возрастает. Самый пессимистический вариант ожидает пациентов с последствиями гемоторакса, которые сопровождаются длительным или одномоментно сильным кровотечением. Здесь речь может идти и о летальном исходе. Самый сложный для прогнозирования случай, когда последствия гемоторакса сопровождаются большим и длительным кровотечением. Здесь велика вероятность летального исхода.
Самый пессимистический вариант ожидает пациентов с последствиями гемоторакса, которые сопровождаются длительным или одномоментно сильным кровотечением. Здесь речь может идти и о летальном исходе. Самый сложный для прогнозирования случай, когда последствия гемоторакса сопровождаются большим и длительным кровотечением. Здесь велика вероятность летального исхода.
Для благоприятного прогноза человеку с гемотораксом достаточно получить своевременную и грамотную помощь, а также соответствующее лечение. В период реабилитации специалисты советуют заниматься спортом: плаваньем, дыхательными упражнениями, спортивной ходьбой. Особенно важны упражнения для легких, ведь они предупреждают появление спаек в плевре, что очень важно для функционирования диафрагмального купола.
Нашли ошибку? Выделите ее и нажмите Ctrl + Enter
Полезная статья Все о целиакии
Целиакия – это врожденное заболевание иммунозависимого характера, которое характеризуется повреждением слизистой тонкого кишечника, что приводит к недостаточному расщеплению глютена. Происходит…
Происходит…
Гемоторакс — это… Что такое Гемоторакс?
скопление крови в плевральной полости.
Наиболее частыми причинами Г. являются закрытые травмы и проникающие ранения груди, при которых кровотечение в плевральную полость происходит из поврежденных межреберных сосудов и сосудов легкого. Г. может быть также осложнением плевральной пункции и любой операции на органах грудной полости. В редких случаях его причинами могут быть разрыв аневризмы крупного внутригрудного сосуда, злокачественная опухоль легкого, плевры, средостения или грудной стенки, нарушение свертываемости крови. В зависимости от количества крови, определяемого в вертикальном положении больного по данным перкуссии и прямой рентгенографии груди, различают следующие объемы Г.: малый (кровь только в плевральных синусах), средний (верхняя граница скопления крови на уровне угла лопатки) и большой, или тотальный (кровь занимает почти всю плевральную полость). Ограниченный Г. образуется при скоплении крови в изолированных сращениями плевральных листков отделах плевральной полости. В случае свертывания крови в плевральной полости Г. называют свернувшимся. При одновременном скоплении в плевральной полости воздуха (см. Пневмоторакс) и крови возникает гемопневмоторакс.
Клиническая картина зависит от объема излившейся в плевральную полость крови и определяется главным образом величиной кровопотери, степенью сдавления и смещения внутригрудных органов, отсутствием или наличием инфекции. При малом гемотораксе клинических проявлений может не быть, а диагноз основывается только на данных рентгенологического исследования. В случае большого гемоторакса отмечают вынужденное сидячее или полусидячее положение больного, одышку, кашель, боли в груди, бледность, цианоз, тахикардию, низкое АД. У больных со средним гемотораксом эти симптомы менее выражены. При физикальном исследовании грудная стенка на стороне среднего и особенно большого Г. отстает при дыхании, перкуторный звук над областью скопления крови притуплен или тупой, голосовое дрожание ослаблено, дыхательные шумы не выслушиваются.
Ограниченный Г. образуется при скоплении крови в изолированных сращениями плевральных листков отделах плевральной полости. В случае свертывания крови в плевральной полости Г. называют свернувшимся. При одновременном скоплении в плевральной полости воздуха (см. Пневмоторакс) и крови возникает гемопневмоторакс.
Клиническая картина зависит от объема излившейся в плевральную полость крови и определяется главным образом величиной кровопотери, степенью сдавления и смещения внутригрудных органов, отсутствием или наличием инфекции. При малом гемотораксе клинических проявлений может не быть, а диагноз основывается только на данных рентгенологического исследования. В случае большого гемоторакса отмечают вынужденное сидячее или полусидячее положение больного, одышку, кашель, боли в груди, бледность, цианоз, тахикардию, низкое АД. У больных со средним гемотораксом эти симптомы менее выражены. При физикальном исследовании грудная стенка на стороне среднего и особенно большого Г. отстает при дыхании, перкуторный звук над областью скопления крови притуплен или тупой, голосовое дрожание ослаблено, дыхательные шумы не выслушиваются.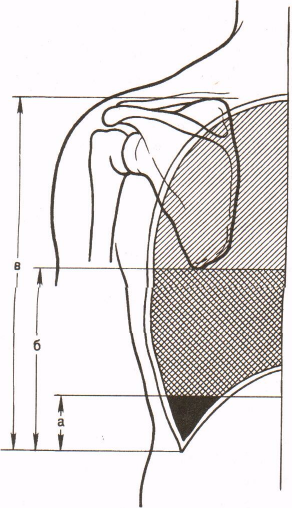 При гемопневмотораксе над областью притупления перкуторного звука определяется тимпанит.
Для уточнения диагноза используют рентгенографию грудной клетки, позволяющую выявить скопление жидкости в плевральной полости, ее количество, локализацию, уточнить место плевральной пункции. Рентгенографию необходимо проводить при вертикальном положении больного, т.к. в горизонтальном положении малый Г. ввиду растекания крови по задней грудной стенке часто не распознается. Компьютерная Томография позволяет выявить небольшое количество крови в плевральной полости и точно определить ее расположение. По специальным показаниям (например, при неясной причине гемоторакса) может быть применена диагностическая торакоскопия (см. Плевра). Во время плевральной пункции (Плевральная пункция) при Г. получают кровь; свертывание отсасываемой крови, как правило, свидетельствует о продолжающемся внутриплевральном кровотечении. Пробы получаемой при плевральной пункции крови направляют в клиническую лабораторию для определения содержания в ней гемоглобина и в бактериологическую лабораторию для бактериологического исследования.
При гемопневмотораксе над областью притупления перкуторного звука определяется тимпанит.
Для уточнения диагноза используют рентгенографию грудной клетки, позволяющую выявить скопление жидкости в плевральной полости, ее количество, локализацию, уточнить место плевральной пункции. Рентгенографию необходимо проводить при вертикальном положении больного, т.к. в горизонтальном положении малый Г. ввиду растекания крови по задней грудной стенке часто не распознается. Компьютерная Томография позволяет выявить небольшое количество крови в плевральной полости и точно определить ее расположение. По специальным показаниям (например, при неясной причине гемоторакса) может быть применена диагностическая торакоскопия (см. Плевра). Во время плевральной пункции (Плевральная пункция) при Г. получают кровь; свертывание отсасываемой крови, как правило, свидетельствует о продолжающемся внутриплевральном кровотечении. Пробы получаемой при плевральной пункции крови направляют в клиническую лабораторию для определения содержания в ней гемоглобина и в бактериологическую лабораторию для бактериологического исследования.
При малом гемотораксе и удовлетворительном состоянии больного может проводиться амбулаторное наблюдение. Небольшие количества крови в плевральной полости обычно бесследно рассасываются без лечения в течение 2—4 нед. Больные со средним и большим гемотораксом подлежат срочной госпитализации в хирургическое или травматологическое отделение. Транспортировка в полусидячем положении.
Основным методом лечения среднего и большого гемоторакса является плевральная пункция с аспирацией крови. Во время пункции следует стремиться удалить из плевральной полости всю излившуюся кровь и не допустить попадания в плевральную полость воздуха. В случае подозрения на продолжающееся внутриплевральное кровотечение показана торакоскопия или торакотомия (вскрытие плевральной полости через грудную стенку), которые позволяют визуально определить источник кровотечения и провести мероприятия, направленные на его остановку. Больным с относительно свежим свернувшимся Г. показано введение в плевральную полость ферментных препаратов, растворяющих сгустки (стрептазы, стрептодеказы, урокиназы). После растворения сгустков крови эффективны плевральные пункции. При инфицированном Г. аспирацию крови во время плевральной пункции сочетают с интенсивным промыванием плевральной полости и введением в нее антисептиков и антибиотиков. Недостаточная эффективность лечебных пункций является основанием для дренирования (Дренирование) плевральной полости с постоянной аспирацией ее содержимого. Проводятся также мероприятия по лечению заболеваний, вызвавших гемоторакс.
У больных, перенесших даже малый Г., в последующем могут образоваться плевральные сращения, ограничивающие подвижность соответствующего купола диафрагмы. Поэтому в стадии реабилитации большое значение имеют дыхательная гимнастика, плавание. Они способствуют восстановлению подвижности грудной стенки, диафрагмы и улучшению дыхательной функции.
Библиогр.: Вагнер Е.А. Хирургия повреждений груди, М., 1981.
После растворения сгустков крови эффективны плевральные пункции. При инфицированном Г. аспирацию крови во время плевральной пункции сочетают с интенсивным промыванием плевральной полости и введением в нее антисептиков и антибиотиков. Недостаточная эффективность лечебных пункций является основанием для дренирования (Дренирование) плевральной полости с постоянной аспирацией ее содержимого. Проводятся также мероприятия по лечению заболеваний, вызвавших гемоторакс.
У больных, перенесших даже малый Г., в последующем могут образоваться плевральные сращения, ограничивающие подвижность соответствующего купола диафрагмы. Поэтому в стадии реабилитации большое значение имеют дыхательная гимнастика, плавание. Они способствуют восстановлению подвижности грудной стенки, диафрагмы и улучшению дыхательной функции.
Библиогр.: Вагнер Е.А. Хирургия повреждений груди, М., 1981.скопление крови в плевральной полости.
Гемото́ракс большо́й (h. magnus) — см. Гемоторакс тотальный.
Гемото́ракс верху́шечный (h. apicalis) — ограниченный Г. в области верхушки легкого.
Гемото́ракс ма́лый (h. minor) — Г., при котором уровень крови в плевральной полости не достигает угла лопатки.
Гемото́ракс междолево́й (h. interlobaris) — ограниченный Г. в междолевых щелях.
Гемото́ракс наддиафрагма́льный (h. supradiaphragmaticus) — ограниченный Г. в участке плевральной полости, прилежащей к диафрагме.
Гемото́ракс ограни́ченный (h. circumscriptus; син. Г. осумкованный) — Г., занимающий небольшой участок плевральной полости, отграниченный спайками.
Гемото́ракс осумко́ванный (h. sacculatus) — см. Гемоторакс ограниченный.
Гемото́ракс паракоста́льный (h. paracostalis) — ограниченный Г. в участке плевральной полости, прилежащем к ребрам.
Гемото́ракс парамедиастина́льный (h. paramediastinalis; греч. para около + анат. mediastinum средостение) — ограниченный Г. в участке плевральной полости, прилежащем к средостению.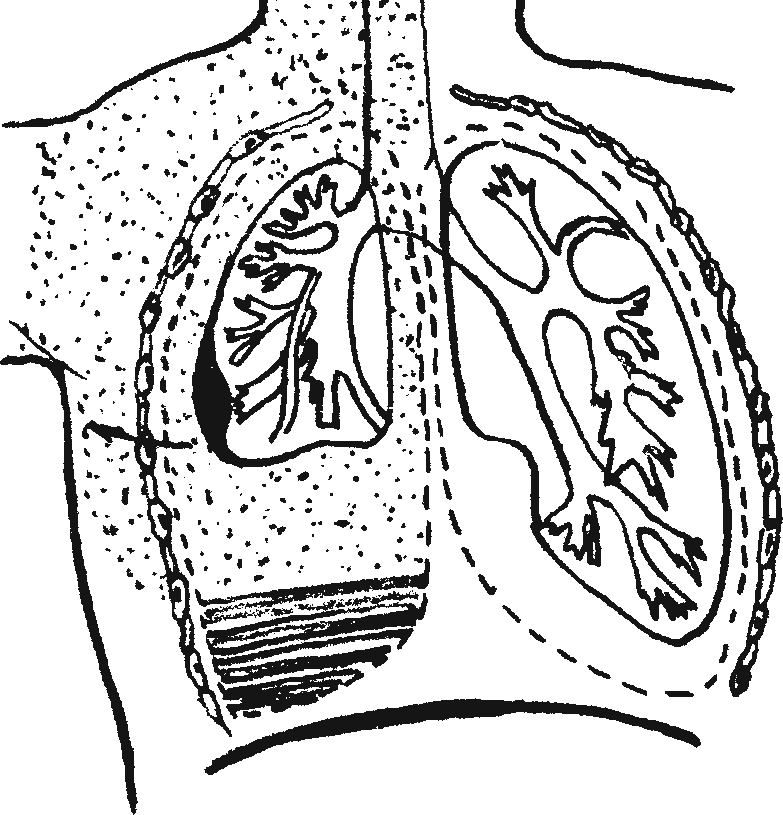
Гемото́ракс сверну́вшийся (h. concretus) — Г., при котором излившаяся кровь. подверглась свертыванию.
Гемото́ракс сре́дний (h. medius) — Г., при котором уровень крови в плевральной. полости достигает угла лопатки.
Гемото́ракс тота́льный (h. totalis; син. Г. большой) — Г., при котором кровь заполняет всю или почти всю плевральную полость.
Характер и степень повреждения здоровья | Размер страховой выплаты (процентов) |
I. Кости черепа. Нервная система | |
1. Перелом костей черепа: |
|
а) перелом наружной пластинки свода, костей лицевого черепа, травматическое расхождение шва | 5 |
б) перелом свода | 15 |
в) перелом основания | 20 |
г) перелом свода и основания | 25 |
2. Открытый перелом костей черепа и (или) оперативные вмешательства на головном мозге и его оболочках в связи с черепно-мозговой травмой — однократно (независимо от количества оперативных вмешательств) | 7 |
21. | 7 |
| (Дополнен — Постановление Правительства Российской Федерации от 21.02.2015 № 150) | |
3. Повреждение головного мозга: | |
а) сотрясение головного мозга при непрерывном лечении: | |
общей продолжительностью не менее 10 дней амбулаторного лечения в сочетании или без сочетания со стационарным лечением | 3 |
общей продолжительностью не менее 28 дней амбулаторного лечения в сочетании со стационарным лечением, длительность которого составила не менее 7 дней | 5 |
б) ушиб головного мозга (в том числе с субарахноидальным кровоизлиянием) при непрерывном лечении: | |
общей продолжительностью не менее 14 дней амбулаторного лечения в сочетании или без сочетания со стационарным лечением | 7 |
общей продолжительностью не менее 28 дней амбулаторного лечения в сочетании со стационарным лечением, длительность которого составила не менее 14 дней | 10 |
общей продолжительностью не менее 28 дней амбулаторного лечения в сочетании со стационарным лечением, длительность которого составила не менее 14 дней, при условии, что субарахноидальное кровоизлияние было подтверждено результатами анализа ликвора | 15 |
в) сдавление эпидуральной гематомой (гематомами) | 20 |
г) сдавление субдуральной, внутримозговой гематомой (гематомами) | 25 |
4. | |
а) сотрясение спинного мозга при непрерывном стационарном лечении общей продолжительностью не менее 7 дней и амбулаторном лечении общей продолжительностью не менее 28 дней | 5 |
б) ушиб спинного мозга, в том числе с субарахноидальным кровоизлиянием, при непрерывном лечении общей продолжительностью не менее 28 дней амбулаторного лечения в сочетании со стационарным лечением, длительность которого составила не менее 14 дней | 10 |
в) сдавление спинного мозга, гематомиелия и (или) частичный разрыв | 25 |
г) полный перерыв спинного мозга | 75 |
5. Повреждение позвоночника, повлекшее за собой оперативное вмешательство на позвоночнике (независимо от количества оперативных вмешательств) | 10 |
51. | 7 |
| (Дополнен — Постановление Правительства Российской Федерации от 21.02.2015 № 150) | |
6. Повреждение, разрыв нервов, нервных сплетений: | |
а) травматический неврит, частичный разрыв нервов, перерыв 2 и более пальцевых нервов, полный разрыв нервных стволов не предусмотренной здесь и далее локализации | 5 |
б) травматический плексит, полный перерыв основных нервных стволов1 на уровне лучезапястного, голеностопного суставов | 10 |
в) полный перерыв основных нервных стволов на уровне предплечья, голени | 20 |
г) частичный разрыв сплетения, полный перерыв основных нервных стволов нижней конечности выше уровня голени, верхней конечности выше уровня предплечья | 40 |
д) полный разрыв сплетения | 70 |
е) сотрясение, ушиб, сдавление спинномозговых нервов | 3 |
(Дополнен — Постановление Правительства Российской Федерации от 21. 02.2015 № 150) 02.2015 № 150) | |
II. Органы зрения | |
7. Повреждение 1 глаза: | |
а) непроникающее ранение, травматическая эрозия роговицы, ожоги II степени, гемофтальм, сквозное ранение века, разрыв или отрыв века, в том числе если указанные повреждения сопровождались конъюнктивитом, кератитом | 5 |
| (В редакции Постановления Правительства Российской Федерации от 21.02.2015 № 150) | |
б) проникающее ранение, контузия глазного яблока, сопровождавшаяся разрывом оболочек, ожог III (II — III) степени, ожог глазного яблока | 10 |
в) разрыв или отрыв глазодвигательного нерва | 10 |
| (Дополнен — Постановление Правительства Российской Федерации от 21.02.2015 № 150) | |
8. Последствия травмы 1 глаза, подтвержденные окулистом (офтальмологом) по истечении 3 месяцев после травмы2: | |
а) дефект радужной оболочки и (или) изменение формы зрачка, смещение, вывих хрусталика (за исключением протезированного), трихиаз (неправильный рост ресниц), неудаленные инородные тела, внедрившиеся в глазное яблоко и ткани глазницы, атрофия (субатрофия) поврежденного глазного яблока, отслоение сетчатки | 10 |
(В редакции Постановления Правительства Российской Федерации от 21. 02.2015 № 150) 02.2015 № 150) | |
б) снижение остроты зрения, в том числе в результате разрыва или отрыва зрительного нерва, без учета коррекции (в том числе искусственным хрусталиком) не менее чем в 2 раза | определяется согласно примечанию к настоящему приложению |
| (В редакции Постановления Правительства Российской Федерации от 21.02.2015 № 150) | |
9. Паралич аккомодации, гемианопсия 1 глаза | 15 |
10. Сужение поля зрения 1 глаза: | |
а) неконцентрическое | 10 |
б) концентрическое | 15 |
11. Пульсирующий экзофтальм 1 глаза | 10 |
12. Перелом орбиты 1 глаза | 10 |
13. Повреждение мышц глазного яблока 1 глаза, вызвавшее травматическое косоглазие, птоз, диплопию | 10 |
14. Последствия повреждения слезопроводящих путей 1 глаза, потребовавшие оперативного лечения | 5 |
III. Органы слуха Органы слуха | |
15. Повреждение ушной раковины, повлекшее за собой: | |
а) отсутствие до одной третьей части ушной раковины | 3 |
б) отсутствие одной третьей — одной второй части ушной раковины | 5 |
в) отсутствие более чем одной второй части ушной раковины | 10 |
16. Посттравматическое снижение слуха 1 уха, установленное аудиометрически по истечении 3 месяцев после травмы, не менее чем на 50 дБ на частотах 500 — 4000 Гц | 5 |
17. Разрыв 1 барабанной перепонки, наступивший в результате прямой травмы, независимо от ее вида | 5 |
IV. Дыхательная система | |
18. Перелом костей носа, передней стенки лобной, гайморовой пазух, решетчатой кости: | |
а) если не проводилось лечение с применением специальных методов (фиксация, операция) | 5 |
б) при лечении с применением специальных методов (фиксация, операция) | 10 |
19. | |
а) гемоторакс, пневмоторакс, подкожная эмфизема с одной стороны | 7 |
б) удаление части легкого | 40 |
в) полное удаление легкого | 60 |
20. Ранение грудной клетки, проникающее в плевральную полость, полость перикарда или клетчатку средостения, в том числе без повреждения внутренних органов | 5 |
201. Травматическая асфиксия | 7 |
| (Дополнен — Постановление Правительства Российской Федерации от 21.02.2015 № 150) | |
21. Перелом: | |
а) грудины | 7 |
б) хрящевой части ребер | 2 |
в) 1 — 2 ребер костного отдела (в том числе в сочетании с хрящом) | 4 |
г) 3-го и каждого последующего ребра костного отдела (в том числе в сочетании с хрящом) | 2 |
22. | |
а) в случае отсутствия повреждения внутренних органов | 5 |
б) при повреждении внутренних органов | 10 |
23. Повреждение дыхательных путей, переломы хрящей, ранение гортани, ранение трахеи, перелом подъязычной кости, ожог верхних дыхательных путей, а также повреждения щитовидной и вилочковой желез: | |
а) не потребовавшие оперативного лечения | 4 |
б) потребовавшие трахеостомии после травмы и до истечения 3 месяцев после нее | 7 |
в) потребовавшие оперативного лечения и (или) наличия трахеостомы в течение 3 месяцев и более | 10 |
V. Сердечно-сосудистая система | |
24. Повреждение подключичной, подкрыльцовой (подмышечной), плечевой, локтевой, лучевой, подвздошной, бедренной, подколенной, передней и задней большеберцовых артерий, плечеголовной, подключичной, подкрыльцовой (подмышечной), бедренной, подколенной вены с одной стороны3: | |
а) не повлекшее за собой впоследствии сосудистой недостаточности: | |
на уровне предплечья, голени | 5 |
выше уровня предплечья и голени | 10 |
б) повлекшее за собой по истечении 3 месяцев сосудистую недостаточность | 25 |
25. | |
а) не повлекшее за собой впоследствии сердечно-сосудистой, сосудистой недостаточности | 15 |
б) повлекшее за собой по истечении 3 месяцев сердечно-сосудистую, сосудистую недостаточность | 30 |
VI. Органы пищеварения | |
26. Перелом верхней челюсти, скуловой кости или нижней челюсти, вывих нижней челюсти, потеря челюсти: | |
а) изолированный перелом альвеолярного отростка челюсти (без потери зубов), отрыв костного фрагмента челюсти, травматический (от внешнего воздействия) вывих челюсти | 3 |
б) полный перелом 1 челюсти | 5 |
в) двойной перелом 1 челюсти, переломы 2 челюстей, переломы в сочетании с вывихом нижней челюсти | 10 |
г) потеря части челюсти, за исключением альвеолярного отростка | 30 |
д) потеря челюсти | 50 |
27. | |
а) 2 — 3 зубов | 5 |
б) 4 — 6 зубов | 10 |
в) 7 — 9 зубов | 15 |
г) 10 и более зубов | 20 |
28. Потеря языка: | |
а) более 1 см, менее одной третьей | 5 |
б) одной третьей и более | 20 |
29. Травматическое повреждение пищевода, желудка, кишечника, поджелудочной железы, печени, желчного пузыря, селезенки5: | |
а) повреждение 1 или 2 органов, потребовавшее стационарного и амбулаторного непрерывного лечения в течение не менее 14 дней | 5 |
б) повреждение 3 и более органов | 10 |
в) повреждение, вызвавшее по истечении 3 месяцев рубцовое сужение (стриктуру), деформацию желудка, кишечника, заднепроходного отверстия, печеночную недостаточность | 20 |
г) повреждение, вызвавшее по истечении 3 месяцев спаечную болезнь, в том числе оперированную | 25 |
д) повреждение, вызвавшее по истечении 3 месяцев кишечный свищ, кишечно-влагалищный свищ, свищ поджелудочной железы | 40 |
е) повреждение, повлекшее за собой потерю желчного пузыря, части печени, до двух третьих желудка, до двух третьих кишечника |
Спецборт МЧС с пострадавшими при стрельбе в Перми прибыл в Москву — РБК
Сотрудники МЧС транспортируют пострадавших во время стрельбы в Пермском государственном национальном исследовательском университете, доставленных спецбортом МЧС в Москву (Фото: РИА Новости)
Самолет МЧС Ил-76, который забрал пострадавших при стрельбе в Пермском государственном национальном исследовательском университете (ПГНИУ) из Перми, совершил посадку в московском аэропорту Внуково. Об этом сообщили в пресс-службе МЧС в Telegram.
Об этом сообщили в пресс-службе МЧС в Telegram.
Всего, по данным спасателей, в Москву перевезли семь человек. В Минздраве ранее говорили, что все они находятся в тяжелом состоянии.
Как сообщил источник РБК, близкий к МВД, по меньшей мере четверых из них отправили в Центр хирургии им. Вишневского. У одного из этих пациентов — девушки 2000 года рождения, — по данным собеседника РБК, огнестрельное ранение брюшной полости, сквозное ранение почки и доли печени, перелом костей таза, забрюшинная гематома и травматический шок второй степени.
У другого пациента — 1998 года рождения: огнестрельное ранение груди, ранение правого легкого, правого желудочка, большой гемоторакс (скопление крови в пространстве рядом с легкими), раны правой кисти и травматический шок четвертой степени.
Семерых пострадавших при стрельбе в пермском вузе перевезут в МосквуСтраница статьи : Детская хирургия
DOI:
Аннотация
Актуальность. Диагностика закрытых повреждений диафрагмы нередко вызывает трудности. Во всех наблюдениях сочетанной травмы разрыв диафрагмы встречается от 0,5 до 5%. Соотношение травматического разрыва диафрагмы слева и справа составляет 84 и 16% соответственно.
Цель. Пример редкого случая изолированного травматического разрыва правого купола диафрагмы.
Пациенты. Девочка 4 лет, травма в результате ДТП, находилась в детском удерживающем устройстве. При поступлении состояние тяжелое, обусловлено дыхательной недостаточностью, травматическим шоком 1-й степени. Одышка до 36 в мин, аускультативно резкое ослабление дыхания справа, сатурация кислорода 90%. Живот умеренно вздут, напряжен, болезненный во всех отделах, положительная перитонеальная симптоматика. В общем анализе крови эритроциты 3,6 Т/л, гемоглобин 100 г/л, лейкоциты 22,9 г/л. По данным рентгенограммы грудной и брюшной полости нельзя исключить гемоторакс и разрыв диафрагмы с дислокацией правой доли печени в правую грудную полость, в связи с этим от выполнения плевральной пункции решено воздержаться.
Диагностика закрытых повреждений диафрагмы нередко вызывает трудности. Во всех наблюдениях сочетанной травмы разрыв диафрагмы встречается от 0,5 до 5%. Соотношение травматического разрыва диафрагмы слева и справа составляет 84 и 16% соответственно.
Цель. Пример редкого случая изолированного травматического разрыва правого купола диафрагмы.
Пациенты. Девочка 4 лет, травма в результате ДТП, находилась в детском удерживающем устройстве. При поступлении состояние тяжелое, обусловлено дыхательной недостаточностью, травматическим шоком 1-й степени. Одышка до 36 в мин, аускультативно резкое ослабление дыхания справа, сатурация кислорода 90%. Живот умеренно вздут, напряжен, болезненный во всех отделах, положительная перитонеальная симптоматика. В общем анализе крови эритроциты 3,6 Т/л, гемоглобин 100 г/л, лейкоциты 22,9 г/л. По данным рентгенограммы грудной и брюшной полости нельзя исключить гемоторакс и разрыв диафрагмы с дислокацией правой доли печени в правую грудную полость, в связи с этим от выполнения плевральной пункции решено воздержаться.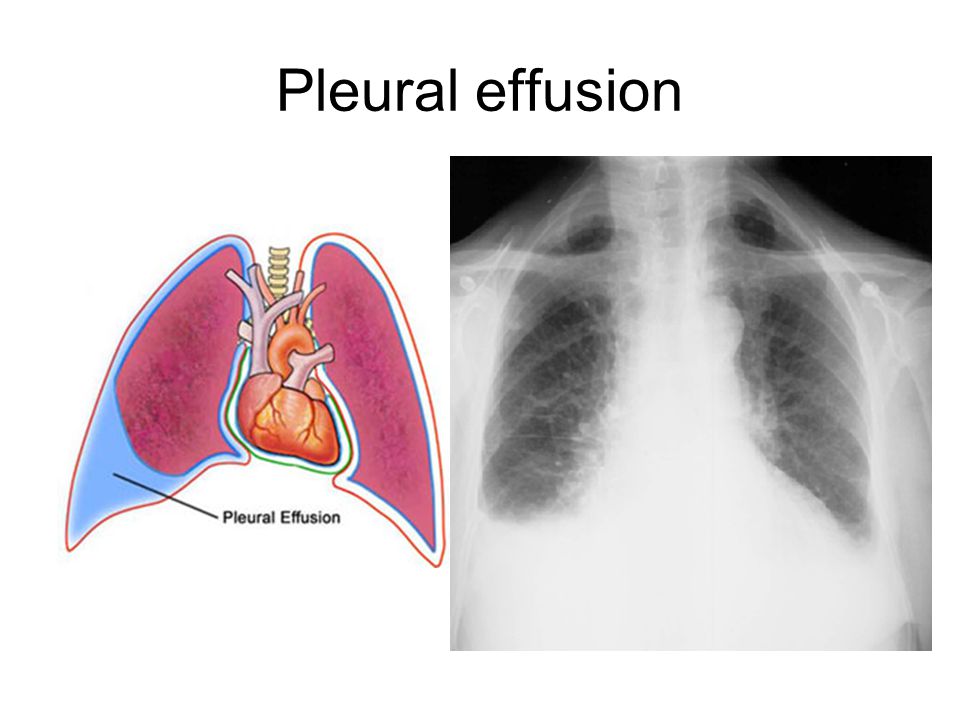 Учитывая клиническую картину, выполнена срединная лапаротомия с продлением разреза в правое подреберье под интубационным наркозом. Выявлен разрыв правого купола диафрагмы 10 × 5 см, звездчатой формы. Правая доля печени находилась в грудной полости. Также выявлен разрыв печени на диафрагмальной поверхности 1 см, гематома брыжейки тонкой кишки. Выполнено: мобилизация печени, перевод в брюшную полость, ушивание диафрагмы П-образным швом, рана печени тампонирована тахокомбом, дренаж в правую плевральную полость по Бюлау, дренаж в брюшную полость. Экстубирована на 5-е сутки. Послеоперационное течение гладкое, ребенок выписан на 13-е сутки с выздоровлением.
Результаты. Рентгенологическая картина позволила заподозрить торакоабдоминальное повреждение с дислокацией печени в грудную полость и отказаться от плевральной пункции.
Заключение. Диагностика закрытых повреждений диафрагмы нередко вызывает трудности, которые обусловлены отсутствием специфических симптомов повреждения.
Учитывая клиническую картину, выполнена срединная лапаротомия с продлением разреза в правое подреберье под интубационным наркозом. Выявлен разрыв правого купола диафрагмы 10 × 5 см, звездчатой формы. Правая доля печени находилась в грудной полости. Также выявлен разрыв печени на диафрагмальной поверхности 1 см, гематома брыжейки тонкой кишки. Выполнено: мобилизация печени, перевод в брюшную полость, ушивание диафрагмы П-образным швом, рана печени тампонирована тахокомбом, дренаж в правую плевральную полость по Бюлау, дренаж в брюшную полость. Экстубирована на 5-е сутки. Послеоперационное течение гладкое, ребенок выписан на 13-е сутки с выздоровлением.
Результаты. Рентгенологическая картина позволила заподозрить торакоабдоминальное повреждение с дислокацией печени в грудную полость и отказаться от плевральной пункции.
Заключение. Диагностика закрытых повреждений диафрагмы нередко вызывает трудности, которые обусловлены отсутствием специфических симптомов повреждения.
Об авторах
Дементьев А.П.ОБУЗ «Областная детская клиническая больница» г. Иваново
Костерина А.М.
ОБУЗ «Областная детская клиническая больница» г. Иваново
Сафронов Б.Г.
ГБОУ ВПО «Ивановская государственная медицинская академия» Минздрава России 153012, Иваново
Сухарев С.Г.
ОБУЗ «Областная детская клиническая больница» г. Иваново
Список литературы
Дополнительные файлы
Для цитирования:
For citation:
Обратные ссылки
- Обратные ссылки не определены
Контент доступен под лицензией Creative Commons Attribution 3. 0 License.
0 License.
ISSN: (Print)
ISSN: (Online)
Клиническая картина гемоторакса: анамнез, физикальное обследование
Май Дж., Адес А. Синдром пористой диафрагмы: гемоторакс, вторичный по отношению к гемоперитонеуму после лапароскопической гистерэктомии. BMJ Case Rep . 2013 5 декабря 2013: [Medline].
Tatebe S, Kanazawa H, Yamazaki Y, Aoki E, Sakurai Y. Спонтанный гемопневмоторакс. Энн Торак Хирург . 1996 Октябрь 62 (4): 1011-5. [Медлайн].
Насон К.С., Ганим РБ, Лукетич Ю.Д.Стенка грудной клетки, легкое, средостение и плевра. Бруникарди ФК, Андерсен Д.К., Биллиар Т.Р., Данн Д.Л., Хантер Дж.Г., Као Л.С. и др., Ред. Принципы хирургии Шварца . 11-е изд. Нью-Йорк: Макгроу-Хилл; 2019. Vol 1: 661-750.
com»> Di Crescenzo V, Laperuta P, Napolitano F, Carlomagno C, Garzi A, Vitale M. Легочная секвестрация представлена массивным левым гемотораксом и связана с первичной саркомой легкого. BMC Surg . 2013 8 октября. 13 Прил. 2: S34. [Медлайн].[Полный текст].
Broderick SR. Гемоторакс: этиология, диагностика и лечение. Клиника торакальной хирургии . 2013 февраля 23 (1): 89-96, vi-vii. [Медлайн].
Johnson EM, Saltzman DA, Suh G, Dahms RA, Leonard AS. Осложнения и риски установки центрального венозного катетера у детей. Хирургия . 1998 ноябрь 124 (5): 911-6. [Медлайн].
Waddington MS, Mullins GC. Раннее осложнение катетеризации центральной вены у детей. Педиатр Анаест . 2005 15 ноября (11): 1001-5. [Медлайн].
Лешер А. П., Кратц Дж. М., Смит CD. Удаление встроенных центральных венозных катетеров. J Педиатр Хирург . 2008 июн. 43 (6): 1030-4. [Медлайн].
П., Кратц Дж. М., Смит CD. Удаление встроенных центральных венозных катетеров. J Педиатр Хирург . 2008 июн. 43 (6): 1030-4. [Медлайн].
Ota H, Kawai H, Matsuo T. Минииторакотомия с видео-ассистированием по поводу тупого разрыва диафрагмы, проявляющегося в виде отсроченного гемоторакса. Ann Thorac Cardiovasc Surg . 2014. 20 Suppl: 911-4. [Медлайн].
Накаяма Д.К., Раменовски М.Л., Роу М.И.Травмы грудной клетки в детстве. Энн Сург . 1989 декабрь 210 (6): 770-5. [Медлайн]. [Полный текст].
Sharma OP, Hagler S, Oswanski MF. Преобладание отсроченного гемоторакса при тупой травме грудной клетки. Am Surg . 2005 июн. 71 (6): 481-6. [Медлайн].
Коттин В., Шине Т., Лаволе А., Корре Р., Маршан Э., Рейно-Гобер М. и др. Легочные артериовенозные мальформации при наследственной геморрагической телеангиэктазии: серия 126 пациентов. Медицина (Балтимор) . 2007 январь 86 (1): 1-17. [Медлайн].
Легочные артериовенозные мальформации при наследственной геморрагической телеангиэктазии: серия 126 пациентов. Медицина (Балтимор) . 2007 январь 86 (1): 1-17. [Медлайн].
Руссе П., Руссе-Яблонски С, Алифано М, Мансуэт-Лупо А, Бай Дж. Н., Ревель МП. Синдром торакального эндометриоза: особенности КТ и МРТ. Клин Радиол . 2014 Март 69 (3): 323-30. [Медлайн].
Синния Д., Нагалингам I. Гемоторакс у новорожденного. Clin Pediatr (Phila) . 1972 г., 11 (2): 84-5. [Медлайн].
Huybrechts S, Wojciechowski M, Poot S, Van Reempts P, Ramet J.Гемоторакс как проявление позднего кровотечения с дефицитом витамина К у месячного ребенка с гомозиготным дефицитом альфа-1-антитрипсина. Eur J Pediatr . 2007 Октябрь 166 (10): 1081-2. [Медлайн].
webmd.com»> Hammoudeh M, Qaddoumi NK. Плевральное кровотечение при пурпуре Шенлейна Геноха. Clin Rheumatol . 1993 12 (4): 538-9. [Медлайн].
Tantraworasin A, Saeteng S. Массивный гемоторакс из-за внутригрудного экстрамедуллярного кроветворения у пациента с болезнью гемоглобина E бета-талассемии. J Med Assoc Thai . 2013 июл.96 (7): 866-9. [Медлайн].
Laberge JM, Puligandla P, Flageole H. Бессимптомные врожденные пороки развития легких. Семин Педиатр Хирург . 2005 14 февраля (1): 16-33. [Медлайн].
Вазири М., Мехразма М. Массивный спонтанный гемоторакс, связанный с болезнью фон Реклингхаузена. Энн Торак Хирург . 2006 Октябрь 82 (4): 1500-1. [Медлайн].
Проппер Р.А., Янг Л.В., Вуд Б.П.Гемоторакс как осложнение реберных хрящевых экзостозов. Педиатр Радиол . 1980, апрель, 9 (3): 135-7. [Медлайн].
Педиатр Радиол . 1980, апрель, 9 (3): 135-7. [Медлайн].
Tomares SM, Jabra AA, Conrad CK, Beauchamp N, Phoon CK, Carroll JL. Гемоторакс у ребенка в результате реберного экзостоза. Педиатрия . 1994 Mar.93 (3): 523-5. [Медлайн].
Джин В., Хён С.И., Рю И., Лим И.С., Ким Дж. Реберная остеохондрома в виде гемоторакса и разрыва диафрагмы. Педиатр Радиол . 2005 июл.35 (7): 706-9. [Медлайн].
Cowles RA, Rowe DH, Arkovitz MS. Наследственные множественные экзостозы ребер: необычная причина гемоторакса и перикардиального выпота. J Педиатр Хирург . 2005 июл. 40 (7): 1197-200. [Медлайн].
Осава Х., Йошии С., Такахаши В., Хосака С., Исикава Н., Мизутани Е. и др. Геморрагический шок из-за внутригрудного разрыва остеосаркомы ребра.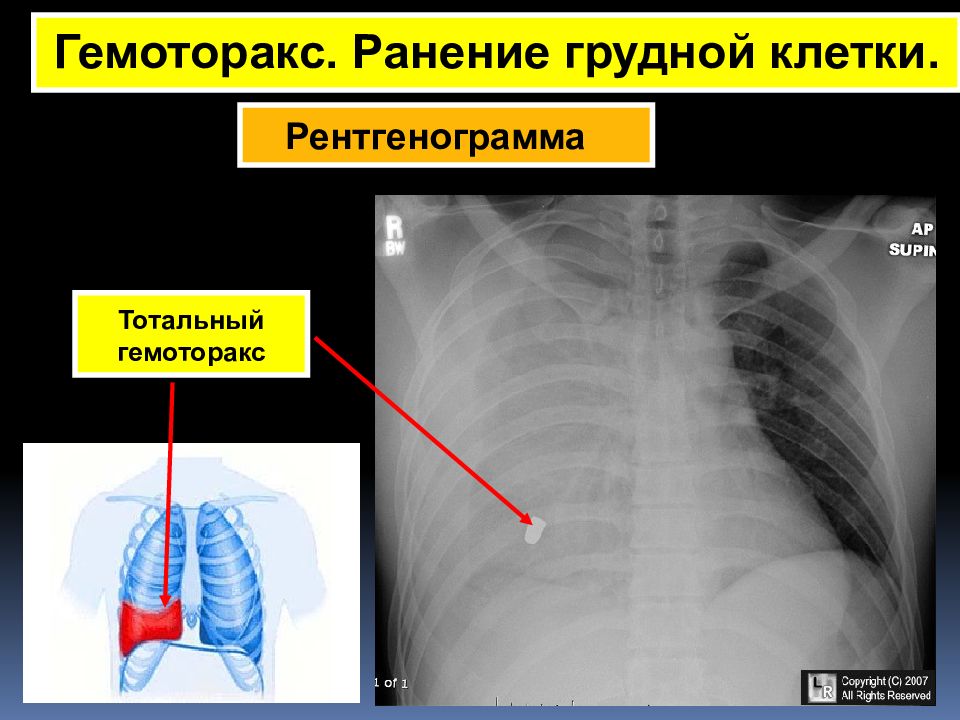 Ann Thorac Cardiovasc Surg .2001 7 августа (4): 232-4. [Медлайн].
Ann Thorac Cardiovasc Surg .2001 7 августа (4): 232-4. [Медлайн].
Ким Э.С., Кан Ч.Й., Пио Ч., Чон Э., Ли В.Б. 12-летний опыт спонтанного гемопневмоторакса. Ann Thorac Cardiovasc Surg . 14 июня 2008 г. (3): 149-53. [Медлайн].
Richardson JD, Miller FB, Carrillo EH, Испания DA. Сложные травмы грудной клетки. Surg Clin North Am . 1996 августа 76 (4): 725-48. [Медлайн].
Пеклет MH, Ньюман KD, Eichelberger MR, Gotschall CS, Garcia VF, Bowman LM.Травма грудной клетки у детей: показатель повышенной смертности. J Педиатр Хирург . 1990 сентября, 25 (9): 961-5; обсуждение 965-6. [Медлайн].
Inci I, Ozcelik C, Nizam O, Eren N, Ozgen G. Проникающие ранения грудной клетки у детей: обзор 94 случаев. J Педиатр Хирург . 1996 май. 31 (5): 673-6. [Медлайн].
1996 май. 31 (5): 673-6. [Медлайн].
Bohosiewicz J, Kudela G, Koszutski T. Результаты процедур Nuss для коррекции pectus excatum. Eur J Pediatr Surg .2005 15 февраля (1): 6-10. [Медлайн].
Иссайванан М., Баранвал П., Аброл С., Баджва Г., Балдауф М., Шукла М. Спонтанный гемопневмоторакс у детей: отчет о болезни и обзор литературы. Педиатрия . 2006 Октябрь 118 (4): e1268-70. [Медлайн].
Parry GW, Morgan WE, Salama FD. Лечение гемоторакса. Ann R Coll Surg Engl . 1996 июл.78 (4): 325-6. [Медлайн]. [Полный текст].
Миллер Л.А.Травма грудной стенки, легкого и плевральной полости. Radiol Clin North Am . 2006 Mar.44 (2): 213-24, viii. [Медлайн].
Мандавиа Д. П., Джозеф А. Прикроватная эхокардиография при травме грудной клетки. Emerg Med Clin North Am . 2004 22 августа (3): 601-19. [Медлайн].
П., Джозеф А. Прикроватная эхокардиография при травме грудной клетки. Emerg Med Clin North Am . 2004 22 августа (3): 601-19. [Медлайн].
Trupka A, Waydhas C, Hallfeldt KK, Nast-Kolb D, Pfeifer KJ, Schweiberer L. Значение компьютерной томографии грудной клетки в первой оценке тяжелораненых пациентов с тупой травмой грудной клетки: результаты проспективного исследования. J Травма . 1997 Sep, 43 (3): 405-11; обсуждение 411-2. [Медлайн].
Chardoli M, Hasan-Ghaliaee T., Akbari H, Rahimi-Movaghar V. Точность рентгенографии грудной клетки по сравнению с компьютерной томографией грудной клетки у гемодинамически стабильных пациентов с тупой травмой грудной клетки. Chin J Traumatol . 2013. 16 (6): 351-4. [Медлайн].
Мур Массачусетс, Уоллес ЕС, Вестра SJ. Визуализация травм грудной клетки у детей. Педиатр Радиол .2009 Май. 39 (5): 485-96. [Медлайн].
Педиатр Радиол .2009 Май. 39 (5): 485-96. [Медлайн].
Chang YT, Dai ZK, Kao EL, Chuang HY, Cheng YJ, Chou SH и др. Ранняя видеоассистированная торакальная хирургия при первичном спонтанном гемопневмотораксе. Мир J Surg . 2007 31 января (1): 19-25. [Медлайн].
Heniford BT, Carrillo EH, Spain DA, Sosa JL, Fulton RL, Richardson JD. Роль торакоскопии в лечении сохраненных грудных коллекций после травм. Энн Торак Хирург .1997 апр. 63 (4): 940-3. [Медлайн].
Лю Д.В., Лю Х.П., Линь П.Дж., Чанг СН. Видеоассистированная торакальная хирургия при лечении травм грудной клетки. J Травма . 1997 Апрель, 42 (4): 670-4. [Медлайн].
Mancini M, Smith LM, Nein A, Buechter KJ. Раннее удаление свернувшейся крови при гемотораксе с помощью торакоскопии: истории болезни. J Травма . 1993, январь, 34 (1): 144-7. [Медлайн].
J Травма . 1993, январь, 34 (1): 144-7. [Медлайн].
Мейер Д.М., Джессен М.Э., Уэйт М.А., Эстрера А.С.Ранняя эвакуация травматических сохраненных гемотораксов с помощью торакоскопии: проспективное рандомизированное исследование. Энн Торак Хирург . 1997 Nov.64 (5): 1396-400; обсуждение 1400-1. [Медлайн].
Navsaria PH, Vogel RJ, Nicol AJ. Торакоскопическая эвакуация оставшегося посттравматического гемоторакса. Энн Торак Хирург . 2004 июл. 78 (1): 282-5; обсуждение 285-6. [Медлайн].
Inci I, Ozçelik C, Ulkü R, Tuna A, Eren N. Внутриплевральное фибринолитическое лечение травматического свернувшегося гемоторакса. Сундук . 1998 июл. 114 (1): 160-5. [Медлайн].
[Рекомендации] Тканевый активатор плазминогена при травматическом гемотораксе.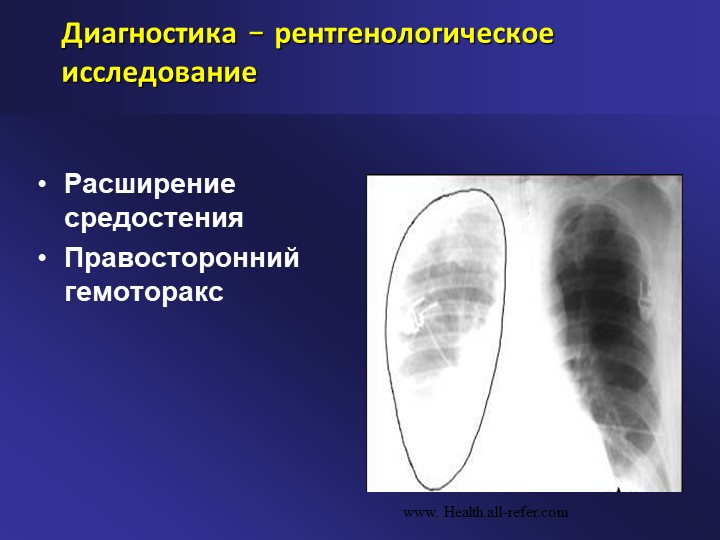 Отделение хирургического образования Регионального медицинского центра Орландо. Доступно на http://www.surgicalcriticalcare.net/Guidelines/tissue_plasminogen_activator.pdf. 4 марта 2008 г .; Дата обращения: 13 июля 2020 г.
Отделение хирургического образования Регионального медицинского центра Орландо. Доступно на http://www.surgicalcriticalcare.net/Guidelines/tissue_plasminogen_activator.pdf. 4 марта 2008 г .; Дата обращения: 13 июля 2020 г.
Chou YP, Kuo LC, Soo KM, Tarng YW, Chiang HI, Huang FD и др. Роль заживления разрывов легких во время эвакуации при торакоскопической хирургии с использованием видео при задержанном гемотораксе, вызванном тупой травмой грудной клетки. евро J Cardiothorac Surg . 2014 июл. 46 (1): 107-11. [Медлайн].
Ernstgård L, Sjögren B, Gunnare S, Johanson G. Кровь и выдыхаемый воздух можно использовать для биомониторинга воздействия гидрофторуглеродов. Toxicol Lett . 2014 10 февраля. 225 (1): 102-9. [Медлайн].
UF Health, University of Florida Health
Определение
Гемоторакс — это скопление крови в пространстве между грудной стенкой и легким (плевральная полость).
Причины
Наиболее частой причиной гемоторакса является травма грудной клетки. Гемоторакс также может возникнуть у людей, у которых:
- Дефект свертывания крови
- Грудная (грудная) или сердечная хирургия
- Смерть легочной ткани (инфаркт легкого)
- Рак легкого или плевры — первичный или вторичный (метастатический, или с другого сайта)
- Разрыв кровеносного сосуда при установке центрального венозного катетера или при сильном повышенном артериальном давлении
- Туберкулез
Симптомы
Симптомы включают:
Обследования и анализы
Ваш лечащий врач может отмечают снижение или отсутствие звуков дыхания на пораженной стороне.Признаки или находки гемоторакса можно увидеть в следующих тестах:
Лечение
Целью лечения является стабилизация состояния пациента, остановка кровотечения и удаление крови и воздуха из плевральной полости.
- Пневматическая трубка вводится через грудную стенку между ребрами для отвода крови и воздуха.

- Его оставляют на месте и прикрепляют к отсасыванию на несколько дней для повторного расширения легкого.
Если плевральная дренажная трубка сама по себе не контролирует кровотечение, для остановки кровотечения может потребоваться операция (торакотомия).
Также будет устранена причина гемоторакса. Основное легкое могло разрушиться. Это может привести к затруднению дыхания. Людям, получившим травму, может потребоваться дренаж плевральной трубки. Хирургия может не потребоваться.
ЧТО ОЖИДАТЬ В ОТДЕЛЕНИИ ЧРЕЗВЫЧАЙНОЙ СИТУАЦИИ
Поставщик будет измерять и контролировать жизненно важные функции человека, включая сатурацию кислорода, пульс, частоту дыхания и артериальное давление. Симптомы будут лечиться по мере необходимости. Человек может получить:
- Дыхательная поддержка — это может включать кислород, неинвазивную поддержку давлением в дыхательных путях, такую как BIPAP, или эндотрахеальную интубацию (введение дыхательной трубки через рот или нос в дыхательные пути) и размещение на аппарате ИВЛ.
 (дыхательный аппарат жизнеобеспечения)
(дыхательный аппарат жизнеобеспечения) - Анализы крови и возможное переливание крови
- Грудная трубка (трубка, проходящая через кожу и мышцы между ребрами в пространство вокруг легких) при коллапсе легкого
- КТ
- Анализ плевральной полости жидкость, Электрокардиограмма (ЭКГ)
- Жидкости, вводимые через вену (IV)
- Лекарства для лечения симптомов
- Рентген грудной клетки и живота или других частей тела при наличии дополнительных травм
Прогноз (прогноз)
Результат зависит от причины гемоторакса, объема кровопотери и того, как быстро будет назначено лечение.
В случае серьезной травмы исход дополнительно будет зависеть от тяжести травмы и скорости кровотечения.
Возможные осложнения
Осложнения могут включать:
- Коллапс легкого или пневмоторакс, приводящий к дыхательной недостаточности (неспособность правильно дышать)
- Фиброз или рубцевание плевральных оболочек и подлежащей ткани легкого
- Инфекция плевральной жидкости ( empyema)
- Шок и смерть в тяжелых обстоятельствах
Когда обращаться к медицинскому работнику
Позвоните 911 или по номеру местной службы экстренной помощи, если у вас есть:
- Любая потенциально серьезная травма груди
- Боль в груди
- Сильная челюсть , боль в шее, плече или руке
- Затрудненное дыхание или одышка
Обратитесь в отделение неотложной помощи или позвоните по местному номеру службы экстренной помощи (например, 911), если у вас есть:
- Головокружение, головокружение, жар и кашель, или ощущение тяжести в груди
Профилактика
Используйте меры безопасности (например, ремень безопасности ts), чтобы избежать травм. В зависимости от причины, гемоторакс невозможно предотвратить.
В зависимости от причины, гемоторакс невозможно предотвратить.
Изображения
Ссылки
Light RW, Lee YCG. Пневмоторакс, хилоторакс, гемоторакс и фиброторакс. В: Broaddus VC, Mason RJ, Ernst JD и др., Ред. Учебник респираторной медицины Мюррея и Наделя . 6-е изд. Филадельфия, Пенсильвания: Эльзевьер Сондерс; 2016: глава 81.
Raja AS. Травма грудной клетки. В: Walls RM, Hockberger RS, Gausche-Hill M, eds. Неотложная медицина Розена: концепции и клиническая практика .9 изд. Филадельфия, Пенсильвания: Эльзевьер; 2018: глава 38.
Семон Дж., Маккарти М. Грудная стенка, пневмоторакс и гемоторакс. В: Кэмерон А.М., Кэмерон Дж. Л., ред. Современная хирургическая терапия . 13-е изд. Филадельфия, Пенсильвания: Эльзевьер; 2020: 1146-1150.
Гемоторакс — Физиопедия
Термин гемоторакс можно определить как попадание плевральной жидкости и крови в плевральную полость. Для диагностики гемоторакса это должна быть плевральная жидкость с гематокритом от 25% до 50% крови пациента. [1]
[1]
Плевра состоит из двух слоев. Один из них покрывает поверхность легких (висцеральную плевру), а другой — внутреннюю часть грудной стенки (париетальная плевра). (Для получения более подробной информации об анатомии легких.) Эти слои плевры слипаются друг с другом, чтобы предотвратить коллапс легкого даже при выдохе воздуха из легкого. Если воздух или жидкость попадают в плевральную полость между этими слоями плевры, это вызывает коллапс легкого из-за его упругой отдачи. Если в плевральную полость попадает только воздух, возникает пневмоторакс.Если жидкость или кровь попадают в плевральную полость, это может вызвать плевральный выпот или гемоторакс. [2]
Основная причина гемоторакса — острая или тупая травма грудной клетки. Ятрогенный или спонтанный гемоторакс встречается реже. Ятрогенный гемоторакс, скорее всего, возникает как осложнение сердечно-легочной хирургии, установки подключичных или яремных катетеров или биопсии легкого и плевры.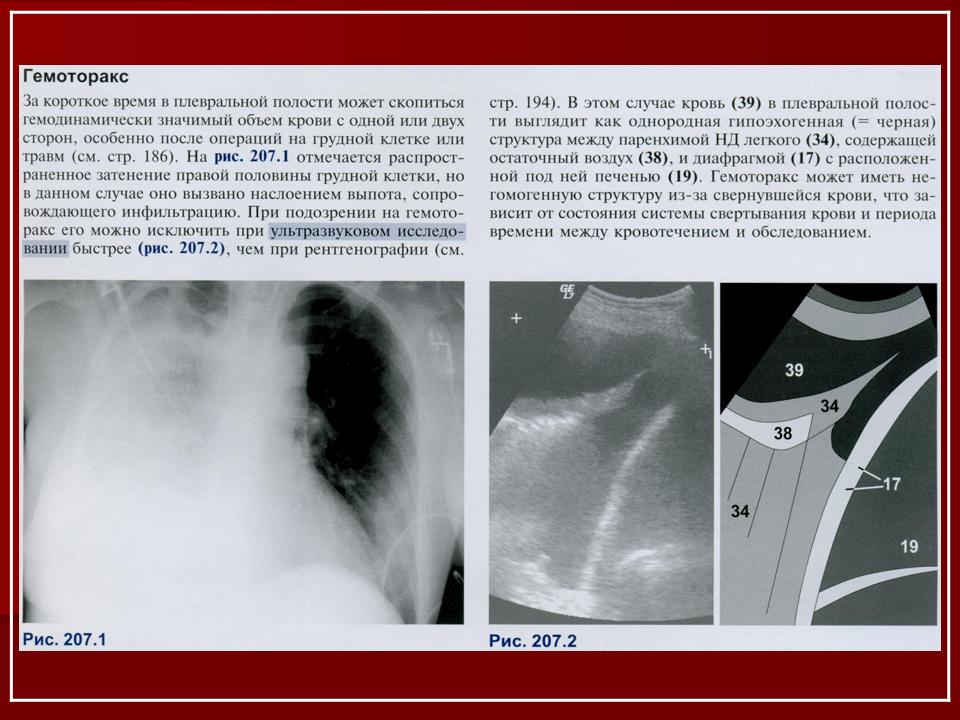 [1] [3] Спонтанный гемоторакс обычно вызывается разрывом спаек плевры, новообразованием, метастазами в плевре и является осложнением антикоагулянтной терапии при тромбоэмболии легочной артерии. [4]
[1] [3] Спонтанный гемоторакс обычно вызывается разрывом спаек плевры, новообразованием, метастазами в плевре и является осложнением антикоагулянтной терапии при тромбоэмболии легочной артерии. [4]
- Боль в груди
- Одышка
- Лихорадка
- Тахикардия
- Снижение звуков дыхания на пораженной стороне
- Бледность
- Холодный пот
Первоначальное лечение в большинстве случаев осуществляется с помощью дренирования плевральной трубки, когда большая трубка является адекватным начальным доступом, если не подозревается расслоение или разрыв аорты. [3] (Для получения дополнительной информации о дренаже грудной клетки). После выполнения торакостомии через трубку следует повторить рентгенографию грудной клетки, чтобы определить положение грудной трубки, выявить другую внутригрудную патологию и подтвердить, полностью ли дренирована кровь в плевральной полости. [4] [2] Плевральный выпот и оценка симптомов (ПОЖАЛУЙСТА) Результаты исследования показывают улучшение одышки и переносимости физической нагрузки у большинства пациентов с симптоматическим плевральным выпотом после дренирования [5] .
Иногда может использоваться хирургическое исследование. Это может быть показано, если кровопотеря через дренаж грудной клетки превышает 1500 мл за 24 часа или 200 мл в час в течение нескольких последовательных часов и при необходимости повторных переливаний крови для поддержания гемодинамической стабильности. [6] [7] [8] Пациентов с активной кровопотерей, но со стабильной гемодинамикой, можно лечить с помощью видео-торакоскопической хирургии (VATS). Это может быть использовано для остановки кровотечения, а также для удаления тромбов и разрушения спаек. Торакотомия — это процедура выбора для хирургического исследования грудной клетки при массивном гемотораксе или постоянном кровотечении. [2]
Нет опубликованных данных о физиотерапевтическом лечении пациентов с пневмотораксом или гемотораксом.
В качестве рекомендаций по ведению пациентов с гемотораксом можно рассматривать:
- Клиническая картина пациента должна помочь физиотерапевту решить, какое лечение ему подходит.

- Если у пациента есть дренажная дренажная трубка и межреберный дренаж, лечение может отличаться от хирургического.
- Помогает улучшить вентиляцию, оксигенацию и повторно наполнить ателектатические области легких. Это можно сделать с помощью упражнений на глубокое дыхание.
- Помогает улучшить переносимость физической нагрузки и подвижность пациента. Это можно сделать с помощью мобилизационных или общеукрепляющих упражнений.
- Помогает поддерживать чистоту дыхательных путей. Это можно сделать, продемонстрировав пациенту приемы оказания помощи при кашле, которые помогут избавиться от любых выделений.
С помощью визуализации диагноз пневмоторакса необходимо аннулировать. Гематокрит жидкости из плевральной полости также можно проверить, чтобы определить, можно ли диагностировать плевральный выпот или гемоторакс.
- ↑ 1.0 1.1 Патрини Д., Панагиотопулос Н., Парараджасингем Дж., Гвинианидзе Л., Икбал Ю.
 , Лоуренс Д. Этиология и лечение спонтанного гемоторакса. Журнал грудных болезней. 2015 Март; 7 (3): 520.
, Лоуренс Д. Этиология и лечение спонтанного гемоторакса. Журнал грудных болезней. 2015 Март; 7 (3): 520.
- ↑ 2,0 2,1 2,2 Boersma WG, Stigt JA, Smit HJ. Лечение гемоторакса. Респираторная медицина. 2010, 1 ноября; 104 (11): 1583-7.
- ↑ 3,0 3,1 Йем I, Сассун С. Гемоторакс и хилоторакс.Curr Opin Pulm Med 1997; 3: 310e4.
- ↑ 4,0 4,1 Бауманн М.Х., Стрэндж К., Хеффнер Дж. Э., Лайт Р., Кирби Т. Дж., Кляйн Дж., Лукетич Дж. Д., Паначек Е. А., Сан С. А.. Консенсусная группа AACP по пневмотораксу. Управление спонтанным пневмотораксом: согласованное заявление Делфи Американского колледжа грудных врачей. Сундук, февраль 2001 г .; 119 (2): 590e602.
- ↑ Муруганандан С., Аззопарди М., Томас Р., Фицджеральд Д. Б., Куок Ю. Дж., Чеа Х. М., Рид К.А., Баджен, Калифорния, Иствуд П.Р., Дженкинс С., Сингх Б. Исследование одышки у пациентов с оценкой плеврального выпота и симптомов (ПОЖАЛУЙСТА).
 симптоматический плевральный выпот.Европейский респираторный журнал. 2020 Янв 1.
симптоматический плевральный выпот.Европейский респираторный журнал. 2020 Янв 1.
- ↑ Али Х.А., Липпманн М., Мундатадже У, Халик Г. Спонтанный гемоторакс: всесторонний обзор. Сундук 2008; 134: 1056e65.
- ↑ Лю Д-В, Лю Х-П, Линь П. Дж. И др. Видеоассистированная торакальная хирургия при лечении травм грудной клетки. J. Trauma 1997; 42: 670e4.
- ↑ Lowdermilk GA, Naunheim KS. Торакоскопическая оценка и лечение травм грудной клетки. Surg Clin North Am 2000; 80: 1535e42.
Гемоторакс — StatPearls — Книжная полка NCBI
Постоянное обучение
Гемоторакс — это скопление крови в пространстве между висцеральной и париетальной плеврой (плевральное пространство).Клинические проявления у таких пациентов включают респираторный дистресс и тахипноэ. Это упражнение иллюстрирует оценку и лечение гемоторакса и рассматривает роль межпрофессиональной группы в улучшении ухода за пациентами с этим заболеванием.
Цели:
-
Обзор эпидемиологии гемоторакса.
-
Опишите использование протокола травм при обследовании пациентов с гемотораксом.
-
Опишите этапы реанимации и лечения гемоторакса.
-
Объясните важность улучшения координации ухода между межпрофессиональной командой для улучшения оказания помощи пациентам, страдающим гемотораксом.
Введение
Гемоторакс — частое последствие травматических повреждений грудной клетки. Это скопление крови в плевральном пространстве, потенциальном пространстве между висцеральной и париетальной плеврой. Наиболее распространенный механизм травмы — это тупое или проникающее повреждение внутригрудных или внегрудных структур, которое приводит к кровотечению в грудной клетке.Кровотечение может возникать из грудной стенки, межреберных или внутренних молочных артерий, магистральных сосудов, средостения, миокарда, паренхимы легких, диафрагмы или брюшной полости.
КТ — предпочтительный метод оценки внутригрудных повреждений; однако это может оказаться невозможным для нестабильного пациента с травмой. Кроме того, в небольших центрах может не быть доступной компьютерной томографии. Рентгенография грудной клетки традиционно использовалась в качестве скринингового инструмента для выявления непосредственных опасных для жизни травм.Недавняя литература предполагает, что ультразвуковое исследование в месте оказания медицинской помощи (POCUS) может быть полезным в качестве дополнения к традиционным методам визуализации. POCUS — это быстрый, надежный, воспроизводимый и, что самое главное, портативный. Его можно использовать у постели больного для сортировки и выявления опасных для жизни травм. Легочные окна были включены в протокол расширенной сфокусированной оценки с помощью сонографии при травмах (eFAST) с середины 2000-х годов. В дополнение к традиционным видам FAST в правом и левом верхнем квадранте оператор может сдвинуть зонд в головку, чтобы быстро оценить наличие жидкости над диафрагмой.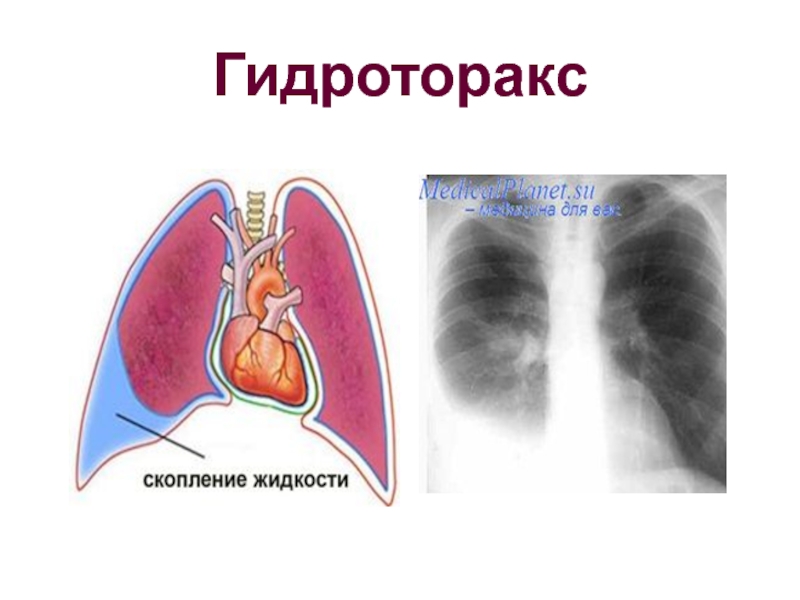 Многочисленные исследования показали, что УЗИ грудной клетки является ценным инструментом в диагностике пациентов с тупой травмой грудной клетки. [1] [2] [3] [4] [5] Ультразвук легких (УЗИ) при оценке гемоторакса продемонстрировал точность и более высокую чувствительность, чем рентгенография грудной клетки. [2] [5] [6] [7]
Многочисленные исследования показали, что УЗИ грудной клетки является ценным инструментом в диагностике пациентов с тупой травмой грудной клетки. [1] [2] [3] [4] [5] Ультразвук легких (УЗИ) при оценке гемоторакса продемонстрировал точность и более высокую чувствительность, чем рентгенография грудной клетки. [2] [5] [6] [7]
Этиология
Гемоторакс — частое проявление травматических повреждений (тупых или проникающих) структур грудной клетки. Большинство случаев гемоторакса возникает по тупому механизму с общей смертностью 9 человек.4% [8] Реже встречаются нетравматические причины. Примеры включают ятрогены, секвестрацию легких, сосудистые заболевания, неоплазию, коагулопатии и инфекционные процессы. [9]
Эпидемиология
Травмы являются серьезной проблемой для здоровья в Соединенных Штатах, вызывая 140000 смертей ежегодно. [10] Травмы грудной клетки встречаются примерно в 60% случаев множественных травм и являются причиной 20-25% смертности от травм. [6] Кроме того, травма является основной причиной смертности в четвертом десятилетии жизни. [7] В Соединенных Штатах автомобильные аварии составляют от 70 до 80% тупых травм грудной клетки. [11] Травма грудных структур может возникнуть в результате прямого удара или быстрого замедления. Недавние исследования показывают, что переломы грудного скелета, ушиб легкого и повреждения диафрагмы являются частыми проявлениями при тупой травме грудной клетки [12]. От 30 до 50 процентов пациентов с тяжелой тупой травмой грудной клетки имели сопутствующий ушиб легких, пневмоторакс и гемоторакс. [11] [13] Пневмоторакс, гемоторакс или гемопневмоторакс были обнаружены у 72.3% случаев травматических переломов ребер в серии, проведенной Сирмали и др. [12]
[7] В Соединенных Штатах автомобильные аварии составляют от 70 до 80% тупых травм грудной клетки. [11] Травма грудных структур может возникнуть в результате прямого удара или быстрого замедления. Недавние исследования показывают, что переломы грудного скелета, ушиб легкого и повреждения диафрагмы являются частыми проявлениями при тупой травме грудной клетки [12]. От 30 до 50 процентов пациентов с тяжелой тупой травмой грудной клетки имели сопутствующий ушиб легких, пневмоторакс и гемоторакс. [11] [13] Пневмоторакс, гемоторакс или гемопневмоторакс были обнаружены у 72.3% случаев травматических переломов ребер в серии, проведенной Сирмали и др. [12]
Патофизиология
Кровотечение в гемиторакс может возникнуть в результате травм диафрагмы, средостения, легких, плевры, грудной стенки и брюшной полости. Каждый гемиторакс может удерживать 40% объема циркулирующей крови пациента. Исследования показали, что повреждение межреберных сосудов (например, внутренних молочных артерий и легочных сосудов) приводит к значительному кровотечению, требующему инвазивного лечения.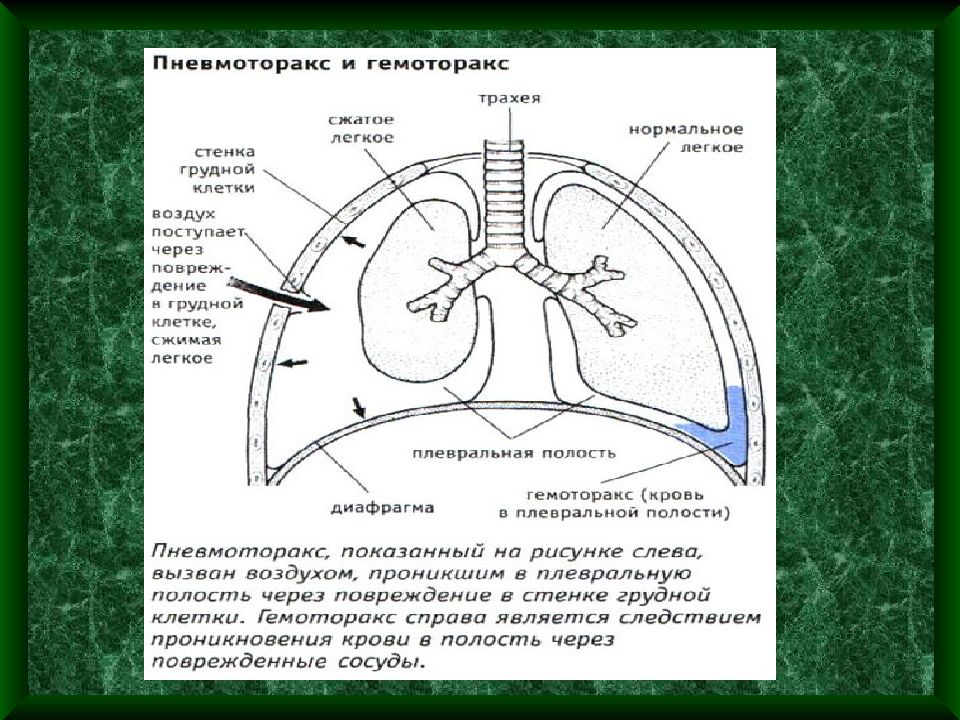 [13] Ранняя физиологическая реакция гемоторакса имеет гемодинамический и респираторный компоненты.Тяжесть патофизиологического ответа зависит от локализации травмы, функционального резерва пациента, объема крови и скорости накопления в гемитораксе. [14] [15] [16] При раннем ответе острая гиповолемия приводит к снижению преднагрузки, дисфункции левого желудочка и снижению сердечного выброса. Кровь в плевральном пространстве влияет на функциональную жизненную емкость легких, вызывая альвеолярную гиповентиляцию, несоответствие V / Q и анатомическое шунтирование. Большой гемоторакс может привести к увеличению гидростатического давления, которое оказывает давление на полую вену и легочную паренхиму, вызывая нарушение преднагрузки и увеличивая сопротивление легочных сосудов.Эти механизмы приводят к физиологическому напряжению гемоторакса и вызывают гемодинамическую нестабильность, сердечно-сосудистый коллапс и смерть.
[13] Ранняя физиологическая реакция гемоторакса имеет гемодинамический и респираторный компоненты.Тяжесть патофизиологического ответа зависит от локализации травмы, функционального резерва пациента, объема крови и скорости накопления в гемитораксе. [14] [15] [16] При раннем ответе острая гиповолемия приводит к снижению преднагрузки, дисфункции левого желудочка и снижению сердечного выброса. Кровь в плевральном пространстве влияет на функциональную жизненную емкость легких, вызывая альвеолярную гиповентиляцию, несоответствие V / Q и анатомическое шунтирование. Большой гемоторакс может привести к увеличению гидростатического давления, которое оказывает давление на полую вену и легочную паренхиму, вызывая нарушение преднагрузки и увеличивая сопротивление легочных сосудов.Эти механизмы приводят к физиологическому напряжению гемоторакса и вызывают гемодинамическую нестабильность, сердечно-сосудистый коллапс и смерть.
Анамнез и физические данные
Тщательный и точный сбор анамнеза пациента, свидетелей или поставщиков догоспитальных услуг помогает определить тех пациентов, у которых риск внутригрудной травмы низкий или высокий. Важные компоненты анамнеза включают боль в груди, одышку, механизм травмы (падение, направление и скорость), употребление наркотиков / алкоголя, сопутствующие заболевания, хирургический анамнез и антикоагулянтную / антитромбоцитарную терапию.Механизмы действия, которые позволили предсказать серьезную травму грудной клетки, включают дорожно-транспортное происшествие со скоростью более 35 миль в час, падение с высоты более 15 футов, катапультирование пешеходом с высоты более 10 футов и травмы с пониженным уровнем сознания. [14]
Важные компоненты анамнеза включают боль в груди, одышку, механизм травмы (падение, направление и скорость), употребление наркотиков / алкоголя, сопутствующие заболевания, хирургический анамнез и антикоагулянтную / антитромбоцитарную терапию.Механизмы действия, которые позволили предсказать серьезную травму грудной клетки, включают дорожно-транспортное происшествие со скоростью более 35 миль в час, падение с высоты более 15 футов, катапультирование пешеходом с высоты более 10 футов и травмы с пониженным уровнем сознания. [14]
Клинические проявления гемоторакса обширны и могут совпадать с пневмотораксом; к ним относятся респираторный дистресс, тахипноэ, снижение или отсутствие звуков дыхания, притупление перкуссии, асимметрия грудной стенки, отклонение трахеи, гипоксия, узкое пульсовое давление и гипотензия.Осмотрите грудную стенку на предмет признаков ушиба, ссадин, «признака ремня безопасности», проникающей травмы, парадоксальных движений («цепная грудь»), экхимоза, деформаций, крепитации и точечной болезненности.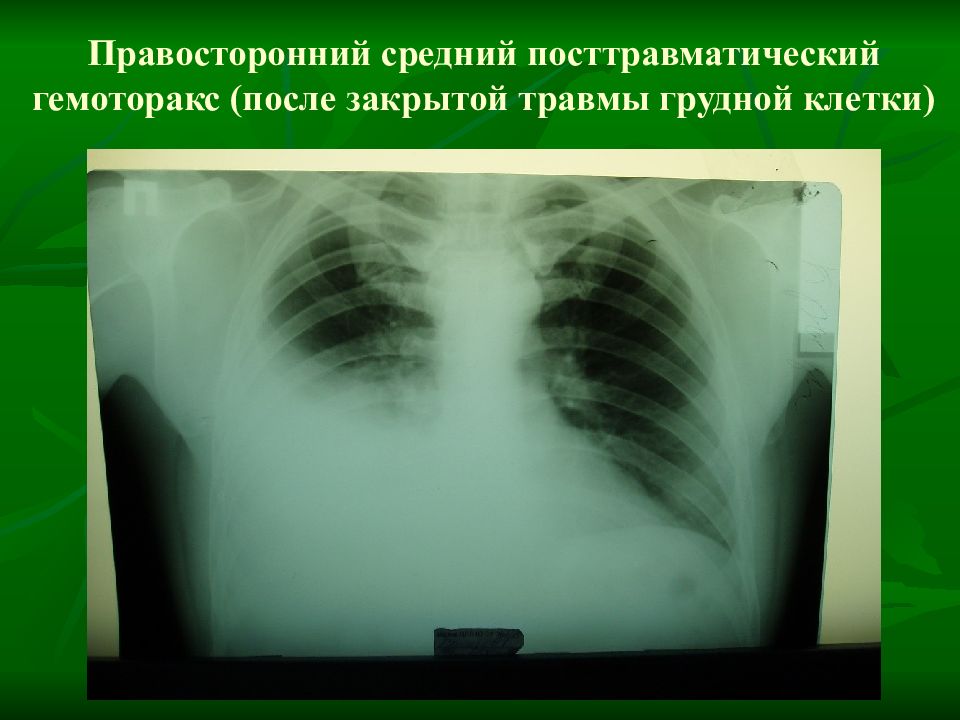 Расширенные шейные вены могут указывать на пневмоторакс или тампонаду перикарда, но может отсутствовать при гиповолемии. Повышенная частота дыхания, усилие и задействование дополнительных мышц могут быть признаками надвигающейся дыхательной недостаточности.
Расширенные шейные вены могут указывать на пневмоторакс или тампонаду перикарда, но может отсутствовать при гиповолемии. Повышенная частота дыхания, усилие и задействование дополнительных мышц могут быть признаками надвигающейся дыхательной недостаточности.
Следующие физические данные должны побудить врача рассмотреть эти условия:
-
Расширение шейных вен → тампонада перикарда, напряженный пневмоторакс, кардиогенная недостаточность, воздушная эмболия
-
«Знак ремня безопасности» → замедление или повреждение сосудов; ушиб / ссадина грудной стенки
-
Парадоксальное движение грудной стенки → грудная клетка
-
отек или цианоз → повреждение верхнего средостения с окклюзией или компрессией верхней полой вены (SVC)
-
Подкожная эмфизема → разорванный бронх или разрыв паренхимы легких
-
Лопатка живота → травма диафрагмы с грыжей содержимого живота в грудную клетку
-
Чрезмерное движение живота с дыханием → травма грудной стенки
- 09 оценка, распознавание и вмешательство в возможные травмы грудной клетки имеют важное значение.
 Американский колледж хирургов разработал протокол American Traumatic Life Support (ATLS), который реализует стандартизированный и методический подход к оценке каждого пациента с травмой. [17] При травмах грудной клетки сердечно-легочная оценка должна иметь приоритет, так как в случае ее пропуска у нее будет самый высокий индекс смертности [18]. Травмы других структур грудной клетки заслуживают рассмотрения; ребра, ключица, трахея, бронхи, пищевод и сосуды.
Американский колледж хирургов разработал протокол American Traumatic Life Support (ATLS), который реализует стандартизированный и методический подход к оценке каждого пациента с травмой. [17] При травмах грудной клетки сердечно-легочная оценка должна иметь приоритет, так как в случае ее пропуска у нее будет самый высокий индекс смертности [18]. Травмы других структур грудной клетки заслуживают рассмотрения; ребра, ключица, трахея, бронхи, пищевод и сосуды. Диагностика: рассвет POCUS
Визуализация играет очень важную роль в лечении травм.Исследование, впервые описанное Rozycki et al., Направлено на обследование перикарда, перипеченки, периспленики и таза на предмет наличия патологической жидкости или скопления воздуха [19].
Доказано, что он обеспечивает быструю и точную оценку травмированного пациента с растущими доказательствами в поддержку его использования для диагностики гемоторакса, пневмоторакса и ушиба легких. [1] [20] Ультразвук легких включен в несколько протоколов недифференцированной одышки: ПАДЕНИЕ, СИНИЙ.
 [21] [22]
[21] [22] Ультразвук в месте оказания медицинской помощи при травмах значительно повлиял на оценку и расположение пациентов с травмами.[23] Он портативный, воспроизводимый, неинвазивный, воспроизводимый и не использует радиацию или контрастные вещества. [7]
В дополнение к четырем стандартным изображениям, eFAST включает в себя наклонные изображения обеих гемидиафрагм для оценки зависимости от жидкости (гемоторакс) и виды спереди для оценки пневмоторакса. В режиме B датчик (криволинейный 5–1 МГц или фазированная решетка 5–1 МГц) размещается в средней части подмышечной впадины в пятом или шестом межреберье, при этом маркер направлен к голове пациента.В хорошо вентилируемом и здоровом легком воздух препятствует прямой визуализации структур глубоко на границе раздела диафрагмы и висцеральной плевры легкого. Гемоторакс будет выглядеть как безэхогенное (черное) пространство между диафрагмой и париетальной плеврой в реберно-диафрагмальном кармане [24]. Жидкость также может содержать неоднородные эхо-сигналы от свернувшейся крови или части разорванной легочной ткани.
 Наличие плевральной жидкости позволяет визуализировать грудной отдел позвоночника за пределами реберно-диафрагмального угла, известного как «признак позвоночника».«Это явление происходит из-за потери артефакта зеркального отражения диафрагмы [5]
Наличие плевральной жидкости позволяет визуализировать грудной отдел позвоночника за пределами реберно-диафрагмального угла, известного как «признак позвоночника».«Это явление происходит из-за потери артефакта зеркального отражения диафрагмы [5] Рентген грудной клетки по-прежнему является первичным диагностическим инструментом при скрининге травматических повреждений грудной клетки. Исследования показывают, что ультразвуковое исследование является лучшим методом диагностики по сравнению с ультразвуковым исследованием. диагностический инструмент для выявления травматических повреждений грудной клетки (например, пневмоторакса и гемоторакса). [5] [6] [7] [20] Системный обзор показал, что ультразвук имеет более высокую чувствительность (67%) по сравнению с рентгеном грудной клетки (54 %). [6] Чувствительность была еще выше — 70%, когда врач скорой помощи выполнил eFAST.В проспективном исследовании чувствительность и специфичность ультразвукового исследования грудной клетки при обнаружении гемоторакса составили 92% и специфичность 100% соответственно [1].
 Кроме того, УЗИ может обнаружить всего 20 мл плевральной жидкости по сравнению с 175 мл при рентгенографии [6] и на 100% чувствителен к обнаружению выпота более 100 мл [24].
Кроме того, УЗИ может обнаружить всего 20 мл плевральной жидкости по сравнению с 175 мл при рентгенографии [6] и на 100% чувствителен к обнаружению выпота более 100 мл [24]. Еще одной особенностью ультразвука является его способность определять объем выпота. Для прогнозирования объема были разработаны и изучены четыре различных сонографических формулы.Две из четырех формул применяются, когда пациент лежит на спине. Датчик размещается перпендикулярно грудной стенке, а измерения проводятся при максимальном вдохе, когда пациенты задерживают дыхание. «X» — это максимальное перпендикулярное (межплевральное) расстояние в мм между задней поверхностью легкого (висцеральной плеврой) и задней стенкой грудной клетки (париетальной плеврой), измеренное [25].
Следующие формулы:
Две другие формулы выполняются с пациентом в сидячем (прямом) положении, что выходит за рамки данного обсуждения.
Рекомендуемое обследование гемоторакса включает общий анализ крови (исходный уровень гемоглобина), CMP (креатинин), тропонин, профиль коагуляции, а также тип и скрининг.
 [14] В нескольких исследованиях сообщается, что лактат в сыворотке является предиктором смертности при травмах. Данные в основном получены из ретроспективных исследований, и ни одно из них не проводилось в условиях тупой травмы грудной клетки. Уровень лактата в сыворотке выше 4 мг / дл коррелирует с более высокой смертностью. Серийные тропонины должны быть получены дополнительно к ЭКГ для оценки сердечного ушиба.
[14] В нескольких исследованиях сообщается, что лактат в сыворотке является предиктором смертности при травмах. Данные в основном получены из ретроспективных исследований, и ни одно из них не проводилось в условиях тупой травмы грудной клетки. Уровень лактата в сыворотке выше 4 мг / дл коррелирует с более высокой смертностью. Серийные тропонины должны быть получены дополнительно к ЭКГ для оценки сердечного ушиба.Лечение / ведение
Выполните первоначальную реанимацию и ведение пациента с травмой в соответствии с протоколом ATLS. У каждого пациента должен быть доступ к двум капельницам большого диаметра, он должен находиться под кардиомонитором и кислородным монитором, а также иметь ЭКГ в 12 отведениях. Немедленные опасные для жизни травмы требуют немедленного вмешательства, такого как торакостомия с помощью декомпрессионной иглы и / или торакостомия с использованием экстренной трубки при большом пневмотораксе, а также начальное лечение гемоторакса. [26]
Минимальный сбор крови (определяется как менее 300 мл) в плевральной полости, как правило, не требует лечения; кровь обычно реабсорбируется в течение нескольких недель.
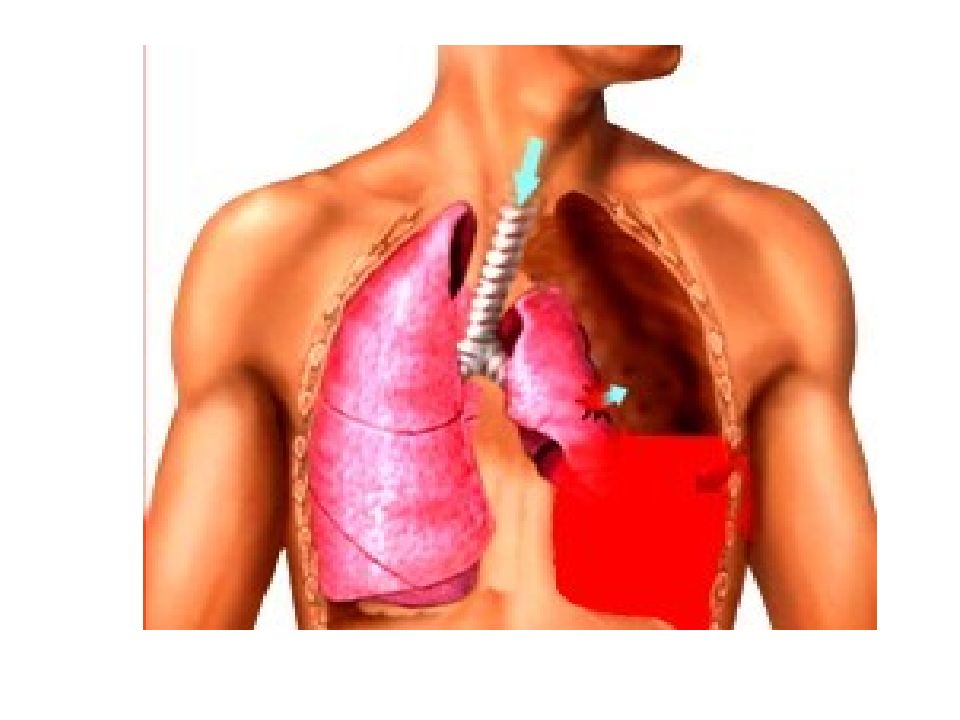 Если состояние пациента стабильное и респираторный дистресс минимальный, оперативное вмешательство обычно не требуется. Эту группу пациентов можно лечить обезболиванием по мере необходимости и наблюдать с повторной визуализацией через 4-6 часов и 24 часа.
Если состояние пациента стабильное и респираторный дистресс минимальный, оперативное вмешательство обычно не требуется. Эту группу пациентов можно лечить обезболиванием по мере необходимости и наблюдать с повторной визуализацией через 4-6 часов и 24 часа. По возможности следует проконсультироваться с кардиоторакальным хирургом или хирургом при травмах для проведения торакостомии с трубкой. Традиционно для эвакуации гемоторакса использовалось 36-40 французских дренажных трубок, но эта практика стала предметом пристального внимания.Недавние исследования показывают, что большинство хирургов используют от 32 до 36 французских трубок. Проспективные исследования демонстрируют отсутствие разницы в результатах при использовании 28–32 французских трубок в травматологических центрах I уровня для эвакуации гемоторакса [17].
При асептическом подходе трубка помещается сзади по направлению к жидкости, зависящей от силы тяжести, в четвертом или пятом межреберье между передней и средней подмышечной линией.
 Затем торакостомическая трубка подсоединяется к гидрозатвору и отсосу, чтобы облегчить быстрый дренаж и предотвратить утечку воздуха.Кроме того, введение трубки обеспечивает количественный анализ крови, чтобы определить, требуется ли хирургическое вмешательство.
Затем торакостомическая трубка подсоединяется к гидрозатвору и отсосу, чтобы облегчить быстрый дренаж и предотвратить утечку воздуха.Кроме того, введение трубки обеспечивает количественный анализ крови, чтобы определить, требуется ли хирургическое вмешательство. Согласно литературным данным, показания к хирургическому вмешательству (срочная передняя торакотомия) включают:
-
1500 мл дренирования крови за 24 часа через дренажную трубку
-
300-500 мл / час в течение 2-4 часов подряд после введения дренажной трубки
-
Повреждение большого сосуда или грудной стенки
-
Тампонада перикарда
Торакотомия позволяет быстро оценить внутригрудные повреждения и гемостаз.
Дренирование гемоторакса при коагулопатии следует проводить осторожно, с учетом основного заболевания. Коррекция коагуляционной функции перед хирургическим вмешательством должна выполняться, если это разрешено клиническим статусом пациента.

Неправильная эвакуация гемоторакса может привести к таким осложнениям, как эмпиема и фиброторакс. Множественные исследования продемонстрировали эффективность видео-торакоскопии для лечения сохраненного гемоторакса. Это положительно сказалось на продолжительности пребывания в больнице и выживаемости пациентов.VATS обеспечивает четкую визуализацию плевральной полости, правильное размещение дренажной трубки для точного контроля кровотечения, удаление оставшегося сгустка, эвакуацию и декортикацию посттравматических эмпием. Кроме того, он обеспечивает оценку подозреваемых повреждений диафрагмы, лечение постоянных утечек воздуха и оценку повреждений средостения. [27]
Дифференциальный диагноз
Дифференциальный диагноз тупой травмы грудной клетки можно разделить на три категории [14]:
Висцеральные травмы
Скелетные травмы
-
Цепной грудной клетки
- 0 Переломы костей грудной клетки
-
Перелом лопатки
-
Перелом или вывих ключицы
-
Травма позвоночника или позвоночника
Сердечно-сосудистые травмы
Прогноз
Травмы и серьезность травм коррелируют с заболеваемостью и летальностью поздних осложнений, а именно эмпиемы и фиброторакса / застойного легкого.
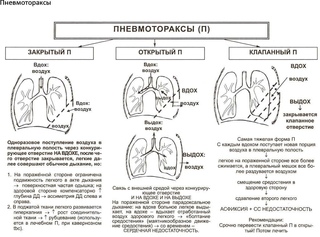 Пациенты с сохраненным гемотораксом подвержены риску развития эмпиемы, что приведет к длительному пребыванию в отделении интенсивной терапии / больнице [27].
Пациенты с сохраненным гемотораксом подвержены риску развития эмпиемы, что приведет к длительному пребыванию в отделении интенсивной терапии / больнице [27]. Осложнения
Осложнения при УЗИ грудной клетки
Массивный гемоторакс может привести к
-
Гемодинамическая нестабильность
-
Шок
-
Гипоксия
-
2
-
2 Смерть
установка дренажной трубки может привести к недостаточному дренированию гемоторакса, что способствует образованию эмпиемы.Исследования показывают, что частота эмпиемы у пациентов с посттравматическим сохраненным гемотораксом составляет 26,8%. Фиброторакс возникает в результате отложения фибрина в плевральной полости. Неправильный дренаж гемоторакса вызывает воспалительный налет в плевральной полости, который препятствует правильному расширению легких. Это явление известно как защемление легких. [28]Сдерживание и обучение пациентов
Исследования показывают, что отсутствие удерживающих устройств и инвалидность водителя являются основными факторами, способствующими тяжелым травмам в дорожно-транспортных происшествиях.
 [29] [30] Медицинские работники должны поощрять принятие мер безопасности, таких как использование ремней безопасности, недопущение нарушения правил вождения и альтернативные транспортные стратегии. [31] [32] [33]
[29] [30] Медицинские работники должны поощрять принятие мер безопасности, таких как использование ремней безопасности, недопущение нарушения правил вождения и альтернативные транспортные стратегии. [31] [32] [33] Жемчуг и другие проблемы
Ультразвук в местах оказания медицинской помощи признан во всем мире в качестве прикроватного обследования в отделениях неотложной помощи. Он также был введен в формальную ординатуру. Это позволяет быстро и с воспроизводимой оценкой травматических повреждений без риска вредного излучения.Различные исследования были направлены на оценку диагностической ценности ультразвукового исследования грудной клетки при травматическом гемотораксе. Систематический обзор и метаанализ показали, что чувствительность ультразвука зависит от оператора и частоты датчика. [6] Проспективное поперечное исследование продемонстрировало, что ультразвук является лучшим методом, чем рентгенография, но по сравнению с компьютерной томографией оно показало более низкую чувствительность [7].

Систематический обзор для определения общей точности ультразвукового исследования при травматической травме грудной клетки имеет несколько ограничений.Неоднородные характеристики результатов УЗИ с разными машинами, датчиками и уровнями опыта влияют на общее методологическое качество этих исследований. [5]
Улучшение результатов медицинской бригады
Ультразвук на месте оказания медицинской помощи при оценке травматических повреждений грудной клетки является ценным вспомогательным инструментом. Его применение при травмах изучалось и анализировалось во множестве систематических обзоров. Будущие рандомизированные исследования должны быть выполнены для оценки соответствующих исходов, таких как смертность, продолжительность пребывания в больнице и затраты.[5] [34] Медсестры должны контролировать вывод через дренажную трубку каждый час во время первичной госпитализации; если результат значительный и непрерывный, следует уведомить торакального хирурга. Хотя большинство случаев разрешается с помощью дренажной трубки, если гемоторакс не эвакуирован, это может привести к эмпиеме, которая часто требует хирургического вмешательства.
 Результаты для большинства пациентов с изолированным гемотораксом хорошие. [35] (уровень V)
Результаты для большинства пациентов с изолированным гемотораксом хорошие. [35] (уровень V) Рисунок
Гемоторакс, Рентген. Предоставлено Стивом Бхимджи, MS, MD, PhD
Рисунок
Правосторонний гемоторакс.Предоставлено Ву Хуи Траном, MD
Рисунок
Травматическая остановка гемоторакса. Автор: Ву Хуй Тран, доктор медицины
Рисунок
Гемоторакс. Предоставлено Vu Huy Tran, MD
Ссылки
- 1.
- Брукс А., Дэвис Б., Сметхерст М., Коннолли Дж. Экстренное ультразвуковое исследование при острой оценке гемоторакса. Emerg Med J. 2004 января; 21 (1): 44-6. [Бесплатная статья PMC: PMC1756377] [PubMed: 14734374]
- 2.
- Stengel D, Leisterer J, Ferrada P, Ekkernkamp A, Mutze S, Hoenning A.Ультрасонография в месте оказания медицинской помощи для диагностики торакоабдоминальных травм у пациентов с тупой травмой. Кокрановская база данных Syst Rev.2018 декабря 12; 12: CD012669. [Бесплатная статья PMC: PMC6517180] [PubMed: 30548249]
- 3.
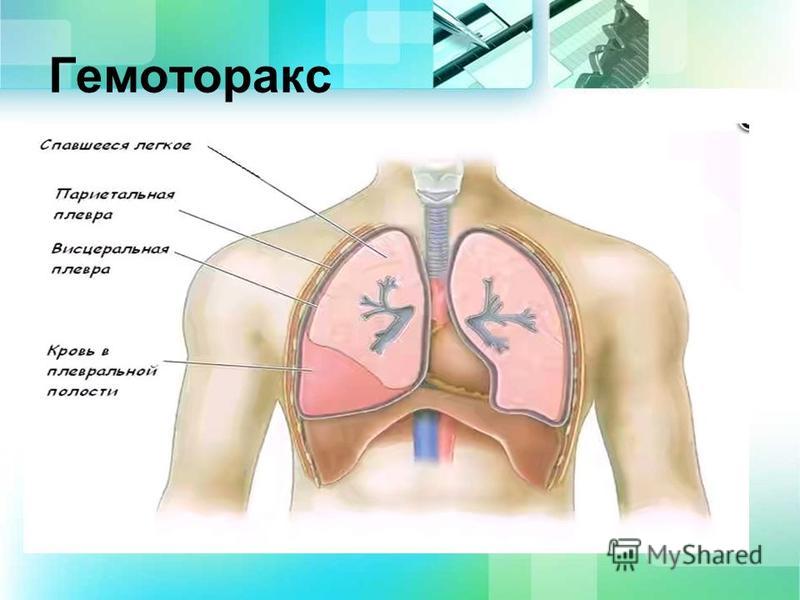
- Abboud PA, Kendall J. УЗИ отделения неотложной помощи при гемотораксе после тупой травмы. J Emerg Med. 2003 августа; 25 (2): 181-4. [PubMed: 12
- 6]
- 4.
- МакЭван К., Томпсон П. Ультразвук для выявления гемоторакса после травмы грудной клетки. Emerg Med J.2007 августа; 24 (8): 581-2. [Бесплатная статья PMC: PMC2660093] [PubMed: 17652688]
- 5.
- Staub LJ, Biscaro RRM, Kaszubowski E, Maurici R. УЗИ грудной клетки для экстренной диагностики травматического пневмоторакса и гемоторакса: систематический анализ и мета-анализ. Травма, повреждение. Март 2018; 49 (3): 457-466. [PubMed: 29433802]
- 6.
- Рахими-Мовагар В., Юсефифард М., Геличхани П., Байкпур М., Тафахори А., Асади Х, Фаридалаи Г., Хоссейни М., Сафари С. Применение ультразвуковой и радиографии для обнаружения гемоторакса; Систематический обзор и метаанализ.Emerg (Тегеран). Лето 2016; 4 (3): 116-26. [Бесплатная статья PMC: PMC44] [PubMed: 27299139]
- 7.
- Вафаэй А.
 , Хатамабади Х. Р., Хейдари К., Алимохаммади Х., Тарбият М. Диагностическая точность ультразвукового исследования и рентгенографии при первоначальной оценке пациентов с травмой грудной клетки. Emerg (Тегеран). 2016 Зима; 4 (1): 29-33. [Бесплатная статья PMC: PMC4744611] [PubMed: 26862547]
, Хатамабади Х. Р., Хейдари К., Алимохаммади Х., Тарбият М. Диагностическая точность ультразвукового исследования и рентгенографии при первоначальной оценке пациентов с травмой грудной клетки. Emerg (Тегеран). 2016 Зима; 4 (1): 29-33. [Бесплатная статья PMC: PMC4744611] [PubMed: 26862547] - 8.
- Broderick SR. Гемоторакс: этиология, диагностика и лечение. Thorac Surg Clin. 2013 Февраль; 23 (1): 89-96, vi-vii.[PubMed: 23206720]
- 9.
- Boersma WG, Stigt JA, Smit HJ. Лечение гемоторакса. Respir Med. 2010 ноя; 104 (11): 1583-7. [PubMed: 20817498]
- 10.
- Гудман М., Льюис Дж., Гитрон Дж., Рид М., Притс Т., Старнес С. Торакоскопическая хирургия с видеосвязью при острой травме грудной клетки. J Emerg Trauma Shock. 2013 Апрель; 6 (2): 106-9. [Бесплатная статья PMC: PMC3665056] [PubMed: 23723618]
- 11.
- Özdil A, Kavurmacı Ö, Akçam Tİ, Ergönül AG, Uz İ, ahutolu C, Yüzkan S, akan Aıcıa.Патология, которую нельзя упускать из виду при тупой травме грудной клетки: Анализ 181 пациента с двусторонним пневмотораксом.
 Ulus Travma Acil Cerrahi Derg. 2018 ноя; 24 (6): 521-527. [PubMed: 30516250]
Ulus Travma Acil Cerrahi Derg. 2018 ноя; 24 (6): 521-527. [PubMed: 30516250] - 12.
- Сирмали М., Тюрют Х., Топчу С., Гюльхан Э., Язичи У., Кая С., Таштепе И. Комплексный анализ травматических переломов ребер: заболеваемость, смертность и лечение. Eur J Cardiothorac Surg. 2003 июл; 24 (1): 133-8. [PubMed: 12853057]
- 13.
- Ота К., Фумимото С., Иида Р., Катаока Т., Ота К., Танигучи К., Ханаока Н., Такасу А.Массивный гемоторакс из-за двух источников кровотечения с легким механизмом травмы: отчет о болезни. J Med Case Rep.7 октября 2018 г .; 12 (1): 291. [Бесплатная статья PMC: PMC6174063] [PubMed: 30292243]
- 14.
- Морли Э. Дж., Джонсон С., Лейбнер Э., Шахид Дж. Оценка отделения неотложной помощи и лечение тупой травмы грудной клетки и легкого (Trauma CME). Emerg Med Pract. 2016 июн; 18 (6): 1-20. [PubMed: 27177417]
- 15.
- Chou YP, Lin HL, Wu TC. Видеоассистированная торакоскопическая хирургия оставшегося гемоторакса при тупой травме грудной клетки.
 Curr Opin Pulm Med. 2015 июл; 21 (4): 393-8. [Бесплатная статья PMC: PMC5633323] [PubMed: 25978625]
Curr Opin Pulm Med. 2015 июл; 21 (4): 393-8. [Бесплатная статья PMC: PMC5633323] [PubMed: 25978625] - 16.
- Скотт М.Ф., Ходавердян Р.А., Шахин Д.Л., Ней А.Л., Найгаард Р.М. Предикторы сохранения гемоторакса после травмы и влияние на исходы пациентов. Eur J Trauma Emerg Surg. 2017 Апрель; 43 (2): 179-184. [PubMed: 26619854]
- 17.
- Эджкомб Л., Сигмон Д.Ф., Галуска М.А., Ангус Л.Д. StatPearls [Интернет]. StatPearls Publishing; Остров сокровищ (Флорида): 2 июня 2021 г. Торакальная травма.[PubMed: 30521264]
- 18.
- Джейн А., Секуски А.Л., Бернс Б. StatPearls [Интернет]. StatPearls Publishing; Остров сокровищ (Флорида): 25 апреля 2021 г. Проникающая травма груди. [PubMed: 30571065]
- 19.
- Richards JR, McGahan JP. Целенаправленная оценка с помощью сонографии при травмах (FAST) в 2017 г .: чему могут научиться радиологи. Радиология. 2017 Апрель; 283 (1): 30-48. [PubMed: 28318439]
- 20.
- Hyacinthe AC, Broux C, Francony G, Genty C, Bouzat P, Jacquot C, Albaladejo P, Ferretti GR, Bosson JL, Payen JF.
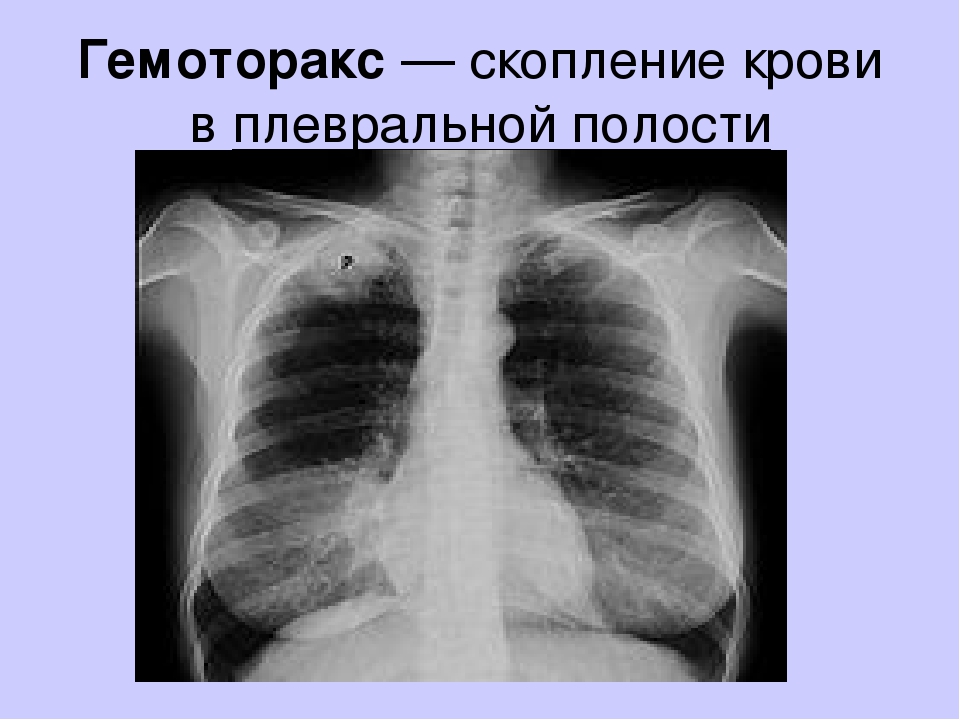 Диагностическая точность ультразвукового исследования при острой оценке поражений грудного отдела грудной клетки после травм. Грудь. 2012 Май; 141 (5): 1177-1183. [PubMed: 22016490]
Диагностическая точность ультразвукового исследования при острой оценке поражений грудного отдела грудной клетки после травм. Грудь. 2012 Май; 141 (5): 1177-1183. [PubMed: 22016490] - 21.
- Лихтенштейн Д. Новые подходы к ультразвуковому исследованию легких и плевральной полости: где мы сейчас? Дыши (Шефф). 2017 июн; 13 (2): 100-111. [Бесплатная статья PMC: PMC5467658] [PubMed: 28620429]
- 22.
- Лихтенштейн Д.А. BLUE-протокол и FALLS-протокол: два применения УЗИ легких у тяжелобольных.Грудь. 2015 июн; 147 (6): 1659-1670. [PubMed: 26033127]
- 23.
- Zieleskiewicz L, Fresco R, Duclos G, Antonini F, Mathieu C, Medam S, Vigne C, Poirier M, Roche PH, Bouzat P, Kerbaul F, Scemama U, Bège T, Thomas PA, Flecher X, Hammad E, Leone M. Интеграция расширенной сфокусированной оценки с сонографией при травме (eFAST) в первоначальную оценку тяжелой травмы: влияние на ведение 756 пациентов. Травма, повреждение. Октябрь 2018; 49 (10): 1774-1780. [PubMed: 30017184]
- 24.
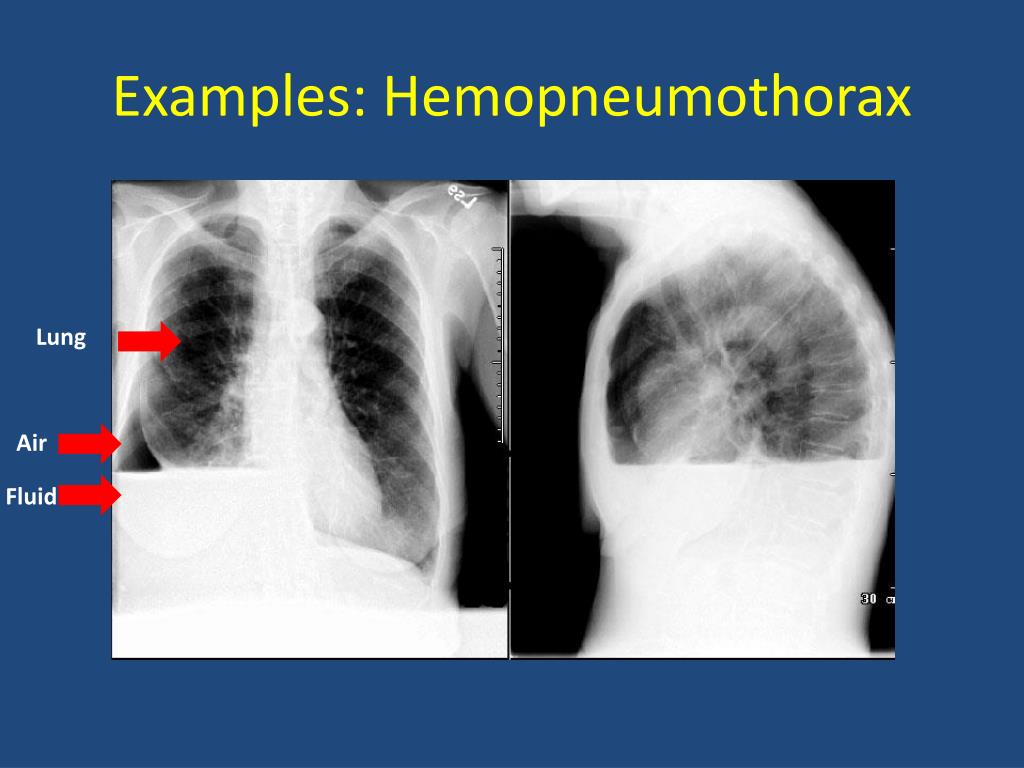
- Сони, штат Нью-Джерси, Франко Р., Велес М. И., Шнобрич Д., Дансел Р., Рестрепо М. И., Майо PH.Ультразвук в диагностике и лечении плеврального выпота. J Hosp Med. 2015 декабрь; 10 (12): 811-6. [Бесплатная статья PMC: PMC4715558] [PubMed: 26218493]
- 25.
- Ибитое Б.О., Идову Б.М., Огунромби А.Б., Афолаби Б.И. Ультрасонографическая количественная оценка плеврального выпота: сравнение четырех формул. Ультразвуковая эхография. 2018 июл; 37 (3): 254-260. [Бесплатная статья PMC: PMC6044225] [PubMed: 29228764]
- 26.
- Dennis BM, Gondek SP, Guyer RA, Hamblin SE, Gunter OL, Guillamondegui OD.Использование доказательного алгоритма для пациентов с травматическим гемотораксом снижает потребность в дополнительных вмешательствах. J Trauma Acute Care Surg. 2017 Апрель; 82 (4): 728-732. [PubMed: 28099387]
- 27.
- Глисон Т., Блехар Д. Ультразвук в месте оказания медицинской помощи при травмах. Семин УЗИ КТ МРТ. 2018 август; 39 (4): 374-383.
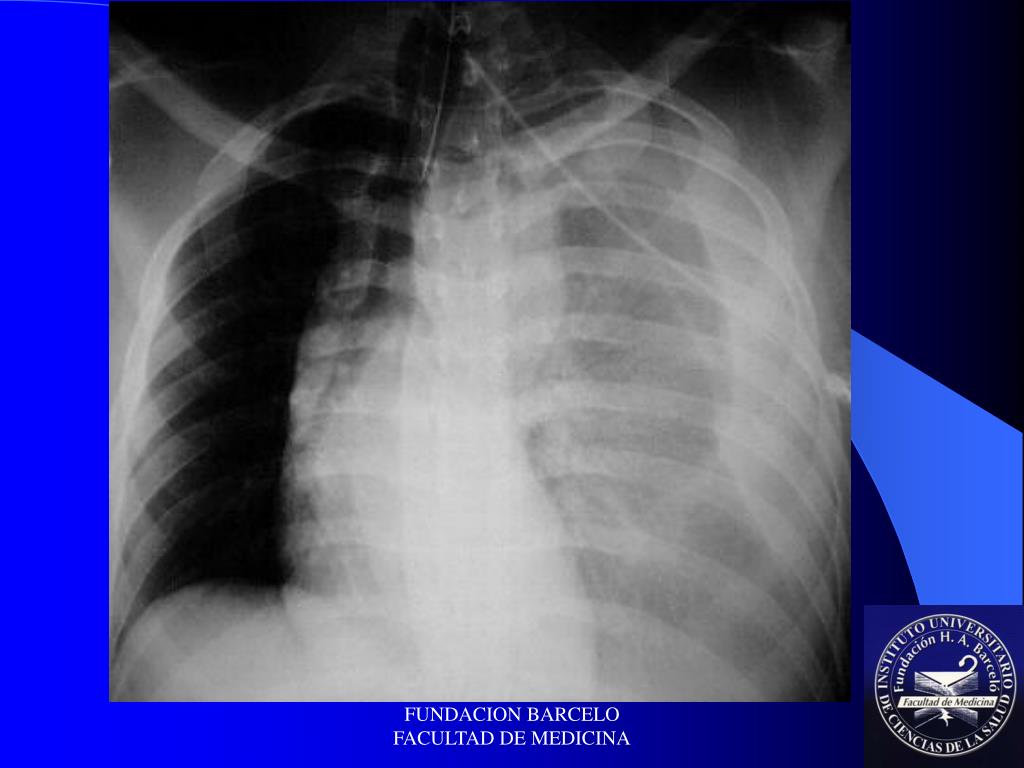 [PubMed: 30070230]
[PubMed: 30070230] - 28.
- Tian Y, Zheng W, Zha N, Wang Y, Huang S., Guo Z. Торакоскопическая декортикация для лечения застойного легкого, вызванного 14-летним пневмотораксом: отчет о клиническом случае.Рак грудной клетки. 2018 августа; 9 (8): 1074-1077. [Бесплатная статья PMC: PMC6068443] [PubMed: 29802756]
- 29.
- Банн Т., Синглтон М., Чен IC. Использование нескольких источников данных для выявления конкретных наркотиков и других факторов, связанных с проверкой на наркотики и алкоголь водителей транспортных средств, получивших смертельные травмы. Accid Anal Пред. 2019 Янв; 122: 287-294. [PubMed: 30396030]
- 30.
- Чжу М., Ли Й., Ван Ю. Дизайн и экспериментальная проверка новой аналитической основы для распознавания моделей травм водителя: с точки зрения мультиклассовой классификации.Accid Anal Пред. 2018 ноя; 120: 152-164. [PubMed: 30138770]
- 31.
- Морган Э. Дилеммы вождения: Руководство по оценке вождения в первичной медицинской помощи.
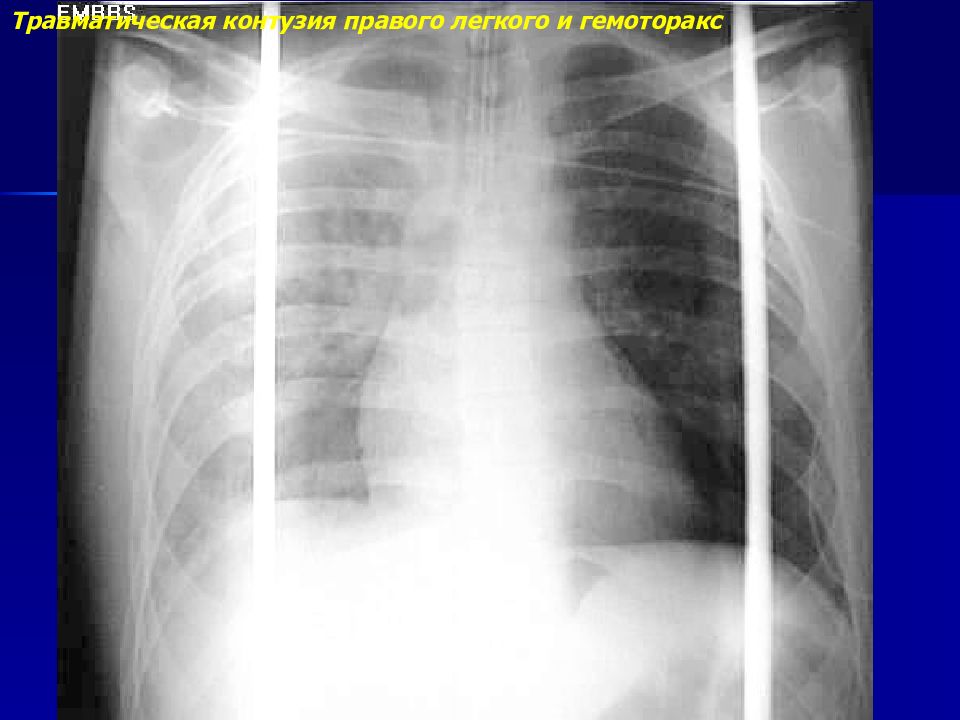 Clin Geriatr Med. 2018 Февраль; 34 (1): 107-115. [PubMed: 210]
Clin Geriatr Med. 2018 Февраль; 34 (1): 107-115. [PubMed: 210] - 32.
- Ecola L, Popper SW, Silberglitt R, Fraade-Blanar L. Дорога к нулю: видение достижения нулевой смертности на дорогах к 2050 году. Rand Health, квартал 2018, октябрь; 8 (2 ): 11. [Бесплатная статья PMC: PMC6183773] [PubMed: 30323994]
- 33.
- Хан Г.М., Ньюмайер А., Ку М.Использование ремня безопасности для экономии денег: влияние на больничные расходы пассажиров, попавших в автомобильные аварии. Int Emerg Nurs. 2017 Март; 31: 2-8. [PubMed: 27177737]
- 34.
- Chung MH, Hsiao CY, Nian NS, Chen YC, Wang CY, Wen YS, Shih HC, Yen DH. Преимущество ультразвука в выборе между трубочной торакостомией и наблюдательным лечением гемоторакса в результате тупой травмы грудной клетки. Мир J Surg. 2018 июл; 42 (7): 2054-2060. [PubMed: 29305713]
- 35.
- Карвер Д.А., Брессан А.К., Шиман К., Грондин С.К., Киркпатрик А.В., Лалл Р., Макбет ПБ, Данхэм МБ, Болл К.Г.Ведение гемоторакса при тупой травме грудной клетки: протокол рандомизированного контролируемого исследования.
 BMJ Open. 2018 03 марта; 8 (3): e020378. [Бесплатная статья PMC: PMC5855202] [PubMed: 29502092]
BMJ Open. 2018 03 марта; 8 (3): e020378. [Бесплатная статья PMC: PMC5855202] [PubMed: 29502092]
Травматический гемоторакс — Core EM
Определение: Накопление крови в плевральной полости в результате тупого или проникающего ранения грудных структур, включая сердце, средостение, легкие, магистральные сосуды, сосудистую сеть легких и грудную стенку.
Эпидемиология:
- Связано с пневмотораксом в 25% случаев
- Связано с внегрудными травмами в 73% случаев
Признаки + симптомы:
- Одышка, боль в груди (плевритная), одышка
- Снижение (или отсутствие) звуков дыхания (высокая частота ложноотрицательных результатов)
- Пониженная тактильная частота пульса
- В зависимости от объема кровотечения у пациента могут появиться признаки геморрагического шока
Источники кровотечения
- Низкое давление: паренхима легкого
- Высокое давление: межреберная артерия, легочная артерия, внутренняя молочная артерия
- Внеторакальные: внутрибрюшные травмы с сочетанной травмой диафрагмы
Управление:
Основы:
- ABCs, IV, O 2 , Кардиомонитор, ЭКГ в 12 отведениях
- Обязательно осмотрите пациента на предмет всех сопутствующих травм, так как у 73% пациентов будут внегрудные травмы.
- Рассмотреть возможность замены факторов свертывания крови у стабильных пациентов с коагулопатией
- Обезболивание по необходимости
Торакостомия с трубкой
Управление торакостомией после трубки
- Антибиотики профилактические
- Недостаточная литература для поддержки использования, но рекомендована Восточной ассоциацией хирургов травматологии (EAST)
- Выбор антибиотика: цефалоспорин 1-го поколения
- Более широкий охват при подозрении на торакоабдоминальное повреждение / повреждение кишечника
- Подтверждение размещения трубки
- Прикроватная:
- Проверить свободный ток крови в пробирке
- Убедитесь, что трубка может свободно вращаться 360 o
- CXR предлагает окончательную оценку
- Прикроватная:
Осложнения
- Инфекция
- Ятрогенное повреждение паренхимы легкого или межреберных артерий
- Случайное попадание в брюшную полость, ведущее к повреждению твердого органа
- Остаточный / оставшийся гемоторакс (из-за недостаточного дренажа) может стать очагом инфекции и развития эмпиемы
Показания к операции после грудной трубки — Roberts + Hedges
Дополнительное управление
- Переливание крови для поддержания гемодинамической стабильности
- Коррекция недостаточности фактора свертывания крови по мере необходимости
- Избранной группе пациентов с травматическим гемотораксом потребуется дополнительное хирургическое вмешательство (немедленное дренирование> 1000 см3 или продолжение кровотечения 200 см3 / час после торакостомии через трубку)
- Процедуры, включающие торакотомию и видео-торакоскопическое лечение (VATS)
Артикул:
Kirsch TD, Sax J: Tube Thoracostomy, in Roberts JR, Hedges JR, Custalow CB, et al (eds): Clinical Procedures in Emergency Medicine, ed 6.Филадельфия, Сондерс, 2013 г., гл. 10: стр. 189-203.
Eckstein M, Henderson SO: Травма грудной клетки; в Marx JA, Hockberger RS, Walls RM, et al (eds): Rosen’s Emergency Medicine: Concepts and Clinical Practice, ed 8. St. Louis, Mosby, Inc., 2014, (Ch) 45: p 431–460.
Кармоди, К., Мур, К., Феллер-Копман, Д. «Ультразвук грудной клетки». Справочник по интенсивной терапии и неотложной ультразвуковой диагностике. Нью-Йорк: McGraw-Hill Medical, 2011.
.Мэрилендский университет неотложной медицины: трубная торакостомия
Обнаружение гемоторакса в реальном времени и мониторинг его развития на модели поросенка с помощью электроимпедансной томографии: технико-экономическое обоснование
Гемоторакс — серьезное заболевание, которое может быть опасным для жизни, если его не лечить.Ранняя диагностика и своевременное лечение имеют большое значение для благоприятного исхода. Хотя доступные в настоящее время диагностические методы, например рентгенография грудной клетки, ультрасонография и КТ, могут точно обнаружить гемоторакс, отсроченный гемоторакс не может быть идентифицирован на ранней стадии, поскольку эти обследования часто проводятся у пациентов до появления заметных симптомов. Следовательно, для раннего обнаружения отсроченного гемоторакса необходим мониторинг в реальном времени с помощью портативных неинвазивных методов визуализации.В этом исследовании мы использовали электроимпедансную томографию (EIT) для обнаружения начала гемоторакса в реальном времени на восьми моделях гемоторакса поросят. Модели были созданы путем инъекции 60 мл свежей аутологичной крови в плевральную полость, и последующее развитие гемоторакса контролировалось непрерывно. Результаты показали, что EIT смогла чувствительно обнаружить гемоторакс объемом до 10 мл, а также его локализацию. Кроме того, развитие гемоторакса в диапазоне от 10 мл до 60 мл хорошо отслеживалось в режиме реального времени с благоприятной линейной зависимостью между изменением импеданса на изображениях EIT и объемом введенной крови.Эти результаты продемонстрировали, что EIT обладает уникальным потенциалом для ранней диагностики и постоянного мониторинга гемоторакса в клинической практике, предоставляя медицинскому персоналу ценную информацию для быстрого выявления и лечения отсроченного гемоторакса.
1. Введение
Гемоторакс — серьезное заболевание, характеризующееся скоплением крови в плевральной полости [1, 2]. Это частое последствие открытой или закрытой травмы грудной клетки, которая встречается примерно в 60% всех случаев политравмы и является второй по частоте травмой [3, 4].Хотя сообщается, что 25% смертей от травм произошло из-за травм грудной клетки, гемоторакс является потенциально смертельной причиной с высокой смертностью [5–7]. Гемоторакс может быть опасен, если его не лечить. Длительная задержка крови в плевральном пространстве может первоначально иметь фиброзную реакцию, которая препятствует адекватному расширению легких, что приводит к ателектазу и несоответствию вентиляции / перфузии [8, 9]. Более того, задержанная кровь также может быть загрязнена бактериями и вызывать эмпиему (даже бактериемию и септический шок) [10, 11].Однако клинические исследования показывают, что раннее выявление и лечение гемоторакса, такое как остановка кровотечения и удаление гематомы из плевральной полости, могут дать явно благоприятный результат [12–14]. Поэтому раннее выявление и своевременное лечение гемоторакса имеют первостепенное значение для улучшения прогноза пациентов.
По времени возникновения гемоторакс можно разделить на острые и отсроченные. В остром случае гемоторакс можно легко идентифицировать на рентгенограмме грудной клетки в вертикальном положении, ультразвуковом исследовании или компьютерной томографии сразу после травмы или во время госпитализации [14].Однако в отсроченном случае, особенно при закрытом травматическом состоянии, современные методы визуализации не могут легко зафиксировать начальное кровотечение в плевральной полости. Это связано с тем, что гемоторакс может возникнуть только через несколько часов или даже дней после травмы, и эти обследования часто проводят до тех пор, пока у пациентов не появятся заметные симптомы [15, 16], включая боль в груди и затрудненное дыхание [14, 17]. При слишком позднем лечении отсроченный массивный гемоторакс может быть опасным для жизни [13, 18]. Следовательно, для пациентов с факторами высокого риска отсроченного гемоторакса, такими как множественные переломы или переломы ребер со смещением [19, 20], портативное, неинвазивное и безрадиационное медицинское устройство крайне необходимо для долгосрочного мониторинга в реальном времени. гемоторакса для раннего выявления [21].
Электроимпедансная томография (EIT), относительно новая технология компьютерной томографии, может создавать изображения поперечного сечения распределения электрического импеданса внутри человеческого тела. В EIT безопасные электрические токи вводятся в тело человека, чтобы вызвать граничные напряжения, которые возникают из внутренних тканей тела и измеряются через массив поверхностных электродов, прикрепленных к выбранной области изображения, такой как грудная клетка. Затем изображения EIT восстанавливаются по измеренным граничным напряжениям с использованием определенного алгоритма восстановления изображения [22].По сравнению с рентгеном, ультрасонографией и КТ, EIT имеет преимущества небольшого размера, низкой стоимости, неинвазивности, отсутствия излучения и высокого временного разрешения, что делает его многообещающим методом визуализации во многих биомедицинских приложениях, особенно при мониторинге в реальном времени. [23]. До настоящего времени ЭИТ широко изучалась с точки зрения применения мониторинга вентиляции и перфузии легких [24–27]. Кроме того, из-за значительной разницы в электрическом импедансе между кровью и другими тканями человека [28, 29], EIT имеет большой потенциал в долгосрочном и непрерывном обнаружении возникновения и прогрессирования внутреннего кровотечения в органах человека, включая гемоторакс. .
На сегодняшний день в нескольких исследованиях сообщается об оценке осуществимости использования EIT для мониторинга внутреннего кровотечения в режиме реального времени. Xu et al., Manwaring et al., Dowrick et al., Sadleir et al. И Dai et al. установили различные модели внутричерепных кровоизлияний (ICH) на животных, включая внутрипаренхимальное кровоизлияние (IPH), субарахноидальное кровоизлияние (SAH) и внутрижелудочковое кровоизлияние (IVH). Они обнаружили, что EIT может точно отражать изменение импеданса в реальном времени, вызванное ICH, даже несмотря на то, что объем крови был намного меньше, чем объем мозга, как в случае модели IPH свиньи с инъекцией 5 мл крови [30–34] .Более того, Shuai et al. исследовали способность EIT контролировать внутрибрюшинное кровоизлияние на модели свиньи и наблюдали, что изменения внутрибрюшинного объема крови можно постоянно идентифицировать, наблюдая изображения EIT на протяжении всего кровотечения [35]. В другом исследовании You et al. успешно применили EIT для динамического мониторинга забрюшинного кровотечения у пациента с травмой почек в течение 9 часов [36]. Вкратце, предыдущие исследования показали, что ЭИТ имеет уникальные преимущества в долгосрочном и непрерывном мониторинге внутреннего кровотечения в различных органах.Однако, насколько нам известно, нет исследований, в которых оценивалась бы возможность непрерывного мониторинга гемоторакса с помощью EIT.
Соответственно, в этом исследовании мы впервые создали модели гемоторакса путем инъекции собственной крови в плевральную полость свиней. Во-вторых, данные EIT легких непрерывно собирались на протяжении всего курса инъекции крови перед обработкой с помощью метода цифровой фильтрации для получения независимого изменения импеданса, вызванного гемотораксом, для реконструкции изображения EIT.Наконец, мы количественно проанализировали взаимосвязь между изменением импеданса, отраженным изображениями EIT, и объемом инъекции крови.
2. Материалы и методы
2.1. Подготовка животных
Все эксперименты в этом исследовании были одобрены институциональными комитетами по уходу и использованию животных Медицинского университета ВВС, Сиань, Шэньси, Китай.
Восемь поросят в возрасте 2 месяцев (вес; четыре самки и четыре самца) были получены из центра экспериментальных животных и выращены на месте.Во избежание обратного потока пищи в желудок, блокирующего дыхательные пути после анестезии, поросят лишали пищи и воды на 12 ч перед экспериментальными процедурами. Все эксперименты проводились при относительно стабильной температуре окружающей среды (), а внутреннюю температуру животных измеряли с помощью ректального термисторного зонда. Первоначально пациенты были анестезированы внутримышечной инъекцией атропина (0,05 мг / кг) для уменьшения респираторной секреции. После седации пентобарбитал вводили внутрибрюшинно (30 мг / кг) для достижения глубокого уровня анестезии для дальнейших хирургических процедур.Панкуроний использовали для поддержания мышечного паралича (0,2 мг / кг, повторяющиеся 0,1 мг / кг). Затем кожу грудной клетки в пределах 15 см позади передних конечностей поросят брили и очищали, чтобы подготовить электроды для крепления EIT.
Для обеспечения нормального дыхания поросят на протяжении всего эксперимента использовали вентилятор для животных. Процедуры интубации трахеи следующие: сначала поросят фиксировали в положении лежа на спине так, чтобы голова и шея были ниже туловища; Затем с помощью ларингоскопа брали язык поросят и надгортанник, чтобы найти отверстие трахеи.Во-вторых, во время ингаляции в трахею вводили трахеальную канюлю на глубину примерно 20-25 см, и интубация трахеи считалась успешной, если появлялся туман. После этого поросята фиксировали в положении лежа. Параметры вентилятора были установлены на частоту дыхания 25 ударов / мин и дыхательный объем 10 мл / кг.
2.2. Создание модели гемоторакса
Для создания модели гемоторакса использовали инъекцию аутологичной крови.Для приготовления инъекции крови из бедренной артерии с помощью шприца на 100 мл забирали 80 мл крови, в которую заранее аспирировали гепарин для предотвращения свертывания крови. Затем 60 мл гепаринизированной крови аспирировали в другой шприц на 100 мл, подсоединенный к пункционной игле через дренажную трубку, которая была прикреплена к микроинъекционному насосу (AT-5803), работающему со скоростью 600 мл / ч. С помощью скальпеля осторожно сделали небольшой разрез (длиной около 0,5 см) между пятым и шестым ребрами, не повредив париетальную плевру (рис. 1).Что касается торакального закрытого дренажа, пункционная игла медленно вводилась через разрез до такой степени, когда было четкое ощущение прорыва, что указывало на попадание пункционной иглы в плевральную полость. Была применена пара гемостатических щипцов, чтобы быстро остановить кровотечение, и использовался вазелиновый уплотнитель для предотвращения утечки воздуха. Наконец, был активирован микроинъекционный насос, чтобы обеспечить непрерывное впрыскивание крови.
2.3. Системный протокол EIT
2.3.1. Применение электродов EIT
Система электродов EIT состояла из 16 одноразовых электродов Ag + / Ag + Cl− (Shanghai Shenfeng Medical & Health Articles Co., Ltd., Шанхай, Китайская Народная Республика) диаметром 10 мм. После того, как сбритая кожа всех поросят была очищена спиртом, электроды прикрепляли к коже на 5 см выше мечевидного отростка, на равном расстоянии от грудной клетки. Для повышения устойчивости электродов использовалась самоклеящаяся повязка (McDavid-4575, Bellwood, США) длиной 1.Для двойного обертывания вокруг грудной клетки использовалась 5-кратная окружность грудной клетки (рис. 2).
2.3.2. Сбор данных EIT
Сбор данных EIT был выполнен с использованием портативной системы EIT (PEIT4) с высокой точностью, а также высокой скоростью сбора данных. Система специально разработана нашей группой для визуализации легких, которая может постоянно работать на частоте 100 кГц и выходном токе 1 мА. Точность измерения лучше 1 ‰, а скорость сбора данных может достигать 12 кадров / с [37].Несмотря на небольшой объем (), эта система может непрерывно работать более 10 часов от литиевой батареи. Для повышения чувствительности к изменениям импеданса, вызванного центральными областями легких, и поддержания хорошего отношения сигнал / шум, протокол измерения, прилегающий к противоположному возбуждению, был принят при сборе данных EIT [38].
Для сравнения данных была получена контрольная группа, состоящая из данных EIT, полученных за 5 минут до инъекции крови, и соответствующих реконструированных изображений.После начала инъекции крови данные EIT непрерывно собирались в течение более 6 мин (рис. 3).
2.3.3. Обработка данных EIT
Данные EIT непрерывно собирались во время нормального дыхания субъектов на протяжении всего процесса инъекции крови. Следовательно, данные EIT отражали изменение импеданса, вызванное как инъекцией крови, так и нормальным дыханием. Чтобы проанализировать взаимосвязь между данными EIT и инъекцией крови, мы использовали технологию цифровой фильтрации для получения независимого изменения импеданса, вызванного инъекцией крови, на основании того факта, что дыхание имело очевидную периодичность, а инъекция крови — нет.Этапы обработки данных EIT были следующими: Сначала были рассчитаны спектры мощности граничных напряжений всех каналов (эти граничные напряжения составляли данные EIT), соответственно. Во-вторых, фильтр Баттерворта нижних частот 4-го порядка с граничной частотой полосы заграждения 0,15 Гц был разработан и использован для обработки данных EIT для получения независимого сигнала инъекции крови, поскольку частота, соответствующая дыханию, составляла примерно 0,4 Гц (частота вентилятора был установлен на 25 ударов в минуту).В-третьих, независимый сигнал, соответствующий дыханию, может быть получен путем вычитания независимого сигнала инъекции крови из необработанных данных EIT.
Для демонстрации изменений данных EIT использовалось общее изменение граничного напряжения (TBVV), которое было рассчитано по следующей формуле: где и обозначают полное граничное напряжение (TBV) в момент времени и контрольный момент времени. — граничное напряжение пары измерительных электродов, когда через пару электродов возбуждается ток.На практике разница напряжений, вызванная импедансом контакта электрода с кожей, намного больше, чем разность напряжений, вызванная импедансом внутренней ткани тела [39]. Более того, контактный импеданс часто изменяется со временем из-за различных неизбежных факторов, таких как потоотделение, изменение температуры, движения пациента и манипуляции со стороны медицинского персонала [40]. Кроме того, трудно точно измерить сопротивление контакта электродов с кожей возбуждающих электродов [41]. Таким образом, измеренные напряжения вычитаются, когда они измеряются на парах электродов, которые составляют один из возбуждающих электродов, т.е.е.,.
2.3.4. EIT Image Reconstruction
EIT разностные изображения были реконструированы с помощью алгоритма затухающих наименьших квадратов (DLS), эффективность которого для мониторинга внутреннего кровотечения была подтверждена в экспериментах на животных и людях [42]. Матрица реконструкции была рассчитана на основе двумерной круговой модели с равномерным распределением электрического импеданса и сохранена заранее. Процесс восстановления изображения был следующим: где представляет вектор изменения импеданса (изображение) между двумя моментами времени, — это линеаризованная матрица чувствительности, обозначает матрицу регуляризации, которая вычисляется на основе предположения о гладкости [43], — это параметр регуляризации, который обычно вычисляется с использованием L-кривой метод (здесь), является матрицей восстановления и является вектором изменения напряжения на границе между двумя моментами времени.где — граничное напряжение в контрольной точке времени и представляет граничное напряжение, полученное в другой момент времени.
2.4. Анализ данных EIT
Чтобы количественно проанализировать изменение импеданса в изображениях EIT в результате pH, мы использовали региональное изменение импеданса (RIV), которое измеряло степень изменения импеданса области, в которую была введена кровь. RIV рассчитывается следующим образом: где представляет собой область инъекции крови; и — восстановленный импеданс и площадь th элемента в области инъекции крови, соответственно, представляющие площадь th элемента во всей области визуализации; и и обозначают количество конечных элементов в области инъекции крови и общее количество конечных элементов во всей области визуализации.
Для определения области инъекции крови на реконструированном изображении использовалась стратегия порогового значения. Прежде всего, максимальное восстановленное значение было найдено путем сравнения восстановленных значений всех конечных элементов на изображениях EIT. Впоследствии область, состоящая из всех конечных элементов с восстановленным значением более 10%, считалась областью, в которую вводилась кровь.
В этом исследовании для проведения статистического анализа использовалась программа IBM SPSS Statistics для Windows (версия 22; IBM Corporation, Армонк, Нью-Йорк, США).Сравнение разницы в RIV за 5 мин до инъекции крови и после введения 10 мл, 20 мл, 30 мл, 40 мл, 50 мл и 60 мл крови проводили с помощью однофакторного дисперсионного анализа (ANOVA). Использовался апостериорный тест, который был признан статистически значимым.
Кроме того, для изучения взаимосвязи между изменением импеданса и инъекцией крови был проведен линейный регрессионный анализ между RIV и временем (а именно, количеством введенной крови) как для отдельных субъектов, так и для объединенных данных.
2,5. Валидация модели Hemothorax
После завершения эксперимента поросенка умерщвляли введением передозировки пентобарбитала. В соответствии с положением пункционной иглы небольшой разрез (длиной 0,5 см), сделанный для введения пункционной иглы, был дополнительно увеличен, чтобы обнажить плевральную полость в месте инъекции крови. Это позволяет нам непосредственно наблюдать за распределением введенной крови.
3. Результаты
Во время всех экспериментов испытуемые поддерживали стабильное дыхание и температуру тела.Во время проверки модели гемоторакса на одном животном мы обнаружили, что кровь вводилась в легочную ткань; поэтому было добавлено еще одно животное. Было успешно собрано восемь наборов данных EIT.
3.1. Модель Hemothorax
На рис. 4 (а) показана линия разреза, по которой обнажалась плевральная полость. Рисунок 4 (b) показывает, что кровь была обнаружена в плевральной полости, что указывает на то, что модель гемоторакса была успешно создана.
3.2. Визуализация EIT в нормальном дыхательном круге
На рисунке 5 показаны граничное напряжение и изображения EIT в нормальном дыхательном круге.Как показано на Рисунке 5 (а), TBVV постепенно увеличивалось во время вдоха и уменьшалось во время выдоха. Точно так же импеданс в области легких постепенно увеличивался во время вдоха и уменьшался во время выдоха, что отражено на изображениях EIT, показанных на рисунке 5 (b). Эти результаты подтвердили надежность и точность системы EIT, использованной в этом исследовании.
3.3. Разделение респираторного импеданса и импеданса инъекции крови посредством фильтрации
На рисунке 6 показана процедура разделения импеданса, вызванного инъекцией крови, от импеданса, вызванного дыханием.Как показано на Рисунке 6 (a), при использовании данных EIT в конце выдоха в качестве опорной рамки изменение импеданса, вызванное инъекцией крови, постепенно перекрывалось изменением импеданса в результате вдоха на изображениях EIT. Кроме того, TBV не только изменяется с дыханием, но также снижается с увеличением объема вводимой крови. Из спектров мощности TBV видно, что TBV содержит два основных фактора, один из которых — сигнал с частотой 0,4 Гц, соответствующий частоте дыхания (25 ударов в минуту), а другой — сигнал ниже 0.1 Гц соответствует скорости введения крови (если инъекция крови считалась сигналом, который менялся очень медленно).
Рисунок 6 (b) показывает, что после фильтрации через фильтр Баттерворта нижних частот 4-го порядка с частотой среза 0,15 Гц на изображениях EIT отображалось только изменение импеданса, вызванное инъекцией крови. Более того, кривая, представляющая TBV, также показывает прямую и исключительную корреляцию с инъекцией крови во времени, что, опять же, демонстрируют спектры мощности.
На рис. 6 (c) показаны независимые TBV и спектры мощности, соответствующие дыханию, которые были получены путем вычитания TBV, вызванного инъекцией крови, из необработанного TBV.
3.4. EIT-изображение процедуры инъекции крови
На рисунке 7 (a) показано изменение изображений EIT за 5 минут до инъекции крови, а также во время всего курса инъекции крови для всех восьми поросят. В целом тенденция изменения импеданса для всех поросят одинакова. Перед инъекцией крови не наблюдалось значительного изменения импеданса.После введения 10 мл крови сопротивление области инъекции уменьшилось. По мере увеличения количества крови изменение импеданса постепенно становилось очевидным, показывая возрастающую величину изменения импеданса и увеличивающуюся площадь. После завершения инъекции крови (60 мл крови) изменение импеданса достигло максимума с наибольшей амплитудой и наибольшей площадью. Однако степень изменения импеданса у всех испытуемых была разной, показывая различные амплитуды (обозначенные цветными полосами) и различные области.
Рисунок 7 (b) определяет области интереса, в которые вводилась кровь для всех субъектов, по которым были рассчитаны вариации регионального импеданса (RIV), вызванные инъекцией крови.
На рисунке 7 (c) значительную разницу в RIV можно наблюдать после того, как было введено только 10 мл крови, сравнивая RIV за 5 минут до инъекции крови (()) с RIV в течение 1 минуты после инъекции крови (-, ). Кроме того, при введении большего количества крови (20 мл, 30 мл, 40 мл, 50 мл и 60 мл) RIV также показали значительное отличие от RIV до инъекции крови ().
Как показано на Рисунке 7 (d) и Таблице 1, линейная регрессия показывает, что RIV благоприятно предсказал объем инъекции крови для каждого поросенка с диапазоном коэффициентов детерминации 0,947-0,995 (). Это было аналогично для объединенных данных от всех восьми поросят (;).
Тема Коэффициент детерминации () Коэффициент регрессии
P1 .1145947 —-2 -4 P2 0,955 —-2 -4 40 -6 P4 0,978 — -2 -5 P5 0,995 840 94011745 1745 –45 П6 0.976 —-2 -5 P7 0,980 —-2 -5 — -7 Объединенные данные 0,669 —-2 -14
40 4.1. Краткое изложение и объяснение результатов
В клинической практике очень важна разработка новых методов раннего выявления отсроченного гемоторакса для получения благоприятных результатов, поскольку современные методы медицинской визуализации, такие как рентгенография грудной клетки, КТ и Ультрасонография, не может выполнять долгосрочное наблюдение в режиме реального времени за пациентами с травмой грудной клетки с высоким риском отсроченного гемоторакса. В этом исследовании мы изучили возможность использования EIT для обнаружения гемоторакса на модели животных.Результаты показали, что EIT смогла точно идентифицировать гемоторакс объемом всего 10 мл и его местоположение. Кроме того, EIT могла проводить мониторинг развития гемоторакса в реальном времени (от 10 мл до 60 мл) на основе желаемой линейной зависимости между изменением импеданса на изображениях EIT и объемом введенной крови.
Во всех экспериментах мы непрерывно собирали данные EIT в течение 11 минут, включая 5 минут до инъекции крови и 6 минут до инъекции крови.В течение первых 5 минут не было значительного изменения импеданса на изображениях EIT для всех субъектов (рисунок 7 (a)), а RIV показал, что импеданс в области инъекции крови не показал значительных изменений по сравнению с таковым после инъекции крови ( Рисунок 7 (в)). Эти результаты демонстрируют надежность системы EIT, использованной в этом исследовании. В течение следующих 6 минут сопротивление в области инъекции крови постепенно уменьшалось по мере того, как было введено больше крови, из-за того, что электрическое сопротивление крови (1.43 Ом · м) намного ниже, чем у тканей легких, например, спущенного легкого (3,82 Ом · м) и раздутого легкого (9,74 Ом · м) [44]. Эти результаты в значительной степени согласуются с отчетами Hahn et al., В которых EIT использовалась для регистрации изменения импеданса в модели гемоторакса свиньи, установленного путем инъекции раствора Рингера в плевральную полость поросят [45]. Кроме того, средний TBV в результате инъекции крови увеличился на 0,86–1,52% во время процесса, что еще раз демонстрирует возможность и высокую чувствительность EIT для выявления гемоторакса.
При анализе изображений EIT мы использовали индекс, называемый RIV, для оценки взаимосвязи между изменением импеданса и инъекцией крови. Для каждого субъекта RIV уменьшался почти линейно при непрерывном введении крови () и значительно коррелировал с объемом крови (). Более того, для всех субъектов может быть до 0,669, что дополнительно демонстрирует благоприятную линейную коррекцию между изменением импеданса и объемом крови. Таким образом, RIV можно рассматривать как чувствительный и практичный показатель, отражающий развитие гемоторакса.Ожидается, что в будущей работе будет найдено больше показателей для изображений EIT, помимо RIV, чтобы сформировать разумную систему индексов для всесторонней количественной оценки инъекции крови.
4.2. Технические соображения и ограничения
В этом исследовании мы собрали данные EIT для каждого субъекта в течение двух периодов времени, которые составляли 6 минут после инъекции крови и 5 минут до этого курса. На протяжении всего процесса сбора данных животное продолжало нормально дышать. Таким образом, полученные данные EIT содержат информацию об импедансе как для дыхания, так и для инъекции крови.Чтобы количественно проанализировать изменение импеданса, вызванное исключительно инъекцией крови, мы разработали цифровой фильтр нижних частот 4-го порядка для разделения двух видов изменения импеданса, учитывая значительную периодичность дыхания, отличную от инъекции крови. Наши результаты говорят о том, что разработанный нами цифровой фильтр действителен. Точно так же в области исследования EIT легких уже было приложено много усилий для разделения различных видов сигналов, таких как сердечные и дыхательные сигналы. Например, Deibele et al.предложил метод, основанный на анализе основных компонентов (PCA-) для разделения респираторных и связанных с перфузией сигналов, в котором функции шаблона для легочного и сердечного компонентов, генерируемых PCA и фильтрацией в частотной области, были включены во входные сигналы [46]. Рахман и др. использовали независимый компонентный анализ (ICA) для определения изменения импеданса как сердечного, так и респираторного характера у субъектов со спонтанным дыханием [47]. В будущем мы сравним эти ранее предложенные методы с методом цифровой фильтрации при извлечении информации об импедансе, связанной с дыханием и гемотораксом (посредством инъекции крови).
В данном исследовании модель реконструкции, которую мы использовали, не идеальна. Во-первых, мы использовали круговую модель с однородным распределением импеданса, чтобы упростить грудную клетку поросят, потому что не были собраны изображения КТ или МРТ грудной клетки всех животных. Эта неточность модели реконструкции должна была вызвать некоторые ошибки в реконструированных изображениях, включая ошибки положения и формы аномалии (кровоизлияния), хотя наши результаты предполагают, что изображения EIT способны точно отражать прогрессирование инъекции крови [48].Во-вторых, поскольку токи протекают в трехмерном пространственном распределении, используемая нами модель двумерной реконструкции также может приводить к ошибкам местоположения и формы, даже если изображения 2D EIT могут отражать информацию об импедансе вблизи плоскости электродов. Эти ошибки визуализации могут иметь определенное влияние на количественный анализ изображений EIT, что неблагоприятно для будущих клинических приложений [49]. Следовательно, будущие работы, особенно эксперименты на людях, необходимы для создания индивидуальной трехмерной модели реконструкции грудной клетки, чтобы уменьшить ошибку визуализации и улучшить качество изображений EIT у пациентов, что может быть достигнуто путем включения точной геометрии и реалистичного распределения импеданса грудной клетки в алгоритм реконструкции изображений на основе изображений КТ или МРТ пациентов.
Чтобы создать воспроизводимую модель гемоторакса на животных, аутологичная кровь обрабатывалась гепарином для предотвращения коагуляции перед инъекцией в плевральную полость. Таким образом, существует разница между установленной моделью гемоторакса и фактическим гемотораксом. Однако наши результаты показали, что EIT может отслеживать изменения крови в плевральном пространстве, что демонстрирует возможность использования EIT для обнаружения гемоторакса в реальном времени. В будущем мы усовершенствуем модель на животных, вводя в плевральную полость неантикоагулированную аутологичную кровь и дополнительно проверяя способность EIT непрерывно контролировать гемоторакс.
4.3. Перспективы будущего клинического применения
Модель гемоторакса на животных была создана в настоящем исследовании путем инъекции крови в плевральную полость легких поросят в течение относительно короткого периода времени (6 минут), а условия эксперимента строго контролировались во всех случаях. случаи. Таким образом, были сведены к минимуму значительные факторы, влияющие на качество собранных данных EIT. С другой стороны, данные EIT в основном отражают изменения импеданса, вызванные дыханием животных и инъекцией крови.Однако в практических клинических случаях часто требуется, чтобы мониторинг в реальном времени осуществлялся в течение длительного периода времени, чтобы вовремя обнаружить отсроченный гемоторакс. Это будет оказывать множество сложных влияний на данные EIT, например, потливость или изменение температуры, приводящие к изменению импеданса контакта электрода с кожей [40], а также перемещение пациента или манипуляции со стороны клинического персонала, приводящие к искаженным измерениям данных [50]. Эти фактические факторы серьезно снизят качество данных EIT.Соответственно, крайне важно изучить соответствующие методы для улучшения качества данных, прежде чем переходить к клиническим применениям для обнаружения гемоторакса.
Во время длительного мониторинга часто могут возникать пот, изменения температуры и влажности на границе раздела электрод-проводящий гель-кожа, дрейф электроники и изменение контакта электрода, которые неизбежно вызывают изменение импеданса контакта электрод-кожа [51] . К сожалению, даже небольшое изменение импеданса контакта электрода с кожей, очевидно, может повлиять на точность измеренных данных EIT, вызывая значительные артефакты на изображениях EIT.Это связано с тем, что и возбуждение тока, и измерение граничного напряжения выполняются через поверхность раздела электрод-кожа [52]. До сих пор импеданс контакта электрода с кожей был основным фактором, влияющим на качество данных и изображения EIT при длительном мониторинге с использованием EIT. Чтобы уменьшить влияние контактного импеданса, были предложены некоторые новые алгоритмы реконструкции с полной моделью электрода (CEM), в которых контактный импеданс вводится в реконструкцию изображения в попытке одновременно восстановить как контактное сопротивление, так и внутреннее сопротивление. сопротивление человеческого тела.Boverman et al. использовали линейно-алгебраические методы при решении обратной задачи для восстановления изменяющегося во времени контактного импеданса и внутреннего импеданса [53]. Демиденко попытался отдельно оценить контактный импеданс, опираясь на аналитическое решение с матрицей Неймана-Дирихле [54]. Tarvainen et al. сформулировал реконструкцию изображения EIT как одну из байесовских оценок для вычисления контактного импеданса [55]. Эксперименты, соответствующие указанным выше алгоритмам, показали возможность значительного уменьшения влияния контактного импеданса.Кроме того, Ян и др. сравнили временные характеристики контактного импеданса 16 комбинаций (включая 4 вида клинических электродов и пять типов обычно используемых проводящих гелей) на десяти добровольцах, чтобы найти оптимальную комбинацию для долгосрочного мониторинга. Их результаты показали, что комбинация порошкового электрода Ag + / Ag + Cl- и проводящего геля с низкой вязкостью может быть лучшим выбором [56]. Поэтому в будущих клинических исследованиях по обнаружению гемоторакса следует применять несколько методов для минимизации воздействия контактного импеданса на изображения EIT, включая использование определенных алгоритмов реконструкции изображения и выбор конкретного электрода и проводящего геля.
Помехи движению тела из-за движений пациента или манипуляций со стороны медицинского персонала являются обычным явлением при длительном мониторинге EIT в клинических условиях. Это может вызвать перемещение электрода и полное или частичное отключение электродов, что приведет к изменению данных измерений и даже значительной потере данных. Чтобы уменьшить помехи движению тела, были разработаны специальные алгоритмы реконструкции изображений и методы предварительной обработки данных. Что касается перемещения электродов, Soleimani et al. разработали новый подход, в котором реконструировались как движения электродов, так и изменение внутреннего импеданса, и результаты показали резкое уменьшение артефактов изображения, вызванных движением электрода, а также хорошую реконструкцию фактического движения электрода [57].Кроме того, в случае полного отключения электродов Zhang et al. недавно разработал метод взвешенного коэффициента корреляции для тестирования нескольких проблемных электродов и использовал данные из предсказаний модели Грея для компенсирующей обработки [58]. Впоследствии для частичного отключения электродов Zhang et al. предложил онлайн-стратегию, основанную на вейвлет-разложении, для управления данными EIT от частично связанных электродов [59]. Следовательно, в будущем предлагается использовать подходы, включающие специальный алгоритм изображения и метод предварительной обработки данных для уменьшения влияния помех движений тела в клинических приложениях EIT для обнаружения отложенного гемоторакса.
4.4. Значение для клинического применения
В клинических условиях накопление патологической жидкости в плевральной полости является обычным симптомом и серьезно влияет на легочную вентиляцию. Таким образом, оценка воздействия EIT имеет большое значение, и этот вопрос исследуется в нескольких текущих исследованиях. Кэмпбелл и др. наблюдали увеличение удельного электрического сопротивления на пораженной стороне грудной клетки у пациентов с односторонним плевральным выпотом из-за рака легких во время ступенчатой аспирации плеврального выпота [60].Арад и др. получили аналогичные результаты при обследовании пациентов с плевральной жидкостью до и после удаления плеврального выпота [61]. Кроме того, Alves et al. использовали EIT для оценки реаэрации легких, повторной вентиляции и синхронности вентилятора до и более чем через час после аспирации плевры [62]. Недавно Becher et al. пришли к выводу, что ЭИТ можно использовать для обнаружения плеврального выпота путем анализа противофазного импеданса между пациентами с плевральной жидкостью и без нее, а также путем сравнения импеданса до и после дренирования выпота [63].Предыдущие исследования полностью продемонстрировали надежность использования ЭИТ для контроля дренирования плеврального выпота, а именно уменьшения жидкости в плевральной полости. Напротив, в этом исследовании мы изучали возможность использования EIT для мониторинга развития гемоторакса, который, по сути, представляет собой увеличение жидкости в плевральной полости. Вкратце, это и предыдущие исследования продемонстрировали способность EIT обнаруживать изменение (уменьшение и увеличение) плевральной жидкости, подтверждая большой потенциал техники EIT для оценки патологического статуса и заболеваний, связанных с плевральной жидкостью.
5. Выводы
В этом исследовании мы изучили возможность и чувствительность использования техники EIT для раннего выявления и постоянного мониторинга развития гемоторакса на моделях гемоторакса поросят, полученных путем инъекции крови в плевральную полость. Для клинической практики необходимы более конкретные исследования, сфокусированные на использовании реалистичной трехмерной модели реконструкции грудной клетки, разработке алгоритмов реконструкции изображений и метода предварительной обработки данных. Несмотря на это, наши результаты в этом исследовании демонстрируют, что EIT обладает уникальным потенциалом для ранней диагностики и постоянного мониторинга гемоторакса у пациентов с факторами высокого риска, предоставляя медицинскому персоналу ценную информацию для быстрого выявления и лечения отсроченного гемоторакса.
Доступность данных
Данные, использованные для подтверждения выводов этого исследования, можно получить у соответствующего автора по запросу.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Вклад авторов
Линь Ян и Чао Чжан внесли равный вклад в эту работу. Благодарности
Осложнение, которое необходимо учитывать: отсроченный травматический гемоторакс у пожилых людей
Введение
Бремя травматических переломов ребер у пожилых пациентов хорошо известно. Гемоторакс (HTX) — частая сопутствующая травма с переломами ребер и обычно диагностируется во время обращения: очень маленькие гемотораксы редко требуют вмешательства, тогда как большие гемотораксы часто подвергаются немедленному дренированию. Тем не менее, новые данные свидетельствуют о том, что при использовании HTX у пожилых людей с переломами ребер может наблюдаться тонкий гемоторакс, который прогрессирует с задержкой в течение нескольких дней.1 2 Если это правда, пожилые люди могут подвергаться риску развития эмпиемы или других осложнений без тщательного наблюдения.
Отсроченное прогрессирование и отсроченное развитие травматического гемоторакса (dHTX) в литературе недостаточно охарактеризованы. Старение населения США и рост числа случаев переломов ребер среди пожилых людей подчеркивают острую необходимость в лучшем понимании этого вопроса3. В этом предварительном исследовании изучались пожилые люди с dHTX после глубоких переломов ребер, чтобы определить направление будущих исследований.Мы предположили, что dHTX будет редкостью, но связан с факторами, которые могут помочь в идентификации.
Методы
Популяция исследования
Мы ретроспективно рассмотрели взрослых людей в возрасте ≥50 лет с диагнозом dHTX после переломов ребер в двух травматологических центрах уровня 1 в период с марта 2018 г. по сентябрь 2019 г. Мы определили dHTX как HTX, обнаруженный через ≥48 часов после поступления КТ грудной клетки. либо нет, либо «минимальный / след» HTX. Мы определили пациентов, запросив журналы регистрации травм и электронные медицинские карты обоих центров для пациентов в возрасте ≥50 лет с переломами ребер и dHTX, диагностированными во время первичной госпитализации или при повторной госпитализации.
Переменные
Мы сообщаем характеристики пациента (возраст, пол, индекс массы тела, статус курения, индекс коморбидности Чарлсона, применение аспирина / антитромбоцитов / антикоагулянтов в течение 7 дней после травмы), характеристики травмы (механизм травмы, количество переломов ребер, свидетельство повреждения паренхимы легкого) и характеристики госпитализации (продолжительность пребывания в больнице (LOS), вмешательства и повторная госпитализация).
Подробная характеристика переломов ребер
Два слепых сертифицированных радиолога проанализировали все стационарные рентгеновские снимки грудной клетки и компьютерную томографию; Снимки каждого пациента были просмотрены одним из двух радиологов.Типы переломов ребер были охарактеризованы в соответствии с таксономией Общества по травмам грудной стенки (CWIS) 4. Таксономия CWIS была создана международной консенсусной группой Delphi и классифицирует переломы ребер на основе степени смещения (несмещение, смещение (<90% кортикального контакта), смещение ( без коркового контакта)), тип перелома (простой, клиновидный, сложный), переломы соседних ребер (серия, а не серия) и расположение грудной стенки (переднее, латеральное, заднее, реберное). Помимо переломов ребер, мы также отметили рентгенологическое повреждение легких (эмфизема мягких тканей грудной клетки, разрыв или ушиб легкого, пневмоторакс).
Результаты
Характеристики пациентов
Мы идентифицировали 14 пожилых людей, перенесших dHTX после переломов ребер, с общим уровнем dHTX 1,3%. У пяти пациентов (36%) было отсроченное прогрессирование следового HTX, а у девяти (64%) было отсроченное развитие HTX после отрицательного результата КТ. Средний возраст составлял 72 года, 86% (n = 12) составляли мужчины (таблица 1). 57% пациентов не принимали препараты для разжижения крови в течение недели до травмы; среди тех, кто принимал участие в исследовании, наиболее распространенным лекарством был аспирин (n = 4, 29%).Пациенты получали низкомолекулярный гепарин для стационарной химиопрофилактики венозной тромбоэмболии. Все пациенты в возрасте 65 лет и старше испытали падение с уровня земли, что является наиболее частым механизмом травм (n = 6, 43%), тогда как пациенты моложе 65 лет испытали более сильные травмы. Дополнительные онлайн-данные подробно описывают индивидуальные характеристики пациента.
Таблица 1Характеристики пациентов в возрасте ≥50 лет с диагнозом отсроченное прогрессирование гемоторакса после переломов ребер в двух учреждениях
Рентгенологические характеристики
Всем пациентам при поступлении была проведена КТ грудной клетки.Шесть пациентов (43%) имели основное повреждение легких. Среднее количество переломов ребер составило 5,8, и четыре пациента (29%) имели грудную клетку с цепом. Согласно таксономии CWIS, у всех пациентов была серия переломов, в среднем 5,6 последовательных перелома ребер. Только у трех пациентов было менее четырех последовательных переломов ребер: у этих пациентов было два последовательных перелома со смещением или с полным смещением. У всех пациентов был как минимум один перелом со смещением или смещением, в среднем 3,5 перелома со смещением или смещением.У всех пациентов были заднебоковые переломы и следующая картина перелома между 6-м и 10-м ребрами: серия заднебоковых переломов, по крайней мере, с одним переломом со смещением или смещением.
Характеристики госпитализации
Шесть пациентов (43%) были диагностированы с dHTX во время первичной госпитализации, но восемь (57%) не были диагностированы до повторной госпитализации. Пациентам был поставлен диагноз dHTX после того, как новая одышка или боль в груди вызвали повторную визуализацию. Отсроченный гемоторакс, обнаруженный при первичной госпитализации, в среднем диагностировали на 5 баллов.Через 3 дня (диапазон 3–8 дней) после приема; dHTX, обнаруженный при повторной госпитализации, диагностировался в среднем через 9,3 дня (диапазон 2–20 дней) после выписки из первичной госпитализации. Из девяти пациентов с профилями коагуляции, отправленных в день диагностики dHTX, у шести были нормальные значения; у трех пациентов были слегка повышенные международные нормализованные отношения (1,3–1,5). В общей сложности семь пациентов получили переливание крови.
Пациенты, которые в конечном итоге были повторно госпитализированы, имели более короткий начальный период LOS в больницу по сравнению с пациентами, которые не были повторно госпитализированы (среднее значение 6.3 против 18,5 дней). Повторно госпитализированные пациенты имели сходную LOS при первичной госпитализации (6,3 ± 1,6 дня) и повторной госпитализации (6,9 ± 1,0 дня). Всем пациентам была выполнена трубочная торакостомия для dHTX, а шести пациентам (42%) — все моложе 65 лет — были выполнены оперативные вмешательства, когда HTX сохранялась, несмотря на трубочную торакостомию. Ни у одного пациента не было эмпиемы.
Обсуждение
Наше предварительное исследование предполагает, что пожилые люди с переломами ребер могут иметь риск замедленного прогрессирования следов гемоторакса или отсроченного развития гемоторакса.Гемоторакс не был очевиден при первоначальной визуализации, рутинная последующая визуализация не была получена, а повторная визуализация выполнялась только при появлении симптомов (после выписки у многих пациентов, требующих длительных повторных госпитализаций). Позднее распознавание гемоторакса иногда требовало хирургического дренирования и декортикации. Пациенты в возрасте 50–64 лет с dHTX испытали более сильную травму и потребовали оперативного вмешательства, фенотип, потенциально отличающийся от фенотипа пациентов старше 65 лет, которые испытали падение с земли и получили лечение с помощью трубчатой торакостомии.
Пожилые люди с dHTX имели признаки серьезной травмы грудной стенки с ≥4 последовательными переломами или двумя переломами со смещением. Распространенной картиной травм была серия заднебоковых переломов со смещением или смещением между 6-м и 10-м ребрами. Анатомия грудной стенки объясняет, почему эта картина травм может быть связана с dHTX. По сравнению с переломами без смещения, переломы со смещением или смещением могут с большей вероятностью разорвать межреберные сосуды при продолжающемся дыхании, вызывая либо отложенное повреждение, либо разрушение сгустка.6–10-е ребра также являются самыми крупными ребрами, связанными с более длинными межреберными артериями, и имеют большую костную массу для разрушения подлежащих сосудов5. В отличие от плавающих (11-е и 12-е) или более черепных ребер, эти нижние ребра непосредственно участвуют в механике дыхания5; большее движение во время дыхания может представлять больший риск со временем повредить подлежащие межреберные артерии. Физиологическое значение сомнительно, но заднебоковые межреберные артерии получают кровь из аорты и больше, чем передние межреберные артерии, ответвляющиеся от внутренних артерий молочной железы.6 Более того, скорость кровотока наиболее высока в нижних межреберных артериях (шестой и каудальной) .7
Отсроченная травматическая HTX после переломов ребер у пожилых людей может быть неуловимым осложнением, которое требует более широкого признания. Осложнение было выявлено в амбулаторных условиях, но, насколько нам известно, в стационарных условиях его еще предстоит охарактеризовать.1 2 Как отсроченное прогрессирование (скудный уровень HTX при поступлении, который накапливается с течением времени), так и задержка развития (отсутствие HTX при обращении) могут быть в игре.Пациенты могут иметь обнадеживающую КТ грудной клетки при поступлении даже без скудного гемоторакса, но накапливаются значительные гемотораксы, которые требуют длительных повторных госпитализаций или оперативных вмешательств. Все пациенты, которые в конечном итоге были повторно госпитализированы, были выписаны домой после более короткой начальной госпитализации и имели симптомы в течение 20 дней после выписки — у пожилых людей со временем может незаметно накапливаться гемоторакс. Отсроченное обнаружение препятствует лечению гемоторакса с помощью зондовой торакостомии, потому что более старая кровь может свертываться или служить очагом эмпиемы.Если dHTX прогрессирует без симптомов, определение факторов риска, таких как типичная картина перелома ребер, может иметь решающее значение для упреждающего выявления пациентов с высоким риском. Для смягчения последствий повторной госпитализации и операций, которых можно избежать, пациентам из группы высокого риска может потребоваться целенаправленная последующая визуализация даже при отсутствии клинических симптомов.
Наше исследование предлагает предварительные результаты для направления будущих исследований и имеет несколько ограничений. Мы обследовали несколько пациентов и не смогли установить частоту dHTX. Это предварительное исследование было основано на анекдотических наблюдениях в двух травматологических центрах уровня 1, чтобы привлечь внимание к малоизученному и малоизученному осложнению среди пожилых людей, поступивших с переломами ребер.Во-вторых, в нашем исследовании были выявлены только пациенты, которые были повторно госпитализированы в наши собственные травматологические центры. Пациенты могли обращаться с dHTX в другие больницы после выписки. Более того, оба травматологических центра принимают большое количество пациентов с переломами ребер, и наши модели управления могут не отражать таковые в нетравматических или травматологических центрах меньшего объема. В-третьих, у нас нет окончательного физиологического объяснения того, почему у пожилых людей может наблюдаться замедленное прогрессирование или развитие гемоторакса. Насколько нам известно, не существует физиологической модели, подтверждающей нашу анатомическую гипотезу о том, что dHTX накапливается из смещенных ребер, разрушая нижележащие межреберные артерии во время движения дыхательной стенки грудной клетки.Физиологическое моделирование, вероятно, непрактично, но более широкое признание этого осложнения может облегчить проверку факторов риска с помощью мультиинституциональных оценок в будущем.
Смягчение последствий dHTX требует более масштабного исследования, чтобы лучше понять распространенность и подтвердить предложенные факторы риска. Исследование случай-контроль для дальнейшей оценки потенциальных факторов риска dHTX может быть полезным, но оно, вероятно, страдает от ошибки проверки. Проспективное когортное исследование необходимо для оценки характера травм и механизмов, которые предвещают повышенный риск dHTX.Также следует изучить взаимосвязь между dHTX и домашним разжижителем крови или дозированием для профилактики венозной тромбоэмболии, количественной оценкой объемов HTX грудной клетки при КТ для руководства лечением, а также роль хирургической стабилизации смещенных переломов ребер для снижения риска dHTX. Анализ рентабельности может определять время и метод целенаправленной последующей визуализации у бессимптомных пациентов.
Заключение
Отсроченное прогрессирование и замедленное развитие HTX у пожилых людей с переломами ребер требует более широкого признания.
- 37 неделя беременности развитие плода вес и рост: что происходит, норма веса ребенка, предвестники родов, УЗИ
- Зловонные выделения у женщин: Выделения с запахом у женщин в интимной зоне | причины неприятного запаха из влагалища
-

 (В редакции Постановления Правительства Российской Федерации от 26.08.2013 № 739)
(В редакции Постановления Правительства Российской Федерации от 26.08.2013 № 739) 02.2015 № 150)
02.2015 № 150) 02.2015 № 150)
02.2015 № 150)
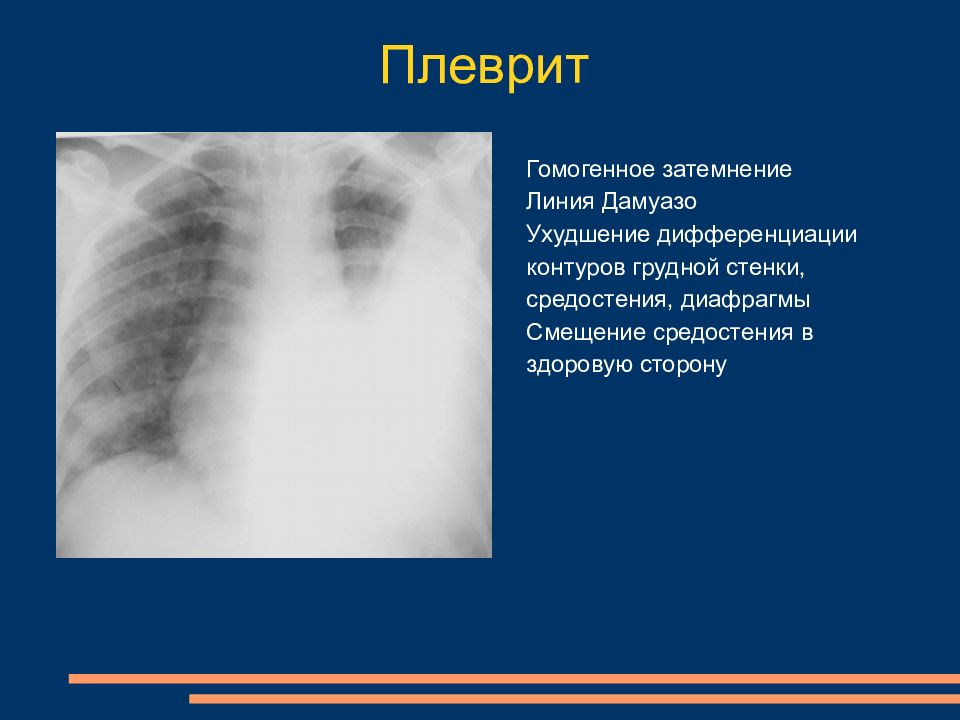 Проникающие ранения черепа без повреждения головного мозга, за исключением переломов костей черепа, учтенных при применении пунктов 1 и 2 настоящего приложения
Проникающие ранения черепа без повреждения головного мозга, за исключением переломов костей черепа, учтенных при применении пунктов 1 и 2 настоящего приложения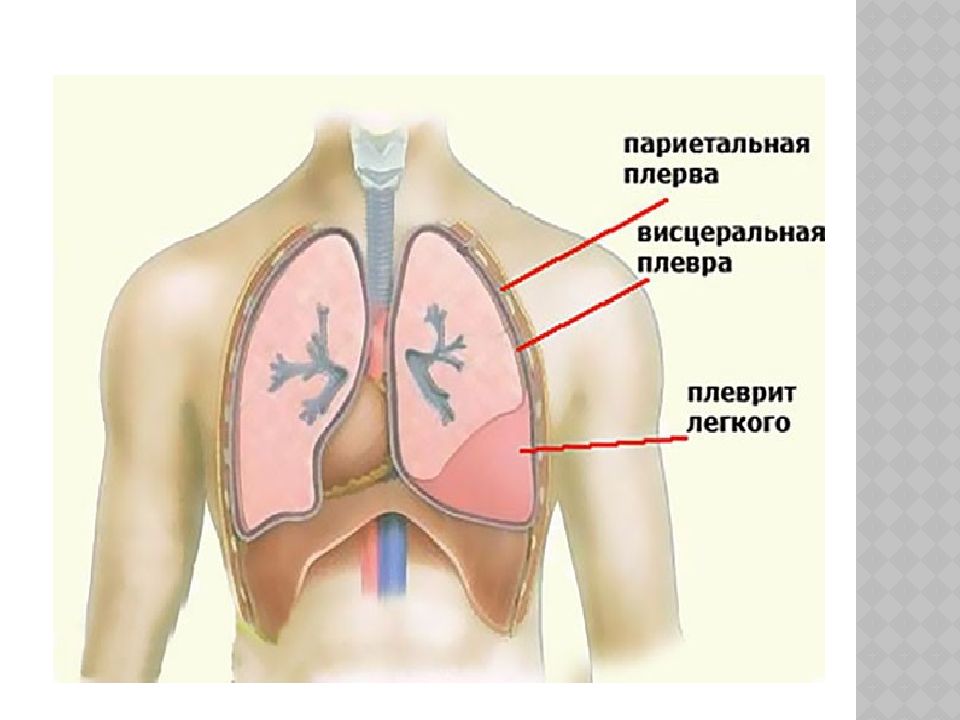 Повреждение спинного мозга на любом уровне, а также повреждение конского хвоста:
Повреждение спинного мозга на любом уровне, а также повреждение конского хвоста: Проникающее ранение позвоночника, за исключением повреждений позвоночника, учтенных при применении пункта 5 настоящего приложения
Проникающее ранение позвоночника, за исключением повреждений позвоночника, учтенных при применении пункта 5 настоящего приложения Повреждение легкого, проникающее ранение грудной клетки, повлекшее за собой гемоторакс, пневмоторакс, подкожную эмфизему, удаление легкого:
Повреждение легкого, проникающее ранение грудной клетки, повлекшее за собой гемоторакс, пневмоторакс, подкожную эмфизему, удаление легкого: Торакотомия по поводу одной травмы (независимо от их количества):
Торакотомия по поводу одной травмы (независимо от их количества):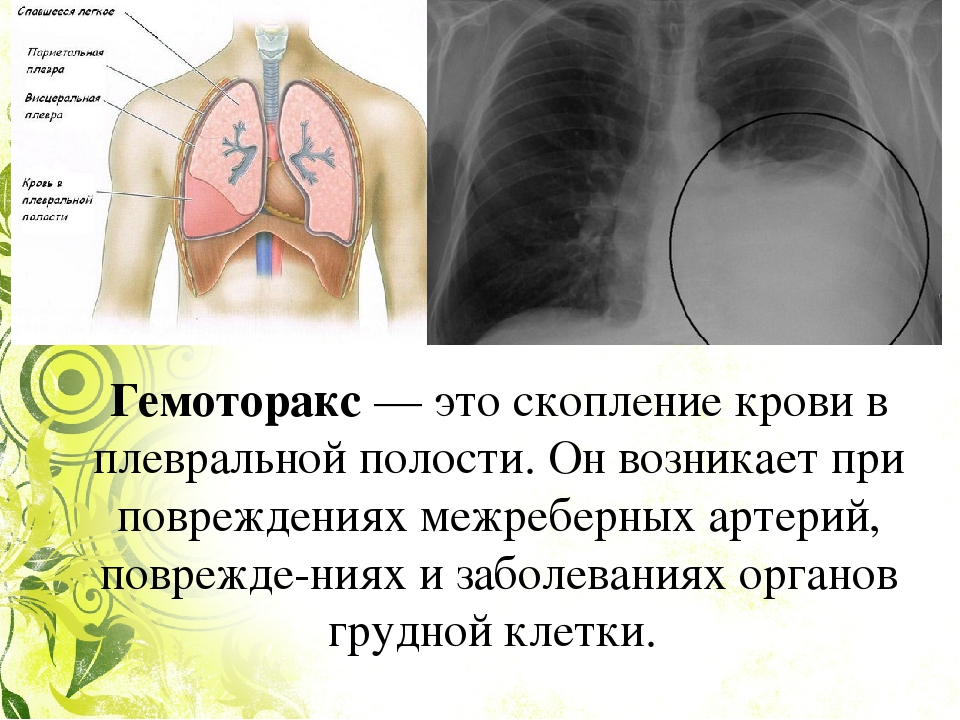 Повреждение сердца, его оболочек, аорты, легочной, безымянной, сонных артерий, внутренней яремной, верхней и нижней полых, воротной вен, их ветвей первого порядка, не указанных в пункте 24 настоящего приложения:
Повреждение сердца, его оболочек, аорты, легочной, безымянной, сонных артерий, внутренней яремной, верхней и нижней полых, воротной вен, их ветвей первого порядка, не указанных в пункте 24 настоящего приложения: Потеря зубов в результате травмы, в том числе полный вывих постоянных, не пораженных заболеваниями (пародонтозом, периодонтитом, кариесом и др.) зубов (не менее 2), включая сопутствующий перелом альвеолярного отростка4:
Потеря зубов в результате травмы, в том числе полный вывих постоянных, не пораженных заболеваниями (пародонтозом, периодонтитом, кариесом и др.) зубов (не менее 2), включая сопутствующий перелом альвеолярного отростка4: