Гипертензия внутрибрюшная: Внутрибрюшная гипертензия у больных тяжелым острым панкреатитом
Внутрибрюшная гипертензия у больных тяжелым острым панкреатитом
Введение
Показатель внутрибрюшного давления (ВБД) является важным фактором оценки тяжести состояния больных при различных ургентных хирургических заболеваниях, в том числе при остром панкреатите (ОП), его измерению и коррекции уделяют большое внимание [3, 4, 12, 22, 31, 35]. У взрослого человека ВБД, равное 5-7 мм рт.ст., считают нормальным. Более высокие значения ВБД расценивают как внутрибрюшную гипертензию (ВБГ). Выделяют [25] 4 степени повышения ВБГ (табл. 1).
Повышению ВБД у больных ОП способствуют следующие факторы: парез кишечника, компрессия двенадцатиперстной кишки, гастростаз, наличие свободной жидкости в брюшной полости и забрюшинном пространстве, ригидность передней брюшной стенки вследствие ее отека и неадекватной аналгезии. Повышенное ВБД приводит к ряду серьезных нарушений функции различных органов. Сдавление нижней полой вены с последующим уменьшением притока венозной крови к сердцу, снижение сердечного выброса при одновременном повышении периферического сосудистого сопротивления обусловливают нарушение микроциркуляции и перфузию тканей [7-9, 14, 20, 24].
Брюшное перфузионное давление (БПД) определяется разницей между средним артериальным давлением (АД) и ВБД. Считают, что для нормального функционирования органов брюшной полости и забрюшинного пространства БПД должно быть выше 60 мм рт.ст. [10, 11, 26].
ВБГ приводит к высокому стоянию купола диафрагмы, уменьшению легочного объема и альвеолярной вентиляции. При этом происходит сдавление лимфатических сосудов и скопление интерстициальной жидкости в легких. Повышение давления вдоха является причиной развития интерстициального отека легких, появления ателектазов и, как следствие, гипоксии и гиперкапнии [18, 29], легочной недостаточности. Искусственная вентиляция легких в таких условиях может приводить к баротравме и развитию респираторного дистресс-синдрома.
Влияние ВБГ на мочевыделительную систему связано с компрессией почечных вен и паренхимы почек, снижением кровотока в почке, гломерулярного фильтрационного давления (определяется разницей между средним АД и ВБД) и фильтрационного градиента (ФГ, определяется разницей между средним АД и удвоенным ВБД).
Повышение ВБД при наличии органной недостаточности определяет наличие абдоминального компартмент-синдрома (АКС). World Society of the Abdominal Compartment Syndrome (2012 г.) дает следующее определение АКС — это стойкое повышение ВБД более 27 см вод. ст., которое ассоциируется с новой дисфункцией/недостаточностью органов. Другими словами, АКС — это сочетание повышения ВБД>20 мм рт.ст. (27 см вод. ст.) и наличие недостаточности хотя бы одного органа.
Было показано, что ВБГ у больных тяжелым ОП формируется с первых дней заболевания, при благоприятном прогнозе сохраняется в течение 3-5 дней, а затем снижается. У всех умерших больных тяжелым ОП давление в брюшной полости остается высоким на протяжении всей первой недели. Повышение ВБД может наблюдаться также при прогрессировании локальных осложнений: острых жидкостных скоплений, распространенного парапанкреатита [15]. Повышение ВБД является одним из механизмов развития недостаточности органов, которая приводит к летальному исходу [37].
Успех лечения больных тяжелым ОП во многом зависит от ранней диагностики и купирования ВБГ, чему способствует мониторирование этого показателя с первых часов заболевания [17, 30, 36]. Раннее мониторирование и лечение ВБГ позволили добиться снижения летальности при тяжелом ОП с 20 до 10% [34].
Для этого авторы [27, 28, 32, 34] проводят адекватное обезболивание с целью уменьшения напряжения передней брюшной стенки, дренирование всех жидкостных скоплений в забрюшинной клетчатке и брюшной полости, декомпрессию желудочно-кишечного тракта, ограничивают водную нагрузку (не более 5 л в сутки), вводят коллоидные и гипертонические растворы, своевременно применяют гемодиализ и ультрафильтрацию. Для поддержания перфузионного давления используют вазоактивные препараты. При рефрактерной ВБГ с развитием АКС прибегают к хирургическим методам: подкожной фасциотомии, лапаростомии с применением сетчатых аллотрансплантатов, сендвич-пакетов и вакуум-ассистированного закрытия ран [13, 17, 22, 23, 36].
При рефрактерной ВБГ с развитием АКС прибегают к хирургическим методам: подкожной фасциотомии, лапаростомии с применением сетчатых аллотрансплантатов, сендвич-пакетов и вакуум-ассистированного закрытия ран [13, 17, 22, 23, 36].
Во многих работах показано, что через несколько часов после декомпрессивной лапаротомии у больных с АКС наступает улучшение функций органов [6, 16, 33]. Это указывает на непосредственную роль ВБГ в развитии дисфункций органов. При ретроспективном анализе результатов лечения было показано, что в группе из 23 больных ОП, осложненным АКС, перенесших декомпрессивную лапаротомию (
Нашей целью было изучение роли парапанкреатита в прогрессировании ВБГ у больных тяжелым ОП с различными проявлениями недостаточности органов.
Материал и методы
Проведен анализ результатов лечения 63 больных тяжелым ОП, поступивших в клинику в течение 1-4 сут (в среднем через 26,4±3 ч) от начала заболевания. Все больные находились в отделении интенсивной терапии. Мужчин было 48 (76%), женщин — 15 (24%). Возраст больных варьировал от 19 лет до 81 года (44,4±2 года). Причиной ОП у 87% больных явился прием алкоголя, у 13% — желчнокаменная болезнь. У 60 больных при поступлении диагностирован ферментативный перитонит, по поводу которого 55 (87,3%) больным была произведена санационная лапароскопия, 5 — лапаротомия (3 — в связи с сопутствующим деструктивным холециститом, 2 — из-за невозможности исключения другого острого хирургического заболевания).
Все больные находились в отделении интенсивной терапии. Мужчин было 48 (76%), женщин — 15 (24%). Возраст больных варьировал от 19 лет до 81 года (44,4±2 года). Причиной ОП у 87% больных явился прием алкоголя, у 13% — желчнокаменная болезнь. У 60 больных при поступлении диагностирован ферментативный перитонит, по поводу которого 55 (87,3%) больным была произведена санационная лапароскопия, 5 — лапаротомия (3 — в связи с сопутствующим деструктивным холециститом, 2 — из-за невозможности исключения другого острого хирургического заболевания).
Все больные были разделены на 4 группы: у 24 больных (1-я группа) признаков недостаточности органов не было, у 15 (2-я группа) отмечена ОДН, у 11 (3-я группа) — ОДН и ОССН, у 13 больных (4-я группа) выявлено сочетание ОДН, ОССН и острой почечной недостаточности (ОПН).
Измерение ВБД осуществляли по методу I. Kron и соавт. [21], показания (в см вод. ст.) снимали на 1, 3, 5, 7-е сутки от начала заболевания. Рассчитывали уровни БПД, ФГ (показания в мм рт.
КТ с болюсным контрастированием проводили 21 больному. Поражение забрюшинной клетчатки оценивали по классификации K. Ishikawa и соавт. [19]. Классификация основана на КТ-признаках распространенности инфильтративно-жидкостных изменений. Авторы выделяют 5 степеней поражения: 1-я степень — изменения в переднем параренальном пространстве или в корне брыжейки поперечной ободочной кишки; 2-я степень — изменения клетчатки в области латерального канала или по заднему листку параренальной фасции, 3-я степень — изменения в ретроколической клетчатке, отграниченные фасцией Тольди, 4-я степень — распространение воспалительного процесса на предбрюшинную клетчатку и (или) на собственную околопочечную клетчатку, 5-я степень — переход на собственно забрюшинную клетчатку (textus cellulosus retroperitonealis). При 4-й и 5-й степенях возможно поражение паравезикальной и пресакральной клетчатки.
У других 42 больных о распространенном панкреатите судили по данным УЗИ, видеолапароскопии, а также по информации, полученной во время операции, и данным патологоанатомического вскрытия.
Для проведения множественных сравнений с контрольной группой использовали метод Данетта, для сравнения двух групп между собой — критерий Стьюдента, для сравнения качественных признаков — критерий &khgr;2 и точный критерий Фишера, для изучения корреляции применяли критерий Пирсона.
Результаты и обсуждение
Показатели ВБД, АРАСНЕ II, БПД и ФГ
Значения ВБД у больных изучаемых групп представлены на рис. 1.Рисунок 1. Показатели ВБД у больных ОП. Здесь и на рис. 2, 4 и 5: НО — недостаточность органов, остальные обозначения в тексте. У больных 1-3-й группы в 1-е сутки уровни ВБД достоверно не различались и соответствовали ВБГ 1-й степени, тогда как у больных 4-й группы ВБД было достоверно выше и соответствовало ВБГ 2-й степени.
На рис. 2 представлены показатели шкалы APACHE II у больных разных групп.Рисунок 2. Показатели шкалы APACHE II у больных ОП. Уже в 1-е сутки у больных 2-4-й группы с проявлениями недостаточности органов, в отличие от больных 1-й группы, отмечены значения, соответствующие тяжелому течению заболевания. Наиболее высокие уровни были в 4-й группе. В динамике у больных 1-й и 2-й групп регистрировалось уменьшение индекса APACHE II, тогда как в 3-й и 4-й группах (несмотря на проводимое лечение) — его увеличение к 5-м и 7-м суткам.
Таким образом, ВБГ отражает тяжесть состояния больных в такой же степени, как и индекс шкалы APACHE II. На
ВБД при различном поражении забрюшинной клетчатки
У больных с распространенным парапанкреатитом (n=39) показатели ВБД (рис. 6) и шкалы АРАСНЕ II (рис. 7), измеренные в динамике с 1-х по 7-е сутки, были достоверно выше, чем у больных с локальными формами парапанкреатита (n=24; p<0,01).Рисунок 6. Показатели ВБД у больных ОП с локальными и распространенными формами парапанкреатита (ЛП и РП соответственно).Рисунок 7. Показатели APACHE II у больных ОП с локальными и распространенными формами парапанкреатита (ЛП и РП соответственно). Следует отметить, что при локальном парапанкреатите, начиная с 3-х суток этот показатель достоверно снижался, тогда как при распространенном поражении забрюшинной клетчатки гипертензия сохранялась. Распространенное поражение забрюшинной клетчатки в большей степени, чем наличие выпота в брюшной полости, определяло стойкое повышение ВБД. Об этом свидетельствуют данные, представленные в табл. 2. Проанализированы результаты обследования 48 больных с наличием ВБГ 1-4-й степени. Санацию и дренирование брюшной полости при ферментативном перитоните производили в 1-3-и сутки с момента заболевания.
6) и шкалы АРАСНЕ II (рис. 7), измеренные в динамике с 1-х по 7-е сутки, были достоверно выше, чем у больных с локальными формами парапанкреатита (n=24; p<0,01).Рисунок 6. Показатели ВБД у больных ОП с локальными и распространенными формами парапанкреатита (ЛП и РП соответственно).Рисунок 7. Показатели APACHE II у больных ОП с локальными и распространенными формами парапанкреатита (ЛП и РП соответственно). Следует отметить, что при локальном парапанкреатите, начиная с 3-х суток этот показатель достоверно снижался, тогда как при распространенном поражении забрюшинной клетчатки гипертензия сохранялась. Распространенное поражение забрюшинной клетчатки в большей степени, чем наличие выпота в брюшной полости, определяло стойкое повышение ВБД. Об этом свидетельствуют данные, представленные в табл. 2. Проанализированы результаты обследования 48 больных с наличием ВБГ 1-4-й степени. Санацию и дренирование брюшной полости при ферментативном перитоните производили в 1-3-и сутки с момента заболевания./21/4.jpg) Не отмечено достоверных различий объема выпота в брюшной полости при разной степени ВБГ, выявлена тенденция к увеличению объема жидкости у больных с локальным парапанкреатитом. Число больных с распространенным парапанкреатитом прогрессивно увеличивалось при повышении степени ВБГ, при этом возрастало число больных с недостаточностью нескольких органов.
Не отмечено достоверных различий объема выпота в брюшной полости при разной степени ВБГ, выявлена тенденция к увеличению объема жидкости у больных с локальным парапанкреатитом. Число больных с распространенным парапанкреатитом прогрессивно увеличивалось при повышении степени ВБГ, при этом возрастало число больных с недостаточностью нескольких органов.
Таким образом, именно распространенное поражение забрюшинной клетчатки играет большую роль в поддержании ВБГ после санации и дренирования жидкостных скоплений в брюшной полости.
Отдельно были рассмотрены больные, у которых проведена КТ с болюсным введением контрастного препарата. У них выраженность парапанкреатита изучена по 5-степенной классификации [19]. При наличии поражения забрюшинной клетчатки 1-2-й степени в 1, 3, 5 и 7-е сутки ВБГ составила 13±0,3, 17±2, 16±4 и 12±2 см вод. ст. соответственно, при 3-й степени — 19±3, 17±2, 15±2 и 13±2 см вод. cт., при 4-5-й степени — 22±3, 20±2, 23±4 и 21±5 см вод. ст., различия в 1-е и 7-е сутки достоверны (p<0,05). При распространенном парапанкреатите (4-5-й степени) не отмечено снижения ВБД в течение 7 дней.
При распространенном парапанкреатите (4-5-й степени) не отмечено снижения ВБД в течение 7 дней.
В сроки 14 дней от начала заболевания из 48 больных с 1-4-й степенью ВБГ умерли 18 (37,5%): с ВБГ 1-й степени — 1 (6,6%), с ВБГ 2-й степени -6 (37,5%), с ВБГ 3-й степени — 7 (58,3%), с ВБГ 4-й степени — 4 (80%). У всех был распространенный парапанкреатит. В последующем гнойные осложнения возникли у 12 (40%) из 30 оставшихся в живых. Поздняя летальность составила 33,3% (умерли 10 больных, у 9 из них был распространенный парапанкреатит).
Таким образом, данные настоящего исследования еще раз подтвердили, что определяющим фактором неблагоприятного исхода у больных тяжелым острым панкреатитом является наличие ранней недостаточности органов.
Показатель внутрибрюшного давления наряду с индексом шкалы АРАСНЕ II позволяет на раннем этапе заболевания предположить неблагоприятный исход. Транзиторная внутрибрюшная гипертензия в течение 3 сут от начала заболевания с последующим снижением внутрибрюшного давления на 5-е сутки, характерная для больных с локальным поражением забрюшинной клетчатки, является важным фактором выживаемости. Определяющим признаком стойкой внутрибрюшной гипертензии (повышение внутрибрюшного давления в течение 5-7 дней), сопровождающейся недостаточностью органов, является распространенный парапанкреатит. Важно выделить эту группу больных, для чего к 3-5-м суткам от начала заболевания необходимо иметь информацию о наличии распространенного перитонита (данные КТ с контрастированием).
Определяющим признаком стойкой внутрибрюшной гипертензии (повышение внутрибрюшного давления в течение 5-7 дней), сопровождающейся недостаточностью органов, является распространенный парапанкреатит. Важно выделить эту группу больных, для чего к 3-5-м суткам от начала заболевания необходимо иметь информацию о наличии распространенного перитонита (данные КТ с контрастированием).
Полученные данные позволяют констатировать, что стойкая внутрибрюшная гипертензия у больных с распространенным парапанкреатитом и полиорганной недостаточностью является показанием к проведению ранних декомпрессионных вмешательств на брюшной стенке, а при наличии предикторов повреждения панкреатического протока и развития внутреннего панкреатического свища — мероприятий, направленных на перевод внутреннего свища в наружный, о чем сообщалось нами ранее [1, 2].
Внутрибрюшная гипертензия и вторичный абдоминальный компартмент-синдром у пациента с краниофарингиомой в послеоперационном периоде
Внутрибрюшная гипертензия и вторичный абдоминальный компартмент-синдром у пациента с краниофарингиомой в послеоперационном периодеПопугаев К. А.
А.
ГБУЗ «НИИ СП им. Н.В. Склифосовского» Департамента здравоохранения Москвы, Москва, Россия
Савин И.А.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н. Н. Бурденко» Минздрава России, 125047, Москва, Россия
Горячев А.С.
НИИ нейрохирургии им. акад. Н.Н. Бурденко РАМН, Москва
Ошоров А.В.
НИИ нейрохирургии им. акад. Н.Н. Бурденко РАМН, Москва
Полупан А.А.
НИИ нейрохирургии им. акад. Н.Н. Бурденко РАМН, Москва
Калинин П.Л.
НИИ нейрохирургии им. Н.Н. Бурденко РАМН, Москва
Кутин М.А.
НИИ нейрохирургии им. Н.Н. Бурденко РАМН, Москва
Лубнин А.Ю.
ГБУЗ МО «Московский областной научно-исследовательский институт акушерства и гинекологии», Москва, Россия, ФГБНУ НИИ нейрохирургии им. Н.Н. Бурденко (дир. — акад. РАН А.А. Потапов), Москва, Россия, Кафедра акушерства и гинекологии ФУВ ГБУЗ МО «Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского», Москва, Россия
Внутрибрюшная гипертензия и вторичный абдоминальный компартмент-синдром у пациента с краниофарингиомой в послеоперационном периоде
Журнал:
Журнал «Вопросы нейрохирургии» имени Н. Н. Бурденко. 2011;75(1): 66‑71
Н. Бурденко. 2011;75(1): 66‑71
Как цитировать
Попугаев К.А., Савин И.А., Горячев А.С., Ошоров А.В., Полупан А.А., Калинин П.Л., Кутин М.А., Лубнин А.Ю.
Внутрибрюшная гипертензия и вторичный абдоминальный компартмент-синдром у пациента с краниофарингиомой в послеоперационном периоде. Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2011;75(1):66‑71.
Popugaev KA, Savin IA, Goriachev AS, Oshorov AV, Polupan AA, Kalinin PL, Kutin MA, Lubnin AYu. Intraabdominal hypertension and secondary abdominal compartment-syndrome in the patient with craniopharyngioma in postoperative period. Zhurnal Voprosy Neirokhirurgii Imeni N. N. Burdenko. 2011;75(1):66‑71. (In Russ.).
N. Burdenko. 2011;75(1):66‑71. (In Russ.).
Авторы:
Попугаев К.А.
ГБУЗ «НИИ СП им. Н.В. Склифосовского» Департамента здравоохранения Москвы, Москва, Россия
Все авторы (8)
Читать метаданные
На сегодняшний день проблема внутрибрюшной гипертензии у пациентов с опухолями головного мозга является фактически неизученной. Авторы приводят клиническое наблюдение, в котором осложненное течение раннего послеоперационного периода у пациента с краниофарингиомой было обусловлено вторичным абдоминальным компартмент-синдромом. Приводится анализ причин развития внутрибрюшной гипертензии у находящихся в отделении реанимации пациентов с поражениями ЦНС. Выявлены факторы риска развития внутрибрюшной гипертензии, наличие которых следует принимать во внимание при проведении интенсивной терапии у нейрореанимационных пациентов.
Ключевые слова:
опухоль ЦНС
внутрибрюшная гипертензия
абдоминальный компартмент-синдром
Авторы:
Попугаев К. А.
А.
ГБУЗ «НИИ СП им. Н.В. Склифосовского» Департамента здравоохранения Москвы, Москва, Россия
Савин И.А.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н. Н. Бурденко» Минздрава России, 125047, Москва, Россия
Горячев А.С.
НИИ нейрохирургии им. акад. Н.Н. Бурденко РАМН, Москва
Ошоров А.В.
НИИ нейрохирургии им. акад. Н.Н. Бурденко РАМН, Москва
Полупан А.А.
НИИ нейрохирургии им. акад. Н.Н. Бурденко РАМН, Москва
Калинин П.Л.
НИИ нейрохирургии им. Н.Н. Бурденко РАМН, Москва
Кутин М.А.
НИИ нейрохирургии им. Н.Н. Бурденко РАМН, Москва
Лубнин А.Ю.
ГБУЗ МО «Московский областной научно-исследовательский институт акушерства и гинекологии», Москва, Россия, ФГБНУ НИИ нейрохирургии им. Н.Н. Бурденко (дир. — акад. РАН А.А. Потапов), Москва, Россия, Кафедра акушерства и гинекологии ФУВ ГБУЗ МО «Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского», Москва, Россия
- РИНЦ AuthorID: 370609
- Scopus AuthorID: 57192157123
- ORCID: 0000-0003-2595-5877
Закрыть метаданные
Внутрибрюшная гипертензия (ВБГ) была впервые описана еще в середине XIX века [14]. С тех пор эта проблема неоднократно переживала периоды полного забвения, которые затем сменялись осознанием ее значимости, когда клиницисты и исследователи проводили активный поиск решений для ее своевременной и эффективной коррекции [27, 28, 34, 35, 37]. Наиболее подробно проблема ВБГ исследована в абдоминальной хирургии, у пострадавших с политравмой и у пациентов после операций на аорте [7, 20, 24, 29, 32, 36]. У пациентов с опухолями головного мозга проблема ВБГ является фактически неизученной. Есть отдельные работы [9, 13], в которых было показано, что у пациентов с черепно-мозговой травмой ВБГ может являться непосредственной причиной внутричерепной гипертензии. В каких-либо других аспектах проблема ВБГ у нейрохирургических пациентов ранее не рассматривалась.
С тех пор эта проблема неоднократно переживала периоды полного забвения, которые затем сменялись осознанием ее значимости, когда клиницисты и исследователи проводили активный поиск решений для ее своевременной и эффективной коррекции [27, 28, 34, 35, 37]. Наиболее подробно проблема ВБГ исследована в абдоминальной хирургии, у пострадавших с политравмой и у пациентов после операций на аорте [7, 20, 24, 29, 32, 36]. У пациентов с опухолями головного мозга проблема ВБГ является фактически неизученной. Есть отдельные работы [9, 13], в которых было показано, что у пациентов с черепно-мозговой травмой ВБГ может являться непосредственной причиной внутричерепной гипертензии. В каких-либо других аспектах проблема ВБГ у нейрохирургических пациентов ранее не рассматривалась.
Приводим клиническое наблюдение, в котором у пациента с краниофарингиомой тяжесть состояния в раннем послеоперационном периоде была обусловлена вторичным абдоминальным компартмент-синдромом.
Пациент С. , 58 лет, поступил в Институт нейрохирургии с диагнозом: крупная стебельно-интравентрикулярная кистозная краниофарингиома. Жалобы при поступлении: головная боль, слабость, снижение остроты и сужение полей зрения. Объективно: грубые мнестические расстройства и дезориентация в месте, времени, личной ситуации. Острота зрения с двух сторон 0,1. Эндокринные нарушения: ожирение III степени, индекс массы тела 40,5, гипопитуитаризм в виде вторичного гипокортицизма, гипотиреоза, гипогонадизма, соматотропной недостаточности. Биохимический и клинический анализы крови без изменений. Живот увеличен в размерах (рис. 1).Рисунок 1. Увеличенный в размерах живот у пациента с морбидным ожирением. При УЗИ органов брюшной полости и забрюшинного пространства увеличения размеров паренхиматозных органов не выявлено, имелись хронические воспалительные изменения печени и поджелудочной железы. Рентгенологически выявлялось усиление легочного рисунка. При магнитно-резонансной томографии (МРТ) головного мозга был подтвержден диагноз крупной кистозной супраселлярной краниофарингиомы (рис.
, 58 лет, поступил в Институт нейрохирургии с диагнозом: крупная стебельно-интравентрикулярная кистозная краниофарингиома. Жалобы при поступлении: головная боль, слабость, снижение остроты и сужение полей зрения. Объективно: грубые мнестические расстройства и дезориентация в месте, времени, личной ситуации. Острота зрения с двух сторон 0,1. Эндокринные нарушения: ожирение III степени, индекс массы тела 40,5, гипопитуитаризм в виде вторичного гипокортицизма, гипотиреоза, гипогонадизма, соматотропной недостаточности. Биохимический и клинический анализы крови без изменений. Живот увеличен в размерах (рис. 1).Рисунок 1. Увеличенный в размерах живот у пациента с морбидным ожирением. При УЗИ органов брюшной полости и забрюшинного пространства увеличения размеров паренхиматозных органов не выявлено, имелись хронические воспалительные изменения печени и поджелудочной железы. Рентгенологически выявлялось усиление легочного рисунка. При магнитно-резонансной томографии (МРТ) головного мозга был подтвержден диагноз крупной кистозной супраселлярной краниофарингиомы (рис. 2).Рисунок 2. МРТ головного мозга при поступлении пациента в институт. Крупная стебельно-интравентрикулярная кистозная краниофарингиома. Сопутствующая патология: гепатит С в стадии ремиссии.
2).Рисунок 2. МРТ головного мозга при поступлении пациента в институт. Крупная стебельно-интравентрикулярная кистозная краниофарингиома. Сопутствующая патология: гепатит С в стадии ремиссии.
На первом этапе хирургического лечения была установлена система Оммайя в кисту опухоли. Операция произведена под внутривенной анестезией пропофолом и фентанилом. Пробуждение было в обычные сроки, пациент был экстубирован через 2 ч после завершения операции. В течение 4 сут после операции состояние было стабильным, пациент находился в нейрохирургическом отделении. В послеоперационном периоде уменьшилась выраженность головной боли. Самостоятельное дыхание было адекватным, гемодинамические показатели — стабильными. Пациент ел самостоятельно, кишечные шумы были ослаблены, но нарушений усвоения и пассажа пищи не было. После очистительных клизм был стул. Однократные в течение суток эпизоды полиурии купировались приемом десмопрессина. Системные маркеры воспаления — количество лейкоцитов, лейкоцитарная формула и С-реактивный белок были в пределах нормы (см. таблицу). Пациенту проводилась инфузионная, гастропротективная, профилактическая антибактериальная и полигормональная заместительная терапия глюкокортикостероидными (гидрокортизон 200 мг/сут), тиреоидными (L-тироксин 200 мкг/сут) и половыми (омнадрен 250 мг, 1 раз в 2 нед) гормонами. На 5-е сутки после операции состояние ухудшилось. Развилось сопорозное состояние. При компьютерной томографии (КТ) головного мозга по сравнению с дооперационным уровнем была выявлена положительная динамика в виде уменьшения размеров желудочковой системы и кисты краниофарингиомы (рис. 3).Рисунок 3. КТ головного мозга после операции. Правильное положение катетера системы Омайя. Базальные цистерны визуализировались хорошо. Гемодинамические показатели оставались в пределах нормы. Появилась одышка. Развился парез желудочно-кишечного тракта (ЖКТ): вздутие живота, тошнота, рвота, отсутствие стула и кишечных шумов. При спиральной КТ брюшной полости выявлены раздутые петли кишечника. Поперечный размер живота был практически равен вертикальному, что является признаком выраженной ВБГ (рис.
таблицу). Пациенту проводилась инфузионная, гастропротективная, профилактическая антибактериальная и полигормональная заместительная терапия глюкокортикостероидными (гидрокортизон 200 мг/сут), тиреоидными (L-тироксин 200 мкг/сут) и половыми (омнадрен 250 мг, 1 раз в 2 нед) гормонами. На 5-е сутки после операции состояние ухудшилось. Развилось сопорозное состояние. При компьютерной томографии (КТ) головного мозга по сравнению с дооперационным уровнем была выявлена положительная динамика в виде уменьшения размеров желудочковой системы и кисты краниофарингиомы (рис. 3).Рисунок 3. КТ головного мозга после операции. Правильное положение катетера системы Омайя. Базальные цистерны визуализировались хорошо. Гемодинамические показатели оставались в пределах нормы. Появилась одышка. Развился парез желудочно-кишечного тракта (ЖКТ): вздутие живота, тошнота, рвота, отсутствие стула и кишечных шумов. При спиральной КТ брюшной полости выявлены раздутые петли кишечника. Поперечный размер живота был практически равен вертикальному, что является признаком выраженной ВБГ (рис. 4) [23].Рисунок 4. Спиральная КТ грудной и брюшной полостей при ухудшении состояния пациента. Равенство поперечного и вертикального размера брюшной полости является объективным признаком выраженной ВБГ. Выявляются паренхиматозные изменения задненижних отделов левого легкого. Темп диуреза замедлился до олигоурии. По лабораторным данным отмечалось существенное нарастание системных маркеров воспаления и повышение уровня мочевины (см. таблицу). Очага инфекции выявлено не было: цитоз ликвора, содержание глюкозы и лактата в ликворе, клинический анализ мочи были в пределах нормы. Придаточные пазухи носа и основания черепа были воздушны (см. рис. 3). При спиральной КТ грудной клетки синусы были свободны, выявлялись изменения в базальных отделах левого легкого, причину которых трактовать однозначно было трудно (см. рис. 4). Эти изменения можно было расценить как пневмонию или ателектаз вследствие элевации диафрагмы и ограничения ее подвижности. Выявлялась диссоциация между незначительными рентгенологическими изменениями, очень высоким уровнем С-реактивного белка, лейкоцитоза, существенным сдвигом лейкоцитарной формулы влево и нормальным уровнем прокальцитонина, который всегда повышается при бактериальной пневмонии [8].
4) [23].Рисунок 4. Спиральная КТ грудной и брюшной полостей при ухудшении состояния пациента. Равенство поперечного и вертикального размера брюшной полости является объективным признаком выраженной ВБГ. Выявляются паренхиматозные изменения задненижних отделов левого легкого. Темп диуреза замедлился до олигоурии. По лабораторным данным отмечалось существенное нарастание системных маркеров воспаления и повышение уровня мочевины (см. таблицу). Очага инфекции выявлено не было: цитоз ликвора, содержание глюкозы и лактата в ликворе, клинический анализ мочи были в пределах нормы. Придаточные пазухи носа и основания черепа были воздушны (см. рис. 3). При спиральной КТ грудной клетки синусы были свободны, выявлялись изменения в базальных отделах левого легкого, причину которых трактовать однозначно было трудно (см. рис. 4). Эти изменения можно было расценить как пневмонию или ателектаз вследствие элевации диафрагмы и ограничения ее подвижности. Выявлялась диссоциация между незначительными рентгенологическими изменениями, очень высоким уровнем С-реактивного белка, лейкоцитоза, существенным сдвигом лейкоцитарной формулы влево и нормальным уровнем прокальцитонина, который всегда повышается при бактериальной пневмонии [8].
Пациент был переведен в отделение реанимации. На фоне инсуффляции кислорода нарушений газового состава артериальной крови не было. При измерении внутрибрюшного давления (ВБД) через мочевой катетер оно составило 23 мм рт.ст., что соответствовало выраженной ВБГ. В дальнейшем, в течение всего времени пребывания пациента в отделении реанимации проводилось дискретное, каждые 6 ч, измерение ВБД также через мочевой катетер при помощи методики, описанной M. Malbrain [23]. Причиной ВБГ, по-видимому, был парез ЖКТ на фоне морбидного ожирения. Начата терапия, направленная на стимуляцию перистальтики ЖКТ: вазелиновое масло, солевые растворы со скоростью 40—60 мл/ч в зонд, антихолинэстеразные препараты, метоклопрамид и эритромицин внутривенно, очистительная клизма (2 раза в сутки). Проводилось парентеральное питание трехкомпонентной смесью Нутрифлекс («BBraun», Германия). Осуществлена коррекция гастропротективной терапии — H3-блокаторы заменены блокаторами протонной помпы, а также терапии тиреоидными гормональными препаратами — к терапии L-тироксином в дозе 200 мкг/сут был добавлен тиреокомб в дозе 2 таблетки в сутки в связи с низким уровнем трийодтиронина (Т3) и свободного трийодтиронина (св. Т3). Несмотря на отсутствие очевидного очага инфекции, эмпирически был назначен сульперазон. В течение суток удалось добиться усвоения глюкозосолевых растворов и незначительного снижения ВБД. Однако ВБГ сохранялась, поэтому было принято решение о проведении продленной эпидуральной анестезии. Эпидуральный катетер был установлен на уровне Th9—Th10 и проведен в краниальном направлении на 5 см. Начато постоянное введение ропивакаина в дозе 20 мг/ч, продолжавшееся в течение 7 сут. ВБД начало снижаться в течение первых 12 ч, а нормализовалось через 1,5 сут. На фоне коррекции терапии тиреоидными препаратами, а также продолжавшейся терапии, направленной на стимуляцию ЖКТ и эпидуральной анестезии, удалось добиться нормализации стула. Кроме этого, удалось купировать одышку. Через 2 сут уровень системных маркеров воспаления начался снижаться, темп диуреза восстановился, а содержание мочевины нормализовалось. Парентеральное питание было прекращено, и было начато энтеральное.
Т3). Несмотря на отсутствие очевидного очага инфекции, эмпирически был назначен сульперазон. В течение суток удалось добиться усвоения глюкозосолевых растворов и незначительного снижения ВБД. Однако ВБГ сохранялась, поэтому было принято решение о проведении продленной эпидуральной анестезии. Эпидуральный катетер был установлен на уровне Th9—Th10 и проведен в краниальном направлении на 5 см. Начато постоянное введение ропивакаина в дозе 20 мг/ч, продолжавшееся в течение 7 сут. ВБД начало снижаться в течение первых 12 ч, а нормализовалось через 1,5 сут. На фоне коррекции терапии тиреоидными препаратами, а также продолжавшейся терапии, направленной на стимуляцию ЖКТ и эпидуральной анестезии, удалось добиться нормализации стула. Кроме этого, удалось купировать одышку. Через 2 сут уровень системных маркеров воспаления начался снижаться, темп диуреза восстановился, а содержание мочевины нормализовалось. Парентеральное питание было прекращено, и было начато энтеральное. К 12 cyт после операции (7-е сутки пребывания пациента в отделении реанимации) состояние пациента стабилизировалось, уровень системных маркеров воспаления вместе с показателями ВБД нормализовались. При повторной спиральной КТ грудной клетки была выявлена положительная динамика, вероятно, связанная с улучшением механики дыхания, увеличением подвижности диафрагмы и разрешением ателектазирования на фоне регресса гипостатических явлений в задненижних отделах легких (рис. 5).Рисунок 5. Спиральная КТ грудной полости на 7-е сутки пребывания пациента в отделении реанимации. Регресс паренхиматозных изменений задненижних отделов левого легкого в течение 1 нед свидетельствует о том, что они были обусловлены ателектазированием, а не пневмонией. Быстрый, в течение 1 нед, регресс рентгенологических изменений в легких — еще один фактор, который свидетельствует в пользу ателектазирования на фоне ВБГ, а не в пользу пневмонии. Повышение уровня маркеров системного воспаления при ухудшении состояния наиболее вероятно было обусловлено бактериемией.
К 12 cyт после операции (7-е сутки пребывания пациента в отделении реанимации) состояние пациента стабилизировалось, уровень системных маркеров воспаления вместе с показателями ВБД нормализовались. При повторной спиральной КТ грудной клетки была выявлена положительная динамика, вероятно, связанная с улучшением механики дыхания, увеличением подвижности диафрагмы и разрешением ателектазирования на фоне регресса гипостатических явлений в задненижних отделах легких (рис. 5).Рисунок 5. Спиральная КТ грудной полости на 7-е сутки пребывания пациента в отделении реанимации. Регресс паренхиматозных изменений задненижних отделов левого легкого в течение 1 нед свидетельствует о том, что они были обусловлены ателектазированием, а не пневмонией. Быстрый, в течение 1 нед, регресс рентгенологических изменений в легких — еще один фактор, который свидетельствует в пользу ателектазирования на фоне ВБГ, а не в пользу пневмонии. Повышение уровня маркеров системного воспаления при ухудшении состояния наиболее вероятно было обусловлено бактериемией. Эпидуральный катетер был удален на 7-е сутки после его установки. Пациент был переведен в нейрохирургическое отделение на следующий день. Реабилитационные мероприятия позволили добиться дальнейшего улучшения состояния. С учетом состояния пациента, МРТ-картины, возраста больного и характера сопутствующей патологии от удаления опухоли было решено отказаться. Пациент был выписан на 21-е сутки после операции в удовлетворительном состоянии.
Эпидуральный катетер был удален на 7-е сутки после его установки. Пациент был переведен в нейрохирургическое отделение на следующий день. Реабилитационные мероприятия позволили добиться дальнейшего улучшения состояния. С учетом состояния пациента, МРТ-картины, возраста больного и характера сопутствующей патологии от удаления опухоли было решено отказаться. Пациент был выписан на 21-е сутки после операции в удовлетворительном состоянии.
Обсуждение
ВБД в норме не превышает 10 мм рт.ст. Внутрибрюшной гипертензией (ВБГ) считается повышение ВБД более 12 мм рт.ст. Выделяют 4 степени ВБГ: I степень — 12—15 мм рт.ст., II степень — 16—20 мм рт.ст., III степень — 21—25 мм рт.ст., IV степень— >25 мм рт.ст. [26]. Как минимум у половины пациентов, находящихся в критическом состоянии, ВБД повышено [17]. ВБГ приводит к бактериемии, полиорганной недостаточности (ПОН) и смерти [4, 17]. ВБГ III—IV степени, вместе с наличием ПОН, являются критериями абдоминального компартмент-синдрома (АКС), который разделяется на первичный, вторичный и третичный [5, 25, 26]. Первичный АКС развивается у пациентов с патологией органов брюшной полости и забрюшинного пространства, вторичный — у пациентов без абдоминальной патологии, третичный — у пациентов, перенесших декомпрессивную лапаротомию, выполненную в связи с первичным или вторичным АКС [26]. При первичном и третичном АКС показаны раннее хирургическое устранение причины, вызвавшей ВБГ, и ранняя декомпрессивная лапаротомия. Причинами вторичного АКС являются сепсис, синдром капиллярной утечки, обширная ожоговая травма, массивная инфузионно-трансфузионная терапия [3, 17, 18]. При этом показана прежде всего консервативная терапия, заключающаяся в коррекции факторов, приведших к повышению ВБД, стимуляции моторики ЖКТ и проведении эпидуральной аналгезии на нижнегрудном уровне [15, 22, 30]. Стимуляция моторики ЖКТ проводится с помощью энтерального введения солевых растворов, по возможности, раннего начала энтерального кормления, внутривенного использования метоклопрамида и эритромицина [11, 16, 22]. Была показана эффективность кормления через назоеюнальный зонд [1].
Первичный АКС развивается у пациентов с патологией органов брюшной полости и забрюшинного пространства, вторичный — у пациентов без абдоминальной патологии, третичный — у пациентов, перенесших декомпрессивную лапаротомию, выполненную в связи с первичным или вторичным АКС [26]. При первичном и третичном АКС показаны раннее хирургическое устранение причины, вызвавшей ВБГ, и ранняя декомпрессивная лапаротомия. Причинами вторичного АКС являются сепсис, синдром капиллярной утечки, обширная ожоговая травма, массивная инфузионно-трансфузионная терапия [3, 17, 18]. При этом показана прежде всего консервативная терапия, заключающаяся в коррекции факторов, приведших к повышению ВБД, стимуляции моторики ЖКТ и проведении эпидуральной аналгезии на нижнегрудном уровне [15, 22, 30]. Стимуляция моторики ЖКТ проводится с помощью энтерального введения солевых растворов, по возможности, раннего начала энтерального кормления, внутривенного использования метоклопрамида и эритромицина [11, 16, 22]. Была показана эффективность кормления через назоеюнальный зонд [1]. Отдельной терапевтической опцией, которой следует придерживаться при лечении любого АКС, является поддержание абдоминального перфузионного давления (АПД) выше 50 мм рт.ст. АПД — разница между ВБД и средним артериальным давлением. В ряде исследований показано, что снижение АПД ниже 50 мм рт.ст. приводит к ухудшению результатов лечения пациентов с АКС [12].
Отдельной терапевтической опцией, которой следует придерживаться при лечении любого АКС, является поддержание абдоминального перфузионного давления (АПД) выше 50 мм рт.ст. АПД — разница между ВБД и средним артериальным давлением. В ряде исследований показано, что снижение АПД ниже 50 мм рт.ст. приводит к ухудшению результатов лечения пациентов с АКС [12].
Наиболее полно изучен первичный и третичный АКС [12, 19]. Данных о вторичном АКС, особенно в нейрохирургической практике, фактически нет. Существуют отдельные работы, в которых изучалась роль ВБГ у нейрохирургических пациентов. Показано, что при ВБГ возрастает внутричерепное давление вследствие повышения внутригрудного давления и ухудшения на этом фоне венозного оттока из полости черепа [9, 13]. Кроме этого, описан феномен ухудшения резорбции ликвора при ВБГ, что также приводит к повышению внутричерепного давления [33]. Безусловно, что при лечении нейрореанимационного пациента с внутричерепной гипертензией существует вероятность ее агравации на фоне ВБГ. Однако комплекс интенсивной терапии внутричерепной гипертензии, включающий применение седативных препаратов, миорелаксантов, поддержание адекватного среднего артериального давления, проведение раннего энтерального питания, одновременно соответствует и рекомендациям по борьбе с ВБГ [10, 12, 15, 22, 30].
Однако комплекс интенсивной терапии внутричерепной гипертензии, включающий применение седативных препаратов, миорелаксантов, поддержание адекватного среднего артериального давления, проведение раннего энтерального питания, одновременно соответствует и рекомендациям по борьбе с ВБГ [10, 12, 15, 22, 30].
У нейрореанимационного пациента, в отличие от больных без повреждения центральной нервной системы, существуют дополнительные причины для развития ВБГ. Функция ЖКТ регулируется диэнцефальными структурами и эндокринной системой [6, 38]. Гормоны щитовидной железы оказывают непосредственное влияние на функцию ЖКТ [38]. Гипотиреоз, как правило, в рамках гипопитуитаризма развивается в 8,5—55% наблюдений у разных групп нейрохирургических пациентов и приводит к развитию пареза ЖКТ [2, 21, 31]. Повреждение диэнцефальных структур также приводит к парезу ЖКТ. Парез ЖКТ вызывает ВБГ. Поэтому среди всей нейрохирургической патологии при опухолях хиазмально-селлярной области риск развития ВБГ вследствие пареза ЖКТ наиболее высокий, поскольку диэнцефальные структуры изначально вовлечены в патологический процесс и у подавляющего большинства этих больных есть тиреоидная недостаточность. С одной стороны, развитие ВБГ у этих пациентов отражает тяжесть повреждения гипоталамо-гипофизарной системы, а с другой, — сформировавшийся АКС приводит к органной недостаточности и повышает внутричерепное давление. Это еще больше ухудшает состояние пациента. Формируется порочный круг, который невозможно прервать без нормализации ВБД. Вместе с этим при некомпенсированной тиреоидной недостаточности и/или при повреждении диэнцефальных структур невозможно нормализовать ВБД.
С одной стороны, развитие ВБГ у этих пациентов отражает тяжесть повреждения гипоталамо-гипофизарной системы, а с другой, — сформировавшийся АКС приводит к органной недостаточности и повышает внутричерепное давление. Это еще больше ухудшает состояние пациента. Формируется порочный круг, который невозможно прервать без нормализации ВБД. Вместе с этим при некомпенсированной тиреоидной недостаточности и/или при повреждении диэнцефальных структур невозможно нормализовать ВБД.
В приведенном наблюдении ухудшение состояния началось с развития пареза ЖКТ, очень быстро приведшего к развитию выраженной ВБГ. Далее развилась дыхательная недостаточность, олигоурия, существенно возрос уровень маркеров воспаления — С-реактивного белка, лейкоцитоза, сдвига лейкоцитарной формулы влево. Это свидетельствовало о формировании вторичного АКС. Проведение комплекса мероприятий, направленных на борьбу с парезом ЖКТ и ВБГ, в том числе эпидуральная анестезия, позволили снизить ВБД. Принципиально важным аспектом в лечении этого пациента, в отличие от больных, не имеющих тиреоидной недостаточности, явилась коррекция схемы проводимой гормональной терапии. Поскольку, несмотря на прием L-тироксина в дозе 200 мкг/сут, у пациента сохранялся низкий уровень Т3 и св. Т3, к терапии был добавлен тиреокомб — препарат, содержащий и тироксин (Т4), и трийодтиронин (Т3). Кроме этого, на протяжении всего времени пребывания пациента в отделении реанимации уровень среднего артериального давления тщательно контролировался для поддержания АПД выше 50 мм рт.ст. После купирования ВБГ у пациента нормализовался уровень системных маркеров воспаления, восстановился адекватный темп диуреза, были купированы признаки дыхательной недостаточности.
Поскольку, несмотря на прием L-тироксина в дозе 200 мкг/сут, у пациента сохранялся низкий уровень Т3 и св. Т3, к терапии был добавлен тиреокомб — препарат, содержащий и тироксин (Т4), и трийодтиронин (Т3). Кроме этого, на протяжении всего времени пребывания пациента в отделении реанимации уровень среднего артериального давления тщательно контролировался для поддержания АПД выше 50 мм рт.ст. После купирования ВБГ у пациента нормализовался уровень системных маркеров воспаления, восстановился адекватный темп диуреза, были купированы признаки дыхательной недостаточности.
Заключение
У нейрохирургических больных даже без какой-либо сопутствующей абдоминальной патологии возможно развитие ВБГ и вторичного АКС, поэтому у таких больных следует рутинно измерять ВБД. Специфическими для нейрохирургических пациентов причинами повышения ВБД являются тиреоидная недостаточность и повреждение диэнцефальных структур. Эти факторы необходимо принимать во внимание при проведении интенсивной терапии нейрореанимационных пациентов.
Комментарий
Внутрибрюшная гипертензия (ВБГ) является новой и малоизученной проблемой интенсивной терапии нейрохирургических больных. Известно, что повышение внутрибрюшного давления помимо развития полиорганной недостаточности может сопровождаться ухудшением венозного оттока от головного мозга и повышением внутричерепного давления, что в свою очередь может ухудшить состояние пациентов с патологией головного мозга.
Представленный клинический случай показывает значимость синдрома ВБГ в течение послеоперационного периода пациента с опухолью головного мозга. Следует отметить системный подход в диагностике осложнений послеоперационного периода, представленный авторами. Несомненно, что без комплексной оценки клинической картины, данных компьютерной томографии головного мозга и легких, а также результатов расширенного лабораторного обследования установить диагноз внутрибрюшной гипертензии и определить его ведущую роль в ухудшении состояния больного было бы практически невозможно. Авторы посчитали причиной развития синдрома ВБГ тиреоидную недостаточность. Однако следует отметить, что установить точную причину развития синдрома ВБГ крайне трудно. Известно, что вызвать ВБГ могут не только серьезные нарушения гемодинамики, газообмена и гормонального статуса, но и такие с виду банальные факторы, как использование преимущественно кристаллоидных препаратов в составе инфузионной терапии.
Авторы посчитали причиной развития синдрома ВБГ тиреоидную недостаточность. Однако следует отметить, что установить точную причину развития синдрома ВБГ крайне трудно. Известно, что вызвать ВБГ могут не только серьезные нарушения гемодинамики, газообмена и гормонального статуса, но и такие с виду банальные факторы, как использование преимущественно кристаллоидных препаратов в составе инфузионной терапии.
К сожалению, в литературе отсутствуют четкие статистические данные о частоте развития ВБГ не только у больных с различной нейрохирургической патологией, но и в принципе у пациентов с острой церебральной недостаточностью. Не сформулированы основные причины развития синдрома ВБГ, не существует четких рекомендаций по диагностике, мониторингу и лечению данной патологии. В связи с этим необходимо проведение многоцентровых эпидемиологических исследований ВБГ у нейрохирургических больных.
С.С. Петриков (Москва)
Внутрибрюшная гипертензия у детей в периоперационном периоде при операциях на брюшной полости
Введение
Брюшная полость человека имеет характеристики закрытой полости с жесткими (ребра, позвоночник, таз) и гибкими (брюшная стенка, диафрагма) стенками и жидкостным содержимым. Именно поэтому любые изменения состояния мягкотканных компонентов и брюшной стенки могут приводить к изменению давления в других органах этой полости и, следовательно, обусловливать нарушение функции сердечно-сосудистой, мочевыделительной, дыхательной, гепатобилиарной, нервной системы, а также изменения со стороны ЖКТ [1].
Именно поэтому любые изменения состояния мягкотканных компонентов и брюшной стенки могут приводить к изменению давления в других органах этой полости и, следовательно, обусловливать нарушение функции сердечно-сосудистой, мочевыделительной, дыхательной, гепатобилиарной, нервной системы, а также изменения со стороны ЖКТ [1].
Операции на брюшной полости сопряжены с риском большого числа осложнений, в том числе с нарушением моторики кишечника, несостоятельностью анастомозов, развитием перитонита. Контроль внутрибрюшного давления (ВБД) в комплексе с другими методиками позволяет оценивать эффективность лечения, раньше диагностировать развитие осложнений [2, 3].
Формирование понятия внутрибрюшной гипертензии
Первые исследования показателей ВБД начались еще в XIX в.: Marey в 1863 г. и Burt в 1870 г. опубликовали работы, в которых описывали связь дыхания с колебаниями ВБД [4]. В 1876 г. Wendt описал отрицательное влияние внутрибрюшной гипертензии на функцию почек. Одной из первых экспериментальных работ по данной тематике стала работа H. Emerson, выполненная в 1911 г. [1]. В ходе исследования автор пришел к выводу, что введение жидкости или газа в брюшную полость сопровождается повышением давления в ней, и продемонстрировал развитие полиорганной недостаточности с последующей гибелью животных при повышении ВБД до 20–30 мм рт. ст. Большинство последующих исследований имели описательный характер — исследователи сообщали о гибели пациентов от полиорганной недостаточности при раннем глухом ушивании брюшной полости при тяжелой травме живота.
Одной из первых экспериментальных работ по данной тематике стала работа H. Emerson, выполненная в 1911 г. [1]. В ходе исследования автор пришел к выводу, что введение жидкости или газа в брюшную полость сопровождается повышением давления в ней, и продемонстрировал развитие полиорганной недостаточности с последующей гибелью животных при повышении ВБД до 20–30 мм рт. ст. Большинство последующих исследований имели описательный характер — исследователи сообщали о гибели пациентов от полиорганной недостаточности при раннем глухом ушивании брюшной полости при тяжелой травме живота.
Важную роль в развитии дальнейших исследований сыграло появление лапароскопической методики операций в 1960-х годах. Эффекты от чрезмерного нагнетания давления в брюшной полости во время наложения пневмоперитонеума были отмечены еще в первых экспериментальных работах, что потребовало подбора оптимального безопасного уровня давления [5–7].
Одним из препятствий к полноценному распространению методики являлось отсутствие стандартизации в методике измерения ВБД. К середине XX в. были выделены 2 основные группы методов измерения ВБД.
К середине XX в. были выделены 2 основные группы методов измерения ВБД.
Прямые методы — инвазивное определение давления непосредственно в брюшной полости с помощью внутрибрюшного катетера с датчиком. Первым такой метод предложил в 1931 г. R.H. Overholt [8].
Непрямые методы — косвенное исследование давления в брюшной полости с использованием стенок других органов и систем как мембраны: измерение давления в мочевом пузыре, желудке, прямой кишке, матке, нижней полой вене, дыхательных путях [9].
Решающими стали исследования Kron и Iberti, которые разработали более простой метод измерения ВБД через мочевой пузырь, впоследствии ставший «золотым стандартом» для всех будущих исследований [10]. На момент написания настоящего обзора нормальным ВБД считается установившееся давление в брюшной полости, которое составляет примерно 5 мм рт. ст. и несколько увеличивается и снижается при дыхании.
В дальнейшем на основе понятия ВБД сформировалось несколько более практических понятий.
Абдоминально-перфузионное давление — разница между средним артериальным давлением и ВБД. Данный показатель схож с показателем церебрально-перфузионного давления, активно используемым в нейрохирургии и характеризующим уровень кровоснабжения тканей головного мозга. По аналогии абдоминально-перфузионное давление характеризует перфузию тканей брюшной полости и связано с локальной ишемией. Нормальные значения для взрослых пациентов — более 60 мм рт. ст.
Интраабдоминальная гипертензия — это устойчивое повышение ВБД до 12 мм рт. ст. и более, которое регистрируется как минимум при 3 стандартных измерениях с интервалом в 4–6 ч. В свою очередь подразделяется на 4 степени: 1-я степень характеризуется внутрипузырным давлением от 12 до 15 мм рт. ст., 2-я степень — 16–20 мм рт. ст., 3-я степень — 21–25 мм рт. ст., 4-я степень — более 25 мм рт. ст.
Синдром абдоминальной гипертензии — это стойкое повышение ВБД более 20 мм рт. ст. (с абдоминально-перфузионным давлением <60 мм рт. ст. или без него), которое ассоциируется с манифестацией органной недостаточности/дисфункции.
ст. или без него), которое ассоциируется с манифестацией органной недостаточности/дисфункции.
Значительную роль в формировании этих понятий сыграло появление Всемирного общества по синдрому интраабдоминальной гипертензии (WSACS), которое существует по настоящее время и периодически проводит согласительные конференции по своей тематике, выпускает рекомендации [11–13].
Патофизиологические механизмы влияния интраабдоминальной гипертензии на органы и системыВлияние на сердечно-сосудистую систему. Одним из первых описал ухудшение гемодинамики на фоне увеличения ВБД H. Quincke в 1878 г. [14]. Дальнейшие исследования выявили следующий механизм: кровеносные сосуды брюшной полости, в частности нижняя полая вена, частично или полностью пережимаются окружающими органами и тканями, что ухудшает венозный отток и снижает преднагрузку [15–17].
Влияние на дыхательную систему. Повышенное ВБД приводит к уменьшению объема грудной клетки за счет смещения купола диафрагмы. Это обусловливает уменьшение дыхательного объема, ухудшение газообмена, спадение альвеол и повышает риск ателектазов. Таким образом, значимая внутрибрюшная гипертензия резко снижает эффективность дыхания [18, 19].
Это обусловливает уменьшение дыхательного объема, ухудшение газообмена, спадение альвеол и повышает риск ателектазов. Таким образом, значимая внутрибрюшная гипертензия резко снижает эффективность дыхания [18, 19].
Влияние на мочевыделительную систему. Механическое сдавление почечной паренхимы извне при повышенном ВБД ухудшает почечный кровоток, что способствует развитию почечной недостаточности. По данным некоторых экспериментальных исследований, уже при 1-й степени внутрибрюшной гипертензии наблюдается двукратное снижение скорости диуреза [20], а повышение ВБД более 30 мм рт. ст. почти всегда приводит к полной анурии [21].
Влияние на гепатобилиарную систему. Механическая компрессия печени нарушает печеночный портальный кровоток, а также ухудшает метаболизм на микроциркуляторном уровне, вплоть до ухудшения усвоения глюкозы.
Влияние на ЦНС. Следствием интраабдоминальной гипертензии является значительное снижение церебрального и спинномозгового перфузионного давления с последующим увеличением уровня маркеров ишемии ЦНС [22].
Проблема повышенного ВБД у детей изучена меньше, чем у взрослых пациентов, однако является столь же актуальной. Вероятнее всего, это связано с тем, что до настоящего момента не все физиологические показатели, затронутые в нашем обзоре, стандартизированы для детского возраста. Это продиктовано малым числом исследований и отсутствием в них единого подхода к измерению давления [23], а также отсутствием специализированных расходных материалов — уреометры, применяемые для прикроватного измерения ВБД, являются более подходящими для взрослых пациентов в связи с их объемом и градуировкой.
В случае со взрослыми пациентами методика измерения стандартизирована — общепринятым является измерение давления в мочевом пузыре с предварительным введением в него 25–50 мл стерильного физиологического раствора [24]. За нулевую отметку при измерении указанным способом принимают среднюю подмышечную линию, а полученные данные приводятся в миллиметрах ртутного столба [9]. Положение больного в момент измерения должно быть строго горизонтальным на спине.
Положение больного в момент измерения должно быть строго горизонтальным на спине.
Для детей наиболее распространенная методика изменена следующим образом: объем вводимого в мочевой пузырь стерильного физиологического раствора определяется из расчета 1 мл на 1 кг массы тела ребенка [25, 26].
Нормальные показатели ВБД здоровых детей, включая новорожденных, как правило, несущественно отличаются от показателей взрослых и составляют около 5 мм рт. ст. [27, 28].
Данные различных исследователей о развитии синдрома интраабдоминальной гипертензии у новорожденных противоречивы. По свидетельству одних авторов, необходимо ориентироваться на цифры ВБД около 20 мм рт. ст. В частности, M. Olisevich et al. [29] выпустили работу по мониторингу ВБД во время операций у 42 новорожденных с пороками брюшной стенки и пришли к выводу, что превышение уровня ВБД 20 мм рт. ст. связано с критическим увеличением частоты осложнений [26]. В то же время другие исследователи говорят о развитии интраабдоминальной гипертензии и синдрома интраабдоминальной гипертензии у новорожденных детей при значительно меньшем давлении в брюшной полости — 10–15 мм рт. ст. [30].
ст. [30].
Измерение ВБД в детской хирургии и анестезиологии-реаниматологии
По данным опроса немецких реаниматологов педиатрического профиля, только около 20% врачей рутинно измеряют ВБД [31].
Наиболее часто измерение ВБД проводится интраоперационно у детей с гастрошизисом и омфалоцеле для принятия решения об объеме погружаемых органов и тканей [12]. Однако высокая прогностическая и диагностическая эффективность данной процедуры как предиктора и признака развития тяжелых осложнений позволяет предлагать ее к использованию при гораздо более широком диапазоне показаний. Показатели ВБД могут быть использованы как один из маркеров уменьшения явлений пареза кишечника, критерий риска развития несостоятельности анастомозов, критерий риска развития бактериальной транслокации и сепсиса, один из признаков перфорации полого органа [22, 32–35].
Исследованиям изменения ВБД при развитии перитонита во взрослой хирургии посвящено довольно большое количество работ [31, 36]. По данным литературы [31, 37], перитонит приводит к развитию внутрибрюшной гипертензии в 64% случаев. При таком сочетании осложнений летальность на фоне лечения достигает 42–68%, а без лечения — 100%.
По данным литературы [31, 37], перитонит приводит к развитию внутрибрюшной гипертензии в 64% случаев. При таком сочетании осложнений летальность на фоне лечения достигает 42–68%, а без лечения — 100%.
В детской хирургии количество подобных работ ограничено.
В качестве примера качественной практической работы можно привести статью P. Deindl et al. [38], в которой продемонстрирована эффективность измерения ВБД у детей после трансплантации печени. Выявлена связь между повышением ВБД и скрытым болевым синдромом у пациента, что позволило оптимизировать анальгетическую терапию и получить обратный результат в виде снижения интраабдоминальной гипертензии. На фоне нормализации ВБД у больных отмечалось улучшение спланхнологического кровотока.
Заключение
Представленные работы открывают широкое поле для изучения вопросов ВБД, синдрома интраабдоминальной гипертензии, абдоминально-перфузионного давления у детей, перенесших операции на брюшной полости. К спектру вопросов, которые особенно актуальны, можно отнести:
К спектру вопросов, которые особенно актуальны, можно отнести:
уточнение показателей нормального ВБД для разных возрастных периодов;
измерение ВБД при различных операциях на брюшной полости в случае неосложненного течения послеоперационного периода;
изменение цифр ВБД при развитии перитонита у детей;
связь динамики изменения абдоминально-перфузионного давления и других показателей восстановления пассажа по ЖКТ в раннем послеоперационном периоде.
Абдоминальный компартмент-синдром – внутрибрюшная гипертензия: определение, диагностика и лечение
1. Malbrain ML, Cheatham ML, Kirkpatrick A, Sugrue M, Parr M, De Waele J, et al. Результаты Международной конференции экспертов по внутрибрюшной гипертензии и абдоминальному компартмент-синдрому. I. Определения. Интенсивная терапия Мед. 2006; 32: 1722–32. [PubMed] [Google Scholar]
2. Фолькманн Р. Об ишемическом мышечном параличе и сокращении. Centralblatt für Chirurgie. 1881; 51: 801–3. [Академия Google]
Centralblatt für Chirurgie. 1881; 51: 801–3. [Академия Google]
3. Марей Э-Дж. Париж: Делахайе; 1863. Медицинская физиология кровообращения; стр. 284–93. [Google Scholar]
4. Берт П. Пэрис: JP Baillère;; 1870. Уроки физиологии дыхания. [Google Scholar]
5. Эмерсон Х. Внутрибрюшное давление. Arch Intern Med. 1911; 7: 754–84. [Google Scholar]
6. Огилви У.Х. Позднее осложнение ранений брюшной полости. Ланцет. 1940; 2: 253–6. [Google Scholar]
7. Гросс RE. Новый метод хирургического лечения крупных омфалоцеле. Операция. 1948;24:277–92. [PubMed] [Google Scholar]
8. Baggot MG. Вздутие живота. Curr Res Anesth Analg. 1951; 30: 295–9. [PubMed] [Google Scholar]
9. Крон И.Л., Харман П.К., Нолан С.П. Измерение внутрибрюшного давления как критерий повторного исследования брюшной полости. Энн Сург. 1984; 199: 28–30. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Fietsam R, Jr, Villalba M, Glover JL, Clark K. Синдром внутрибрюшного компартмента как осложнение восстановления разрыва аневризмы брюшной аорты. Am Surg. 1989;55:396–402. [PubMed] [Google Scholar]
Am Surg. 1989;55:396–402. [PubMed] [Google Scholar]
11. Мерц Л., Каплан Л.Дж. Абдоминальный компартмент-синдром. Крит Уход Мед. 2008;36:S212–5. [PubMed] [Google Scholar]
12. Moore EE, Burch JM, Franciose RJ, Offner PJ, Biffl WL. Поэтапное физиологическое восстановление и хирургическое лечение повреждений. Мир J Surg. 1998; 22:1184–90. [PubMed] [Google Scholar]
13. Папаврамидис Т.С., Дурос В., Михалопулос А., Пападопулос В.Н., Парамитиотис Д., Харлафтис Н. Изменения внутрибрюшного давления после чрескожного дренирования большой псевдокисты поджелудочной железы. БМК Гастроэнтерол. 2009 г.;9:42. [Бесплатная статья PMC] [PubMed] [Google Scholar]
14. De Laet IE, Malbrain M. Современные представления о внутрибрюшной гипертензии и абдоминальном компартмент-синдроме. Мед Интенсив. 2007; 31:88–99. [PubMed] [Google Scholar]
15. Санчес Н.К., Тенофски П.Л., Дорт Дж.М., Шен Л.И., Хелмер С.Д., Смит Р.С. Что такое нормальное внутрибрюшное давление? Am Surg. 2001; 67: 243–8. [PubMed] [Google Scholar]
2001; 67: 243–8. [PubMed] [Google Scholar]
16. Лернер С.М. Обзорная статья: синдром абдоминального компартмента. Алимент Фармакол. 2008; 28: 377–84. [PubMed] [Академия Google]
17. Читэм М.Л., Уайт М.В., Сагрейвс С.Г., Джонсон Д.Л., Блок Э.Ф. Абдоминальное перфузионное давление: лучший параметр для оценки внутрибрюшной гипертензии. J Травма. 2000;49:621–6. [PubMed] [Google Scholar]
18. Sugrue M, Jones F, Deane SA, Bishop G, Bauman A, Hillman K. Внутрибрюшная гипертензия является независимой причиной послеоперационной почечной недостаточности. Арка Сур. 1999; 134:1082–5. [PubMed] [Google Scholar]
19. Сугрю М. Абдоминальный компартмент-синдром. Curr Opin Crit Care. 2005; 11: 333–38. [PubMed] [Академия Google]
20. Ламберт Д.М., Марсо С., Форс Р.А. Внутрибрюшное давление при морбидном ожирении. Обес Сур. 2005; 15:1225–32. [PubMed] [Google Scholar]
21. Карлотти А., Карвалью В. Абдоминальный компартмент-синдром: обзор. Pediatr Crit Care Med. 2009;10:115–20. [PubMed] [Google Scholar]
2009;10:115–20. [PubMed] [Google Scholar]
22. Malbrain ML, Deeren D, De Potter TJ. Внутрибрюшная гипертензия у тяжелобольных: пора обратить внимание. Curr Opin Crit Care. 2005; 11: 156–71. [PubMed] [Академия Google]
23. Grillner S, Nilsson J, Thorstensson A. Изменения внутрибрюшного давления при естественных движениях человека. Acta Physiol Scand. 1978; 103: 275–83. [PubMed] [Google Scholar]
24. Balogh Z, Moore FA, Moore EE, Biffl WL. Синдром вторичного абдоминального компартмента: потенциальная угроза для всех врачей-травматологов. Рана. 2007; 38: 272–9. [PubMed] [Google Scholar]
25. Wilson M, Dziewulski P. Тяжелое желудочно-кишечное кровотечение и ишемический некроз тонкой кишки у ребенка с 70% ожогами полной толщины: клинический случай. Бернс. 2001; 27: 763–6. [PubMed] [Академия Google]
26. Cheatham ML, Malbrain ML, Kirkpatrick A, Sugrue M, Parr M, De Waele J, et al. Результаты Международной конференции экспертов по внутрибрюшной гипертензии и абдоминальному компартмент-синдрому. II. Рекомендации. Интенсивная терапия Мед. 2007; 33: 951–62. [PubMed] [Google Scholar]
II. Рекомендации. Интенсивная терапия Мед. 2007; 33: 951–62. [PubMed] [Google Scholar]
27. Sugrue M, Bauman A, Jones F, Bishop G, Flabouris A, Parr M, et al. Клиническое обследование является неточным предиктором внутрибрюшного давления. Мир J Surg. 2002; 26:1428–31. [PubMed] [Академия Google]
28. Мальбрейн МЛ. Внутрибрюшное давление у тяжелобольных. Curr Opin Crit Care. 2000; 6: 17–29. [Google Scholar]
29. Schachtrupp A, Henzler D, Orfao S, Schaefer W, Schwab R, Becker P, et al. Оценка модифицированного пьезорезистивного метода и метода водяных капсул для прямого и непрерывного измерения внутрибрюшного давления на модели свиньи. Крит Уход Мед. 2006; 34:74–50. [PubMed] [Google Scholar]
30. Мальбрейн М. Различные методы измерения внутрибрюшного давления (ВБД): время для критической переоценки. Интенсивная терапия Мед. 2004; 30: 357–71. [PubMed] [Академия Google]
31. Шир В., Рознер М.Х. Острая почечная недостаточность вследствие синдрома абдоминального компартмента. J Нефрол. 2006; 19: 556–65. [PubMed] [Google Scholar]
J Нефрол. 2006; 19: 556–65. [PubMed] [Google Scholar]
32. Рид С.Ф., Бритт Р.К., Коллинз Дж., Вейретер Л., Коул Ф., Бритт Л.Д. Агрессивное наблюдение и ранняя катетерная терапия при лечении внутрибрюшной гипертензии. J Травма. 2006; 61: 1359–65. [PubMed] [Google Scholar]
33. De Waele JJ, Cheatham ML, Malbrain ML, Kirkpatrick AW, Sugrue M, Balogh Z, et al. Рекомендации для исследований Международной конференции экспертов по внутрибрюшной гипертензии и абдоминальному компартмент-синдрому. Акта Клин Белг. 2009 г.;64:203–9. [PubMed] [Google Scholar]
34. Cheatham ML. Неоперативное лечение внутрибрюшной гипертензии и синдрома абдоминального компартмента. Мир J Surg. 2009; 33:1116–22. [PubMed] [Google Scholar]
35. Malbrain ML, Chiumello D, Pelosi P, Bihari D, Innes R, Ranieri VM, et al. Частота и прогноз интраабдоминальной гипертензии в смешанной популяции больных в критическом состоянии: многоцентровое эпидемиологическое исследование. Крит Уход Мед. 2005; 33: 315–22. [PubMed] [Академия Google]
[PubMed] [Академия Google]
36. Читэм М.Л. Абдоминальный компартмент-синдром: патофизиология и определения. Scand J Trauma Resusc Emerg Med. 2009;17:10. [Бесплатная статья PMC] [PubMed] [Google Scholar]
37. Malbrain ML, De laet IE. Внутрибрюшная гипертензия: развитие концепций. Клин Грудь Med. 2009; 30:45–70. [PubMed] [Google Scholar]
38. Каштан Дж., Грин Дж.Ф., Парсонс Э.К., Холкрофт Дж.В. Гемодинамический эффект повышенного внутрибрюшного давления. J Surg Res. 1981; 30: 249–55. [PubMed] [Академия Google]
39. Ridings PC, Bloomfield GL, Blocher CR, Sugerman HJ. Сердечно-легочные эффекты повышенного внутрибрюшного давления до и после увеличения внутрисосудистого объема. J Травма. 1995; 39:1071–5. [PubMed] [Google Scholar]
40. Richardson JD, Trinkle JK. Гемодинамические и дыхательные изменения с повышением внутрибрюшного давления. J Surg Res. 1976; 20: 401–4. [PubMed] [Google Scholar]
41. Malbrain ML, Cheatham ML. Кардиоваскулярные эффекты и маркеры оптимальной преднагрузки при внутрибрюшной гипертензии. В: Винсент Дж. Л., редактор. Ежегодник интенсивной терапии и неотложной медицины. Берлин: Спрингер; 2004. стр. 519.–43. [Google Scholar]
В: Винсент Дж. Л., редактор. Ежегодник интенсивной терапии и неотложной медицины. Берлин: Спрингер; 2004. стр. 519.–43. [Google Scholar]
42. Cheatham M, Malbrain M. Сердечно-сосудистые последствия повышенного внутрибрюшного давления. В: Иватури Р., Читэм М., Мальбрейн М., Сугрю М., редакторы. Абдоминальный компартмент-синдром. Джорджтаун: Landes Bioscience; 2006. С. 89–104. [Google Scholar]
43. Simon RJ, Friedlander MH, Ivatury RR, DiRaimo R, Machiedo GW. Кровотечение снижает порог легочной дисфункции, вызванной внутрибрюшной гипертензией. J Травма. 1997; 42: 398–403. [PubMed] [Академия Google]
44. Pelosi P, Ravagnan I, Giurati G, Panigada M, Bottino N, Tredici S, et al. Положительное давление в конце выдоха улучшает дыхательную функцию у тучных, но не у здоровых людей во время анестезии и паралича. Анестезиология. 1999;91:1221–31. [PubMed] [Google Scholar]
45. Sugrue M, D’Amours S. Проблемы с положительным давлением в конце выдоха (PEEP) в связи с абдоминальным компартмент-синдромом (ACS) J Trauma. 2001; 51: 419–20. [PubMed] [Google Scholar]
2001; 51: 419–20. [PubMed] [Google Scholar]
46. Sussman AM, Boyd CR, Williams JS, DiBenedetto RJ. Влияние положительного давления в конце выдоха на внутрибрюшное давление. Саут Мед Дж. 1991;84:697–700. [PubMed] [Google Scholar]
47. Bloomfield GL, Ridings PC, Blocher CR, Marmarou A, Sugerman HJ. Предполагаемая связь между повышенным внутрибрюшным, внутригрудным и внутричерепным давлением. Крит Уход Мед. 1997; 25: 496–503. [PubMed] [Google Scholar]
48. Cheatham ML, Block EF, Nelson LD, Safcsak K. Превосходный предиктор гемодинамического ответа на введение жидкости у пациентов в критическом состоянии. Грудь. 1998; 114:1226–7. [PubMed] [Академия Google]
49. Cheatham ML, Nelson LD, Chang MC, Safcsak K. Индекс конечно-диастолического объема правого желудочка как предиктор состояния преднагрузки у пациентов с положительным давлением в конце выдоха. Крит Уход Мед. 1998; 26:1801–6. [PubMed] [Google Scholar]
50. Schachtrupp A, Graf J, Tons C, Hoer J, Fackeldey V, Schumpelick V. Истощение внутрисосудистого объема в 24-часовой модели внутрибрюшной гипертензии у свиней. J Травма. 2003; 55: 734–40. [PubMed] [Google Scholar]
Истощение внутрисосудистого объема в 24-часовой модели внутрибрюшной гипертензии у свиней. J Травма. 2003; 55: 734–40. [PubMed] [Google Scholar]
51. Michard F, Alaya S, Zarka V, Bahloul M, Richard C, Teboul JL. Глобальный конечно-диастолический объем как показатель сердечной преднагрузки у пациентов с септическим шоком. Грудь. 2003;124:1900–8. [PubMed] [Google Scholar]
52. Michard F, Teboul JL. Прогнозирование реакции на жидкость у пациентов в отделении интенсивной терапии: критический анализ доказательств. Грудь. 2002; 121:2000–8. [PubMed] [Google Scholar]
53. Duperret S, Lhuillier F, Piriou V, Vivier E, Metton O, Branche P, et al. Повышенное внутрибрюшное давление влияет на дыхательные колебания артериального давления у здоровых свиней с нормоволемией и гиповолемией, находящихся на ИВЛ. Интенсивная терапия Мед. 2007; 33: 163–71. [PubMed] [Академия Google]
54. Мальбрейн М.Л., Де Лаэт И. Функциональная гемодинамика при внутрибрюшной гипертензии: что можно использовать, а что нельзя. Acta Anaesthesiol Scand. 2008; 52: 576–7. [PubMed] [Google Scholar]
Acta Anaesthesiol Scand. 2008; 52: 576–7. [PubMed] [Google Scholar]
55. Barnes GE, Laine GA, Giam PY, Smith EE, Granger HJ. Сердечно-сосудистые реакции на повышение внутрибрюшного гидростатического давления. Am J Physiol. 1985; 248: R208–13. [PubMed] [Google Scholar]
56. Cheatham ML. Абдоминальный компартмент-синдром: патофизиология и определения. Scand J Trauma Resusc Emerg Med. 2009 г.;17:10. [Бесплатная статья PMC] [PubMed] [Google Scholar]
57. Goodale RL, Beebe DS, McNevin MP, Boyle M, Letourneau JG, Abrams JH, et al. Гемодинамические, респираторные и метаболические эффекты лапароскопической холецистэктомии. Am J Surg. 1993; 166: 533–7. [PubMed] [Google Scholar]
58. Watson RA, Howdieshell TR. Абдоминальный компартмент-синдром. South Med J. 1998; 91: 326–32. [PubMed] [Google Scholar]
59. MacDonnell SP, Lalude OA, Davidson AC. Абдоминальный компартмент-синдром: физиологические и клинические последствия повышенного внутрибрюшного давления. J Am Coll Surg. 1996;183:419–20. [PubMed] [Google Scholar]
1996;183:419–20. [PubMed] [Google Scholar]
60. Ranieri VM, Brienza N, Santostasi S, Puntillo F, Mascia L, Vitale N, et al. Нарушение механики легких и грудной клетки у пациентов с острым респираторным дистресс-синдромом: роль вздутия живота. Am J Respir Crit Care Med. 1997; 156:1082–91. [PubMed] [Google Scholar]
61. Gattinoni L, Pelosi P, Suter PM, Pedoto A, Vercesi P, Lissoni A. Острый респираторный дистресс-синдром, вызванный легочным и внелегочным заболеванием. Различные синдромы? Am J Respir Crit Care Med. 1998;158:3–11. [PubMed] [Google Scholar]
62. Quintel M, Pelosi P, Caironi P, Meinhardt JP, Luecke T, Herrmann P, et al. Повышение внутрибрюшного давления усиливает отек легких при повреждении легких, вызванном олеиновой кислотой. Am J Respir Crit Care Med. 2004; 169: 534–41. [PubMed] [Google Scholar]
63. Richards WO, Scovill W, Shin B, Reed W. Острая почечная недостаточность, связанная с повышением внутрибрюшного давления. Энн Сург. 1983; 197: 183–187. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
64. Шенаски Дж.Х. Почечные гемодинамические и функциональные эффекты внешнего противодавления. Хирургический гинекологический акушер. 1972; 134: 253–8. [PubMed] [Google Scholar]
65. Doty JM, Saggi BH, Blocher CR, Fakhry I, Gehr T, Sica D, et al. Влияние повышенного паренхиматозного давления на функцию почек. J Травма. 2000;48:874–7. [PubMed] [Google Scholar]
66. Doty JM, Saggi BH, Sugerman HJ, Blocher CR, Pin R, Fakhry I, et al. Влияние повышенного почечного венозного давления на функцию почек. J Травма. 1999;47:1000–3. [PubMed] [Google Scholar]
67. Sugrue M, Hallal A, D’Amours S. Гипертензия внутрибрюшного давления и почки. В: Иватури Р., Читэм М., Мальбрейн М., Сугрю М., редакторы. Абдоминальный компартмент-синдром. Джорджтаун (Техас): Landes Bioscience; 2006. С. 119–28. [Google Scholar]
68. Sugrue M, Buist MD, Hourihan F, Deane S, Bauman A, Hillman K. Проспективное исследование внутрибрюшной гипертензии и функции почек после лапаротомии. Бр Дж Сур. 1995; 82: 235–8. [PubMed] [Академия Google]
Бр Дж Сур. 1995; 82: 235–8. [PubMed] [Академия Google]
69. Kirkpatrick AW, Colistro R, Laupland KB, Fox DL, Konkin DE, Kock V, et al. Реакция почечного артериального резистивного индекса на внутрибрюшную гипертензию на модели свиньи. Крит Уход Мед. 2006; 35: 207–13. [PubMed] [Google Scholar]
70. Bloomfield GL, Blocher CR, Fakhry IF, Sica DA, Sugerman HJ. Повышенное внутрибрюшное давление увеличивает активность ренина в плазме и уровень альдостерона. J Травма. 1997; 42: 997–1004. [PubMed] [Google Scholar]
71. Улятт БД. Повышенное внутрибрюшное давление. Ауст Анаес. 1992;10:108–14. [Google Scholar]
72. Лука А., Феу Ф., Гарсия-Паган Дж. К., Хименес В., Арройо В., Бош Дж. и др. Благоприятное влияние тотального парацентеза на внутренностную гемодинамику у больных циррозом печени с напряженным асцитом. Гепатология. 1994; 20:30–3. [PubMed] [Google Scholar]
73. Smith JH, Merrell RC, Raffin TA. Лечение послеоперационной анурии декомпрессивной целиотомией. Arch Intern Med. 1985; 145: 553–4. [PubMed] [Google Scholar]
Arch Intern Med. 1985; 145: 553–4. [PubMed] [Google Scholar]
74. Unsal MA, Imamoğlu M, Cay A, Kadioglu M, Aydin S, Ulku C, et al. Острые изменения биохимии, морфологии и сократительной способности изолированного мочевого пузыря крыс вследствие повышения внутрибрюшного давления. Гинеколь Обстет Инвест. 2006;61:179–87. [PubMed] [Google Scholar]
75. Friedlander MH, Simon RJ, Ivatury R, DiRaimo R, Machiedo GW. Влияние кровоизлияния на кровоток в верхней брыжеечной артерии при повышении внутрибрюшного давления. J Травма. 1998; 45: 433–89. [PubMed] [Google Scholar]
76. Caldwell CB, Ricotta JJ. Изменения висцерального кровотока при повышении внутрибрюшного давления. J Surg Res. 1987; 43:14–20. [PubMed] [Google Scholar]
77. Рейнтам А., Парм П., Китус Р., Старкопф Дж., Керн Х. Оценка желудочно-кишечной недостаточности у пациентов в критическом состоянии: проспективное обсервационное исследование. Критический уход. 2008;12:R90. [Бесплатная статья PMC] [PubMed] [Google Scholar]
78. Sugrue M, Jones F, Janjua KJ, Deane SA, Bristow P, Hillman K. Временное закрытие брюшной полости: проспективная оценка его воздействия на почки и дыхательные пути физиология. J Травма. 1998;45:914–21. [PubMed] [Google Scholar]
Sugrue M, Jones F, Janjua KJ, Deane SA, Bristow P, Hillman K. Временное закрытие брюшной полости: проспективная оценка его воздействия на почки и дыхательные пути физиология. J Травма. 1998;45:914–21. [PubMed] [Google Scholar]
79. Дибель Л.Н., Дульчавский С.А., Браун В.Дж. Спланхническая ишемия и бактериальная транслокация при синдроме абдоминального компартмента. J Травма. 1997; 43:852–5. [PubMed] [Google Scholar]
80. Дибель Л.Н., Дульчавский С.А., Уилсон Р.Ф. Влияние повышенного внутрибрюшного давления на кровоток в брыжеечных артериях и слизистой оболочке кишечника. J Травма. 1992;33:45–8. [PubMed] [Google Scholar]
81. Malbrain ML, De Laet I. СПИД приближается к вашему отделению интенсивной терапии: будьте готовы к острому повреждению кишечника и острому кишечному дистресс-синдрому. Интенсивная терапия Мед. 2008; 34:1565–9. [PubMed] [Google Scholar]
82. Хрипун А.И., Эттингер А.П., Чадаев А.П., Татьков С.С. Изменения сократительной и биоэлектрической активности тонкого кишечника крыс в условиях повышенного внутрибрюшного давления. Изв Акад Наук Сер Биол. 1997; 5: 596–602. [PubMed] [Академия Google]
Изв Акад Наук Сер Биол. 1997; 5: 596–602. [PubMed] [Академия Google]
83. Доддс В.Дж., Хоган В.Дж., Стюарт Э.Т., Стеф Дж.Дж., Арндорфер Р.К. Влияние повышенного внутрибрюшного давления на перистальтику пищевода. J Appl Physiol. 1974; 37: 378–83. [PubMed] [Google Scholar]
84. Unsal MA, Imamoglu M, Kadioglu M, Aydin S, Ulku C, Kesim M, et al. Острые изменения биохимии, морфологии и сократительной способности изолированного терминального отдела подвздошной кишки у крыс из-за повышения внутрибрюшного давления. Фармакол рез. 2006; 53: 135–41. [PubMed] [Google Scholar]
85. Mogilner JG, Bitterman H, Hayari L, Brod V, Coran AG, Shaoul R, et al. Влияние повышенного внутрибрюшного давления и гипероксии на кровоток в воротной вене, пролиферацию гепатоцитов и апоптоз в модели крыс. Eur J Pediatr Surg. 2008;18:380–6. [PubMed] [Академия Google]
86. Дибель Л.Н., Уилсон Р.Ф., Дульчавский С.А., Сакс Дж. Влияние повышенного внутрибрюшного давления на печеночный артериальный, портальный венозный и печеночный микроциркуляторный кровоток. J Травма. 1992; 33: 279–82. [PubMed] [Google Scholar]
J Травма. 1992; 33: 279–82. [PubMed] [Google Scholar]
87. Wendon J, Biancofiore G, Auzinger G. Внутрибрюшная гипертензия и печень. В: Иватури Р., Читэм М., Мальбрейн М., Сугрю М., редакторы. Абдоминальный компартмент-синдром. Джорджтаун (Техас): Landes Bioscience; 2006. С. 138–43. [Академия Google]
88. Cade R, Wagemaker H, Vogel S, Mars D, Hood-Lewis D, Privette M, et al. Гепаторенальный синдром. Изучение влияния объема сосудов и внутрибрюшинного давления на функцию почек и печени. Am J Med. 1987; 82: 427–38. [PubMed] [Google Scholar]
89. Накатани Т., Сакамото Ю., Канеко И., Андо Х., Кобаяши К. Влияние внутрибрюшной гипертензии на энергетический метаболизм печени на модели кролика. J Травма. 1998; 44: 446–53. [PubMed] [Google Scholar]
90. Luca A, Cirera I, García-Pagan JC, Feu F, Pizcueta P, Bosch J, et al. Гемодинамические эффекты острых изменений внутрибрюшного давления у больных циррозом печени. Гастроэнтерология. 1993;104:222–7. [PubMed] [Google Scholar]
91. Burchard KW, Ciombor DM, McLeod MK, Slothman GJ, Gann DS. Положительное давление в конце выдоха с повышенным внутрибрюшным давлением. Хирургический гинекологический акушер. 1985; 161: 313–8. [PubMed] [Google Scholar]
Burchard KW, Ciombor DM, McLeod MK, Slothman GJ, Gann DS. Положительное давление в конце выдоха с повышенным внутрибрюшным давлением. Хирургический гинекологический акушер. 1985; 161: 313–8. [PubMed] [Google Scholar]
92. Biancofiore G, Bindi ML, Boldrini A, Consani G, Bisà M, Esposito M, et al. Внутрибрюшное давление у реципиентов трансплантата печени: частота и клиническое значение. Пересадка Proc. 2004; 36: 547–9. [PubMed] [Академия Google]
93. Biancofiore G, Bindi ML, Romanelli AM, Boldrini A, Consani G, Bisà M, et al. Мониторинг внутрибрюшного давления у реципиентов трансплантата печени: проспективное исследование. Интенсивная терапия Мед. 2003; 29:30–6. [PubMed] [Google Scholar]
94. Deeren DH, Dits H, Malbrain ML. Взаимосвязь между внутрибрюшным и внутричерепным давлением при нетравматическом поражении головного мозга. Интенсивная терапия Мед. 2005; 31: 1577–81. [PubMed] [Google Scholar]
95. Джозефс Л.Г., Эсте-Макдональд Дж.Р., Биркетт Д.Х., Хирш Э. Ф. Диагностическая лапароскопия повышает внутричерепное давление. J Травма. 1994;36:815–8. [PubMed] [Google Scholar]
Ф. Диагностическая лапароскопия повышает внутричерепное давление. J Травма. 1994;36:815–8. [PubMed] [Google Scholar]
96. Bloomfield GL, Ridings PC, Blocher CR, Marmarou A, Sugerman HJ. Влияние повышенного внутрибрюшного давления на внутричерепное и церебральное перфузионное давление до и после увеличения объема. J Травма. 1996;40:936–41. [PubMed] [Google Scholar]
97. Citerio G, Vascotto E, Villa F, Celotti S, Pesenti A. Синдром индуцированного абдоминального компартмента увеличивает внутричерепное давление у пациентов с нейротравмой: проспективное исследование. Крит Уход Мед. 2001;29: 1466–71. [PubMed] [Google Scholar]
98. Citerio G, Berra L. Внутрибрюшная гипертензия и центральная нервная система. В: Иватури Р., Читэм М., Мальбрейн М., Сугрю М., редакторы. Абдоминальный компартмент-синдром. Джорджтаун (Техас): Landes Bioscience; 2006. стр. 144–56. [Google Scholar]
99. Халверсон А.Л., Барретт В.Л., Иглесиас А.Р., Ли В.Т., Гарбер С.М., Сакьер Дж.М. Снижение всасывания спинномозговой жидкости при абдоминальной инсуффляции. Surg Endosc. 1999; 13: 797–800. [PubMed] [Академия Google]
Surg Endosc. 1999; 13: 797–800. [PubMed] [Академия Google]
100. Иргау И., Койфман Ю., Тикеллис Д.И. Элективный интраоперационный мониторинг внутричерепного давления при лапароскопической холецистэктомии. Арка Сур. 1995; 130:1011–3. [PubMed] [Google Scholar]
101. Джозеф Д.К., Даттон Р.П., Аараби Б., Скалея Т.М. Декомпрессивная лапаротомия для лечения трудноизлечимой внутричерепной гипертензии после черепно-мозговой травмы. J Травма. 2004; 57: 687–93. [PubMed] [Google Scholar]
102. Diebel L, Saxe J, Dulchavsky S. Влияние внутрибрюшного давления на кровоток в брюшной стенке. Am Surg. 1992;58:573–5. [PubMed] [Google Scholar]
103. Mutoh T, Lamm WJ, Embree LJ, Hildebrandt J, Albert RK. Объемное вливание вызывает вздутие живота, компрессию легких и жесткость грудной клетки у свиней. J Appl Physiol. 1992; 72: 575–82. [PubMed] [Google Scholar]
104. Догерти Э.Л., Хунъян Лян, Тайчман Д., Хансен-Флашен Дж., Фукс Б.Д. Синдром абдоминального компартмента часто встречается у пациентов отделений интенсивной терапии, получающих реанимацию большого объема. J Интенсивная терапия Мед. 2007;22:294–9. [PubMed] [Google Scholar]
J Интенсивная терапия Мед. 2007;22:294–9. [PubMed] [Google Scholar]
105. Balogh Z, McKinley BA, Holcomb JB, Miller CC, Cocanour CS, Kozar RA, et al. Как первичный, так и вторичный абдоминальный компартмент-синдром можно предсказать на ранней стадии, и они являются предвестниками полиорганной недостаточности. J Травма. 2003; 54: 848–59. [PubMed] [Google Scholar]
106. Иватури Р.Р., Портер Дж.М., Саймон Р.Дж., Ислам С., Джон Р., Шталь В.М. Внутрибрюшная гипертензия после опасной для жизни проникающей травмы живота: профилактика, заболеваемость и клиническое значение рН слизистой оболочки желудка. J Травма. 1998;44:1016–21. [PubMed] [Google Scholar]
107. Balogh Z, Caldwell E, Heetveld M, D’Amours S, Schlaphoff G, Harris I, et al. Институциональные практические рекомендации по ведению гемодинамической нестабильности, связанной с переломом таза: имеют ли они значение? J Травма. 2005; 58: 778–82. [PubMed] [Google Scholar]
108. Horwood J, Akbar F, Maw A. Начальный опыт лапаростомии с немедленной вакуумной терапией у пациентов с тяжелым перитонитом. Энн Р. Колл Surg Engl. 2009; 91: 681–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Энн Р. Колл Surg Engl. 2009; 91: 681–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
109. Сугрю М., Бухкари З.Ю. Внутрибрюшное давление и абдоминальный компартмент-синдром в неотложной общей хирургии. Мир J Surg. 2009;33:1123–7. [PubMed] [Google Scholar]
110. Polat C, Arikan Y, Vatansev C, Akbulut G, Yilmaz S, Dilek FH, et al. Влияние повышенного внутрибрюшного давления на анастомоз толстой кишки. Surg Endosc. 2002; 16:1314–9. [PubMed] [Google Scholar]
111. Иватури Р.Р., Сугерман Х.Дж. Абдоминальный компартмент-синдром: век спустя, не пора ли обратить внимание? Крит Уход Мед. 2000; 28:2137–8. [PubMed] [Академия Google]
112. Mayberry JC, Mullins RJ, Crass RA. Профилактика абдоминального компартмент-синдрома путем закрытия рассасывающимся сетчатым протезом. Арка Сур. 1997; 9: 957–61. [PubMed] [Google Scholar]
113. Hakkiluoto A, Hannukainen J. Открытое лечение пациентов с внутрибрюшными абсцессами или разлитым перитонитом с помощью сетки и молнии. Евро J Surg. 1992; 158:403–5. [PubMed] [Google Scholar]
Евро J Surg. 1992; 158:403–5. [PubMed] [Google Scholar]
114. Акерс Д.Л., Фаул Р.Дж., Кемпчински Р.Ф. Временное закрытие брюшной стенки пластинами из силиконовой резины после оперативного лечения разрыва аневризмы брюшной аорты. J Vasc Surg. 1991;14:48–52. [PubMed] [Google Scholar]
115. Wild JM, Loundon MA. Модифицированный сэндвич Opsite для временного закрытия брюшной полости: нетравматичный опыт. Энн Р. Колл Surg Engl. 2007; 89: 57–61. [Бесплатная статья PMC] [PubMed] [Google Scholar]
116. Кирштейн Б., Рой-Шапира А., Ланцберг Л., Мизрахи С. Использование «мешка Боготы» для временного закрытия брюшной полости у пациентов со вторичным перитонитом. AM J Surg. 2007; 73: 249–52. [PubMed] [Google Scholar]
117. Pliakos I, Papavramidis TS, Mihalopoulos N, Koulouris H, Kesisoglou I, Konstantinos Sapalidis, et al. Вакуумное закрытие при тяжелом абдоминальном сепсисе с последовательным закрытием фасции с удерживающими швами или без него: клиническое испытание. Операция. 2010 В печати. [PubMed] [Академия Google]
Операция. 2010 В печати. [PubMed] [Академия Google]
118. Mayberry JC, Burgess EA, Goldman RK. Кожно-кишечный свищ и вентральная грыжа после закрытия рассасывающимся сетчатым протезом по поводу травмы: чистая правда. J Травма. 2004; 1: 157–62. [PubMed] [Google Scholar]
119. Nagy KK, Fildes JJ, Mahr C. Опыт использования трех протезных материалов для временного закрытия брюшной стенки. Am J Surg. 1996; 5: 331–5. [PubMed] [Google Scholar]
120. Текин С., Текин А., Кучуккарталлар Т., Чакир М., Картал А. Использование хориоамниотической мембраны вместо боготского мешка при открытой брюшной полости: как мне это сделать? Мир J Гастроэнтерол. 2008;14:815–6. [Бесплатная статья PMC] [PubMed] [Google Scholar]
121. Stone HH, Fabian TC, Turkleson ML, Jurkiewicz MJ. Лечение острой полнослойной потери брюшной стенки. Энн Сург. 1981; 193: 612–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
122. Фрай Д.Э., Ослер Т. Соображения брюшной стенки и осложнения в повторной хирургии. Surg Clin North Am. 1991;71:1–11. [PubMed] [Google Scholar]
Surg Clin North Am. 1991;71:1–11. [PubMed] [Google Scholar]
123. Miller PR, Thompson JT, Faler BJ, Meredith JW, Chang MC. Позднее закрытие фасции вместо вентральной грыжи: следующий шаг в лечении открытой брюшной полости. J Травма. 2002; 53: 842–9.. [PubMed] [Google Scholar]
124. Jernigan TW, Fabian TC, Croce MA, Moore N, Pritchard FE, Minard G, et al. Этапное лечение гигантских дефектов брюшной стенки: неотложные и отдаленные результаты. Энн Сург. 2003; 238:349–55. [Бесплатная статья PMC] [PubMed] [Google Scholar]
125. Deligiannidis N, Papavramidis T, Papavramidis S, Gkoutzamanis G, Kessissoglou I, Papavasiliou I, et al. Два разных протезных материала при лечении больших дефектов брюшной стенки. NZ Med J. 2008; 121:19–24. [PubMed] [Google Scholar]
126. Bee TK, Croce MA, Magnotti LJ, Zarzaur BL, Maish GO, 3rd, Minard G, et al. Методы временного закрытия брюшной полости: проспективное рандомизированное исследование, сравнивающее полиглактин 910 меш и закрытие с помощью вакуума. J Травма. 2008; 65: 337–42. [PubMed] [Google Scholar]
J Травма. 2008; 65: 337–42. [PubMed] [Google Scholar]
127. Cothren CC, Moore EE, Johnson JL, Moore JB, Burch JM. Стопроцентная фасциальная аппроксимация с последовательным абдоминальным закрытием открытой брюшной полости. Am J Surg. 2006; 192: 238–42. [PubMed] [Академия Google]
128. Reimer MW, Yelle JD, Reitsma B, Doumit G, Allen MA, Bell MS. Лечение открытых ран брюшной полости с помощью динамической фасциальной шовной системы. Может J Surg. 2008; 51: 209–14. [Бесплатная статья PMC] [PubMed] [Google Scholar]
129. Tieu BH, Cho SD, Luem N, Riha G, Mayberry J, Schreiber MA. Использование заплаты Виттмана способствует высокой частоте фасциального закрытия у пациентов с тяжелыми травмами и у пациентов в критическом состоянии после неотложной хирургии. J Травма. 2008; 65: 865–70. [PubMed] [Академия Google]
130. Poulakidas S, Kowal-Vern A. Техника разделения компонентов для реконструкции брюшной стенки у ожоговых больных с декомпрессивной лапаротомией. J Травма. 2009;67:1435–8. [PubMed] [Google Scholar]
2009;67:1435–8. [PubMed] [Google Scholar]
131. Kushimoto S, Miyauchi M, Yokota H, Kawai M. Хирургия контроля повреждений и открытое лечение брюшной полости: последние достижения и наш подход. J Nippon Med Sch. 2009; 76: 280–90. [PubMed] [Google Scholar]
132. Консультативная группа Open Abdomen. Ведение открытой брюшной полости: от первоначальной операции до окончательного закрытия. Am Surg. 2009 г.;75:С1–22. [PubMed] [Google Scholar]
133. Cheatham ML, Safcsak K. Улучшает ли выживаемость развивающееся лечение внутрибрюшной гипертензии и абдоминального компартмент-синдрома? Крит Уход Мед. 2010;38:402–7. [PubMed] [Google Scholar]
Внутрибрюшная гипертензия и абдоминальный компартмент-синдром у пациентов, поступивших в отделение интенсивной терапии | Анналы интенсивной терапии
- Исследования
- Открытый доступ
- Опубликовано:
- Марие Смит Orcid: Orcid.org/0000-0002-4658-7287 1 ,
- Bart Koopman 1 ,
- Willem Dieperink 1 ,
- января. ,
- Матийс ван Мерс 1 и
- …
- Ян Г. Зейлстра 1
Анналы интенсивной терапии том 10 , Номер статьи: 130 (2020) Процитировать эту статью
8826 доступов
7 цитирований
20 Альтметрика
Сведения о показателях
Abstract
История вопроса
Внутрибрюшная гипертензия часто присутствует у пациентов в критическом состоянии и является независимым предиктором смертности. Факторы риска внутрибрюшной гипертензии и синдрома абдоминального компартмента широко исследованы. Однако данные о распространенности и исходах у пациентов с высоким риском отсутствуют. Наши цели в этом исследовании заключались в изучении распространенности и исходов внутрибрюшной гипертензии и абдоминального компартмент-синдрома у пациентов с высоким риском в проспективном обсервационном одноцентровом когортном исследовании.
Факторы риска внутрибрюшной гипертензии и синдрома абдоминального компартмента широко исследованы. Однако данные о распространенности и исходах у пациентов с высоким риском отсутствуют. Наши цели в этом исследовании заключались в изучении распространенности и исходов внутрибрюшной гипертензии и абдоминального компартмент-синдрома у пациентов с высоким риском в проспективном обсервационном одноцентровом когортном исследовании.
Результаты
В период с марта 2014 г. по март 2016 г. мы включили 503 пациента, 307 мужчин (61%) и 196 женщин (39%). В исследование были включены пациенты, поступившие в отделение интенсивной терапии с диагнозом панкреатит, плановая или экстренная операция на брюшной аорте, ортотопическая трансплантация печени, другие плановые или экстренные обширные абдоминальные операции и травма. У 164 (33%) пациентов развилась внутрибрюшная гипертензия, а у 18 (3,6%) пациентов развился абдоминальный компартмент-синдром. Наиболее высокая распространенность абдоминального компартмент-синдрома наблюдалась при панкреатите (57%), за которым следовали ортотопическая трансплантация печени (7%) и операции на брюшной аорте (5%). Продолжительность пребывания в реанимации увеличилась в 4 раза у больных с внутрибрюшной гипертензией и в 9 разпри абдоминальном компартмент-синдроме по сравнению с пациентами с нормальным внутрибрюшным давлением. Частота заместительной почечной терапии была выше при абдоминальном компартмент-синдроме (38,9%) и внутрибрюшной гипертензии (8,2%) по сравнению с пациентами с нормальным внутрибрюшным давлением (1,2%). И смертность при интенсивной терапии, и 90-дневная смертность были значительно выше при внутрибрюшной гипертензии (4,8% и 15,2%) и синдроме абдоминального компартмента (16,7% и 38,9%) по сравнению с нормальным внутрибрюшным давлением (1,2% и 7,1%). Индекс массы тела (отношение шансов 1,08, 95% доверительный интервал 1,03–1,13), искусственная вентиляция легких при поступлении (ОШ 3,52, 95% ДИ 2,08–5,96) и оценка по шкале Apache IV (ОШ 1,03, 95% ДИ 1,02–1,04) были независимыми факторами риска развития внутрибрюшного гипертензия или абдоминальный компартмент-синдром.
Продолжительность пребывания в реанимации увеличилась в 4 раза у больных с внутрибрюшной гипертензией и в 9 разпри абдоминальном компартмент-синдроме по сравнению с пациентами с нормальным внутрибрюшным давлением. Частота заместительной почечной терапии была выше при абдоминальном компартмент-синдроме (38,9%) и внутрибрюшной гипертензии (8,2%) по сравнению с пациентами с нормальным внутрибрюшным давлением (1,2%). И смертность при интенсивной терапии, и 90-дневная смертность были значительно выше при внутрибрюшной гипертензии (4,8% и 15,2%) и синдроме абдоминального компартмента (16,7% и 38,9%) по сравнению с нормальным внутрибрюшным давлением (1,2% и 7,1%). Индекс массы тела (отношение шансов 1,08, 95% доверительный интервал 1,03–1,13), искусственная вентиляция легких при поступлении (ОШ 3,52, 95% ДИ 2,08–5,96) и оценка по шкале Apache IV (ОШ 1,03, 95% ДИ 1,02–1,04) были независимыми факторами риска развития внутрибрюшного гипертензия или абдоминальный компартмент-синдром.
Выводы
Распространенность абдоминального компартмент-синдрома составила 3,6%, а распространенность внутрибрюшной гипертензии — 33% в этой когорте пациентов высокого риска. Заболеваемость и смертность увеличивались при наличии внутрибрюшной гипертензии или синдрома абдоминального компартмента. Пациент с наибольшим риском ИАГ или ОКС в этой когорте высокого риска имеет ИМТ > 30 кг/м 2 и поступил в отделение интенсивной терапии после экстренной абдоминальной операции или с диагнозом панкреатит.
Заболеваемость и смертность увеличивались при наличии внутрибрюшной гипертензии или синдрома абдоминального компартмента. Пациент с наибольшим риском ИАГ или ОКС в этой когорте высокого риска имеет ИМТ > 30 кг/м 2 и поступил в отделение интенсивной терапии после экстренной абдоминальной операции или с диагнозом панкреатит.
История вопроса
Внутрибрюшная гипертензия (ВБГ) часто присутствует у пациентов в критическом состоянии и является независимым предиктором смертности [1,2,3]. Когда ИАГ прогрессирует до абдоминального компартмент-синдрома (ОКС), органная недостаточность возникает по определению [4] и смертность очень высока [5]. В рекомендациях Всемирного общества абдоминального компартмент-синдрома (WSACS, в настоящее время WSACS — Общество абдоминального компартмента) рекомендуется проводить протоколированный мониторинг внутрибрюшного давления (ВБД) у пациентов с высоким риском каждые 4–6 ч [4, 6] . Однако 18–82% врачей указывают, что они не измеряют ВБД [7, 8], поэтому соблюдение этих рекомендаций может быть улучшено. Современные данные о частоте и прогнозе ИАГ и ОКС могут еще больше улучшить распознавание пациентов с риском и, таким образом, внести вклад в оптимизацию мониторинга и лечения. Лучшее понимание рисков, связанных с ИАГ, необходимо для улучшения результатов [9].].
Современные данные о частоте и прогнозе ИАГ и ОКС могут еще больше улучшить распознавание пациентов с риском и, таким образом, внести вклад в оптимизацию мониторинга и лечения. Лучшее понимание рисков, связанных с ИАГ, необходимо для улучшения результатов [9].].
Недавно данные о распространенности ВБГ и ОКС были обобщены Padar et al. [5]. Данные 285 последовательных пациентов из смешанного медико-хирургического отделения интенсивной терапии (ОИТ) показали, что ОКС возникал у 3% пациентов [3]. В смешанном многоцентровом отделении интенсивной терапии из 491 пациента ОКС развился у 6% пациентов. Различие между исследованиями объяснялось разным набором случаев [10].
Факторы риска ВБГ и ОКС широко исследованы и включают установленный диагноз панкреатита, абдоминальную хирургию, кишечную непроходимость, внутрибрюшную инфекцию и пациентов, перенесших тяжелую травму [11, 12]. В крупнейшем на сегодняшний день исследовании Reintam Blaser et al. сообщили о факторах риска ИАГ у 563 пациентов на ИВЛ [13]. Индекс массы тела (ИМТ) > 30 кг/м 2 , положительное давление в конце выдоха (ПДКВ) > 10 смH 2 O, отношение парциального давления кислорода в артериальной крови к доле кислорода во вдыхаемом воздухе (PaO2/FiO2) < 300, применение вазопрессоров/инотропов, панкреатит, печеночная недостаточность/ цирроз печени с асцитом, желудочно-кишечное (ЖК) кровотечение и лапаротомия в день поступления были факторами риска ИАГ. Примечательно, что в качестве параметра исхода сообщалось только о смертности в ОИТ.
Индекс массы тела (ИМТ) > 30 кг/м 2 , положительное давление в конце выдоха (ПДКВ) > 10 смH 2 O, отношение парциального давления кислорода в артериальной крови к доле кислорода во вдыхаемом воздухе (PaO2/FiO2) < 300, применение вазопрессоров/инотропов, панкреатит, печеночная недостаточность/ цирроз печени с асцитом, желудочно-кишечное (ЖК) кровотечение и лапаротомия в день поступления были факторами риска ИАГ. Примечательно, что в качестве параметра исхода сообщалось только о смертности в ОИТ.
Мы провели текущее исследование, чтобы получить больше информации о распространенности и исходах ВБГ и ОКС у пациентов с высоким риском в ОИТ. Нашей целью было сначала изучить распространенность ВБГ и ОКС в когорте пациентов с высоким риском. Во-вторых, мы исследовали заболеваемость путем регистрации частоты заместительной почечной терапии, продолжительности искусственной вентиляции легких, продолжительности пребывания в отделении интенсивной терапии и лечения ОКС. В-третьих, мы зафиксировали смертность в отделении интенсивной терапии и 90-дневная смертность в этой когорте. Наша гипотеза заключалась в том, что в когорте пациентов с высоким риском распространенность ИАГ и ОКС будет выше, чем сообщалось в литературе, для последовательных пациентов, поступивших в ОИТ, и что заболеваемость и смертность будут выше при ИАГ и ОКС, как сообщалось в других исследованиях. когорты. Кроме того, мы предположили, что возможна дальнейшая идентификация пациента с наибольшим риском ВБГ и ОКС в когорте высокого риска.
В-третьих, мы зафиксировали смертность в отделении интенсивной терапии и 90-дневная смертность в этой когорте. Наша гипотеза заключалась в том, что в когорте пациентов с высоким риском распространенность ИАГ и ОКС будет выше, чем сообщалось в литературе, для последовательных пациентов, поступивших в ОИТ, и что заболеваемость и смертность будут выше при ИАГ и ОКС, как сообщалось в других исследованиях. когорты. Кроме того, мы предположили, что возможна дальнейшая идентификация пациента с наибольшим риском ВБГ и ОКС в когорте высокого риска.
Методы
В этом проспективном обсервационном одноцентровом когортном исследовании мы последовательно включали взрослых пациентов с известными факторами риска первичной ВБГ, госпитализированных в отделение интенсивной терапии академической клинической больницы третичного уровня. Тип поступления (плановая абдоминальная хирургия, неотложная абдоминальная хирургия и нехирургическая операция) и два основных диагноза были зарегистрированы при поступлении.
Критериями включения были: основной диагноз панкреатита, плановая или экстренная открытая операция на брюшной аорте, ортотопическая трансплантация печени (ОТП), другие плановые или экстренные обширные абдоминальные операции и травма либо с повреждением живота, либо с комбинацией травмы грудной клетки и таза ( так как у последних пациентов высок риск сочетанной травмы живота). Критериями исключения были: возраст < 18 лет и противопоказания для установки мочевого катетера.
ВБД измеряли сразу после поступления в отделение интенсивной терапии, а затем каждые 4 часа в течение семи дней или до выписки из отделения интенсивной терапии. ВБД измеряли в соответствии со стандартизированным протоколом с использованием 25 мл стерильного физиологического раствора в качестве исходного объема с лобковым симфизом в качестве контрольной точки. Пациенты находились в положении лежа на спине во время измерения ВБД. Если измерение ВБД невозможно было выполнить в положении лежа на спине по соображениям ухода за пациентом, допускается подъем изголовья кровати до 30 градусов.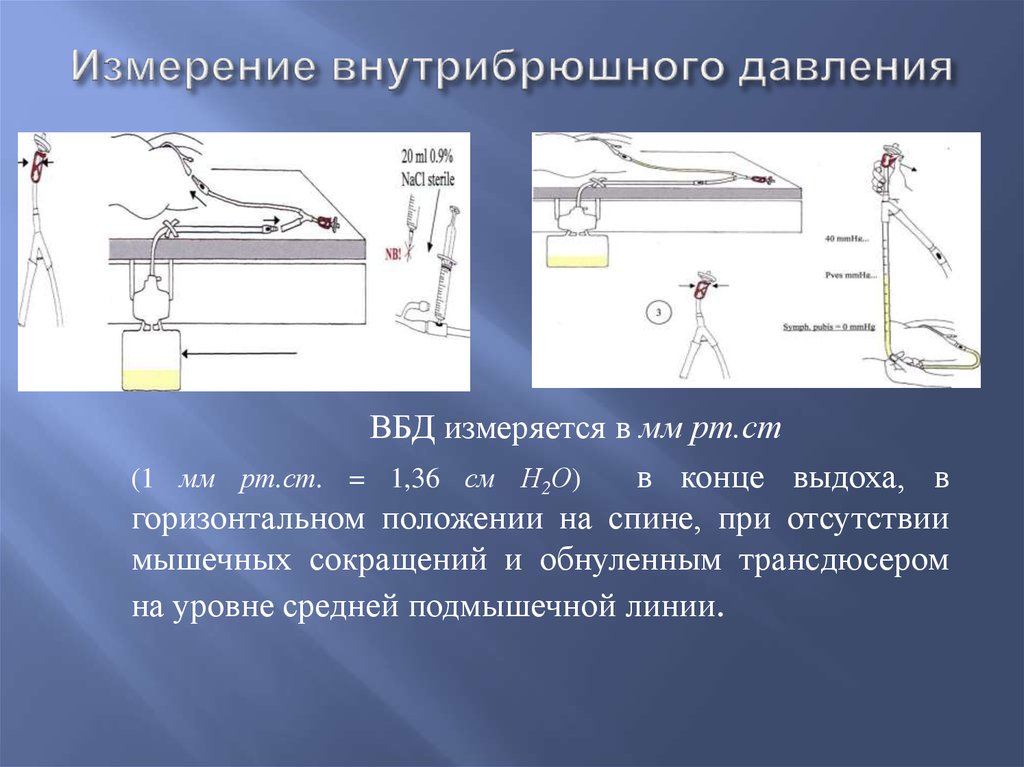 Если ВБД было ≥ 20 мм рт. ст. в любое время, измерение ВБД повторяли через 1 час. Если был диагностирован ОКС (определения ВАГ и ОКС см. в Таблице 1), лечащему врачу оставалось решать вопрос о том, было ли выполнено вмешательство (медикаментозное, интервенционное радиологическое или хирургическое). Возможные вмешательства основывались на рекомендациях WSACS по ведению ОКС [4]. Медикаментозное лечение включало временное прекращение энтерального питания, введение назогастрального зонда и дренирование содержимого желудка, усиление седативного эффекта и/или обезболивания, введение нервно-мышечных блокаторов, установку ректальной канюли или ректальной клизмы и удаление жидкости с помощью диуретиков или заместительной почечной терапии. (РРТ). ЗПТ состояла из непрерывной вено-венозной гемофильтрации (CVVH) или гемодиализа. Интервенционное радиологическое лечение включало дренирование асцита или других абдоминальных скоплений жидкости, а хирургическое лечение включало хирургическую декомпрессию.
Если ВБД было ≥ 20 мм рт. ст. в любое время, измерение ВБД повторяли через 1 час. Если был диагностирован ОКС (определения ВАГ и ОКС см. в Таблице 1), лечащему врачу оставалось решать вопрос о том, было ли выполнено вмешательство (медикаментозное, интервенционное радиологическое или хирургическое). Возможные вмешательства основывались на рекомендациях WSACS по ведению ОКС [4]. Медикаментозное лечение включало временное прекращение энтерального питания, введение назогастрального зонда и дренирование содержимого желудка, усиление седативного эффекта и/или обезболивания, введение нервно-мышечных блокаторов, установку ректальной канюли или ректальной клизмы и удаление жидкости с помощью диуретиков или заместительной почечной терапии. (РРТ). ЗПТ состояла из непрерывной вено-венозной гемофильтрации (CVVH) или гемодиализа. Интервенционное радиологическое лечение включало дренирование асцита или других абдоминальных скоплений жидкости, а хирургическое лечение включало хирургическую декомпрессию. Цель состояла в том, чтобы выполнить хирургическую декомпрессию опытным абдоминальным хирургом в течение 6 часов после неэффективности медикаментозного и интервенционного радиологического лечения при ОКС. Если у больного не было признаков клинического улучшения, по мнению лечащего врача, исследование продолжалось дольше семи дней до улучшения состояния больного.
Цель состояла в том, чтобы выполнить хирургическую декомпрессию опытным абдоминальным хирургом в течение 6 часов после неэффективности медикаментозного и интервенционного радиологического лечения при ОКС. Если у больного не было признаков клинического улучшения, по мнению лечащего врача, исследование продолжалось дольше семи дней до улучшения состояния больного.
Полная таблица
Определения
См. Таблицу 1 для определений IAH, степеней IAH и ACS.
Институциональный наблюдательный совет нашей больницы одобрил исследование (METc 2013/123).
Статистический анализ
Статистический анализ выполнен с использованием IBM SPSS Statistics 22. Для непрерывных переменных был выполнен однофакторный дисперсионный анализ для расчета разницы между группами нормального ВБД, ВБГ и ОКС и между группами планового абдоминального хирургия, неотложная абдоминальная хирургия и нехирургические пациенты. Тесты хи-квадрат на независимость были выполнены для категориальных переменных. Был проведен бинарный логистический регрессионный анализ, чтобы проанализировать, являются ли независимыми факторы риска ВБГ или ОКС, которые были значимы в однофакторном анализе.
Тесты хи-квадрат на независимость были выполнены для категориальных переменных. Был проведен бинарный логистический регрессионный анализ, чтобы проанализировать, являются ли независимыми факторы риска ВБГ или ОКС, которые были значимы в однофакторном анализе.
Результаты
Демография
Во время включения в исследование с 3 марта 2014 г. по 31 марта 2016 г. было включено 503 пациента. Всего за исследуемый период в отделение интенсивной терапии нашей больницы поступило 7703 пациента. ВБД измеряли 5908 раз, из них 127 раз (2%) с подъемом изголовья до 30 градусов. Было включено 339 пациентов после плановой операции (67%), 120 пациентов после неотложной операции (24%) и 44 нехирургических пациента (9%) (таблица 2). Среднее ВБД при поступлении в отделение интенсивной терапии составляло 11,1 мм рт. ст. (стандартное отклонение 5,5). У 212 пациентов (42%) ВБД было ≥ 12 мм рт. ст. при поступлении (дополнительный файл 1: рисунок S1). Во время пребывания в отделении интенсивной терапии ВБГ (устойчивое ВБД≥≥ 12 мм рт. ст.) развилась у 164 пациентов (33%), а у 18 пациентов (3,6%) развился ОКС. Из 164 больных с ИАГ у 111 был поставлен этот диагноз при поступлении (67,7%). У большинства пациентов с ИАГ была ИАГ II степени (рис. 1).
ст.) развилась у 164 пациентов (33%), а у 18 пациентов (3,6%) развился ОКС. Из 164 больных с ИАГ у 111 был поставлен этот диагноз при поступлении (67,7%). У большинства пациентов с ИАГ была ИАГ II степени (рис. 1).
Полная таблица
Рис. 1 Высшая степень ВБГ у пациентов с ВБГ или ОКС ( N = 164) группа плановой абдоминальной хирургии, неотложной абдоминальной хирургии и группы нехирургического лечения. В группе плановой абдоминальной хирургии у 18,0% пациентов развились ИАГ или ОКС, а в группе неотложной абдоминальной хирургии у 56,7% развились ИАГ или ОКС. У 35 из 44 пациентов в группе нехирургического лечения развилась ВБГ или ОКС (79)..5%). Однако 12 пациентов в этой группе перенесли экстренную абдоминальную операцию в течение 24 часов после поступления в отделение интенсивной терапии, но были проанализированы в нехирургической группе. У десяти пациентов (83%) развилась ИАГ или ОКС. Наиболее частыми диагнозами у остальных 32 пациентов были панкреатит у 7 пациентов и травма у 7 пациентов.
У десяти пациентов (83%) развилась ИАГ или ОКС. Наиболее частыми диагнозами у остальных 32 пациентов были панкреатит у 7 пациентов и травма у 7 пациентов.
Полная таблица
ИАГ или ОКС развились у 6/7 пациентов с панкреатитом (85,7%), у 25/42 пациентов после ОТП (59,5%) и у 23/58 пациентов после операции на аорте (39,7%). Самая высокая распространенность ОКС наблюдалась при панкреатите (57,1%), затем следовали ОТП (7,1%) и плановые или экстренные операции на аорте (5,2%). Хотя ни у одного из 17 пациентов с травмой не развился ОКС, у 10 из 17 пациентов развилась ИАГ (58,8%).
В таблице 4 приведены факторы риска ВБГ и ОКС по типу госпитализации. Средний ИМТ не отличался между группами плановой абдоминальной хирургии, неотложной абдоминальной хирургии и нехирургических пациентов (, стр. 9).0314 = 0,77). Баллы Apache IV и количество пациентов с ВБГ и ОКС значительно различались между всеми 3 группами ( p < 0,01). Механическая вентиляция при поступлении значительно различалась между группой плановой абдоминальной хирургии и группой экстренной абдоминальной хирургии ( p <0,01), а также между группой плановой абдоминальной хирургии и группой без хирургического вмешательства ( p < 0,01).
Механическая вентиляция при поступлении значительно различалась между группой плановой абдоминальной хирургии и группой экстренной абдоминальной хирургии ( p <0,01), а также между группой плановой абдоминальной хирургии и группой без хирургического вмешательства ( p < 0,01).
Полная таблица
В бинарном логистическом регрессионном анализе ИМТ [отношение шансов (ОШ) 1,08, 95% доверительный интервал (ДИ) 1,03–1,13], оценка Apache IV (ОШ 1,03, 95% ДИ 1,02–1,04), госпитализация после экстренной операции (ОШ 2,8, 95% ДИ 1,61–4,87) и ИВЛ при поступлении (ОШ 3,52, 95% ДИ 2,08–5,96) были независимыми факторами риска развития ВБГ или ОКС в этой когорте (табл. 5). Отношение шансов для ИАГ или ОКС в этом исследовании было выше при неотложной абдоминальной хирургии (ОШ 2,80, 95% ДИ 1,61–4,87) и у нехирургических пациентов (ОШ 8,9).0, 95% ДИ 3,62–21,90) по сравнению с пациентами с плановой абдоминальной хирургией.
Полная таблица
Лечение ОКС
Лечение ОКС было медикаментозным или радиологическим у 12/18 (66,7%) пациентов и хирургическим у 6 /18 (33,3%) больных (табл. 6). Медикаментозное лечение включало временное прекращение энтерального питания ( n = 1), отсасывание назогастрального зонда ( n = 4), дополнительное обезболивание ( n = 5), введение ректальной канюли ( n = 2), ректальная клизма ( n = 4) и/или удаление жидкости с помощью диуретиков или диализа ( n = 2). Рентгенологическое лечение включало дренирование асцита ( n = 2). Хирургическое лечение включало релапаротомию и первичное ушивание брюшной полости у 3 пациентов с ОТП. Причиной ОКС в этих случаях были периоперационные кровотечения и коагулопатия. Еще 3 больным выполнена декомпрессивная лапаротомия с открытым ведением брюшной полости. Диагнозы у этих пациентов были панкреатитом ( n = 1), желудочно-кишечный сепсис ( n = 1) и внутригрудную холангиокарциному ( n = 1), по поводу которых была выполнена плановая расширенная правосторонняя гемигепатэктомия. Открытая брюшная полость управлялась с помощью коммерческой вакуумной системы с отрицательным давлением (KCI Abthera, GD medical, Эйндховен, Нидерланды) у всех пациентов. Эти 3 пациента умерли в отделении интенсивной терапии с полиорганной недостаточностью. У умерших пациентов были более высокие баллы по шкале Apache IV (97 против 83 у всех пациентов с ОКС) и чаще требовалась ЗПТ, чем у выживших (100% против 39).% у всех пациентов с ОКС). У больного с желудочно-кишечным сепсисом отсрочены декомпрессивная лапаротомия и открытое ведение брюшной полости. Первичное закрытие брюшной полости было выполнено во время релапаротомии после установления диагноза ОКС, а декомпрессивная лапаротомия с открытой брюшной полостью была выполнена через сутки в связи с продолжающейся гемодинамической нестабильностью.
Диагнозы у этих пациентов были панкреатитом ( n = 1), желудочно-кишечный сепсис ( n = 1) и внутригрудную холангиокарциному ( n = 1), по поводу которых была выполнена плановая расширенная правосторонняя гемигепатэктомия. Открытая брюшная полость управлялась с помощью коммерческой вакуумной системы с отрицательным давлением (KCI Abthera, GD medical, Эйндховен, Нидерланды) у всех пациентов. Эти 3 пациента умерли в отделении интенсивной терапии с полиорганной недостаточностью. У умерших пациентов были более высокие баллы по шкале Apache IV (97 против 83 у всех пациентов с ОКС) и чаще требовалась ЗПТ, чем у выживших (100% против 39).% у всех пациентов с ОКС). У больного с желудочно-кишечным сепсисом отсрочены декомпрессивная лапаротомия и открытое ведение брюшной полости. Первичное закрытие брюшной полости было выполнено во время релапаротомии после установления диагноза ОКС, а декомпрессивная лапаротомия с открытой брюшной полостью была выполнена через сутки в связи с продолжающейся гемодинамической нестабильностью.
Полная таблица
Заболеваемость и смертность
Частота ЗПТ была значительно выше при ВБГ и ОКС по сравнению с группой с нормальным ВБД (8,2% и 38,9% против 1,2%) ( p < 0,01), а продолжительность ИВЛ была больше (91,8 и 196,3 ч против . 14,0 ч) ( p < 0,01). Продолжительность пребывания в ОИТ была больше при ВБГ и ОКС по сравнению с группой с нормальным ВБД (6,1 и 12,0 дней против 1,3 дня) ( p < 0,01). Смертность в ОИТ была значительно выше в группе ВБГ и ОКС по сравнению с группой нормального ВББ (4,8% и 16,7% против 1,2%) (9).0401 p < 0,01). 90-дневная смертность была выше при ВБГ и ОКС по сравнению с группой с нормальным ВББ (15,2% и 38,9% против 7,1%) ( p < 0,01) (таблица 7).
Таблица 7 Заболеваемость и смертность пациентов с ВБГ и ОКС по сравнению с пациентами с нормальным ВБДПолная таблица
Обсуждение
Это проспективное исследование демонстрирует общую заболеваемость ОКС на уровне 3,6% в когорте с высоким оценочным априорным риском . Частота ИАГ в нашем исследовании составила 33%. По сравнению с данными литературы частота ОКС в этой когорте была низкой.
Частота ИАГ в нашем исследовании составила 33%. По сравнению с данными литературы частота ОКС в этой когорте была низкой.
В исследовании 83 пациентов, опубликованном в 2008 г., частота ОКС составила 12% в неоднородной популяции интенсивной терапии [14]. Частота возникновения ОКС в текущем исследовании сравнима с недавним исследованием в смешанном медико-хирургическом отделении интенсивной терапии, где ОКС возник у 3% пациентов, хотя в это исследование были включены последовательные пациенты отделения интенсивной терапии, которые не были отобраны из-за их высокого риска ИАГ или ОКС. [3]. Это можно объяснить тем фактом, что 67% пациентов в текущем исследовании были госпитализированы после плановой абдоминальной хирургии. Распространенность ВБГ была относительно низкой в этой группе (18%) по сравнению с госпитализацией после неотложной абдоминальной хирургии (57%) и группой госпитализации без хирургического вмешательства (80%).
Наибольшая распространенность ОКС наблюдалась у пациентов с панкреатитом, ОТП и операциями на брюшной аорте. Более ранние исследования сообщают о частоте ОКС при панкреатите в 25-56% и в 33-41% после обширных абдоминальных операций [15,16,17]. Частота ОКС после ОТП составила 31% при исследовании 108 пациентов в 2003 г. [18]. Низкая распространенность ОКС в нашей когорте может быть связана с улучшением периоперационной и интенсивной терапии, включая ограничительное периоперационное введение жидкости и тщательный гемостаз. Более того, ОКС может снижаться благодаря раннему распознаванию и лечению ИАГ [9].].
Более ранние исследования сообщают о частоте ОКС при панкреатите в 25-56% и в 33-41% после обширных абдоминальных операций [15,16,17]. Частота ОКС после ОТП составила 31% при исследовании 108 пациентов в 2003 г. [18]. Низкая распространенность ОКС в нашей когорте может быть связана с улучшением периоперационной и интенсивной терапии, включая ограничительное периоперационное введение жидкости и тщательный гемостаз. Более того, ОКС может снижаться благодаря раннему распознаванию и лечению ИАГ [9].].
У шести из 7 пациентов с диагнозом панкреатит была ИАГ (86%), у 4 — ОКС (57%). Эти высокие цифры подтверждают результаты нашего более раннего ретроспективного когортного исследования, которое показало, что ВБГ и ОКС часто встречаются у пациентов с тяжелым острым панкреатитом. Это исследование привело к внедрению протокола мониторинга ВБД в нашем отделении интенсивной терапии и потребовало обновления национальных и международных руководств по панкреатиту, чтобы включить мониторинг ВБД в качестве стандарта лечения. В настоящее время ВБД измеряют каждые 4 ч у пациентов с риском ИАГ (в том числе с панкреатитом) в нашем отделении интенсивной терапии [19].]. Распространенность ОКС выше, чем описано в обзоре 2014 г., где распространенность ИАГ и ОКС при панкреатите составляла 54–66% и 22–38% соответственно [20]. Это расхождение можно объяснить тем, что в исследовании участвовало всего 7 больных панкреатитом. Более того, отбор пациентов с панкреатитом произошел, поскольку наша больница является специализированным центром для пациентов с панкреатитом, и пациентов обычно направляют в нашу больницу, когда вмешательство неизбежно или когда возникают осложнения. ВБГ может ухудшиться при агрессивной инфузионной терапии [21]. Стратегии ограничения жидкости, такие как рекомендованные Aggarwal et al. не применялись в группе больных панкреатитом, что могло способствовать развитию ИАГ и ОКС [21]. Ни у одного из 17 пациентов с травмами в этом исследовании не развился ОКС. Однако частота ИАГ составила 10/17 (58,8%).
В настоящее время ВБД измеряют каждые 4 ч у пациентов с риском ИАГ (в том числе с панкреатитом) в нашем отделении интенсивной терапии [19].]. Распространенность ОКС выше, чем описано в обзоре 2014 г., где распространенность ИАГ и ОКС при панкреатите составляла 54–66% и 22–38% соответственно [20]. Это расхождение можно объяснить тем, что в исследовании участвовало всего 7 больных панкреатитом. Более того, отбор пациентов с панкреатитом произошел, поскольку наша больница является специализированным центром для пациентов с панкреатитом, и пациентов обычно направляют в нашу больницу, когда вмешательство неизбежно или когда возникают осложнения. ВБГ может ухудшиться при агрессивной инфузионной терапии [21]. Стратегии ограничения жидкости, такие как рекомендованные Aggarwal et al. не применялись в группе больных панкреатитом, что могло способствовать развитию ИАГ и ОКС [21]. Ни у одного из 17 пациентов с травмами в этом исследовании не развился ОКС. Однако частота ИАГ составила 10/17 (58,8%). Эти результаты подтверждают исследование у 81 пациента с травмой, где частота ВБГ составила 75%, и ни у одного пациента не развился ОКС [22]. Таким образом, мы разделяем вывод авторов о том, что ослабление острого коронарного синдрома до менее опасного ИАГ можно считать успехом развития в области травматологии и интенсивной терапии.
Эти результаты подтверждают исследование у 81 пациента с травмой, где частота ВБГ составила 75%, и ни у одного пациента не развился ОКС [22]. Таким образом, мы разделяем вывод авторов о том, что ослабление острого коронарного синдрома до менее опасного ИАГ можно считать успехом развития в области травматологии и интенсивной терапии.
В исследование «Заболеваемость, факторы риска и исходы внутрибрюшной гипертензии у пациентов в критическом состоянии» (IROI) [10] был включен 491 последовательный пациент из 15 отделений интенсивной терапии по всему миру. По сравнению с нашим исследованием, в него были включены пациенты с плановой операцией и смесь пациентов с искусственной вентиляцией легких и спонтанно дышащих. ВБГ присутствовала у 34% в день поступления и у 48,9% больных в период наблюдения. ИАГ наблюдалась у 99 терапевтических больных (53,2%), у 86 больных экстренной хирургии (56,6%) и у 55 больных плановой хирургии (35,9%).%). ОКС отмечен у 6,3% больных. В нашем исследовании у пациентов с ИАГ наиболее часто встречалась ИАГ II степени. Это противоречит результатам других исследований, в том числе исследования IROI, в котором наиболее распространен IAH степени [10, 13]. Различия в распространенности ИАГ и ОКС между исследованиями, вероятно, связаны с отбором пациентов. Когда у пациентов с высоким риском в нашем исследовании развилась ВБГ, степень ВБГ была выше, чем в исследованиях с последовательными пациентами ОИТ. Это может свидетельствовать об их более высоком риске развития ВБГ и ОКС. Почти 68% пациентов с ИАГ или ОКС были диагностированы при поступлении в ОРИТ. Это согласуется с другими исследованиями, в которых ИАГ развилась после 1-го дня только у 31–34% пациентов [3, 10, 14]. ВБД было ≥ 12 мм рт.ст. при поступлении у 42% пациентов. Это могло быть связано с возбуждением и/или болью сразу после операции или после транспортировки в отделение интенсивной терапии. Быстрое снижение ВБД можно объяснить адекватным уходом за больным в ОИТ, включая обезболивание. Заболеваемость и смертность увеличились в группе ВБГ и ОКС по сравнению с группой нормального ВББ.
Это противоречит результатам других исследований, в том числе исследования IROI, в котором наиболее распространен IAH степени [10, 13]. Различия в распространенности ИАГ и ОКС между исследованиями, вероятно, связаны с отбором пациентов. Когда у пациентов с высоким риском в нашем исследовании развилась ВБГ, степень ВБГ была выше, чем в исследованиях с последовательными пациентами ОИТ. Это может свидетельствовать об их более высоком риске развития ВБГ и ОКС. Почти 68% пациентов с ИАГ или ОКС были диагностированы при поступлении в ОРИТ. Это согласуется с другими исследованиями, в которых ИАГ развилась после 1-го дня только у 31–34% пациентов [3, 10, 14]. ВБД было ≥ 12 мм рт.ст. при поступлении у 42% пациентов. Это могло быть связано с возбуждением и/или болью сразу после операции или после транспортировки в отделение интенсивной терапии. Быстрое снижение ВБД можно объяснить адекватным уходом за больным в ОИТ, включая обезболивание. Заболеваемость и смертность увеличились в группе ВБГ и ОКС по сравнению с группой нормального ВББ.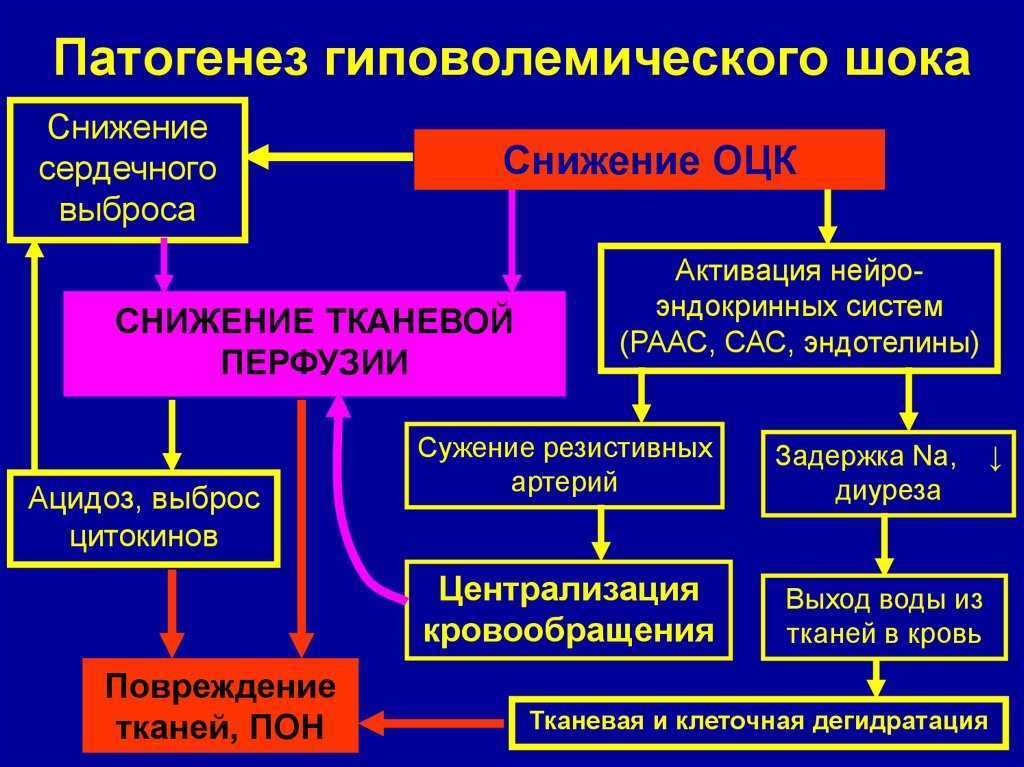 Это наблюдение согласуется с литературными данными, в которых было обнаружено, что ВБГ является независимым предиктором смертности в ОИТ [2]. Олигурия и почечная дисфункция являются одними из самых ранних признаков повышения ВБД [23], а ВБД является независимой причиной почечной недостаточности [16]. Мы обнаружили, что частота ЗПТ была значительно выше при ВБГ и ОКС (8,2% и 38,9%).%) по сравнению с группой с нормальным ВБД (1,2%).
Это наблюдение согласуется с литературными данными, в которых было обнаружено, что ВБГ является независимым предиктором смертности в ОИТ [2]. Олигурия и почечная дисфункция являются одними из самых ранних признаков повышения ВБД [23], а ВБД является независимой причиной почечной недостаточности [16]. Мы обнаружили, что частота ЗПТ была значительно выше при ВБГ и ОКС (8,2% и 38,9%).%) по сравнению с группой с нормальным ВБД (1,2%).
В 2004 г. Malbrain обнаружил, что ИМТ является единственным независимым фактором риска развития ВБГ [24]. В исследовании IROI ИМТ, оценка по шкале APACHE II ≥ 18, ПДКВ > 7 см H 2 O, наличие вздутия живота и отсутствие кишечных шумов были связаны с ИАГ [10]. В бинарном логистическом регрессионном анализе факторов риска ВБГ или ОКС в текущем исследовании ИМТ, оценка Apache IV и вентиляция легких при поступлении были независимыми факторами риска. Мерфи и др. обнаружили, что тип поступления (медикаментозное, хирургическое или травматическое) не является предиктором ИАГ [3]. Вопреки этим выводам, отношение шансов ИАГ или ОКС в этом исследовании было повышено при неотложной абдоминальной хирургии (на 2,8) и у нехирургических пациентов (на 8,9).) по сравнению с пациентами после плановой абдоминальной хирургии. Однако эти отношения шансов следует интерпретировать с осторожностью. Важно отметить, что в нехирургической группе было всего 44 пациента (менее 9% от общего числа пациентов в исследовании), 12 из этих пациентов перенесли экстренную абдоминальную операцию в течение 24 ч после поступления в ОИТ и были проанализированы в нехирургической группе, и у 10/12 развился ИАГ/ОКС. На основании этих данных мы делаем вывод о повышенном риске ИАГ или ОКС при неотложной абдоминальной хирургии по сравнению с плановой абдоминальной хирургией и у пациентов с диагнозом панкреатит, поскольку этот диагноз был наиболее распространенным среди остальных 32 пациентов в нехирургическая группа с распространенностью ИАГ/ОКС 85,7%. Следовательно, пациент с наибольшим риском ИАГ и ОКС в этой когорте высокого риска — это пациент с ИМТ > 30 кг/м 9 .
Вопреки этим выводам, отношение шансов ИАГ или ОКС в этом исследовании было повышено при неотложной абдоминальной хирургии (на 2,8) и у нехирургических пациентов (на 8,9).) по сравнению с пациентами после плановой абдоминальной хирургии. Однако эти отношения шансов следует интерпретировать с осторожностью. Важно отметить, что в нехирургической группе было всего 44 пациента (менее 9% от общего числа пациентов в исследовании), 12 из этих пациентов перенесли экстренную абдоминальную операцию в течение 24 ч после поступления в ОИТ и были проанализированы в нехирургической группе, и у 10/12 развился ИАГ/ОКС. На основании этих данных мы делаем вывод о повышенном риске ИАГ или ОКС при неотложной абдоминальной хирургии по сравнению с плановой абдоминальной хирургией и у пациентов с диагнозом панкреатит, поскольку этот диагноз был наиболее распространенным среди остальных 32 пациентов в нехирургическая группа с распространенностью ИАГ/ОКС 85,7%. Следовательно, пациент с наибольшим риском ИАГ и ОКС в этой когорте высокого риска — это пациент с ИМТ > 30 кг/м 9 . 0282 2 , поступивших в отделение интенсивной терапии после неотложной абдоминальной операции или с диагнозом панкреатит.
0282 2 , поступивших в отделение интенсивной терапии после неотложной абдоминальной операции или с диагнозом панкреатит.
В этом обсервационном исследовании в когорте пациентов с высоким риском стратегии ведения ОКС не были стандартизированы. Они состояли из медикаментозного, интервенционной радиологии и хирургического или комбинированного подходов. Большинству пациентов удалось обойтись без декомпрессивной лапаротомии. Все эти пациенты пережили пребывание в отделении интенсивной терапии. Это также иллюстрирует, что нехирургическое лечение является важным вариантом лечения у пациентов в критическом состоянии с повышенным ВБД [25]. При выполнении декомпрессивной лапаротомии и вскрытия живота все пациенты умерли от полиорганной недостаточности в ОРИТ. Хотя наше исследование не было разработано для изучения эффектов лечения, а цифры слишком малы для выводов, этот уровень смертности выше, чем в литературе, где смертность после хирургической декомпрессии колеблется от 18 до 49. % [26,27,28]. Возможные объяснения высокой смертности в отделении интенсивной терапии в этой небольшой группе пациентов, кроме совпадения, могут заключаться в том, что, о чем свидетельствует их оценка по шкале Apache IV, эти пациенты были еще более серьезно больны, чем другие пациенты с ОКС, и в задержке декомпрессивной лапаротомии, которая произошла в один из пациентов. На сегодняшний день не проводилось интервенционных исследований, чтобы ответить на важный вопрос, какие пациенты с ОКС нуждаются в медикаментозном, радиологическом или хирургическом лечении. Поэтому место и сроки выполнения декомпрессивной лапаротомии при ОКС до сих пор неизвестны [28].
% [26,27,28]. Возможные объяснения высокой смертности в отделении интенсивной терапии в этой небольшой группе пациентов, кроме совпадения, могут заключаться в том, что, о чем свидетельствует их оценка по шкале Apache IV, эти пациенты были еще более серьезно больны, чем другие пациенты с ОКС, и в задержке декомпрессивной лапаротомии, которая произошла в один из пациентов. На сегодняшний день не проводилось интервенционных исследований, чтобы ответить на важный вопрос, какие пациенты с ОКС нуждаются в медикаментозном, радиологическом или хирургическом лечении. Поэтому место и сроки выполнения декомпрессивной лапаротомии при ОКС до сих пор неизвестны [28].
Следствием гетерогенности популяции пациентов с риском развития ОКС в сочетании с низкой заболеваемостью ОКС является то, что интервенционные исследования могут проводиться только в крупных многоцентровых исследованиях. Многоцентровое исследование, рандомизированное между ранней декомпрессивной хирургией с открытой брюшной полостью и медикаментозным лечением пациентов с ОКС, могло бы ответить на некоторые из многих остающихся вопросов.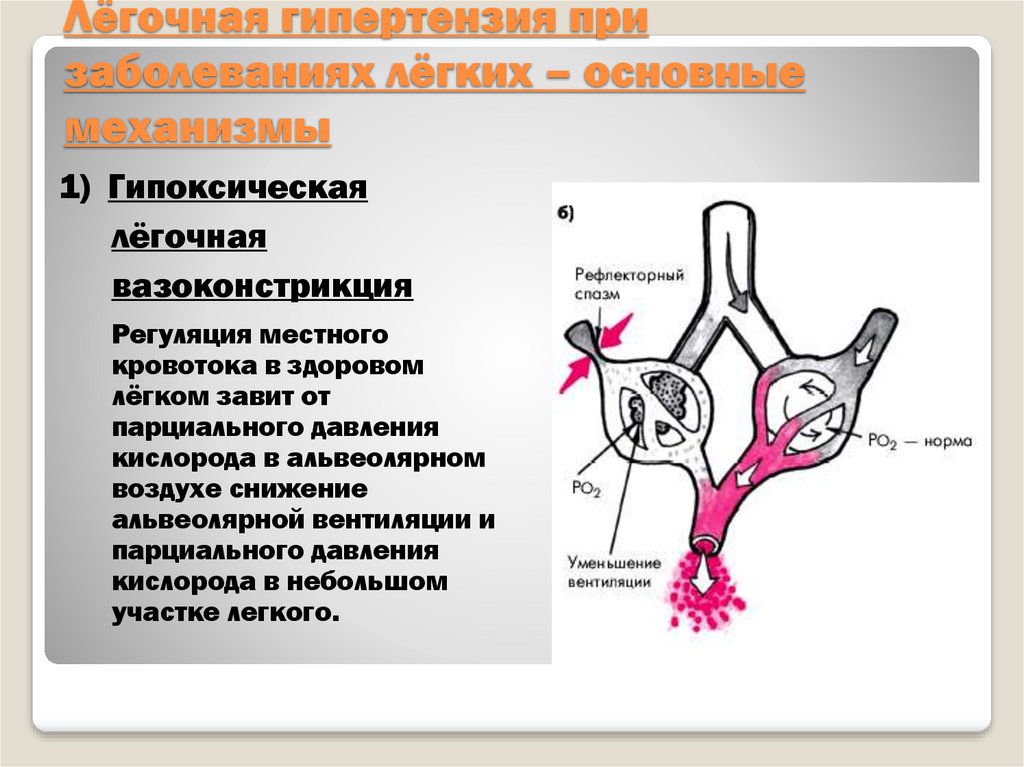 Для обоснования ведения открытой брюшной полости на основании достаточных доказательств в 2015 г. был введен реестр лапаростомии под названием «Открытый абдоминальный путь» [29].]. Промежуточный анализ показывает, что у 649 пациентов с открытым ведением живота показанием к открытию живота был послеоперационный ОКС у 19 пациентов (2,9%) и панкреатит у 37 пациентов (5,7%) [30]. В ближайшем будущем, пока не будет получено больше данных, лечение этого опасного для жизни синдрома будет зависеть от здравого клинического суждения и тесного сотрудничества между отделениями интенсивной терапии, гастроэнтерологии и хирургии.
Для обоснования ведения открытой брюшной полости на основании достаточных доказательств в 2015 г. был введен реестр лапаростомии под названием «Открытый абдоминальный путь» [29].]. Промежуточный анализ показывает, что у 649 пациентов с открытым ведением живота показанием к открытию живота был послеоперационный ОКС у 19 пациентов (2,9%) и панкреатит у 37 пациентов (5,7%) [30]. В ближайшем будущем, пока не будет получено больше данных, лечение этого опасного для жизни синдрома будет зависеть от здравого клинического суждения и тесного сотрудничества между отделениями интенсивной терапии, гастроэнтерологии и хирургии.
Хотя мы выбрали для анализа пациентов в этом исследовании в 3 группы: с нормальным ВБД, с ВБГ и с ОКС, наши данные показывают, что ВБГ и ОКС представляют собой континуум заболеваний, причем ОКС является наиболее серьезным. Раннее распознавание и лечение ИАГ может иметь ключевое значение для предотвращения возникновения ОКС с его повышенной заболеваемостью и смертностью. По нашему мнению, для раннего выявления и лечения ВБГ и ОКС крайне важно, чтобы рутинное измерение ВБД выполнялось у пациентов с высоким риском, особенно у пациентов с панкреатитом и пациентов после экстренной абдоминальной хирургии.
По нашему мнению, для раннего выявления и лечения ВБГ и ОКС крайне важно, чтобы рутинное измерение ВБД выполнялось у пациентов с высоким риском, особенно у пациентов с панкреатитом и пациентов после экстренной абдоминальной хирургии.
Сильные стороны и ограничения этого исследования
Наше исследование является крупнейшим на сегодняшний день проспективным исследованием, в котором изучалась распространенность и различные параметры исходов ВБГ и ОКС у пациентов с высоким риском в ОИТ. Однако это было одноцентровое исследование в больнице третичного уровня, что может ограничивать применимость данных.
Стандартизированный подход к измерению ВБД важен для обеспечения воспроизводимости [6]. В этом исследовании ВБД постоянно измеряли, используя в качестве контрольной точки лобковый симфиз, а не среднюю подмышечную линию, как рекомендуется в недавних рекомендациях [4]. Поскольку ВБД, измеренное по средней подмышечной линии в качестве точки отсчета, значительно выше, чем лобковый симфиз в положении лежа на спине [31], в этом исследовании могла иметь место недооценка ВБД и, следовательно, недооценка числа пациентов с ИАГ.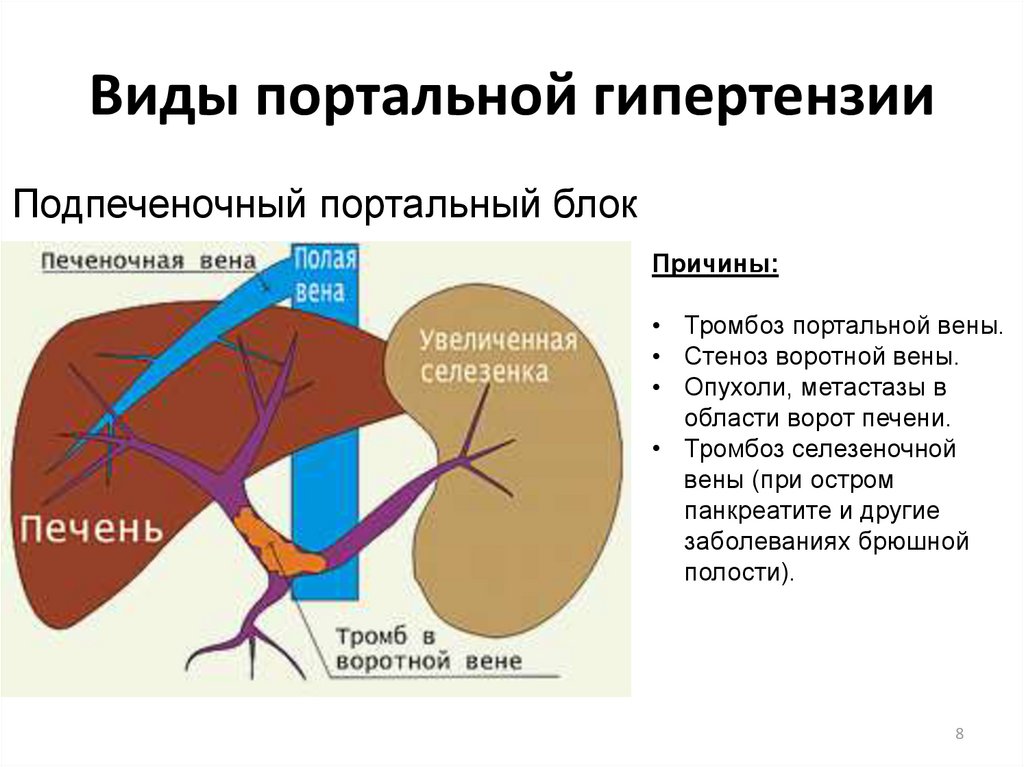 и АКС. ВБД следует измерять в положении лежа [4]. В этом исследовании допускается подъем изголовья кровати до 30 градусов, если ВБД нельзя было выполнить в положении лежа на спине по соображениям ухода за пациентом. Это произошло в 2% измерений ВБД. Поскольку клинически значимые изменения ВБД происходят при увеличении изголовья выше 20 градусов [32], подъем изголовья кровати может привести к увеличению ВБД у этого меньшинства пациентов. Диагнозы в нашем исследовании были основаны на двух основных диагнозах, зарегистрированных при поступлении, и на основе этих данных был проведен анализ. Не вся необходимая информация могла быть доступна на момент поступления. Кроме того, поскольку мы не измеряли ВБД непрерывно, точную продолжительность ВБГ нельзя сделать из настоящего исследования.
и АКС. ВБД следует измерять в положении лежа [4]. В этом исследовании допускается подъем изголовья кровати до 30 градусов, если ВБД нельзя было выполнить в положении лежа на спине по соображениям ухода за пациентом. Это произошло в 2% измерений ВБД. Поскольку клинически значимые изменения ВБД происходят при увеличении изголовья выше 20 градусов [32], подъем изголовья кровати может привести к увеличению ВБД у этого меньшинства пациентов. Диагнозы в нашем исследовании были основаны на двух основных диагнозах, зарегистрированных при поступлении, и на основе этих данных был проведен анализ. Не вся необходимая информация могла быть доступна на момент поступления. Кроме того, поскольку мы не измеряли ВБД непрерывно, точную продолжительность ВБГ нельзя сделать из настоящего исследования.
Выводы
Распространенность ОКС в группе высокого риска в отделении интенсивной терапии составила 3,6%, а распространенность ИАГ — 33%. Самая высокая распространенность ОКС наблюдалась в подгруппах пациентов с панкреатитом (57%), за которыми следовали ортотопическая трансплантация печени (7%) и плановые или экстренные операции на брюшной аорте (5%).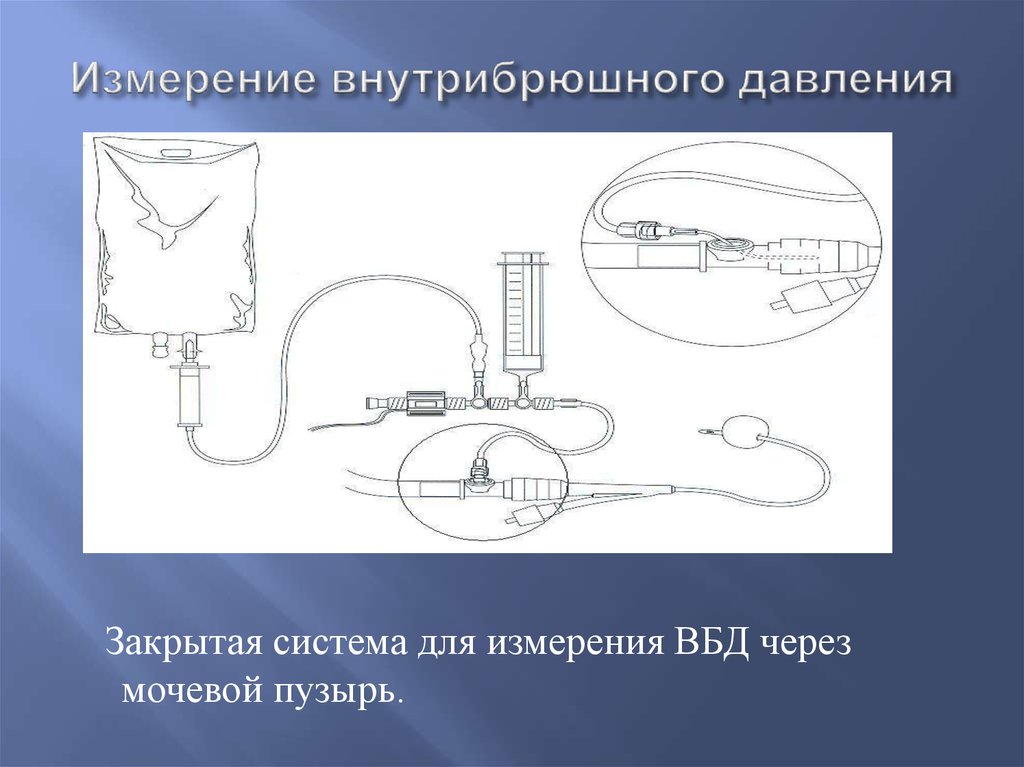 Заболеваемость и смертность увеличивались при наличии ИАГ или ОКС. Пациент с наибольшим риском ИАГ или ОКС в этой когорте высокого риска имеет ИМТ > 30 кг/м 2 и был госпитализирован в отделение интенсивной терапии после неотложной абдоминальной операции или с диагнозом панкреатит.
Заболеваемость и смертность увеличивались при наличии ИАГ или ОКС. Пациент с наибольшим риском ИАГ или ОКС в этой когорте высокого риска имеет ИМТ > 30 кг/м 2 и был госпитализирован в отделение интенсивной терапии после неотложной абдоминальной операции или с диагнозом панкреатит.
Доступность данных и материалов
Наборы данных, использованные и/или проанализированные в ходе текущего исследования, можно получить у соответствующего автора по обоснованному запросу.
Сокращения
- ACS:
Абдоминальный компартмент-синдром
- Оценка Apache:
Оценка острой физиологии и хронического состояния здоровья
- ИМТ:
Индекс массы тела
- КИ:
Доверительный интервал
- CVVH:
Непрерывная вено-венозная гемофильтрация
- ГИ:
Желудочно-кишечный тракт
- ИАХ:
Внутрибрюшная гипертензия
- ИП:
Внутрибрюшное давление
- ОИТ:
Отделение интенсивной терапии
- METc:
Medische ethische toetsingscommissie (Институциональный наблюдательный совет)
- OLT:
Ортотопическая трансплантация печени
- ИЛИ:
Отношение шансов
- Соотношение PaO2/FiO2:
Отношение парциального давления кислорода в артериальной крови к фракционному вдыхаемому кислороду
- ПДКВ:
Положительное давление в конце выдоха
- РРТ:
Заместительная почечная терапия
- WSACS:
Всемирное общество синдрома абдоминального компартмента (в настоящее время WSACS, общество абдоминального компартмента)
Ссылки
- «>
Malbrain MLNG, Chiumello D, Cesana BM, Reintam Blaser A, Starkopf J, Sugrue M, et al. Систематический обзор и метаанализ данных отдельных пациентов о внутрибрюшной гипертензии у пациентов в критическом состоянии: проект пробуждения. Всемирная инициатива по эпидемиологии абдоминальной гипертензии, объединяющий проект (ПРОБУЖДЕНИЕ!). Минерва Анестезиол. 2014; 80: 293–306.
КАС пабмед Google ученый
Murphy PB, Parry NG, Sela N, Leslie K, Vogt K, Ball I. Внутрибрюшная гипертензия встречается чаще, чем считалось ранее: проспективное исследование в смешанном медико-хирургическом отделении интенсивной терапии.
 Care Med: крит; 2018.
Care Med: крит; 2018.Книга Google ученый
Kirkpatrick AW, Roberts DJ, De Waele J, Jaeschke R, Malbrain MLNG, De Keulenaer B, et al. Внутрибрюшная гипертензия и синдром абдоминального компартмента: обновленные согласованные определения и рекомендации по клинической практике от Всемирного общества синдрома абдоминального компартмента. Интенсивная терапия Мед. 2013;39: 1190–206.
Артикул Google ученый
Padar M, Reintam Blaser A, Talving P, Lipping E, Starkopf J. Абдоминальный компартмент-синдром: улучшение результатов с помощью междисциплинарного подхода — описательный обзор. J Multidiscip Healthc Dove Press. 2019;12:1061–74.
Артикул Google ученый
Sugrue M, De Waele JJ, De Keulenaer BL, Roberts DJ, Malbrain MLNG. Руководство пользователя по измерению внутрибрюшного давления.
 Анестезиол Интенсив Тер. 2015; 47: 241–51.
Анестезиол Интенсив Тер. 2015; 47: 241–51.Артикул Google ученый
Bahten LCV, Lange PAL, Alves RFF, Soares HMN, de Souza TM, Bahten ACV. Абдоминальный компартмент-синдром: знания медицинского персонала университетской больницы в Куритибе. Преподобный полковник Брас Cir Colégio Brasileiro de Cirurgiões. 2018;45:e1884.
Google ученый
Wise R, Rodseth R, Blaser A, Roberts D, De Waele J, Kirkpatrick A, et al. Осведомленность и знания о внутрибрюшной гипертензии и синдроме абдоминального компартмента: результаты повторного международного перекрестного исследования. Анестезиол Интенсив Термедия. 2019;51:186–99.
Артикул Google ученый
Де Ваеле Дж.Дж., Мальбрейн МЛНГ, Киркпатрик А.В. Синдром абдоминального компартмента: развивающиеся концепции и будущие направления.
 Критический уход. 2015;19:211.
Критический уход. 2015;19:211.Артикул Google ученый
Reintam Blaser A, Regli A, De Keulenaer B, Kimball EJ, Starkopf L, Davis WA, et al. Заболеваемость, факторы риска и исходы внутрибрюшной гипертензии у пациентов в критическом состоянии — проспективное многоцентровое исследование (исследование IROI). Крит Уход Мед. 2019;47:535–42.
Артикул Google ученый
Холодинский Дж.К., Робертс Д.Дж., Болл К.Г., Блазер А.Р., Старкопф Дж., Зигун Д.А., и другие. Факторы риска внутрибрюшной гипертензии и абдоминального компартмент-синдрома у взрослых пациентов отделений интенсивной терапии: систематический обзор и метаанализ. Критический уход. 2013;17:R249.
Артикул Google ученый
Рейнтам А., Парм П., Китус Р., Керн Х., Старкопф Дж. Первичная и вторичная внутрибрюшная гипертензия – различное влияние на исход в отделении интенсивной терапии.
 Интенсивная терапия Med Springer-Verlag. 2008; 34:1624–31.
Интенсивная терапия Med Springer-Verlag. 2008; 34:1624–31.Артикул Google ученый
Reintam Blaser A, Blaser AR, Parm P, Par P, Kitus R, Starkopf J. Факторы риска внутрибрюшной гипертензии у пациентов с механической вентиляцией легких. Acta Anaesthesiol Scand. 2011;55:607–14.
КАС Статья Google ученый
Видаль М.Г., Руис Вайссер Дж., Гонсалес Ф., Торо М.А., Лудет С., Баласини С. и др. Заболеваемость и клинические эффекты внутрибрюшной гипертензии у пациентов в критическом состоянии. Крит Уход Мед. 2008; 36: 1823–31.
Артикул Google ученый
De Waele JJ, De Laet I, Kirkpatrick AW, Hoste E. Внутрибрюшная гипертензия и абдоминальный компартмент-синдром. Am J почек Dis. 2011;57:159–69.
Артикул Google ученый
«>Sugrue M, Buist MD, Hourihan F, Deane S, Bauman A, Hillman K. Проспективное исследование внутрибрюшной гипертензии и функции почек после лапаротомии. Бр Дж Сур. 1995; 82: 235–8.
КАС Статья Google ученый
Бьянкофиоре Г., Бинди М.Л., Романелли А.М., Болдрини А., Консани Г., Биза М. и др. Мониторинг внутрибрюшного давления у реципиентов трансплантата печени: проспективное исследование. Интенсивная терапия Мед. 2003;29: 30–6.
Артикул Google ученый
Смит М., Баддинг К.Т., Босма Б., Ньювенхуйс В.Б., Хофкер Х.
 С., Зийлстра Дж.Г. Синдром абдоминального компартмента и внутрибрюшная ишемия у больных с тяжелым острым панкреатитом. Мир J Surg. 2016;40:1454–61.
С., Зийлстра Дж.Г. Синдром абдоминального компартмента и внутрибрюшная ишемия у больных с тяжелым острым панкреатитом. Мир J Surg. 2016;40:1454–61.КАС Статья Google ученый
ван Браншот С., Шут А.Дж., Боувенсе С.А., Бесселинк М.Г., Баккер О.Дж., ван Гур Х. и др. Абдоминальный компартмент-синдром при остром панкреатите: систематический обзор. Поджелудочная железа. 2014;43:665–74.
Артикул Google ученый
Aggarwal A, Manrai M, Kochhar R. Жидкостная реанимация при остром панкреатите. Мир J Гастроэнтерол. 2014;20:18092–103.
Артикул Google ученый
Балог З.Дж., Мартин А., ван Вессем К.П., Кинг К.Л., Маккей П., Хэвилл К. Миссия по устранению посттравматического абдоминального компартмент-синдрома. Арка Сур. 2011; 146:938–43.
Артикул Google ученый
«>Malbrain MLNG, Chiumello D, Pelosi P, Wilmer A, Brienza N, Malcangi V, et al. Распространенность внутрибрюшной гипертензии у пациентов в критическом состоянии: многоцентровое эпидемиологическое исследование. Интенсивная терапия Мед. 2004; 30: 822–9..
Артикул Google ученый
Де Кеуленаер Б.Л., Де Ваеле Дж.Дж., Мальбрейн МЛНГ. Неоперативное лечение внутрибрюшной гипертензии и синдрома абдоминального компартмента: развивающиеся концепции. Am Surg. 2011; 77 (Приложение 1): S34–41.
ПабМед Google ученый
Mentula P, Hienonen P, Kemppainen E, Puolakkainen P, Leppäniemi A.
 Хирургическая декомпрессия при абдоминальном компартмент-синдроме при тяжелом остром панкреатите. Арка Сур. 2010; 145:764–9.
Хирургическая декомпрессия при абдоминальном компартмент-синдроме при тяжелом остром панкреатите. Арка Сур. 2010; 145:764–9.Артикул Google ученый
Кьяра О., Симбанасси С., Боати С., Басси Г. Хирургическое лечение абдоминального компартмент-синдрома. Минерва Анестезиол. 2011;77:457–62.
КАС пабмед Google ученый
De Waele JJ, Hoste EA, Malbrain ML. Декомпрессивная лапаротомия при абдоминальном компартмент-синдроме — критический анализ. Критический уход. 2006;10:R51.
Артикул Google ученый
Виллмс А., Мюйсомс Ф., Гусген С., Шваб Р., Лок Дж., Шааф С. и др. Открытый абдоминальный маршрут от EuraHS: введение набора данных и первоначальных результатов процедур и осложнений, связанных с процедурами. Грыжа. 2017;21:279–89.
КАС Статья Google ученый
«>Де Ваэле Дж.Дж., Де Лаэт И., Де Кеуленаер Б., Виддер С., Киркпатрик А.В., Крессвелл А.Б. и др. Влияние различных положений эталонного датчика на измерение внутрибрюшного давления: многоцентровый анализ. Интенсивная терапия Мед. 2008; 34:1299–303.
Артикул Google ученый
Макбет П.Б., Зигун Д.А., Виддер С., Читэм М., Зенгеринк И., Глова Дж. и др. Влияние положения пациента на мониторирование внутрибрюшного давления. Am J Surg. 2007;193:644–7 (обсуждение 647) .
Артикул Google ученый
Malbrain MLNG, Chiumello D, Pelosi P, Bihari D, Innes R, Ranieri VM, et al. Частота и прогноз интраабдоминальной гипертензии в смешанной популяции больных в критическом состоянии: многоцентровое эпидемиологическое исследование. Крит Уход Мед. 2005; 33: 315–22.
Артикул Google ученый
Sugrue M, Jones F, Deane SA, Bishop G, Bauman A, Hillman K. Внутрибрюшная гипертензия является независимой причиной послеоперационной почечной недостаточности. Арка Сур. 1999;134:1082–5.
КАС Статья Google ученый
Mohmand H, Goldfarb S. Почечная дисфункция, связанная с внутрибрюшной гипертензией и синдромом абдоминального компартмента. J Am Soc Нефрол. 2011;22:615–21.
Артикул Google ученый
Coccolini F, Ceresoli M, Kluger Y, Kirkpatrick A, Montori G, Salvetti F, et al. Открытый живот и кишечно-атмосферные свищи: промежуточный анализ из Международного регистра открытого живота (IROA). Рана. 2019;50:160–6.
Артикул Google ученый
Загрузить ссылки
Благодарности
Мы благодарны всем медсестрам интенсивной терапии, медсестрам-исследователям и членам команды студентов интенсивной терапии за их помощь в сборе данных.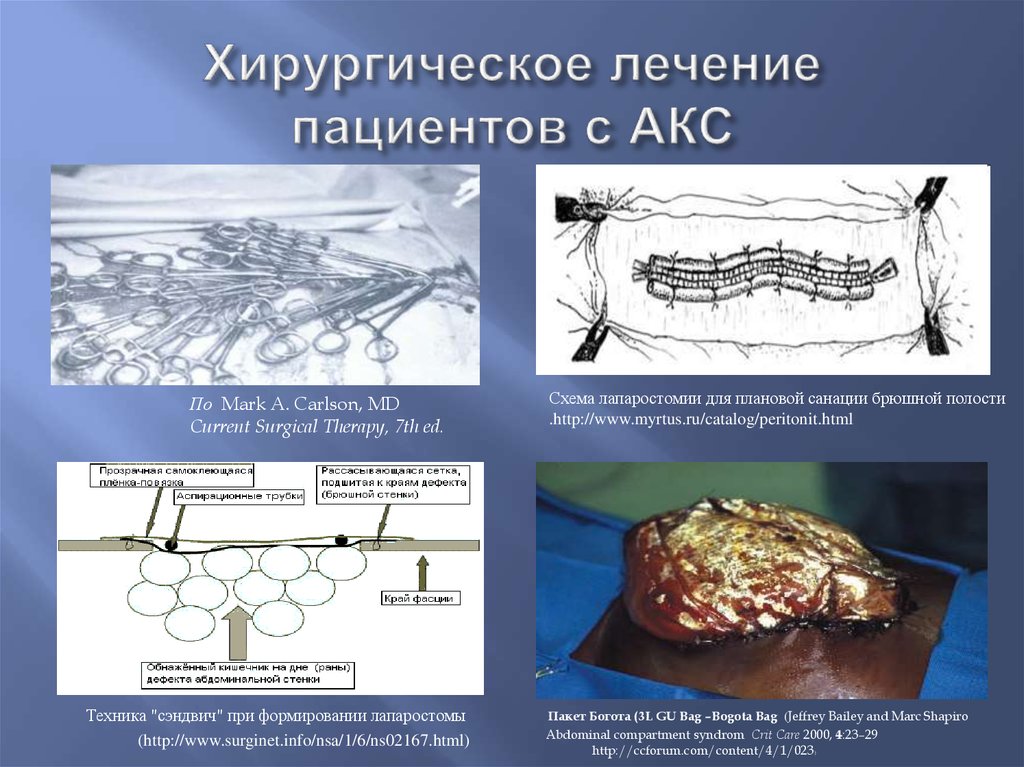
Финансирование
Институциональное ведомственное финансирование.
Информация об авторе
Авторы и организации
Отделение интенсивной терапии (BA 49), Медицинский центр Университета Гронингена, Университет Гронингена, а/я 30001, 9700 RB, Гронинген, Нидерланды
Мария Смит, Барт Купман, Виллем Диперинк, Матийс ван Мерс и Ян Г. Zijlstra
Кафедра детской хирургии, Университетский медицинский центр Гронингена, Гронингенский университет, а/я 30001, 9700 RB, Гронинген, Нидерланды
Ян Б. Ф. Хюльшер
Хирургический факультет, Университет Гронингена Гронинген, а/я 30001, 9700 RB, Гронинген, Нидерланды
H. Sijbrand Hofker
Авторы
- Marije Smit
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Bart Koopman
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Виллем Диперинк
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Jan B.
 F. Hulscher
F. HulscherПросмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- H. Sijbrand Hofker
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Matijs van Meurs
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Jan G. Zijlstra
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Вклады
MS: дизайн исследования, сбор данных, анализ и интерпретация данных, написание и редактирование рукописи. БК: сбор данных, написание и редактирование рукописи. WD: дизайн базы данных, сбор данных, написание и редактирование рукописи. JBFH: дизайн исследования, написание и редактирование рукописи. HSH: дизайн исследования, написание и редактирование рукописи. MvM: дизайн исследования, интерпретация данных, написание и редактирование рукописи. JGZ: дизайн исследования, интерпретация данных, написание и редактирование рукописи. Все авторы прочитали и одобрили окончательный вариант рукописи.
MvM: дизайн исследования, интерпретация данных, написание и редактирование рукописи. JGZ: дизайн исследования, интерпретация данных, написание и редактирование рукописи. Все авторы прочитали и одобрили окончательный вариант рукописи.
Автор, ответственный за переписку
Переписка с Мария Смит.
Декларация этики
Одобрение этики и согласие на участие
Институциональный наблюдательный совет нашей больницы одобрил исследование (METc 2013/123).
Согласие на публикацию
Неприменимо
Конкурирующие интересы
Авторы заявляют об отсутствии конкурирующих интересов.
Дополнительная информация
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Дополнительная информация
Дополнительный файл 1: Рисунок S1. Выдача ВБД при поступлении.
Права и разрешения
Открытый доступ Эта статья находится под лицензией Creative Commons Attribution 4.0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или в любом формате при условии, что вы укажете авторство оригинальный автор(ы) и источник, предоставьте ссылку на лицензию Creative Commons и укажите, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons на статью, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/.
Перепечатки и разрешения
Об этой статье
Внутрибрюшная гипертензия и абдоминальный компартмент-синдром при заболеваниях печени
- Панель авторов Вход
Что такое открытый доступ?
Открытый доступ — это инициатива, направленная на то, чтобы сделать научные исследования бесплатными для всех. На сегодняшний день наше сообщество сделало более 100 миллионов загрузок. Он основан на принципах сотрудничества, беспрепятственного открытия и, самое главное, научного прогресса. Будучи аспирантами, нам было трудно получить доступ к нужным нам исследованиям, поэтому мы решили создать новое издательство с открытым доступом, которое уравняет правила игры для ученых со всего мира. Как? Упрощая доступ к исследованиям и ставя академические потребности исследователей выше деловых интересов издателей.
На сегодняшний день наше сообщество сделало более 100 миллионов загрузок. Он основан на принципах сотрудничества, беспрепятственного открытия и, самое главное, научного прогресса. Будучи аспирантами, нам было трудно получить доступ к нужным нам исследованиям, поэтому мы решили создать новое издательство с открытым доступом, которое уравняет правила игры для ученых со всего мира. Как? Упрощая доступ к исследованиям и ставя академические потребности исследователей выше деловых интересов издателей.
Наши авторы и редакторы
Мы являемся сообществом из более чем 103 000 авторов и редакторов из 3 291 учреждения в 160 странах мира, включая лауреатов Нобелевской премии и самых цитируемых исследователей мира. Публикация на IntechOpen позволяет авторам получать цитирование и находить новых соавторов, а это означает, что больше людей увидят вашу работу не только из вашей собственной области исследования, но и из других смежных областей.
Оповещения о содержимом
Краткое введение в этот раздел, описывающий открытый доступ, особенно с точки зрения IntechOpen
Как это работаетУправление предпочтениями
Контакты
Хотите связаться? Свяжитесь с нашим головным офисом в Лондоне или командой по работе со СМИ здесь:
Карьера:
Наша команда постоянно растет, поэтому мы всегда ищем умных людей, которые хотят помочь нам изменить мир научных публикаций.
Рецензируемая глава в открытом доступе
Автор:
Хиротэру Камимура, Томоюки Сугано, Рёко Хоригоме, Нарухиро Кимура, Масааки Такамура, Хирокадзу Каваи, Сатоши Ямагива и Шуджи Тераи
Представлено: 10 февраля 2018 г. Просвещенное: 8 апреля 2018 года.
Обзор показателей главы
1 103 загрузки глав
Посмотреть полные показатели
СКАЧАТЬ БЕСПЛАТНОРекламное объявление
Abstract
Внутрибрюшная гипертензия (ВБГ) определяется как внутрибрюшное давление (ВБД) выше 12 мм рт. ст. Абдоминальный компартмент-синдром (ACS) определяется как внутрибрюшное давление выше 20 мм рт. ст. с признаками органной недостаточности. Кроме того, ИАГ/ОКС является состоянием, которое может вызвать острую почечную недостаточность, дыхательную недостаточность, нарушение кровообращения, желудочно-кишечную дисфункцию и печеночную недостаточность из-за повышенного ВБД. Заболеваемость ИАГ/ОКС увеличивается у пациентов в более критическом состоянии и связана со значительным увеличением заболеваемости и смертности. Асцит, кровь или опухоли увеличивают ВБД. При циррозе печени часто встречается массивный асцит. Следовательно, профилактика ИАГ/ОКС может улучшить исходы у пациентов с заболеваниями печени.
ст. Абдоминальный компартмент-синдром (ACS) определяется как внутрибрюшное давление выше 20 мм рт. ст. с признаками органной недостаточности. Кроме того, ИАГ/ОКС является состоянием, которое может вызвать острую почечную недостаточность, дыхательную недостаточность, нарушение кровообращения, желудочно-кишечную дисфункцию и печеночную недостаточность из-за повышенного ВБД. Заболеваемость ИАГ/ОКС увеличивается у пациентов в более критическом состоянии и связана со значительным увеличением заболеваемости и смертности. Асцит, кровь или опухоли увеличивают ВБД. При циррозе печени часто встречается массивный асцит. Следовательно, профилактика ИАГ/ОКС может улучшить исходы у пациентов с заболеваниями печени.
Ключевые слова
- внутрибрюшная гипертензия (ВБГ)
- абдоминальный компартмент-синдром (АКС)
- гепаторенальный синдром (ГРС)
1. Введение
Давление в брюшной полости в норме немного выше атмосферного давление менее 0 мм рт. Определенные физиологические состояния, такие как патологическое ожирение и беременность, могут быть связаны с хроническим повышением ВБД. Однако даже небольшое повышение внутрибрюшного давления может оказывать неблагоприятное воздействие на функцию почек, сердечный выброс, печеночный кровоток, дыхательную механику, внутренностную перфузию и внутричерепное давление. ВБД составляет приблизительно 5–7 мм рт. ст. у взрослых в критическом состоянии.
Определенные физиологические состояния, такие как патологическое ожирение и беременность, могут быть связаны с хроническим повышением ВБД. Однако даже небольшое повышение внутрибрюшного давления может оказывать неблагоприятное воздействие на функцию почек, сердечный выброс, печеночный кровоток, дыхательную механику, внутренностную перфузию и внутричерепное давление. ВБД составляет приблизительно 5–7 мм рт. ст. у взрослых в критическом состоянии.
Wendt et al. впервые описал олигурию на фоне повышенного внутрибрюшного давления в 1876 г. [1]. В 1947 г. Bradley опубликовал оригинальное исследование почечных эффектов повышенного внутрибрюшного давления у людей [2]. Несмотря на эти ранние описания побочных эффектов ВБГ, врачи не уделяют должного внимания значимости повышенного внутрибрюшного давления.
До недавнего времени пациентов с ОКС нередко лечили в отделении интенсивной терапии, и обычно у них наблюдались вздутие живота, повышение пикового давления на вдохе, тяжелая гиперкапния, гипотензия и олигурия. Абдоминальный асцит обычно возникает на конечной стадии печеночной недостаточности. Массивный асцит также влияет на ВБД и вызывает олигурию и острое повреждение почек. Обычно мы распознаем этот симптом и путаем его с гепаторенальным синдромом (HRS). У таких пациентов следует учитывать повышение давления в почечной паренхиме и в почечных венах, поскольку они, вероятно, являются механизмами почечной недостаточности. Обратите внимание, что IAH/ACS и HRS происходят одновременно. Недавно Мацумото и соавт. сообщили, что расширение почечных вен предсказывает плохой исход у пациентов с рефрактерным цирротическим асцитом [3].
Абдоминальный асцит обычно возникает на конечной стадии печеночной недостаточности. Массивный асцит также влияет на ВБД и вызывает олигурию и острое повреждение почек. Обычно мы распознаем этот симптом и путаем его с гепаторенальным синдромом (HRS). У таких пациентов следует учитывать повышение давления в почечной паренхиме и в почечных венах, поскольку они, вероятно, являются механизмами почечной недостаточности. Обратите внимание, что IAH/ACS и HRS происходят одновременно. Недавно Мацумото и соавт. сообщили, что расширение почечных вен предсказывает плохой исход у пациентов с рефрактерным цирротическим асцитом [3].
Объявление
2. Патофизиология ОКС
Патология ВБГ/ОКС – дисбаланс перфузии во многих органах: сдавление портальной системы в брюшной полости, сдавление системы нижней полой вены в органах забрюшинного пространства, сдавление диафрагмы во внутригрудном органе и перфузионная дисфункция мозгового кровообращения за счет повышения внутригрудного давления [4].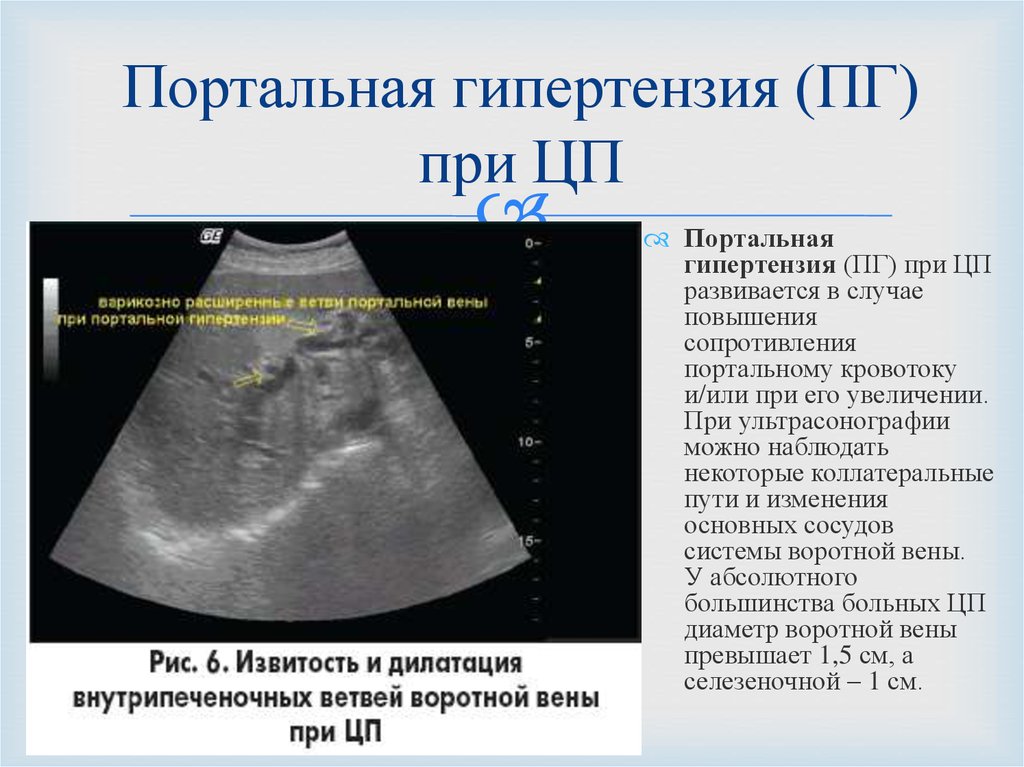
Перфузионный дисбаланс в верхней части тела возникает из брюшной полости, что вызывает нарушение кровообращения и дальнейшее повышение внутригрудного и забрюшинного давления. Этот дисбаланс представляет собой функциональное расстройство, которое существенно влияет на многие органы.
ОКС подобен компартмент-синдрому при мышечных заболеваниях. Это болезнь кровообращения, вызванная внутренним давлением органов, рассеченных в небольшой стенке податливости анатомически [5]. Нормальное ВБД колеблется от субатмосферного уровня до 0 мм рт.ст. Определенные физиологические состояния, такие как патологическое ожирение и беременность, могут быть связаны с хроническим повышением ВБД. Кроме того, ВБГ определяется как ВБД выше 12 мм рт.ст. ОКС определяется как ВБД выше 20 мм рт.ст. с признаками органной недостаточности [6]. ВБД — это стационарное состояние давления, скрытого в брюшной полости. Нормальное ВБД для пациентов в критическом состоянии составляет 5–7 мм рт.ст. После повышения ВБД больные переходят в состояние ВБГ. ВБГ признается устойчивым ВБД выше 12 мм рт.ст. ВБГ также можно разделить на подклассы в зависимости от продолжительности симптомов на одну из четырех групп. Этот молниеносный пример ИАГ обычно приводит к быстрому развитию ОКС. При своем развитии в течение длительного времени брюшная стенка адаптируется и постепенно растягивается в ответ на увеличение ВБД, что дает организму время для физиологической адаптации. Клиническое рассмотрение подтипов ВАГ полезно при назначении лечения пациентам с риском развития ОКС (табл. 1) [6].
ВБГ признается устойчивым ВБД выше 12 мм рт.ст. ВБГ также можно разделить на подклассы в зависимости от продолжительности симптомов на одну из четырех групп. Этот молниеносный пример ИАГ обычно приводит к быстрому развитию ОКС. При своем развитии в течение длительного времени брюшная стенка адаптируется и постепенно растягивается в ответ на увеличение ВБД, что дает организму время для физиологической адаптации. Клиническое рассмотрение подтипов ВАГ полезно при назначении лечения пациентам с риском развития ОКС (табл. 1) [6].
| Классификация IAH | ||||
|---|---|---|---|---|
| Гиперакута IAH | Повышенные IAP для Seconds | Сторонняя активность. | Повышенное ВБД, которое развивается в течение нескольких часов и может привести к быстрому развитию ОКС | Вторичное после травмы или внутрибрюшного кровотечения |
| Подострая ИАГ | Повышенное ВБД, которое развивается в течение нескольких дней и может также привести к ОКС | Медицинские пациенты | ||
| Хронический ВБГ | Повышенное ВБД, которое развивается в течение месяцев или лет. | Беременность, морбидное ожирение, внутрибрюшная опухоль, асцит | ||
Таблица 1.
Классификация внутрибрюшной гипертензии.
ИАГ, внутрибрюшная гипертензия; ОКС, абдоминальный компартмент-синдром.
Первичный ОКС характеризуется наличием острой или подострой ИАГ относительно короткой продолжительности, возникающей в результате интраабдоминальной причины, такой как тяжелый острый панкреатит, абдоминальная травма, разрыв аневризмы брюшной аорты и трансплантация печени [7].
Вторичный ОКС характеризуется наличием подострого или хронического ВБГ, при котором развивается массивная инфузионная терапия, такая как экстраабдоминальная причина, такая как сепсис, капиллярная утечка, ожоги [8].
Всемирное общество абдоминального компартмент-синдрома классифицировало ВАГ на I–IV степени и ОКС (табл. 2) [9].
| Степень IAH | ||
|---|---|---|
| Степень I | ВБД 12-15 мм рт. 1076 1076 | IAP 16-20 мм рт. Ст. Берч и др. предположили, что большинству пациентов с III степенью и всем пациентам с IV степенью следует проводить абдоминальную декомпрессию [10]. Реклама 3. ОКС приводит к неабдоминальной недостаточности органов3.1. Сердечно-сосудистые заболеванияИз-за повышенного внутригрудного давления непрямые измерения сердечного наполнения, такие как центральное венозное давление и давление окклюзии легочной артерии, дают неточные результаты и могут быть увеличены, несмотря на глубокое снижение внутрисосудистого объема. Таким образом, снижение сердечного выброса, вызванное внутрибрюшной гипертензией, усугубляется гиповолемией [11]. 3.2. Респираторные органы Дыхательная недостаточность и дыхательная недостаточность. Начальные признаки ОКС включают повышенное пиковое давление в дыхательных путях у интубированных пациентов со сниженным дыхательным объемом. Последующее повышение внутригрудного давления и гипоксическая легочная вазоконстрикция могут привести к легочной гипертензии [12]. 3.3. НеврологическийВнутричерепное перфузионное давление снижается за счет повышения внутричерепного давления (ВЧД), вызванного нарушением венозного перфузии, включая почечную недостаточность. Было показано, что при повышенном ВЧД декомпрессивная лапаротомия снижает стойкое повышенное ВЧД у пациентов с ИАГ, а сдавление мочеточников, как полагают, не способствует почечной дисфункции, поскольку установка мочеточниковых стентов не приводит к улучшению диуреза [13]. ]. Объявление 4. Внутрибрюшная органная недостаточность при ОКС4.1. Нарушение функции почек ОКС характеризуется выраженным снижением скорости клубочковой фильтрации (СКФ) и почечного плазмотока при отсутствии других причин почечной недостаточности. Более того, изменения сердечного выброса, прямое сдавление почечных сосудов или почечной паренхимы с уменьшением почечного кровотока, повышение сопротивления почечных сосудов и распределение крови от коры почек к мозговому веществу являются механизмами почечной дисфункции [14]. 4.2. Нарушение функции печениDiebel et al. сообщили, что давление в воротной вене (ПВ) экспериментально снизилось у 65% пациентов с ВБД 40 мм рт. ст., а количество микроциркуляции ткани печени уменьшилось до 71% [16]. Дисфункция печени возникает из-за снижения потока ЛВ из-за ВБГ. Кроме того, при сердечной дисфункции усугубляется ишемия печени. Стойкое ВБД снижает среднее артериальное давление в верхней брыжеечной артерии (ВБА) и кровоток в ЛВ на 50% [17]. Расмуссен и соавт. сообщили, что ВБД 25 мм рт. ст. приводит к снижению кровотока в легочной вене на 66 % и 6,5-кратному увеличению портального/печеночного сосудистого сопротивления по сравнению с исходными уровнями [18]. Кроме того, в исследованиях, оценивающих влияние повышенного ВБД на гепатоциты, следует ожидать, что характеристики синусоиды объяснят дисфункцию печени в результате повышенного ВБД. 4.3. Функциональные расстройства желудочно-кишечного трактаДля определения возможности бактериальной транслокации (БТ), которая заключается в нарушении барьерного механизма слизистых оболочек, вызванном снижением кровообращения в слизистых оболочках, а также снижением рН в слизистых оболочках. Кроме того, этот феномен расценивают как причину синдрома полиорганной дисфункции (СПОН) после ОКС, но прямых доказательств нет. Даже если ВБД находится на уровне 20 мм рт.ст., приток крови к слизистой оболочке кишечника снижается до 28 % экспериментально при 61 % исходного значения 40 мм рт.ст. [16]. При СПОН наблюдается ацидоз слизистых оболочек желудочно-кишечного тракта, при котором ВБД, как ожидается, будет на уровне 10 мм рт.ст., обусловленный ОКС. Объявление 5. Диагностика ОКС Диагностика ОКССуществуют различные методы измерения перемежающегося ВБД, такие как инвазивные (прямой, т. или «мочевой пузырь», давление в желудке, толстой кишке или матке через баллонный катетер). Рекомендуется неинвазивное измерение внутреннего давления в мочевом пузыре и внутрижелудочного давления. Внутреннее давление в мочевом пузыре обычно связано с ВБД, измеряемым непосредственно в диапазоне 5–70 мм рт.ст. [6]. Мониторинг внутрипузырного давления, оцененный для ВБД, может быть получен либо с помощью метода закрытого датчика, либо методом закрытого манометра Фолея, который кажется безопасным и не влияет на риск ИМП у пациентов в критическом состоянии [19] (рис. 1). Рис. 1.Измерение внутрибрюшного давления с помощью измерений давления в мочевом пузыре. Реклама 6.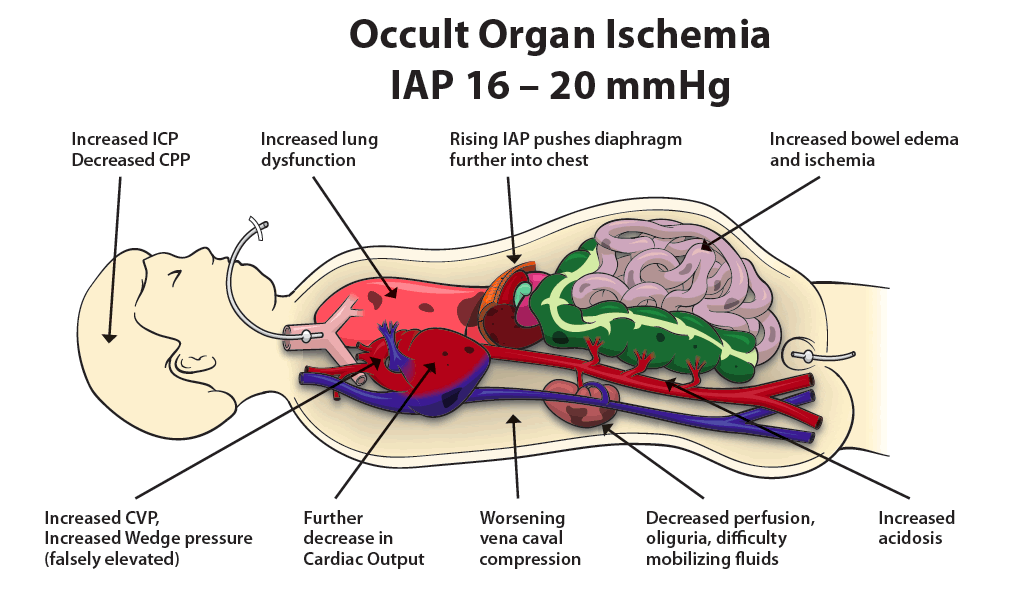 Лечение ОКС Лечение ОКСДискуссии о том, что ВБД должно стать адаптационным стандартом декомпрессии, разделились, но предполагается, что более 25 мм рт. ст. является предварительным клиническим стандартом адаптации. Однако в последнее время необходимо учитывать сообщения о желудочно-кишечных расстройствах из-за нарушения внутрибрюшного давления в нижних отделах брюшной полости. Всемирное общество абдоминального компартмент-синдрома предложило алгоритм ведения ИАГ/ОКС [20]. Было показано, что ранняя индикация метода открытой брюшной полости снижает смертность [21]. Чен и др. сообщили, что лапароскопия может использоваться как безопасная альтернатива декомпрессии ОКС [22]. Всемирное общество абдоминального компартмент-синдрома отмечает, что правильная инфузионная терапия и перфузионная поддержка во время реанимации являются краеугольным камнем медикаментозного лечения пациентов с абдоминальной гипертензией [23]. Фармакотерапия менее эффективна, чем дренажные процедуры. Если у пациента наблюдается декомпенсация, ОКС следует повторно обследовать как потенциальную причину. Advertisement 7. Возможное участие ВБГ/ОКС и ГРСМы сообщили о случае вскрытия с ГРС и ОКС, у которых клинически и гистопатологически были диагностированы заболевания печени и почек. Необходимы дальнейшие клинические исследования для улучшения лечения почечной недостаточности у пациентов с острой печеночной недостаточностью и прогрессирующим циррозом печени (рис. 2 и 3) [25]. Рисунок 2. Печень: терминальная стадия цирроза печени. Микроскопические данные показали расширение синусоидов печени из-за портальной гипертензии и тяжелой желтухи. Рисунок 3.Почка: микроскопия показала опухоль в почечных канальцах. В клубочках и собирательных трубочках изменений не было, почечного фиброза не было. КТ правая почечная вена сдавлена массивным асцитом (стрелка). HRS был впервые описан в 1863 г. Flint как ассоциация между заболеванием печени и олигурической почечной недостаточностью при отсутствии значительных гистологических изменений почек [26]. HRS распознается по интенсивному внутрипочечному вазоспазму, вызванному дисбалансом между сосудорасширяющими и сосудосуживающими медиаторами, наблюдаемым на терминальной стадии заболевания печени [27]. Хотя точная роль ВБГ в ГРС остается не до конца понятой, можно утверждать, что снижение клубочковой перфузии из-за венозного застоя приводит к дальнейшему снижению СКФ. Кейд и др. сообщили о значительном увеличении скорости потока мочи и клиренса креатинина после снижения ВБД с 22 до 10 мм рт. Реклама 8. Лекарственная стратегия при ОКССообщается о нескольких методах контроля рефрактерного абдоминального асцита при терминальной стадии цирроза печени, таких как отказ от нестероидных противовоспалительных препаратов [30], ограничение потребления натрия с пищей [31] , диуретик, LVP, бесклеточная и концентрированная реинфузионная терапия асцита [32], трансъюгулярное внутрипеченочное портосистемное шунтирование [33] и перитонеовенозное шунтирование [34]. ВБД определяется как ВБД выше 12 мм рт. Реклама 9. Заключение Массивный асцит также влияет на ВБД и вызывает олигурию и острое повреждение почек (ОПП). Реклама БлагодарностиАвторы хотели бы поблагодарить Такао Цучиду из отделения гастроэнтерологии и гепатологии Университета Ниигата за его прекрасную помощь в гистологическом анализе. ФинансированиеЭта работа была поддержана грантом в поддержку исследовательской деятельности 17H06691 от Министерства образования, культуры, спорта, науки и технологий (MEXT) Хиротэру Камимура. Каталожные номера
|

 Care Med: крит; 2018.
Care Med: крит; 2018.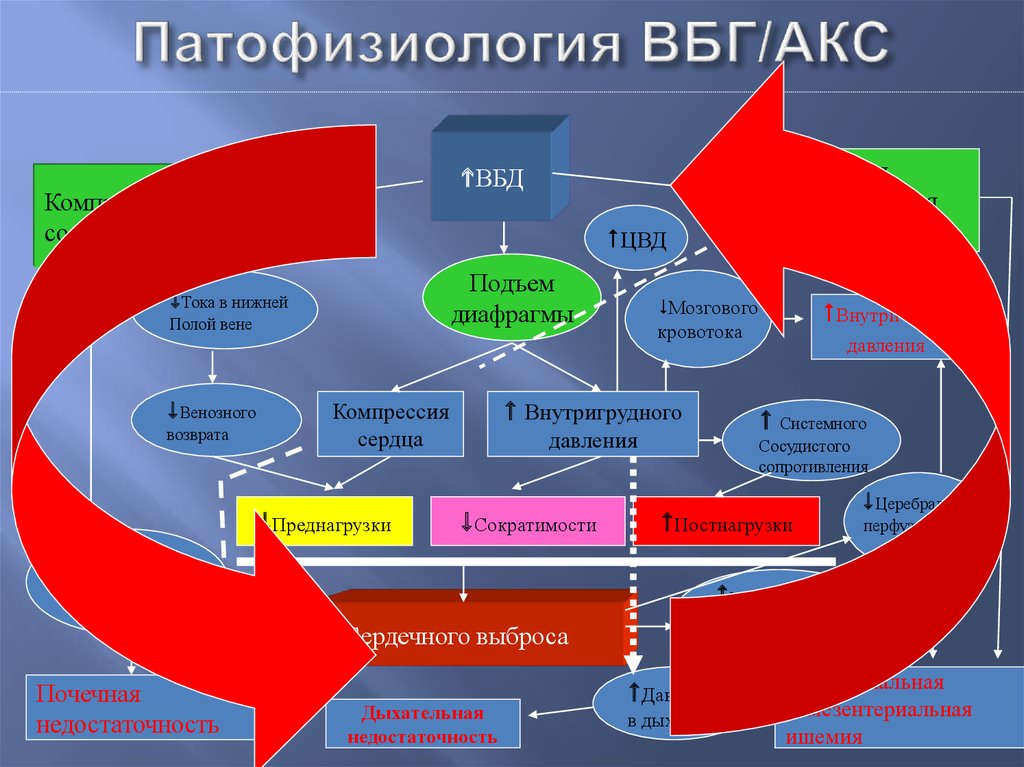 Анестезиол Интенсив Тер. 2015; 47: 241–51.
Анестезиол Интенсив Тер. 2015; 47: 241–51. Критический уход. 2015;19:211.
Критический уход. 2015;19:211. Интенсивная терапия Med Springer-Verlag. 2008; 34:1624–31.
Интенсивная терапия Med Springer-Verlag. 2008; 34:1624–31. С., Зийлстра Дж.Г. Синдром абдоминального компартмента и внутрибрюшная ишемия у больных с тяжелым острым панкреатитом. Мир J Surg. 2016;40:1454–61.
С., Зийлстра Дж.Г. Синдром абдоминального компартмента и внутрибрюшная ишемия у больных с тяжелым острым панкреатитом. Мир J Surg. 2016;40:1454–61. Хирургическая декомпрессия при абдоминальном компартмент-синдроме при тяжелом остром панкреатите. Арка Сур. 2010; 145:764–9.
Хирургическая декомпрессия при абдоминальном компартмент-синдроме при тяжелом остром панкреатите. Арка Сур. 2010; 145:764–9. F. Hulscher
F. Hulscher
 Брэдли и соавт. первыми сообщили, что у животных развивается анурия при ВБД 30 мм рт.ст. [2]. Дополнительными факторами, которые приводят к тому, что ВБД достигает диапазона ОКС, являются снижение сердечного выброса и повышенный уровень катехоламинов [15]. Ренин, ангиотензин и воспалительные цитокины также могут играть роль, еще больше ухудшая функцию почек.
Брэдли и соавт. первыми сообщили, что у животных развивается анурия при ВБД 30 мм рт.ст. [2]. Дополнительными факторами, которые приводят к тому, что ВБД достигает диапазона ОКС, являются снижение сердечного выброса и повышенный уровень катехоламинов [15]. Ренин, ангиотензин и воспалительные цитокины также могут играть роль, еще больше ухудшая функцию почек.
 Агусти и др. сообщили, что добутамин восстанавливает кровоток в слизистой оболочке кишечника в модели внутрибрюшного гипертензии у свиней [24].
Агусти и др. сообщили, что добутамин восстанавливает кровоток в слизистой оболочке кишечника в модели внутрибрюшного гипертензии у свиней [24].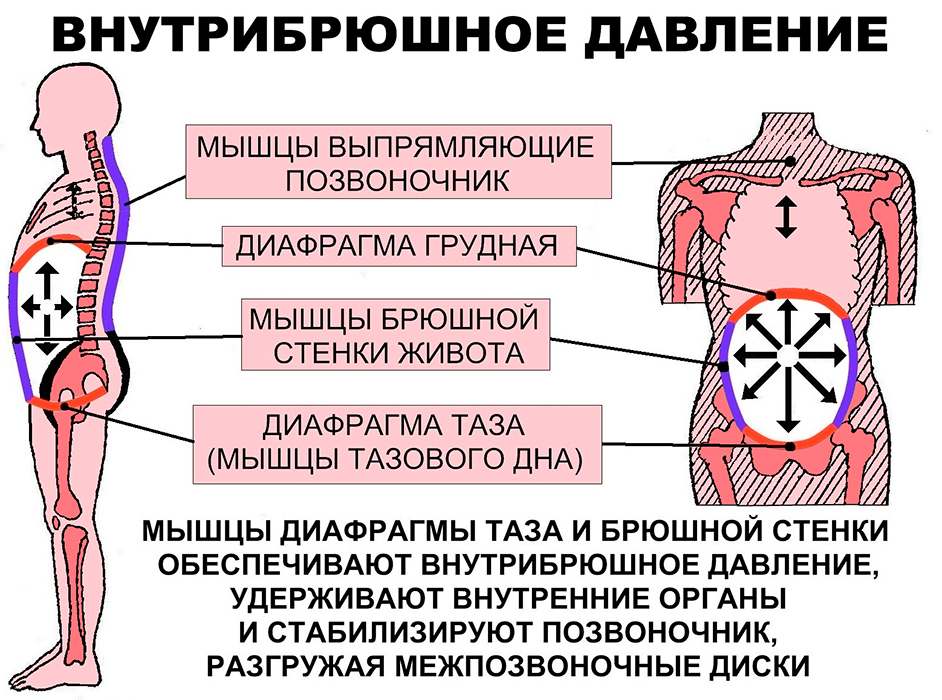
 ст. при парацентезе у пациентов с циррозом печени [28]. Кроме того, предполагается, что компрессия почечной вены играет жизненно важную роль в развитии почечной дисфункции. ВБГ является значимым патологическим механизмом и независимым фактором риска возникновения и развития ГРС [29].]. Кроме того, следует попытаться снизить внутрибрюшное давление после хирургической декомпрессии, парацентеза большого объема (LVP) и применения соответствующих диуретиков.
ст. при парацентезе у пациентов с циррозом печени [28]. Кроме того, предполагается, что компрессия почечной вены играет жизненно важную роль в развитии почечной дисфункции. ВБГ является значимым патологическим механизмом и независимым фактором риска возникновения и развития ГРС [29].]. Кроме того, следует попытаться снизить внутрибрюшное давление после хирургической декомпрессии, парацентеза большого объема (LVP) и применения соответствующих диуретиков. ст. Следовательно, абдоминальный асцит на ранней стадии цирроза печени следует лечить, а раннюю стадию асцита у амбулаторных больных следует лечить немедленно. Амбулаторным пациентам с клинически выраженным асцитом потребуется диуретическая терапия в дополнение к диетическому ограничению натрия. Диуретическая терапия обычно состоит из схемы лечения цирротического асцита, такой как комбинация перорального приема спиронолактона и фуросемида. В последнее время аквапорин-2 представляет собой регулируемый вазопрессином водный канал, экспрессируемый в собирательных трубочках почек. Аквапорин-2 мочи считается маркером реакции собирательных трубочек на толваптан. В Японии в сентябре 2013 г. толваптан был одобрен (в дозах до 7,5 мг/сут) для лечения пациентов с асцитом, которые показали неадекватный ответ на обычные диуретики [35].
ст. Следовательно, абдоминальный асцит на ранней стадии цирроза печени следует лечить, а раннюю стадию асцита у амбулаторных больных следует лечить немедленно. Амбулаторным пациентам с клинически выраженным асцитом потребуется диуретическая терапия в дополнение к диетическому ограничению натрия. Диуретическая терапия обычно состоит из схемы лечения цирротического асцита, такой как комбинация перорального приема спиронолактона и фуросемида. В последнее время аквапорин-2 представляет собой регулируемый вазопрессином водный канал, экспрессируемый в собирательных трубочках почек. Аквапорин-2 мочи считается маркером реакции собирательных трубочек на толваптан. В Японии в сентябре 2013 г. толваптан был одобрен (в дозах до 7,5 мг/сут) для лечения пациентов с асцитом, которые показали неадекватный ответ на обычные диуретики [35]. Обычно мы распознаем этот симптом на стадии терминальной стадии цирроза печени. Этот симптом имеет возможную связь с HRS. У таких пациентов следует учитывать повышение давления в почечной паренхиме и в почечных венах, поскольку они, вероятно, являются механизмами почечной недостаточности. Обратите внимание, что IAH/ACS и HRS происходят одновременно. Гепатологи должны учитывать ИАГ и ОКС при терминальной стадии цирроза печени.
Обычно мы распознаем этот симптом на стадии терминальной стадии цирроза печени. Этот симптом имеет возможную связь с HRS. У таких пациентов следует учитывать повышение давления в почечной паренхиме и в почечных венах, поскольку они, вероятно, являются механизмами почечной недостаточности. Обратите внимание, что IAH/ACS и HRS происходят одновременно. Гепатологи должны учитывать ИАГ и ОКС при терминальной стадии цирроза печени. Ueber den einfluss des intraabdominalenn druckes auf die absonderungsgeschwindigkeit des harnes. Архив физиологии и Heilkunde. 1876;57:527
Ueber den einfluss des intraabdominalenn druckes auf die absonderungsgeschwindigkeit des harnes. Архив физиологии и Heilkunde. 1876;57:527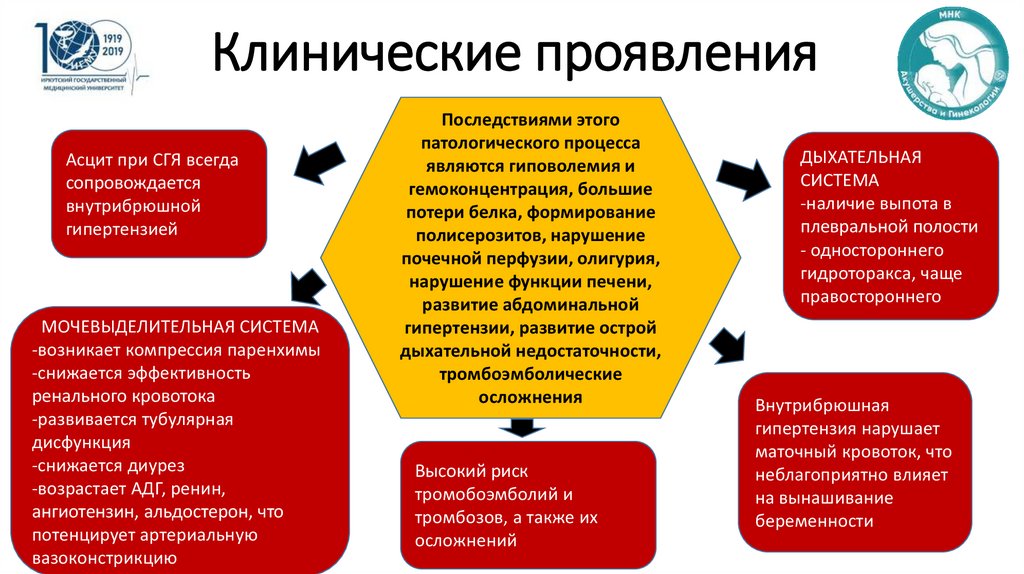 Артроскопия. 2016;32:1478-1486
Артроскопия. 2016;32:1478-1486 , Де Поттер Т.Дж. Внутрибрюшная гипертензия у тяжелобольных: пора обратить внимание. Текущее мнение в области интенсивной терапии; 2005;11:156-171
, Де Поттер Т.Дж. Внутрибрюшная гипертензия у тяжелобольных: пора обратить внимание. Текущее мнение в области интенсивной терапии; 2005;11:156-171 Журнал нейрохирургии. Oct 1988; 69(4):540-544
Журнал нейрохирургии. Oct 1988; 69(4):540-544 Часть A. 2009; 19 (Дополнение 1): S59-S62
Часть A. 2009; 19 (Дополнение 1): S59-S62 Внутрибрюшная гипертензия и синдром абдоминального компартмента: обновленные согласованные определения и рекомендации по клинической практике Всемирного общества синдрома абдоминального компартмента. Медицина интенсивной терапии. 2013;39:1190-1206
Внутрибрюшная гипертензия и синдром абдоминального компартмента: обновленные согласованные определения и рекомендации по клинической практике Всемирного общества синдрома абдоминального компартмента. Медицина интенсивной терапии. 2013;39:1190-1206 , Сифуэнтес А., Фонтаналс Дж., Таура П. Добутамин восстанавливает кровоток слизистой оболочки кишечника в модели внутрибрюшного гипертензии у свиней. Медицина интенсивной терапии. 2000;28:467-472
, Сифуэнтес А., Фонтаналс Дж., Таура П. Добутамин восстанавливает кровоток слизистой оболочки кишечника в модели внутрибрюшного гипертензии у свиней. Медицина интенсивной терапии. 2000;28:467-472 Исследования влияния объема сосудов и внутрибрюшинного давления на функцию почек и печени. Американский журнал медицины. 1987;82:427-438
Исследования влияния объема сосудов и внутрибрюшинного давления на функцию почек и печени. Американский журнал медицины. 1987;82:427-438 Лечение трудноизлечимого асцита путем непрерывной реинфузии стерилизованной, бесклеточной и концентрированной асцитической жидкости. Сделки — Американское общество искусственных внутренних органов. 1977;23:699-702
Лечение трудноизлечимого асцита путем непрерывной реинфузии стерилизованной, бесклеточной и концентрированной асцитической жидкости. Сделки — Американское общество искусственных внутренних органов. 1977;23:699-702