Кушингоидное лицо фото: что такое кушингоидный синдром и как его лечить?
что такое кушингоидный синдром и как его лечить?
Синдром, или болезнь Иценко-Кушинга возникает при нарушении работы надпочечников, которые выделяют слишком много кортизола — гормона стресса. Своё название патология получила благодаря двум исследователям, которые изучали её. В 1912 году этот синдром описал американский врач Харви Кушинг, и независимо от него в 1924-м — одесский невролог Николай Иценко. Заболеванию в 8-10 раз чаще подвержены женщины, чем мужчины. Возраст заболевших в основном от 20 до 40 лет. О том, кто ещё находится в зоне риска, рассказала врач-эндокринолог муниципальной аптечной сети Елена Куран.
Анна Крафт
13:01, 28 октября 2018
«Это люди, которые перенесли черепно-мозговую травму, воспалительные заболевания головного мозга, имеют различные сосудистые аномалии — врождённые либо приобретённые. Также важны инфекционные заболевания, например, тот же туберкулёз гипофиза может быть предпосылкой такого заболевания. Сейчас считается, что генетические дефекты приводят к развитию опухоли в надпочечниках, и вызваны длительным хроническим воздействием глюкокортикоидов на органы и системы», — объяснила врач.
Как отличить кушингоидный синдром от другого заболевания? Есть несколько ярких симптомов, в частности, центральное ожирение.
Фото: nsknews.info
«Происходит перераспределение жировой ткани — она с избытком откладывается в области туловища, живота, груди, плечевого пояса, спины, то есть это такое непропорциональное ожирение. Кожа становится сухой, истончённой. Пациент отмечает у себя общую слабость, сниженную работоспособность, головные боли. На коже живота, плечевого пояса, внутренней поверхности бёдер, ягодицах могут появляться разрывы, они ярко багровые, достаточно широкие.
Болезнь затрагивает и кости. Выработанные гормоны, с одной стороны, негативно влияют на процесс усвоения кальция, а с другой — разрушают белок. Для того чтобы поставить диагноз, врач проведёт осмотр пациента и назначит анализы, говорит врач-эндокринолог муниципальной аптечной сети.
«Ключевым моментом является исследование уровня кортизола либо в крови, либо в слюне. При этом заболевании он будет повышенным. Для уточнения состояния назначаем общие клинические анализы. Исследуем биохимические показатели, уровень сахара в крови, свёртывающую систему и эндокринный статус. Проводим инструментальную диагностику, чтобы определить причину заболевания, т.е. либо это избыточная выработка АКТГ в гипофизе, либо это гормонопродуцирующая опухоль надпочечника. Проводим МРТ головного мозга, УЗИ, КТ или МРТ надпочечников», — объяснила представтель аптечной сети.
Кроме того, для выявления осложнений проводят полное обследование организма. Чтобы избавиться от синдрома Кушинга, необходимо установить его причину и нормализовать уровень кортизола в крови. Лечение включает в себя медикаментозную, хирургическую и лучевую терапию.
«Основным способом лечения синдрома и болезни Иценко-Кушинга является хирургический. При болезни Иценко-Кушинга проводится удаление аденомы гипофиза, при синдроме Иценко-Кушинга удаляют опухоль надпочечника. Заболевание лечится медикаментозно на этапе подготовки к операции, чтобы стабилизировать состояние пациента. В ряде случаев, если операция противопоказана по каким-либо причинам, пациент находится на постоянном медикаментозном лечении. Также мы проводим симптоматическое лечение: это и снижение сахара в крови, снижение артериального давления», — поделилась Елена Куран.
Врач-эндокринолог советует: если резко поднимается артериальное давление, происходит неравномерно перераспределение подкожной жировой клетчатки, а также появляются разрывы на коже — нужно обратиться к терапевту.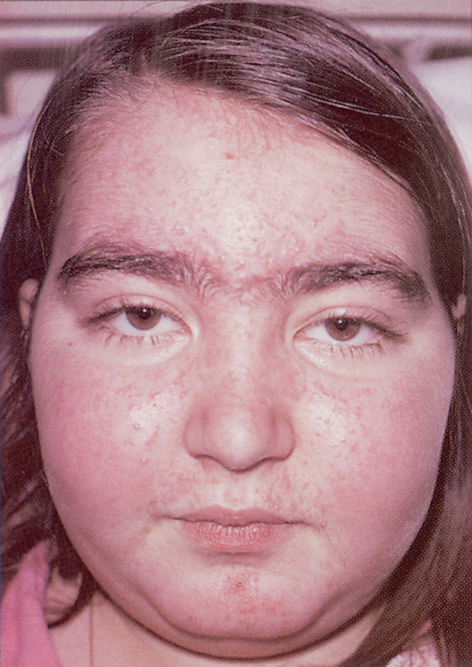
#Здоровье #Здравоохранение #Консультация специалиста #Интервью #Будьте здоровы
Синдром Иценко-Кушинга: симптомы, признаки и лечение
Болезнь Иценко-Кушинга (а также и синдром) развивается либо вследствие длительного и частого лечения гормональными препаратами, либо возникает на фоне повышенного синтеза кортикостероидных гормонов в организме. В связи с этим появляется определенный симптомокомплекс.
Данное патологическое состояние характерно еще и тем, что значительно повышается продуцирование адренокортикотропного гормона. И уже следствием этого является избыточная выработка надпочечниками кортизола. Такая цепочка гормональных нарушений и есть гиперкортицизм или кушингоид. Необходимо знать основные симптомы синдрома кушинга у женщин.
Описание синдрома
Как уже говорилось выше, синдром кушинга характерен излишней деятельностью надпочечников, в результате которой организм перенасыщается кортизолом. Этот процесс становится возможным благодаря контролю гипофиза, который, в свою очередь, вырабатывает адренокортикотропный гормон. И уже на деятельность гипофиза влияет гипоталамус, продуцирующий либерины и статины. Получается своеобразная цепочка, нарушение которой в любом ее звене и становится причиной повышенной секреции коры надпочечников. В связи со всем этим и развивается синдром Иценко-Кушинга.
Превышение количества кортизола в организме провоцирует распад и расщепление белковых соединений. Из-за этого многие ткани и структуры претерпевают негативные изменения.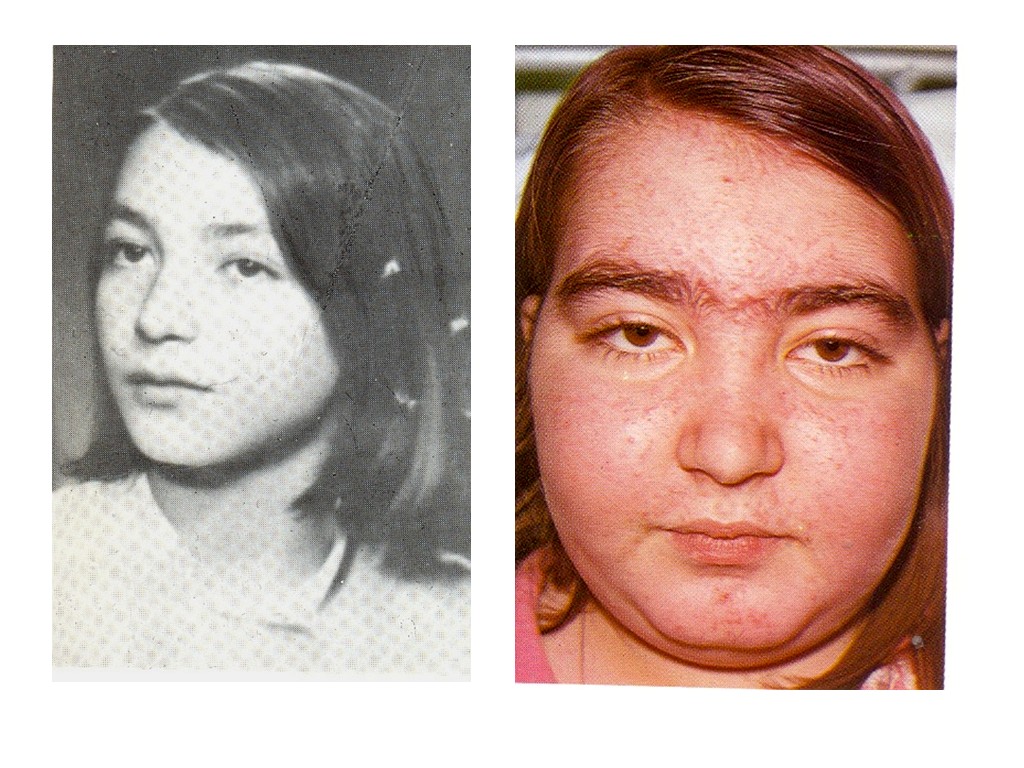 В первую очередь страдают кости, кожа, мышцы и внутренние органы. Чем дальше заходит процесс распада, тем более ярко проявляются процессы дистрофии и атрофии в организме. Нарушениям также подвержен обмен жирами и углеводами.
В первую очередь страдают кости, кожа, мышцы и внутренние органы. Чем дальше заходит процесс распада, тем более ярко проявляются процессы дистрофии и атрофии в организме. Нарушениям также подвержен обмен жирами и углеводами.
к содержанию ↑Женщины репродуктивного возраста от 25 до 40 лет гораздо чаще испытывают симптомы синдрома кушинга.
Формы синдрома
- АКТГ — зависимая форма включает в себя синдром эктопической продукции АКТГ и болезнь Кушинга, когда повышается уровень АКТГ. Результатом всего этого является разрастание отдельных зон надпочечников, из-за чего кортизол и андрогены и вырабатывается в больших объемах, чем это необходимо организму. На такую форму приходится 15-20% от общего количества диагностирования синдрома Кушинга. В некоторых случаях у больных может даже отсутствовать признаки повышенного уровня глюкокортикостероидов – такое состояние может быть обусловлено стремительным протеканием болезни. Это характерно для людей, болеющих мелкоклеточным раком легких – прогнозы для них самые неблагоприятные. Эктопическая секреция АКТГ может быть и признаком классической формы синдрома Кушинга. Это сильно затрудняет диагностику симптомов у женщин – опухолевые образования не всегда заметны на рентгене.
- АКТГ — независимый синдром Кушинга – возникновением данного состояния становится первичное опухолевое новообразование надпочечников (к примеру, аденома или рак), либо их узелковое разрастание. При таком прогрессировании синдрома выработка АКТГ гипофизом подавляется повышенной выработкой кортизола. 10% — это доброкачественные опухоли надпочечников (аденома и другие). 70% синдрома Кушинга приходится именно на эту форму. Женщины страдают от этого в 8 раз чаще, чем мужчины. Возраст 20-40 лет, но редко возрастная группа может охватывать пациентов до 70 лет.
Причины развития
| Основная причина | Группы риска | Симптомы и проявления |
|---|---|---|
| Опухоль | Женщины, имеющие злокачественные образования. | 1-2% случаев развития синдрома Кушинга. Причина – это опухоль, вырабатывающая такие же гормоны. Локализация опухоли может быть самая разная – половые железы, легкие, печень и прочие органы. |
| Аденома надпочечников | Женщины с нарушениями в функционировании эндокринной системы. | 14-18% от общего количества синдрома Кушинга. Причина кроется в опухолевом процессе коры надпочечников (аденома и другие образования). |
| Рак в надпочечниках | У женщин с генетической предрасположенностью. | Очень редко, когда от родителей к ребенку передается предрасположенность к образованию опухолей эндокринной природы. Из-за этого повышается вероятность возникновения новообразований, которые, в свою очередь, и станут причиной развитиясиндрома Кушинга. |
| Болезнь Иценко-Кушинга | У женщин с 20 до 40 лет. | В 80% случаев пациентов ссиндромом Кушинга его причиной становится именно болезнь Иценко-Кушинга. Тогда избыточное количество АКТГ вырабатывается микроаденомой гипофиза (опухолью доброкачественного характера очень маленького размера – до 2 см).Болезнь же Иценко-Кушинга возникает в связи с травмой головы и инфекции, пагубно влияющие на головной мозг. Этаболезньможет также развиться у женщин, сразупослеродов. |
| Медикаменты | У женщин с 20 до 40 лет. | Прием медикаментов, имеющих в своем составе глюкокортикоидные гормоны. Ярким тому подтверждение является препараты Преднизолон и Дексаметазон, а также другие лекарственные средства, применяемые для лечения волчанки, бронхиальной астмы и прочих заболеваний. Если причина именно в препаратах, то необходимо в самые короткие сроки максимально снизить дозу их применения. Необходимо это сделать без особого ущерба для лечения основного заболевания, от которого они назначались. |
Симптомы и признаки синдрома Кушинга
Симптомы синдрома кушинга у женщин:
- Ожирение.
 Такой симптом у женщин достаточно просто визуализировать, так как при этом сильно меняется ее внешний вид: обильные жировые отложения на лице, шее, груди и животе. Значительная прибавка массы тела – самый первый и частый симптом синдрома Кушинга. Удивительно то, что руки и ноги при таких жировых отложениях достаточно худые и даже могут уменьшаться в объеме. Особенно значительные жировые складки находятся на шее и на затылке. Крайне редки случаи, когда жировые отложения отсутствуют.
Такой симптом у женщин достаточно просто визуализировать, так как при этом сильно меняется ее внешний вид: обильные жировые отложения на лице, шее, груди и животе. Значительная прибавка массы тела – самый первый и частый симптом синдрома Кушинга. Удивительно то, что руки и ноги при таких жировых отложениях достаточно худые и даже могут уменьшаться в объеме. Особенно значительные жировые складки находятся на шее и на затылке. Крайне редки случаи, когда жировые отложения отсутствуют. - Еще один видимый симптом — «лунообразное лицо» или кушингоидное лицо – ярко-красный цвет лица, иногда даже с признаками цианоза.
- Симптом изменения кожных покровов. Эпидермис в результате развития синдрома становится тонким и сухим, он сильно шелушится и под ним становится явно выражен рисунок сосудов у женщин. Кожа настолько тонкая и хрупкая, что возможно образование кровоподтеков даже в результате незначительного травмирования – это бывает в 40% при данном синдроме. Данному синдрому характерны угревые высыпания на коже и гиперпигментация у женщин. Любые ранки и повреждения очень плохо заживают, может быть даже отмечено расползание швов после оперативного вмешательства. Слизистые оболочки легко подвергаются воздействию грибковых инфекций (лишай, стоматит и прочие).
- Растяжки – тоже частый симптом описываемого синдрома (50%). Стрии имеют фиолетовый или красный оттенок и отличаются крупными размерами (до нескольких сантиметров). Однако, у женщин старше 40 лет такое явление достаточно редкое. Как правило, они возникают на животе, но могут быть и на груди, ягодицах, подмышками и на бедрах.
- Гирсутизм – это избыточный рост жестких темных волос по мужскому признаку. Это происходит из-за повышенной работы надпочечников и наблюдается примерно в 80% случаев у женщин при синдроме Кушинга. В основном оволосение происходит на лице, но может затрагивать также грудь, плечи и живот. Такое явление, как гирсутизм, часто идет вместе с угрями и даже себореей у женщин.
 Крайне редко может встречаться такой симптом синдрома кушинга, как вирилизация – появление в облике женщины мужских черт. Обычно, оно проявляется при раке надпочечников.
Крайне редко может встречаться такой симптом синдрома кушинга, как вирилизация – появление в облике женщины мужских черт. Обычно, оно проявляется при раке надпочечников. - Гипертония – частый признак, сопутствующий синдрому Кушинга (75% случаев). Высокое давление и особенно осложнения, вызванные ею, становятся частой причиной смертности таких пациентов.
- Дисфункция половых желез. Тоже один из наиболее часто встречающихся симптомов синдрома кушинга. У женщин он выражается в повышенной выработке андрогенов и кортизола. При этом состоянии 75% женщин страдает бесплодием или аменореей.
- Психические расстройства и нарушения в этой области — частое явление у таких пациентов. Повышенная раздражительность, депрессивные состояния, изменение концентрации внимания и расстройства памяти, симптомы бессонницы – такие признаки очень часто бывают при синдроме Кушинга. Реже – маниакальные проявления, эйфорические состояния, психозы с бредом, попытки самоубийства. В особенно тяжелых случаях даже может снижаться объем головного мозга.
- Ощущение слабости в мышцах имеет место быть у 60% пациентов. Особенно этот симптом ощутим на мышцах ног. Это связано с тем, что снижается количество белка в организме и, как следствие, безжировая масса тела.
- Снижение плотности костей (остеопороз) вызывается глюкокортикоидами. Это опасно частыми переломами ребер, конечностей, позвонков (сдавливающие переломы позвонков встречаются у 15-20% ). Первый признак – боли в спине. Потеря костной массы (остеопения) у пациентки любого возраста – веская причина для тщательного обследования состояния надпочечников. Не рентгенологическом снимке можно обнаружить «стеклянные позвонки», это явление, когда отдельные позвонки выглядят полностью просвечивающимися. Вместе с атрофическим состоянием мышц из-за такого явления часто развивается сколиоз у женщин.
- Симптомы мочекаменной болезни есть в 15% синдрома Кушинга.
 Это происходит из-за того, что при повышенной концентрации глюкокортикоидов в организме, в моче наблюдается избыток кальция. Как ни странно, но диагностировать синдром Кушинга у некоторых женщин случалось именно из-за его обращения к врачу в связи с жалобами на колики в почках.
Это происходит из-за того, что при повышенной концентрации глюкокортикоидов в организме, в моче наблюдается избыток кальция. Как ни странно, но диагностировать синдром Кушинга у некоторых женщин случалось именно из-за его обращения к врачу в связи с жалобами на колики в почках. - Симптомы синдрома Кушинга в виде сильной жажды и повышенная выработка мочи (полиурия).
- Кардиомиопатия. Гормоны негативно воздействуют на средний мышечный слой сердца (миокард). Из-за этого случаются сбои сердечного ритма и сердечная недостаточность. Такой симптом крайне опасен и часто становится причиной смерти пациентов с симптомом Кушинга.
- Возникновение сахарного диабета стероидного типа (10-20% пациентов с синдромом Кушинга). В возникновении такого сахарного диабета поджелудочная железа не играет никакой роли (как в обычных случаях).
Осложнения при синдроме Кушинга
Осложнения симптомов синдрома кушинга у женщин:
- перехождение процесса и симптомов в хроническую форму. Без квалифицированного медицинского лечения у женщины симптомов синдрома Кушинга это часто является причиной летального исхода. Хронический процесс чреват инсультами, сбоями деятельности сердца, серьезными нарушениями в позвоночнике.
- надпочечниковый или адреналиновый криз проявляется такими симптомами, как рвота и боли в области живота, снижение сахара в крови, повышенное артериальное давление и расстройство сознания.
- грибковые образования, фурункулы и флегмоны, различные процессы гнойного характера – все это может быть из-за снижения сопротивляемости организма к различного рода инфекциям.
- симптомы мочекаменной болезни у женщины из-за повышенного вывода кальция и фосфатов из организма вместе с мочой.
Беременность при синдроме Кушинга
Прогноз вынашиваемости беременности в совокупности с такими симптомами крайне неблагоприятный. Очень часто беременность самопроизвольно обрывается уже на самых ранних сроках или же случаются роды раньше времени. Плод сильно отстает в развитии, из-за чего и возможна его смерть в этот период.
Плод сильно отстает в развитии, из-за чего и возможна его смерть в этот период.
Невынашиваемость беременности связана с надпочечниковой недостаточностью у эмбриона из-за такой же патологии у матери.
Можно с уверенностью назвать беременность фактором развития осложнений симптомов данного синдрома у женщины. Это опасно настолько, что может возникнуть непосредственная угроза жизни пациентки.
Если все же беременность протекает согласно нормам, очень важно постоянно наблюдаться у специалистов и получать курсы симптоматической терапии для поддержания состояния будущей роженицы.
к содержанию ↑Диагностика
Методы диагностики симптомов синдрома кушинга у женщин:
- Скрининговый тест, направленный на обнаружение количества кортизола в суточной дозы мочи. Если по результатам теста выходит, что уровень этого гормона повышен в 3-4 раза, то это явный симптом синдрома Кушинга у женщин.
- Малая дексаметазоновая проба – это исследование может точно подтвердить или опровергнуть эндогенную природу симптомов синдрома у женщины. В ходе этого исследования у здорового человека после приема соответствующего препарата (применяемого при исследовании) концентрация кортизола в крови снизится в 2 раза. Если же есть синдром Кушинга, то такого снижения не наблюдается.
- Большая дексаметазоновая проба (показана при положительной малой пробе). Она способна с точностью диагностировать как саму болезнь Иценко-Кушинга, так и синдром. Разница с малой пробой лишь в количестве введенного препарата – оно значительно больше. Снижение уровня кортизола в крови на 50% означает болезнь Иценко-Кушинга, а отсутствие любых изменений – синдром.
- Анализы крови и мочи. В составе крови замечается значительное повышение гемоглобина, холестерина и эритроцитов. В ходе лабораторного исследования замечается высокое содержание оксикортикостероидов и низкое – кетостероидов.
- МРТ или КТ надпочечников для определения расположения опухолей и прочих патологических процессов необходимо для назначения адекватного лечения женщины от симптомов синдрома Кушинга.

- Рентгенография для обнаружения симптомов деформаций позвоночника, переломов ребер и почечных камней у женщин.
- ЭКГ необходимо для определения электролитных процессов и нарушений в работе сердца.
Лечение симптомов у женщины
Методы лечения женщин с симптомами синдрома кушинга:
- Медикаментозное лечение. Для этого используются лекарственные средства, действующие на гипофиз таким образом, что идет уменьшение выработки адренокортикотропного гормона, высокая секреция которого и есть причина синдрома. Одновременно с такой терапией обязательно показано симптоматическое лечение у женщины основных симптомов синдрома Кушинга – понижение сахара в крови, артериального давления. Лечение лекарственными средствами симптомов синдрома Кушинга у женщин обязательно включает в себя прием антидепрессантов и препаратов, повышающих плотность костей. Назначение лекарств проводится только врачом после рассмотрения результатов исследований и самих симптомов.
- Хирургическое лечение симптомов синдрома кушинга. Если болезнь Иценко-Кушинга является следствием аденомы гипофиза, то ее удаляют хирургическим путем. Это, пожалуй, самый эффективный и, по сути, единственный метод устранения проблемы. Операцию проводят при наличии четких границ опухоли и результат такого вмешательства очень хороший.
- Лучевая терапия – эффективная методика борьбы с синдромом, дающая хорошие шансы на выздоровление. Такое лечение симптомов синдрома Кушинга у женщин может проводиться в комплексе с оперативным иссечением новообразования.
Прогноз синдрома Кушинга
При отсутствии необходимого и своевременного лечения вероятность летального исхода составляет 40-50% всех случаев синдрома Кушинга. Это происходит из-за необратимых изменений в организме пациента.
Если имеют место злокачественные новообразования при синдроме Кушинга, ставшие причиной данного состояния, то прогноз не может порадовать. Лишь в 20-25% случаев, после проведения операции и соответствующего послеоперационного лечения, возможен более-менее положительный результат.
Лишь в 20-25% случаев, после проведения операции и соответствующего послеоперационного лечения, возможен более-менее положительный результат.
Если опухоль при синдроме Кушинга имела доброкачественную природу, то после ее оперативного иссечения, положительная динамика наблюдается почти в 100% случаев.
Иценко-Кушинга болезнь (гиперкортицизм) › Болезни › ДокторПитер.ру
Болезнь Иценко-Кушинга (БИК) — тяжелое многосимптомное заболевание, возникающее в случае нарушения регуляции гипоталамо-гипофизарно-надпочечниковой системы, когда образуется переизбыток гормонов надпочечников — кортикостероидов, и при образовании опухоли гипофиза (кортикотропиномы) или его гиперплазии.
Симптомы этой болезни были описаны в разное время двумя учеными – американским нейрохирургом Харви Кушингом и одесским невропатологом Николаем Иценко.
Американский специалист связал болезнь с опухолью гипофиза, советский ученый предположил, что причина заболевания кроется в изменениях гипоталамуса — участка мозга, отвечающего за взаимодействие нервной и эндокринной систем. Сегодня ученые пришли к мнению, что болезнь Иценко-Кушинга возникает в результате сбоев в работе гипоталамо-гипофизарной системы — оба исследователя оказались правы.
Признаки
Жалобы основаны на проявлениях артериальной гипертензией (головная боль, мелькание «мушек» перед глазами), развивающемся катаболическом синдроме (резкая мышечная слабость, боль в пояснице, невозможность выполнения физической работы) или возникающих на фоне болезни половых расстройствах. Несмотря на специфические изменения внешности, они редко беспокоят пациентов, за исключением случаев, когда у женщин развивается очень заметный гипертрихоз.
Клиническая картина болезни Иценко-Кушинга очень характерна. У больных увеличивается масса тела, перераспределяется подкожно-жировая клетчатка («кушингоидный» тип ожирения) – полнеет область плечевого пояса, надключичных пространств, шейных позвонков («климактерический горбик»), живота.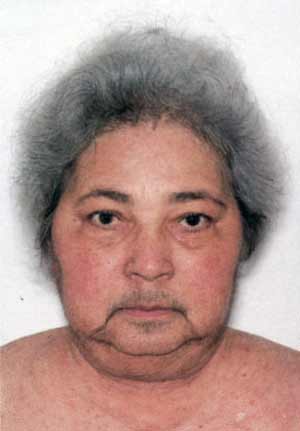 При этом происходит утончение конечностей в результате уменьшения жировой клетчатки и атрофии мышечной ткани. Лицо становится круглым («лунообразным»), щеки – багрово-красного цвета («матронизм»), проявляются трофические изменения кожи с развитием длительно незаживающих язв, ее сухость и повышенное шелушение. На бедрах, груди, плечах, животе появляются своеобразные полосы растяжения – стрии красно-фиолетового цвета. Мельчайшие сосуды – капилляры становятся ломкими, поэтому даже при небольших травмах образуются синяки (гематомы).
При этом происходит утончение конечностей в результате уменьшения жировой клетчатки и атрофии мышечной ткани. Лицо становится круглым («лунообразным»), щеки – багрово-красного цвета («матронизм»), проявляются трофические изменения кожи с развитием длительно незаживающих язв, ее сухость и повышенное шелушение. На бедрах, груди, плечах, животе появляются своеобразные полосы растяжения – стрии красно-фиолетового цвета. Мельчайшие сосуды – капилляры становятся ломкими, поэтому даже при небольших травмах образуются синяки (гематомы).
Наряду с этим отмечается гиперпигментация кожных покровов в местах трения (шея, локтевые суставы, подмышечные впадины). У женщин часто наблюдается рост волос (гирсутизм) на лице и груди.
Одним из ранних симптомов являются половые расстройства в виде нарушения менструаций, снижения потенции.
Описание
Одним из грозных проявлений болезни является поражение сердечно-сосудистой системы, в виде развития гипертонии с нарушениями обмена веществ в сердечной мышце. Атрофируются и другие мышцы с соответствующими клиническими проявлениями (например, при атрофии мышц брюшной стенки образуется «лягушачий» живот). Развиваются электролитные нарушения, остеопороз, сахарный диабет.
В результате снижения иммунитета развиваются гнойничковые (акне) или грибковые поражения кожи и ногтей, трофические язвы голеней, хронический и трудно поддающийся лечению пиелонефрит. Ярко выражено нарушение мозговой деятельности (энцефалопатия) в виде эмоционально-личностных сдвигов: от нарушения настроения, сна и до выраженных психозов.
Системный остеопороз представляет собой распространенное и нередко тяжело протекающее проявление гиперкортицизма.
Причины болезни Иценко-Кушинга точно не установлены. Возникает она в любом возрасте, но чаще в 20-40 лет. При этом женщины болеют в 10 раз чаще, чем мужчины, наблюдается зависимость от беременности и родов, а также от травм головного мозга и нейроинфекций.
У 85 % больных обнаруживается аденома передней доли гипофиза, что, по современным представлениям, является первопричиной заболевания.
Опухоли гипофиза (микро-и макроаденомы), воспалительные процессы головного мозга у женщин часто развивается после родов. Опухоли надпочечника (глюкостеромы, глюкоандростеромы), опухоли легких, бронхов, средостения, поджелудочной железы, вырабатывающие адренокортикотропный гормон (АКТГ), синдром эктопической продукции АКТГ вызывают синдром Кушинга, характеризующийся сходными клиническими симптомами.
Диагностика
При подозрении на болезнь Иценко-Кушинга после сбора анамнеза и клинического осмотра у всех больных с помощью методов лабораторной диагностики необходимо подтвердить наличие гиперкортицизма путем определения суточной секреции кортизола крови, содержание свободного кортизола в суточной моче.
В сомнительных случаях проводится малая проба с дексаметазоном (отрицательная малая проба с дексаметазоном и положительная большая дексаметазовая проба позволяют поставить диагноз опухоли гипофиза).
При выявлении повышенной продукции кортизола необходимо провести следующий этап обследования — дифференциальную диагностику между болезнью Иценко-Кушинга, АКТГ-эктопированным синдромом и синдромом Иценко-Кушинга.
Затем производят топическую диагностику с использованием таких методов диагностики, как рентгенографию костей черепа, компьютерной и магнитно-резонансной томографии головного мозга. Применение этих методик позволяет не только определить на ранних стадиях наличие опухоли гипофиза, но и установить ее точную локализацию, размеры, направление роста, взаимоотношение с окружающими тканями.
Также проводят ультразвуковое исследование надпочечников и компьютерную и магнитно-резонансную томографию надпочечников.
При обнаружении (или отсутствии) аденомы гипофиза врач принимает решение о проведении лечения и выборе наиболее подходящего метода.
Лечение
Различают легкую, средней тяжести и тяжелую формы заболевания. Его течение может быть прогрессирующим (развитие всей симптоматики за 6-12 месяцев) и торпидным (симптомы постепенно нарастают в течение 3-10 лет).
Эффективность лечения зависит от точности диагностики, правильной оценки активности гиперкортицизма и тяжести заболевания, а также от индивидуального подхода к выбору методов лечения. Оно должно быть направлено на исчезновение основных клинических симптомов гиперкортицизма, стойкую нормализацию уровня АКТГ и кортизола в плазме крови с восстановлением их суточного ритма и нормализацию кортизола в суточной моче.
При легком и среднетяжелом течении назначают медикаментозное лечение, блокирующее избыточную выработку АКТГ или кортикостероидов или проводят лучевую терапию межуточно-гипофизарной области (гамма-терапия или протонотерапия), с помощью которой удается «подавить» активность гипофиза. Если лучевая терапия неэффективна, проводится хирургическое лечение — удаление опухоли гипофиза. Одной из разновидностей хирургического лечения является разрушение опухоли гипофиза с помощью низких температур (криохирургия). Для этих целей используется жидкий азот, который подводят в область опухоли. При стремительном развитии заболевания и неэффективности терапевтического лечения выполняют операцию по удалению одного или двух надпочечников (адреналэктомия). После этой операции развивается хроническая надпочечниковая недостаточность, что требует постоянной заместительной терапии.
Симптоматическая терапия направлена на компенсацию белкового, минерального и углеводного обмена, контроль артериального давления. Чаще всего в лечении болезни Иценко-Кушинга и синдрома Иценко-Кушинга используют сочетание различных методов: медикаментозного и хирургического лечения, медикаментозной и лучевой терапии и т.д.
© Доктор Питер
Глюкокортикоидный синдром Кушинга в практике ревматолога (обзор литературы) Текст научной статьи по специальности «Клиническая медицина»
ОБЗОРЫ
Глюкокортикоидный синдром Кушинга в практике ревматолога (обзор литературы)
А. М. Сатыбалдыев
М. Сатыбалдыев
ФГБУ«Научно-исследовательский институт ревматологии им. В.А. Насоновой» РАМН, Москва
Глюкокортикоиды (ГК) используют для лечения различных воспалительных и аутоиммунных заболеваний благодаря их противовоспалительным и иммунорегуляторным свойствам. Однако ГК могут приводить к развитию многих нежелательных реакций (НР): артериальная гипертония, сахарный диабет, нарушения липидного обмена, апноэ сна, остеопороз, миопатия и нарушения коагуляции и фибринолиза, которые являются компонентами синдрома Иценко — Кушинга (СК). Известно, что НР, индуцированные ГК, зависят от их состава, способа введения, дозы и продолжительности лечения. Однако основные патогенетические механизмы НР четко не определены. Имеются доказательства, указывающие на роль дисбаланса между вазоконстрикцией и вазоди-латацией, а также возможную связь с оксидом азота, простаноидами (простагландины, простациклин и тромбоксан), ангиотензином II, вазопрессином, аргинином, эндотелинами, катехоламинами, нейропептидами У и предсердным натрийуретическим пептидом. Также свой вклад вносят усиление окислительного стресса, активизация системы ренин — ангиотензин, эскалация прес-сорного ответа, метаболический синдром и апноэ сна. Идеальным могло бы стать прерывание лечения ГК, но чаще всего это невозможно из-за последующего обострения заболевания. Кроме того, необходимо тщательно планировать выбор дозы, времени и способа введения ГК и оценивать каждую НР. Центральное место в исследованиях должна занимать разработка ГК с выраженным противовоспалительным действием и незначительными метаболическими эффектами.
Ключевые слова: эндогенный и экзогенный синдром Иценко — Кушинга; глюкокортикоиды; нежелательные реакции.
Контакты: Азамат Махмудович Сатыбалдыев [email protected]
Для ссылки: Сатыбалдыев АМ. Глюкокортикоидный синдром Кушинга в практике ревматолога (обзор литературы). Современная ревматология. 2013;(4):78—84.
Глюкокортикоидный синдром Кушинга в практике ревматолога (обзор литературы). Современная ревматология. 2013;(4):78—84.
Cushing’s glucocorticoid syndrome in the practice of a rheumatologist (A review of literature)
A.M. Satybaldyev
V.A. Nasonova Research Institute of Rheumatology, Russian Academy of Medical Sciences, Moscow
Glucocorticoids (GCs) are used to treat different inflammatory and autoimmune diseases due to their anti-inflammatory and immunoregulato-ry properties. However, GC may lead to the development of many adverse reactions (ARs): hypertension, diabetes mellitus, lipid metabolic disturbances, sleep apnea, osteoporosis, myopathy, and coagulation and fibrinolysis disorders, which are components of the Itsenko — Cushing syndrome. ARs induced by GCs are known to depend on their composition, route of administration, dose, and duration of treatment. However, the major pathogenic mechanisms of ARs are not clearly defined. There is evidence suggesting a role for imbalance between vasoconstriction and vasodilation, and its possible association with nitric oxide, prostanoids (prostaglandins, prostacyclin, and thromboxane), angiotensin II, vasopressin, arginine, endothelins, catecholamines, neuropeptides Y, and atrial natriuretic peptide. Enhanced oxidative stress, activated ren-inangiotensin system, escalating pressor response, metabolic syndrome, and sleep apnea also make their contribution. It could be ideal to discontinue GC treatment; but this is most commonly impossible because of a further disease exacerbation. In addition, it is necessary to carefully plan the choice of the dose, time, and route of administration of GCs and to evaluate each AR. The design of a GC with marked anti-inflammatory activity and insignificant metabolic effects must hold a central position in its researches.
Key words: endogenous and exogenous Itsenko — Cushing syndrome; glucocorticosteroids; adverse reactions.
Contact: Azamat Makhmudovich Satybaldyev [email protected]
For reference: Satybaldyev AM. Cushing’s glucocorticoid syndrome in the practice of a rheumatologist (a review of literature). Modern Rheumatology Journal. 2013;(4):78—84.
DOI: http://dx.doi.org/10.14412/1996-7012-2013-2443
Синдром Кушинга (СК, или синдром Иценко — Кушинга, синдром гиперкортицизма, кушингоид) объединяет группу заболеваний, развивающихся вследствие длительного хронического воздействия на организм избыточного количества гормонов коры надпочечников, независимо от причины, которая вызвала повышение их уровня в крови. В ос-
нове патогенеза патологических изменений большинства органов и систем лежит в первую очередь гиперпродукция кортизола. Синдром чаще развивается при избыточном применении синтетических глюкокортикоидов (ГК).
Классификация. Различают эндогеннный СК — ЭнСК (избыточный уровень кортизола вырабатывает организм хо-
ОБЗОРЫ
зяина) и экзогенный СК — ЭкСК (в организм извне поступает избыточное количество, как правило, синтетических ГК — лекарственный, ятрогенный СК).
Гиперкортицизм оказывает отрицательное воздействие на организм. ЭнСК развивается примерно в 10—15 случаях на
1 млн ежегодно, обычно поражает взрослых в возрасте 20— 50 лет. Об ЭнСК говорят при избыточной продукции кортизола в случае микроаденомы гипофиза (гипофизарный СК) или эктопированной злокачественной кортикотропиномы, локализующейся в бронхах, яичках, яичниках (эктопический СК). Реже ЭнСК возникает при первичном поражении коры надпочечников доброкачественной или злокачественной опухолью, или при ее гипертрофии (надпочечниковый СК). Гормонально-активная опухоль коры надпочечников называется кортикостеромой. Из-за поступления в кровь избыточного количества кортизола снижается продукция адрено-кортикотропного гормона (АКТГ), а оставшаяся ткань надпочечников подвергается атрофическим изменениям [1, 2].
Реже ЭнСК возникает при первичном поражении коры надпочечников доброкачественной или злокачественной опухолью, или при ее гипертрофии (надпочечниковый СК). Гормонально-активная опухоль коры надпочечников называется кортикостеромой. Из-за поступления в кровь избыточного количества кортизола снижается продукция адрено-кортикотропного гормона (АКТГ), а оставшаяся ткань надпочечников подвергается атрофическим изменениям [1, 2].
Наиболее распространенной причиной СК является длительный прием синтетических ГК, которые назначают ревматологи, аллергологи, эндокринологи и врачи другого профиля. Ревматологи используют преднизолон и его аналоги при системной красной волчанке (СКВ), ревматоидном артрите (РА), системных васкулитах и других аутоиммунных заболеваниях, при которых иммуноциты организма воздействуют на ткани и/или органы хозяина. При этом ГК используются для подавления иммунного ответа и уменьшения повреждения организма. В клинической практике СК наиболее часто наблюдается при лечении различных заболеваний и передозировке ГК. Знание причин и проявлений ЭкСК важно для ревматолога, нередко назначающего как повышенные дозы ГК, так и низкие на длительный срок. При воспалительных и аутоиммунных ревматических заболеваниях ГК обычно дают быстрый клинический эффект, но при этом отсутствует возможность быстрой отмены препарата. Это часто приводит к нежелательным реакциям (НР) и развитию ЭкСК. В проведенном в США крупном исследовании, посвященном лечению РА, выявлена ассоциация РА и ЭкСК при высоком относительном риске (ЯЯ=3,2) [3].
В МКБ-10 СК отведено место в IV классе болезней («Болезни эндокринной системы, расстройства питания, нарушения обмена веществ» — Е00-Е90) в блоке «Нарушения других эндокринных желез» — Е20-Е35 под кодом Е24 «Синдром Иценко — Кушинга». В блок входят: Е24.0 — «Болезнь Иценко — Кушинга гипофизарного происхождения»; Е24.1 — «Синдром Нельсона»; Е24.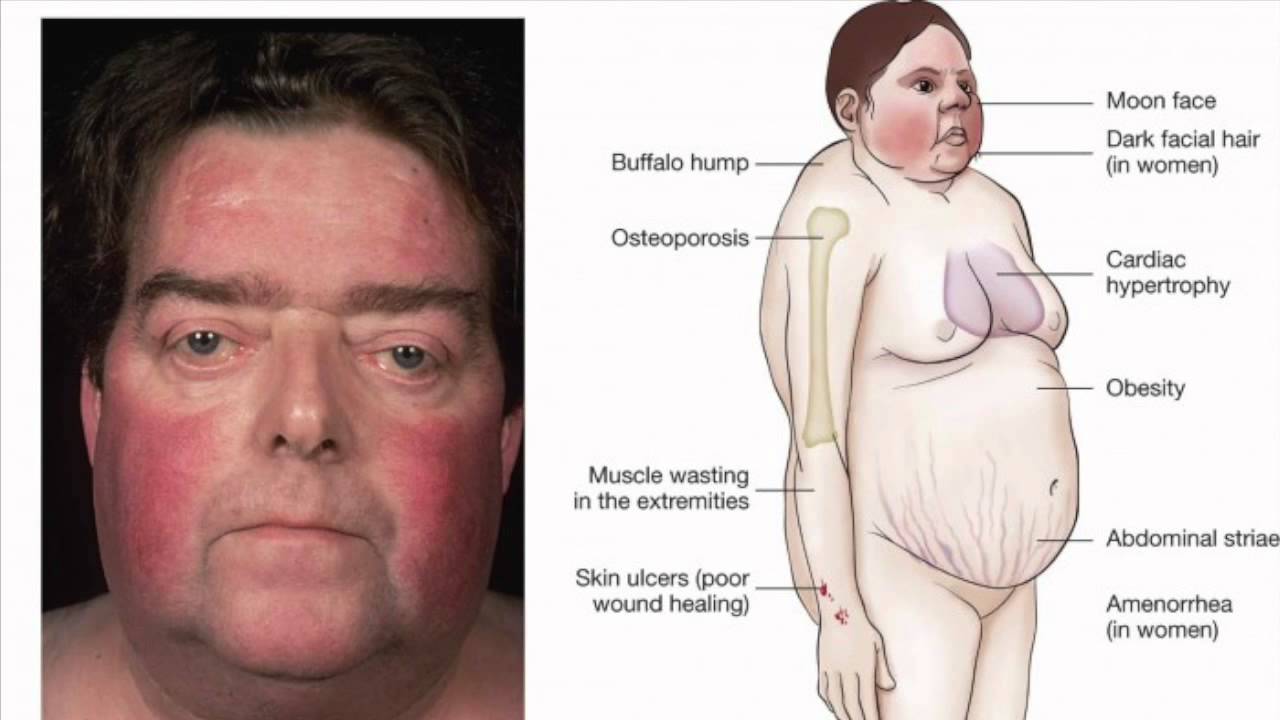 2 — «Медикаментозный синдром Иценко — Кушинга»; Е24.3 — «Эктопический АКТГ-синдром»; Е24.4 — «Кушингоидный синдром, вызванный алкоголем»; Е24.8 — «Другие состояния, характеризующиеся кушингоидным синдромом»; Е24.9 — «Синдром Иценко — Кушинга неуточненный» [2].
2 — «Медикаментозный синдром Иценко — Кушинга»; Е24.3 — «Эктопический АКТГ-синдром»; Е24.4 — «Кушингоидный синдром, вызванный алкоголем»; Е24.8 — «Другие состояния, характеризующиеся кушингоидным синдромом»; Е24.9 — «Синдром Иценко — Кушинга неуточненный» [2].
Настоящий обзор посвящен ЭкСК, связанному с использованием ГК и кодируемому в МКБ 10 как Е24.2 — «Медикаментозный синдром Иценко — Кушинга».
Применение ГК. ГК широко используются во всем мире. В США около 0,5% населения получает ГК по поводу различных хронических воспалительных и аутоиммунных заболеваний [4], ежегодно регистрируется примерно для 10 млн новых назначений ГК. Нередко пациенты не знают о том, что препараты, которые они принимают, содержат ГК [5]. Описаны случаи ЭкСК, развившегося вследствие при-
менения препаратов, в состав которых входили неупомянутые (скрытые) ГК [6]. Противовоспалительный эффект и иммунорегуляция делают ГК средством выбора при различных ревматических заболеваниях.
Клинические проявления СК часто усиливаются при применении высоких доз ГК [4]. Наблюдаются полнокровие, висцеральное ожирение, кровоподтеки от легкой травмы, истончение кожи, стрии, миопатия, депрессия или психоз, плохое заживление ран, учащение случаев инфицирования, глаукома и другие болезни глаз, артериальная гипертония (АГ). Осложнения: остеонекроз, остеопороз и спинальный эпидуральный липоматоз. Уровень андрогенов при ЭкСК возрастает нечасто, поэтому признаки вирилизации (гирсу-тизм и др.) развиваются редко [4].
НР и ЭкСК могут наблюдаться при приеме всех синтетических дериватов ГК: преднизона, преднизолона, метил-преднизолона, дексаметазона (ДМ), бетаметазона и триам-цинолона [4]. Остается неясным, какой из них имеет наибольший потенциал в отношении развития СК.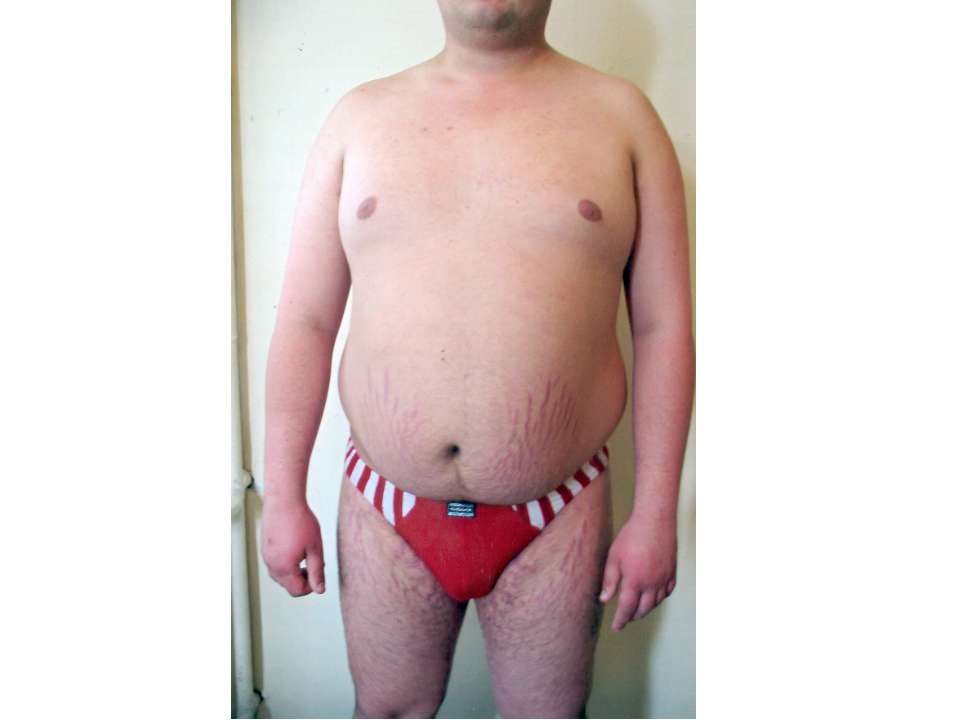 Это зависит от состава ГК, формы, фармакокинетики, афинности к рецепторам, биологических возможностей организма, продолжительности применения и разного уровня чувствительности у отдельных пациентов [4]. Прием ГК внутрь хорошо коррелирует с ЭкСК. Большинство врачей осознают эту опасность и, прежде чем назначить ГК, оценивают соотношение «польза — вред» у конкретного пациента [4]. Любая форма (локальная, аэрозольная, ингаляционная, инъекционная) введения этих препаратов может привести к НР (включая ЭкСК) [4, 7—11].
Это зависит от состава ГК, формы, фармакокинетики, афинности к рецепторам, биологических возможностей организма, продолжительности применения и разного уровня чувствительности у отдельных пациентов [4]. Прием ГК внутрь хорошо коррелирует с ЭкСК. Большинство врачей осознают эту опасность и, прежде чем назначить ГК, оценивают соотношение «польза — вред» у конкретного пациента [4]. Любая форма (локальная, аэрозольная, ингаляционная, инъекционная) введения этих препаратов может привести к НР (включая ЭкСК) [4, 7—11].
Доза ГК, необходимая для контроля заболевания, является важнейшим фактором, определяющим развитие ЭкСК и других НР. СК обусловлен приемом (даже краткосрочным) высоких доз ГК или длительным использованием их низких доз (даже с коротким периодом полувыведения — гидрокортизон и кортизон) [4].
Состояния, связанные с ЭкСК (индуцированным ГК):
АГ — характерна для больных с ЭкСК и дозозависимо развивается примерно в 20% случаев [4, 12, 13]. Наиболее доказательна теория дисбаланса между вазоконстрикцией и вазодилатацией и усиления вазоконстрикции, приводящей к АГ [12, 13]. Основные звенья патогенеза АГ, связанной с ГК, показаны на рис. 1. Результатом представленных изменений являются нарушения гемодинамики в различных отделах сосудистого русла.
Использование ДМ в дозе 0,5 мг/кг в сутки внутрь у собак сопровождалось уменьшением сердечного выброса и увеличением общего сопротивления периферических сосудов [17], при исследованиях у людей ДМ (3 мг/сут в течение 7 дней) повышал центральное и общее сопротивление периферических сосудов, не изменяя сердечного выброса [18]. Ограниченные исследования подтверждают влияние ДМ на региональную гемодинамику: 24-часовая инфузия
(125 мг/кг в час) повышала среднее давление крови и снижала кровоток в почках и брыжейке и их проходимость [24].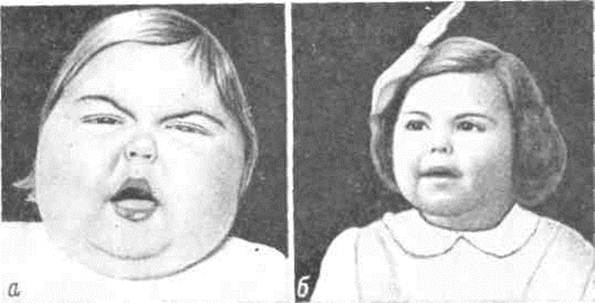
Метаболические нарушения способствуют развитию и ухудшению течения АГ, индуцированной ГК. Ожирение связано со снижением экскреции натрия, увеличением объема плазмы и внеклеточной жидкости и усугублением АГ [12, 13]. Инсулинорезистентность (ИР) приводит к задержке натрия и воды, повышает активность симпатико-адрена-ловой системы, активирует локально систему ренин — анги-
ОБЗОРЫ
I. Увеличение симпатической активности: повышенный синтез катехоламинов, экспрессия 1@-адренергических рецепторов [12, 13]
II. Повышенный синтез эндотелина I[14]
III. Катализ продукции адреналина, изменение чувствительности а1-адренергических рецепторов
в гладкой мускулатуре сосудов [15—17]
IV. Повышенный синтез вазоактивных веществ
и их рецепторов (нейропептид У, аргинин — вазопрессин, предсердный натрийуретический пептид) [13]
V. Активация системы ренин — ангиотензин: влияние ГК на печень — повышение синтеза ангиотензиногена, SQ14225[12, 13, 17]
VI. Изменение чувствительности тканей (снижение порога и макс. ответа на норадреналин в сосудах брыжейки крыс, получавших ДМ) [17, 18]
VII. Недостаток N0 вследствие подавления его синтеза (снижение экспрессии и активности синтеза N0, доступности тетрагидробиоптерина и предшественник N0 Ь-аргинина). Избыток супероксида (пероксинитрит) инактивирует N0 [19, 20]
VIII. Снижение продукции вазодилататоров: простациклина, простагландина Е2, калликреина [21—23]
Рис. 1. ГК и АГ
1. ГК и АГ
отензин, сосудистую гипертрофию, повышает сосудистое сопротивление и приводит к АГ [12, 13].
ГК регулируют кровяное давление, влияя на ЦНС. При подкожном введении крысам меченного тритием ДМ изотопы были выявлены в таламусе (боковое ядро), гипоталамусе (переднемедиальное, перивентрикуляр-ное, паравентрикулярное, дугообразное ядра), клетках голубоватого пятна, самого заднего поля и ядре одиночного пучка. При системном назначении ДМ проникает в мозг и цереброспинальную жидкость [25].
Остеопороз (ОП) — важный компонент ЭкСК [4]. Потеря кости наиболее быстрая в первые 6 мес лечения, затем замедляется, развиваются остеопения и ОП. Трабекулярная кость и корковый слой тел позвонков более чувствительны к воздействию ГК и после их отмены быстро восстанавливаются. Переломы происходят у 30—50% больных, леченных ГК, независимо от минеральной плотности костной ткани [26] и отличаются по локализации: например, при бронхиальной астме длительный прием ГК ассоциируется с частыми переломами ребер и позвоночника [27]. Ретроспективное когортное исследование 244 235 больных РА, принимающих ГК внутрь, показало дозозависимое увеличение частоты переломов шейки бедра, предплечья и позвонков (даже при низких дозах —
2,5 мг/сут) [28]. Прямую связь при приеме ГК между потерей костной ткани и реальным риском переломов трудно оценить из-за многофакторного происхождения изменений костного метаболизма. ГК замедляют метаболизм кальция и ремоделирование кости, снижая костеобразование и повышая резорбцию кости (рис. 2), уменьшают всасывание кальция в кишечнике и его реабсорбцию в почках. Это приводит к гиперкальциурии, вторичному гиперпа-ратиреозу и повышенной резорбции кости [26].
ГК тормозят остеобластогенез, снижая синтез коллагена 1 типа и инсулиноподобного фактора роста, изменяя анаболический эффект трансформирующего фактора роста в (ТФР|3), ингибируя Wnt-передачу и индуцируя апоптоз остеобластов и остеоцитов [26]. Циркуляция провоспалитель-ных цитокинов снижает активность 11|3-гидроксистероид-дегидрогеназы 1 типа и повышает активность 11|3-гидро-ксистероиддегидрогеназы 2 типа, оказывает противоположный ГК эффект на паратгормон и тестостерон и является основным механизмом патогенеза повышенной резорбции кости. Другой ее механизм — стимуляция пролиферации остеокластов через подавление синтеза остеопротегерина, продукция активатора рецептора ядерного фактора кВ и снижение продукции эстрогена и андрогенов [26, 28, 29].
Циркуляция провоспалитель-ных цитокинов снижает активность 11|3-гидроксистероид-дегидрогеназы 1 типа и повышает активность 11|3-гидро-ксистероиддегидрогеназы 2 типа, оказывает противоположный ГК эффект на паратгормон и тестостерон и является основным механизмом патогенеза повышенной резорбции кости. Другой ее механизм — стимуляция пролиферации остеокластов через подавление синтеза остеопротегерина, продукция активатора рецептора ядерного фактора кВ и снижение продукции эстрогена и андрогенов [26, 28, 29].
Нарушения системы коагуляции/фибринолиза — тромбоэмболия является серьезным осложнением у больных с СК
и ассоциируется с повышенной заболеваемостью и смертностью [4, 30]. Клинические исследования больных с СК показали активацию системы коагуляции (более высокие плазменные уровни фактора Виллебранда, факторов VIII, IX и XII), сниженную фибринолитическую активность (более низкие уровни РАН, tPA, или время лизиса сгустка эуг-лобина) и повышенные уровни факторов VIII, IX, XII и XI плазминогена и а2-антиплазмина [31]. Эти эффекты связаны с ГК и полностью исчезают после хирургического лечения (при ЭнСК). ГК вызывают нарушения фибринолитиче-ской системы и коагуляции: повышение синтеза/секреции РАН, уровня комплекса тромбин — антитромбин и плазменных факторов VII, VIII, XI и фибриногена [32].
Скелетно-мышечные расстройства (миопатия) — характерны для СК и проявляются такими НР, как неспособность подняться с корточек из-за слабости проксимальных мышц ног и плечевого пояса [4, 33]. ГК влияют на мышечные волокна быстрого сокращения (тип 2В — фазические), вызывая атрофию (но не некроз) — следствие сниженного мышечного протеинового синтеза. Это опосредуется через повышенное окислительное фосфорилирование, ингиби-цию синтеза протеинов и нарушение возбудимости мышечной мембраны. Острая форма миопатии с проксимальной и дистальной мышечной слабостью коррелирует с повышен-
ОБЗОРЫ
Рис. 2. СК, индуцированный ГК, и ОП
2. СК, индуцированный ГК, и ОП
ным уровнем сывороточной КФК и является индикатором фокального или диффузного мышечного некроза, опосредуется гипокалиемией и рассматривается как результат прямого влияния ГК на скелетную мышцу. Она может сохраняться от 6 нед до нескольких месяцев даже после прекращения терапии ГК. Хроническая форма проявляется уже в начале использования ГК: первично вовлекаются проксимальные мышцы (уровень КФК нормальный или слегка повышенный), при этом не выявляются признаки фокального или диффузного мышечного некроза. Прямой корреляции миопатии с дозой ГК нет — миопатия может развиться у больных, которые получали всего 10 мг/сут преднизона [34].
Метаболический синдром — сниженная толерантность к глюкозе, сахарный диабет, дислипидемия и жировая дистрофия печени являются характерными НР при лечении ГК [35]. Экспериментальные и клинические данные подтверждают теорию влияния ГК на различные стороны белкового, липидного и углеводного обмена, включая скелетную мускулатуру, печень и жировую ткань. ГК индуцируют ИР, непосредственно воздействуя на инсулиновый сигнальный каскад. В биоптатах скелетной мышцы у здоровых добровольцев после
приема ДМ в дозе 4 мг/сут и у больных после трансплантации почки, получавших высокие дозы ГК, обнаружено снижение активности гликогенсинта-зы [36, 37]. ГК индуцируют катаболизм белка, способствуя атрофии, уменьшению мышечной массы и повышению катаболизма аминокислот [38], которые негативно влияют на сигнальный инсулин [39], накопление глюкозы и синтез гликогена в мышце [40].
ГК индуцируют процесс липолиза в организме [40] и ИР печени, приводя к повышению уровня свободных жирных кислот и триглицеридов в плазме [41] и печени с НР инсулиновой чувствительности в мышцах и нарушениями углеводного обмена, повреждая инсулиновый сигнал непосредственно и опосредованно [42]. После кратковременного использования ГК у здоровых выявлено повышение уровня эндогенной глюкозы [43, 44]. ГК повышают содержание жира и изменяют его распределение посредством регуляции ГК-чувствительной липазы и активности липопротеиновой липазы [45], модулируют биологию жировой ткани, изменяя секрецию адипокиназ через ИР либо непосредственно [46].
После кратковременного использования ГК у здоровых выявлено повышение уровня эндогенной глюкозы [43, 44]. ГК повышают содержание жира и изменяют его распределение посредством регуляции ГК-чувствительной липазы и активности липопротеиновой липазы [45], модулируют биологию жировой ткани, изменяя секрецию адипокиназ через ИР либо непосредственно [46].
Также ГК могут тормозить функцию в-клеток поджелудочной железы, которая зависит от длительности использования этих препаратов, их дозы, восприимчивости к ним пациента. ИР, индуцированная ГК, нарушение метаболизма глюкозы, ожирение и висцеральное ожирение — компоненты метаболического синдрома, ассоциирующегося с повышенной заболеваемостью и смертностью от сердечно-сосудистых заболеваний.
Сердечно-сосудистые заболевания — у пациентов с доказанным ЭкСК отмечается повышение частоты сердечно-сосудистых заболеваний и смертности от них [4, 47—49]. О повышенной смертности вследствие сердечно-сосудистых заболеваний сообщалось у больных с воспалительным артритом, гигантоклеточным артериитом, бронхиальной астмой, хронической обструктивной болезнью легких [50, 51]. Популяционное исследование показало, что пациенты, принимавшие системно ГК (>7,5 мг/сут преднизолона), имели более высокую частоту сердечно-сосудистых заболеваний (инфаркт миокарда, остановка сердца и цереброваскулярная болезнь) в течение 1—5 лет наблюдения [49]. Ассоциация не была очевидной у пациентов, принимавших или низкие дозы ГК, или ГК «несистемно» (т.е. локально и ректально). Прослеживается прямая причинно-следственная связь между приемом ГК и развитием сердечно-сосудистых заболеваний. При этом имеют значение доза, кумулятивная доза, продолжительность приема и путь введения. Сегодня нет ответа на вопросы: 1) опосредуется ли развитие сердечно-сосудистой патологии предрасположенностью
ОБЗОРЫ
Клинические признаки ЭкСК и ЭнСК
Клинические признаки
Выраженность или зависимость признака ЭкСК ЭнСК
Гирсутизм
Степень выраженности АГ Асептический некроз Спинальный эпидуральный липоматоз Связанные с фармакокинетикой ГК
Афинность к ГК-рецепторам
±
+
++
++ Связывание с альбумином +++
++
+++
±
±
Связывание с кортизол-зависимым глобулином
Развитие АГ при сверхфизиологических дозах ГК или кортизола ДМ: у человека — Кортизол 80 и 200 мг:
1-2 дня; у человека — 24 ч
у крыс и собак — 1-2 дня
Минералокортикоидная зависимость Задержка натрия в организме Избыток натрия
Повышение супероксидной продукции
АГ вследствие низкой биоактивности N0
Снижение АД в ответ на лечение аргинином
Снижение АД в ответ на лечение аспирином (антиоксидант)
Снижение АД в ответ на лечение антагонистом рецептора вазопрессина V!
Не зависит Не зависит Не усугубляет АГ
+
+
Не зависит Не зависит Может усугублять АГ
+
+
+
+
Предупреждение АГ дегидроандростероном
+
+
+
Примечание. (+) — выраженный признак, (±) — слабовыраженный признак, (—) — отсутствие признака.
(+) — выраженный признак, (±) — слабовыраженный признак, (—) — отсутствие признака.
больного и индукцией нескольких факторов риска и 2) что преобладает, прямое негативное влияние ГК на сердечнососудистую систему или их позитивный противовоспалительный и антипролиферативный эффект [52, 53]?
ЭкСК и фетальное программирование
Нередко женщины, страдающие СКВ и РА и длительно принимающие ГК, беременеют и рожают детей. Какое влияние могут оказывать ГК на возникновение заболеваний в будущем, а не только на развитие плода? Большой интерес в последние 5 лет вызывает использование ГК при планировании беременности [4, 53]. Ключевую роль здесь играют ГК-рецепторы, ось гипоталамус — гипофиз — надпочечники и экспрессия гена 11|3-гидроксистероидной дегидрогеназы 2 типа. Назначение ГК беременным для обеспечения развития органов плода и предотвращения угрозы жизни матери и плода, уменьшения эффектов врожденной гиперплазии надпочечников и предупреждения преждевременных родов связано как с текущим преимуществом, так и с потенциально долгосрочными НР [54, 55]. Ряд доказательств, полученных при экспериментальных и клинических исследованиях, поддерживают теорию дозозависимого влияния ГК на развитие плода и болезни, возникающие в последующем у взрослых [56]. АГ у взрослого проявляется вследствие влияния ГК на созревание тканей плода, контролирующих кровяное давление (число клу-
бочков, размер почек, экспрессия рецепторов катехоламина и вторая сигнальная система в почечной и сосудистой ткани, связанные с факторами роста и углеводным и жировым гомеостазом). Кроме того, ГК потенцируют вазокон-стрикторное влияние на сосудистую сеть и регулируют синтез катехоламинов, оксида азота (N0) и ангиотензино-гена [57, 58]. АГ сопряжена с тканеспецифическим повышением экспрессии ГК-рецепторов и снижением регуляции активности 11|3-гидроксистероидной дегидрогеназы
2 типа в плаценте, почках и надпочечниках, повышая чувствительность и избыточное влияние ГК на органы.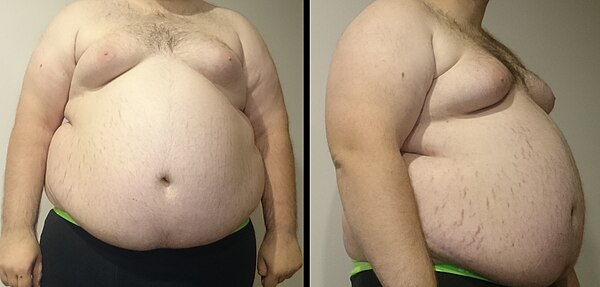 ГК также вовлекаются в эмбриональное программирование сахарного диабета 2-го типа, сердечно-сосудистой патологии, других проявлений метаболического синдрома, некоторых функций ЦНС и психических синдромов. Однако полностью основные механизмы этого влияния еще не объяснены и нуждаются в дальнейшем изучении.
ГК также вовлекаются в эмбриональное программирование сахарного диабета 2-го типа, сердечно-сосудистой патологии, других проявлений метаболического синдрома, некоторых функций ЦНС и психических синдромов. Однако полностью основные механизмы этого влияния еще не объяснены и нуждаются в дальнейшем изучении.
ЭкСК (сравнение с ЭнСК) и АГ
Хотя клинические проявления ЭкСК и ЭнСК не имеют существенных различий, наблюдается ряд особенностей при использовании больших доз ГК [4]. Основные клинические признаки этих видов СК, их сходство и различия представлены в таблице. По-видимому, при ЭкСК и ЭнСК в развитие АГ вовлекаются разные механизмы патогенеза или одни и те же, но вклад их неодинаков.
ОБЗОРЫ
Лечение
У пациентов с ревматическими заболеваниями, длительно использующих ГК, могут развиться АГ и другая патология, связанная с ЭкСК. В этих случаях идеально было бы отказаться от ГК еще до появления НР, но чаще всего это нельзя сделать из-за возможности обострения заболевания, поэтому ГК отменяют постепенно. Прием ГК в низких дозах снижает метаболические эффекты и помогает профилактике НР. К лечению каждого пациента необходимо подходить с осторожностью, индивидуально: назначать ГК с повышенной противовоспалительной и меньшей минерало-кортикоидной активностью (преднизолон), в формах, позволяющих доставлять ГК к месту воспаления (внутрисус-тавно, внутримышечно, ректально, наружно, глазные капли), оптимизировать режим дозирования (достаточная, но минимальная доза) и время приема ГК [59].
Для оптимизации лечения ГК и уменьшения НР разрабатываются новые формы этих препаратов, например, комбинированный препарат преднизон/дипиридамол, инновационные формы в виде лиганд ГК-рецепторов, экспериментальный селективный агонист ГК-рецепторов (8ЕвЯА) с выраженными противовоспалительными и иммуносупрессивными свойствами и низкой вероятностью НР (атрофия кожи) [59]. Появилась новая хроноте-рапевтическая форма преднизона, высвобождаемого после приема внутрь через 4 ч благодаря поздней пенетрации. Использование этой формы сопровождается меньшим числом НР, она одобрена в 16 странах Европы, Австралии, Израиле и США [59].
Появилась новая хроноте-рапевтическая форма преднизона, высвобождаемого после приема внутрь через 4 ч благодаря поздней пенетрации. Использование этой формы сопровождается меньшим числом НР, она одобрена в 16 странах Европы, Австралии, Израиле и США [59].
В большинстве случаев пациенты нуждаются в лечении НР, связанных с ГК. Для терапии АГ рекомендуется эплеренон (относительно селективный препарат, блокирующий рекомбинантные минералокортикоиды, прогес-тероновые и андрогенные рецепторы), антагонисты рецепторов ангиотензина, ингибиторы ангиотензинпревра-
щающего фермента (АПФ). Приветствуется изменение образа жизни (снижение массы тела) [60].
У пациентов с ИР используют бигуаниды и активаторы пероксисомных пролифераторов ядерных рецепторов. Лечение апноэ сна с помощью длительного поддержания положительного давления в воздухоносных путях эффективно при одышке, АГ, ИР и повышенном риске сердечно-сосудистых заболеваний [60]. Бисфосфонаты (средства первой линии) или терипаратид (препарат второй линии) в сочетании с кальцием и витамином Б должны назначаться большинству пациентов.
Пациентам, длительно получающим ГК, у которых развивается мышечная слабость, рекомендуется биопсия мышцы. Для лечения ГК-миопатии предлагают использовать фе-нитоин (миорелаксант, антиаритмический и противосудо-рожный препарат), но это нуждается в дальнейшем изучении. В настоящее время терапия СК строится на тех же принципах, что и лечение тромботических нарушений. Необходимы дальнейшие исследования типа, интенсивности и длительности профилактики тромбозов у пациентов с ЭкСК и ЭнСК [60].
Заключение
ЭкСК, вызванный приемом ГК, является серьезной медицинской проблемой. Оценка состояния больного затруднена из-за несовершенства трактовки симптомов СК. План лечения ГК, их формы, пути введения, дозу и длительность использования нужно определять для каждого больного индивидуально еще до начала терапии, а эффективность и переносимость терапии необходимо оценивать при каждом посещении врача. Обязательно лечение выраженных НР, индуцированных ГК. Стратегия ведения больного должна охватывать не только предупреждение НР, но и изменение образа жизни. Усилия ученых должны быть направлены на создание ГК с выраженным противовоспалительным действием и незначительными метаболическими эффектами.
План лечения ГК, их формы, пути введения, дозу и длительность использования нужно определять для каждого больного индивидуально еще до начала терапии, а эффективность и переносимость терапии необходимо оценивать при каждом посещении врача. Обязательно лечение выраженных НР, индуцированных ГК. Стратегия ведения больного должна охватывать не только предупреждение НР, но и изменение образа жизни. Усилия ученых должны быть направлены на создание ГК с выраженным противовоспалительным действием и незначительными метаболическими эффектами.
ЛИТЕРАТУРА
1. Newell-Price J, Bertagna X, Grossman A, Nieman L. Cushing’s syndrome. Lancet.
2006;367(9522):1605—17. DOI:
http://dx.doi.org/10.1016%2FS0140-
6736%2806%2968699-6.
2. Международная классификация болезней МКБ-10. Электронная версия. Класс: Болезни эндокринной системы, расстройства питания и нарушения обмена веществ. Доступ по ссылке: http://www.mkb10.ru/ [Mezhdunarodnaya klassi-fikatsiya bolezney MKB-10. Elektronnaya versiya. Klass: Bolezni endokrinnoy sistemy, rasstroystva pitaniya i narusheniya obmena veshchestv. Available from: http://www.mkb10.ru/]
3. Pivonello R, de Martino MC, de Leo M et al. Cushing’s syndrome. Endocrinol Metab Clin North Am. 2008;37(1):135—49. ix. DOI: http://dx.doi.org/10.1016%2Fj.ecl.2007.10.010.
4. Chrousos GP. Glucocorticoid therapy. In: Felig P, Frohman L, editors. Endocrinology and Metabolism. 4th ed. New York: McGraw-Hill Incorporated; 2001. pp. 609—632.
5. Andersen FA, Bergfeld WF, Belsito DV et al.
Final amended safety assessment of hydroquinone as used in cosmetics. Int J Toxicol. 2010;29 Suppl 4:274S—87. DOI:
Int J Toxicol. 2010;29 Suppl 4:274S—87. DOI:
http://dx.doi.org/10.1177%2F1091581810385957.
6. Azizi F, Jahed A, Hedayati M et al. Outbreak of exogenous Cushing’s syndrome due to unlicensed
medications. Clin Endocrinol (Oxf).
2008;69(6):921—5. DOI: 10.1111/j.1365-2265.2008.03290.x. Epub 2008 May 6.
7. Ermis B, Ors R, Tastekin A, Ozkan B. Cushing’s syndrome secondary to topical corticosteroids abuse. Clin Endocrinol (Oxf). 2003;58(6):795—6.
8. Lipworth BJ. Systemic adverse effects of inhaled corticosteroid therapy: a systematic review and meta-analysis. Arch Intern Med.
1999;159(9):941—955. DOI: http://dx.doi.org/10.1001%2Farchinte.159.9.941.
9. Perry RJ, Findlay CA, Donaldson MD. Cushing’s syndrome, growth impairment, and occult adrenal suppression associated with intranasal steroids. Arch Dis Child. 2002;87(1):45—8. DOI: http://dx.doi.org/10.1136%2Fadc.87.1.45.
10. Kumar S, Singh RJ, Reed AM, Lteif AN. Cushing’s syndrome after intra-articular and intra-dermal administration of triamcinolone acetonide in three pediatric patients. Pediatrics.
2004;113(6):1820—4. DOI: http://dx.doi.org/10.1542%2Fpeds.113.6.1820.
11. Lansang MC, Farmer T, Kennedy L. Diagnosing the unrecognized systemic absorption of intra-artic-ular and epidural steroid injections. Endocr Pract. 2009;15(3):225—8. DOI: http://dx.doi.org/10.4158%2FEP.15.3.225.
12. Saruta T, Suzuki H, Handa M et al. Multiple factors contribute to the pathogenesis of hyperten-
Multiple factors contribute to the pathogenesis of hyperten-
sion in Cushing’s syndrome. J Clin Endocrinol Metab. 1986;62(2):275—9. DOI: http://dx.doi.org/10.1210%2Fjcem-62-2-275.
13. Magiakou MA, Smyrnaki P, Chrousos GP Hypertension in Cushing’s syndrome. Best Pract Res Clin Endocrinol Metab. 2006;20(3):467—82. DOI: http://dx.doi.org/10.1016%2Fj.beem.2006. 07.006.
14. Kirilov G, Tomova A, Dakovska L et al. Elevated plasma endothelin as an additional cardiovascular risk factor in patients with Cushing’s syndrome. Eur J Endocrinol. 2003;149(6):549—53. DOI: http://dx.doi.org/10.1530%2Feje.0.1490549.
15. Sakaue M, Hoffman BB. Glucocorticoids induce transcription and expression of the alpha 1B adrenergic receptor gene in DTT1 MF-2 smooth muscle cells. J Clin Invest. 1991;88(2):385-9. DOI: http://dx.doi.org/10.1172%2FJCI115315.
16. Haigh RM, Jones CT. Effect of glucocorticoids on alpha 1-adrenergic receptor binding in rat vascular smooth muscle. J Mol Endocrinol.
1990;5(1):41—8.
17. Nakamoto H, Suzuki H, Kageyama Y et al. Characterization of alterations of hemodynamics and neuroendocrine hormones in dexamethasone induced hypertension in dogs. Clin Exp Hypertens A. 1991;13(4):587—606. DOI: http://dx.doi.org/10.3109%2F10641969109045071.
18. Pirpiris M, Sudhir K, Yeung S et al. Pressor
ОБЗОРЫ
responsiveness in corticosteroid-induced hypertension in humans. Hypertension. 1992;19(6 Pt 1):567—74. DOI:
http://dx.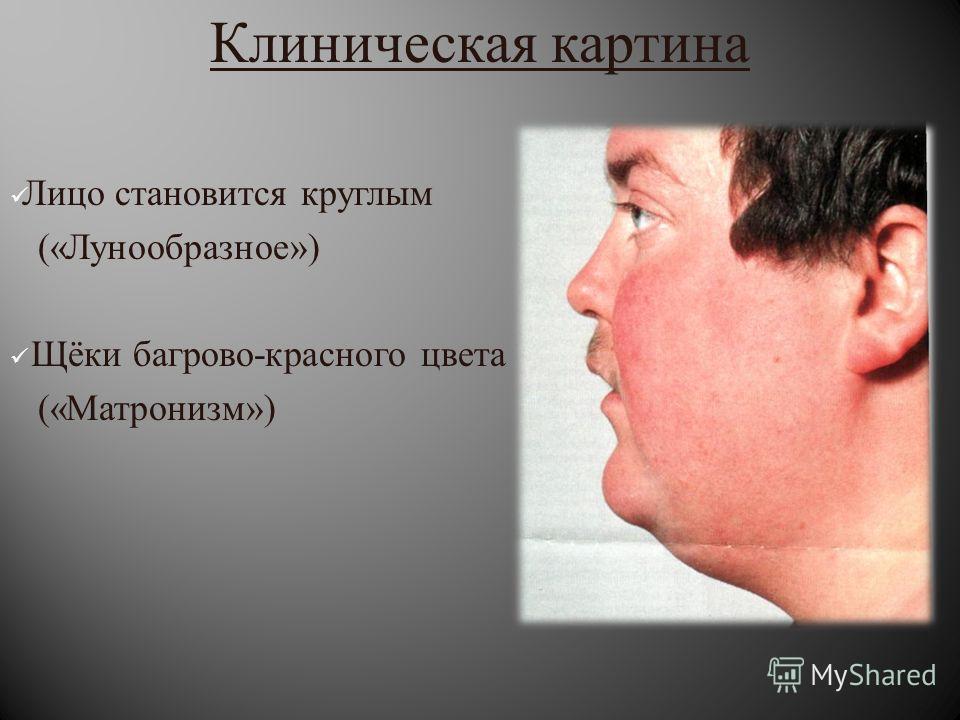 doi.org/10.1161%2F01.HYP.19.6.567.
doi.org/10.1161%2F01.HYP.19.6.567.
19. Pacher P, Beckman JS, Liaudet L. Nitric oxide and peroxynitrite in health and disease. Physiol Rev. 2007;87(1):315—424. DOI: http://dx.doi.org/10.1152%2Fphysrev.00029.2006.
20. Iuchi T, Akaike M, Mitsui T et al. Glucocorticoid excess induces superoxide production in vascular endothelial cells and elicits vascular endothelial dysfunction. Circ Res. 2003;92(1):81—7. DOI:
http://dx.doi.org/10.1161%2F01.RES.0000050588.
35034.3C.
21. Zhang Y, Hu L, Mori TA, Barden A et al. Arachidonic acid metabolism in glucocorticoid-induced hypertension. Clin Exp Pharmacol Physiol. 2008;35(5—6):557—62. DOI: http://dx.doi.org/10.1111%2Fj.1440-1681.2007.04839.x.
22. Falardeau P, Martineau A. Prostaglandin I2 and glucocorticoid-induced rise in arterial pressure in the rat. J Hypertens. 1989;7(8):625—32.
23. Nasjletti A, Erman A, Cagen LM, Baer PG. Plasma concentrations, renal excretion, and tissue release of prostaglandins in the rat with dexametha-sone-induced hypertension. Endocrinology. 1984;114(3):1033—40. DOI: http://dx.doi.org/10.1210%2Fendo-114-3-1033.
24. Gardiner SM, Kemp PA, March JE, Bennett T Effects of dexamethasone and SB 209670 on the regional haemodynamic responses to lipopolysac-charide in conscious rats. Br J Pharmacol. 1996;118(1):141—9. DOI: http://dx.doi.org/10.1111%2Fj.1476-5381.1996.tb15377.x.
25. Wang LL, Ou CC, Chan JY. Receptor-independent activation of GABA ergic neurotransmission and receptor-dependent nontranscriptional activation of phosphatidylinositol 3-kinase/protein kinase Akt pathway in short-term cardiovascular actions of dexamethasone at the nucleus tractus solitarii of the rat. Mol Pharmacol.
Mol Pharmacol.
2005;67(2):489—98.
26. Shaker JL, Lukert BP Osteoporosis associated with excess glucocorticoids. Endocrinol Metab Clin North Am. 2005;34(2):341—56. VIII-IX. DOI: http://dx.doi.org/10.1016%2Fj.ecl.2005.01.014.
27. Adinoff AD, Hollister JR. Steroid-induced fractures and bone loss in patients with asthma. N Engl J Med. 1983;309(5):265—8. DOI: http://dx.doi.org/10.1056%2FNEJM198308043090 502.
28. Van Staa TP, Leufkens HG, Abenhaim L et al. Use of oral corticosteroids and risk of fractures. J Bone Miner Res. 2000;15(6):993—1000. DOI: http://dx.doi.org/10.1359%2Fjbmr.2000.
15.6.993.
29. Cooper MS, Rabbitt EH, Goddard PE et al. Osteoblastic 11beta-hydroxysteroid dehydrogenase type 1 activity increases with age and glucocorticoid exposure. J Bone Miner Res. 2002;17(6):979—86. DOI: http://dx.doi.org/10.1359%2Fjbmr.2002. 17.6.979.
30. La Brocca A, Terzolo M, Pia A et al. Recurrent thromboembolism as a hallmark of Cushing’s syndrome. J Endocrinol Invest. 1997;20(4):211—4.
31. Erem C, Nuhoglu I, Yilmaz M et al. Blood coagulation and fibrinolysis in patients with Cushing’s syndrome: increased plasminogen activator inhibitor-1, decreased tissue factor pathway inhibitor, and unchanged thrombin-activatable fibrinolysis inhibitor levels. J Endocrinol Invest.
2009;32(2):169—74.
32. Brotman DJ, Girod JP, Posch A et al. Effects of short-term glucocorticoids on hemostatic factors in healthy volunteers. Thromb Res.
2006;118(2):247—52. DOI:
DOI:
http://dx.doi.org/10.1016%2Fj.throm-
res.2005.06.006.
33. Hasselgren PO. Glucocorticooids and muscle catabolism. Curr Opin Clin Nutr Metab Care. 1999;2(3):201—5. DOI: http://dx.doi.org/10.1097%2F00075197-199905000-00002.
34. Van Marle W, Woods KL. Acute hydrocortisone myopathy. Br Med J. 1980;281(6235):271-72. DOI: http://dx.doi.org/10.1136%2Fbmj.281.
6235.271-a.
35. Larsson H, Ahren B. Insulin resistant subjects lack islet adaptation to short-term dexamethasone-induced reduction in insulin sensitivity.
Diabetologia. 1999;42(8):936-43. DOI: http://dx.doi.org/10.1007%2Fs001250051251.
36. Henriksen JE, Alford F, Vaag A et al. Intracellular skeletal muscle glucose metabolism is differentially altered by dexamethasone treatment of normoglycemic relatives of type 2 diabetic patients. Metabolism. 1999;48(9):1128-35. DOI: http://dx.doi.org/10.1016%2FS0026-0495%2899%2990126-9.
37. Ekstrand A, Schalin-Ja ntti C, Lo fman M et al. The effect of (steroid) immunosuppression on skeletal muscle glycogen metabolism in patients after kidney transplantation. Transplantation.
1996;61(6):889—93. DOI:
http://dx.doi.org/10.1097%2F00007890-
199603270-00008.
38. Schakman O, Gilson H, Thissen JP.
Mechanisms of glucocorticoid-induced myopathy. J Endocrinol. 2008;197(1):1—10. DOI: http://dx.doi.org/10.1677%2FJOE-
2008;197(1):1—10. DOI: http://dx.doi.org/10.1677%2FJOE-
07-0606.
39. Krebs M, Krssak M, Bernroider E et al. Mechanism of amino acid-induced skeletal muscle insulin resistance in humans. Diabetes. 2002;51(3):599—605. DOI: http://dx.doi.org/10.2337%2Fdiabetes.51.3.599.
40. Dinneen S, Alzaid A, Miles J, Rizza R. Effects of the normal nocturnal rise in cortisol on carbohydrate and fat metabolism in IDDM. Am J Physiol. 1995;268(4 Pt 1):E595-603.
41. Wajchenberg BL. Subcutaneous and visceral adipose tissue: their relation to the metabolic syndrome. Endocr Rev. 2000;21(6):697—738. DOI: http://dx.doi.org/10.1210%2Fer.2L6.697.
42. Parekh S, Anania FA. Abnormal lipid and glucose metabolism in obesity: implications for nonalcoholic fatty liver disease. Gastroenterology. 2007;132(6):2191—207. DOI: http://dx.doi.org/10.1053%2Fj.gastro.2007.03.055.
43. Nielsen MF, Caumo A, Chandramouli V et al. Impaired basal glucose effectiveness but unaltered fasting glucose release and gluconeogenesis during short-term hypercortisolemia in healthy subjects. Am J Physiol Endocrinol Metab. 2004;286(1):E102—10. DOI: http://dx.doi.org/10.1152%2Fajpendo.00566.2002.
44. Rooney DP, Neely RD, Cullen C et al.
The effect of cortisol on glucose/glucose-6-phos-phate cycle activity and insulin action.
J Clin Endocrinol Metab. 1993;77(5):1180-3. DOI: http://dx.doi.org/10.1210%2Fjc.77.5.1180.
45. Morton NM, Seckl JR. 11beta-hydroxysteroid dehydrogenase type 1 and obesity. Front Horm Res. 2008;36:146-64. DOI: 10.1159/0000115363.
2008;36:146-64. DOI: 10.1159/0000115363.
46. Fasshauer M, Paschke R. Regulation of
adipocytokines and insulin resistance. Diabetologia. 2003;46(12):1594-603. DOI: http://dx.doi.org/10.1007%2Fs00125-003-1228-z.
47. Mancini T, Kola B, Mantero F et al. High cardiovascular risk in patients with Cushing’s syndrome according to 1999 WHO/ISH guidelines. Clin Endocrinol (Oxf). 2004;61(6):768-77. DOI: http://dx.doi.org/10.1111%2Fj.1365-2265.2004.02168.x.
48. Wei L, MacDonald TM, Walker BR. Taking glucocorticoids by prescription is associated with subsequent cardiovascular disease. Ann Intern Med. 2004;141(10):764-70. DOI: http://dx.doi.org/10.7326%2F0003-4819-141-10-200411160-00007.
49. Souverein PC, Berard A, Van Staa TP
et al. Use of oral glucocorticoids and risk of cardiovascular and cerebrovascular disease in a population based case-control study. Heart. 2004;90(8):859-65. DOI: http://dx.doi.org/10.1136%2Fhrt.2003.020180.
50. DeMaria AN. Relative risk of cardiovascular events in patients with rheumatoid arthritis. Am J Cardiol. 2002;89(6A):33D-8D. DOI: http://dx.doi.org/10.1016%2FS0002-9149%2802%2902235-X.
51. Uddhammar A, Eriksson AL, Nystrom L et al. Increased mortality due to cardiovascular disease in patients with giant cell arteritis in northern Sweden. J Rheumatol. 2002;29(4):737-42.
52. Nashel DJ. Is atherosclerosis a complication of long-term corticosteroid treatment? Am J Med. 1986;80(5):925-29. DOI: http://dx.doi.org/10.1016%2F0002-9343%2886%2990639-X.
53. Maxwell SR, Moots RJ, Kendall MJ. Corticosteroids: do they damage the cardiovascular system? Postgrad Med J. 1994;70(830):863-70. DOI: http://dx.doi.org/10.1136%2Fpgmj.70.830.863.
Maxwell SR, Moots RJ, Kendall MJ. Corticosteroids: do they damage the cardiovascular system? Postgrad Med J. 1994;70(830):863-70. DOI: http://dx.doi.org/10.1136%2Fpgmj.70.830.863.
54. Bertram CE, Hanson MA. Prenatal programming of postnatal endocrine responses by glucocorticoids. Reproduction. 2002;124(4):459-67. DOI: http://dx.doi.org/10.1530%2Freprod%2 F124.4.459.
55. Kay HH, Bird IM, Coe CL, Dudley DJ. Antenatal steroid treatment and adverse fetal effects: what is the evidence? J Soc Gynecol Investig. 2000;7(5):269-78. DOI: http://dx.doi.org/10.1016%2FS1071-5576%2800%2900075-7.
56. Newnham JP. Is prenatal glucocorticoid administration another origin of adult disease? Clin Exp Pharmacol Physiol. 2001;28(11):957-61. DOI: http://dx.doi.org/10.1046%2Fj.1440-1681.2001.03559.x.
57. Langley-Evans SC, Sherman RC, Welham SJ et al. Intrauterine programming of hypertension: the role of the renin-angiotensin system. Biochem Soc Trans. 1999;27(2):88-93.
58. Benediktsson R, Lindsay R, Noble J et al. Glucocorticoid exposure in utero: new model for adult hypertension. Lancet.
1993;341(8841):339-41. DOI:
http://dx.doi.org/10.1016%2F0140-
6736%2893%2990138-7.
59. Buttgereit F. A Fresh Look at Glucocorticoids. How to Use an Old Ally More Effectively. Bulletin of theNYU Hospital for Joint Diseases. 2012;70 Suppl 1:S26-9.
60. Peppa M, Krania M, Raptis SA. Hypertension and other morbidities with Cushing’s syndrome associated with corticosteroids: a review. Integr Blood Press Control. 2011;4:7-16. DOI: 10.2147/IBPC.S9486. Epub 2011 Mar 3.
Integr Blood Press Control. 2011;4:7-16. DOI: 10.2147/IBPC.S9486. Epub 2011 Mar 3.
Кушингоид — это… Что такое Кушингоид?
Синдром гиперкортицизма (синдром Иценко-Кушинга, кушингоид) включает в себя группу заболеваний, при которых происходит длительное хроническое воздействие на организм избыточного количества гормонов коры надпочечников, независимо от причины, которая вызвала повышение количества этих гормонов в крови. Впервые описан в 1932 году американским врачом Гарвеем Кушингом, а независимо от него в 1924-м — одесским неврологом Н. М. Иценко.
Причины
Причиной синдрома Кушинга могут быть различные состояния. Чаще всего синдром гиперкортицизма (избыточное образование гормонов коры надпочечников) бывает обусловлен повышенной выработкой адренокортикотропного гормона гипофиза (болезнь Иценко-Кушинга). Этот гормон может вырабатываться микроаденомой гипофиза или эктопированной (расположенной не на обычном месте) кортикотропиномой. Эктопированная злокачественная кортикотропинома может располагаться в бронхах, яичках, яичниках.
Реже синдром Кушинга возникает при первичном поражении коры надпочечников (доброкачественные или злокачественные опухоли коры надпочечников, гиперплазия коры надпочечников). Гормонально-активная опухоль коры надпочечника называется кортикостерома. Она продуцирует в кровь избыточное количество глюкокортикоидов. При этом из-за избыточного количества глюкокортикоидов в крови снижается количество адренокортикотропного гормона гипофиза и оставшаяся ткань надпочечников подвергается атрофическим изменениям.
Синдром гиперкортицизма может возникнуть при лечении различных заболеваний при помощи гормонов коры надпочечников (глюкокортикоидов), если происходит передозировка препарата. Изредка возникают необычные синдромы гиперкортицизма, обусловленные приемом пищи или алкогольным отравлением.
Биохимия
При синдроме гиперкортицизма возникают однотипные проявления.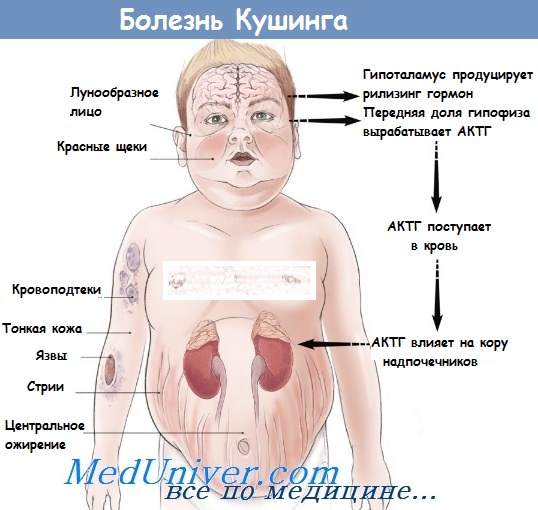 Нарушается обмен белков, жиров и углеводов. Активируется распад белков, образуется избыточное количество свободных жиров в крови, повышается количество глюкозы в крови пациента, что может привести к развитию сахарного диабета.
Нарушается обмен белков, жиров и углеводов. Активируется распад белков, образуется избыточное количество свободных жиров в крови, повышается количество глюкозы в крови пациента, что может привести к развитию сахарного диабета.
Проявления болезни Кушинга обусловлены избыточной секрецией гормонов коры надпочечников, прежде всего глюкокортикоидов.
Симптомы
Наиболее ранним признаком болезни является ожирение, с типичным отложением жировой клетчатки в области лица, шеи, груди живота. Лицо при этом выглядит округлым, лунообразным. На щеках появляется пурпурный румянец.
Глюкокортикоиды вызывают повышение аппетита и изменяют обмен веществ, увеличивая уровень глюкозы в крови и усиленное отложение жира. Конечности наоборот становятся тонкими из-за уменьшения массы мышечной ткани.
На коже в области живота, плечевого пояса, ягодиц и бедер появляются багрово-синюшные полосы растяжения — стрии. Это результат растяжения кожи при избыточном отложении жиров и нарушения обмена белка, из-за чего кожа истончается и легко растягивается. На коже появляются угревые высыпания. Раны и порезы заживают медленно.
В местах трения в области воротника на шее, в области живота, локтей возникает усиленная окраска кожных покровов. В этих местах откладывается меланин, количество которого увеличивается вместе с количеством адренокортикотропного гормона.
У женщин возникает гирсутизм (избыточное оволосение). Появляются волосы на верхней губе, подбородке, груди. Избыточный рост волос у женщин обусловлен усилением продукции мужских половых гормонов андрогенов корой надпочечников, что у женщин вызывает также нарушения менструального цикла. У мужчин возникает импотенция.
Вначале появляется периодическое, затем постоянное повышение артериального давления. Постепенно развивается разрежение костной ткани — остеопороз, который проявляется сначала болями в костях и суставах, затем могут возникнуть спонтанные переломы ребер, конечностей. Избыток глюкортикоидов вызывает как нарушение образования белковой основы костей, так и усиливает выход кальция из костной ткани.
Пациенты жалуются на слабость, головные боли, увеличение массы тела. Иногда у больных болезнью с гиперкортицизмом возникают нарушения психики. Появляются депрессия, различные нарушения сна, психозы.
Лечение
Цель лечения — нормализация уровня гормонов коры надпочечников в крови. Применяются препараты снижающие продукцию гормонов в коре надпочечников — низорал, мамомит, метапирон — в течение длительного времени.
Проводится симптоматическое лечение, направленное на коррекцию нарушений белкового и углеводного обмена, нормализацию уровня артериального давления, лечение сердечной недостаточности. При наличии у пациента кортикостеромы, производится одностороннее удаление надпочечника (односторонняя адреналэктомия).
Wikimedia Foundation. 2010.
Болезнь и синдром Иценко-Кушинга — ПроМедицина Уфа
Болезнь и синдром Иценко-Кушинга – это достаточно редкостное заболевание, которое сопровождается избытком гормонов глюкокортикоидов. Именно эти гормоны в норме вырабатываются надпочечниками. А вот когда их концентрация довольно таки высока, возникает кушингоид, или как упоминалось выше болезнь и синдром Иценко-Кушинга.
Заболевание названо по имени американского хирурга двадцатого столетия, который идентифицировал его. Это заболевание вызвано высоким содержанием в крови кортизола (важного кортикостероидного гормона). Кортизол вырабатывается в коре надпочечников — органе, который расположен в верхней части каждой почки и составляет часть эндокринной системы организма. Выработка кортизола стимулируется выбросом адренокортикотропного гормона (АКТГ) из гипофиза. Болезнь и синдром Иценко-Кушинга возникает из-за перепроизводства кортизола надпочечниками или употребления чрезмерных количеств кортизона при лечении ряда болезней.
Причины
Опухоль коры надпочечников
Надпочечником называется железа, какая имеет 2 слоя – корковый, а также мозговой. В основном в большинстве случаев развивается опухоль мозгового слоя, и впоследствии надпочечник начинает вырабатывать в несколько раз больше гормонов, чем нужно.
Рак
Порой злокачественные опухоли хорошо маскируются под железу и начинают вырабатывать гормоны альдостерон и кортизол, что в свою очередь приводит к повышению их концентраций в человеческом организме. При всем этом собственные железы понемногу начинают атрофироваться – таким образом организм старается бороться с избытком гормонов.
Лекарственный синдром Кушинга развивается в основном у тех людей, продолжительное время принимавших глюкокортикоиды с какими-либо лечебными целями.
Временами наблюдается небольшое повышение уровня гормонов надпочечников во время вынашивания ребенка, сахарном диабете, алкоголизме, а также некоторых болезнях печени.
Необходимо помнить, что под этим синдромом объединяется ряд патологических состояний: значительное увеличение секреции гипофизом АКТГ, аденома или рак надпочечника и подобные.
Синдром возникает в любом возрасте, но чаще всего в 20-40 лет; женщины поражаются в десять раз чаще, чем мужчины.
Симптомы
Самым важным симптомом, по какому сразу же можно заподозрить болезнь и синдром Иценко-Кушинга – это неравномерное ожирение. В основном жировая клетчатка откладывается на верхней части туловища, при этом ноги остаются нормальными. Ладони тоже не полнеют, на их тыльной стороне полностью истончается жировая клетчатка. Лицо становится довольно таки круглым, своим видом напоминает луну, цвет — багрово-красный. А вот кожа лица и тела остается тонкой, сухой, часто возникают многочисленные угревидные высыпания. На бедрах, предплечьях, животе можно увидеть растяжки ярко-красного или даже фиолетового цвета.
У женщин, по причине избытка половых гормонов, возникают признаки излишнего оволосения: может начаться рост волос над губой и на подбородке, появляются существенные перебои менструального цикла.
За счет неправильного и неравномерного жироотложения происходит необратимая деформация позвоночника, и больные сутулится. А вот за счет избытка гормонов могут возникать гипертония, приступы агрессивности, депрессия, нарушения терморегуляции – именно такие больные очень часто потеют, а также могут мерзнуть в жаркую погоду.
Диагностика и лечение
Болезнь и синдром Иценко-Кушинга всегда диагностируют на основании клинических проявлений, а также разнообразных методов лабораторной диагностики. Больной человек обязательно должен сдать кровь и мочу на анализы, в которых определяют уровень кортизола, а также других гормонов. Позже в обязательном порядке назначается УЗИ, компьютерная или же магнитно-резонансная томография – это исследование на аппаратах, какие позволят увидеть, где именно локализована данная опухоль.
Цель лечения – нормализация уровня гормонов коры надпочечников в крови. Применяются препараты снижающие продукцию гормонов в коре надпочечников. Проводится симптоматическое лечение, направленное на коррекцию нарушений белкового и углеводного обмена, нормализацию уровня артериального давления, лечение сердечной недостаточности. При наличии у пациента кортикостеромы, производится одностороннее удаление надпочечника (односторонняя адреналэктомия).
Преднизолон-Ферейн р-р для в/в и в/м введ.30мг/мл в амп.1мл в уп №5х2 — Планета Здоровья
Наименование
Преднизолон-ферейн
Основное действующее вещество
Преднизолон
Форма выпуска
раствор для внутривенного и внутримышечного введения По 1 мл препарата в ампулы стеклянные или ампулы стеклянные с кольцом излома. По 3, 5 или 10 ампул препарата вместе с инструкцией по медицинскому применению и диском режущим керамическим для открытия ампул вкладывают в пачку из картона коробочного с перегородками или гофрированной вкладкой, или с полимерной вкладкой из пленки поливинилхлоридной для размещения и фиксации ампул. По 1 мл препарата в ампулы стеклянные с кольцом излома объемом 1 мл. По 5 ампул препарата вкладывают в блистер из пленки поливинилхлоридной, который покрывают пачку из картона коробочного (хром-эрзац).
Дозировка
30 мг / 1 мл 1 мл
Фармакодинамика
Оказывает противовоспалительное, противоаллергическое, иммунодепрессивное, противошоковое и антитоксическое действие. В относительно больших дозах угнетает активность фибробластов, синтез коллагена, ретикулоэндотелия и соединительной ткани (торможение пролиферативной фазы воспаления), задерживает синтез и ускоряет катаболизм белка в мышечной ткани, но повышает его синтез в печени.
Противоаллергические и иммуносупрессивные свойства препарата обусловлены торможением развития лимфоидной ткани с её инволюцией при длительном применении, снижением числа циркулирующих Т- и В-лимфоцитов, угнетением дегрануляции тучных клеток, подавлением продукции антител.
Противошоковое действие препарата обусловлено повышением реакции сосудов на эндо- и экзогенные сосудосуживающие вещества, с восстановлением чувствительности рецепторов сосудов к катехоламинам и усилением их гипертензивного эффекта, а также задержкой выведения из организма натрия и воды.
Антитоксическое действие препарата связано со стимуляцией в печени процессов синтеза белка и ускорением инактивации в ней эндогенных токсических метаболитов и ксенобиотиков, а также с повышением стабильности клеточных мембран, в т.ч. гепатоцитов. Усиливает в печени депонирование гликогена и синтез глюкозы из продуктов белкового обмена. Повышение уровня глюкозы в крови активизирует выделение инсулина. Угнетает захват глюкозы жировыми клетками, что приводит к активации липолиза. Однако, вследствие увеличения секреции инсулина происходит стимуляция липогенеза, что способствует накоплению жира.
Снижает всасывание кальция в кишечнике, повышает вымывание его из костей и экскрецию почками. Подавляет высвобождение гипофизом адренокортикотропного гормона и β-липотропина, в связи с чем при длительном применении препарат может способствовать развитию функциональной недостаточности коры надпочечников.
Главными факторами, ограничивающими длительную терапию преднизолоном, являются остеопороз и синдром Иценко-Кушинга. Преднизолон угнетает секрецию тиреотропного и фолликулостимулирующего гормонов.
В высоких дозах может повышать возбудимость тканей мозга и способствовать снижению порога судорожной готовности.
В относительно больших дозах угнетает активность фибробластов, синтез коллагена, ретикулоэндотелия и соединительной ткани (торможение пролиферативной фазы воспаления), задерживает синтез и ускоряет катаболизм белка в мышечной ткани, но повышает его синтез в печени.
Противоаллергические и иммуносупрессивные свойства препарата обусловлены торможением развития лимфоидной ткани с её инволюцией при длительном применении, снижением числа циркулирующих Т- и В-лимфоцитов, угнетением дегрануляции тучных клеток, подавлением продукции антител.
Противошоковое действие препарата обусловлено повышением реакции сосудов на эндо- и экзогенные сосудосуживающие вещества, с восстановлением чувствительности рецепторов сосудов к катехоламинам и усилением их гипертензивного эффекта, а также задержкой выведения из организма натрия и воды.
Антитоксическое действие препарата связано со стимуляцией в печени процессов синтеза белка и ускорением инактивации в ней эндогенных токсических метаболитов и ксенобиотиков, а также с повышением стабильности клеточных мембран, в т.ч. гепатоцитов. Усиливает в печени депонирование гликогена и синтез глюкозы из продуктов белкового обмена. Повышение уровня глюкозы в крови активизирует выделение инсулина. Угнетает захват глюкозы жировыми клетками, что приводит к активации липолиза. Однако, вследствие увеличения секреции инсулина происходит стимуляция липогенеза, что способствует накоплению жира.
Снижает всасывание кальция в кишечнике, повышает вымывание его из костей и экскрецию почками. Подавляет высвобождение гипофизом адренокортикотропного гормона и β-липотропина, в связи с чем при длительном применении препарат может способствовать развитию функциональной недостаточности коры надпочечников.
Главными факторами, ограничивающими длительную терапию преднизолоном, являются остеопороз и синдром Иценко-Кушинга. Преднизолон угнетает секрецию тиреотропного и фолликулостимулирующего гормонов.
В высоких дозах может повышать возбудимость тканей мозга и способствовать снижению порога судорожной готовности. Стимулирует избыточную секрецию соляной кислоты и пепсина в желудке, в связи с чем может способствовать развитию пептической язвы.
Стимулирует избыточную секрецию соляной кислоты и пепсина в желудке, в связи с чем может способствовать развитию пептической язвы.
Фармакокинетика
При внутримышечном введении всасывается в кровь быстро, однако по сравнению с достижением максимального уровня в крови фармакологический эффект препарата значительно запаздывает и развивается 2-8 часов. В плазме крови большая часть преднизолона связывается с транскортином (кортизолсвязывающим глобулином), а при насыщении процесса — с альбумином. При снижении синтеза белка наблюдается снижение связывающей способности альбуминов, что может вызвать увеличение свободной фракции преднизолона и, как следствие, проявление его токсического действия при применении обычных терапевтических доз. Период полувыведения у взрослых — 2-4 часа, у детей — короче. Биотрансформируется путем окисления преимущественно в печени, а также в почках, тонкой кишке, бронхах. Окисленные формы глюкуронизируются или сульфатируются и в виде конъюгатов выводятся почками. Около 20 % преднизолона экскретируется из организма почками в неизмененном виде; небольшая часть -выделяется с желчью. При заболеваниях печени метаболизм преднизолона замедляется и снижается степень его связывания с белками плазмы крови, что приводит к увеличению периода полувыведения препарата.
Показания к применению
Внутримышечное, внутривенное введение: системные заболевания соединительной ткани: системная красная волчанка, дерматомиозит, склеродермия, узелковый периартериит, болезнь Бехтерева;
гематологические заболевания: острая гемолитическая анемия, лимфогранулематоз, гранулоцитопения, тромбоцитопеническая пурпура, агранулоцитоз, различные формы лейкемии;
кожные заболевания: обычная экзема, мультиформная экссудативная эритема, пузырчатка обычная, эритродермия, эксфолиативный дерматит, себорейный дерматит, псориаз, аллопеция, адреногенитальный синдром;
заместительная терапия: Аддисонов криз;
неотложные состояния: тяжелые формы неспецефического язвенного колита и болезни Крона, шок (ожоговый, травматический, операционный, анафилактический, токсический, трансфузионный), астматический статус, острая недостаточность коры надпочечников, печеночная кома, тяжёлые аллергические и анафилактические реакции, гипогликемические реакции;
Внутрисуставное введение: хронический полиартрит, остеоартрит больших суставов, ревматоидный артрит, посттравматический артрит, артроз;
При инфекционных заболеваниях и латентных формах туберкулёза препарат следует назначать только в комбинации с антибиотиками и противотуберкулёзными средствами. При необходимости применения преднизолона на фоне приёма пероральных гипогликемизирующих препаратов или антикоагулянтов необходимо корректировать режим дозирования последних. У больных тромбоцитопенической пурпурой препарат применять только внутривенно.
После прекращения лечения возможно возникновение синдрома отмены, недостаточности надпочечников, а также обострение заболевания, в связи с которым был назначен преднизолон. Если после окончания лечения преднизолоном наблюдается функциональная недостаточность надпочечников, следует немедленно возобновить применение препарата, а уменьшение дозы проводить очень медленно и с осторожностью (например, суточную дозу нужно уменьшать на 2-3 мг на протяжение 7-10 дней). Из-за опасности развития гиперкортицизма новый курс лечения кортизоном, после проведенного ранее длительного лечения преднизолоном на протяжение нескольких месяцев, всегда нужно начинать с низких начальных доз (за исключением острых состояний, опасных для жизни).
Следует особенно тщательно контролировать электролитный баланс при комбинированном применении преднизолона с диуретиками. При длительном лечении преднизолоном с целью профилактики гипокалиемии необходимо назначать препараты калия и соответстующую диету в связи с возможным повышением внутриглазного давления и риском развития субкапсулярной катаракты.
Во время лечения, особенно длительного, необхимо наблюдение окулиста. При указаниях на псориаз в анамнезе преднизолон в высоких дозах применять с особой осторожностью.
Если в анамнезе есть психоз, судороги, преднизолон следует применять только в минимальных эффективных дозах.
С особенной осторожностью следует назначать препарат при мигрени, наличии в анамнезе данных о некоторых паразитарных заболеваниях (особенно амебиаз).
Детям преднизолон назначать с особой острожностью.
С особой острожностью назначать при иммунодефицитных состояниях (в том числе при СПИД или ВИЧ-инфицировании). Также с осторожностью назначать после недавно перенесеного инфаркта миокарда (у больных с острым, подострым инфарктом миокарда возможно расширение очага некроза, замедление формирования рубцевой ткани, разрыв сердечной мышцы).
При необходимости применения преднизолона на фоне приёма пероральных гипогликемизирующих препаратов или антикоагулянтов необходимо корректировать режим дозирования последних. У больных тромбоцитопенической пурпурой препарат применять только внутривенно.
После прекращения лечения возможно возникновение синдрома отмены, недостаточности надпочечников, а также обострение заболевания, в связи с которым был назначен преднизолон. Если после окончания лечения преднизолоном наблюдается функциональная недостаточность надпочечников, следует немедленно возобновить применение препарата, а уменьшение дозы проводить очень медленно и с осторожностью (например, суточную дозу нужно уменьшать на 2-3 мг на протяжение 7-10 дней). Из-за опасности развития гиперкортицизма новый курс лечения кортизоном, после проведенного ранее длительного лечения преднизолоном на протяжение нескольких месяцев, всегда нужно начинать с низких начальных доз (за исключением острых состояний, опасных для жизни).
Следует особенно тщательно контролировать электролитный баланс при комбинированном применении преднизолона с диуретиками. При длительном лечении преднизолоном с целью профилактики гипокалиемии необходимо назначать препараты калия и соответстующую диету в связи с возможным повышением внутриглазного давления и риском развития субкапсулярной катаракты.
Во время лечения, особенно длительного, необхимо наблюдение окулиста. При указаниях на псориаз в анамнезе преднизолон в высоких дозах применять с особой осторожностью.
Если в анамнезе есть психоз, судороги, преднизолон следует применять только в минимальных эффективных дозах.
С особенной осторожностью следует назначать препарат при мигрени, наличии в анамнезе данных о некоторых паразитарных заболеваниях (особенно амебиаз).
Детям преднизолон назначать с особой острожностью.
С особой острожностью назначать при иммунодефицитных состояниях (в том числе при СПИД или ВИЧ-инфицировании). Также с осторожностью назначать после недавно перенесеного инфаркта миокарда (у больных с острым, подострым инфарктом миокарда возможно расширение очага некроза, замедление формирования рубцевой ткани, разрыв сердечной мышцы). С особой острожностью назначают при печеночной недостаточности, состояниях, которые обуславливают возникновение гипоальбуминемии, ожирении III- IV степени.
Женщинам во время менопаузы необходимо проходить исследования относительно возможного возникновения остеопороза.
При печени глюкокортикоидами на протяжении длительного времени рекомендуется регулярно контролировать артериальное давление, определять уровень глюкозы в моче и крови, проводить анализ кала на скрытую кровь, анализы показателей свертываемости крови, рентгенологический контроль позвоночника. Перед началом лечения глюкокортикоидами нужно провести тщательное обследование желудочно-кишечного тракта для исключения язвенной болезни желудка и двенадцатиперстной кишки.
С особой острожностью назначают при печеночной недостаточности, состояниях, которые обуславливают возникновение гипоальбуминемии, ожирении III- IV степени.
Женщинам во время менопаузы необходимо проходить исследования относительно возможного возникновения остеопороза.
При печени глюкокортикоидами на протяжении длительного времени рекомендуется регулярно контролировать артериальное давление, определять уровень глюкозы в моче и крови, проводить анализ кала на скрытую кровь, анализы показателей свертываемости крови, рентгенологический контроль позвоночника. Перед началом лечения глюкокортикоидами нужно провести тщательное обследование желудочно-кишечного тракта для исключения язвенной болезни желудка и двенадцатиперстной кишки.
Способ применения и дозы
Доза лекарственного средства и продолжительность лечения устанавливается врачом индивидуально в зависимости от показаний и тяжести заболевания.
Преднизолон вводят внутривенно (капельно или струйно) или внутримышечно. Внутривенно лекарственное средство обычно вводят сначала струйно, затем капельно.
При острой недостаточности надпочечников разовая доза лекарственного средства составляет 100 — 200 мг, суточная 300-400 мг.
При тяжелых аллергических реакциях Преднизолон вводят в суточной дозе 100-200 мг в течение 3- 16 дней.
При бронхиальной астме лекарственное средство вводят в зависимости от тяжести заболевания и эффективности комплексного лечения от 75 мг до 675 мг на курс лечения от 3 до 16 дней; в тяжелых случаях доза может быть повышена до 1400 мг на курс лечения и более с постепенным снижением дозы.
При астматическом статусе Преднизолон вводят в дозе 500-1200 мг в сутки с последующим снижением до 300 мг в сутки и переходом на поддерживающие дозы.
При тиреотоксическом кризе вводят по 100 мг лекарственного средства в суточной дозе 200-300 мг; при необходимости суточная доза может быть увеличена до 1000 мг. Длительность введения зависит от терапевтического эффекта, обычно до 6 дней.
При шоке, резистентном к стандартной терапии, Преднизолон в начале терапии обычно вводят струйно, после чего переходят на капельное введение. Если в течение 10-20 минут артериальное давление не повышается, повторяют струйное введение лекарственного средства. После выведения из шокового состояния продолжают капельное введение до стабилизации артериального давления. Разовая доза составляет 50-150 мг (в тяжелых случаях — до 400 мг). Повторно лекарственное средство вводят через 3-4 часа. Суточная доза может составлять 300- 1200 мг (с последующим снижением дозы).
При острой печеночно-почечной недостаточности (при острых отравлениях, в послеоперационном и послеродовом периодах и др.) Преднизолон вводят по 25-75 мг/сут; при наличии показаний суточная доза может быть увеличена до 300-1500 мг/сут и выше.
При ревматоидном артрите и системной красной волчанке Преднизолон вводят дополнительно к системному приему лекарственного средства в дозе 75-125 мг в сутки не более 7-10 дней.
При остром гепатите Преднизолон вводят но 75-100 мг/сут в течение 7-10 дней.
При отравлениях прижигающими жидкостями с ожогами пищеварительного тракта и верхних дыхательных путей Преднизолон назначают в дозе 75-400 мг/сут в течение 3-18 дней.
При невозможности внутривенного введения Преднизолон вводят внутримышечно в тех же дозах. После купирования острого состояния назначают внутрь Преднизолон в таблетках, с последующим постепенным уменьшением дозы.
При длительном приеме лекарственного средства суточную дозу следует снижать постепенно.
Длительную терапию нельзя прекращать внезапно!
Дети
Применять детям старше 6 лет исключительно по назначению и под контролем врача. Дозы и длительность терапии доктор определяет индивидуально, в зависимости от возраста и тяжести течения заболевания. При длительном применении у детей возможно замедление роста, поэтому необходимо ограничиваться применением минимальных доз по определённым показаниям в течение самого короткого времени. Польза от лечения должна превышать возможный риск возникновения побочных реакций.
Если в течение 10-20 минут артериальное давление не повышается, повторяют струйное введение лекарственного средства. После выведения из шокового состояния продолжают капельное введение до стабилизации артериального давления. Разовая доза составляет 50-150 мг (в тяжелых случаях — до 400 мг). Повторно лекарственное средство вводят через 3-4 часа. Суточная доза может составлять 300- 1200 мг (с последующим снижением дозы).
При острой печеночно-почечной недостаточности (при острых отравлениях, в послеоперационном и послеродовом периодах и др.) Преднизолон вводят по 25-75 мг/сут; при наличии показаний суточная доза может быть увеличена до 300-1500 мг/сут и выше.
При ревматоидном артрите и системной красной волчанке Преднизолон вводят дополнительно к системному приему лекарственного средства в дозе 75-125 мг в сутки не более 7-10 дней.
При остром гепатите Преднизолон вводят но 75-100 мг/сут в течение 7-10 дней.
При отравлениях прижигающими жидкостями с ожогами пищеварительного тракта и верхних дыхательных путей Преднизолон назначают в дозе 75-400 мг/сут в течение 3-18 дней.
При невозможности внутривенного введения Преднизолон вводят внутримышечно в тех же дозах. После купирования острого состояния назначают внутрь Преднизолон в таблетках, с последующим постепенным уменьшением дозы.
При длительном приеме лекарственного средства суточную дозу следует снижать постепенно.
Длительную терапию нельзя прекращать внезапно!
Дети
Применять детям старше 6 лет исключительно по назначению и под контролем врача. Дозы и длительность терапии доктор определяет индивидуально, в зависимости от возраста и тяжести течения заболевания. При длительном применении у детей возможно замедление роста, поэтому необходимо ограничиваться применением минимальных доз по определённым показаниям в течение самого короткого времени. Польза от лечения должна превышать возможный риск возникновения побочных реакций.
Применение при беременности и в период лактации
Во время беременности препарат не применять.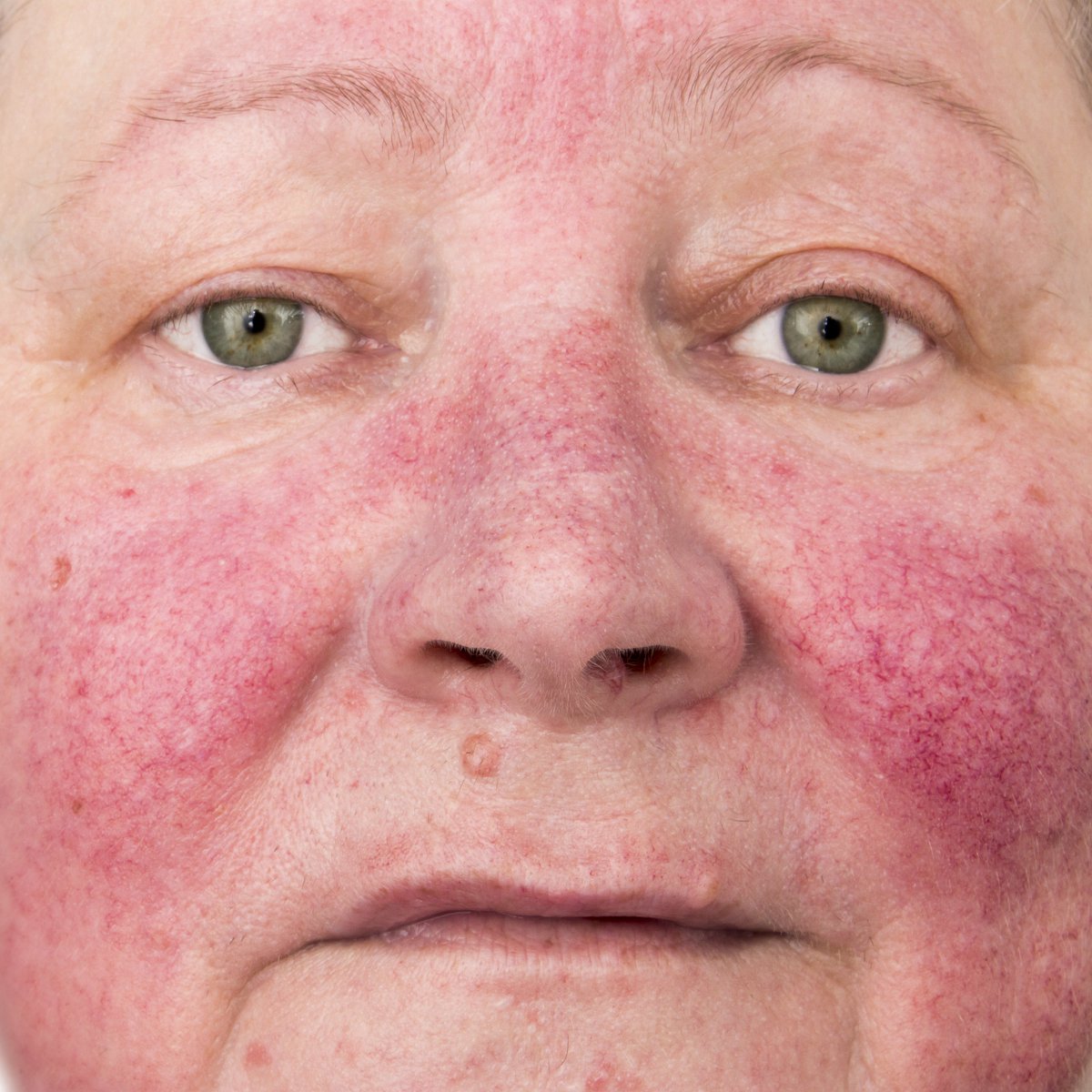 В случае необходимости применения препарата в период лактации кормление грудью рекомендуется прекратить.
В случае необходимости применения препарата в период лактации кормление грудью рекомендуется прекратить.
Меры предосторожности
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами Пациентам, которые лечатся преднизолоном, следует воздержаться от потенциально опасных видов деятельности, которые требуют повышенного внимания скорости психических и двигательных реакций. Особые группы пациентов Пожилой возраст При длительной терапии могут наблюдаться атрофия мышц, боли в мышцах или слабость, замедленное заживление ран, атрофия белковой матрицы кости, ведущая к остеопорозу, компрессионные переломы позвонков, асептический некроз головки бедра или головки плеча, патологические переломы длинных трубчатых костей. Могут наблюдаться особенно серьезные осложнения у пациентов пожилого возраста и ослабленных пациентов. Перед началом глюкокортикоидной терапии у женщин в постменопаузе необходимо учитывать, что такие пациенты особенно склонны к остеопорозу. Применять с осторожностью у пациентов с остеопорозом. Нарушения функции печени У пациентов с циррозом наблюдается усиление эффекта глюкокортикоидов. Нарушения функции почек. Применять с осторожностью.
Взаимодействие с другими препаратами
Антикоагулянты: при одновременном применении с глюкокортикоидами может усиливаться или уменьшаться действие антикоагулянтов. Парентеральное введение преднизолона вызывает тромболитическое действие антагонистов витамина К (флуиндион, аценокумарол).
Салицилаты и другие нестероидные противоспалительные препараты: одновременное применение салицилатов, индометацина и других нестероидных противовоспалительных препаратов может повышать вероятность образования язв слизистой оболочки желудка. Преднизолон уменьшает уровень салицилатов в сыворотке крови, увеличивая их почечный клиренс. Необходима осторожность при уменьшении дозы преднизолона при длительном одновременном применении.
Гипогликемические препараты: преднизолон частично угнетает гипогликемический эффект пероральных сахароснижающих средств и инсулина. Индукторы печёночных ферментов, например, барбитураты, фенитоин, пирамидон, карбамазепин и римфампицин увеличивают системный клиренс преднизолона, таким образом уменьшая эффект преднизолона практически в 2 раза.
Ингибиторы CYP3A4, например, эритромицин, кларитромицин, кетоконазол, дилтиазем, апрепитант, итраконазол и олеандомицин увеличивают элиминацию и уровень преднизолона в плазме крови, что усиливает терапевтический и побочные эффекты преднизолона.
Эстроген может потенциировать эффект преднизолона, замедляя его метаболизм. Не рекомендуется регулировать дозы преднизолона женщинам, применяющим пероральные контрацептивы, которые содействуют не только увеличению периода полувыведения, а и развитию атипичного иммуносупрессивного эффекта преднизолона.
Фторхинолоны: одновременное применение может привести к повреждению сухожилий. Амфотерицин, диуретики и слабительные средства: преднизолон может повышать выведение калия из организма у пациентов, которые получают одновременно эти препараты. Иммунодепрессанты: преднизолон имеет активные иммуносупрессивные свойства, которые могут вызывать увеличение терапевтических эффектов или риск развития разных побочных реакций при одновременном применении с другими иммунодепрессантами. Только некоторые из них можна объяснить фармакокинетическими взаимодейстиями. Глюкокортикоиды повышают противорвотную эффективность противорвотных препаратов, которые используются параллельно при терапии противоопухолевыми препаратами, вызывающими рвоту.
Кортикостероиды могут повышать концентрацию такролимуса в плазме крови при их одновременном применении, при их отмене концентрация такролимуса в плазме крови снижается.
Иммунизация: глюкортикоиды могут уменьшать эффективность иммунизации и увеличивать риск неврологических осложнений. Применение терапевтических (иммуносупрессивных) доз глюкокортикоидов с живыми вирусными вакцинами могут увеличивать риск развития вирусных заболеваний. На протяжении терапии препаратом могут быть применены вакцины экстренного типа.
Индукторы печёночных ферментов, например, барбитураты, фенитоин, пирамидон, карбамазепин и римфампицин увеличивают системный клиренс преднизолона, таким образом уменьшая эффект преднизолона практически в 2 раза.
Ингибиторы CYP3A4, например, эритромицин, кларитромицин, кетоконазол, дилтиазем, апрепитант, итраконазол и олеандомицин увеличивают элиминацию и уровень преднизолона в плазме крови, что усиливает терапевтический и побочные эффекты преднизолона.
Эстроген может потенциировать эффект преднизолона, замедляя его метаболизм. Не рекомендуется регулировать дозы преднизолона женщинам, применяющим пероральные контрацептивы, которые содействуют не только увеличению периода полувыведения, а и развитию атипичного иммуносупрессивного эффекта преднизолона.
Фторхинолоны: одновременное применение может привести к повреждению сухожилий. Амфотерицин, диуретики и слабительные средства: преднизолон может повышать выведение калия из организма у пациентов, которые получают одновременно эти препараты. Иммунодепрессанты: преднизолон имеет активные иммуносупрессивные свойства, которые могут вызывать увеличение терапевтических эффектов или риск развития разных побочных реакций при одновременном применении с другими иммунодепрессантами. Только некоторые из них можна объяснить фармакокинетическими взаимодейстиями. Глюкокортикоиды повышают противорвотную эффективность противорвотных препаратов, которые используются параллельно при терапии противоопухолевыми препаратами, вызывающими рвоту.
Кортикостероиды могут повышать концентрацию такролимуса в плазме крови при их одновременном применении, при их отмене концентрация такролимуса в плазме крови снижается.
Иммунизация: глюкортикоиды могут уменьшать эффективность иммунизации и увеличивать риск неврологических осложнений. Применение терапевтических (иммуносупрессивных) доз глюкокортикоидов с живыми вирусными вакцинами могут увеличивать риск развития вирусных заболеваний. На протяжении терапии препаратом могут быть применены вакцины экстренного типа.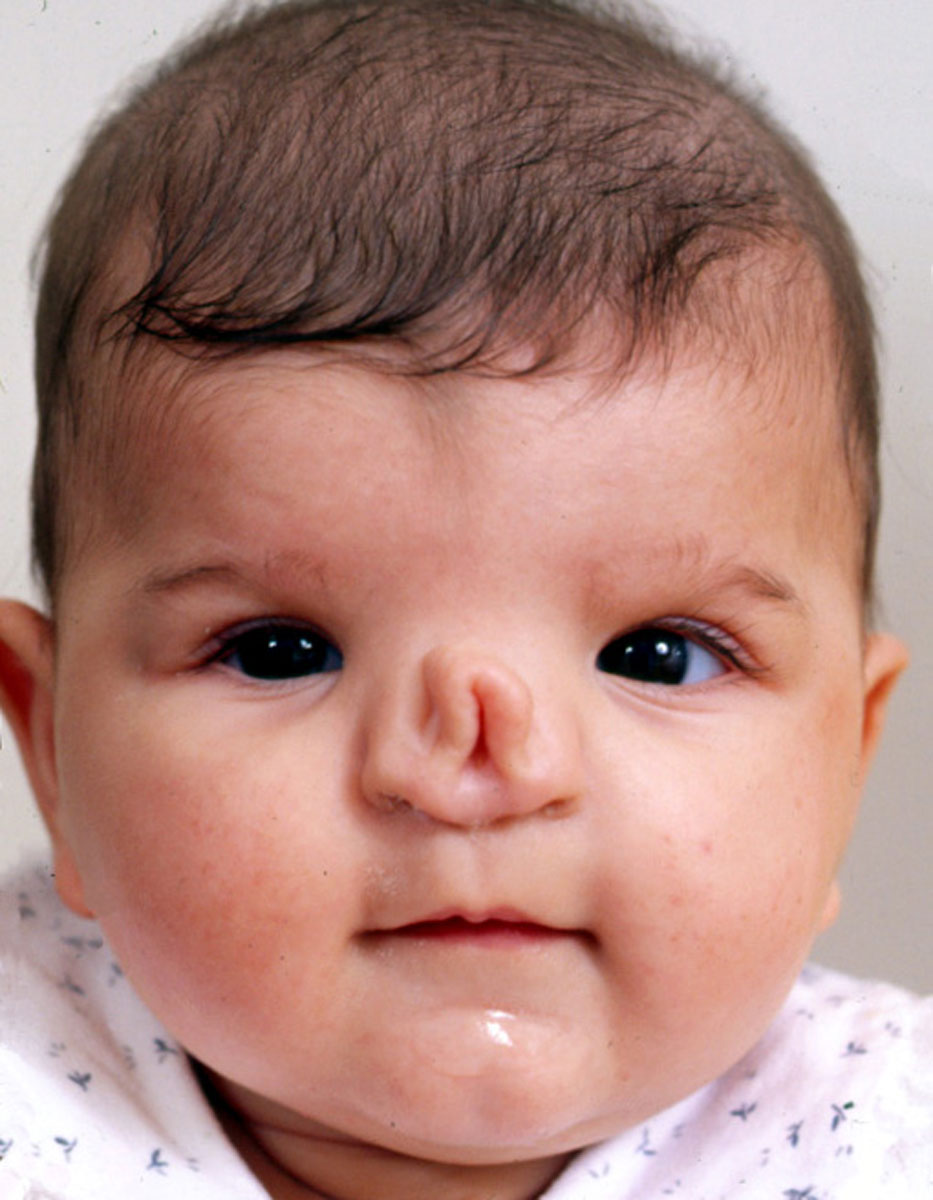 Антихолинэстеразные средства: у больных миастенией применение глюкокортикоидов и антихолинэстеразных средств может вызывать мышечную слабость, особенно у пациентов с миастенией gravis.
Сердечные гликозиды: повышается риск развития гликозидной интоксикации.
Другие: сообщалось о двух серьёзных случаях острой миопатии у пациентов пожилого возраста, которые принимали доксокариума хлорид и преднизолон в высоких дозах. При длительной терапии глюкокортикоиды могут уменшать эффект соматотропина.
Описаны случаи возникновения острой миопатии при применении кортикостероидов у больных, которые одновременно получают лечение блокаторами нервно-мышечной передачи (например, панкурониум).
При одновременном применении преднизолона и циклоспорина были отмечены случаи возникновения судорог. Поскольку одновременное введение этих препаратов вызывает взаимное торможение метаболизма, вероятно, что судороги и другие побочные эффекты, связанные с применением каждого с этих препаратов как монотерапии, при их одновременном применении могут возникать чаще. Одновременное применение может вызывать увеличение концентрации других препаратов в плазме крови.
Антигистаминные лекарственные средства снижают эффект преднизолона.
При одновременном применении преднизолона с гипотензивными препаратами возможно снижение эффективности последних.
Преднизолон нельзя смешивать и применять одновременно с другими препаратами в одной и той же инфузионной системе или шприце.
При смешивании раствора преднизолона с гепарином образуется осадок.
Несовместим с аэрозолями симпатомиметических средств для лечения бронхиальной астмы у детей (опасность развития паралича дыхания).
Антихолинэстеразные средства: у больных миастенией применение глюкокортикоидов и антихолинэстеразных средств может вызывать мышечную слабость, особенно у пациентов с миастенией gravis.
Сердечные гликозиды: повышается риск развития гликозидной интоксикации.
Другие: сообщалось о двух серьёзных случаях острой миопатии у пациентов пожилого возраста, которые принимали доксокариума хлорид и преднизолон в высоких дозах. При длительной терапии глюкокортикоиды могут уменшать эффект соматотропина.
Описаны случаи возникновения острой миопатии при применении кортикостероидов у больных, которые одновременно получают лечение блокаторами нервно-мышечной передачи (например, панкурониум).
При одновременном применении преднизолона и циклоспорина были отмечены случаи возникновения судорог. Поскольку одновременное введение этих препаратов вызывает взаимное торможение метаболизма, вероятно, что судороги и другие побочные эффекты, связанные с применением каждого с этих препаратов как монотерапии, при их одновременном применении могут возникать чаще. Одновременное применение может вызывать увеличение концентрации других препаратов в плазме крови.
Антигистаминные лекарственные средства снижают эффект преднизолона.
При одновременном применении преднизолона с гипотензивными препаратами возможно снижение эффективности последних.
Преднизолон нельзя смешивать и применять одновременно с другими препаратами в одной и той же инфузионной системе или шприце.
При смешивании раствора преднизолона с гепарином образуется осадок.
Несовместим с аэрозолями симпатомиметических средств для лечения бронхиальной астмы у детей (опасность развития паралича дыхания).
Противопоказания
Повышенная чувствительность к компонентам препарата; язвенная болезнь желудка и двенадцатиперстной кишки, остеопороз, болезнь Иценко-Кушинга, склонность к тромбоэмболии, почечная недостаточность, артериальная гипертензия, вирусные инфекции (в том числе вирусные поражения глаз и кожи), декомпенсированный сахарный диабет, период вакцинации (не менее 14 дней до и после проведения профилактической иммунизации), лимфаденит после вакцинации БЦЖ, активная форма туберкулеза, глаукома, катаракта, продуктивная симптоматика при психических заболеваниях, психозы, депрессии; системный микоз, герпетические заболевания, сифилис, тяжелая миопатия (за исключением миастений), полиомиелит (за исключением бульбарно- энцефалитической формы), период беременности и кормления грудью. Для внутрисуставных инъекций — инфекции в месте введения.
Для внутрисуставных инъекций — инфекции в месте введения.
Состав
действующее вещество: 1 мл раствора содержит преднизототкг на преднизолон — 30 мг; вспомогательные вещества: натрия гидрофосфат безводный, натрия дигидрофосфат дигидрат, пропиленгликоль, вода для инъекций. Основные физико-химические свойства: прозрачный бесцветный или почти бесцветный раствор.
Передозировка
В случае передозировки возможны тошнота, рвота, брадикардия, аритмия, усиление явлений сердечной недостаточности, остановка сердца; гипокалиемия, повышение артериального давления, судороги мышц, гипергликемия, тромбоэмболия, острый психоз, головокружение, головная боль, возможно развитие симптомов гиперкортицизма: увеличение массы тела, развитие отеков, артериальная гипертензия, глюкозурия, гипокалиемия. У детей при передозировке возможно угнетение гипоталамо-гипофизарно- надпочечниковой системы, синдром Иценко-Кушинга, снижение экскреции гормона роста, повышение внутричерепного давления. Специфеского антидота нет. Лечение: прекращение применения препарата, симптоматическая терапия, при необходимости — коррекция электролитного баланса.
Побочное действие
Развитие тяжелых побочных реакций зависит от дозы и от длительности лечения. Побочные реакции обычно развиваются при длительном лечении препаратом. На протяжении короткого периода риск их возникновения маловероятен.
Инфекции и инвазии: повышенная чувствительность к бактериальным, вирусным, грибковым инфекциям, их тяжесть с маскированием симптомов, опортунистические инфекции.
Со стороны системы крови и лимфатической системы: повышение общего количества лейкоцитов при снижении количества эозинофилов, моноцитов и лимфоцитов. Масса лимфоидной ткани уменьшается. Может повышаться свертывание крови, которое приводит к тромбозам, тромбоэмболиям.
Со стороны эндокринной системы и метаболизма: угнетение гипоталамо-гипофизарно- надпочечниковой системы, замедление роста у детей и подростков, нарушение менструального цикла, нарушение секреции половых гормонов (аменорея), постклимактерические кровотечения, кушингоидное лицо, гирсутизм, увеличение массы тела, снижение толерантности к углеводам, повышение потребности в инсулине и пероральних сахаропонижающих препаратах, гиперлипидемия, негативный баланс азота и кальция, повышение аппетита, нарушение минерального обмена и электролитного баланса, гипокалиемический алкалоз, гипокалиемия, возможна задержка жидкости и натрия в организме. Психические нарушения: раздражительность, эуфобия, депрессия, склонность к суициду, бессонница, лабильное настроение, повышение концентрации, психологическая зависимость, мания, галлюцинации, обострение шизофрении, деменция, психозы, тревожность, нарушение сна, эпилептические приступы, когнитивная дисфункция (включая амнезию и нарушение сознания), повышение внутричерепного давления, которое сопровождается тошнотой и отёком диска глазного нерва у детей.
Со стороны нервной системы: повышение внутричерепного давления, эпилептические приступы, периферичные нейропатии, парестезии, головокружение, головная боль, вегетативные нарушения.
Со стороны органов зрения: повышение внутриглазного давления, глаукома, отёчность глазного нерва, катаракта, истончение роговицы и склеры, обострение глазных вирусных и грибковых инфекций, экзофтальм.
Со стороны сердечно-сосудистой системы: миокардиальный разрыв вследствие инфаркта миокарда, артериальная гипо- или гипертензия, брадикардия, комбинированная вентрикулярная аритмия, асистолия (вследствие быстрого введения препарата), атеросклероз, тромбоз, васкулит, сердечная недостаточноть, периферические отеки.
У больных с острым инфарктом миокарда — распространение очага некроза, замедление формирования рубца.
Со стороны иммунной системы: аллергические реакции, которые вызывают анафилактический шок с летальным исходом, ангионевротичный отёк, аллергический дерматит, изменение реакции на кожные пробы, рецедив туберкулёза, иммуносупрессия, реакции гиперчувствительности, включая сыпь, зуд кожи.
Со стороны желудочно-кишечного тракта: тошнота, вздутие, неприятный привкус во рту, диспепсия, пептические язвы с перфорацией и кровотечением, язва пищевода, кандидоз пищевода, панкреатит, перфорация жёлчного пузыря, желудочное кровотечение, местный илеит и язвенный колит.
На протяжении применения препарата может наблюдаться повышение АлТ, АсТ и щелочной фосфатазы, что обычно не является существенным и обратимо после отмены препарата.
Со стороны кожи: замедление регенерации, атрофия кожи, образование гематом и атрофических полос кожи (стрии), телеангиэктазия, угревая сыпь, акне, гирсутизм, микрокровоизлияния, экхимоз, пурпура, гипо- или гиперпигментация, постстероидный панникулит, который характеризуется появлением эритематоза, горячих подкожных утолщений на протяжении 2 недель после отмены препарата, саркома Капоши.
Психические нарушения: раздражительность, эуфобия, депрессия, склонность к суициду, бессонница, лабильное настроение, повышение концентрации, психологическая зависимость, мания, галлюцинации, обострение шизофрении, деменция, психозы, тревожность, нарушение сна, эпилептические приступы, когнитивная дисфункция (включая амнезию и нарушение сознания), повышение внутричерепного давления, которое сопровождается тошнотой и отёком диска глазного нерва у детей.
Со стороны нервной системы: повышение внутричерепного давления, эпилептические приступы, периферичные нейропатии, парестезии, головокружение, головная боль, вегетативные нарушения.
Со стороны органов зрения: повышение внутриглазного давления, глаукома, отёчность глазного нерва, катаракта, истончение роговицы и склеры, обострение глазных вирусных и грибковых инфекций, экзофтальм.
Со стороны сердечно-сосудистой системы: миокардиальный разрыв вследствие инфаркта миокарда, артериальная гипо- или гипертензия, брадикардия, комбинированная вентрикулярная аритмия, асистолия (вследствие быстрого введения препарата), атеросклероз, тромбоз, васкулит, сердечная недостаточноть, периферические отеки.
У больных с острым инфарктом миокарда — распространение очага некроза, замедление формирования рубца.
Со стороны иммунной системы: аллергические реакции, которые вызывают анафилактический шок с летальным исходом, ангионевротичный отёк, аллергический дерматит, изменение реакции на кожные пробы, рецедив туберкулёза, иммуносупрессия, реакции гиперчувствительности, включая сыпь, зуд кожи.
Со стороны желудочно-кишечного тракта: тошнота, вздутие, неприятный привкус во рту, диспепсия, пептические язвы с перфорацией и кровотечением, язва пищевода, кандидоз пищевода, панкреатит, перфорация жёлчного пузыря, желудочное кровотечение, местный илеит и язвенный колит.
На протяжении применения препарата может наблюдаться повышение АлТ, АсТ и щелочной фосфатазы, что обычно не является существенным и обратимо после отмены препарата.
Со стороны кожи: замедление регенерации, атрофия кожи, образование гематом и атрофических полос кожи (стрии), телеангиэктазия, угревая сыпь, акне, гирсутизм, микрокровоизлияния, экхимоз, пурпура, гипо- или гиперпигментация, постстероидный панникулит, который характеризуется появлением эритематоза, горячих подкожных утолщений на протяжении 2 недель после отмены препарата, саркома Капоши. Со стороны костно-мышечной системы: проксимальная миопатия, остеопороз, разрыв сухожилий, мышечная слабость, атрофия, миопатия, переломы позвоночника и длинных костей, асептический остеонекроз.
Со стороны мочевыделительной системы: повышение риска образования уролитов и содержание лейкоцитов и эритроцитов в моче без явного повреждения почек.
Общие: недомогание, стойкая икота при применении препарата в высоких дозах, недостаточность надпочечников, что приводит к артериальной гипотензии, гипогликемия и летальные исходы в стрессовых ситуациях, таких как хирургическое вмешательство, травма или инфекция, если доза преднизолона не увеличена.
При резкой отмене препарата возможны синдром отмены, тяжесть симптомов зависит от степени атрофии надпочечников, наблюдается головная боль, тошнота, боль в брюшной полости, головокружение, анорексия, слабость, изменения настроения, летаргия, повышение температуры тела, миалгия, артралгия, ринит, конъюнктивит, болевой синдром кожи, потеря массы тела. В более тяжёлых случаях — тяжёлые психические нарушения и повышение внутричерепного давления, стероидный псевдоревматизм у пациентов с ревматизмом, летальный исход.
Реакции на месте введения: боль, жжение, изменение пигментации (депигментация, лейкодерма), атрофия кожи, стерильные абсцессы, редко — липоатрофия.
Со стороны костно-мышечной системы: проксимальная миопатия, остеопороз, разрыв сухожилий, мышечная слабость, атрофия, миопатия, переломы позвоночника и длинных костей, асептический остеонекроз.
Со стороны мочевыделительной системы: повышение риска образования уролитов и содержание лейкоцитов и эритроцитов в моче без явного повреждения почек.
Общие: недомогание, стойкая икота при применении препарата в высоких дозах, недостаточность надпочечников, что приводит к артериальной гипотензии, гипогликемия и летальные исходы в стрессовых ситуациях, таких как хирургическое вмешательство, травма или инфекция, если доза преднизолона не увеличена.
При резкой отмене препарата возможны синдром отмены, тяжесть симптомов зависит от степени атрофии надпочечников, наблюдается головная боль, тошнота, боль в брюшной полости, головокружение, анорексия, слабость, изменения настроения, летаргия, повышение температуры тела, миалгия, артралгия, ринит, конъюнктивит, болевой синдром кожи, потеря массы тела. В более тяжёлых случаях — тяжёлые психические нарушения и повышение внутричерепного давления, стероидный псевдоревматизм у пациентов с ревматизмом, летальный исход.
Реакции на месте введения: боль, жжение, изменение пигментации (депигментация, лейкодерма), атрофия кожи, стерильные абсцессы, редко — липоатрофия.
Условия хранения
Хранить в оригинальной упаковке для защиты от действия света при температуре не выше 25°C. Хранить в недоступном для детей месте.
Лунное лицо: причины и лечение
Если ваше лицо постепенно опухло до округлой формы, у вас может быть лунное лицо. Также называется лунным лицом, это обычно несерьезно. Но это может заставить вас чувствовать себя неловко.
Лунная фация возникает, когда по бокам лица накапливается лишний жир. Это часто связано с ожирением, но может быть связано с синдромом Кушинга. Вот почему люди иногда называют это внешностью кушингоидов. Синдром Кушинга возникает, когда организм в течение длительного времени подвергается воздействию высоких уровней гормона кортизола.
Симптомы и причины лунных фаций
Лунные фации могут привести к постепенному округлению, полноте или отечности лица. Боковые стороны лица могут стать настолько круглыми из-за скопления жира, что уши не будут видны спереди. Отложения жира по бокам черепа также могут сделать лицо более круглым.
Высокий выброс гормонов, особенно кортизола, является причиной лунного лица. Это называется гиперадренокортикализмом или гиперкортизолизмом. Надпочечники, железы треугольной формы, расположенные над почками, выделяют кортизол.
Состояния, связанные с лунными фациями
Состояния, которые чаще всего приводят к гиперкортизолизму и симптому лунных фаций, включают:
- Повышенное высвобождение гормона (АКТГ) из гипофиза; АКТГ побуждает надпочечники вырабатывать кортизол.
- Негипофизарные опухоли, такие как опухоли легких, поджелудочной железы или тимуса, которые также могут вызывать большие выбросы АКТГ
- Доброкачественные опухоли или рак надпочечников
- Долгосрочное использование стероидных препаратов, таких как преднизон, для лечения состояний например, ревматоидный артрит или другие аутоиммунные заболевания
Чтобы подтвердить, что лунная фация является результатом аномального уровня кортизола, ваш врач может провести анализы крови и мочи.Чтобы подтвердить причину высокого уровня кортизола, вам могут потребоваться другие тесты, такие как МРТ или компьютерная томография.
Лунная фация и синдром Кушинга
Диагностировать синдром Кушинга бывает сложно. Это потому, что такие признаки и симптомы, как отек лица, могут быть вызваны другими заболеваниями. Но более вероятно, что это будет синдром Кушинга, если лунное лицо будет постепенно ухудшаться вместе с другими характерными симптомами.
Продолжение
Например, жир также может постепенно накапливаться в задней части шеи, живота или туловища, но ноги и руки часто остаются тонкими.Этот тип центрального ожирения является наиболее частым признаком синдрома Кушинга.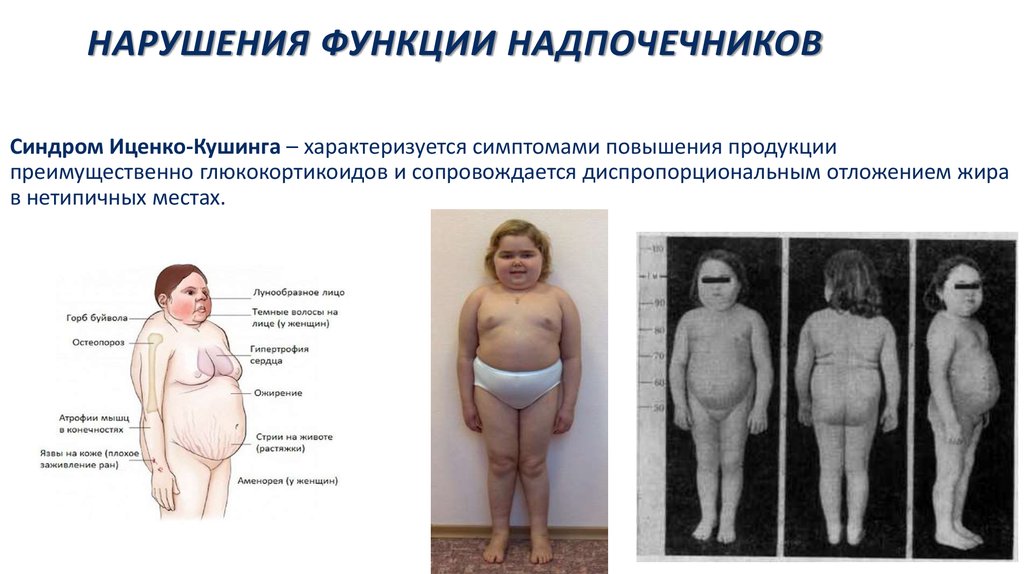 Однако, если вы сидите на диетах или много занимаетесь спортом, у вас может быть небольшой набор веса или он не прибавится вовсе, или лунное лицо может быть очень незначительным.
Однако, если вы сидите на диетах или много занимаетесь спортом, у вас может быть небольшой набор веса или он не прибавится вовсе, или лунное лицо может быть очень незначительным.
Лечение синдрома Кушинга зависит от того, что его вызывает. В некоторых случаях хирург может удалить опухоль. В других случаях могут помочь лекарства, лучевая терапия или физиотерапия.
Лунная фация и лечение стероидами
Длительное употребление стероидов, таких как преднизон, может вызвать многие из тех же признаков и симптомов синдрома Кушинга.Хотя миллионы американцев принимают эти типы лекарств, многие другие могут пострадать от лунных фаций, но не знают их причины.
Фактически, увеличение веса с перераспределением жира, такое как лунные фации, является одним из наиболее распространенных признаков употребления стероидов. Ваш риск развития этих признаков зависит от дозы лекарств и от того, как долго вы их принимаете. При приеме стероидов увеличение аппетита и приема пищи может способствовать увеличению веса.
Продолжение
Симптомы обычно возникают в результате длительного приема пероральных стероидов.Но реже инъекционные или вдыхаемые стероиды также могут вызывать симптомы и симптомы Кушинга.
Лучший способ уменьшить влияние симптомов — уменьшить дозу лекарства или полностью отменить его, но никогда не следует делать это самостоятельно. Если вам нужно продолжить его использование, ваш врач попросит вас попробовать минимальную эффективную дозу. Например, прием лекарства через день может иногда уменьшить кушингоидные изменения. Если это не помогает устранить фацию луны и другие симптомы, ваш врач может предложить попробовать другие виды лечения.
Синдром / болезнь Кушинга — причины, симптомы, диагностика и лечение
| Синдром / болезнь Кушинга | Американская ассоциация неврологических хирургов |
Синдром Кушинга — это заболевание, вызванное чрезмерным воздействием на организм гормона кортизола. Кортизол влияет на все ткани и органы тела. Эти эффекты вместе известны как синдром Кушинга.
Кортизол влияет на все ткани и органы тела. Эти эффекты вместе известны как синдром Кушинга.
Синдром Кушинга может быть вызван чрезмерным употреблением препаратов кортизола, как это наблюдается при лечении хронической астмы или ревматоидного артрита (ятрогенный синдром Кушинга), избыточной выработкой кортизола опухолью в надпочечнике или других частях тела (эктопический синдром Кушинга) или опухоль гипофиза, секретирующего адренокортикотропный гормон (АКТГ), который стимулирует чрезмерную выработку кортизола надпочечниками (болезнь Кушинга).
Кортизол — это нормальный гормон, вырабатываемый внешней частью надпочечников. При правильном функционировании кортизол помогает организму реагировать на стресс и изменения. Он мобилизует питательные вещества, изменяет реакцию организма на воспаление, стимулирует печень к повышению уровня сахара в крови и помогает контролировать количество воды в организме. Производство кортизола регулируется АКТГ, вырабатываемым гипофизом.
Распространенность синдрома Кушинга
- По оценкам, ежегодно поражается 10-15 человек на миллион человек.
- Аденомы гипофиза (болезнь Кушинга) составляют более 70 процентов случаев у взрослых и около 60-70 процентов случаев у детей и подростков.
- Синдром Кушинга чаще всего поражает взрослых в возрасте от 20 до 50 лет и чаще встречается у женщин, составляя около 70 процентов всех случаев.
Основные причины
Аденомы гипофиза — болезнь Кушинга
Аденомы гипофиза — это доброкачественные опухоли гипофиза, которые секретируют повышенное количество АКТГ, вызывая чрезмерное производство кортизола.У большинства пациентов наблюдается одиночная аденома. Болезнь Кушинга, впервые описанная в 1912 году нейрохирургом Харви Кушингом, доктором медицины, в его книге Гипофиз и его расстройства , является наиболее частой причиной спонтанного синдрома Кушинга, составляя 60-70 процентов всех случаев.
Внематочный синдром АКТГ
Некоторые доброкачественные или злокачественные (раковые) опухоли, возникающие за пределами гипофиза, могут продуцировать АКТГ. Это состояние известно как синдром эктопического АКТГ.Опухоли легких (злокачественные аденомы или карциноиды) вызывают более 50 процентов этих случаев. Другими менее распространенными типами опухолей, которые могут продуцировать АКТГ, являются тимомы, опухоли островковых клеток поджелудочной железы и медуллярные карциномы щитовидной железы.
Опухоли надпочечников
Аномалия надпочечников, например опухоль надпочечников, может вызвать синдром Кушинга. Большинство этих случаев связаны с доброкачественными опухолями, называемыми аденомами надпочечников, которые выделяют избыток кортизола в кровь.
Адренокортикальные карциномы или рак надпочечников — наименее частая причина синдрома Кушинга. Раковые клетки секретируют избыточный уровень нескольких гормонов коры надпочечников, включая кортизол и андрогены надпочечников. Карциномы надпочечников часто вызывают очень высокий уровень гормонов и быстрое проявление симптомов.
Семейный синдром Кушинга
Большинство случаев синдрома Кушинга не являются генетическими. Однако у некоторых людей может развиться синдром Кушинга из-за наследственной тенденции к развитию опухолей одной или нескольких желез внутренней секреции.При первичной пигментной микронодулярной болезни надпочечников у детей или молодых людей развиваются небольшие кортизол-продуцирующие опухоли надпочечников. При множественной эндокринной неоплазии I типа (МЭН I) могут возникать гормон-секретирующие опухоли паращитовидных желез, поджелудочной железы и гипофиза. Синдром Кушинга у мужчин I типа может быть вызван опухолью гипофиза, внематочной опухолью или опухолью надпочечников.
Признаки и симптомы, связанные с синдромом / болезнью Кушинга:
- Увеличение веса лица (лунное лицо)
- Прибавка в весе над ключицей (надключичная жировая подушечка)
- Прибавка в весе на затылке (буйволиный горб)
- Кожные изменения с легкими синяками на конечностях и появлением лиловых растяжек (стрий), особенно в области живота или подмышечной области
- Красный, круглое лицо (полнокровие)
- Центральное ожирение с увеличением веса, сосредоточенным в области груди и живота, с тонкими руками и ногами
- Чрезмерный рост волос (гирсутизм) на лице, шее, груди, животе и бедрах
- Облысение у женщин
- Общая слабость и утомляемость
- Расплывчатое зрение
- Головокружение
- Слабость мышц
- Нарушения менструального цикла у женщин (аменорея)
- Снижение фертильности и / или полового влечения (либидо)
- Гипертония
- Плохое заживление ран
- Сахарный диабет
- Тяжелая депрессия
- Экстремальные перепады настроения
Диагностика
Диагноз синдрома Кушинга основан на клиническом подозрении в сочетании с обзором истории болезни пациента, физическим осмотром и лабораторными тестами, чтобы помочь определить наличие чрезмерного уровня кортизола. Пациент с подозрением на синдром Кушинга должен изначально иметь внешний вид, указывающий на избыточное производство кортизола в сочетании с повышенной 24-часовой экскрецией кортизола с мочой. При оценке физических особенностей синдрома Кушинга часто бывает полезно сравнить старые и недавние фотографии, чтобы выявить классические изменения лица и тела, связанные с этим расстройством.
Пациент с подозрением на синдром Кушинга должен изначально иметь внешний вид, указывающий на избыточное производство кортизола в сочетании с повышенной 24-часовой экскрецией кортизола с мочой. При оценке физических особенностей синдрома Кушинга часто бывает полезно сравнить старые и недавние фотографии, чтобы выявить классические изменения лица и тела, связанные с этим расстройством.
Следующие тесты могут помочь определить, есть ли чрезмерный уровень продуцирования кортизола:
- Суточный тест на кортизол в моче измеряет количество кортизола, вырабатываемого в моче в течение всего дня.Уровни выше 50-100 мкг в день у взрослого человека предполагают наличие синдрома Кушинга. Хотя у большинства пациентов с синдромом Кушинга уровень кортизола повышен, становится все более очевидным, что многие пациенты с легкой формой синдрома Кушинга также могут иметь нормальный уровень кортизола, что приводит к нескольким 24-часовым сборам мочи для подтверждения диагноза.
- Тест на подавление низких доз дексаметазона измеряет реакцию надпочечников на АКТГ и широко используется в течение четырех десятилетий.Он включает в себя прием небольшой дозы кортизолоподобного препарата, дексаметазона (1 мг), в 23:00, а затем взятие крови на анализ на кортизол на следующее утро. У пациентов без синдрома Кушинга утренний уровень кортизола обычно очень низкий, что указывает на подавление секреции АКТГ вечерней дозой дексаметазона. У пациентов с синдромом Кушинга утренний уровень кортизола будет высоким. Очевидно, что нормальные пациенты подавляют свой кортизол до очень низкого уровня (1.8 мг / дл), в то время как страдающие синдромом Кушинга — нет. Используя этот строгий критерий, этот тест должен обеспечить оценочную диагностическую точность 95–97 процентов. Однако некоторые пациенты с легкой формой синдрома Кушинга могут подавлять свой кортизол до низкого уровня, что затрудняет полную диагностику с помощью этого теста.

- Ночной тест на кортизол слюны — относительно новый тест, который проверяет повышенный уровень кортизола в слюне между 11 часами дня.м. и полночь. Секреция кортизола поздно ночью обычно очень низкая, но у пациентов с синдромом Кушинга уровень всегда будет повышенным в это время. Для сбора слюны необходимы специальные пробирки; тем не менее, это простой тест для пациентов, который можно проводить несколько раз. Нормальный уровень кортизола в ночной слюне практически исключает диагноз синдрома Кушинга. При правильном проведении этот тест должен обеспечивать оценочную диагностическую точность 93–100%.
После постановки окончательного диагноза необходимо определить источник. Первым шагом к выявлению первопричины является измерение уровня АКТГ. Пациенты с опухолями, секретирующими АКТГ, будут иметь нормальный или повышенный уровень АКТГ. Напротив, у пациентов с избытком кортизола надпочечников уровень кортизола будет ниже нормы. В этой ситуации может оказаться полезным проведение теста на подавление высоких доз дексаметазона. Этот тест, аналогичный тесту на подавление низких доз дексаметазона, предполагает прием высокой дозы дексаметазона (8 мг) в 11 ч.м. затем на следующее утро сдают кровь на анализ на наличие кортизола. У здоровых пациентов утренний уровень кортизола снова будет очень низким. Пациенты с опухолями гипофиза также будут снижать уровень кортизола в сыворотке, но пациенты с опухолями надпочечников будут поддерживать высокий уровень выработки кортизола. Высокий уровень кортизола указывает на негипофизарный источник.
Несмотря на описанные выше тесты, отличить гипофиз от опухоли, не секретирующей АКТГ, может быть сложно с диагностической точки зрения.Большинство пациентов с опухолями, секретирующими АКТГ, имеют поражение гипофиза, которое часто бывает очень маленьким.
Рекомендуются следующие тесты:
- Магнитно-резонансная томография (МРТ) гипофиза с повышением содержания гадолиния является рекомендуемым подходом.
 Когда очевидная опухоль гипофиза (> 5 мм) идентифицируется с помощью МРТ, дальнейшая диагностическая оценка может не потребоваться в зависимости от клинической картины. Однако около 50 процентов пациентов будут иметь «нормальную» МРТ гипофиза, а у 10 процентов — случайные опухоли, не связанные с производством АКТГ.В таких случаях МРТ не даст точного диагноза, и потребуются дополнительные тесты.
Когда очевидная опухоль гипофиза (> 5 мм) идентифицируется с помощью МРТ, дальнейшая диагностическая оценка может не потребоваться в зависимости от клинической картины. Однако около 50 процентов пациентов будут иметь «нормальную» МРТ гипофиза, а у 10 процентов — случайные опухоли, не связанные с производством АКТГ.В таких случаях МРТ не даст точного диагноза, и потребуются дополнительные тесты. - Взятие пробы каменной пазухи — это тест, используемый для определения источника секреции АКТГ, и его следует проводить только после подтверждения диагноза синдрома Кушинга. АКТГ и другие гормоны гипофиза, вырабатываемые гипофизом, попадают в кровоток путем дренирования через вены, называемые нижними каменистыми пазухами. Для выполнения этой процедуры катетер помещается в обе вены одновременно, и кровь отбирается на АКТГ до и после введения кортикотропин-высвобождающего гормона (CRH), а также с двух-, пяти- и 10-минутными интервалами.Этот инвазивный метод должен выполняться в медицинском центре профессиональным медиком, имеющим большой опыт в этой процедуре. При правильном проведении этот тест должен обеспечивать оценочную диагностическую точность 95–98 процентов.
Лечение синдрома Кушинга
Лечение синдрома Кушинга зависит от первопричины избыточного кортизола, но, возможно, может включать хирургическое вмешательство, лучевую терапию, химиотерапию или использование препаратов, ингибирующих кортизол.Если причина является ятрогенной из-за длительного использования глюкокортикоидных гормонов для лечения другого заболевания, врач постепенно снижает дозу вводимого извне стероида до самой низкой дозы, достаточной для контроля этого расстройства. После установления контроля дозу глюкокортикоидных гормонов можно вводить через день, чтобы уменьшить побочные эффекты для пациента.
Лечение болезни Кушинга
Микрохирургическая резекция аденомы гипофиза, секретирующей АКТГ, является оптимальным методом лечения болезни Кушинга с коэффициентом излечения 80-90 процентов в случае обнаружения опухоли.Чаще всего операция проводится через трансназальный транссфеноидальный доступ, при котором не остается видимого рубца. Этот тип хирургии может быть выполнен по желанию хирурга с использованием минимально инвазивного операционного микроскопа или эндоскопа. Частичное удаление гипофиза (субтотальная гипофизэктомия) может использоваться у пациентов без четко идентифицируемых аденом.
У пациентов, у которых после операции не наступила ремиссия, можно использовать различные лекарства, которые могут подавлять выработку кортизола, например:Эти агенты не так эффективны, как хирургическое вмешательство, и считаются курсом лечения второй линии.У некоторых пациентов, которые особенно устойчивы ко всем формам терапии, может быть рассмотрен вариант двустороннего удаления надпочечников (двусторонняя адреналэктомия).
После операции, при успешном удалении опухоли, продукция АКТГ падает ниже нормы. Это снижение является естественным и временным, и пациентам назначают синтетическую форму кортизола, такую как гидрокортизон или преднизон, чтобы компенсировать это изменение. Большинство пациентов могут прекратить заместительную терапию в течение 6–12 месяцев, но другим может потребоваться прием пероральных стероидов в течение нескольких лет, возможно, в течение всей жизни.Пациентам, которым требуется операция на надпочечниках, также может потребоваться заместительная стероидная терапия.
Одним из дополнительных вариантов лечения пациентов, которые потерпели неудачу при хирургических вмешательствах или которые с медицинской точки зрения слишком высоки, чтобы довести их до операции, является лучевая терапия. Лучевая терапия, которую вводят в гипофиз в течение шестинедельного периода, дала улучшение у 40-50 процентов взрослых и до 85 процентов детей.
Стереотаксическая радиохирургия также оказалась эффективным методом лечения пациентов с аденомами гипофиза, секретирующими АКТГ.Недавнее исследование продемонстрировало эндокринную ремиссию у 54 процентов пациентов и контроль роста опухоли у 96 процентов. Однако необходимо постоянное наблюдение для отслеживания роста опухоли, рецидива заболевания, развития дефицита новых гормонов и повреждения зрительных путей и головного мозга.
Синдром Кушинга / Ресурсы по болезни
AANS не одобряет какие-либо виды лечения, процедуры, продукты или врачей, упомянутые в этих информационных бюллетенях о пациентах.Эта информация предоставляется в качестве образовательной услуги и не предназначена для использования в качестве медицинской консультации. Любой, кому нужен конкретный нейрохирургический совет или помощь, должен проконсультироваться со своим нейрохирургом или найти его в своем районе с помощью онлайн-инструмента AANS «Найди сертифицированного нейрохирурга».
Синдром Кушинга — NHS
Синдром Кушинга — это состояние, вызванное наличием в организме слишком большого количества гормона кортизола. Это может быть серьезно, если не лечить.
Кто и почему получает
Синдром Кушинга встречается редко. В основном это поражает людей, которые долгое время принимали стероидные препараты, особенно стероидные таблетки. Стероиды содержат синтетическую версию кортизола.
Очень редко это может быть вызвано организмом, вырабатывающим слишком много кортизола.
Обычно это результат:
- рост (опухоль) в гипофизе в головном мозге
- опухоль в 1 надпочечнике над почками
Опухоли обычно не злокачественные (доброкачественные) .Чаще всего они встречаются у молодых женщин.
Симптомы синдрома Кушинга
Симптомы синдрома Кушинга могут возникать внезапно или постепенно. Если их не лечить, они имеют тенденцию к медленному ухудшению.
Одним из основных признаков является увеличение веса и увеличение количества жира в организме, например:
- увеличение жира на груди и животе, но тонкие руки и ноги
- скопление жира на задней части шеи и плеч , известный как «буйволиный горб»
- красное, пухлое, округлое лицо
Другие симптомы включают:
- кожа, на которой легко появляются синяки
- большие фиолетовые растяжки
- слабость в плечах и бедрах
- уменьшенная сексуальное влечение (низкое либидо) и проблемы с фертильностью
- депрессия и перепады настроения
Синдром Кушинга также может вызывать высокое кровяное давление, которое может быть серьезным, если его не лечить.
Когда обращаться за медицинской помощью
Обратитесь к терапевту, если у вас есть симптомы синдрома Кушинга, особенно если вы принимаете стероиды.
Не прекращайте прием лекарств без консультации с врачом.
Многие вещи могут вызывать симптомы, похожие на синдром Кушинга, поэтому рекомендуется пройти обследование, чтобы выяснить, в чем проблема.
Тесты и диагностика
Ваш врач может заподозрить синдром Кушинга, если у вас есть типичные симптомы и вы принимаете стероидные препараты.
Если вы не принимаете стероиды, диагностика может быть затруднена, поскольку симптомы могут быть аналогичны другим состояниям.
При подозрении на синдром Кушинга количество кортизола в вашем теле можно измерить по:
Если эти тесты показывают высокий уровень кортизола, вас могут направить к специалисту по гормональным заболеваниям (эндокринологу) для подтверждения или решения синдром Кушинга.
Вам также могут потребоваться другие тесты или сканирование, чтобы выяснить причину.
Лечение синдрома Кушинга
Синдром Кушинга обычно проходит после лечения, хотя для полного выздоровления может потребоваться много времени.
Лечение зависит от причины.
Если это вызвано приемом стероидов:
- ваша доза стероидов будет постепенно снижаться или прекращаться
Если это вызвано опухолью , лечение может включать:
- операция по удалению опухоли
- лучевая терапия для уничтожения опухоли
- лекарства для уменьшения воздействия кортизола на ваш организм
Поговорите со своим врачом о преимуществах и рисках различных вариантов лечения.
Дополнительная информация
Узнайте больше о синдроме Кушинга и основных методах лечения от Pituitary Foundation
Последняя проверка страницы: 25 марта 2021 г.
Срок следующей проверки: 25 марта 2024 г.
Синдром Кушинга | DermNet NZ
Автор: Ванесса Нган, штатный писатель, 2005 г.
Что такое синдром Кушинга?
Синдром Кушинга — это гормональное заболевание, вызванное длительным воздействием чрезмерно высоких уровней глюкокортикоидных (также называемых кортизолом) гормонов в плазме.Глюкокортикоидные гормоны поддерживают регуляцию глюкозы, подавляют иммунный ответ и высвобождаются как часть реакции организма на стресс. Производство кортизола из коры надпочечников регулируется небольшой железой прямо под мозгом, называемой гипофизом.
Существует несколько причин синдрома Кушинга:
- Гиперплазия надпочечников (разрастание коры надпочечников), вторичная по отношению к гипофизу гиперпродукции адренокортикотропного гормона (АКТГ)
- Доброкачественные или злокачественные опухоли надпочечников, выделяющие избыток глюкокортикоидов в кровь
- Внематочный синдром АКТГ — секреция АКТГ злокачественными или доброкачественными опухолями, возникающими в структурах, отличных от гипофиза или надпочечников
- Введение экзогенных стероидов — обычно в результате приема высоких доз системных кортикостероидов, таких как преднизон, при заболеваниях, вызывающих образование пузырей, астме, артрите и других воспалительных заболеваниях.
Кто подвержен риску синдрома Кушинга?
Наиболее частой причиной синдрома Кушинга является прием экзогенных глюкокортикоидов в течение нескольких месяцев или дольше.
Синдром Кушинга, вызванный опухолью надпочечников или гипофиза, поражает женщин в пять раз чаще, чем мужчин, и чаще всего возникает в возрасте от 25 до 40 лет.
Каковы признаки и симптомы синдрома Кушинга?
Наиболее отличительными чертами синдрома Кушинга являются отложения жира на ключицах и задней части шеи (буйволиный горб), округлое пухлое лицо (лунное лицо, лицо томата) с контрастирующими тонкими истощенными конечностями.Кости ослаблены, и такие действия, как сгибание, подъем или вставание со стула, могут привести к болям в спине, переломам ребер и позвоночника. Многие люди страдают от сильной усталости, слабых мышц, высокого кровяного давления, высокого уровня сахара в крови, раздражительности, беспокойства и депрессии.
Признаки и симптомы, появляющиеся на коже, включают:
- Легкие синяки (пурпура) и фиолетовые стрии на коже на животе, ягодицах и бедрах
- Телеангиэктатические щеки (сломанные капилляры)
- Хрупкая кожа и плохое заживление ран
- Угри и гирсутизм (чрезмерный рост волос у женщин на лице, шее, груди, животе и бедрах)
- У женщин также может быть гипертрофия клитора и облысение по мужскому типу
Синдром Кушинга
Как ставится диагноз?
Хотя диагноз синдрома Кушинга может быть установлен клинически, важно подтвердить его и объяснить его причины.Лабораторные тесты могут включать:
- Кортизол сыворотки, измеренный в определенное время дня или ночи
- Тест на кортизол в слюне, обычно проводится поздно ночью
- Кортизол в суточной моче для определения общего производства кортизола
- Тест на подавление дексаметазона: дексаметазон должен подавлять секрецию кортизола, но этого не происходит при синдроме Кушинга
- Тест на стимуляцию кортикотропином (АКТГ): АКТГ должен стимулировать выработку кортизола, но при синдроме Кушинга ответа может не быть
Визуализация для определения местонахождения опухоли может включать компьютерную томографию, МРТ или ультразвук.
Как лечить синдром Кушинга?
Лечение зависит от причины избытка глюкокортикоидов и может включать хирургическое вмешательство, лучевую терапию, химиотерапию или лекарственную терапию.
| Причина | Лечение |
|---|---|
| Введение экзогенных стероидов |
|
| Опухоли гипофиза |
|
| Опухоли надпочечников |
|
| Синдром эктопического АКТГ |
|
Лекарства, ингибирующие глюкокортикоидные гормоны (например, митотан), иногда могут использоваться в сочетании с вышеуказанными методами лечения.
Болезнь Кушинга: MedlinePlus Genetics
Генетическая причина болезни Кушинга часто остается неизвестной.Лишь в нескольких случаях было обнаружено, что мутации в определенных генах приводят к болезни Кушинга. Эти генетические изменения называются соматическими мутациями. Они приобретаются человеком при жизни и присутствуют только в определенных клетках. Участвующие гены часто играют роль в регулировании активности гормонов.
Болезнь Кушинга вызывается повышением уровня гормона кортизола, который помогает поддерживать уровень сахара в крови, защищает организм от стресса и останавливает (подавляет) воспаление. Кортизол вырабатывается надпочечниками — маленькими железами, расположенными в верхней части каждой почки.Производство кортизола запускается высвобождением гормона, называемого адренокортикотропным гормоном (АКТГ), из гипофиза, расположенного в основании мозга. Надпочечники и гипофиз являются частью гормональной (эндокринной) системы организма, которая регулирует развитие, обмен веществ, настроение и многие другие процессы.
Болезнь Кушинга возникает, когда доброкачественная (доброкачественная) опухоль, называемая аденомой, формируется в гипофизе, вызывая чрезмерное высвобождение АКТГ и, как следствие, повышенное производство кортизола.Длительное воздействие повышенного уровня кортизола приводит к появлению признаков и симптомов болезни Кушинга: изменение количества и распределения жира в организме, уменьшение мышечной массы, ведущее к слабости и снижению выносливости, истончение кожи, вызывающее растяжки и легкие синяки, как следствие, истончение костей. при остеопорозе — повышенное кровяное давление, нарушение регуляции уровня сахара в крови, ведущее к диабету, ослабленная иммунная система, неврологические проблемы, нерегулярные менструации у женщин и замедление роста у детей.Гиперактивные надпочечники, вырабатывающие кортизол, также могут вырабатывать повышенное количество мужских половых гормонов (андрогенов), что приводит к гирсутизму у женщин. Влияние избытка андрогенов на мужчин неясно.
Чаще всего болезнь Кушинга возникает сама по себе, но редко она проявляется как симптом генетических синдромов, характерных чертой которых являются аденомы гипофиза, таких как множественная эндокринная неоплазия 1 типа (MEN1) или семейная изолированная аденома гипофиза (FIPA).
Болезнь Кушинга — это разновидность более крупного состояния, называемого синдромом Кушинга, которое возникает, когда уровень кортизола повышается по одной из нескольких возможных причин.Иногда аденомы, которые возникают в органах или тканях, отличных от гипофиза, например аденомы надпочечников, также могут увеличивать выработку кортизола, вызывая синдром Кушинга. Некоторые лекарства, отпускаемые по рецепту, могут вызвать увеличение выработки кортизола и привести к синдрому Кушинга. Иногда продолжительные периоды стресса или депрессии могут вызвать повышение уровня кортизола; когда это происходит, состояние известно как синдром псевдо-Кушинга. Не считая увеличения кортизола из-за отпускаемых по рецепту лекарств, аденомы гипофиза вызывают подавляющее большинство синдрома Кушинга у взрослых и детей.
Сара Хайланд начинает серьезно относиться к преднизону «Лунное лицо»
Современная семья Звезда Сара Хайланд открыто рассказывала о своем опыте с дисплазией почек, состоянием, которое вызывает аномальное развитие почек, и о том факте, что она перенесла трансплантация почки в 2012 году. Теперь она делится с фанатами информацией о «лунном лице», отеках, вызванных преднизоном, одним из лекарств, которые она теперь должна принимать регулярно.
В субботу Хайленд разместила в Instagram видео с историями о своем уходе за кожей, сообщает The Mighty.Сначала она показала поклонникам сыворотку для лица, которой любит пользоваться. Затем она достала валик для массажа лица и сказала: «Я использую эту штуку, чтобы выкатить лицо. Не знаю, работает это или нет ». Затем она объяснила, что ей нравится «выкатывать лицо» из-за преднизона, который она принимает.
Преднизон — синтетический стероидный гормон, имитирующий действие кортизола, гормона, который вырабатывается естественным путем, Джеймс Дж. Галлиган, доктор философии, профессор фармакологии и токсикологии и директор программы нейробиологии в Университете штата Мичиган, говорит СЕБЕ.«Преднизон чаще всего используется в качестве противовоспалительного препарата, поскольку он подавляет иммунную систему», — объясняет он, добавляя, что люди, перенесшие трансплантацию почки, часто принимают препарат, чтобы предотвратить отторжение пересаженной почки их иммунной системой.
К сожалению, преднизон имеет множество побочных эффектов, и некоторые из них серьезны.
«Когда мы используем преднизон, мы всегда думаем о том, как быстро избавить людей от него и как использовать наименьшее количество», — Линн М.Людмер, доктор медицины, ревматолог из Балтиморского медицинского центра милосердия, рассказывает SELF. Клиника Мэйо объясняет, что его можно назначать при многих состояниях, включая тяжелые аллергические реакции, астму, артрит и волчанку.
Побочные эффекты включают то, что пациенты называют «лунным лицом», что в основном выражается в сильном отеке лица. «При длительном приеме преднизона у людей действительно опухают щеки», — говорит доктор Людмер. Но опухоль не ограничивается только щеками — у некоторых пациентов появляется так называемый «буйволиный горб» у основания шеи.По словам доктора Галлигана, ни один из этих эффектов не является вредным, «но [они] могут вызвать у пациента чувство социального дискомфорта, поскольку его внешний вид заметно меняется».
Другие побочные эффекты могут быть более серьезными. По словам доктора Галлигана, люди часто теряют мышечную массу, когда принимают преднизон в течение длительного периода времени, а подавление иммунной системы может сделать пациентов восприимчивыми к инфекции. «Преднизон также может вызывать беспокойство у некоторых пациентов и проблемы со сном», — говорит он.По словам доктора Людмера, у некоторых пациентов может развиться остеопороз, если они принимали препарат в течение нескольких месяцев, а также могут возникнуть проблемы с артериальным давлением и сахаром в крови.
Многие из вредных побочных эффектов преднизона могут проявиться уже через несколько недель приема препарата, говорит доктор Людмер, поэтому врачи серьезно относятся к его назначению. «Это не леденец, — говорит доктор Людмер. «Это то, что нужно контролировать».
Хотя катание на лице теоретически имеет смысл как средство от отека, на самом деле это вряд ли поможет.
Доктор Людмер говорит, что это первый раз, когда она слышала об этом как о возможном способе избавиться от отека лица, связанного с преднизоном. «Вряд ли это будет очень полезно, — говорит доктор Галлиган. Это потому, что отек — это продукт преднизона, который фактически изменяет распределение жира в организме человека, что может привести к тому, что у кого-то будет больше жира на лице, объясняет он. Использование валика по этой области позволит массировать жир, но не избавит от него навсегда.
Как я лечил болезнь Кушинга до, во время и после постановки диагноза
Всем привет!
На этой неделе я хочу перейти к более личному.Многие читатели спрашивали, как я боролся с болезнью Кушинга. Итак, я хочу поделиться с вами этой частью моей истории.
Я в 2014 году. (Фото Катарины Луро-Матос)В некотором смысле справиться с болезнью Кушинга стало легче, когда мне поставили диагноз. Прежде чем я узнал, что такое Кушинг, я думал, что схожу с ума. В течение почти двух лет я продолжала набирать вес, регулярно ходя в спортзал и хорошо питаясь. Не было объяснения или веской причины, почему это происходило. Однако после встречи со своим эндокринологом все обрело смысл.
В октябре 2014 года я начал все время невероятно уставать. В январе 2015 года я заметила небольшую выпуклость внизу живота. В то время я не особо об этом думал, но после того, как мне поставили диагноз в августе 2016 года, эти события в моей жизни начали обретать смысл. Эта крошечная выпуклость продолжала расти и расти, и мое истощение вышло на совершенно новый уровень. Я не мог спать по ночам, и мне всегда было жарко и потно.
Январь 2015 года, когда я заметил появление выпуклости. Очень маленькая, но все же разница, которую я заметилПеренесемся вперед с января 2015 года по октябрь 2015 года.Мой кишечник становился больше, и у меня были прыщи на груди, спине и лице. У меня никогда не было проблем с прыщами, поэтому я подумал, что это странно. Я также начал отращивать много волос по бокам лица, живота и поясницы. Люди начали предлагать мне восковую депиляцию, а я не спрашивал их мнения — как будто мои волосы на лице лично их беспокоили. Конечно, от этого мне стало плохо. Менеджер на прежней работе даже посоветовал мне купить лекарство Аккутан (изотретиноин) от прыщей на груди. Этот комментарий продолжал беспокоить меня, пока я не получил свой диагноз.
К июню 2016 года у меня было полное лунное лицо, и мой кишечник как-то все еще продолжал расти. Я не влез ни в какую одежду. Моя память была расстреляна. У меня все болело. И мне посчастливилось спать по три часа каждую ночь. В этот момент я чувствовал себя потерянным, безнадежным и напуганным.
Октябрь 2015 г. (Фото Катарины Луро-Матос)Все, что происходило со мной, не прекращалось, независимо от того, сколько диет я придерживался чувствительных к пище, сколько упражнялся или как сильно я хотел, чтобы все это прошло. далеко.Мне казалось, что я схожу с ума. Люди вокруг меня не могли поверить в это. Некоторые сомневались, что я соблюдаю диету или занимаюсь спортом. Мне стало стыдно, и я ненавидел показывать свое лицо и тело на публике. Я пойду на работу, а потом пойду домой. Я больше никуда не ходил.
Все изменилось, когда я встретил своего эндокринолога, который упомянул болезнь Кушинга. Я быстро обыскал этот термин сразу после выхода из его офиса. Я знал, что это то, что у меня было. До того, как он объяснил это, и до того, как он обсудил разницу между синдромом поликистозных яичников (СПКЯ) и болезнью Кушинга (СПКЯ — это то, о чем думал мой натуропат), все мои фибры говорили мне, что у меня синдром Кушинга.
Конечно, было страшно. Но официальный диагноз 15 августа 2016 года принес мне облегчение. С моих плеч упал огромный груз. Я знал, что у меня болезнь Кушинга, и я знал, что это была опухоль гипофиза. Мое отношение полностью изменилось, и после постановки диагноза я стал более позитивным человеком.
С декабря 2015 г. по декабрь 2016 г., за месяц до операции. (Фото Катарины Луро-Матос)Позитивность и честность с окружающими в отношении моей ситуации — вот как я справился с ситуацией Кушинга.До постановки диагноза мне было стыдно, поэтому я был негативен и постоянно подавлен. Большинство людей удивляются тому, что я перестал быть негативным, потому что, когда они слышат мою историю, они предполагают, что в той ситуации они были бы негативными.
Позитивное отношение к себе было невероятно важным и, по словам моих врачей, главной причиной, по которой я чувствую себя хорошо. Я была рада диагнозу, прекрасным докторам и возможности снова жить жизнью после операции и длительного выздоровления. Путь к операции и выздоровлению был долгим и нелегким.

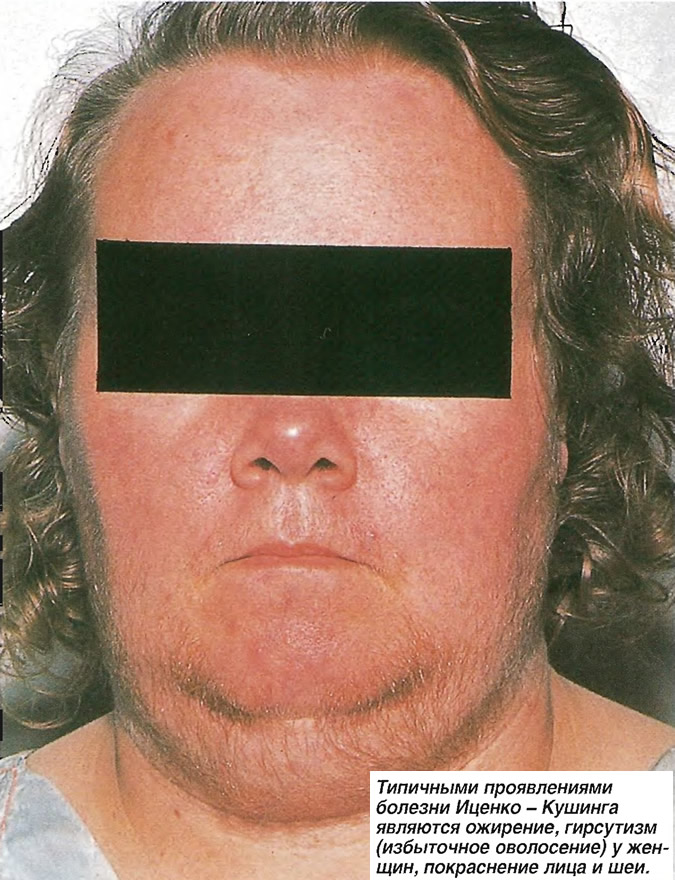 Такой симптом у женщин достаточно просто визуализировать, так как при этом сильно меняется ее внешний вид: обильные жировые отложения на лице, шее, груди и животе. Значительная прибавка массы тела – самый первый и частый симптом синдрома Кушинга. Удивительно то, что руки и ноги при таких жировых отложениях достаточно худые и даже могут уменьшаться в объеме. Особенно значительные жировые складки находятся на шее и на затылке. Крайне редки случаи, когда жировые отложения отсутствуют.
Такой симптом у женщин достаточно просто визуализировать, так как при этом сильно меняется ее внешний вид: обильные жировые отложения на лице, шее, груди и животе. Значительная прибавка массы тела – самый первый и частый симптом синдрома Кушинга. Удивительно то, что руки и ноги при таких жировых отложениях достаточно худые и даже могут уменьшаться в объеме. Особенно значительные жировые складки находятся на шее и на затылке. Крайне редки случаи, когда жировые отложения отсутствуют.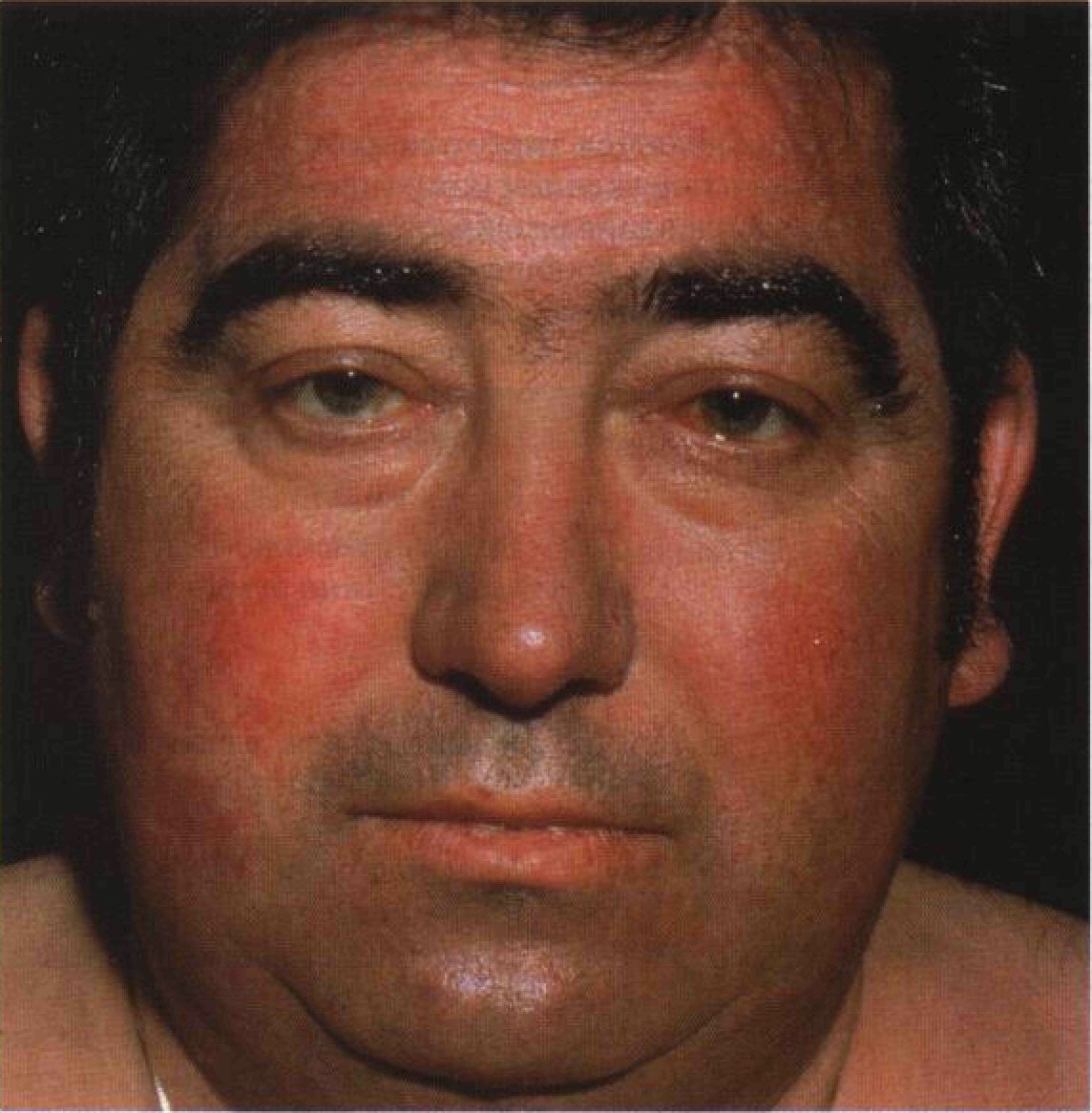 Крайне редко может встречаться такой симптом синдрома кушинга, как вирилизация – появление в облике женщины мужских черт. Обычно, оно проявляется при раке надпочечников.
Крайне редко может встречаться такой симптом синдрома кушинга, как вирилизация – появление в облике женщины мужских черт. Обычно, оно проявляется при раке надпочечников. Это происходит из-за того, что при повышенной концентрации глюкокортикоидов в организме, в моче наблюдается избыток кальция. Как ни странно, но диагностировать синдром Кушинга у некоторых женщин случалось именно из-за его обращения к врачу в связи с жалобами на колики в почках.
Это происходит из-за того, что при повышенной концентрации глюкокортикоидов в организме, в моче наблюдается избыток кальция. Как ни странно, но диагностировать синдром Кушинга у некоторых женщин случалось именно из-за его обращения к врачу в связи с жалобами на колики в почках.
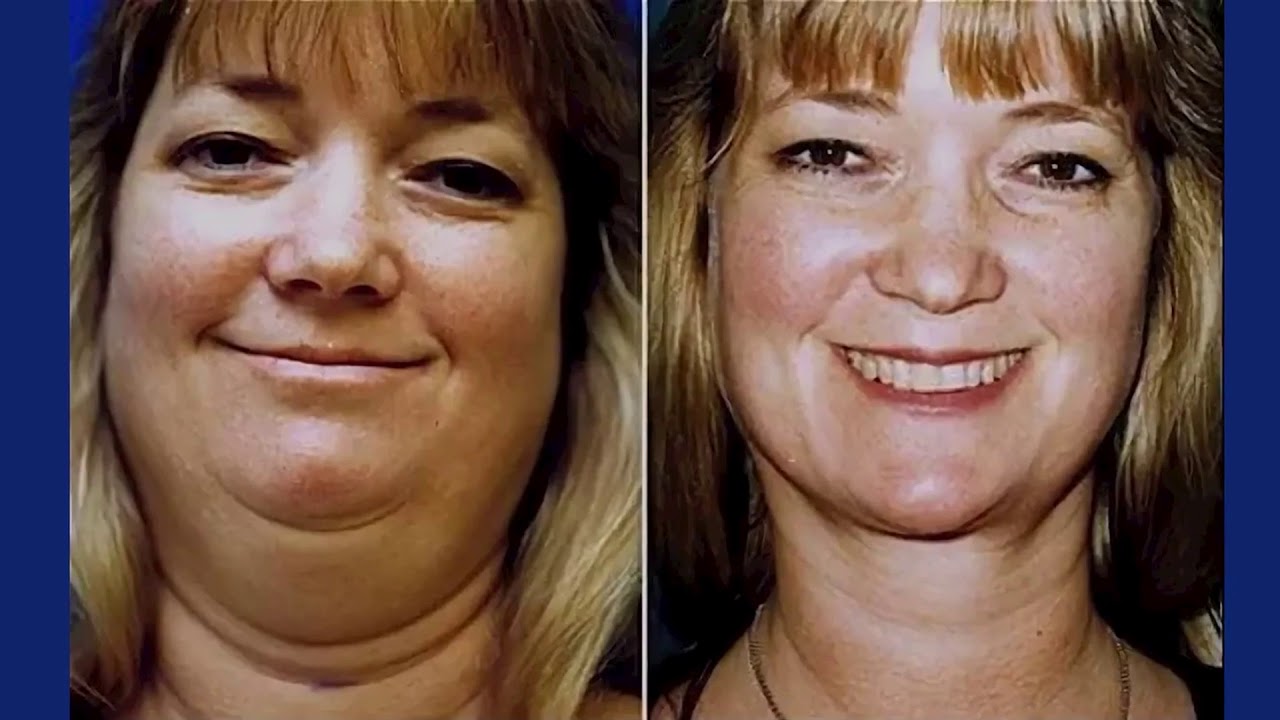
 Когда очевидная опухоль гипофиза (> 5 мм) идентифицируется с помощью МРТ, дальнейшая диагностическая оценка может не потребоваться в зависимости от клинической картины. Однако около 50 процентов пациентов будут иметь «нормальную» МРТ гипофиза, а у 10 процентов — случайные опухоли, не связанные с производством АКТГ.В таких случаях МРТ не даст точного диагноза, и потребуются дополнительные тесты.
Когда очевидная опухоль гипофиза (> 5 мм) идентифицируется с помощью МРТ, дальнейшая диагностическая оценка может не потребоваться в зависимости от клинической картины. Однако около 50 процентов пациентов будут иметь «нормальную» МРТ гипофиза, а у 10 процентов — случайные опухоли, не связанные с производством АКТГ.В таких случаях МРТ не даст точного диагноза, и потребуются дополнительные тесты.