Лейкоплакия голосовых связок: Охриплость голоса — хрипота — полип голосовые связки — ВПЧ папиллом гортани — голосовые связки Лейкоплакия — рак горла — Pavlos Tsolaridis, M.D. — Хирург
Рак голосовых связок – Лечение в Киеве – Стоимость операции
Рак голосовых связок
Рак голосовых связок – одна из разновидностей карциномы гортани. Голосовые связки расположены в срединном отделе гортани и отвечают за тональность, тембр и звучность голоса. Возникновению рака голосовых связок более подвержены мужчины, нежели женщины. Средний возраст пациентов с опухолями голосовых связок составляет от 40 до 65 лет.
Существует две ключевых причины развития рака голосовых связок — паппиломы слизистой гортани, или папилломатоз (в большинстве случаев врожденное заболевание), а также дисплазии слизистой гортани. Причинами возникновения второго является воздействие внешних факторов, таких как курение табака и употребление спиртных напитков.
В отличие от рака верхнего отдела гортани, рак голосовых связок отмечается низкой степенью агрессивности. Опухоль развивается постепенно и характеризуется локальным характером, не особо быстро распространяется на лимфатические узлы и другие ткани шейного отдела.
Лечение
Радиохирургическая система КиберНож позволяет лечить опухоли даже самых труднодоступных для традиционной хирургии локализаций
Традиционно, для лечения рака голосовых связок, выявленного на ранней стадии, применялась хирургия, предусматривающая удаление пораженной связки.
Особенностью хирургического лечения опухолей голосовых связок является высочайшая сложность операции. Последствиями такого вмешательства с большой долей вероятности становятся потеря голоса, вкуса, частично — обоняния и слуха. Поэтому хирургическое лечение этого вида рака оправдано в случае значительного распротсранения опухоли, угрожающей жизненным функциям организма.
На ранних стадиях альтернативой операции в лечении данного заболевания является бескровное радиохирургическое лечение на системе КиберНож
.С помощью технологии Кибернож (CyberKnife) лучевой терапевт получает в свое распоряжение высокоточный инструмент, который разрушает опухоль, останавливая биологические процессы в ее клетках путем воздействия высоких (абляционных) доз ионизирующего излучения.
Точность подведения каждого из лучей излучения, на пересечении которых формируется высокая доза, составляет доли миллиметра. Такая точность в сочетании с системой контроля положения опухоли и коррекции подачи каждого отдельного пучка в соответствии с движением опухоли, позволяет лечить рак голосовых связок с минимальным воздействием на окружающие ткани.
Если после хирургического лечения пациент зачастую теряет голос, то после лечения на КиберНоже (при условии небольшого размера опухоли) в большинстве случаев речевая функция сохраняется.
К сожалению, рак голосовых связок редко диагностируется на ранней стадии, поэтому в статистике большая часть пациентов с таким диагнозом получили сочетанное лечение на основе
Технология IMRT, также как и КиберНож позволяет создавать зоны высокой дозы ионизирующего облучения, в т.ч. сложной пространственной формы, соответствующие форме и размеру опухолевого поражения при раке гортани.
Чем отличается лучевая терапия IMRT от менее точных методов лучевого лечения?
Зоны высокой дозы ионизирующего излучения произвольной пространственной формы при IMRT складывается из доз пересекающихся полей излучения заданной формы (автоматически задается мультилепестковым коллиматором), что позволяет доставлять требуемое количество облучения точно в границы опухоли, независимо от сложности ее формы, а также моделировать формы полей и общей зоны таким образом, чтобы исключить облучение критических структур организма (например, при лечении рака голосовых связок — это спинной мозг, слюнные железы, мышцы гортани и т.д.), а также минимизировать до безопасных значений дозу радиации для здоровых тканей, которые расположены на пути каждого из полей облучения.
Пространственная форма зон с различным размером разрешенной дозы (от нулевой до максимальной) устанавливается на 3d-модели, сформированной из массива снимков КТ- и МРТ-диагностики, а размеры доз для каждой из областей (защищаемые «холодные зоны», опухоль, здоровые ткани) назначает врач в соответствии с мировыми протоколами.-Step-17-Version-2.jpg)
План лечения на линейном ускорителе, с распределением доз облучения для различных типов биологических тканей
После задания параметров лечения, медицинский физик в специальном программном комплексе сформирует план подачи множества полей излучения, в котором каждое поле будет иметь уникальную форму и положение, из которого будет доставляться излучение. Далее пациенту предстоит пройти, в среднем, 20-30 ежедневных фракций (сеансов) лучевой терапии.
Лечение на линейном ускорителе проходит амбулаторно, нет необходимости в анестезии, во время фракций (сеансов) пациент удобно располагается на специальном столе, а подвижная часть линейного ускорителя поочередно занимает различные позиции, подавая дозы ионизирующего излучения пучками, точно повторяющими форму опухоли.
Перед каждым сеансом проводится точная укладка и сверка положения пациента, его голова его фиксируется индивидуальной маской, исключающей смещение от первоначального положения. После окончания фракции пациент может вернуться к привычному графику своего дня.
Как назначается лечение при раке голосовых связок?
Как и любое лечение в онкологии, лечение рака голосовых связок будет определено после проведения междисциплинарного консилиума, на котором будут рассмотрены все аспекты конкретного случая заболевания: расположение, распространение опухоли, объем поражения и прочее, а также будет избрана тактика лечения: объем, последовательность, состав методов, его стоимость.
Диагностика
Ввиду глубокого залегания гортани, точность визуального обследования голосовых связок можно достичь при фиброларингоскопии (эндоскопическом исследовании гортани). Поэтому чаще всего, при первичном подозрении на развитие опухолевого процесса голосовых связок (например, у семейного врача или ЛОР-специалиста) назначаются компьютерная томография (КТ) и магнитно-резонансная томография (МРТ). Также, ввиду невысокой стоимости исследования и его неинвазивности, проводят УЗИ лимфоузлов, в которые могут распространяться метастазы.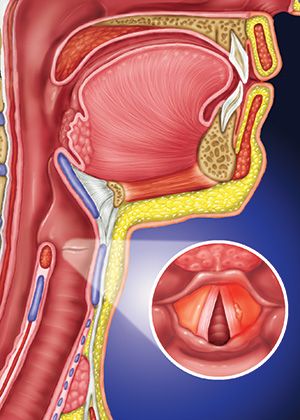
Заключительным этапом диагностики, подтверждающим тип новообразования, является биопсия (забор образца ткани опухоли), для последующего лабораторного исследования.
Симптомы
На ранних стадиях заболевания симптомы могут быть схожи с симптомами простуды и инфекционных заболеваний, это в частотности, осиплость и появление хрипоты в голосе, а также продолжительный кашель, что и так свойственно курильщикам, это усложняет задачу раннего выявления патологического процесса.
По мере роста опухоли, на более поздних стадиях заболевания, симптомы рака голосовых связок могут включать:
- ощущение инородного тела в горле;
- свистящее дыхание;
- болезненные ощущения при глотании;
- общую слабость и быструю утомляемость.
ABC-медицина
Раком горла называют злокачественную опухоль в пределах гортани и глотки. На долю этого заболевания приходится порядка 3 % случаев формирования всех злокачественных опухолей у человека.
Локализация опухоли
В гортани выделяется 3 отдела: надсвязочный, связочный и подсвязочный. Раковая опухоль чаще всего поражает надсвязочный отдел (65 % случаев), причем данный вид новообразования – самый злокачественный: быстро развивается и рано метастазирует. Опухоль на голосовых связках встречается в 32 % случаев и несколько менее опасна. Подсвязочный отдел гортани поражается раком реже всего (3 % случаев), однако новообразование часто развивается в подслизистом слое, что способствует более позднему обнаружению.
Причины
Как и для всех остальных форм рака, причины злокачественной опухоли горла до сих пор точно не установлены. Однако врачи выявили целую группу факторов, способных повысить вероятность развития заболевания.
- Курение (подавляющее число больных являются злостными курильщиками).
- Употребление алкогольных напитков.
- Работа в неблагоприятных условиях (запыленность, повышенная температура, повышенное содержание в атмосфере табачного дыма, нефтепродуктов, бензола, сажи, фенольных смол).

- Наличие предраковых состояний (лейкоплакии слизистой оболочки гортани, пахидермии, кисты гортанных желудочков).
- Наличие хронических воспалительных процессов.
Симптомы
Конкретные признаки рака горла зависят от локализации опухоли, а также от формы ее роста.
- Рак надскладочного отдела проявляется болями при глотании, иррадиирующими в ухо на стороне поражения.
- По мере роста новообразования появляется ощущение инородного тела в горле.
- Один из самых ярко проявляющихся симптомов – боль. Из-за нее пациент сокращает прием пищи, что приводит к истощению организма.
- К опухолевому процессу присоединяется воспаление окружающих тканей.
- При заполнении опухолевыми массами голосовых связок появляется и нарастает охриплость, вплоть до потери голоса;
- При поражении просвета гортани обнаруживается затруднение дыхания. Распад опухоли проявляется кровохарканьем и гнилостным запахом изо рта.

Лечение
Хирургическая операция. Она проводится обычно при небольших размерах опухоли на начальных (1 и 2) стадиях заболевания. Объем удаленной ткани зависит от степени поражения. На 3 и 4 стадиях резекция гортани (удалении ее части) или ларингэктомия (полное удаление) проводятся только после облучения всей шеи.
Лучевая терапия. Облучение основной опухолевой массы проводят совместно с метастазами. Такое лечение противопоказано, если наблюдаются серьезные поражения близлежащих тканей (перихондрит хрящей, прорастание опухоли в пищевод, кровеносные сосуды, появление обширных регионарных и отдаленных метастазов) или больной находится в тяжелом состоянии.
Для диагностики и выработки тактики лечения рака горла Вы можете обратиться к врачам-онкологам клиники «ABC-Медицина». Если у Вас возникли вопросы о наших услугах или Вы хотите записаться на прием к врачу, звоните нам по телефону в Москве +7 (495) 223-38-83.
Рак голосовых связок
Рак голосовых связок – одна из форм злокачественного заболевания гортани. Встречается чаще у мужчин среднего и старшего возраста. В Израиле патологию диагностируют на ранних этапах, что позволяет применять щадящие методики. Средняя пятилетняя выживаемость – около 60-80%, а при локализованных формах – больше 85-90%.
Встречается чаще у мужчин среднего и старшего возраста. В Израиле патологию диагностируют на ранних этапах, что позволяет применять щадящие методики. Средняя пятилетняя выживаемость – около 60-80%, а при локализованных формах – больше 85-90%.
Причины и статистика
Основным фактором риска при развитии этой формы рака считается курение. На голосовые связки и гортань регулярно попадают ароматические углеводы и нитрозамины, которые под влиянием ряда ферментов превращаются в канцерогенные вещества. По некоторым данным, вероятность возникновения рака голосовых связок у курящий зависит от активности энзимов, обусловленной генетически.
В меньшей мере эту опухоль гортани связывают с алкоголем. Но злоупотребление спиртными напитками нередко сочетается с сигаретами, что усугубляет проблему. Около 90% случаев рака голосовых связок связано с этими двумя факторами.
Определенную роль в развитии рака голосового аппарата играют вирусы простого герпеса (ВПГ) и папилломы (ВПЧ). Папилломатоз, вызванный ВПЧ 16 и 18 серотипов, у 1-3% больных переходит в плоскоклеточный рак. Также рассматривается негативное влияние на голосовые связки и гортань химических веществ – полициклических ароматических углеводов, формальдегида, асбеста, кремнезема, угольной пыли.
Папилломатоз, вызванный ВПЧ 16 и 18 серотипов, у 1-3% больных переходит в плоскоклеточный рак. Также рассматривается негативное влияние на голосовые связки и гортань химических веществ – полициклических ароматических углеводов, формальдегида, асбеста, кремнезема, угольной пыли.
Рак голосовых связок занимает 60% от всех карцином гортани (встречаются в среднем у 3 человек на 100 000 населения). Существует четкая половая корреляция и разница между регионами. Соотношение заболеваемости мужчин и женщин – 7,1:1, а смертности – 2,6:0,3. В некоторых странах есть тенденция к увеличению количества опухолей гортани среди представительниц слабого пола (приблизительно на 2% в год).
Высокая частота рака голосовых связок среди мужчин афроамериканцев, жителей Южной, Восточной и Центральной Европы (10 на 100 000 населения). В Израиле заболеваемость 4,8/100 000 среди мужчин и 0,82/100 000 среди женщин, наблюдается медленная тенденция к снижению. Выявляется опухоль голосовых связок после 40 лет, у более молодых она крайне редкая.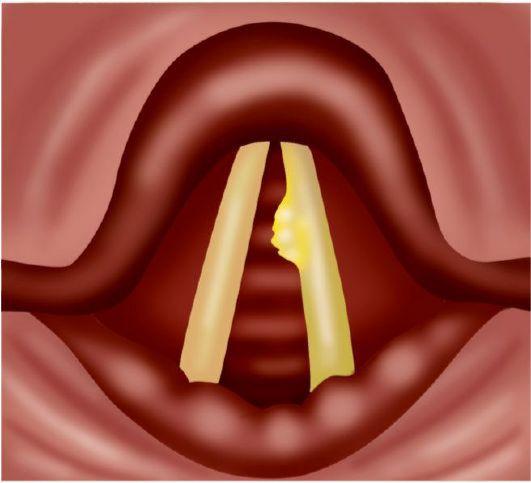 В Британии ¾ диагнозов выставляют пациентам, старше 60 лет.
В Британии ¾ диагнозов выставляют пациентам, старше 60 лет.
Узнать точную стоимость лечения
Симптомы заболевания
Начальным признаком рака голосовых связок является дисфония. Сначала голос пропадает эпизодически, затем симптом становится устойчивым. Кроме этого пациенты с опухолью голосового аппарата предъявляют такие жалобы:
- Дискомфорт при глотании
- Навязчивый кашель
- Боли и першение в горле
- Ощущение инородного тела в гортани
- Боли в ушах
- Одышка и шумное дыхание
- Кровохарканье
Появление таких симптомов, как одышка, кровохарканье, говорит о запущенности процесса и поздних стадиях рака голосовых связок.
Важно значение предраковых состояний в гортани, переходящих в злокачественные формы. Они характеризуются изменениями в клетках (увеличение ядерно-плазматического соотношения, числа митозов) и эпителиальной ткани. К ним относятся:
- Гиперемический ларингит
- Эритроплакия
- Псевдомикседематозный гипертрофический ларингит
- Кератоз
- Лейкоплакия
- Дисплазия
- Папилломатоз
Стадии
По гистологическому строению выделяют следующие типы рака голосовых связок:
- Плоскоклеточный (90%)
- Сосочковый
- Веретенообразноклеточный
Редко встречаются железистоклеточный тип рака, саркома, лимфома и нейроэндокринные опухоли, локализованные в голосовых связках.
Рак голосовых связок разделяют на стадии согласно американской классификации AJCC. Она учитывает систему баллов TNM, где T – опухоль, N – задействованные лимфоузлы, M – метастазы.
0 стадия (TinsN0M0)
Опухоль не выходит за базальную мембрану эпителия, лимфоузлы не задействованы, метастазов нет.
I стадия (T1N0M0)
Опухоль прорастает через базальный слой, но связки остаются подвижными.
II стадия (T2N0M0)
Задействованы обе связки (они остаются подвижными) или близлежащие ткани гортани.
III стадия (T3N0M0)
Связки становятся неподвижными, либо процесс распространяется за пределы гортани, на любой близлежащий отдел шеи (щитовидный хрящ, надгортанник).
III стадия (T3N1M0)
Любой тип опухоли с задействованием лимфатического узла на одной половине шеи, с диаметром до 3 см.
IVA стадия (T4аN0M0)
Прорастание опухолью щитовидного хряща, трахеи, щитовидной железы, пищевода.
IVA стадия (T4N1M0)
Та же ситуация с вовлечением узла на половине шеи, с диаметром до 3 см.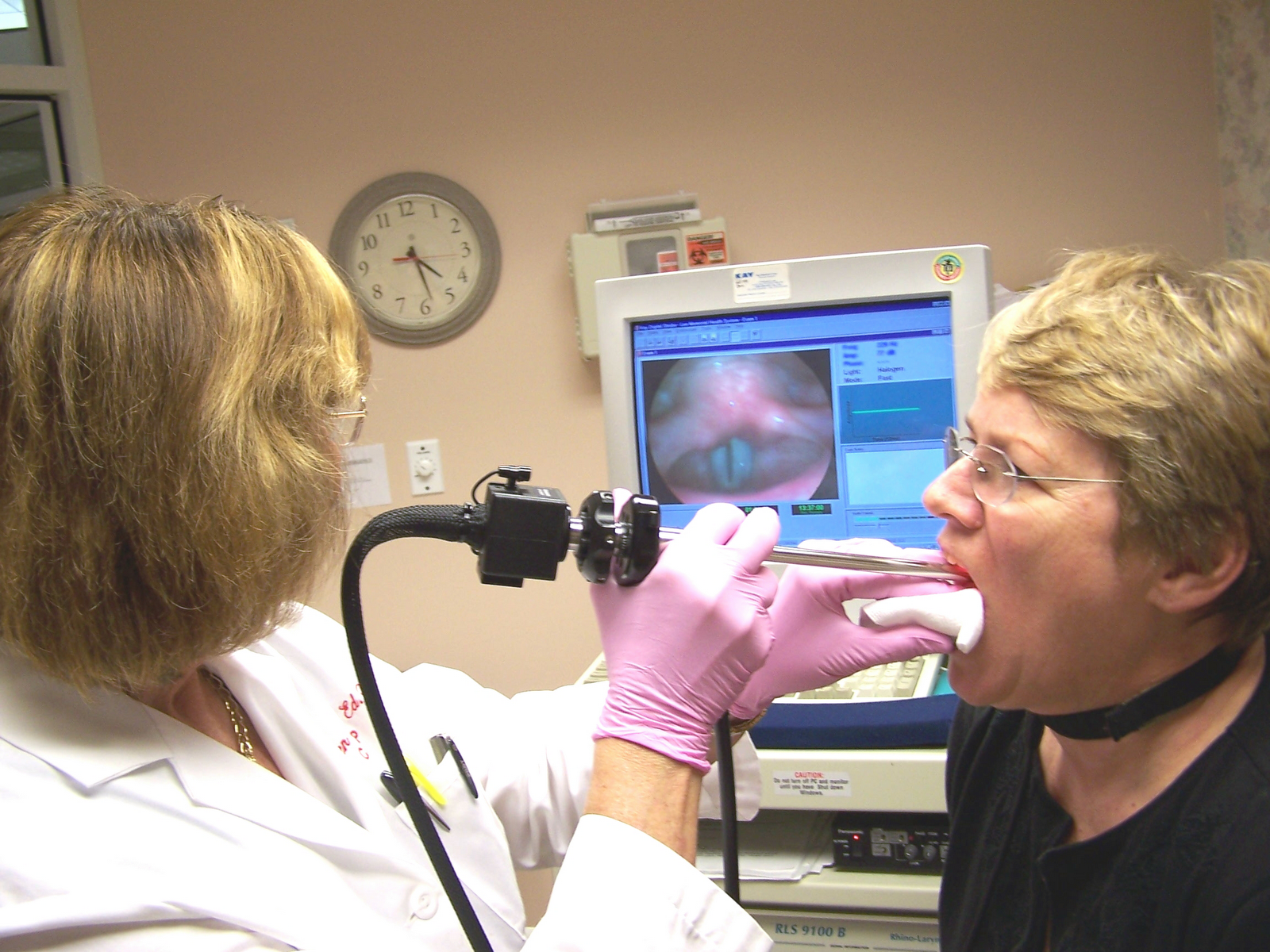
IVA стадия (T1- 4аN2M0)
Любая стадия опухоли. Поражение одного или нескольких лимфоузлов с диаметром 3-6 см по одну сторону шеи. Включение в процесс узла на противоположной половине, с диаметром до 6 см.
IVB стадия (T4вNлюбойM0)
Карцинома из гортани прорастает в пространство возле позвоночника, сонной артерии или легких.
IVB стадия (TлюбойN3M0)
Задействованный лимфоузел превышают 6 см, либо процесс выходит за его пределы.
IVC стадия (TлюбойNлюбойM1)
Метастазы опухоли
Методы диагностики рака голосовых связок в Израиле
Подозрение на рак в гортани, если пациент жалуется на постепенное исчезновение голоса, боль и дискомфорт в горле и гортани, навязчивый кашель. В первую очередь такие симптомы настораживают у курильщиков с длительным стажем.
Чтобы поставить правильный онкологический диагноз в Израиле проводят ряд обследований:
- Осмотр гортани с помощью зеркал
- Ларингоскопию (твердым и гибким ларингоскопом)
- КТ с контрастом и без него
- МРТ
- ПЭТ-томографию
- УЗИ гортани
- Рентгенографию
Эти методы диагностики рака голосовых связок используются в комплексе. Сейчас в Израиле для выявления пораженных узлов и метастазов при МРТ пробуют использовать контраст USPIO (суперпарамагнитный оксид железа), покрытый декстраном. Он поглощается клетками ретикуло-эндотелиальной системы, что позволяет визуализировать патологические процессы в гортани.
Сейчас в Израиле для выявления пораженных узлов и метастазов при МРТ пробуют использовать контраст USPIO (суперпарамагнитный оксид железа), покрытый декстраном. Он поглощается клетками ретикуло-эндотелиальной системы, что позволяет визуализировать патологические процессы в гортани.
Перед началом терапии рака голосовых связок в клиниках Израиля также назначают:
- Клинический анализ крови
- Печеночные пробы
- Ионограмму
- Креатинин
- Мочевину
- Коагулограмму
- ЭКГ и ЭхоКГ
Стоимость диагностики
| Cтоимость диагностики | $ |
|---|---|
| Профессор Флисс, лор – консультация (Prof. Fliss, ENT – consultation) | от 650 |
| Анализы крови, включая онкомаркеры (Blood test (oncological pack)) | 635 |
| ПЭТ-КТ (PET-CT) | 1470 |
Узнать точную стоимость диагностики
Гарантированный ответ в течение 30 минут
Методы и стоимость лечения рака голосовых связок в Израиле
Для удаления опухоли на голосовых связках в Израиле используются такие техники:
- Хордэктомия (субэпителиальная, сублигаментарная, субмускулярная, тотальная, расширенная).

- Гемиларингоэктомия (вертикальная, антериальная).
- Ларингэктомия (над перстневидным хрящом, полная).
Чем больше пораженный опухолью участок гортани, тем вмешательство радикальнее. В современной хирургии в Израиле все чаще используются щадящие неинвазивные операции:
- СО₂-лазерная деструкция
- KTP-лазер (с применением титанилфосфата калия)
- Радиотерапия
Эти методы сохраняют пациенту связки, наносят минимальные повреждения тканям гортани. Если степень распространения процесса не предусматривает щадящей операции, в Израиле делается пластика голосового аппарата, помогающая восстановить звукообразование. После нее пациентам проводится реабилитация.
Сейчас в Израиле изучаются новые способы хирургии опухоли:
- Трансоральная робототехническая (TORS). Вмешательство с помощью роботов, управляемых хирургом.
- Видеоларингоскопическая (TOVS). Тонкие инструменты вводят под контролем видеотехники. Подходит для высечения мелких структур.

При обширном поражении опухолью голосовых связок (Т3-Т4), вовлечении в процесс внутренних органов, используется химиотерапия. Она показана также пациентам, отказавшимся от ларингоэктомии по поводу рака. Иногда удается уменьшить объем пораженного участка и сохранить голосовые связки. Чаще всего в протоколах используют таксаны, цисплатин и 5-фторурацил.
Исследования показали, что злокачественные клетки имеют увеличенное количество рецепторов к эпидермальному фактору роста. В качестве вспомогательной терапии рака голосовых связок в Израиле пробуют использовать их ингибиторы – нинотузумаб, пембрулизумаб, ниволумаб, ипилимумаб. Они усиливают цитостатический эффект основных химиотерапевтических препаратов.
Прогноз
На этапе Т1 во многих клиниках Израиля удается добиться у 85-95% пациентов с раком голосовых связок пятилетней продолжительности жизни. При стадии рака Т2 показатель 60-94% (после лучевой терапии – 60-85%, частичной резекции классическим способом – 70-94%, СО₂-лазера – 70-85%). При стадии рака Т3 абсолютная выживаемость 50-60%, при Т4 – 30-40%.
При стадии рака Т3 абсолютная выживаемость 50-60%, при Т4 – 30-40%.
Преимущества лечения в Израиле
Первый медицинский центр Тель-Авива – одна из лучших клиник Израиля по лечению рака голосовых связок и гортани. Стаж работы ЛОР-специалистов больше 15 лет. Они проходили обучение в самом Израиле, Европе и США.
Здесь практикуется щадящая хирургия для максимального сохранения тканей гортани и голосовых связок, часто с применением лазера. Массивные резекции завершаются пластикой для максимального возобновления работы голосового аппарата. Сотрудники изучают последние научные достижения в лечении рака и вводят их в свою практику.
Основные преимущества лечения рака голосовых связок в Израиле:
- Высокоточная диагностика
- Наличие новейшей аппаратуры для проведения хирургических процедур
- Качественная пластика гортани после вмешательства
- Применение оптимальных протоколов химиотерапии и радиотерапии
- Своевременное выявление и коррекция осложнений
- Разумная ценовая политика
- Оптимальные условия пребывания в стационаре
Стоимость лечения
| Cтоимость лечения | $ |
|---|---|
| Химиотерапия 1 курс, включая дневной стационар | от 850 |
| Лучевая терапия (стоимость 1 поля) | от 180 |
Узнать точную стоимость лечения
Гарантированный ответ в течение 30 минут
Выбор врача
Диагностикой и хирургией рака голосовых связок занимает ЛОР. Для проведения химиотерапии и радиотерапии вам могут понадобиться врачи соответствующей квалификации. При наличии сопутствующих болезней вы сможете получить необходимые консультации. Выбрать подходящего специалиста в Израиле вам поможет координатор.
Для проведения химиотерапии и радиотерапии вам могут понадобиться врачи соответствующей квалификации. При наличии сопутствующих болезней вы сможете получить необходимые консультации. Выбрать подходящего специалиста в Израиле вам поможет координатор.
Получить помощь в подборе специалиста
Гарантированный ответ в течение 30 минут
Предраковые заболевания гортани
Предраковое заболевание, предраковое состояние или предрак гортани – понятие собирательное, так как оно включает несколько нозологических форм.
Изучение предракового состояния заслуживает большого внимания, оставаясь чрезвычайно важной проблемой в оториноларингологии. Своевременное выявление предракового процесса может, в известной степени, предрешать развитие злокачественного образования и, в некоторой степени объясняет причины, условия возникновения и роста опухоли гортани
По классификации предраковые заболевания гортани делятся на две большие группы: облигатный и факультативный предрак.
Облигатные предраковые заболевания гортани – это заболевания, с течением времени обязательно переходящие в злокачественное заболевание гортани. К ним относятся: хронический гиперпластический ларингит, дискератозы (лейкоплакия, лейкокератоз, пахидермия и т.д.), папилломатоз гортани (в зависимости от типа вируса).
Факультативные предраковые заболевания гортани – заболевания, малигнизация которых возможна, но не является обязательной. К ним относятся: контактные гранулемы, рубцовые изменения гортани. Особое внимание следует обратить на случаи, когда заболевание сопровождается дисплазией слизистой оболочки (т.е. цитологическими и структурными изменениями эпителия).
В ФГБУ НМИЦ оториноларингологии ФМБА России обследование пациентов с предраковыми заболеваниями гортани провят специалисты научно-клинического отдела заболеваний гортани под руководством д.м.н. Нажмутдинова И.И. Всем пациентам проводится общеклиническое обследование (ОА крови, мочи, биохимия крови, ЭКГ, Rg ОГК).
Основным методом диагностики является визуальный осмотр методом непрямой эндоскопической виеоларингоскопии. При выраженном рвотном рефлексе или иных технических сложностях, проводится осмотр гибким волоконнооптическим фиброскопом. Важную роль в обследовании пациентов выполняет аутофлюоресцентная диагностика.
При необходимости проводится взятие биопсии для гистологической верификации и определения степени дисплазии.
Пациенты должны знать, что в группе риска предраковых заболеваний гортани находятся курящие пациенты, работники «голосовых» профессий (педагоги, певцы и т.д., а также люди, имеющие постоянный контакт с пылью.
Медикаментозная терапия является первым этапом лечения данных пациентов, проводятся различные виды ингаляций (щелочно-масляные, с глюкокортикостероидами) и вливание в гортань растворов глюкокортикостероидов (гидрокортизон и пр.). Консервативная терапия проводится в срок не более 2, максимум 3 недель, отсутствие клинического эффекта является прямым показанием к хирургическому лечению.
Хирургическое лечение делится на две группы :
1. Удаление образования «холодным» микроинструментом (щипчики, выкусыватели, щейвер и т.д.). Преимуществом этого метода является относительная дешевизна, возможность использования под местной анестезией. К минусам данного метода можно отнести недостаточный контроль за объемом удаляемой ткани, который привдит как к повреждению голосовой связки и необратимому изменению голоса, так и к неполному удалению измененных тканей.
2. Удаление образования с использованием различного типа лазеров (различного вида диодные лазеры, СО2 лазер, PDL и KTP лазеры, NdYag лазер и т.д.). «Золотым стандартом» в мировой практике является применение СО2 лазера.
Послеоперационное ведение пациентов заключается в соблюдении голосового режима на срок до недели, а также противоотечной терапии (внутривенное и эндоларингеальное введение растворов глюкокортикостероидов). Антибактериальная терапия, как правило, не показана.
К особым группам пациентов относятся беременные женщины, люди пожилого возраста, пациенты с сопутствующей патологией.
Все пациенты с данной патологией после хирургического лечения наблюдаются в течение 3 месяцев. Больные с гистологически подтвержденной дисплазией эпителия II и III степени нуждаются в обязательном диспансерном наблюдении на срок до 5 лет.
Лучшие врачи эксцизионной хирургии лейкоплакии в больнице Фортис Ноида
Нужна помощь в выборе правильного врача
Получите помощь в вашем лечении от нашей опытной команды!
Чтобы преодолеть ограничения, связанные с вирусом короны, мы предлагаем платные теле / видео консультации от ведущих врачей. Сообщите нам, если вы заинтересованы, и мы свяжемся с вами.
Выберите СтрануАфганистанАландские островаАлбанияАлжирАмериканское СамоаАндорраАнголаАнгильяАнтарктидаАнтигуа и БарбудаАргентинаАрменияАрубаАвстралияАвстрияAZERBAIJANБагамские островаБахрейнБангладешБарбадосБеларусьБельгияБелизБенинБермудские островаБутанБоливияБосния и ГерцеговинаБотсванаОстров БувеБразилияБританская территория Индийского океанаБританские Виргинские островаБрунейБолгарияБуркина-ФасоБурундиКамбоджаКамерунКанадаКабо-ВердеКарибский НидерландыКаймановы островаЦентрально-Африканская РеспубликаЧадЧилиКитайОстров РождестваКокосовые (Килинг) островаКолумбияКоморские островаКонго (Браззавиль)Конго (Киншаса)Острова КукаКоста-РикаХорватияКубаКюрасаоКипрЧешская РеспубликаДанияДжибутиДоминикаДоминиканская РеспубликаЭквадорЕгипетСальвадорЭкваториальная ГвинеяЭритреяЭстонияЭфиопияФолклендские островаФарерские островаФиджиФинляндияФранцияФранцузская ГвианаФранцузская ПолинезияЮжные Французские ТерриторииГабонГамбияГрузияГерманияГанаГибралтарГреции-ГренландияГренадаГваделупаГуамГватемалашерстяная фуфайкаГвинеяГвинея-БисауГайанаГаитиОстров Херд и острова МакдональдГондурасГонконг, КитайВенгрияИсландияИндияИндонезияИранИракИрландияОстров МэнИзраильИталияКот-д’ИвуарЯмайкаЯпонияДжерсиДжорданРеспублика КазахстанКенияКирибатиКувейтКиргизстан ЛаосЛатвииЛиванЛесотоЛиберияЛивияЛихтенштейнЛитваЛюксембургМакао, КитайМакедонияМадагаскарМалавиМалайзияМальдивыМалиМальтаМаршалловы островаМартиникаМавританияМаврикийМайоттаМексикаМикронезияМолдоваМонакоМонголияЧерногорияМонсерратМароккоМозамбикМьянмаНамибияНауруНепалНидерландыНидерландские Антильские островаНовая КаледонияНовая ЗеландияНикарагуаНигерНигерияNiueОстров НорфолкСеверные Марианские островаСеверная КореяНорвегияОманПакистанПалауПалестинская территорияПанамаПапуа-Новая ГвинеяПарагвайПеруФилиппиныПиткэрнПольшаПортугалияПуэрто-РикоКатарВстречаРумынияРоссияРуандаСен-БартельмиСвятой ЕленыСент-Китс и НевисСент-ЛюсияСен-Мартен (французская часть)Сен-Пьер и МикелонСент-Винсент и ГренадиныСамоаСан-МариноСан-Томе и ПринсипиСаудовская АравияСенегал СербияСейшельские островаСьерра-ЛеонеСингапурСинт-МаартенСловакияСловенияСоломоновы островаСомалиЮжно-Африканская Республика Южная Джорджия и Южные Сандвичевы островаЮжная КореяЮжный СуданИспанияШри-ЛанкаСуданСуринамШпицберген и Ян-МайенСвазилендШвецияШвейцарияСирияТайваньТаджикистанТанзанияТаиландТимор-ЛештиТогоТокелауТонгаТринидад и ТобагоТунисТурцияТуркменистанОстрова Теркс и КайкосТувалуАмериканские Виргинские островаУгандаУкраинаОбъединенные Арабские ЭмиратыАнглияСШАСША Внешние малые островаУругвайУзбекистанВануатуВатиканВенесуэлаВьетнамУоллис и ФутунаЗападная СахараЙеменЗамбияЗимбабвеКосово
Выбрать РегионАндхра-ПрадешАруначал-ПрадешАссамБихарЧхаттисгархДелиГоаГуджаратХарьянаХимачал-ПрадешДжамму и КашмирДжаркхандКарнатакаКералаМадхья-ПрадешМахараштраМанипурMeghalayaMizoramNagalandOdishaПенджабРаджастханСиккимТамилнадTelanganaТрипураУттаракхандУттар-ПрадешЗападная Бенгалия
Мне нужно визовое приглашение.
У меня все в порядке с платной теле / видео консультацией
Отправить запрос
Хронический ларингит — как распознать и успешно вылечить заболевание?
Цветной бульвар
Москва, Самотечная, 5
круглосуточно
Преображенская площадь
Москва, Б. Черкизовская, 5
Ежедневно
c 09:00 до 21:00
Бульвар Дмитрия Донского
Москва, Грина, 28 корпус 1
Ежедневно
c 09:00 до 21:00
Мичуринский проспект
Москва, Большая Очаковская, 3
Ежедневно
c 09:00 до 21:00
| Подробное описание | Оптимальная продолжительность голосового покоя Голос после фонохирургии при доброкачественных нарушений голоса: Проспективное рандомизированное исследование Фон: Фонохирургия проводится с целью улучшения качества голоса пациентов с разным голосом. |
|---|
Белые бляшки лейкоплакии гортани на голосовых связках
Первоначальное определение лейкоплакии, данное Всемирной организацией здравоохранения (ВОЗ) как «белое поражение слизистой оболочки», было уточнено, чтобы обозначить «белое пятно или бляшку, которые клинически или патологически не могут быть охарактеризованы как любые другие болезнь» — с неотъемлемым признанием того, что поражение может представлять рак или предвестник развития рака.
Дальнейшее уточнение определения привело к современному определению лейкоплакии как «белых бляшек сомнительного риска, исключающих (другое) известное заболевание или нарушение, которые не несут повышенного риска развития рака»
В некоторых отчетах термины кератоз и лейкоплакия используются как синонимы
Обнаружение
1.Часто бессимптомно — случайно (гортань осматривается при анестезии / желудочно-кишечном тракте / ринологии)
2.Ассоциации: дисфония (раздражение горла / хронический кашель редко являются результатом лейкоплакии)
Заболеваемость/распространенность
1. Вскрытие (37 лет назад) – 19% мужчин с «кератозом гортани» – 80% были курильщиками.
Кератоз гортани наблюдается только у 4,2% некурящих (Muller 1980)
2. Обзор медицинской документации 1935-84 г. Рочестер, Миннесота (Bouguot 1991)
Ежегодная частота обнаружения:
кератоз голосовых складок у 10. 2/100 000 мужчин и 2,1/100 000 женщин 90 005
2/100 000 мужчин и 2,1/100 000 женщин 90 005
Бессимптомный кератоз гортани (лейкоплакия) не был включен в исследование
Таблица ниже взята из Isenberg, Crozier and Dailey (2008) «Институциональный и всесторонний обзор лейкоплакии гортани» Ann otol Rhinol Laryngol 2008; 117:74-9:
| Лейкоплакия | Н | Нет дисплазии | Легкая/Mod Дисплазия | Тяжелая дисплазия/СНГ |
| Университет Висконсина | 208 биопсий 136 пациентов | 53% | 18% | 15% |
| 15 публикаций | 2188 биопсий | 53.6% | 33,5% | 15,2% |
Отмечено расхождение с путаницей среди патологоанатомов в отношении степени дисплазии (Gupta 2010) и (El-Naggar AK 2017)
Каталожные номера:
Гейл и др. «Эпителиальные предраковые поражения» в публикации Барнса и др. (ред.) Патология и генетика: опухоли головы и шеи IARC Press 2005
(ред.) Патология и генетика: опухоли головы и шеи IARC Press 2005
Warnakulasuria et al: Номенклатура и классификация потенциально злокачественных заболеваний слизистой оболочки полости рта.Дж Орал Патол Мед. 2007;36:575-80
Bouquot JE, Gnepp DR (1991) Предшественник гортани: обзор литературы, комментарии и сравнение с
лейкоплакией полости рта. Шея головы. 13:488-97
Bouquot et al. Обнаружение рака Пред. 1991;15:83-91
Muller and Krohn J Cancer Res Clin oncol. 1980;96:211-7
Isenberg, Crozier and Dailey (2008) «Институциональный и всесторонний обзор лейкоплакии гортани» Ann otol Rhinol Laryngol 2008;117:74-9
Гупта Х.Т., Робинсон Р.А., Мюррей Р.К., Карнелл Л.Х., Смит Р.Дж.Х. и Хоффман Х.Т.: Степени дисплазии и использование цидофовира у пациентов с рецидивирующим респираторным папилломатозом Ларингоскоп 120:698-702, 2010
El-Naggar AK, Chan JKC, Grandis JR, Takata Takashi и Slootweg PJ: Классификация ВОЗ опухолей головы и шеи. 4-е издание Международного агентства по изучению рака, Лион, 2017 г.
4-е издание Международного агентства по изучению рака, Лион, 2017 г.
Косвей Б. и Палери В.: Дисплазия гортани: блок-схема, основанная на фактических данных, для руководства и последующего наблюдения Журнал ларингологии и отологии (2015), 129, 598-599
Обзор плоскоклеточной дисплазии | Iowa Head and Neck Protocols
Обзор плоскоклеточной дисплазии
Вернуться к: Белые бляшки при лейкоплакии гортани на голосовых связках
Перейти к: Легкая плоскоклеточная дисплазия, вызывающая лейкоплакию гортани
Перейти к: Умеренная плоскоклеточная дисплазия, вызывающая лейкоплакию гортани
Перейти к: Тяжелая плоскоклеточная дисплазия или карцинома in situ, вызывающая лейкоплакию гортани
Перейти к: Инвазивная плоскоклеточная карцинома, вызывающая лейкоплакию гортани
см. также: Карцинома in situ против тяжелой дисплазии
Плоскоклеточная дисплазия определяется ВОЗ как «измененный эпителий с повышенной вероятностью прогрессирования в плоскоклеточный рак (SCC). Он может показать различные как архитектурные, так и цитологические аномалии (таблица 1), которые рассматриваются в комбинации для определения степени поражения слизистой оболочки. Степень связана с относительным риском развития инвазивной карциномы. В Университете Айовы мы используем классификационную схему ВОЗ 2005 г. для классификации предшествующих поражений (таблица 2).
Он может показать различные как архитектурные, так и цитологические аномалии (таблица 1), которые рассматриваются в комбинации для определения степени поражения слизистой оболочки. Степень связана с относительным риском развития инвазивной карциномы. В Университете Айовы мы используем классификационную схему ВОЗ 2005 г. для классификации предшествующих поражений (таблица 2).
Таблица 1. Архитектурные и цитологические аномалии, присутствующие при дисплазии
Архитектурные изменения | Цитологические изменения |
Нарушение клеточной стратификации | Анизонуклеоз (изменчивость размеров ядер) |
Потеря полярности сотовой связи | Ядерный плеоморфизм (изменение формы ядра) |
Митотические фигуры над базальной зоной | Анизоцитоз (вариабельность размера клеток) |
Дискератоз (преждевременное ороговение) | Повышенное ядерно-цитоплазматическое (N/C) соотношение |
Глубокое кератиновое жемчужное образование | Атипичные митозы |
| Изменения ядерного хроматина (гиперхромазия) |
Таблица 2. Схемы классификации предраковых плоскоклеточных поражений головы и шеи
Схемы классификации предраковых плоскоклеточных поражений головы и шеи
Плоскоклеточная интраэпителиальная неоплазия (SIN) | Люблянская классификация плоскоклеточных интраэпителиальных поражений (SIL) | |
|---|---|---|
Легкая дисплазия | СИН 1 | Базально-/парабазально-клеточная гиперплазия |
Умеренная дисплазия | СИН 2 | Атипическая гиперплазия |
Тяжелая дисплазия | СИН 3 | Атипическая гиперплазия |
Карцинома in situ | СИН 3 | Карцинома in situ |
Обычно мы используем следующую рубрику для определения степени дисплазии:
Легкая дисплазия: Архитектурное нарушение, как правило, ограниченное нижней третью слизистой оболочки с минимальными цитологическими аномалиями. Если митозы присутствуют, они ограничены базальным/парабазальным слоями. Также отсутствует разрастание слизистой оболочки. См. пример легкой дисплазии ниже.
Если митозы присутствуют, они ограничены базальным/парабазальным слоями. Также отсутствует разрастание слизистой оболочки. См. пример легкой дисплазии ниже.
Умеренная дисплазия: Архитектурное нарушение распространяется на среднюю треть слизистой оболочки с сопутствующими более значительными цитологическими аномалиями. Митозы обычно ограничиваются нижними участками слизистой оболочки. На этой стадии слизистая оболочка может иметь аномальный эпителиально-стромальный интерфейс и может иметь место разрастание слизистой оболочки вниз.Является ли это ранним вторжением, может быть чрезвычайно трудно определить. Важно помнить, что если цитологические изменения явно ненормальны, умеренная дисплазия может перейти в тяжелую дисплазию/карциному in situ. См. пример умеренной дисплазии ниже.
Тяжелая дисплазия/карцинома in situ: В то время как другие пытаются разделить эти две степени дисплазии, мы предпочитаем считать их синонимами, поскольку оба имеют значительно повышенный потенциал быть последним наблюдаемым этапом перед стромальной инвазией. Архитектурное расстройство обычно распространяется на верхнюю треть слизистой оболочки и сопровождается выраженной вариабельностью размера ядер, аномальной формой ядер и ядерной гиперхромазией. Митозы обычно локализуются в верхних слоях слизистой оболочки и могут быть даже атипичными формами. На этой стадии наблюдается более очевидный нисходящий, выпуклый или почковательный характер роста, указывающий на наличие измененного эпителиально-стромального интерфейса. Особое внимание к этому соединению имеет решающее значение для исключения ранней инвазивной карциномы.См. пример тяжелой плоскоклеточной дисплазии/карциномы in situ ниже.
Архитектурное расстройство обычно распространяется на верхнюю треть слизистой оболочки и сопровождается выраженной вариабельностью размера ядер, аномальной формой ядер и ядерной гиперхромазией. Митозы обычно локализуются в верхних слоях слизистой оболочки и могут быть даже атипичными формами. На этой стадии наблюдается более очевидный нисходящий, выпуклый или почковательный характер роста, указывающий на наличие измененного эпителиально-стромального интерфейса. Особое внимание к этому соединению имеет решающее значение для исключения ранней инвазивной карциномы.См. пример тяжелой плоскоклеточной дисплазии/карциномы in situ ниже.
При рассмотрении всех форм дисплазии мы подчеркиваем необходимость развития и поддержания прочных коллегиальных отношений между хирургом головы и шеи и хирургическим патологоанатомом, чтобы при биопсии и исследовании лейкоплакического поражения возникала соответствующая клинико-патологическая корреляция, поскольку последствия для пациента могут быть значительным. Если когда-либо обнаруживается несоответствие между клиническим впечатлением и патоморфологическим диагнозом, рекомендуется совместное рассмотрение, например, в комиссии по опухолям.
Если когда-либо обнаруживается несоответствие между клиническим впечатлением и патоморфологическим диагнозом, рекомендуется совместное рассмотрение, например, в комиссии по опухолям.
Примеры плоскоклеточной дисплазии | ||
|---|---|---|
Легкая дисплазия: Архитектурное расстройство, обычно ограниченное нижней третью слизистой оболочки с легким ядерным плеоморфизмом и гиперхроматизмом. Отмечены митоз (черная стрелка) и пара дискератотических клеток (белые стрелки). | Умеренная дисплазия: архитектурные изменения распространяются на среднюю треть этой биопсии с умеренным ядерным плеоморфизмом, аномалиями ядерного хроматина (грубыми и гиперхроматическими) и митозом среднего слоя (черная стрелка). | Тяжелая дсплазия/карцинома in situ: архитектурное нарушение почти полной толщины с выраженным ядерным плеоморфизмом и гиперхроматизмом, дискератозом (белые стрелки) и митозами верхнего слоя (черные стрелки). |
Сообщается, что конверсия рака голосовой щели in situ в инвазивный рак голосовой щели произошла у 5,4% из 3738 пациентов, идентифицированных в базе данных SEER с 1988 по 2012 год (Khaja 2016).Когда инвазивный рак впоследствии обнаруживается после лечения с помощью биопсии или удаления CIS, трудно отличить персистенцию от неполной резекции от продолжающейся трансформации «полевой раковой слизистой оболочки» (Gailey 2015). В других ретроспективных когортных исследованиях, проведенных в одном учреждении, прогрессирование до инвазивного рака описано у 11% (Sengupta, 2010) и 9,6% (Karatayli-Ozgurosoy, 2015). Объединенный метаанализ 9 исследований Weller et al (2010) сообщил о 30% злокачественной трансформации тяжелой дисплазии/CIS.Считается, что влияние продолжительного курения и употребления алкоголя является важной переменной, повышающей риск злокачественной трансформации.
Каталожные номера:
Хаджа С. Ф., Хоффман Х.Т. и Пейдждар Н.А.: Тенденции лечения и выживания при карциноме голосовой щели in situ и раке Satge I с 1988 по 2012 год Анналы отологии, ринологии и ларингологии 125(4) 2016
Ф., Хоффман Х.Т. и Пейдждар Н.А.: Тенденции лечения и выживания при карциноме голосовой щели in situ и раке Satge I с 1988 по 2012 год Анналы отологии, ринологии и ларингологии 125(4) 2016
Сенгупта Н., Моррис К.Г., Кирван Дж., Амдур Р.Дж., Менденхолл В.М. Окончательная лучевая терапия рака in situ истинных голосовых связок.Am J клин Oncol. 2010;33(1):94-95
Weller MD, Nankivell PC, Mcconkey C, Paleri V, Mehanna HM. Риск и интервал малигнизации больных с дисплазией гортани; систематический обзор серии случаев и метаанализ. Клин Отоларингол. 2010;35(5):364-372
Каратайли-Озгурсой с, Пачеко-Лопес П, Гилель А.Т., Бест С.Р., Бишоп Ю.А., Акст Л.М. Дисплазия гортани, демография и лечение: одно учреждение, 20-летний обзор. JAMA Otolaryngol Head Neck Surg. 2015;141(4):313-318
«Лейкоплакия» (глава книги) Гейли М. и Хоффмана Х. в «Учебнике отоларингологии Саталоффа» под редакцией доктораРоберт Саталофф 2015
Тяжелая плоскоклеточная дисплазия или карцинома in situ, вызывающая лейкоплакию гортани
(Нажмите на фотографию и используйте клавиши со стрелками вправо и влево для переключения вперед и назад)
Тяжелая плоскоклеточная дисплазия или карцинома in situ, вызывающая лейкоплакию гортани
Вернуться к: Белые бляшки при лейкоплакии гортани на голосовых связках
Вернуться к: Обзор плоскоклеточной дисплазии
Перейти к: Инвазивная плоскоклеточная карцинома, вызывающая лейкоплакию гортани
Тяжелая плоскоклеточная дисплазия и карцинома in situ являются формами дисплазии высокой степени, обе несут значительный риск прогрессирования в инвазивную карциному. Фактически, оба могут представлять собой последний наблюдаемый шаг перед тем, как произойдет вторжение. Таким образом, наше соглашение состоит в том, чтобы использовать термины как синонимы, отдавая предпочтение последнему термину в диагностической строке. Наше предпочтение основано на том факте, что мы не можем сказать, когда поражение высокой степени будет распространяться, а когда останется ограниченным слизистой оболочкой, особенно в его ороговевающей форме. Самое главное, оба поражения должны лечиться хирургом головы и шеи одинаково и должны тщательно наблюдаться для выявления признаков подслизистой инвазии.
Фактически, оба могут представлять собой последний наблюдаемый шаг перед тем, как произойдет вторжение. Таким образом, наше соглашение состоит в том, чтобы использовать термины как синонимы, отдавая предпочтение последнему термину в диагностической строке. Наше предпочтение основано на том факте, что мы не можем сказать, когда поражение высокой степени будет распространяться, а когда останется ограниченным слизистой оболочкой, особенно в его ороговевающей форме. Самое главное, оба поражения должны лечиться хирургом головы и шеи одинаково и должны тщательно наблюдаться для выявления признаков подслизистой инвазии.
Важно осознавать, что эта степень атипии может принимать различные формы и что, казалось бы, более низкие степени дисплазии для нетренированных глаз могут быть повышены до карциномы in situ на основе крайних проявлений цитоморфологической атипии. В большинстве случаев архитектурные аномалии легко достигают верхней трети слизистой оболочки, а цитологическая атипия является тяжелой. Митозы могут присутствовать по всей глубине слизистой оболочки и может присутствовать аномальное ороговение (дискератоз). Критическое исследование эпителиально-стромального интерфейса необходимо для исключения инвазивного процесса.
Митозы могут присутствовать по всей глубине слизистой оболочки и может присутствовать аномальное ороговение (дискератоз). Критическое исследование эпителиально-стромального интерфейса необходимо для исключения инвазивного процесса.
Тяжелая плоскоклеточная дисплазия/карцинома in situ | |||
|---|---|---|---|
Для большинства патологов тяжелая плоскоклеточная дисплазия и карцинома in situ неразличимы. Эта биопсия показывает полнослойный ядерный гиперхроматизм и плеоморфизм с митозами верхнего уровня (черные стрелки) и дискератозными клетками (белые стрелки). | Карцинома in situ с расширением базального слоя на всю толщину.На самом деле, в этой биопсии трудно определить, какое направление вверх и вниз, если игнорировать подслизистую оболочку. | Карцинома in situ, демонстрирующая глубокую ядерную атипию (черные стрелки) с выраженным архитектурным нарушением. | Эта биопсия показывает выраженный ядерный гиперхроматизм и плеоморфизм с высокой степенью расширения базального слоя.В средней половине отмечен митоз (черная стрелка), а вблизи поверхности присутствуют аномально крупные клетки (белые стрелки). |
Эта биопсия интересна тем, что показывает переход рака in situ (слева от черной линии) в более низкую степень дисплазии (справа от черной линии). Слева архитектурное нарушение, больше ядерного гиперхроматизма и расширение базального слоя. | |||
Сообщается, что конверсия рака голосовой щели in situ в инвазивный рак голосовой щели произошла у 5,4% из 3738 пациентов, идентифицированных в базе данных SEER с 1988 по 2012 год (Khaja 2016). Когда инвазивный рак впоследствии обнаруживается после лечения с помощью биопсии или удаления CIS, трудно отличить персистенцию от неполной резекции от продолжающейся трансформации «полевой раковой слизистой оболочки» (Gailey 2015). В других ретроспективных когортных исследованиях, проведенных в одном учреждении, прогрессирование до инвазивного рака описано у 11% (Sengupta, 2010) и 9,6% (Karatayli-Ozgurosoy, 2015). Объединенный метаанализ 9 исследований Weller et al (2010) сообщил о 30% злокачественной трансформации тяжелой дисплазии/CIS. Считается, что влияние продолжительного курения и употребления алкоголя является важной переменной, повышающей риск злокачественной трансформации.
В других ретроспективных когортных исследованиях, проведенных в одном учреждении, прогрессирование до инвазивного рака описано у 11% (Sengupta, 2010) и 9,6% (Karatayli-Ozgurosoy, 2015). Объединенный метаанализ 9 исследований Weller et al (2010) сообщил о 30% злокачественной трансформации тяжелой дисплазии/CIS. Считается, что влияние продолжительного курения и употребления алкоголя является важной переменной, повышающей риск злокачественной трансформации.
Каталожные номера:
Хаджа С.Ф., Хоффман Х.Т. и Пейдждар Н.А.: Тенденции лечения и выживания при карциноме голосовой щели in situ и раке Satge I с 1988 по 2012 год Анналы отологии, ринологии и ларингологии 125(4) 2016
Сенгупта Н., Моррис К.Г., Кирван Дж., Амдур Р.Дж., Менденхолл В.М.Окончательная лучевая терапия рака in situ истинных голосовых связок. Am J клин Oncol. 2010;33(1):94-95
Weller MD, Nankivell PC, Mcconkey C, Paleri V, Mehanna HM. Риск и интервал малигнизации больных с дисплазией гортани; систематический обзор серии случаев и метаанализ. Клин Отоларингол. 2010;35(5):364-372
Клин Отоларингол. 2010;35(5):364-372
Каратайли-Озгурсой с, Пачеко-Лопес П, Гилель А.Т., Бест С.Р., Бишоп Ю.А., Акст Л.М. Дисплазия гортани, демография и лечение: одно учреждение, 20-летний обзор.JAMA Otolaryngol Head Neck Surg. 2015;141(4):313-318
«Лейкоплакия» (глава книги) Гейли М. и Хоффмана Х. в «Учебнике отоларингологии Саталоффа» под редакцией доктора Роберта Саталоффа, 2015 г.
Анализ 178 случаев
Цель . Оценить эффективность и определить типы лейкоплакии голосовых складок, подходящие для консервативного лечения. Методы . Лейкоплакия голосовых складок у 178 больных была разделена по макроскопическому типу на три подтипа: плоская и гладкая, приподнятая и гладкая, шероховатая.Все пациенты получали нехирургическое лечение, включая отказ от курения и употребления алкоголя, голосовой покой, омепразол и китайскую медикаментозную терапию. Клинический ответ трех подтипов оценивали после 6-месячного наблюдения. Результаты . Подтипы лейкоплакии голосовых складок включали плоскую и гладкую (; 37,1%), приподнятую и гладкую (; 57,9%) и шероховатую (; 5,0%). Частота полного ответа составила 80,3 %, 66,0 % и 0,0 % для 3 типов поражений соответственно (шероховатый по сравнению с плоским и гладким; шероховатый по сравнению с приподнятым и гладким, точный критерий Фишера).Частота карциномы при грубой лейкоплакии была значительно выше, чем при гладкой лейкоплакии (44,4% против 2,4%, точный критерий Фишера). Клинический тип был единственным значимым фактором клинического ответа на консервативное лечение (порядковая логистическая регрессия). Выводы . Эффективность нехирургического лечения гладкой лейкоплакии голосовых складок выше по сравнению с грубой лейкоплакией голосовых складок. С гладкой лейкоплакией можно справиться нехирургическим путем; при грубой лейкоплакии следует рассматривать более агрессивные методы лечения.
Подтипы лейкоплакии голосовых складок включали плоскую и гладкую (; 37,1%), приподнятую и гладкую (; 57,9%) и шероховатую (; 5,0%). Частота полного ответа составила 80,3 %, 66,0 % и 0,0 % для 3 типов поражений соответственно (шероховатый по сравнению с плоским и гладким; шероховатый по сравнению с приподнятым и гладким, точный критерий Фишера).Частота карциномы при грубой лейкоплакии была значительно выше, чем при гладкой лейкоплакии (44,4% против 2,4%, точный критерий Фишера). Клинический тип был единственным значимым фактором клинического ответа на консервативное лечение (порядковая логистическая регрессия). Выводы . Эффективность нехирургического лечения гладкой лейкоплакии голосовых складок выше по сравнению с грубой лейкоплакией голосовых складок. С гладкой лейкоплакией можно справиться нехирургическим путем; при грубой лейкоплакии следует рассматривать более агрессивные методы лечения.
1. Введение
Лейкоплакия голосовых складок клинически определяется как поражение слизистой оболочки белого цвета, которое не может быть охарактеризовано как какое-либо другое состояние, и патологически делится на два подтипа следующим образом: кератоз с недисплазией и кератоз с дисплазией [1, 2]. Лейкоплакия без дисплазии не несет предракового потенциала, а лейкоплакия с дисплазией демонстрирует предраковый потенциал [3]. Тем не менее, доброкачественные и злокачественные поражения голосовой лейкоплакии не могут быть клинически различимы без патологической биопсии; таким образом, согласованная стратегия лечения, варьирующая от наблюдения до полной резекции лейкоплакии голосовых складок, не была достигнута [4].
Лейкоплакия без дисплазии не несет предракового потенциала, а лейкоплакия с дисплазией демонстрирует предраковый потенциал [3]. Тем не менее, доброкачественные и злокачественные поражения голосовой лейкоплакии не могут быть клинически различимы без патологической биопсии; таким образом, согласованная стратегия лечения, варьирующая от наблюдения до полной резекции лейкоплакии голосовых складок, не была достигнута [4].
Лейкоплакию голосовых складок следует лечить индивидуально в зависимости от ее доброкачественного или злокачественного характера. Консервативная терапия или стратегия наблюдения приносят пользу людям с низким риском злокачественных новообразований [1, 5]. По данным, хирургическая терапия остается наиболее широко изученным методом лечения. Ricci и Isenberg сообщили, что примерно у 50% пациентов с клиническим диагнозом лейкоплакия голосовых складок дисплазия отсутствует [6, 7], что указывает на то, что эти пациенты получали ненужное хирургическое лечение.
Принимая во внимание макроскопический вид, была предложена система классификации и стадирования лейкоплакии полости рта [8]. Однако помимо системы оценки ларингоскопической визуализации, разработанной Fang et al. [9], было немного сообщений о методе клинической классификации лейкоплакии голосовых складок, чтобы отличить доброкачественные образования от злокачественных. Таким образом, метод классификации лейкоплакии голосовых складок может просто и всесторонне отражать степень поражения.
Однако помимо системы оценки ларингоскопической визуализации, разработанной Fang et al. [9], было немного сообщений о методе клинической классификации лейкоплакии голосовых складок, чтобы отличить доброкачественные образования от злокачественных. Таким образом, метод классификации лейкоплакии голосовых складок может просто и всесторонне отражать степень поражения.
В некоторых исследованиях оценивалась эффективность нехирургических вмешательств при лейкоплакии полости рта [10, 11], показывая значительный эффект нехирургической терапии.Тем не менее, до сих пор неясно, могут ли пациенты с лейкоплакией голосовых складок получить пользу от нехирургического лечения. Большинство исследований были сосредоточены на хирургическом лечении, но игнорировали консервативное лечение лейкоплакии голосовых складок.
Целью данного исследования было предложить новый метод классификации лейкоплакии голосовых складок и оценить клинический ответ на нехирургическое лечение для оптимизации стратегии лечения.
2. Материалы и методы
Протокол данного исследования был одобрен Наблюдательным советом Института глаз и ушей, носа, горловой больницы Университета Фудань, Шанхай, Китай.
2.1. Пациенты
Проанализированы клинические данные 604 амбулаторных пациентов с первичным диагнозом лейкоплакия голосовых складок за период с января 2010 г. по декабрь 2014 г. В исследование были включены пациенты, которым было назначено консервативное лечение. Клинический диагноз лейкоплакии был подтвержден тремя опытными ларингологами по данным анамнеза и ларингоскопического исследования. Любые другие специфические заболевания, которые могли проявляться белым поражением голосовых связок, такие как инфекции верхних дыхательных путей, туберкулез гортани и грибковая инфекция гортани, были исключены.Исключались пациенты, у которых в анамнезе были респираторные инфекции в течение последних двух недель, перенесенная или текущая туберкулезная инфекция или длительное употребление стероидов. Пациенты с патологическим диагнозом плоскоклеточного рака гортани или перенесшие операцию или лучевую терапию гортани также были исключены.
Пациенты с патологическим диагнозом плоскоклеточного рака гортани или перенесшие операцию или лучевую терапию гортани также были исключены.
2.2. Клинические данные
Были собраны клинические данные, включая пол, возраст, историю курения, употребление алкоголя, ларингофарингеальный рефлюкс, злоупотребление голосом, историю приема лекарств, ларингоскопические изображения до и после лечения, а также послеоперационные патологические записи.Курение определялось как выкуривание более 10 сигарет в день в течение как минимум 1 года. Употребление алкоголя определяли как потребление более 80 мл чистого алкоголя в день. Случаи, которые считались нарушителями голоса, соответствовали по крайней мере одному из следующих критериев: (1) время фонирования составляло не менее 4 часов в день и (2) профессиональные пользователи голоса (такие как учителя, ведущие, телемаркетологи, продавцы, инструкторы, певцы и т. д.). актеры). Диагноз ларингофарингеального рефлюкса устанавливался на основании показателей индекса симптомов рефлюкса (RSI) [12].
2.3. Клинические типы
Регистрировали морфологические характеристики, включая поверхность, края и текстуру; затем лейкоплакия голосовых складок была разделена тремя опытными ларингологами независимо на три категории: плоская и гладкая, приподнятая и гладкая и шероховатая (табл. 1). Репрезентативные фотографии каждого типа поражения показаны на рисунке 1. Когда лейкоплакия голосовых складок имела более одного морфологического проявления в разных местах, поражение классифицировалось как приподнятое и гладкое, если плоская и гладкая лейкоплакия и приподнятая и гладкая лейкоплакия сосуществовали на голосовых связках. ; грубая лейкоплакия определялась при появлении шероховатых очагов на голосовых связках.
| ||||||||||||||||
2.
 4. Лечение
4. ЛечениеПациентам с грубой лейкоплакией настоятельно рекомендовалось удаление слизистой оболочки голосовых складок углекислотным (CO 2 ) лазером. Нехирургическое лечение проводилось у пациентов с гладкой лейкоплакией голосовых складок или у пациентов с грубой лейкоплакией, у которых имелись медицинские проблемы высокого риска в хирургии или остро требовалась консервативная терапия.
Нехирургические методы лечения включали отказ от курения и употребления алкоголя, строгий голосовой покой, терапию ингибиторами протонной помпы (омепразол 20 мг два раза в день), если она сопровождалась ларингофарингеальным рефлюксом, и китайские препараты (гранулы Xuanboshuangsheng, 8 мг два раза в день).Основными ингредиентами гранул Xuanboshuangsheng являются травы, в том числе Radix Scrophulariae, Cortex Phellodendri и Radix Glycyrrhizae (номер одобрения лекарственного средства: Z05170495, Шанхай, Китай; Медицинское учреждение: Больница для лечения ушей, носа, горла Университета Фудань, Шанхай, Китай; Ассоциированное учреждение: Шанхай Лянтан Фармасьютикал Корпорэйшн Лимитед).
Непрерывная нехирургическая терапия длилась 6 недель. Пациентов осматривали с интервалами от 2 до 4 недель в первые 3 месяца и с интервалами от 4 до 12 недель в последующие месяцы и оценивали с помощью ларингоскопии в кабинете врача.Удаление слизистой оболочки голосовых складок с помощью лазера CO 2 было выполнено для пациентов, у которых не было улучшений по сравнению с предыдущим нехирургическим лечением после последующего наблюдения в течение 6 месяцев.
2.5. Оценка клинического ответа
Три опытных ларинголога сравнили ларингоскопические изображения каждого пациента до и после лечения. Полный ответ (ПО) определяли как полное исчезновение поражения в течение как минимум 4 недель. Частичный ответ (PR) определяли как уменьшение размера поражения на 50% и более в течение как минимум 4 недель.Отсутствие ответа (NR) определяли как отсутствие значительных изменений в течение как минимум 4 недель, включая стабилизацию заболевания, снижение менее чем на 50% и поражение с увеличением менее чем на 25%. Прогрессирующее заболевание (ПЗ) определяли как появление любых новых поражений, которые ранее не были идентифицированы, или предполагаемое увеличение существующих поражений на 25% или более, или прогрессирование от гладкого поражения к грубому поражению [13]. Время до полного ответа пациентов было временем от первого визита пациента до полного исчезновения поражения.
Прогрессирующее заболевание (ПЗ) определяли как появление любых новых поражений, которые ранее не были идентифицированы, или предполагаемое увеличение существующих поражений на 25% или более, или прогрессирование от гладкого поражения к грубому поражению [13]. Время до полного ответа пациентов было временем от первого визита пациента до полного исчезновения поражения.
2.6. Гистологическая оценка
Все ткани подвергались стандартной обработке для патологического исследования. Фиксированные в формалине и залитые парафином препараты были независимо просмотрены и гистологически оценены тремя патологоанатомами в отделении патологии глаза и уха, носа, горловой больницы Университета Фудань, Шанхай, Китай. Эпителиальную дисплазию определяли в соответствии с классификацией Всемирной организации здравоохранения 2005 г., в которой лейкоплакия голосовых складок подразделяется на следующие категории: плоскоклеточная гиперплазия с недисплазией, легкая дисплазия, умеренная дисплазия, тяжелая дисплазия и карцинома [14]. Плоскоклеточная гиперплазия с недисплазией описывает увеличение количества клеток, но архитектура показывает регулярное расслоение и нет клеточной атипии. Легкая дисплазия описывает легкую цитологическую атипию, наиболее выраженную в базальной трети эпителия. Умеренная дисплазия описывает более цитологическую атипию, изменения, присутствующие в нижних двух третях эпителия. Тяжелая дисплазия описывает цитологическую атипию, затрагивающую более двух третей толщины эпителия. Карцинома описывает архитектурные аномалии полной толщины в жизнеспособных клеточных слоях, сопровождающиеся цитологической атипией.
Плоскоклеточная гиперплазия с недисплазией описывает увеличение количества клеток, но архитектура показывает регулярное расслоение и нет клеточной атипии. Легкая дисплазия описывает легкую цитологическую атипию, наиболее выраженную в базальной трети эпителия. Умеренная дисплазия описывает более цитологическую атипию, изменения, присутствующие в нижних двух третях эпителия. Тяжелая дисплазия описывает цитологическую атипию, затрагивающую более двух третей толщины эпителия. Карцинома описывает архитектурные аномалии полной толщины в жизнеспособных клеточных слоях, сопровождающиеся цитологической атипией.
2.7. Статистический анализ
Все статистические анализы проводились с использованием программного обеспечения SPSS версии 23.0 (IBM Corporation, 2015, США). Все сравнения клинических данных между тремя группами проводились с помощью точного критерия Фишера, за исключением возраста (однофакторный дисперсионный анализ). Точный критерий Фишера был проведен для оценки клинического ответа трех групп. Затем были проведены попарные сравнения между тремя группами с использованием теста Бонферрони. Полный ответ гладких типов также был представлен в виде кривых Каплана-Мейера со статистическим сравнением с использованием логарифмического рангового критерия.Модель порядковой логистической регрессии была проведена для определения различных клинических факторов, влияющих на клинический ответ. Точный критерий Фишера и критерий Крускала-Уоллиса с последующим критерием Немени использовались для оценки взаимосвязи между патологическими классами и клиническими типами. Двусторонние значения <0,05 были статистически значимыми для анализа, за исключением теста Бонферрони (значения <0,017).
Затем были проведены попарные сравнения между тремя группами с использованием теста Бонферрони. Полный ответ гладких типов также был представлен в виде кривых Каплана-Мейера со статистическим сравнением с использованием логарифмического рангового критерия.Модель порядковой логистической регрессии была проведена для определения различных клинических факторов, влияющих на клинический ответ. Точный критерий Фишера и критерий Крускала-Уоллиса с последующим критерием Немени использовались для оценки взаимосвязи между патологическими классами и клиническими типами. Двусторонние значения <0,05 были статистически значимыми для анализа, за исключением теста Бонферрони (значения <0,017).
3. Результаты
3.1. Характеристики пациентов
В это исследование было включено в общей сложности 178 пациентов с лейкоплакией голосовых складок, получавших консервативное лечение.Характеристики исходной информации о пациентах представлены в таблице 2. Из них в 66 (37,1%) случаях наблюдалась плоская и гладкая лейкоплакия, в 103 (57,9%) — возвышенная и гладкая лейкоплакия, а в 9 (5%) — грубая лейкоплакия.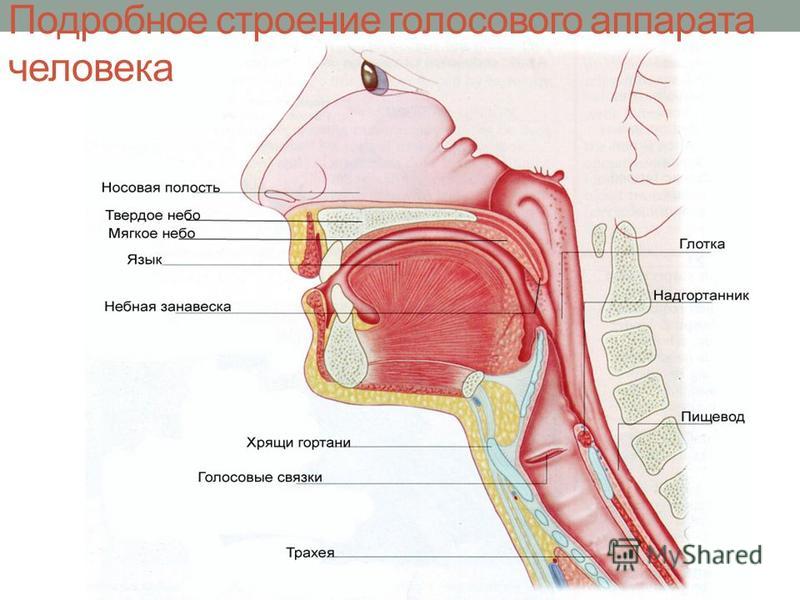 171 (96,1%) пациент был мужчиной и только 7 (3,9%) пациентом были женщины, средний возраст которых составлял годы (от 28 до 73 лет). Средний возраст пациентов с шероховатой лейкоплакией был значительно старше, чем у пациентов с гладкой лейкоплакией (шероховатая по сравнению с плоской и гладкой, грубая по сравнению с приподнятой и гладкой группой, ).В остальном группы были хорошо сбалансированы.
171 (96,1%) пациент был мужчиной и только 7 (3,9%) пациентом были женщины, средний возраст которых составлял годы (от 28 до 73 лет). Средний возраст пациентов с шероховатой лейкоплакией был значительно старше, чем у пациентов с гладкой лейкоплакией (шероховатая по сравнению с плоской и гладкой, грубая по сравнению с приподнятой и гладкой группой, ).В остальном группы были хорошо сбалансированы.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

3.2. Клинический ответ после нехирургического лечения
Клинический ответ пациентов с лейкоплакией голосовых складок показан в таблице 3. Частота полного ответа в трех группах значительно различалась (точный критерий Фишера). После попарных сравнений у пациентов с гладкой лейкоплакией частота полных ответов была значительно выше, чем у пациентов с грубой лейкоплакией (плоская и гладкая по сравнению с грубой, ОШ, 0,20, 95% ДИ, 0,12–0,32, точный критерий Фишера; повышенная и гладкая по сравнению с шероховатой, ИЛИ, 0.34, 95% ДИ, от 0,26 до 0,45, точный критерий Фишера). Частота полного ответа при плоской и гладкой лейкоплакии и приподнятой и гладкой лейкоплакии не имела существенной разницы (ОШ, 0,48, 95% ДИ, от 0,23 до 0,99, точный критерий Фишера). Появление клинического ответа для вокальной складки лейкоплакии показано на рисунке 1.
Среднее время полного ответа составило дни для двух гладких типов.Частота полного ответа гладких типов впоследствии оценивалась по кривым выживаемости Каплана-Мейера и сравнивалась с использованием логарифмического рангового критерия. Анализ Каплана-Мейера показал, что уровень полного ответа через 3 месяца составил 72,7% для плоского и гладкого типа по сравнению с 60,2% для приподнятого и гладкого типа. Через 6 месяцев частота полного ответа составила 80,3% и 66,0% соответственно (логарифмический ранговый критерий; рис. 2). Порядковый логистический регрессионный анализ показал, что клинический тип () был единственной значимой переменной, которая влияла на клинический ответ.
3.3. Послеоперационные патологические результаты В общей сложности 51 пациент, у которых не было улучшения после консервативной терапии после последующего наблюдения в течение 6 месяцев, был прооперирован. Из этих случаев в 11 (21,6%) случаях наблюдалась плоская и гладкая лейкоплакия, в 31 (60,8%) — приподнятая и гладкая лейкоплакия, в 9 (17,6%) — грубая лейкоплакия. Патологические результаты лейкоплакии голосовых складок приведены в таблице 5. Частота карциномы при грубой лейкоплакии была значительно выше, чем при гладкой лейкоплакии (44.4% против 2,4%, ОШ, 32,8, 95% ДИ, от 3,04 до 354,4, точный критерий Фишера). Коэффициент корреляции трех морфологических групп и степеней патологии составил . Результат теста Крускала-Уоллиса с последующим тестом Неменьи показал, что наблюдались статистически значимые различия между грубой лейкоплакией и гладкой лейкоплакией, соответственно (шероховатая по сравнению с плоской и гладкой, шероховатая по сравнению с приподнятой и гладкой, ).
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
4.Обсуждение
Лейкоплакия голосовых складок может быть гистологически диагностирована как плоскоклеточная гиперплазия, легкая дисплазия, умеренная дисплазия, тяжелая дисплазия и карцинома в соответствии с системами патологической классификации [14]. Однако было немного сообщений о клинической классификации лейкоплакии голосовых складок. Лейкоплакию полости рта разделили на два подтипа: негомогенную и гомогенную [8]. Ли и др. разделили лейкоплакию голосовых складок на три морфологические группы: поверхностный тип, экзофитный тип и язвенный тип [15].Фанг и др. предложили метод классификации лейкоплакии голосовых складок на основе оценки морфологических характеристик, включая толщину, текстуру, цвет, гиперемию, размер и симметрию [9]. Точно так же в этом исследовании предложена новая морфологическая классификация лейкоплакии голосовых складок. В последние десятилетия новые эндоскопические инструменты, особенно узкоспектральная визуализация, использовались для клинической классификации голосовой лейкоплакии на основе микрососудистых изменений [16], в то время как существующая классификация по макроскопическим признакам обеспечивает ценный источник ларингоскопического исследования, которое более широко применяется в клинической практике.
Однако было немного сообщений о клинической классификации лейкоплакии голосовых складок. Лейкоплакию полости рта разделили на два подтипа: негомогенную и гомогенную [8]. Ли и др. разделили лейкоплакию голосовых складок на три морфологические группы: поверхностный тип, экзофитный тип и язвенный тип [15].Фанг и др. предложили метод классификации лейкоплакии голосовых складок на основе оценки морфологических характеристик, включая толщину, текстуру, цвет, гиперемию, размер и симметрию [9]. Точно так же в этом исследовании предложена новая морфологическая классификация лейкоплакии голосовых складок. В последние десятилетия новые эндоскопические инструменты, особенно узкоспектральная визуализация, использовались для клинической классификации голосовой лейкоплакии на основе микрососудистых изменений [16], в то время как существующая классификация по макроскопическим признакам обеспечивает ценный источник ларингоскопического исследования, которое более широко применяется в клинической практике.
До сих пор нет единого мнения о лечении лейкоплакии голосовых складок. По имеющимся данным, хирургическое лечение предлагалось как вариант [1, 4]. Хотя исчезновение и уменьшение лейкоплакии полости рта при нехирургической терапии были зарегистрированы в прошлом [17, 18]. Насколько нам известно, имеется несколько записей об эффективности нехирургического лечения лейкоплакии голосовых складок. Сюй и др. обнаружили, что полный ответ до 85% наблюдался при голосовой лейкоплакии при терапии андрографолидом с последующим наблюдением в течение 12 месяцев [19].В нашем исследовании у 127 из 178 пациентов (71,3%) после консервативного лечения наблюдался полный или частичный ответ. Кроме того, мы впервые проанализировали время до полного ответа (среднее ± стандартное отклонение, дни) нехирургического лечения лейкоплакии голосовых складок. Эти результаты продемонстрировали, что некоторые очаги лейкоплакии голосовых складок могут исчезнуть или уменьшиться в размерах без хирургического лечения, и эти поражения могут улучшиться при консервативном вмешательстве.
Исследование лейкоплакии полости рта без хирургического лечения показало 32.5% гомогенных поражений и 24,3% негомогенных поражений, соответственно, исчезли или уменьшились [20]. Аналогичным образом, анализ данных (таблица 3) показал, что эффективность гладкой лейкоплакии была выше по сравнению с грубой лейкоплакией. Нехирургическое лечение показало значительный лечебный эффект в отношении сглаживания лейкоплакии. Результат анализа Каплана-Мейера показал, что не было существенной разницы в скорости полного ответа для двух гладких типов. Приподнятая и гладкая лейкоплакия ведет себя так же, как плоская и гладкая лейкоплакия, и поэтому лечить их следует аналогично.
Факторы риска, включая курение табака, употребление алкоголя, злоупотребление голосом и ларингофарингеальный рефлюкс, могут быть связаны с лейкоплакией голосовых складок [14]. Сообщалось, что курение табака является наиболее важным фактором, который может ускорить исчезновение лейкоплакии полости рта [17]. Тем не менее, мы провели всесторонний анализ, основанный на различных клинических факторах, включая клинический тип, пол, возраст, курение, употребление алкоголя, злоупотребление голосом, ларингофарингеальный рефлюкс и место поражения. Единственным значимым фактором, связанным с клиническим ответом, был клинический тип лейкоплакии голосовых складок.Основываясь на наших регрессионных моделях многофакторного анализа, пациенты с гладкой лейкоплакией голосовых складок лучше всего лечиться консервативным лечением, а пациенты с грубой лейкоплакией голосовых складок нуждаются в агрессивной терапии. Кроме того, остается неизвестным, повлияет ли патологическая степень лейкоплакии голосовых складок на клинический ответ на нехирургическое лечение. В настоящем исследовании этот вопрос о лейкоплакии голосовых складок не может быть исследован, поскольку патологические результаты не могут быть определены без биопсии, которая может ухудшить качество голоса.
Единственным значимым фактором, связанным с клиническим ответом, был клинический тип лейкоплакии голосовых складок.Основываясь на наших регрессионных моделях многофакторного анализа, пациенты с гладкой лейкоплакией голосовых складок лучше всего лечиться консервативным лечением, а пациенты с грубой лейкоплакией голосовых складок нуждаются в агрессивной терапии. Кроме того, остается неизвестным, повлияет ли патологическая степень лейкоплакии голосовых складок на клинический ответ на нехирургическое лечение. В настоящем исследовании этот вопрос о лейкоплакии голосовых складок не может быть исследован, поскольку патологические результаты не могут быть определены без биопсии, которая может ухудшить качество голоса.
Лейкоплакию голосовых складок следует лечить с точки зрения ее доброкачественного и злокачественного характера. Гиперплазия с недисплазией или легкая дисплазия не могут рассматриваться как предраковое поражение гортани и должны лечиться без хирургического вмешательства; поражение с более чем умеренной дисплазией требует более агрессивного лечения [5, 21, 22]. В настоящем исследовании удаление слизистой оболочки голосовых складок с помощью лазера CO 2 было выполнено у 51 пациента, у которых не было улучшений после предшествующего нехирургического лечения.Результаты патологической диагностики показали, что гладкие поражения в основном представлены недисплазией и легкой дисплазией при патологии, тогда как грубые поражения в основном представлены тяжелой дисплазией и карциномой. Мы считали, что этот метод классификации полезен для дифференциации доброкачественных и злокачественных образований. Кроме того, согласно клиническим данным трех сравниваемых групп (таблица 2), средний возраст пациентов с грубой лейкоплакией был значительно старше, чем у пациентов с гладкой лейкоплакией; поэтому возраст был важным фактором, который необходимо учитывать при определении типов лейкоплакии голосовых складок, подходящих для нехирургического лечения на основе этого метода классификации.
В настоящем исследовании удаление слизистой оболочки голосовых складок с помощью лазера CO 2 было выполнено у 51 пациента, у которых не было улучшений после предшествующего нехирургического лечения.Результаты патологической диагностики показали, что гладкие поражения в основном представлены недисплазией и легкой дисплазией при патологии, тогда как грубые поражения в основном представлены тяжелой дисплазией и карциномой. Мы считали, что этот метод классификации полезен для дифференциации доброкачественных и злокачественных образований. Кроме того, согласно клиническим данным трех сравниваемых групп (таблица 2), средний возраст пациентов с грубой лейкоплакией был значительно старше, чем у пациентов с гладкой лейкоплакией; поэтому возраст был важным фактором, который необходимо учитывать при определении типов лейкоплакии голосовых складок, подходящих для нехирургического лечения на основе этого метода классификации.
Первым ограничением этого исследования является отсутствие контрольной группы пациентов, перенесших операцию. Во-вторых, количество пациентов с грубой лейкоплакией составило всего 9 из-за нашей рекомендации, что пациентов с грубой лейкоплакией следует лечить хирургическим путем с учетом риска злокачественного новообразования. В-третьих, взаимосвязь между клиническим типом и степенью патологии необходимо изучать с большим размером выборки. Наконец, требуется проспективное когортное исследование, чтобы подтвердить использование метода классификации и признать влияние нехирургического лечения.
Во-вторых, количество пациентов с грубой лейкоплакией составило всего 9 из-за нашей рекомендации, что пациентов с грубой лейкоплакией следует лечить хирургическим путем с учетом риска злокачественного новообразования. В-третьих, взаимосвязь между клиническим типом и степенью патологии необходимо изучать с большим размером выборки. Наконец, требуется проспективное когортное исследование, чтобы подтвердить использование метода классификации и признать влияние нехирургического лечения.
5. Заключение
Эффективность нехирургического лечения лейкоплакии гладких голосовых складок значительно выше по сравнению с лейкоплакией шероховатых голосовых складок. Метод классификации рекомендуется для руководства при принятии решения о показаниях к лечению. В целом с гладкой лейкоплакией можно справиться нехирургическим путем; при грубой лейкоплакии следует рассматривать более агрессивные методы лечения.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов в связи с публикацией данной статьи.
Вклад авторов
Мин Чен и Лэй Ченг внесли равный вклад в эту работу.
Благодарности
Это исследование финансировалось Комиссией по науке и технологиям муниципалитета Шанхая, Китай (гранты № 15401971600 и 15pj1401000).
Предраковая дисплазия голосовых связок
Об этой программе
Команда Центра хирургии гортани и голосовой реабилитации Массачусетской больницы общего профиля (Voice Center) установила стандарт лечения дисплазии голосовых связок.За последние 15 лет наша команда усовершенствовала и усовершенствовала лечение, которое описано в группе публикаций. Нас пригласили поделиться и обучить этим инновационным методам в Соединенных Штатах и во всем мире. Основываясь на этом комплексе работ, Голосовой центр получил признание на национальном и международном уровне за свои очень успешные новаторские хирургические методы восстановления и сохранения голоса у пациентов с дисплазией голосовых связок.
О состоянии
В мембранах голосовых связок могут развиться предраковые поверхностные изменения, известные как дисплазия или атипия. На этой стадии у них еще нет рака; однако, если их не лечить, эти пораженные участки могут прогрессировать и стать раковыми. Другие термины, связанные с этим предраковым изменением голосовых связок, включают:
На этой стадии у них еще нет рака; однако, если их не лечить, эти пораженные участки могут прогрессировать и стать раковыми. Другие термины, связанные с этим предраковым изменением голосовых связок, включают:
- Эритроплазия, эритроплакия — красное пятно
- Кератоз – кожное утолщение поверхности
- Лейкоплакия — белое пятно
Большинство пациентов с дисплазией в какой-то момент своей жизни курили, хотя это могло произойти за много лет до развития дисплазии голосовых связок.У небольшой группы некурящих может развиться дисплазия, вызванная вирусом.
Лазер на титанилфосфате калия (KTP)
Когда у пациентов развивается предраковая дисплазия голосовых связок, появляется возможность вылечить заболевание до того, как оно перерастет в рак. Цель состоит в том, чтобы аккуратно удалить больные оболочки голосовых связок с сохранением или восстановлением голоса. Первоначально пациенту планируют отправиться в операционную для осмотра гортани с помощью операционного микроскопа (микроларингоскопия) под общим наркозом. Эта малоинвазивная операция проводится исключительно через рот. Во время процедуры дисплазия обычно подвергается биопсии, а также лечится с помощью импульсного калий-титанил-фосфатного (KTP) лазера. Пациент обычно покидает больницу позже в тот же день, через несколько часов после процедуры.
Эта малоинвазивная операция проводится исключительно через рот. Во время процедуры дисплазия обычно подвергается биопсии, а также лечится с помощью импульсного калий-титанил-фосфатного (KTP) лазера. Пациент обычно покидает больницу позже в тот же день, через несколько часов после процедуры.
Лазерное лечение в офисе
Использование лазера KTP на базе офиса.Для мембран голосовых связок обычно повторно развивается дисплазия после успешного лечения, как у людей с поврежденной солнцем кожей.Команда Mass General Voice Center может лечить рецидивирующую голосовую дисплазию после того, как она была первоначально диагностирована и вылечена в операционной с помощью процедуры в офисе, которая не требует общей анестезии и длится около 20 минут.
Фактически, офисная лазерная хирургия гортани — как для дисплазии голосовых связок, так и для рецидивирующего респираторного папилломатоза гортани, или RRP — была первоначально создана членами команды Mass General Voice Center.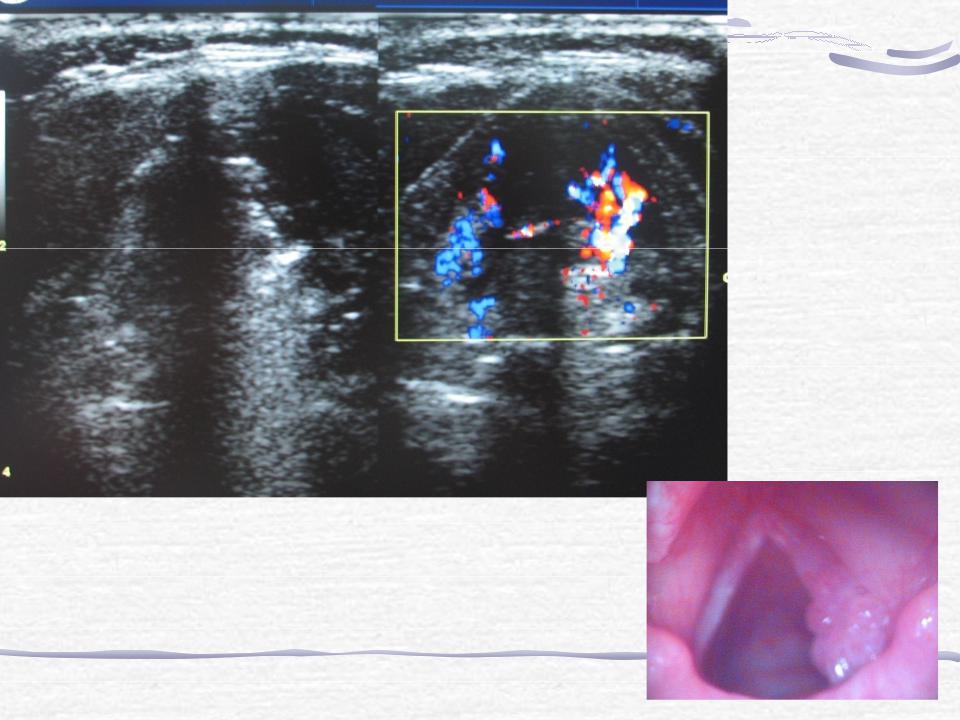
Мы категорически не согласны с философией многих врачей, которые просто наблюдают дисплазию голосовых связок до тех пор, пока она не переродится в рак.Мы считаем, что выжидательное ожидание дисплазии голосовых связок позволяет неконтролируемому перерождению предракового поражения в рак. Наши хирурги разработают программу лечения с учетом индивидуальных особенностей пациента.
Пациент с предраковой дисплазией голосовых связок до (слева) и после (справа) оперативного лечения.
Пациент с предраковой дисплазией голосовых связок до (слева) и после (справа) оперативного лечения.
Пациент с предраковой дисплазией голосовых связок до (слева) и после (справа) хирургического лечения.
Пациент с предраковой дисплазией голосовых связок до (слева) и после (справа) оперативного лечения.
1 из 4
Пример лейкоплакии.
Пример лейкоплакии.
Пример эритроплазии.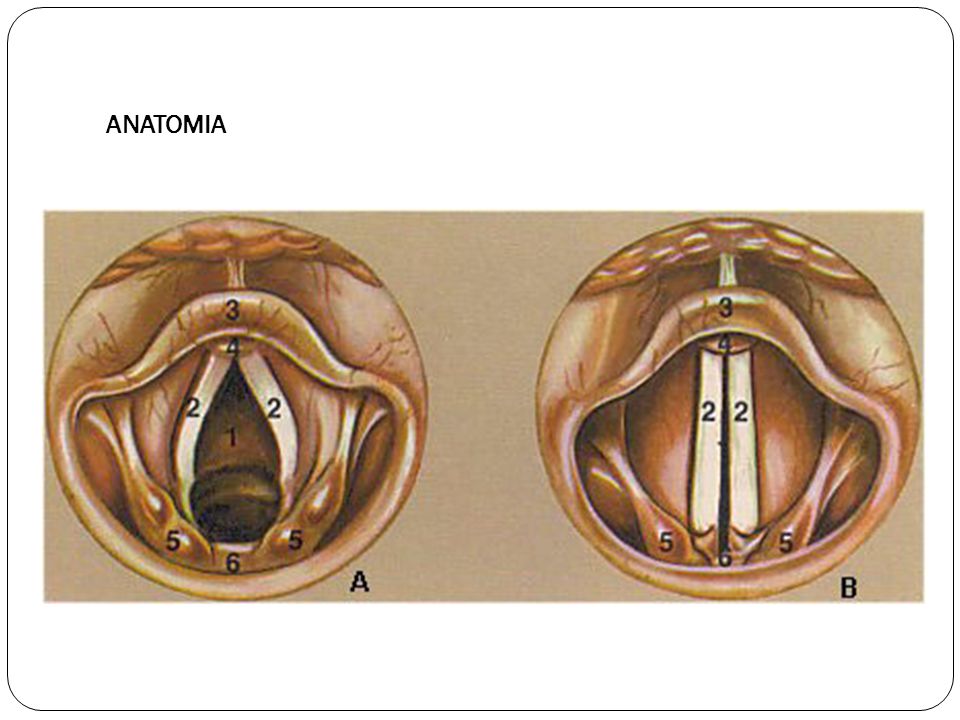
Пример эритроплазии.
1 из 4
(PDF) Лейкоплакия голосовых связок: характеристики и патологическое значение
12
JAYPEE
Yusuf Kizil et al
В англоязычной литературе исследований лейкоплакии голосовых связок
немного.Многие исследования касаются дисплазии голосовых связок и степени злокачественной трансформации
диспластических поражений голосовых связок во времени. Локализация
лейкоплакии голосовых связок на сегодняшний день также малоизучена.
Верхняя поверхность и передние отделы голосовых связок, как сообщается
, в большей степени поражаются дисплазией голосовой щели, но данные
относительно общих локализаций лейкоплакии голосовых связок
, согласно нашим данным, отсутствуют.
15,16
В настоящем исследовании
мы обнаружили, что, как и лейкоплакии, обычно
локализуются в передней и медиальной частях спинного мозга, а
поражение задних отделов встречается редко. Всесторонний обзор
Всесторонний обзор
лейкоплакии гортани, проведенный Isenberg et al., был опубликован в
2008 г.
17
биоптатов лейкоплакии соответственно.Общая частота злокачественной трансформации
составила 8,2% при
дисплазии голосовых связок. Частота злокачественной трансформации в период наблюдения
составила 3,7, 10,1 и 18,1% у пациентов без дисплазии
, с легкой и умеренной дисплазией и с тяжелой дисплазией
соответственно. В этом обзоре авторы не сообщили о частоте рака при первичной биопсии. Суммарная частота
дисплазий и рака in situ в нашем исследовании составляет 48.5%
и соответствует ставкам, указанным в этом обзоре. В нашем исследовании
рак был обнаружен у 18,2 % пациентов с
лейкоплакией голосовых связок и является относительно высоким показателем.
В этом исследовании мы наблюдали, что локализованные и односторонние
поражения в большей степени связаны с развитием рака, однако
эту связь нельзя было подтвердить статистически. Будущие исследования
Будущие исследования
могут показать возможную связь между локализованными поражениями
и повышенным риском развития рака.Сильная связь
тяжелой истории курения с высоким уровнем развития рака
уровня лейкоплакии голосовых связок была задокументирована в
нашем исследовании, так что группа высокого риска четко определена. Хотя
разница не была статистически значимой, мы
рекомендуем биопсию локализованной и односторонней лейкоплакии
сразу же при наличии курения в анамнезе.
ССЫЛКИ
1. Гейл Н., Зидар Н. Доброкачественные и потенциально злокачественные поражения
плоскоклеточного эпителия и плоскоклеточного рака.In:
Cardesa A, Slootweg PJ (Eds). Патология головы и шеи.
Springer, Берлин-Гейдельберг, 2006; 1-29.
2. Карвалью А.Л., Нисимото И.Н., Калифано Дж.А., Ковальски Л.П. Тенденции
заболеваемости и прогноза рака головы и шеи в Соединенных Штатах
: специфический анализ базы данных SEER.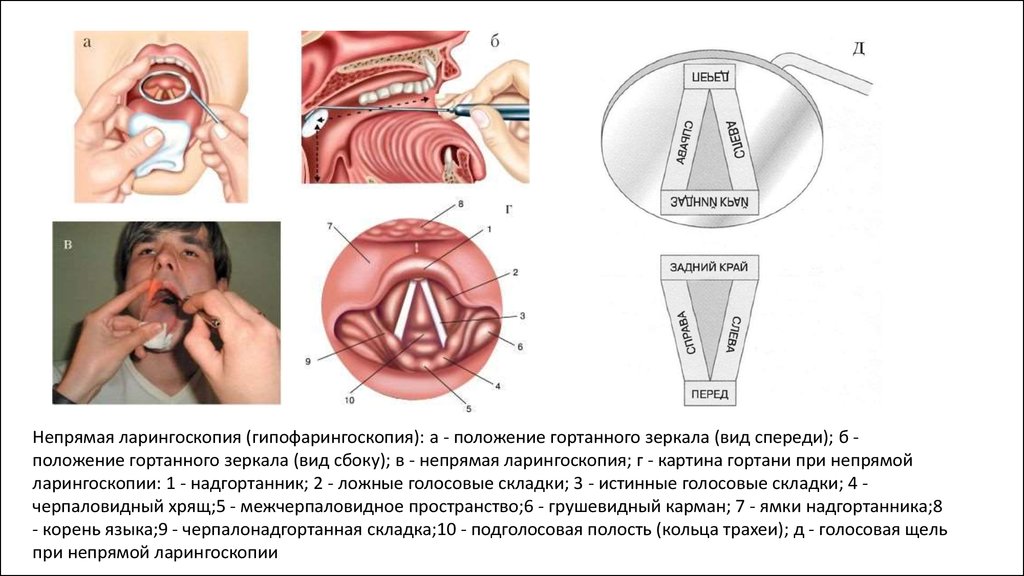 Int J
Int J
Рак 2005;114:806-16.
3. Hellquist H, Cardesa A, Gale N, Kambic V, Michaels L. Критерии
для классификации эпителиальных
гиперпластических поражений гортани по Люблянской классификации.Исследование членов рабочей группы
по эпителиальным гиперпластическим поражениям гортани
Европейского общества патологий. Гистопатология 1999;34:
226-33.
4. Устундаг Э., Каур А.С., Боячи З., Кескин Г., Айдын О. Комбинированное использование гистопатологии
с цитологией сенсорного мазка в биопсиях
гортани. Eur Arch Otorhinolaryngol 2006; 263:
866-71.
5. Kraft M, Glanz H, von Gerlach S, Wisweh H, Lubatschowski
H, Arens C.Клиническое значение оптической когерентной томографии в
ларингологии. Шея головы 2008; 30: 1628-35.
6. Ватанабэ А., Танигучи М., Цудзи Х., Хосокава М., Фудзита М.,
Сасаки С. Значение узкоспектральной визуализации для раннего выявления
рака гортани. Eur Arch Otorhinolaryngol 2009;266:
Eur Arch Otorhinolaryngol 2009;266:
1017-23.
7. Arens C, Reussner D, Woenkhaus J, Leunig A, Betz CS, Glanz
H. Непрямая флуоресцентная ларингоскопия в диагностике
предраковых и раковых поражений гортани.Eur Arch
Otorhinolaryngol 2007;264:621-26.
8. Warnecke A, Averbeck T, Leinung M, Soudah B, Wenzel GI,
Kreipe HH, Lenarz T, Stöver T. Контактная эндоскопия для
оценки слизистой оболочки глотки и гортани.
Ларингоскоп 2010;120:253-58.
9. Malzahn K, Dreyer T, Glanz H, Arens C. Аутофлуоресценция
эндоскопия в диагностике раннего рака гортани и его
поражений-предшественников. Ларингоскоп 2002;112:488-93.
10. Issing WJ, Struck R, Naumann A. Долгосрочное наблюдение
лейкоплакии гортани при лечении ретинилпальмитатом. Шея головы
1996;18:560-65.
11. Симпсон С.Б., Арчилла А.С., Веласкес Р.А., Макгафф Х.С.
Разрешение лейкоплакии голосовых складок с помощью ингибитора протонной помпы
Терапия. Ухо, горло, нос, J 2006; 85: 362–64.
Ухо, горло, нос, J 2006; 85: 362–64.
12. Minni A, Barbaro M, Rispoli G, Diaferia F, Bernardeschi D,
Filipo R. Лечение с помощью лазера CO
2
кордэктомия и клинические
последствия в лечении предрака гортани легкой и средней степени тяжести
Eur Arch Otorhinolaryngol 2008; 265:189-93.
13. Gallo A, de Vincentiis M, Della Rocca C, Moi R, Simonelli M,
Minni A, Shaha AR. Эволюция предраковых поражений гортани
: клинико-патологическое исследование с длительным наблюдением за
259 пациентами. Шея головы 2001; 23:42-47.
14. Садри М., МакМахон Дж., Паркер А. Лечение дисплазии гортани
: обзор. Eur Arch Otorhinolaryngol 2006;263:
843-52.
15. Лахав Ю., Бернс Дж.А., Файнберг С., Хитон Дж.Т., Зейтельс С.М.Начальная
анатомо-географическая картина дисплазии голосовой щели. Ann Otol
Rhinol Laryngol 2009;118:321-25.
16. Цейтельс С.М. Предраковый эпителий и микроинвазивный рак
голосовых складок: эволюция фономикрохирургического
лечения. Ларингоскоп 1995;105(S1):1-44.
Ларингоскоп 1995;105(S1):1-44.
17. Изенберг Дж.С., Крозье Д.Л., Дейли С.Х. Институциональный и
комплексный обзор лейкоплакии гортани. Ann Otol
Rhinol Laryngol 2008;117:74-79.
. , MD запустила программы «Новое направление» и «Перспективы» в феврале 2003 года в Медицинской группе Джефферсон-Сити. До того, как открыть свою практику в Джефферсон-Сити, доктор Кейс работал в программе «Новое направление», получая стипендию и проводя исследования в Медицинском колледже Бэйлора в Хьюстоне, штат Техас.Он был настолько впечатлен медицинскими улучшениями участников программы, что был вынужден найти способ предоставлять такие услуги в сочетании со своей местной практикой. Мы с гордостью сообщаем, что всего через год работы наша программа была признана корпорацией Robard как Центр передового опыта.
Доктор Кристофер Кейс также вносит свой вклад на национальном уровне; он является членом медицинской консультативной группы, которая обеспечивает руководство, обучение и экспертизу для руководящих принципов программы New Direction and Outlook под медицинским наблюдением Робарда.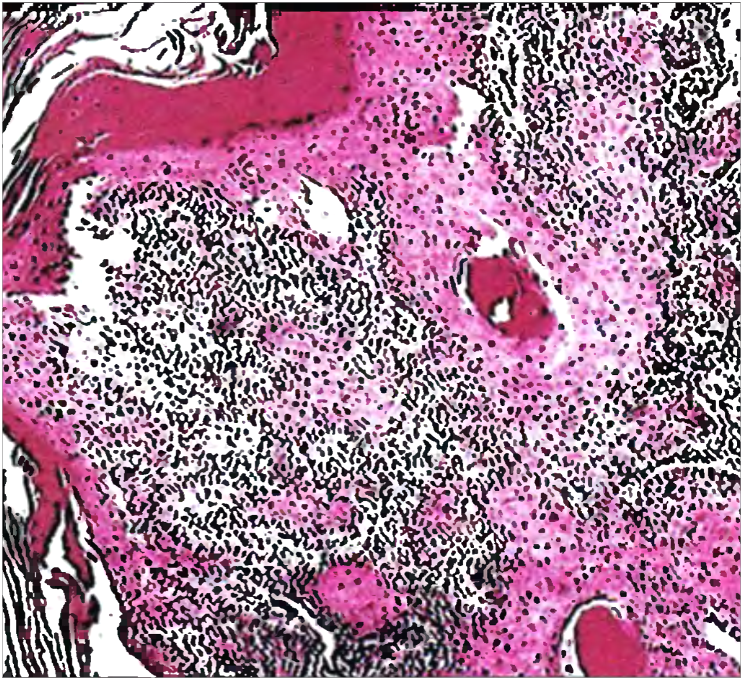
Мы гордимся тем, что у нас есть квалифицированные и преданные своему делу сотрудники, которые сотрудничают с нами, чтобы обеспечить сострадательный, чуткий и исключительный уход за участниками нашей программы. В дополнение к нашим наблюдающим врачам, наш штат состоит из зарегистрированных диетологов, бихевиористов и административного помощника — все они посвящены поддержке участников нашей программы, когда они открывают для себя более здоровую, сбалансированную и счастливую жизнь!
Позвоните нам, чтобы узнать больше!
Познакомьтесь с координатором нашей программы Адамом Уивером
Адам Уивер присоединился к команде Центра лечения лишнего веса JCMG в качестве координатора нашей клиники осенью 2021 года.Он страстно любит здоровье и хорошее самочувствие, всегда ставя общее психическое и физическое здоровье своих пациентов превыше всего. Вот что он говорит:
Выросший в Мид-Миссури, я был очарован сильными корнями сельского хозяйства в нашем штате. Я вспоминаю бескрайние кукурузные и соевые поля вдоль шоссе Миссури, когда наши семейные поездки проходили по дну рек Среднего Запада. В то время я не оценил пленительный мир сельского хозяйства.
Я вспоминаю бескрайние кукурузные и соевые поля вдоль шоссе Миссури, когда наши семейные поездки проходили по дну рек Среднего Запада. В то время я не оценил пленительный мир сельского хозяйства.
От семян до фруктов, сельское хозяйство и питание объединяет общая тема: продукты питания.Именно в школьные годы я осознал существенную связь между этими двумя понятиями. В то время я изо всех сил пытался понять концепции питания в своих усилиях «быть здоровее».
По мере того, как я начинала терять связь с едой, во мне росло жгучее желание и любопытство узнать больше о питании и здоровье. Во время учебы в магистратуре Получив диплом диетолога в Университете Миссури, я также обнаружил страсть к обучению и поддержке других в их стремлении к здоровью.Я нашел это особенно полезным в практической области медицинского управления весом.
Как зарегистрированный диетолог я знаю, что существует множество факторов, влияющих на управление весом, а не только еда и физические упражнения. Эти факторы вступают в игру на протяжении всего нашего юношеского начала и продолжаются во взрослой жизни. Факторы могут включать генетику, гормоны, лекарства, поведение, сон, стресс и, конечно же, выбор продуктов питания. Несмотря на то, что эти области деятельности имеют большое значение, также верно и то, что каждый человек имеет уникальную историю и опыт в отношении еды.Таким образом, можно себе представить, что не существует шаблонного подхода к долгосрочному успешному управлению весом.
Эти факторы вступают в игру на протяжении всего нашего юношеского начала и продолжаются во взрослой жизни. Факторы могут включать генетику, гормоны, лекарства, поведение, сон, стресс и, конечно же, выбор продуктов питания. Несмотря на то, что эти области деятельности имеют большое значение, также верно и то, что каждый человек имеет уникальную историю и опыт в отношении еды.Таким образом, можно себе представить, что не существует шаблонного подхода к долгосрочному успешному управлению весом.
Подобно мультидисциплинарному аспекту нашего личного отношения к еде, междисциплинарный подход к снижению веса является эффективной стратегией для достижения долгосрочного успеха. При различной степени факторов, влияющих на управление весом, «балансирование» еды и питания может быть затруднено. Теперь, занимая должность координатора Центра лечения лишнего веса в JCMG, я еще раз свидетельствую о ценности междисциплинарной команды врачей, медсестер, психологов и дипломированных диетологов, работающих с клиентами для изучения их отношений с едой и здоровьем.

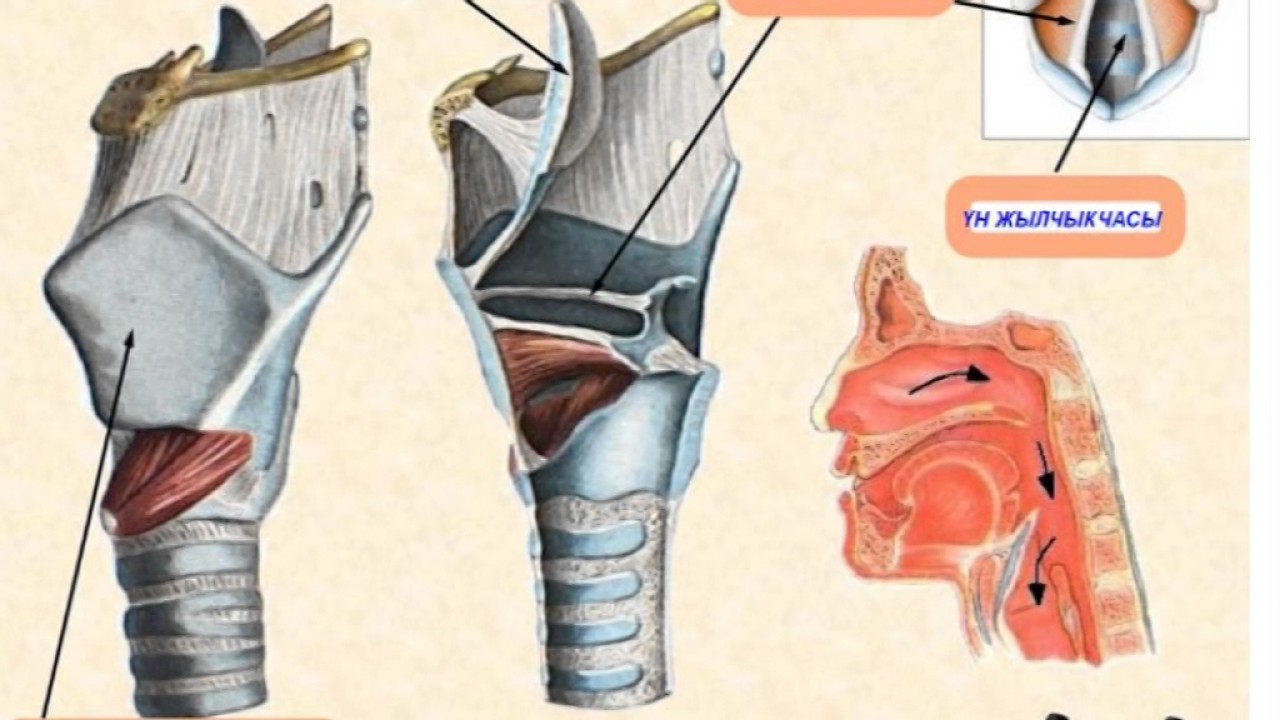

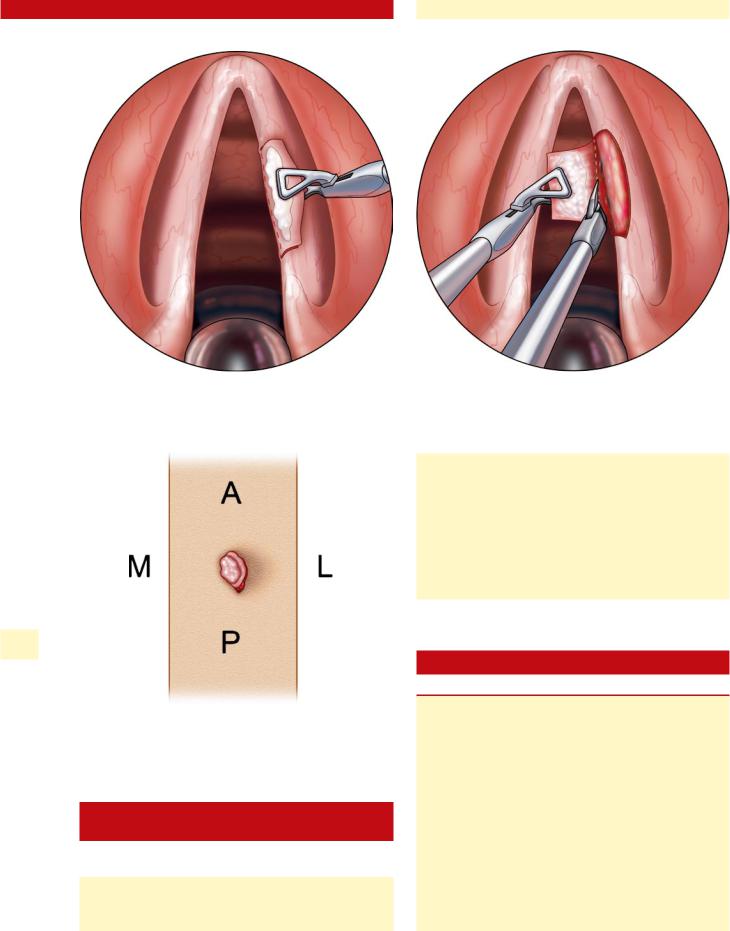
 патологии складок, включая узелки, кисты, полипы, гранулемы, лейкоплакию и субэпителиальные отек. После операции на голосовых связках принято предписывать пациентам отдых для голоса. однако, согласно современной литературе, не известно, как долго пациенты должны норм голосовой покой после фонохирургии (независимо от типа доброкачественного поражения) чтобы добиться наилучшего качества передачи голоса. В литературе есть одно предварительное исследование, которое показывает, что при оценке качества голоса через 15 дней после операции пациенты с голосовой отдых в течение 10 дней давал лучшие результаты по сравнению с пациентом с 5-дневным голосом отдых (1). Противоречивое исследование, в котором измерялись голосовые исходы у пациентов 1, 3 и 6 лет. месяцев после операции, показывает, что короткий голосовой отдых в течение 3 дней приводит к лучшим голосовым результатам по сравнению с 7-дневным отдыхом для голоса (2). Целью нашего исследования является определение оптимальной продолжительности (3 против 7 дней) голосового отдыха.
патологии складок, включая узелки, кисты, полипы, гранулемы, лейкоплакию и субэпителиальные отек. После операции на голосовых связках принято предписывать пациентам отдых для голоса. однако, согласно современной литературе, не известно, как долго пациенты должны норм голосовой покой после фонохирургии (независимо от типа доброкачественного поражения) чтобы добиться наилучшего качества передачи голоса. В литературе есть одно предварительное исследование, которое показывает, что при оценке качества голоса через 15 дней после операции пациенты с голосовой отдых в течение 10 дней давал лучшие результаты по сравнению с пациентом с 5-дневным голосом отдых (1). Противоречивое исследование, в котором измерялись голосовые исходы у пациентов 1, 3 и 6 лет. месяцев после операции, показывает, что короткий голосовой отдых в течение 3 дней приводит к лучшим голосовым результатам по сравнению с 7-дневным отдыхом для голоса (2). Целью нашего исследования является определение оптимальной продолжительности (3 против 7 дней) голосового отдыха. после фонохирургии для пациентов, перенесших из-за доброкачественного фонохирургии голосовых связок для улучшения качества голоса в послеоперационном периоде. В этом исследовании пациенты будут случайным образом распределяется по одной из 2 разных групп продолжительности голосового отдыха: 3 или 7 дней после операции. Пациентам будет выполнено голосование до и после операции (через 1, 3 и 6 месяцев). тестирование. Тестирование качества голоса будет: перцепционный анализ голоса с использованием GRABS. шкала (оценка, грубость, астения, одышка, напряжение), Индекс нарушения голоса-10 (ДМС) анкета, измерение количества времени звучания (MPT) и компьютерный анализ голоса включая интенсивность голоса, основную частоту (F0), дрожание, мерцание и дисфонию индекс серьезности (DSI).
после фонохирургии для пациентов, перенесших из-за доброкачественного фонохирургии голосовых связок для улучшения качества голоса в послеоперационном периоде. В этом исследовании пациенты будут случайным образом распределяется по одной из 2 разных групп продолжительности голосового отдыха: 3 или 7 дней после операции. Пациентам будет выполнено голосование до и после операции (через 1, 3 и 6 месяцев). тестирование. Тестирование качества голоса будет: перцепционный анализ голоса с использованием GRABS. шкала (оценка, грубость, астения, одышка, напряжение), Индекс нарушения голоса-10 (ДМС) анкета, измерение количества времени звучания (MPT) и компьютерный анализ голоса включая интенсивность голоса, основную частоту (F0), дрожание, мерцание и дисфонию индекс серьезности (DSI).
 Обратите внимание, что, несмотря на небольшое поверхностное созревание, диагноз по-прежнему остается карциномой in situ.
Обратите внимание, что, несмотря на небольшое поверхностное созревание, диагноз по-прежнему остается карциномой in situ.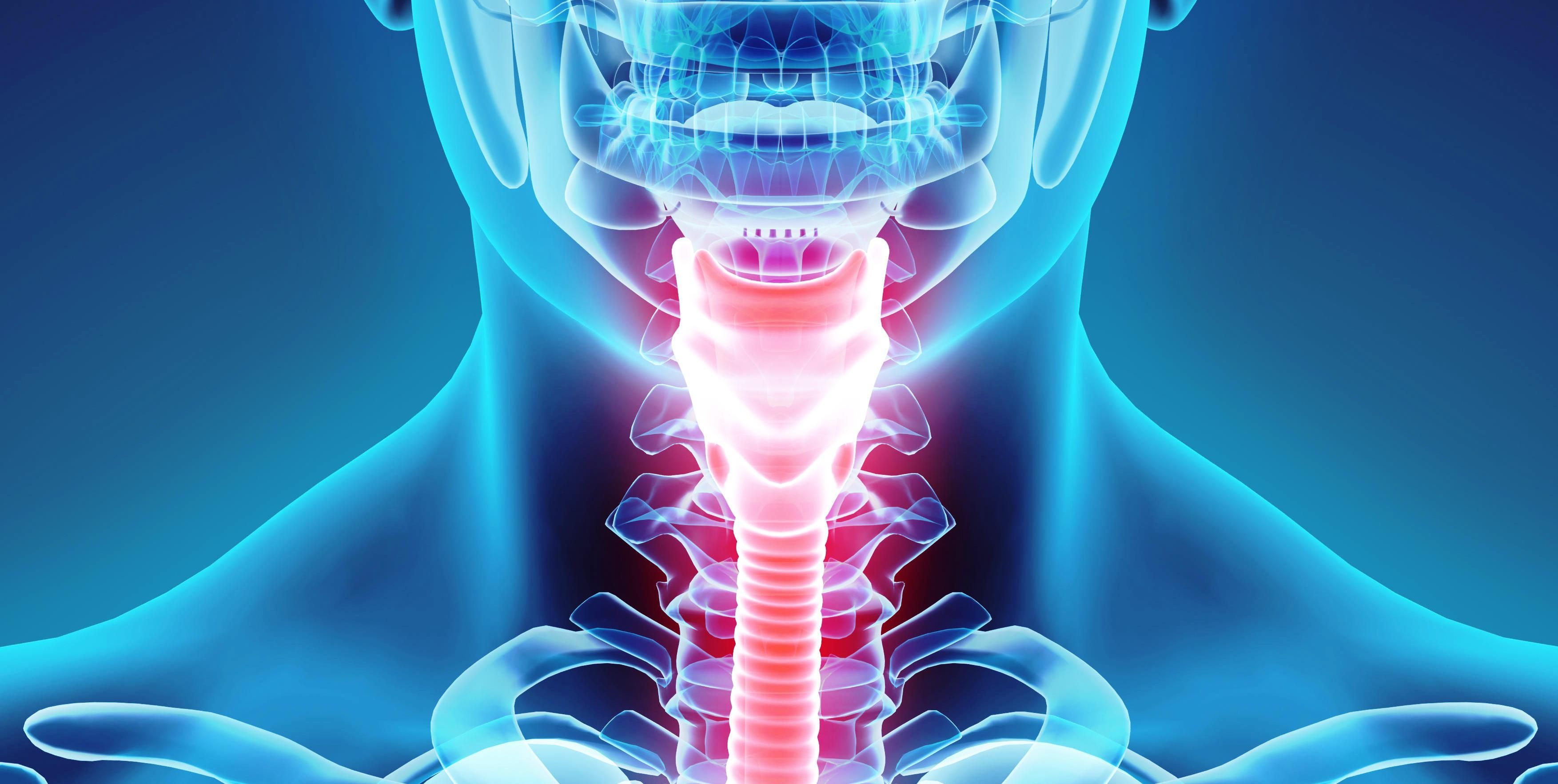 132 на
132 на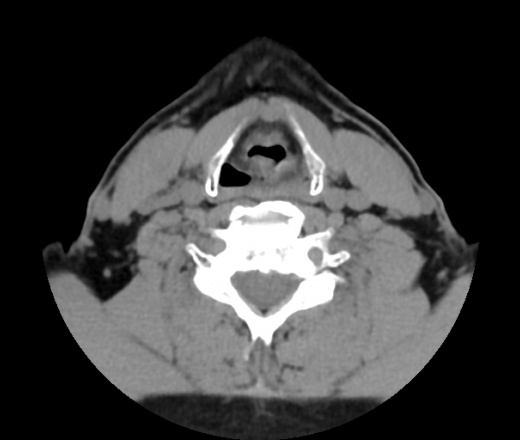 3%)
3%) Другие факторы, в том числе пол, возраст, курение, употребление алкоголя, ларингофарингеальный рефлюкс, нарушение голоса и место поражения, оказались незначительными при клиническом ответе (таблица 4).
Другие факторы, в том числе пол, возраст, курение, употребление алкоголя, ларингофарингеальный рефлюкс, нарушение голоса и место поражения, оказались незначительными при клиническом ответе (таблица 4). 447
447