Заболевание лейшманиоз: причины появления, симптомы заболевания, диагностика и способы лечения
Что такое Лейшманиоз? Симптомы, диагностика, лечение, профилактика
09.12.2020
Мы продолжаем рассказывать о простейших, которые могут вызывать у человека самые разнообразные заболевания. Казалось бы — одноклеточный организм! Но все не так просто, как нам хотелось бы.
Одним из таких заболеваний является лейшманиоз — звучит жутко, но из названия понятно, что вызывается он простейшими рода Leishmania.
Лейшманиозы распространены по всему миру — инфекция у человека вызывается 20 видами Leishmania!
В зависимости от географии, они делятся на лейшманиозы Нового и Старого Света. В зависимости же от клинических проявлений — при поражении только кожи, кожи и слизистых оболочек или внутренних органов — они подразделяются на кожную, кожно-слизистую и висцеральную форму болезни соответственно.
Возбудителями кожного лейшманиоза являются L.L. major, L.L. tropica (Центральная и Юго-восточная Азия, средний Восток, Африка), L. L. aethiopica (Эфиопия, Кения, Уганда), L.L. mexicana, L.V. braziliensis (Центральная и Южная Америка, Мексика, Перу и Аргентина), L.V. guyanensis (Панама, Коста-Рика, Эквадор, Перу, Венесуэла). Последние 4 группы из них способны вызвать диффузные кожные лейшманиозы и кожно-слизистые формы заболевания. Висцеральные формы лейшманиоза чаще всего вызывают L.L. infantum, L.L. donovani (Средиземноморье, Северная Африка, Ближний Восток, Центральная и Юго-Западная Азия, Балканы, Китай, Индия, Китай, Пакистан, Центральная и Южная Америка).
L. aethiopica (Эфиопия, Кения, Уганда), L.L. mexicana, L.V. braziliensis (Центральная и Южная Америка, Мексика, Перу и Аргентина), L.V. guyanensis (Панама, Коста-Рика, Эквадор, Перу, Венесуэла). Последние 4 группы из них способны вызвать диффузные кожные лейшманиозы и кожно-слизистые формы заболевания. Висцеральные формы лейшманиоза чаще всего вызывают L.L. infantum, L.L. donovani (Средиземноморье, Северная Африка, Ближний Восток, Центральная и Юго-Западная Азия, Балканы, Китай, Индия, Китай, Пакистан, Центральная и Южная Америка).
Лейшманиозы — группа трансмиссивных заболеваний, это значит, что они передаются через укусы насекомых, в частности при укусах москитов видов Phlebotomus, Lutzomyia в зависимости опять же от географии. Источником инфекции и резервуаром являются человек и различные виды животных грызуны, собаки и другие — это также зависит от видов лейшманий и географического положения.
После укуса москита лейшмании могут либо оставаться в пределах кожи ограниченно или диффузно, либо распространяться на слизистые оболочки — в основном носа, ротоглотки, либо через лимфатическую систему разноситься к другим органам и тканям организма — проникать в селезенку, костный мозг, печень, кишечник и др.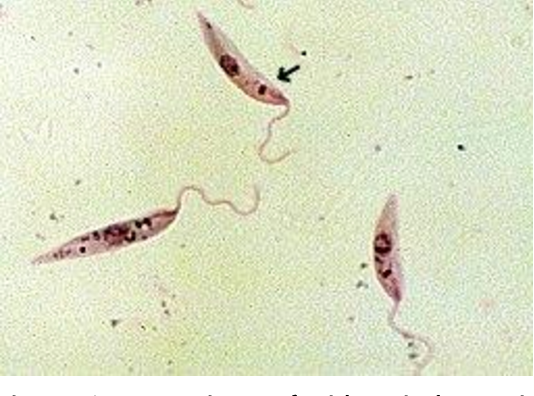
Кожный лейшманиоз.
Поражение кожи развивается на месте укуса москита через несколько недель или даже месяцев. Множественные поражения кожи могут быть результатом неоднократных укусов. Изначально это папула, которая медленно увеличивается, в центре образуется язвочка и развивается приподнятая эритематозная граница, где сконцентрированы внутриклеточные паразиты. Язвочки чаще всего безболезненны, но присоединение вторичной бактериальной флоры может привести к прогрессированию заболевания и нагноению. Изъязвления обычно заживают спонтанно через несколько месяцев, но могут сохраняться в течение многих лет.
Диффузный кожный лейшманиоз.
Диффузная форма кожного лейшманиоза развивается редко, в основном лейшманиями Нового Света. Характеризуется распространенным утолщением кожи в форме бляшек, папул или множественных узелковых образований, особенно на лице и наружней повержности конечностей, напоминая поражения при лепре. Изъязвления и поражение слизистых оболочек чаще отсутствуют, но болезнь не проходит спонтанно и отличается склонностью к рецидивам после лечения.
Кожно-слизистый лейшманиоз.
Начинается с первичной кожной язвочки, как и другие формы кожного лейшманиоза. Это поражение кожи проходит спонтанно. Метастатическое распространение процесса на слизистые оболочки носа, ротоглотки могут произойти как на ранней стадии болезни, так и спустя многие годы. Патогенетически при данном процессе происходит разрушение мягких тканей и хрящей, отек носа и губ. Как правило, у пациентов появляются заложенность носа, выделения и боль. Но болевой синдром может отсутствовать.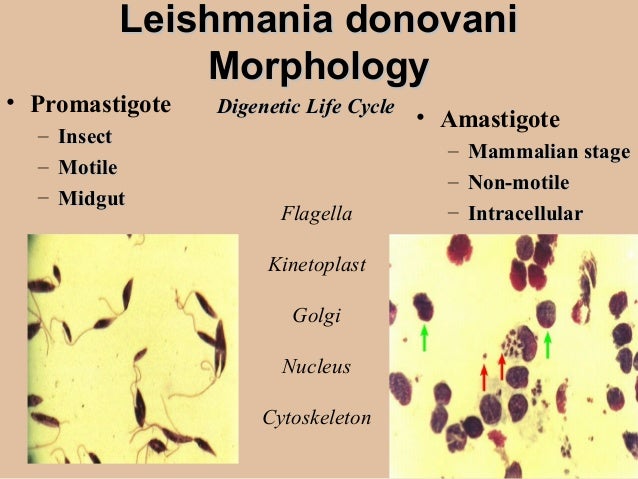 Со временем развиваются массивные поражения носа, неба или лица, обезображивающие больного. Опасно присоединение вторичной бактериальной инфекции. Летальные исходы у таких пациентов наступают из-за бактериальных осложнений и истощения.
Со временем развиваются массивные поражения носа, неба или лица, обезображивающие больного. Опасно присоединение вторичной бактериальной инфекции. Летальные исходы у таких пациентов наступают из-за бактериальных осложнений и истощения.
Висцеральный лейшманиоз.
Клинические проявления могут развиться остро (например при иммунодефицитных состояниях), но могут начать проявляться через многие месяцы. Некоренные жители могут заразиться при посещение эндемичных районов — в таком случае инкубационные=й период может длиться до 2 лет.
Характерны волнообразная лихорадка с ознобом, чаще всего два пика температуры в течение суток, гепатоспленомегалия, лимфаденопатия, истощение, отеки. Лабораторно выявляются панцитопения, гипоальбуминемия, гипергаммаглобулинемия, нарушение свертываемости крови. Поражения кожи встречаются редко. Нередко присоединяется вторичная бактериальная инфекция. При несвоевременном неадекватном лечении или его отсутствии в течение нескольких месяцев-лет наступает летальный исход.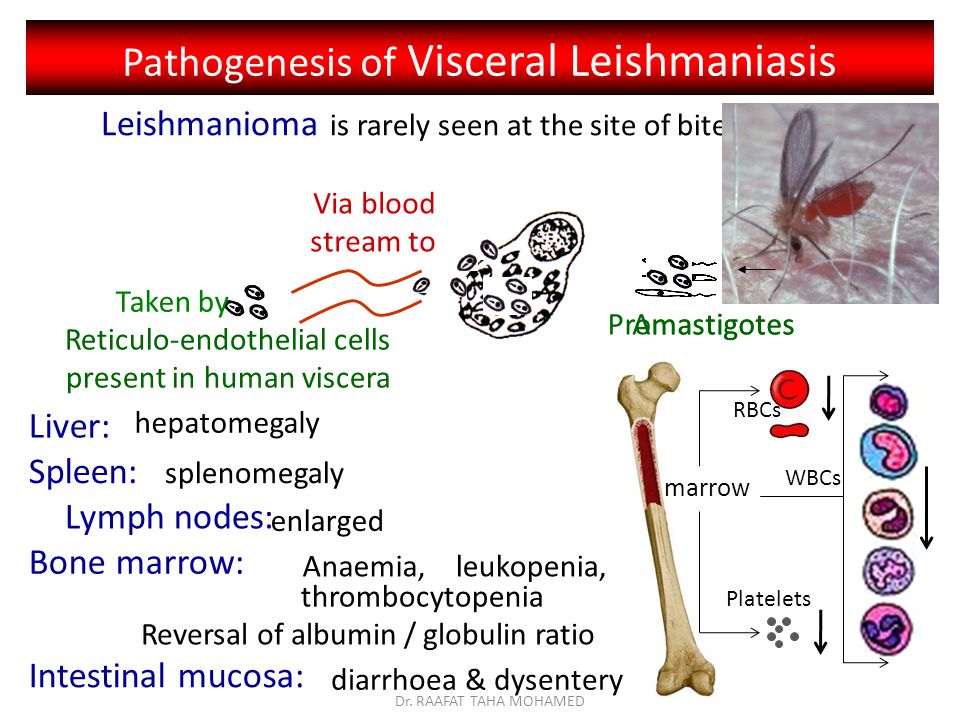
У пациентов, у которых нет клинических проявлений (например жители эндемичных районов), либо наступает самоизлечение, либо у оставшихся в живых после успешного лечения, наблюдается резистентность к дальнейшим заражениям — формируется стойкий иммунитет. Однако возможно возникновение рецидива болезни через многие годы.
В Индии висцеральный лейшманиоз называют “кала-азар” или “черная болезнь”, так как из-за поражения надпочечников часто отмечается потемнение кожи лица, рук, живота, стоп. Примерно у 10% таких больных через несколько месяцев и до двух лет возникает посткалаазарный кожный лейшманиоз — поражение характеризуется плоскими или узловыми повреждениями кожи, в которых содержится множество паразитов — эти поражения считаются резервуаром, они способствуют распространению инфекции в этих областях.
При подозрении на лейшманиоз любой формы для подтверждения диагноза могут быть использованы следующие методы диагностики:
-
Микроскопия и ПЦР-исследование пунктатов органов и тканей, соскоба с пораженной области кожи
-
-
Серологическое исследование (ИФА IgG) применяется при подозрении на висцеральный лейшманиоз, но стоит помнить, что возможно получение как ложноотрицательных результатов (например, при ВИЧ-инфекции, при раннем и пожилом возрастах), так и ложноположительных (СКФ, лейкоз, сифилис, и др.
 ). При этом серологические исследования не проводятся для определения эффективности проводимого лечения — это связано с длительным обнаружением IgG в крови после излечения.
). При этом серологические исследования не проводятся для определения эффективности проводимого лечения — это связано с длительным обнаружением IgG в крови после излечения.
-
Также может быть информативным культуральное исследование пунктатов — посев на специальные среды.
Лечение лейшманиоза является сложным, что в некоторой степени обусловлено возрастающей резистентностью микроорганизмов к применяемым препаратам. Выбор препаратов зависит от следующих факторов:
-
Клинический синдром
-
Подтвержденный диагноз лейшманиоза
-
Географический регион (место заражения)
-
Вероятная восприимчивость микроорганизма к лечению
-
Иммунный статус хозяина (иммунодефицитные состояния)
Подходы к лечению кожного и висцерального лейшманиоза сильно отличаются. При кожном лейшманиозе имеет большое значение клиническая тяжесть инфекции, например при кожном ограниченном лейшманиозе без риска возникновения проявления со стороны слизистых оболочек может применяться только местная терапия, в то время как при кожно-слизистом или диффузном кожном лейшманиозах необходима системная терапия. В случае висцерального лейшманиоза кала-азар при отсутствии лечения летальность составляет до 90%, здесь не стоит вопрос о необходимости терапии, выбор препаратов основан на доступности и сведениях о резистентности. А при развитии лейшманиоза на фоне прогрессирующей ВИЧ-инфекции требуется не только системная терапия противопаразитарными препаратами, но и скорейшее начало антиретровирусной терапии, без которой клинический эффект от проводимой терапии будет недостаточен.
При кожном лейшманиозе имеет большое значение клиническая тяжесть инфекции, например при кожном ограниченном лейшманиозе без риска возникновения проявления со стороны слизистых оболочек может применяться только местная терапия, в то время как при кожно-слизистом или диффузном кожном лейшманиозах необходима системная терапия. В случае висцерального лейшманиоза кала-азар при отсутствии лечения летальность составляет до 90%, здесь не стоит вопрос о необходимости терапии, выбор препаратов основан на доступности и сведениях о резистентности. А при развитии лейшманиоза на фоне прогрессирующей ВИЧ-инфекции требуется не только системная терапия противопаразитарными препаратами, но и скорейшее начало антиретровирусной терапии, без которой клинический эффект от проводимой терапии будет недостаточен.
Почему важно знать о лейшманиозе?
География путешествий человека расширяется, но для того, чтобы увеличить риск заражения лейшманиозом, не обязательно лететь в южную Африку. Риск заражения лейшманиозом остается при посещении стран ближнего зарубежья: Азербайджана, Армении, Грузии, Кыргызстана, Таджикистана, Узбекистана в пик активности переносчиков возбудителя. В России регистрируются только завозные случаи лейшманиоза. Инкубационный период развития заболевания у туристов может достигать нескольких лет, поэтому очень важны сведения о посещении и длительности пребывания на тех или иных эндемичных территориях, а также указания на взаимодействия с москитами и другими вредными насекомыми :)
Риск заражения лейшманиозом остается при посещении стран ближнего зарубежья: Азербайджана, Армении, Грузии, Кыргызстана, Таджикистана, Узбекистана в пик активности переносчиков возбудителя. В России регистрируются только завозные случаи лейшманиоза. Инкубационный период развития заболевания у туристов может достигать нескольких лет, поэтому очень важны сведения о посещении и длительности пребывания на тех или иных эндемичных территориях, а также указания на взаимодействия с москитами и другими вредными насекомыми :)
Специфической профилактики не разработано, поэтому путешественникам в эндемичных областях на открытые участки кожи следует использовать средства от насекомых, содержащие диэтилтолуамид, пропитывать одежду репеллентами. Также могут быть эффективны противомоскитные сетки, сетки на кроватях, особенно если пропитать их перметрином или пиретрумом.
Услуги, упомянутые в статье*:
-
Микроскопическое исследование соскобов с кожи, папул и краев язв на лейшмании (А26.

-
Микроскопическое исследование пунктатов органов кроветворения на лейшмании (А26.05.014)
-
Определение антител класса G к возбудителю лейшманиоза в крофи методом ИФА
-
Определение ДНК лейшманий в крови методом ПЦР (А26.06.053.s01)
*Назначение и интерпретация результатов анализов должны проводиться только лечащим врачом
Автор: врач-инфекционист Университетской клиники H-Clinic Анастасия Александровна Коновалова.
Медицинский редактор: руководитель Университетской клиники, к.м.н., врач-инфекционист Коннов Данила Сергеевич.
Возврат к списку
ГБУ РО «ЦГБ им. Н.А. Семашко» в г. Ростове-на-Дону
Лейшманиозы — заболевания, вызываемые паразитическими простейшими из рода Leischmania. Первые клинические описания болезни появились в европейской медицинской литературе в середине XVIII века. В 1898 г. русский военный врач П. Ф. Боровский открыл возбудителя кожного лейшманиоза (болезнь Боровского),
В 1898 г. русский военный врач П. Ф. Боровский открыл возбудителя кожного лейшманиоза (болезнь Боровского),
в 1900 г. Лейшман, а в 1903 г. Донован обнаружили возбудителя висцерального лейшманиоза(кала-азара).
Распространение лейшманиозов москитами установлено в 1921 г. Ежегодно в мире болеют лейшманиозами не менее 60 млн. человек.
Этиология лейшманиозов.
Возбудитель кожного лейшманиоза — Leishmania tropica. Есть две разновидности возбудителя кожного лейшманиоза: L. tropica minor, что вызывает кожный лейшманиоз антропонозного (городского) типа и L. tropica major, обуславливающий кожный лейшманиоз зоонозного (сельского) типа.
Возбудитель средиземноморского висцерального лейшманиоза — L. donovani infantum. Лейшмании относятся к типу простейших.
Цикл развития лейшманий связан со сменой хозяев — позвоночного животного (человека), в организме которого паразиты находятся в безжгутиковой форме, и кровососущего насекомого (москита), где лейшмании переходят в жгутиковую форму.
Москиты заражаются при сосании крови или межтканевой жидкости зараженных лейшманиозом животных (человека). В организме москита происходит размножение лейшманий, и спустя 6-8 дней паразиты скапливаются в глотке москита, откуда при укусе человека проникают в ранку, внедряются в клетки кожи или внутренних органов (в зависимости от вида лейшманий).
Эпидемиология. Средиземноморско-среднеазиатский лейшманиоз — зоонозное заболевание. Различают три типа очагов:
1. природные очаги, в которых возбудитель циркулирует среди диких животных (шакалы, лисицы, суслики и др. грызуны), являющихся источником инвазии;
2. сельские очаги, в которых возбудитель циркулирует у собак -главных источников инвазии, а также у диких животных;
3. городские (синантропные) очаги, в которых основным источником инвазии служат собаки и синантропные крысы.
Переносчики — различные виды москитов — флеботомусы.
Болеют в основном дети в возрасте от 1 года до 5 лет, а также взрослые — приезжие из неэндемичных районов.
Заболеваемость носит спорадический характер; в городах возможны вспышки. Сезон заражения — лето, а сезон заболеваемости — осень этого года или весна следующего.
Очаги регистрируются в странах Средиземноморья, Китая, Ближнего Востока, Латинской Америки.
Спорадические случаи регистрируются в Средней Азии и Закавказье: Туркменистан, юг Казахстана, Грузия, Армения, Азербайджан.
Зоонозный кожный лейшманиоз. Источниками инфекции являются животные: песчанки, тонкопалый суслик, домовые мыши, ежи. Заражение человека происходит в конце лета — начале осени — в период максимальной численности москитов.
Инкубационный период от 2 до 6 нед, затем на месте внедрения возбудителя образуется небольшой бугорок, в последующем изъязвляющийся, в дальнейшем язвы рубцуются. Таких образований может быть несколько. В неосложненных случаях заболевание продолжается 2-4 мес. После заболевания остается стойкий иммунитет.
Это природно-очаговая инфекция, очаги расположены в сельской местности. Из местного населения заболевают преимущественно дети, поскольку взрослые ранее перенесли эту болезнь. Среди приезжих и солдат могут быть массовые заболевания кожным лейшманиозом. Например, в 1885 г. в отряде русских войск, прибывших в Мервский оазис, заболело кожным лейшманиозом 85% личного состава.
Из местного населения заболевают преимущественно дети, поскольку взрослые ранее перенесли эту болезнь. Среди приезжих и солдат могут быть массовые заболевания кожным лейшманиозом. Например, в 1885 г. в отряде русских войск, прибывших в Мервский оазис, заболело кожным лейшманиозом 85% личного состава.
Антропонозный (городской) кожный лейшманиоз. Инкубационный период от 2 мес до 2 лет. Стадия бугорка и инфильтрата продолжается 4-6 мес, стадия язвы — 6 мес, период рубцевания — 1-2 мес. Общая продолжительность болезни до 1 года. В месте поражения очень много лейшманий. Иммуногенез замедлен. Оба варианта кожного лейшманиоза дают перекрестный иммунитет. Источником инфекции является человек, однако не исключается роль собак и грызунов. Заболеваемость носит выраженный очаговый характер: поражаются жители определенных кварталов, домов. Сезонность не выражена.
В настоящее время эта болезнь у нас практически ликвидирована.
Средиземноморский висцеральный лейшманиоз
Длительность инкубационного периода колеблется от 10-20 дней до 1 года. Заболевание начинается с появлением папулы на месте укуса москита. Отсюда лейшмании гематогенно попадают в клетки ретикулоэндотелиальной системы. Развивающийся системный паразитарный ретикулоэндотелиоз приводит к увеличению печени, селезенки, лимфатических узлов и нарушению их функции. Отмечается общая интоксикация, нарушение кроветворения и аллергизация организма. Заболевание протекает на фоне лихорадки. Нелеченый висцеральный лейшманиоз часто имеет летальный исход.
Заболевание начинается с появлением папулы на месте укуса москита. Отсюда лейшмании гематогенно попадают в клетки ретикулоэндотелиальной системы. Развивающийся системный паразитарный ретикулоэндотелиоз приводит к увеличению печени, селезенки, лимфатических узлов и нарушению их функции. Отмечается общая интоксикация, нарушение кроветворения и аллергизация организма. Заболевание протекает на фоне лихорадки. Нелеченый висцеральный лейшманиоз часто имеет летальный исход.
В городах источниками инфекции являются собаки, а в сельской местности — шакалы, лисы, дикобразы. Заражения происходят летом, но ввиду длительности инкубационного периода заболевания чаще возникают в холодное время года. Среди заболевших 80-90% приходится на детей до 3 лет.
Осложнения кожного лейшманиоза
Возможно инфицирование язв вторичной бактериальной флорой, что затягивает выздоровление, может привести к развитию рожи, абсцесса. Прогноз благоприятный, возможны косметические дефекты.
Диагноз кожный лейшманиоз
Опорными симптомами клинической диагностики кожного лейшманиоза является образование на месте укуса москита папулы с последовательным превращением в лейшмании, язву с подрытыми краями и последующим рубцеванием.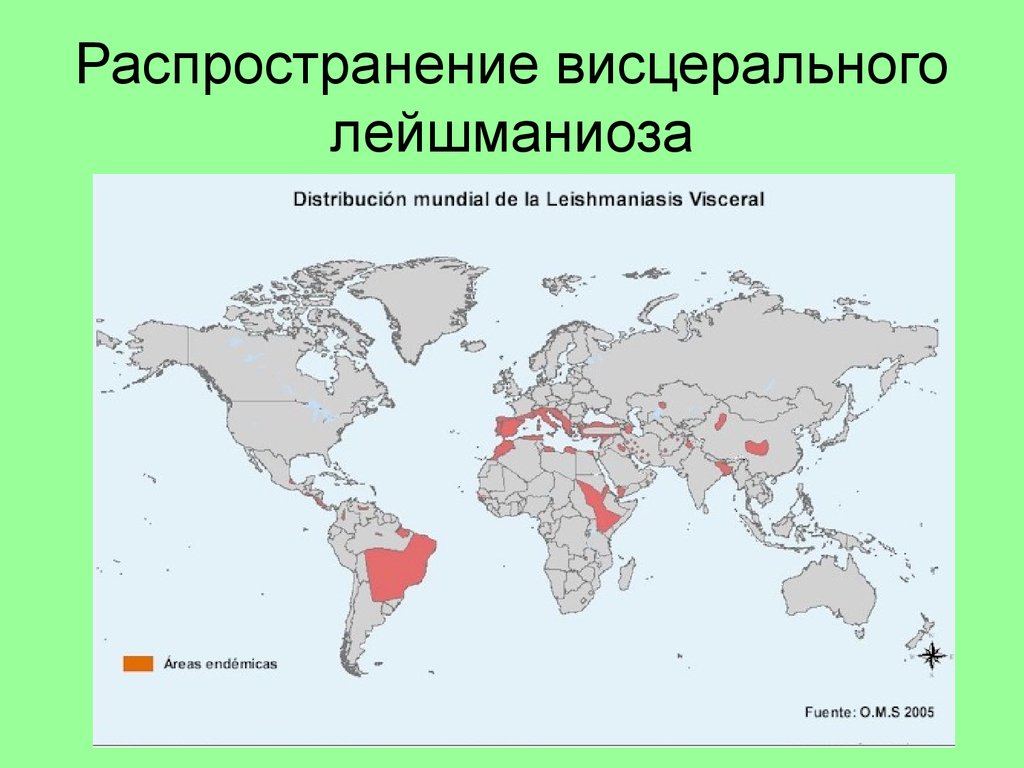 Большое значение имеют эпидемиологические данные — пребывание в эндемичных регионах в последние два месяца.
Большое значение имеют эпидемиологические данные — пребывание в эндемичных регионах в последние два месяца.
Специфическая диагностика кожного лейшманиоза
Проводится микроскопия содержимого язв и краевого инфильтрата. Поскольку лейшманий в материале немного, микроскопическое исследование проводят несколько раз. Применяют кожную аллергическую пробу Монтенегро с лейшманином (поверхностная жидкость убитых фенолом лейшманий). Используют также биологическую пробу на белых мышах и хомяках, которых заражают внутрикожно материалом из язв больного.
Дифференциальная диагностика кожного лейшманиоза
Дифференциальная диагностика проводится с фурункулезом, проказой, сифилисом, эпителиома, трофической язвой, сибирской язвой и т.п.
Лечение кожного лейшманиоза
Лечение преимущественно местное. Применяют примочки с фурацилином, грамицидина, мази: 0,5% акрихинову, мономицинову, Вишневского. В ранний период болезни лейшманиомы рекомендуется присыпать или внутрикожно обкалывать акрихином, мономицином, берберина сульфатом или гексаметилентетрамином. В последние годы применяют лазерную терапию, преимущество которой в заживлении язв без рубцевания. В случае множественных язв со значительными инфильтратами назначают парентерально мономицин по 0,25 г 3 раза в сутки в течение 10-14 дней, аминохииол по 0,2 г. З раза в день (на курс 10-12 г). Широко применяют стимулирующее и общеукрепляющее лечение, поливитаминные препараты и тому подобное
В последние годы применяют лазерную терапию, преимущество которой в заживлении язв без рубцевания. В случае множественных язв со значительными инфильтратами назначают парентерально мономицин по 0,25 г 3 раза в сутки в течение 10-14 дней, аминохииол по 0,2 г. З раза в день (на курс 10-12 г). Широко применяют стимулирующее и общеукрепляющее лечение, поливитаминные препараты и тому подобное
Профилактика лейшманиозов
При зоонозном кожном лейшманиозе необходимы дератизационные мероприятия, направленные против основного источника инфекции — больших песчанок. Мероприятия проводятся в радиусе 2,5-3км вокруг населенного пункта.
При антропонозной форме кожного лейшманиоза (источник инфекции — человек) больных госпитализируют в недоступные для москитов помещения; кожные поражения защищают повязкой от укусов москитов.
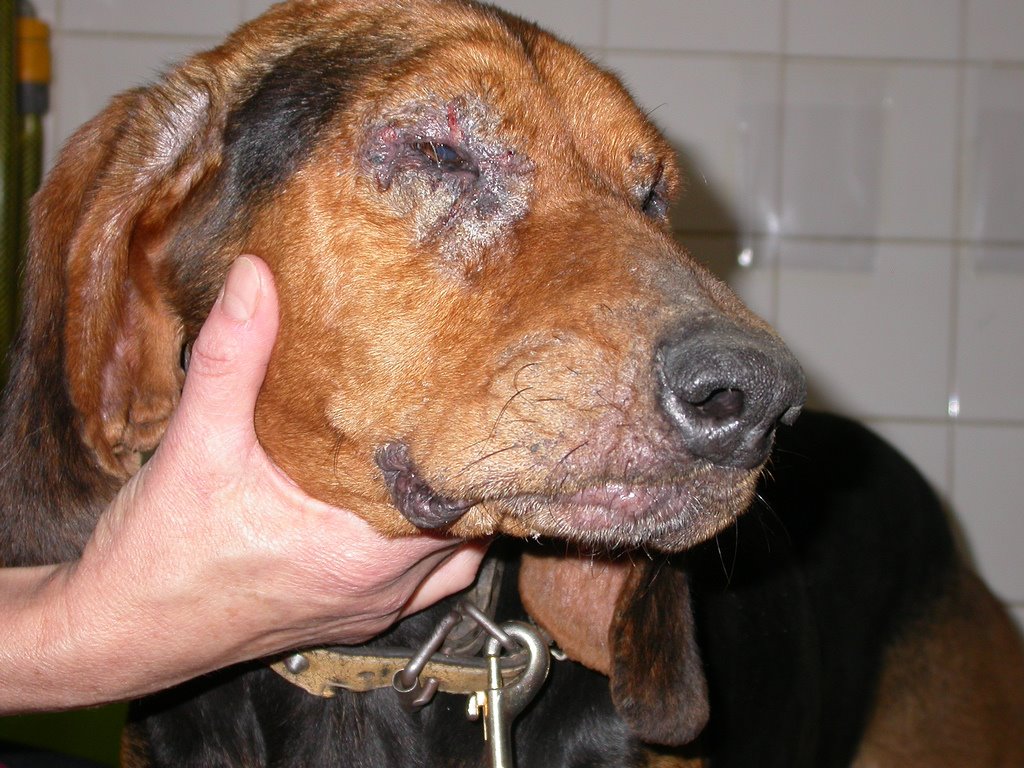
При висцеральном лейшманиозе проводят уничтожение больных собак (с кожными поражениями, истощенных, облысевших) и отлов бродячих собак.
Меры по предупреждению передачи болезни едины при всех формах лейшманиоза, поскольку во всех случаях переносчиками являются москиты. В населенных пунктах инсектицидами обрабатывают места выплода москитов, а также места их дневок.
В населенных пунктах инсектицидами обрабатывают места выплода москитов, а также места их дневок.
Определенное значение имеют меры индивидуальной защиты от москитов — применение пологов, сеток,репеллентов.
В природных очагах лейшманиоза детям и прибывающим на работу и на постоянное жительство взрослым проводят искусственную иммунизацию путем внутрикожного введения живой культуры L. tropica major. Возникает доброкачественный местный процесс, заканчивающийся рубцеванием. Поскольку культуру вводят в участки тела, покрытые одеждой, косметический дефект незначителен. Иммунитет вырабатывается через 3 мес после прививки.
Лейшманиоз
лейшманиоз- All topics »
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- x
- Y
- Z
- 0004
Ресурсы »
- Бюллетени
- Факты в картинках
- Мультимедиа
- Публикации
- Вопросы и Ответы
- Инструменты и наборы инструментов
- Популярный »
- Загрязнение воздуха
- Коронавирусная болезнь (COVID-19)
- Гепатит
- оспа обезьян
- Все страны »
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- o
- P
- Q
- 40004
- 400059
- Q
- 40004
- 40004 40005
- Q
- 9
- 400059
- Q 9
- Q
- 40005
- .

- U
- V
- W
- X
- Y
- Z
- Регионы »
- Африка
- Америка
- Юго-Восточная Азия
- Европа
- Восточное Средиземноморье
- Западная часть Тихого океана
- ВОЗ в странах »
- Статистика
- Стратегии сотрудничества
- Украина ЧП
- все новости »
- Выпуски новостей
- Заявления
- Кампании
- Комментарии
- События
- Тематические истории
- Выступления
- Прожекторы
- Информационные бюллетени
- Библиотека фотографий
- Список рассылки СМИ
- Заголовки »
- Сосредоточиться на »
- Афганистан кризис
- COVID-19 пандемия
- Кризис в Северной Эфиопии
- Сирийский кризис
- Украина ЧП
- Вспышка оспы обезьян
- Кризис Большого Африканского Рога
- Последний »
- Новости о вспышках болезней
- Советы путешественникам
- Отчеты о ситуации
- Еженедельный эпидемиологический отчет
- ВОЗ в чрезвычайных ситуациях »
- Наблюдение
- Исследовать
- Финансирование
- Партнеры
- Операции
- Независимый контрольно-консультативный комитет
- Призыв ВОЗ о чрезвычайной ситуации в области здравоохранения 2023 г.

- Данные ВОЗ »
- Глобальные оценки здоровья
- ЦУР в области здравоохранения
- База данных о смертности
- Сборы данных
- Панели инструментов »
- Информационная панель COVID-19
- Приборная панель «Три миллиарда»
- Монитор неравенства в отношении здоровья
- Основные моменты »
- Глобальная обсерватория здравоохранения
- СЧЕТ
- Инсайты и визуализации
- Инструменты сбора данных
- Отчеты »
- Мировая статистика здравоохранения 2022 г.
- избыточная смертность от COVID
- DDI В ФОКУСЕ: 2022 г.
- О ком »
- Люди
- Команды
- Состав
- Партнерство и сотрудничество
- Сотрудничающие центры
- Сети, комитеты и консультативные группы
- Трансформация
- Наша работа »
- Общая программа работы
- Академия ВОЗ
- Деятельность
- Инициативы
- Финансирование »
- Инвестиционный кейс
- Фонд ВОЗ
- Подотчетность »
- Аудит
- Программный бюджет
- Финансовые отчеты
- Портал программного бюджета
- Отчет о результатах
- Управление »
- Всемирная ассамблея здравоохранения
- Исполнительный совет
- Выборы Генерального директора
- Веб-сайт руководящих органов
- Портал государств-членов
- Дом/
- Вопросы здравоохранения/
- Лейшманиоз
Ламек Ододо/DNDi
Чепсера Лимару присматривает за своим сыном Птуру Лимарук, страдающим кала-азаром, в больнице Амудат в Уганде.
© Кредиты
Информационные бюллетени
Вопросы и ответы
- Часто задаваемые вопросы о лейшманиозе
Резолюция ВОЗ
Группы ВОЗ
- Забытые тропические болезни
Наша работа
Публикации
Все →Несмотря на значительную роль борьбы с переносчиками в национальных программах борьбы с лейшманиозом, программное сообщество воспринимает борьбу с переносчиками как…
В документе представлены результаты многоцентрового исследования ВОЗ (2020–2022 гг.), проведенного восемью лабораториями. в разных регионах ВОЗ и экспертом ВОЗ…
Лейшманиоз продолжает оставаться проблема здоровья в 4 эколого-эпидемиологических регионы мира: Америка, Восток Африка, Северная Африка и Запад…
Интерактивная хронология фактов
Эта интерактивная хронология дает некоторое представление об истории болезни с вдохновляющими моментами. Он состоит из коротких рассказов, сгруппированных по шести категориям (эпидемиология, борьба с болезнями, партнерство, борьба с переносчиками болезней, ведение пациентов и политика), обозначенных разными цветами.
Панель дисплея в правом нижнем углу окна (значок инструмента) может использоваться для выбора и отображения одной или нескольких определенных категорий.
Временную шкалу можно просмотреть как в 2D, так и в 3D, нажав кнопку в левом нижнем углу.
Навигация упрощается путем прокрутки вверх или вниз с помощью мыши.
Доступ к временной шкале
Мультимедиа
20 ноября 2017 г.
Глобальная эпидемиология лейшманиоза
20 июля 2017 г.
Жизненный цикл лейшманиоза у человека
31 декабря 2015 г.
Что такое лейшманиоз?
14 октября 2014 г.
Жизненный цикл Leishmania у насекомых-переносчиков
Связанные ссылки
Peer-рецензируемые публикации (PubMed)
Результаты для Leishmaniasis
Who Collaborating Centres
Fundrese SondrerAl EntranciOn.0401
Instituto de Salud Carlos III
Instituto Ramón y Cajal de Investigación Sanitaria
Контакт
[email protected]
Доктор Хосе Руис Постиго 1 [электронная почта защищена] Доктор Саураб Джайн [электронная почта защищена]
Ученый Темы, связанные со здоровьем
Лейшманиоз — StatPearls — Книжная полка NCBI
Непрерывное обучение, задание
Лейшманиоз — это протозойное заболевание, передающееся москитами, которое чаще всего встречается в Европе, Африке, Азии и Латинской Америке. По мере изменения моделей поездок это заболевание все чаще заносится в развитые районы. Заболевание может быть кожным или системным. Идентификация микроорганизма и знание эндемичных видов помогут членам межпрофессиональной команды поставить точный диагноз и при необходимости назначить таргетную терапию. В этом задании описываются эпидемиология, клинические проявления, диагностика и лечение лейшманиоза. В этом обзоре подчеркивается роль межпрофессиональной команды в уходе за больными пациентами и подготовке к возможным будущим случаям лейшманиоза в развитых странах.
По мере изменения моделей поездок это заболевание все чаще заносится в развитые районы. Заболевание может быть кожным или системным. Идентификация микроорганизма и знание эндемичных видов помогут членам межпрофессиональной команды поставить точный диагноз и при необходимости назначить таргетную терапию. В этом задании описываются эпидемиология, клинические проявления, диагностика и лечение лейшманиоза. В этом обзоре подчеркивается роль межпрофессиональной команды в уходе за больными пациентами и подготовке к возможным будущим случаям лейшманиоза в развитых странах.
Цели:
Опишите эпидемиологию лейшманиоза.
Опишите синдромы кожного, слизисто-кожного и висцерального лейшманиоза.
Объясните, как диагностировать лейшманиоз.
Определить важность улучшения координации помощи, уделяя особое внимание общению между межпрофессиональными медицинскими бригадами, для улучшения оперативного и тщательного оказания помощи пациентам с лейшманиозом.

Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Лейшманиоз – это заболевание, вызываемое простейшими Leishmania , которое чаще всего передается инфицированными москитами. Исторически он был широко распространен в тропическом климате на нескольких континентах, включая Европу, Африку, Азию и Америку. У людей эти паразиты размножаются внутриклеточно и классически проявляются висцеральным или кожным заболеванием.
Лейшманиоз имеет огромное историческое значение, поскольку заболевание было зарегистрировано за тысячи лет до нашей эры (до н. э.) [1]. Исследование древних египетских и христианских нубийских мумий, датируемых периодом с 3500 по 2800 год до нашей эры, дало успешную амплификацию ДНК Leishmaniasis donovani . Считается, что в период называемый Средним царством египетские торговые и военные экспедиции с участием Нубии (современный Судан) стали причиной заноса лейшманиоза в Египет, поскольку до этого периода ДНК-положительные образцы не наблюдались.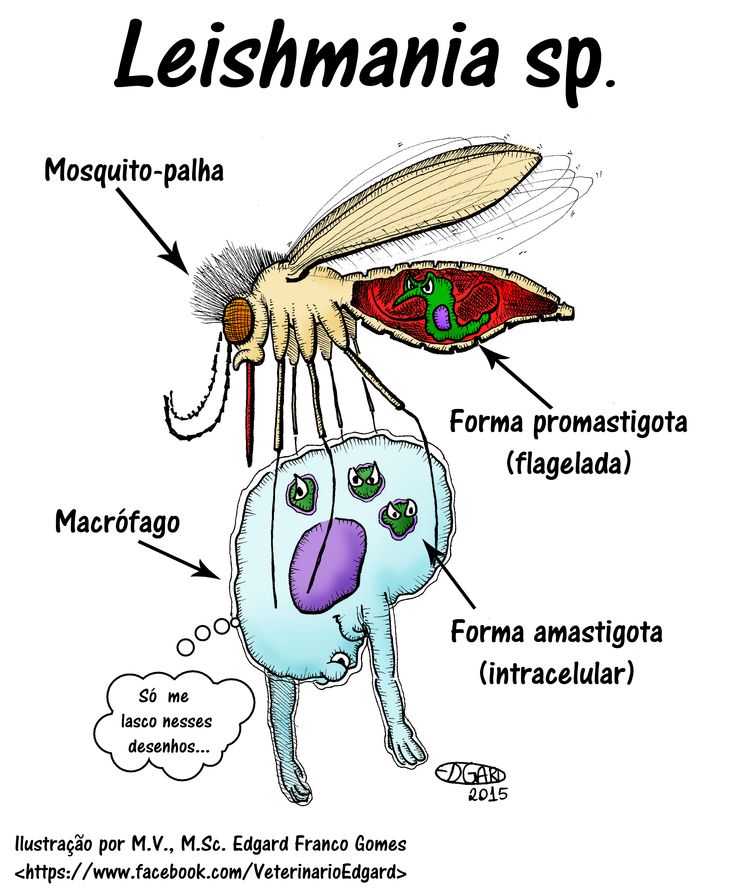 Кроме того, некоторые источники подозревают Судан в качестве исходного очага висцерального лейшманиоза (ВЛ) [2]. Кроме того, медицинские рукописи под названием «Папирус Эберса» от 1500 г. до н.э. описывают кожное заболевание, считающееся кожным лейшманиозом, которое тогда называли «нильским прыщом». Имея в виду эту древнюю концепцию болезни, на Ближнем Востоке и в Центральной Азии были предприняты первые попытки вакцинации. Это было выполнено путем взятия экссудатов активных поражений и инокуляции их в ягодицы детей.
Кроме того, некоторые источники подозревают Судан в качестве исходного очага висцерального лейшманиоза (ВЛ) [2]. Кроме того, медицинские рукописи под названием «Папирус Эберса» от 1500 г. до н.э. описывают кожное заболевание, считающееся кожным лейшманиозом, которое тогда называли «нильским прыщом». Имея в виду эту древнюю концепцию болезни, на Ближнем Востоке и в Центральной Азии были предприняты первые попытки вакцинации. Это было выполнено путем взятия экссудатов активных поражений и инокуляции их в ягодицы детей.
В течение следующей тысячи лет были описаны кожные язвы, характерные для лейшманиоза, а в историческом северном Афганистане теперь считается, что болезнь, называемая «Балхская язва», была вызвана L. tropica . В Азии и на Ближнем Востоке болезнь продолжали документировать, а состояния называли «алеппским кипением», «иерихонским кипением» и «багдадским кипением». Многие из этих имен остаются актуальными и в наше время.
С ранним признанием инфекционной природы лейшманиоза впервые столкнулся шотландский врач, который заметил паразитов в делийском фурункуле, но только после того, как аналогичные находки были обнаружены русским врачом Петром Фокичем Боровским, эти тела в азиатских язвах на самом деле были предположительно простейшие, опубликованные в 189 г. 8. В 1900 году британский патологоанатом заметил овоидные тела и предположил, что они представляют собой выродившиеся трипаносомы. Затем он назвал эту болезнь «лихорадкой дум-дум». Примерно в то же время ирландский врач Чарльз Донован опубликовал статью об аналогичных яйцевидных телах из селезенки коренных азиатских индейцев. Исследование индийской болезни кала-азар и селезеночных овоидных тел, описанных патологом Лейшманом и клиницистом Донаваном, показало, что эти овоидные тельца выродились не трипаносомами, а новым видом простейших, позже названным Leishmania donovani. В течение следующих десятилетий будут идентифицированы подвиды, включая L. tropica, L. aethiopica, и многие другие. Классификация болезни на лейшманиоз нового мира и лейшманиоз старого мира будет тогда основана на этих организмах и их географическом распространении.[1]
8. В 1900 году британский патологоанатом заметил овоидные тела и предположил, что они представляют собой выродившиеся трипаносомы. Затем он назвал эту болезнь «лихорадкой дум-дум». Примерно в то же время ирландский врач Чарльз Донован опубликовал статью об аналогичных яйцевидных телах из селезенки коренных азиатских индейцев. Исследование индийской болезни кала-азар и селезеночных овоидных тел, описанных патологом Лейшманом и клиницистом Донаваном, показало, что эти овоидные тельца выродились не трипаносомами, а новым видом простейших, позже названным Leishmania donovani. В течение следующих десятилетий будут идентифицированы подвиды, включая L. tropica, L. aethiopica, и многие другие. Классификация болезни на лейшманиоз нового мира и лейшманиоз старого мира будет тогда основана на этих организмах и их географическом распространении.[1]
Этиология
Лейшманиоз — заболевание, вызываемое простейшими из семейства Trypanosomatidae, порядка Kinetoplastida, рода Leishmania. Двумя стадиями развития являются амастигота и промастигота, причем первая заражает лизосомальные вакуоли в фагоцитирующих клетках. Промастигота представляет собой внеклеточную форму, которая прикрепляется к микроворсинкам насекомых. Насекомое-переносчик, москит, имеет несколько видов, но разные подмножества. Болезни Старого Света чаще всего передаются Флеботомус и Сергентомия . Видом москитов, печально известным распространением болезни Нового Света, является Lutzomyia. Сводный список распространенных подвидов лейшманиоза, поражающих Новый и Старый Свет, можно увидеть в таблице 1.[3]
Двумя стадиями развития являются амастигота и промастигота, причем первая заражает лизосомальные вакуоли в фагоцитирующих клетках. Промастигота представляет собой внеклеточную форму, которая прикрепляется к микроворсинкам насекомых. Насекомое-переносчик, москит, имеет несколько видов, но разные подмножества. Болезни Старого Света чаще всего передаются Флеботомус и Сергентомия . Видом москитов, печально известным распространением болезни Нового Света, является Lutzomyia. Сводный список распространенных подвидов лейшманиоза, поражающих Новый и Старый Свет, можно увидеть в таблице 1.[3]
Взрослые москиты очень маленькие, около одной трети размера небольшого комара или < 3,5 мм в длину. Они подвержены обезвоживанию и поэтому процветают во влажном климате, отсюда и распространение болезней. Эти мухи ведут ночной образ жизни, а днем их можно найти в норах, под камнями или другими укрытиями. У них характерная форма «V» на спине в состоянии покоя и отчетливый грудной горб, который толкает голову вниз. В то время как мужчины и женщины получают углеводы из растительных соков, женщинам требуется кровь. Именно во время этой трапезы муха-переносчик передает простейших человеку-хозяину.[3]
В то время как мужчины и женщины получают углеводы из растительных соков, женщинам требуется кровь. Именно во время этой трапезы муха-переносчик передает простейших человеку-хозяину.[3]
Эпидемиология
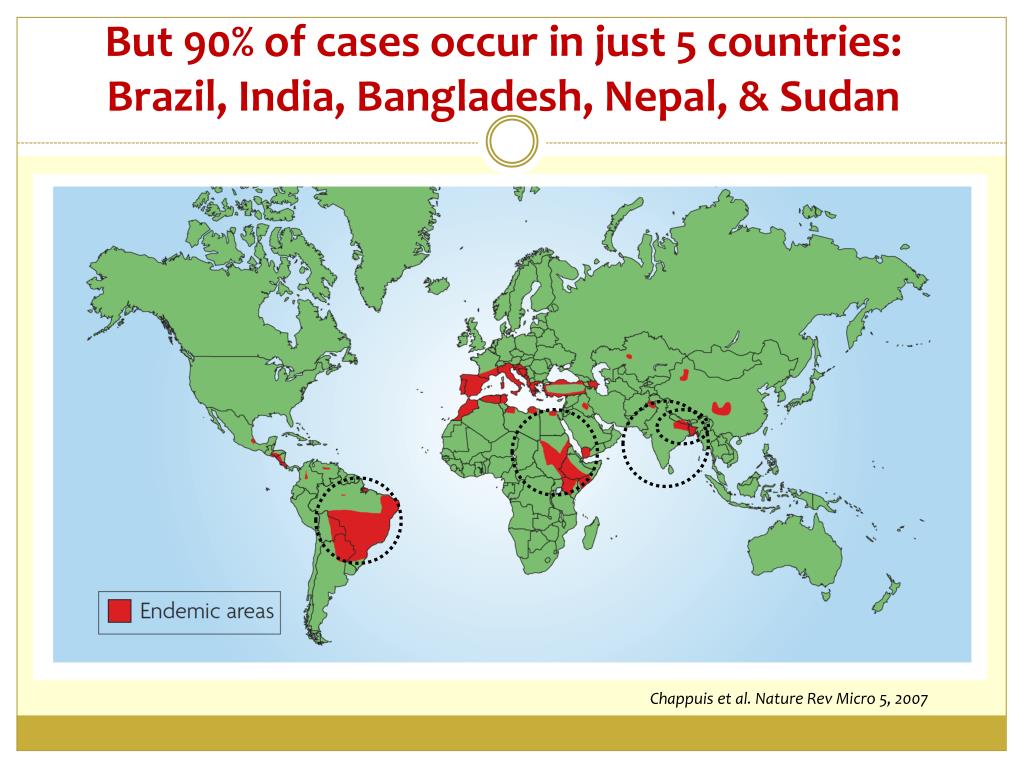
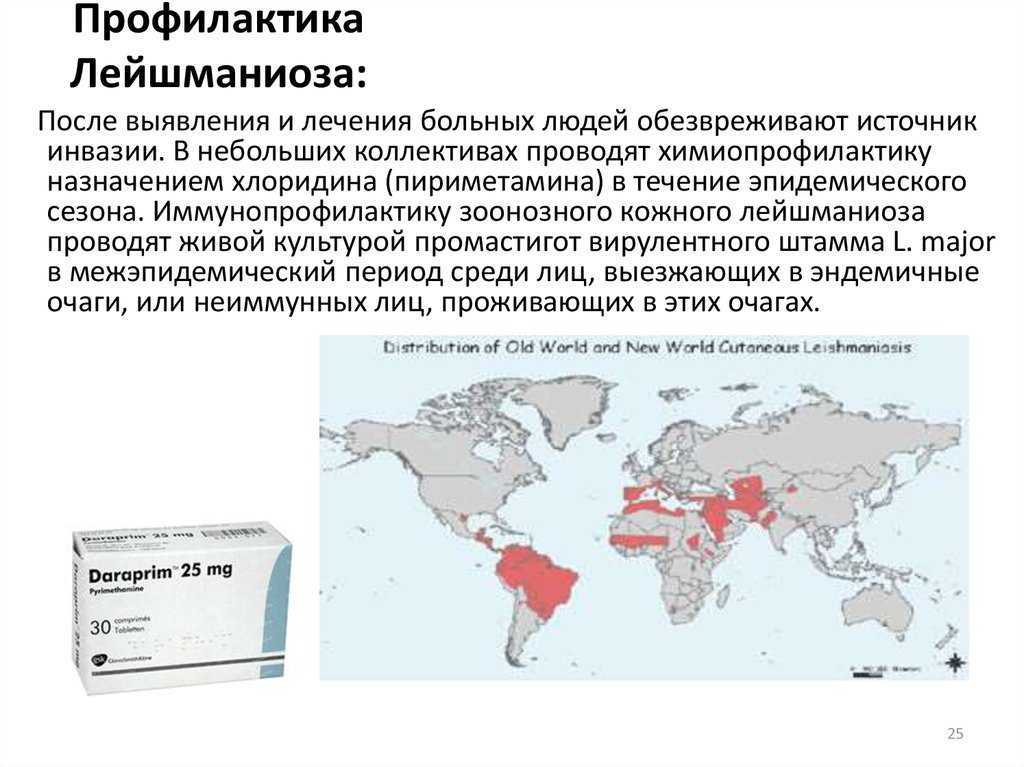
Лейшманиоз эндемичен для Азии, Ближнего Востока, Северной Африки, Средиземноморья, Южной и Центральной Америки. Он встречается в 89 странах, и ежегодно во всем мире регистрируется от 1,5 до 2 миллионов новых случаев. Лейшманиоз может вызывать кожно-слизистые или висцеральные заболевания, от него ежегодно умирают 70 000 человек. Всемирная организация здравоохранения (ВОЗ) в 2012 г. сообщила, что большинство висцеральных и кожных заболеваний были обнаружены в отдельных странах. [Таблица 2] [1][2][4]
Патофизиология
Паразиты Leishmania передаются через укусы москитов, при этом представители родов Phlebotomus и Lutzomyia являются наиболее распространенными переносчиками болезней Старого и Нового Света, соответственно.[1] Как уже упоминалось, только самки москитов нуждаются в питании кровью, и во время этих приемов пищи Leishmanis spp.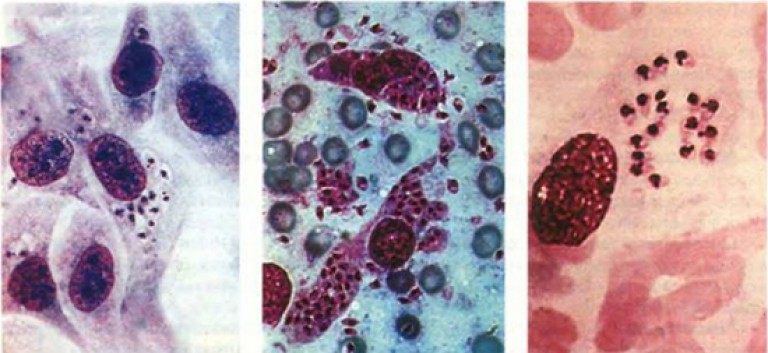 приобретаются мухой и передаются хозяину. Когда москитная муха, не зараженная болезнями, атакует зараженного хозяина, они используют пилообразные ротовые части, вставленные в кожу, чтобы создать небольшую рану, из которой стекает кровь из поврежденных капилляров. Инфекционный промастигот проникает в переднюю кишку москита и размножается.[5][6][7] Когда муха питается собаками, грызунами, сумчатыми или людьми, это приводит к передаче болезни новому хозяину.
приобретаются мухой и передаются хозяину. Когда москитная муха, не зараженная болезнями, атакует зараженного хозяина, они используют пилообразные ротовые части, вставленные в кожу, чтобы создать небольшую рану, из которой стекает кровь из поврежденных капилляров. Инфекционный промастигот проникает в переднюю кишку москита и размножается.[5][6][7] Когда муха питается собаками, грызунами, сумчатыми или людьми, это приводит к передаче болезни новому хозяину.
Как только простейшие получают доступ к хозяину, простейшие проникают в фаголизосомы. В зависимости от того, какой подтип фагоцитирующих клеток инфицирован, возникает кожный лейшманиоз (КЛ) или висцеральный лейшманиоз (ВЛ). При КЛ паразиты заражают резидентные макрофаги в коже, и как только каждая скомпрометированная клетка заполнена амастиготами, она разрывается, обеспечивая быстрое высвобождение и заражение соседних макрофагов. ВЛ отличается тем, что амастиготы гематогенно распространяются в мононуклеарные клетки печени, селезенки, костного мозга и лимфатических узлов кишечника. [1]
[1]
Гистопатология
Идентификация паразитов путем гистопатологического исследования фиксированной ткани или культуры паразита in vitro является золотым стандартом диагностики. Отбор образцов ткани из края кожной язвы обеспечивает наивысший результат при окрашивании по Гимзе образцов биопсии или мазков-отпечатков.[8] Сравнение мазков соскобов и цитологии тонкоигольной аспирации показало, что аспирация иглой улучшила как обнаружение амастигот, так и комфорт пациента.[9] Также использовался упрощенный метод сбора, называемый «пресс-отпечаток-мазок», и по сравнению с гистопатологией кожных заболеваний он имел значительно более высокую чувствительность, чем гистопатологические исследования. Этот метод выполняется с использованием 3-миллиметровой пункционной биопсии, аналогичной той, которая получается при гистопатологии, фиксированной формалином. Однако при пресс-отпечатке-мазке фрагмент ткани помещают между двумя предметными стеклами в продольном направлении (эпидермис перпендикулярен предметным стеклам) и сдавливают. Давление сосредоточено на центре предметного стекла и позволяет «соку» и тканям распространяться по обоим предметным стеклам. Затем предметные стекла разделяют, удаляют ткань и дают предметным стеклам высохнуть на воздухе. Затем слайды фиксируют ментолом, окрашивают по Гимзе и исследуют под микроскопом с помощью масляной иммерсионной линзы.[10]
Давление сосредоточено на центре предметного стекла и позволяет «соку» и тканям распространяться по обоим предметным стеклам. Затем предметные стекла разделяют, удаляют ткань и дают предметным стеклам высохнуть на воздухе. Затем слайды фиксируют ментолом, окрашивают по Гимзе и исследуют под микроскопом с помощью масляной иммерсионной линзы.[10]
Исследование любого метода выявляет классические организмы в виде круглых овальных тел размером от 2 до 4 мкм с характерными ядрами и кинетопластами.[8][10]
Анамнез и физикальное исследование
Клинические проявления традиционно подразделяются на три основных синдрома: кожный, слизисто-кожный и висцеральный.[11][4] Организмы , ответственные за каждое клиническое подмножество, перечислены в таблице 1. Кожное заболевание является наиболее частым проявлением лейшманиоза и далее подразделяется на локализованное кожное заболевание и диффузное кожное заболевание. Локализованные кожные поражения часто имеют инкубационный период от 2 до 4 недель, когда в месте инокуляции появляются бессимптомные папулы, множественные папулы или узелки. Они увеличиваются и трансформируются в четко очерченные язвы с приподнятой фиолетовой каймой и разрушением эпидермиса. Эти поражения часто заживают спонтанно в течение 2–5 лет (в зависимости от вида) с образованием вторичного вдавленного рубца.[5][4] Характеристики ограниченных кожных поражений, связанных с отдельными подвидами, перечислены в таблице 3.[4]
Они увеличиваются и трансформируются в четко очерченные язвы с приподнятой фиолетовой каймой и разрушением эпидермиса. Эти поражения часто заживают спонтанно в течение 2–5 лет (в зависимости от вида) с образованием вторичного вдавленного рубца.[5][4] Характеристики ограниченных кожных поражений, связанных с отдельными подвидами, перечислены в таблице 3.[4]
Диффузный кожный лейшманиоз также начинается с безболезненного узелка, но может прогрессировать и поражать всю поверхность кожи. У него есть пристрастие к лицу, ушам и разгибательным поверхностям, таким как колени и локти. Инвазия слизистой оболочки носоглотки и полости рта может наблюдаться у трети пациентов. Прогрессирующее заболевание может привести к львиному лицу. Организмами, наиболее ассоциированными с диффузным кожным лейшманиозом, являются L. aethiopica в Старом Свете и L. mexicana 9.0547 в болезни Нового Света. Поражения кожи могут в дальнейшем прогрессировать до диффузных гипопигментированных бляшек и пятен.
Поражение слизистых оболочек связано с гематогенным или лимфатическим распространением и часто возникает после разрешения кожных поражений. Начало проявлений на слизистых оболочках обычно происходит в течение двух лет, но может быть отсрочено на десятилетия. L. braziliensis вызывает большинство кожно-слизистых заболеваний, хотя могут быть вовлечены и другие микроорганизмы (таблица 1). Преимущественно поражается слизистая оболочка полости рта и носа, хотя язвенное поражение может распространяться на голосовые связки и хрящи трахеи, но костные структуры не затрагиваются. Заболевание слизистой оболочки может быть тяжелым и опасным для жизни [4].
Висцеральный лейшманиоз также известен под термином кала-азар, впервые описанным в Индии в 1800-х годах.[1][11][4] При поражении внутренних органов часто сочетаются лихорадка, спленомегалия, гипергаммаглобулинемия и панцитопения. Часто эти клинические последствия являются вторичными по отношению к непосредственно инфицированным органам, включая печень, селезенку, костный мозг или другие внутренние органы.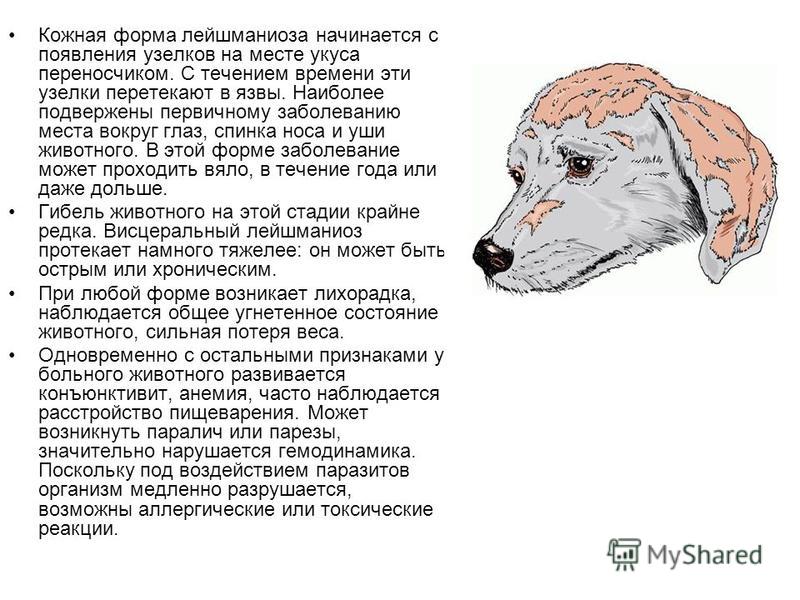 Наиболее часто возбудителями являются L. donovani, L. infantum, и L. chagasi. [11][4] Поражение внутренних органов, как и кожное заболевание, имеет сезонные пики весной, которые, вероятно, связаны с температурой, влажностью и привычками переносчиков.[11]
Наиболее часто возбудителями являются L. donovani, L. infantum, и L. chagasi. [11][4] Поражение внутренних органов, как и кожное заболевание, имеет сезонные пики весной, которые, вероятно, связаны с температурой, влажностью и привычками переносчиков.[11]
Иногда поражение кожи может проявиться после лечения висцерального заболевания в виде папулезной сыпи на лице и верхних конечностях. Для описания этого был придуман термин «посткала-азарский кожный лейшманиоз», и эти кожные поражения не вызывают уродства и проходят сами по себе.[4]
Оценка
Как уже упоминалось, золотым стандартом диагностики является гистопатологическое исследование образцов тканей. Примечательно, что чувствительность исследуемой ткани низкая, и чувствительность можно повысить, используя метод прессования-отпечатка-мазка. Можно использовать пробирки для культивирования паразитов со средой Нови-МакНила-Николя, но это технически сложно из-за низкой чувствительности. Технологии микрокультуры обладают повышенной чувствительностью до 98,4% и являются 100% специфичными. Серологические исследования, включая иммуноферментный анализ, вестерн-блоттинг или прямую агглютинацию, используются редко из-за плохого гуморального ответа при лейшманиозе и, следовательно, низкой чувствительности. Очищенные антигенные препараты или рекомбинантные антигены повышают эффективность этих исследований. Было отмечено, что сывороточные уровни анти-альфа-Gal IgG повышены у лиц, инфицированных L. tropica и L. major . Этот тест может быть полезен в качестве маркера излечения КЛ Старого Света. Применялись внутрикожные кожные пробы с хорошей чувствительностью и специфичностью, при этом кожные реакции гиперчувствительности замедленного типа, равные 5 мм, считаются положительными. Большим недостатком является неспособность кожных проб различить предшествующую или текущую инфекцию. Полимеразная цепная реакция и тесты амплификации нуклеиновых кислот используются все шире и являются одновременно чувствительными и специфичными.[8] Диагностика заболевания в клинических условиях часто определяется доступными ресурсами.
Серологические исследования, включая иммуноферментный анализ, вестерн-блоттинг или прямую агглютинацию, используются редко из-за плохого гуморального ответа при лейшманиозе и, следовательно, низкой чувствительности. Очищенные антигенные препараты или рекомбинантные антигены повышают эффективность этих исследований. Было отмечено, что сывороточные уровни анти-альфа-Gal IgG повышены у лиц, инфицированных L. tropica и L. major . Этот тест может быть полезен в качестве маркера излечения КЛ Старого Света. Применялись внутрикожные кожные пробы с хорошей чувствительностью и специфичностью, при этом кожные реакции гиперчувствительности замедленного типа, равные 5 мм, считаются положительными. Большим недостатком является неспособность кожных проб различить предшествующую или текущую инфекцию. Полимеразная цепная реакция и тесты амплификации нуклеиновых кислот используются все шире и являются одновременно чувствительными и специфичными.[8] Диагностика заболевания в клинических условиях часто определяется доступными ресурсами.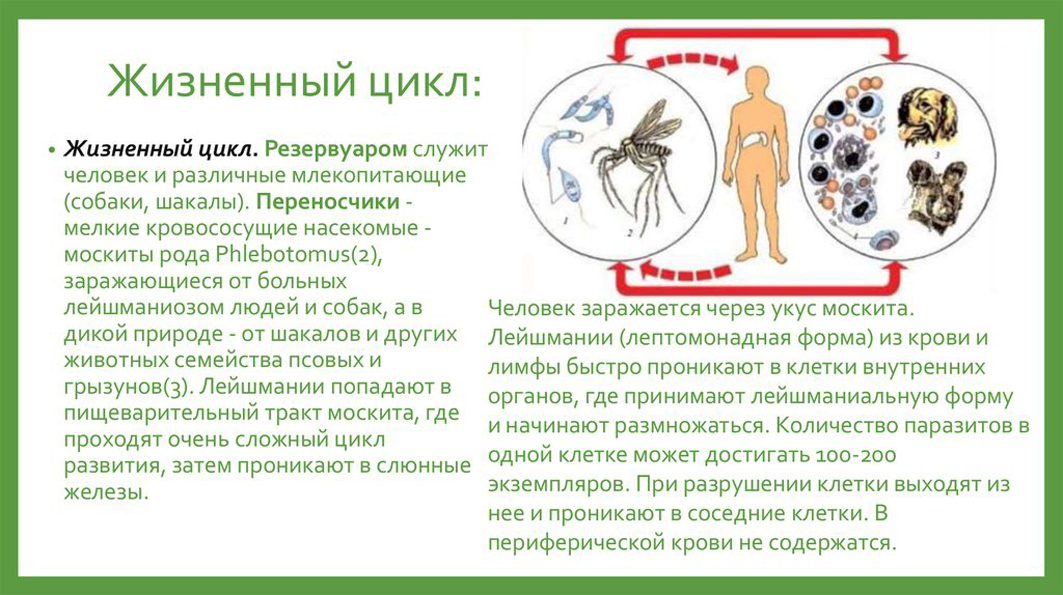
У пациентов с подозрением на висцеральное заболевание получить образцы тканей может быть нелегко, и тесты с прямой агглютинацией и тесты с тест-полосками на rK39 могут иметь большую пользу. Прямая агглютинация у пациентов с висцеральным/системным поражением имеет чувствительность 97-100% и специфичность 86-92%. Может потребоваться биопсия костного мозга, которая обычно бывает положительной у пациентов с подозрением на поражение костного мозга.[11]
Лечение/управление
При инфекционных заболеваниях первоначальные меры часто направлены на профилактику. Важно знать эндемичные районы, знать о ночной активности москитов и контактировать с животными в районах, где, как известно, распространены болезни. Поскольку москиты очень маленькие, даже меньше, чем комары, требуется надкроватная сетка с узором в виде лабиринта, в три раза меньшего размера, чем стандартная. Дальнейшая пропитка перметрином также может снизить риск. Также было показано, что попытки вакцинировать собак и использовать собачьи ошейники с инсектицидами снижают бремя болезней.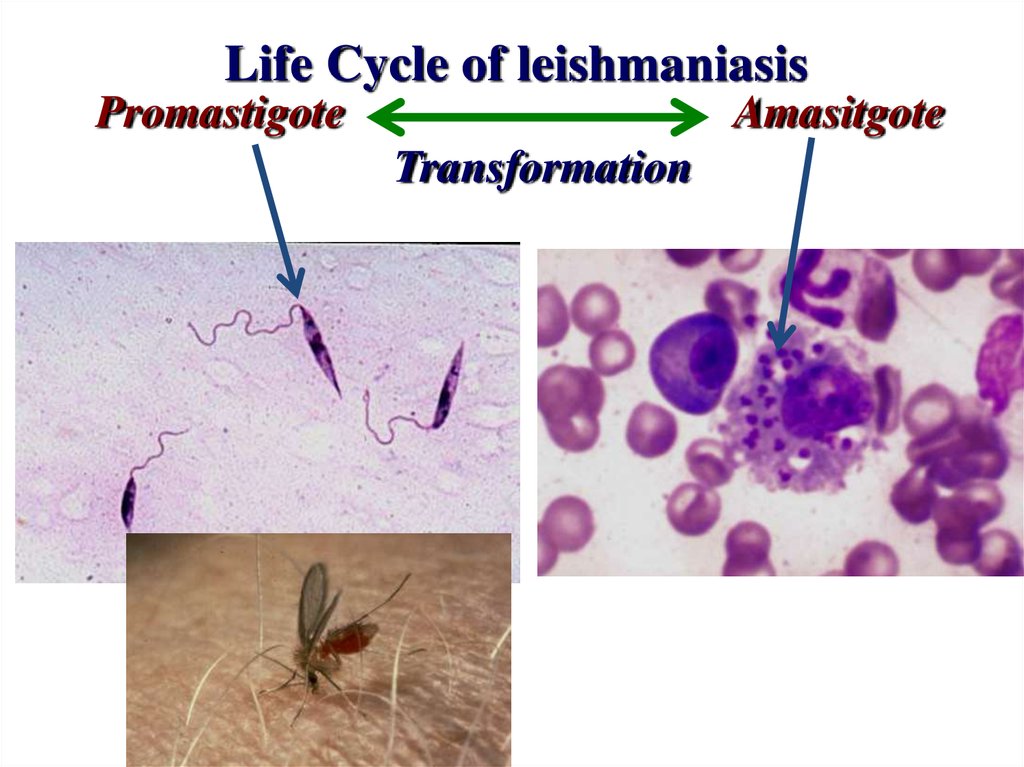 [8]
[8]
При ограниченном КЛ болезнь часто разрешается спонтанно. Однако дерматологические заболевания могут быть разрушительными, усиливать вторичные инфекции или оставлять необратимые шрамы, приводящие к инвалидности. Варианты лечения первой линии для ограниченного кожного заболевания включают внутриочаговые формы пятивалентных препаратов сурьмы, включая стиболглюконат натрия и меглюмина антимониат. Альтернативные схемы включают системное введение милтефозина, амфотерицина В, пентамидина изетионата, паромомицина или гранулоцитарно-макрофагального колониестимулирующего фактора. Многие из этих системных агентов ограничены серьезными побочными эффектами. Тепловая или криотерапия являются вариантами лечения, зарезервированными для случаев < 5 кожных поражений. [8]
Пациентам с кожно-слизистым лейшманиозом часто требуется системное лечение. Меглюмин или стибоглюконат были терапией первой линии, и ВОЗ рекомендует пятивалентную сурьму для лечения кожно-слизистых заболеваний. Показатели успеха лечения достигают 95%, если используются стратегии с высокими дозами, хотя стратегии с низкими дозами часто используются для минимизации побочных эффектов. Терапия азолом (т. е. флуконазол, кетоконазол, итраконазол) использовалась изолированно и в сочетании с амфотерицином В. Их использование ограничено региональными вариантами заболевания и резистентностью, а также наличием минимального дополнительного преимущества по сравнению с уже эффективным амфотерицином. Установлены агенты с хорошими показателями излечения (= 90%) включают амфотерицин В (липосомная или коллоидная дисперсия), амфотерицин В дезоксихолат и пентамидин. Другие, менее эффективные методы лечения включают пятивалентную сурьму и итраконазол.[12]
Терапия азолом (т. е. флуконазол, кетоконазол, итраконазол) использовалась изолированно и в сочетании с амфотерицином В. Их использование ограничено региональными вариантами заболевания и резистентностью, а также наличием минимального дополнительного преимущества по сравнению с уже эффективным амфотерицином. Установлены агенты с хорошими показателями излечения (= 90%) включают амфотерицин В (липосомная или коллоидная дисперсия), амфотерицин В дезоксихолат и пентамидин. Другие, менее эффективные методы лечения включают пятивалентную сурьму и итраконазол.[12]
Висцеральный лейшманиоз требует лечения, и обычно используемые агенты включают стибоглюконат натрия сурьмы, амфотерицин, паромомицин и пероральный милтефозин. Агент выбора часто определяется местными видами, поскольку устойчивость сильно различается. Суммируя, стибоглюконат натрия используется в Восточной Африке, но имеет высокий процент неудач в Индии. Липосомальный амфотерицин B доступен в основном в странах, богатых ресурсами, а другие формы амфотерицина B используются в Индии. Паромомицин имеет хорошие показатели излечения в Индии, но не так эффективен в Африке. Он используется в качестве комбинированной терапии в Африке со стибоглюконатом натрия. Пентамидин используется в Южной Америке для первичного лечения и в качестве вторичной профилактики заболевания у больных СПИДом в Европе.[13]
Паромомицин имеет хорошие показатели излечения в Индии, но не так эффективен в Африке. Он используется в качестве комбинированной терапии в Африке со стибоглюконатом натрия. Пентамидин используется в Южной Америке для первичного лечения и в качестве вторичной профилактики заболевания у больных СПИДом в Европе.[13]
Differential Diagnosis
Cutaneous ulcers in tropical regions include[4]:
Furuncular myiasis
Staphylococcal infection
Lepromatous leprosy (leonine facies)
Tuberculoid leprosy (hypopigmented patches and plaques)
Фрамбезия (первичная стадия язвенных или узловатых поражений нижних конечностей)
Прогноз
Ограниченное кожное заболевание часто проходит спонтанно, в зависимости от врожденной иммунной системы хозяина.
Смертность, наблюдаемая среди пациентов с висцеральным заболеванием, различается при обследовании населения в больницах, в отличие от записей о смертности по месту жительства.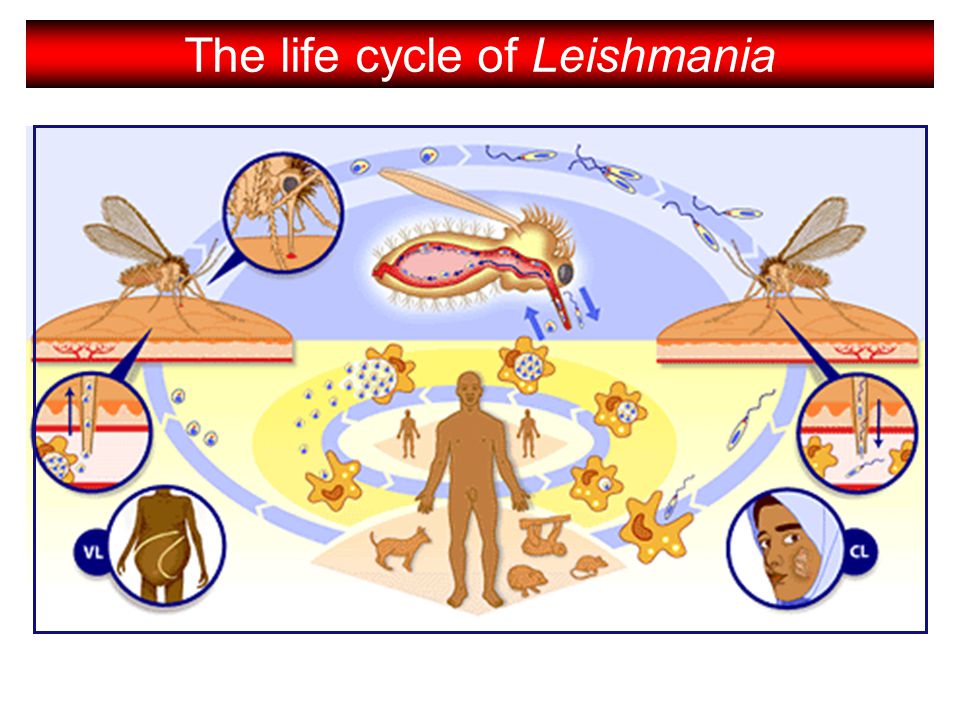 В целом ВОЗ предварительно установила смертность на уровне 10%.[14]
В целом ВОЗ предварительно установила смертность на уровне 10%.[14]
При лечении часто достигается излечение, и показатели приведены выше в соответствующих разделах. Однако среди пациентов с ВИЧ смертность значительно выше, о чем свидетельствует уровень смертности 33,6% у ВИЧ-положительных лиц в Эфиопии по сравнению с 3,6% у ВИЧ-отрицательных лиц в Эфиопии. Несмотря на хорошее лечение, побочные эффекты лекарств распространены и часто серьезны.[12][14][13]
Pearls and Other Issues
КЛ является наиболее частым проявлением лейшманиоза, и часто лабораторные исследования недоступны из-за условий, в которых возникает заболевание. Заподозрить КЛ можно по эпидемиологическим условиям эндемичной тропической сельской местности. Признаки и симптомы включают покрытые коркой язвенные поражения со сателлитными поражениями или без них, распространение лимфангита или поражение слизистой оболочки.
Поражение внутренних органов обычно проявляется лихорадкой, бледностью и слабостью или анорексией. Объективные данные включают спленомегалию, гепатомегалию, анемию, тромбоцитопению и реже лейкопению.
Объективные данные включают спленомегалию, гепатомегалию, анемию, тромбоцитопению и реже лейкопению.
Улучшение результатов работы команды здравоохранения
Лейшманиоз является глобальным заболеванием, и необходимы усилия по предоставлению образования, диагностических инструментов и лечения в эндемичных районах. Координация через ВОЗ и литературу из стран всего мира позволила получить представление о лечении, лекарственной устойчивости и передаче.
Оценка индивидуальных методов лечения проводилась во всем мире. Эффективность амфотерицина при лечении ВЛ хорошо известна.[15] (Уровень II) Милтефозин является единственным пероральным препаратом, одобренным для ВЛ, и сходная эффективность была продемонстрирована по сравнению с амфотерицином в азиатско-индийском населении.[16] (Уровень III) Другим агентом, часто используемым с хорошими результатами, является соединение пятивалентной сурьмы стибоглюконат натрия.[17] (Уровень III)
Дополнительные глобальные эпидемии, включая популяцию ВИЧ/СПИДа, были соответствующим образом изучены с одной ретроспективной когортой, показывающей, что антиретровирусное лечение значительно снижает рецидивы среди пациентов с ВЛ. [18] (Уровень III)
[18] (Уровень III)
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Рисунок
Лейшманиоз Таблицы. Предоставлено доктором Люком Максфилдом
Литература
- 1.
Стевердинг Д. История лейшманиоза. Векторы паразитов. 2017 15 февраля; 10 (1): 82. [Бесплатная статья PMC: PMC5312593] [PubMed: 28202044]
- 2.
Цинк А.Р., Шпигельман М., Шраут Б., Гринблатт К.Л., Нерлих А.Г., Донохью Х.Д. Лейшманиоз в Древнем Египте и Верхней Нубии. Эмердж Инфекция Дис. 2006 Октябрь; 12 (10): 1616-7. [Бесплатная статья PMC: PMC3290941] [PubMed: 17176592]
- 3.
Claborn DM. Биология и борьба с переносчиками лейшманиоза. J Glob Infect Dis. 2010 май; 2(2):127-34. [Бесплатная статья PMC: PMC2889652] [PubMed: 20606968]
- 4.
Хэндлер М.З., Патель П.А., Капила Р.
 , Аль-Кубати Ю., Шварц Р.А. Кожный и кожно-слизистый лейшманиоз: дифференциальный диагноз, диагностика, гистопатология и лечение. J Am Acad Дерматол. 2015 декабрь;73(6):911-26; 927-8. [PubMed: 26568336]
, Аль-Кубати Ю., Шварц Р.А. Кожный и кожно-слизистый лейшманиоз: дифференциальный диагноз, диагностика, гистопатология и лечение. J Am Acad Дерматол. 2015 декабрь;73(6):911-26; 927-8. [PubMed: 26568336]- 5.
Torres-Guerrero E, Quintanilla-Cedillo MR, Ruiz-Esmenjaud J, Arenas R. Лейшманиоз: обзор. F1000рез. 2017;6:750. [Бесплатная статья PMC: PMC5464238] [PubMed: 28649370]
- 6.
Разнорабочий Э., Буллен Д.В. Взаимодействие Leishmania с макрофагом хозяина. Тенденции Паразитол. 2002 авг; 18 (8): 332-4. [PubMed: 12377273]
- 7.
Rogers ME, Chance ML, Bates PA. Роль промастиготного секреторного геля в происхождении и передаче инфекционной стадии Leishmania mexicana москитом Lutzomyia longipalpis. Паразитология. 2002 г., май; 124 (часть 5): 495–507. [PubMed: 12049412]
- 8.
де Врис Х.Дж., Ридейк С.Х., Шаллиг Х.Д. Кожный лейшманиоз: последние достижения в диагностике и лечении. Am J Clin Дерматол.
 2015 апр; 16 (2): 99-109. [Бесплатная статья PMC: PMC4363483] [PubMed: 25687688]
2015 апр; 16 (2): 99-109. [Бесплатная статья PMC: PMC4363483] [PubMed: 25687688]- 9.
Хоссейнзаде М., Омидифар Н., Лохрасб М.Х. Использование тонкоигольной аспирационной цитологии в диагностике кожного лейшманиоза: сравнение с обычным методом соскоба. Троп Док. 2012 г., апрель; 42(2):112-3. [PubMed: 22431831]
- 10.
Соуза А.К., Помпеу М.М., Фрутуозо М.С., Лима Дж.В., Тинел Дж.М., Пирсон Р.Д. Мазок пресс-отпечатка: быстрый, простой и дешевый метод диагностики кожного лейшманиоза, вызванного Leishmania (Viannia) braziliensis. Am J Trop Med Hyg. 2014 ноябрь; 91 (5): 905-7. [Бесплатная статья PMC: PMC4228884] [PubMed: 25114007]
- 11.
Тофиги Наим А., Махмуди С., Сабуи Ф., Хаджаран Х., Пуракбари Б., Мохебали М., Заркеш М.Р., Мамиши С. Клинические особенности и лабораторные данные висцерального лейшманиоза у детей, направленных в больницу Детского медицинского центра, Тегеран, Иран, в 2004-2011 гг. Иран J Параситол.
 2014 март;9(1):1-5. [Бесплатная статья PMC: PMC4289866] [PubMed: 25642253]
2014 март;9(1):1-5. [Бесплатная статья PMC: PMC4289866] [PubMed: 25642253]- 12.
Амато В.С., Туон Ф.Ф., Сикейра А.М., Никодемо А.С., Нето В.А. Лечение лейшманиоза слизистых оболочек в Латинской Америке: систематический обзор. Am J Trop Med Hyg. 2007 г., август; 77 (2): 266–74. [PubMed: 176]
- 13.
Мур Э.М., Локвуд Д.Н. Лечение висцерального лейшманиоза. J Glob Infect Dis. 2010 май; 2(2):151-8. [Бесплатная статья PMC: PMC2889655] [PubMed: 20606971]
- 14.
Alvar J, Vélez ID, Bern C, Herrero M, Desjeux P, Cano J, Jannin J, den Boer M., Группа ВОЗ по борьбе с лейшманиозом. Лейшманиоз во всем мире и глобальные оценки его заболеваемости. ПЛОС Один. 2012;7(5):e35671. [Бесплатная статья PMC: PMC3365071] [PubMed: 22693548]
- 15.
Berman JD, Badaro R, Thakur CP, Wasunna KM, Behbehani K, Davidson R, Kuzoe F, Pang L, Weerasuriya K, Bryceson AD. Эффективность и безопасность липосомального амфотерицина В (Амбисома) при висцеральном лейшманиозе в эндемичных развивающихся странах.


 ). При этом серологические исследования не проводятся для определения эффективности проводимого лечения — это связано с длительным обнаружением IgG в крови после излечения.
). При этом серологические исследования не проводятся для определения эффективности проводимого лечения — это связано с длительным обнаружением IgG в крови после излечения.


 , Аль-Кубати Ю., Шварц Р.А. Кожный и кожно-слизистый лейшманиоз: дифференциальный диагноз, диагностика, гистопатология и лечение. J Am Acad Дерматол. 2015 декабрь;73(6):911-26; 927-8. [PubMed: 26568336]
, Аль-Кубати Ю., Шварц Р.А. Кожный и кожно-слизистый лейшманиоз: дифференциальный диагноз, диагностика, гистопатология и лечение. J Am Acad Дерматол. 2015 декабрь;73(6):911-26; 927-8. [PubMed: 26568336] 2015 апр; 16 (2): 99-109. [Бесплатная статья PMC: PMC4363483] [PubMed: 25687688]
2015 апр; 16 (2): 99-109. [Бесплатная статья PMC: PMC4363483] [PubMed: 25687688] 2014 март;9(1):1-5. [Бесплатная статья PMC: PMC4289866] [PubMed: 25642253]
2014 март;9(1):1-5. [Бесплатная статья PMC: PMC4289866] [PubMed: 25642253]