Фиброз корней: симптомы, лечение и профилактика — Медицинский центр «Лотос»
Фиброз легких: причины, симптомы, лечение заболевания | Диффузный, интерстициальный, линейный, очаговый, идиопатический легочный фиброз
Фиброз – диагноз, указывающий на образование рубцов, фиброз легких – образование рубцов в легких. У пациентов с таким диагнозом снижены эластичные свойства и растяжимость легочной ткани, затруднено прохождение кислорода через стенки альвеол. Заболевание крайне сложно лечится и может привести к необратимым последствиям. Патология обнаруживается в большинстве случаев у людей старше 60 лет.
Симптоматика фиброза
Среди ярко выраженных симптомов фиброза легких:
- одышка, которая усиливается после физической нагрузки,
- приступы сухого кашля,
- не проходящая боль в области грудной клетки,
- хрипы,
- изменение окраски губ и конечностей,
- увеличение фаланг,
- снижение массы тела,
- быстрая утомляемость и общая слабость.
Другие болезни органов дыхательной системы также обладают схожей симптоматикой, поэтому при появлении неприятных сигналов лучше всего незамедлительно обратиться к врачу. Точно поставленный диагноз поможет в короткие сроки принять наиболее верное решение о схеме лечения и приступить к ее реализации.
Причины заболевания
Патология может быть вызвана различными причинами:
- наследственная предрасположенность,
- воспалительные процессы в легких,
- инфекционные заболевания,
- негативное влияние окружающей среды,
- работа на вредном производстве,
- воздействие лучевой терапии,
- хронические аутоиммунные болезни,
- осложнение болезней легких,
- лечение различными препаратами.
Вредные привычки, например курение, также могут вызвать опасную патологию. Однако встречаются случаи развития болезни без наличия какой-либо ярко выраженной причины. Каждый конкретный пациент должен пройти полноценное обследование для выявления факторов, повлиявших на возникновение патологии, это поможет подобрать правильное лечение, которое значительно улучшит состояние.
Виды заболевания
Выделяют два основных вида легочного фиброза:
- идиопатический фиброз легких, когда невозможно установить причину заболевания,
- интерстициальный фиброз, когда причина четко установлена.
Кроме того, по форме заболевание может быть односторонним и двусторонним, очаговым, когда поражен небольшой отдельный участок органа, и тотальным.
Методы диагностики
С целью диагностики заболевания врач-пульмонолог назначит пациенту:
- общий анализ крови,
- рентгеновское обследование,
- КТ и МРТ легких,
- биопсию тканей,
- проведение дыхательных тестов.
Какие бывают осложнения?
Если оставить симптомы фиброза легких без внимания, возможны серьезные последствия и осложнения:
- дыхательная недостаточность,
- легочная гипертензия,
- хроническое легочное сердце,
- вторичные инфекции.
Методы профилактики
Для того чтобы сохранить здоровье легких, важно соблюдать важные правила:
- использовать средства индивидуальной защиты при работе на вредных производствах,
- отказаться от вредных привычек,
- своевременно лечить болезни легких и другие инфекционные заболевания,
- контролировать состояние органов дыхания при прохождении различных методов диагностики и лечения, а также приеме определенных препаратов.
Лечение фиброза
Лечение заболевания назначается профессиональным специалистом, с учетом результатов обследования и особенностей течения болезни у пациента. Существует целый ряд препаратов, которые помогают предотвратить присоединение различных инфекций, развитие воспалений. Лечение фиброза подкрепляется лечебной дыхательной гимнастикой и полным исключением провоцирующих факторов. При тотальной форме заболевания рекомендуется оперативное вмешательство.
На ранних стадиях заболевания применяется терапия, способствующая уменьшению образования рубцов.
УЗНАТЬ ЦЕНЫ
Насколько фатальны для легких последствия коронавируса и есть ли шанс их восстановить: отвечает профессор-пульмонолог
А также у кого повышенный риск развития фиброза, пояснил один из ведущих экспертов по COVID-19, доктор медицинских наук Кирилл Зыков.
ЧТО ЗНАЧАТ ДИАГНОЗЫ «ПНЕВМОСКЛЕРОЗ» И «ПНЕВМОФИБРОЗ»
— Больше всего пациенты, переболевшие коронавирусной инфекцией, боятся фиброза легких, именно о нем нас спрашивают чаще всего, — рассказывает врач-пульмонолог, доктор медицинских наук, профессор РАН, заведующий кафедрой факультетской терапии и профболезней Московского государственного медико-стоматологического университета им. А.И. Евдокимова Кирилл Зыков.
— В диагнозе может быть написано «пневмосклероз», «пневмофиброз» — это, по большому счету, синонимы. Речь идет о разрастании в легких соединительной ткани. Это бывает по разным причинам: из-за воспалительного, из-за дистрофического процесса. В итоге нарушается основная задача легких: обеспечение газообмена. У людей из-за этого возникает одышка, сначала при физнагрузках, а при обширном фиброзе — даже в состоянии покоя.
При этом нужно помнить, что возможности наших легких очень значительны. И если после перенесенного заболевания, в том числе COVID-19, есть какой-то локальный пневмосклероз, относительно небольшие изменения, это не влияет на функциональные возможности легких. То есть человек попросту не почувствует каких-то неприятных последствий.
— Можно ли назвать процент или примерный масштаб повреждения легких, при которых такие последствия уже будут ощутимы?
— В ситуации с COVID-19 обнаружилась поразительная особенность: клиническое состояние, ощущения самого пациента могут не совпадать со степенью повреждения легких на КТ (компьютерной томографии) и по лабораторным данным. Этот одна из загадок новой инфекции.
ЧЕМ ДОЛЬШЕ ТЕЧЕНИЕ БОЛЕЗНИ, ТЕМ БОЛЬШЕ ФИБРОЗНЫЕ ИЗМЕНЕНИЯ
— От врачей сейчас часто можно услышать: о коронавирусной инфекции мы пока знаем мало, и непонятно, что дальше будет с легкими у переболевших.
— На самом деле сейчас мы можем ориентироваться на опыт предыдущих вспышек коронавирусов — SARS, или атипичной пневмонии, в 2002 — 2003 гг. и MERS, или Ближневосточного респираторного синдрома, в 2012 — 2013 гг. Срок наблюдения за пациентами, перенесшими эти виды коронавирусной инфекции, уже достаточно большой. В то время как срок нашего знакомства с COVID-19 всего около полугода.
Поэтому мы можем экстраполировать, то есть переносить данные предыдущих наблюдений на нынешнюю ситуацию. Если говорить об оценках последствий и конкретных цифрах, то большую роль играет тяжесть состояния, в котором госпитализировались пациенты. От этого зачастую зависят и шансы выжить, и частота и масштаб фиброзных изменений в легких. По разным данным, у пациентов с SARS такие изменения в легких встречались в 10 — 20% случаев (как раз в зависимости от тяжести состояния).
— И как долго сохранялись фиброзные изменения в легких?
— Есть наблюдения, что у части пациентов неблагоприятные изменения сохранялись через 9 месяцев после выписки из госпиталя. При этом выраженность фиброза зависела от длительности заболевания и его лечения. Чем дольше течение болезни, тем выше вероятность того, что у человека будут фиброзные изменения.
В ТЕМУ
У кого чаще развивается фиброз легких:
— Люди старшего возраста (65+)
— Курильщики
— Люди с генетической предрасположенностью к развитию фиброза (если этим страдали родители или один из них, бабушки, дедушки)
— Пациенты с системными воспалительными заболеваниями соединительной ткани (системная красная волчанка, склеродермия, болезнь Шегрена и другие)
— Также уже появились данные, что при COVID-19 повышен риск фиброза у пациентов с высоким маркером воспаления, то есть с более выраженными лабораторными показателями воспаления, — рассказывает профессор Кирилл Зыков. — Речь идет, в частности, об уровне С-реактивного белка в крови, уровне Интерлейкина-6 и некоторых других воспалительных маркеров. И также важным фактором является картина изменений на компьютерной томографии, которая тоже показывает уровень воспаления.
— Речь идет, в частности, об уровне С-реактивного белка в крови, уровне Интерлейкина-6 и некоторых других воспалительных маркеров. И также важным фактором является картина изменений на компьютерной томографии, которая тоже показывает уровень воспаления.
Чем больше уровень повреждений на КТ, тем выше вероятность того, что разовьются фиброзные изменения. Для тех, кто интересуется, упрощенно можно представить себе это процесс так: при «Ковиде» повреждается альвеолярный эпителий (оболочка альвеол, пузырьков в легких), резко возрастает воспалительный ответ. Как защитная реакция организма, в том числе, активируются клетки-фибробласты, формируется коллаген, и это является основной фиброза в дальнейшем
РЕШАЮЩИЙ СРОК — ПЕРВЫЙ ГОД
— 19-летнее наблюдение за пациентами, которые перенесли SARS, показало, что в течение первого года после болезни может идти уменьшение уплотнений в легких, которые обычно считают фиброзными изменениями, — продолжает эксперт.
— После года подвижек в положительную сторону уже не было.
— Но ведь считается, что фиброз необратим? Переродившуюся ткань как легких, так и любого другого органа, в клинической практике еще вроде бы не научились превращать снова в полноценно работающие клетки?
— Да, это так. В том-то и дело, что нередко за фиброз сразу после болезни принимают и другие изменения, которые обратимы, могут пройти. По данным наблюдений именно фиброз начинает формироваться обычно не раньше 3-ей недели после начала выраженного воспалительного процесса. Специалисты-морфологи (исследователи строения живых тканей. — Ред.) могут определить фиброзные изменения, которые действительно уже никуда не исчезнут.
-Так что на практике переболевшим остается ждать в течение года, чтобы понять масштаб «настоящего» фиброза и надеяться, что часть изменений пройдет, так?
— Главное, в течение этого года не усугубить ситуацию, не ухудшить состояние легких, а также принимать меры для восстановления и реабилитации.
Что показывает КТ при фиброзе легких
Главная статьи КТ-диагностика при фиброзе легкихФиброз — это разрастание соединительной ткани с появлением рубцов из-за нарушения механизмов заживления раневой поверхности.
Когда заживление протекает неправильно, могут возникать рубцовые изменения, приводящие к тому, что орган не может функционировать в полном объеме.
Соответственно, фиброз легких представляет собой рубцовые изменения ткани легких. Количество клеток, способных насыщать кровь кислородом, уменьшается. Следовательно, снижается дыхательная эффективность — развивается дыхательная недостаточность, приводящая к интоксикации, сначала при нагрузке, при усугублении течения заболевания — в покое, а далее — даже во сне. Рубцовая ткань в легких не только обладает пониженными функциональными свойствами, но и служит прекрасной средой для развития присоединенных инфекций, например, таких как бактериальная (пневмококковая или стафилококковая) пневмония.
Фиброз легких — это исход воспаления тканей во время интерстициального (то есть с поражением межклеточной соединительной ткани) заболевания легких. К причинам развития подобного заболевания могут относиться травмы легких, высокая загрязненность окружающей среды, курение, вдыхание наркотических веществ, плесени, органической, асбестовой, кварцевой и угольной пыли, инфекционные, аутоиммунные, вирусные заболевания и их осложнения — бронхит, туберкулез, пневмония, COVID-19 и многое другое.
Еще недавно синонимом самих интерстициальных заболеваний был пневмофиброз, но, к счастью, было установлено, что не все варианты таких заболеваний легких являются фиброзирующими.
Самый сложный и практически не поддающийся лечению — первичный, или идиопатический фиброз легких — быстро прогрессирующее фиброзирующее заболевание легких, причина которого неизвестна.
Симптомы фиброза легких
Легочный фиброз характеризуется симптомами одышки и сухого кашля (редко продуктивного — с мокротой) при физической нагрузке, непрекращающейся болью в области грудной клетки, быстрой утомляемостью на фоне затрудненного дыхания, похудением без изменения диеты. При аускультации легких (выслушивании с помощью фонендоскопа) выявляются ранние (в фазе вдоха) инспираторные, то есть дыхательные хрипы, чаще всего локализующиеся в нижних задних зонах легких.
При аускультации легких (выслушивании с помощью фонендоскопа) выявляются ранние (в фазе вдоха) инспираторные, то есть дыхательные хрипы, чаще всего локализующиеся в нижних задних зонах легких.
Фиброз может развиваться как в одном легком, так и в двух одновременно. Также возможны очаговая и тотальная формы фиброза. При тотальной форме зачастую требуется оперативное вмешательство, так как поражена большая часть легких. При очаговой форме изменения носят локальный характер.
КТ-диагностика фиброза легких
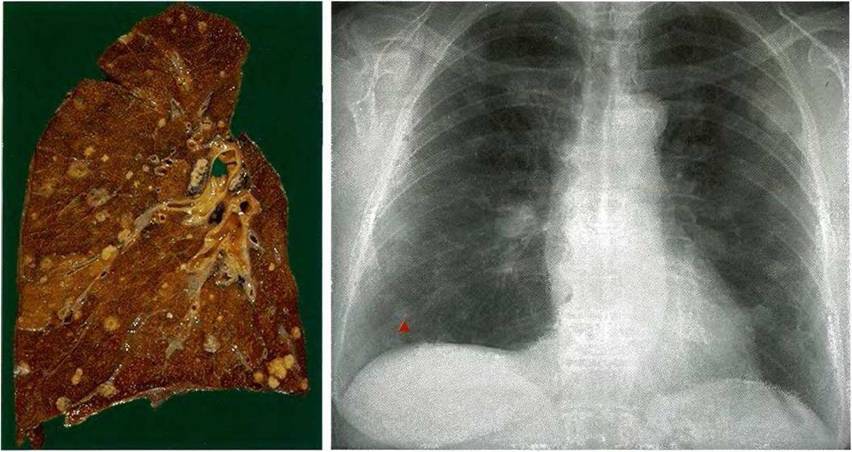
Золотой стандарт диагностики фиброза легких — компьютерная томография высокого разрешения. КТ-диагностика легочного фиброза позволяет достоверно выявить степень поражения легких, определить локализацию рубцовой ткани. Этот метод диагностики признан одним из самых чувствительных неинвазивных методов выявления легочного фиброза. Так, проведенные сравнительные исследования уже в 1990 году показали, что фиброз легких с помощью компьютерной томографии в режиме высокого разрешения (КТВР) был обнаружен в 91% случаев и только в 39% — с использованием рентгенографии органов грудной клетки.
При наличии фиброза легких в серьезной стадии на КТ виден паттерн (термин, принятый для обозначения патологических признаков в медицине) так называемого «сотового» легкого — это состояние видно на сканах как однотипные, расположенные в несколько рядов кисты, содержащие воздух, в пораженных частях одного или обоих легких. На ранних стадиях легочного фиброза подобная картина не наблюдается, поэтому потребовался поиск признаков на КТ, позволяющих выявить болезнь в ее начале. Одним из таких признаков оказалось наличие на снимках картины «матового стекла» — очагов незначительного уплотнения легочной ткани. Также специфические признаки фиброза у пациента можно обнаружить при проведении КТ легких с функциональными пробами. Так, один из признаков — субплевральное усиление периферического легочного интерстиция — ранее считался признаком отсутствия патологии.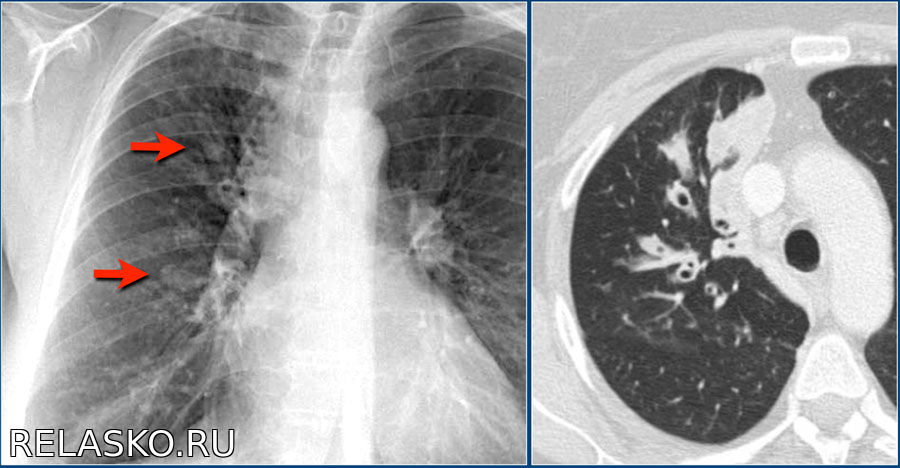 Подобные изменения практически невозможно отследить при помощи других методов аппаратной диагностики.
Подобные изменения практически невозможно отследить при помощи других методов аппаратной диагностики.
На данный момент точность методов КТ-диагностики растет благодаря введению новых протоколов исследований и тщательного изучения результатов многочисленных исследований. При этом ведущая роль в диагностическом процессе отводится врачу-рентгенологу, который трактует видимые изменения как легочный фиброз или его отсутствие. Поиск ранних лучевых признаков фиброзирующей болезни легких — ключевой момент для своевременного назначения противофибротической терапии.
Также именно мультисрезовая КТ при поставленном диагнозе используется для оценки скорости прогрессирования заболевания, выявления благоприятного и неблагоприятного типов фиброзных изменений, успеха лечения и правильности подбора терапевтический препаратов.
НЕОБРАТИМОЕ ЗАБОЛЕВАНИЕ ЛЕГКИХ ТЕПЕРЬ МОЖНО ЛЕЧИТЬ
Доктора Президентской клиники применяют уникальные препараты, замедляющие распространение такого тяжелого заболевания, как фиброз легких. Пока что это единственный лекарственный метод лечения болезни. Альтернатива ему – лишь трансплантация органа.
«Нас обнадеживает то, что сегодня медицинской наукой создано два препарата, которые позволят нам, судя по результатам больших исследований, по крайней мере, замедлить темпы прогрессирования болезни. Это таблетки, которые к счастью зарегистрированы на этот год в Казахстане. Для этого в нашей стране был пересмотрен клинический протокол, что позволит нам законным путем применять эти препараты» — рассказала главный терапевт Больницы, доктор медицинских наук, Роза Бакенова во время обучающего семинара для врачей.
Причины смертельного заболевания на сегодняшний день так и не найдены. Фиброз распознают по рубцам на ткани органа. Из-за них в легких нарушается газообмен, и человек часто страдает от недостатка воздуха. У больных развиваются одышка и хронический кашель, которые усугубляются со временем: люди с таким диагнозом в среднем живут не больше четырех-пяти лет. Это редкое заболевание имеет самую высокую смертность — выше, чем при различных видах рака, потому внедрение инновационных препаратов в Казахстане на базе Больницы Медицинского центра – пока что единственная возможность для пациентов остановить болезнь.
Фиброз распознают по рубцам на ткани органа. Из-за них в легких нарушается газообмен, и человек часто страдает от недостатка воздуха. У больных развиваются одышка и хронический кашель, которые усугубляются со временем: люди с таким диагнозом в среднем живут не больше четырех-пяти лет. Это редкое заболевание имеет самую высокую смертность — выше, чем при различных видах рака, потому внедрение инновационных препаратов в Казахстане на базе Больницы Медицинского центра – пока что единственная возможность для пациентов остановить болезнь.
ХАРАКТЕРИСТИКА ОЧАГОВ В ЛЕГКИХ, ВЫЯВЛЕННЫХ ПРИ КОМПЬЮТЕРНОЙ ТОМОГРАФИИ У ДЕТЕЙ И ПОДРОСТКОВ ИЗ ГРУПП РИСКА ПО ТУБЕРКУЛЕЗУ | Шепелева
1. Лазарева Я.В. Компьютерная томография в диагностике туберкулеза органов дыхания: Дис. … д-ра мед. наук. М.; 2002.
2. Власов П.В., Нуднов Н.В., Шейх Ж.В. Компьютерно-томографическая семиотика в пульмонологии. Медицинская визуализация. 2010; 6: 75–83.
3. Воробьев А.А., Ловачева О.В., Варшавский О.В. и др. Возможности КТ-исследования органов грудной клетки больных туберкулезом легких на предоперационном этапе. Проблемы туберкулеза и болезней легких. 2005; 8: 23–6.
4. Колесникова Е.К., Георгиади С.Г. Компьютерно-томографическая картина лимфатических узлов средостения в норме. Вестник рентгенологии и радиологии. 1990; 4: 72–7.
5. Остроумова О.М., Ивановский В.Б., Грицай И.Ю. Компьютерная томография в комплексной диагностике туберкулеза органов дыхания. Туберкулез и болезни легких. 2011; 5: 88–9.
6. Харченко В.П., Котляров П.М. Методы медицинской визуализации в диагностике заболеваний органов дыхания. Пульмонология. 1999; 9: 48–52.
Харченко В.П., Котляров П.М. Методы медицинской визуализации в диагностике заболеваний органов дыхания. Пульмонология. 1999; 9: 48–52.
7. Webb W.R. High-resolution CT of the lung parenchyma. Radiol. Clin. North. Am. 1998; 27: 1085–97.
8. Aziz Z.A., Padley S.P., Hansell D.M. CT techniques for imaging the lung: recommendations for multi-slice and single slice computed tomography. Eur. J. Radiol. 2004; 24: 119–36.
9. Миллер С.В., Фролова И.Г., Величко С.А., Тузиков С.А. Одиночные округлые образования в легком, тактика ведения. Бюллетень сибирской медицины. 2012; 5: 80–2.
Видеоассистированные резекции доли легкого — medexpert
PAEDIATRIC SURGERY.UKRAINE.2019.1(62):43-46; DOI 10.15574/PS.2019.62.43
Опанасенко М. С., Шалагай С. М., Коник Б. М., Терешкович О. В., Кшановский О. Е., Леванда Л. И.
ГУ «Национальный институт фтизиатрии и пульмонологии имени Ф.Г. Яновского НАМН Украины», г. Киев
Видеоассистированные (VATS) лобектомии проводятся с использованием эндоскопических инструментов на основе степлер-техники и общехирургических элементов. Приоритет отдается выполнению типичных резекций с раздельной обработкой элементов корня доли (артерий, вен, бронха).
Материалы и методы. За последние 5 лет (с 2014 по 2018) в отделении торакальной хирургии и инвазивных методов диагностики ГУ «Национальный институт фтизиатрии и пульмонологии имени Ф.Г. Яновского НАМН Украины» было выполнено 36 VATS-резекций доли легкого. Все 36 (100,0%) VATS-резекций проводились при использовании бронхиальной интубации контрлатерального легкого. Миниторакотомный разрез был не более 8 см. Обработка элементов корня доли проводилась с использованием эндоскопических сшивающих аппаратов на основе степлер-техники, интраоперационно проводилась механическая френикотрипсия.
Результаты. Интраоперационные осложнения были диагностированы у 2 (5,6%) пациентов. У 1 (2,8%) больного была проведена конверсия в широкую торакотомию с остановкой кровотечения. Общий уровень послеоперационных осложнений составил 5 (13,9%) наблюдений. Средняя продолжительность резекционных оперативных вмешательств составила 188,4±73,6 мин, а средняя интраоперационная кровопотеря – 86,1±154,1 мл. Средняя продолжительность лечения в послеоперационном периоде составила 29,2±14,1 дня.
Выводы. VATS-резекции доли легкого являются малотравматичными и перспективными методами лечения, обеспечивающими анатомическое препарирование элементов корня доли легкого. Их можно рассматривать как альтернативу открытой лобектомии. Широкому использованию данного метода препятствуют выраженный фиброз корня легкого и спайковый процесс вследствие длительного воспалительного процесса и медикаментозного лечения, а также стоимость эндоскопических инструментов.
Ключевые слова: VATS-лобектомия, резекция доли, видеоассистированная резекция.
Статья поступила в редакцию 20.10.2018 г., принята к печати 15.01.2019 г.
ЛИТЕРАТУРА
1. Chung JH et al. (2015, Jun). Uniportal video-assisted thoracoscopic lobectomy: an alternative to conventional thoracoscopic lobectomy in lung cancer surgery? Interact Cardiovasc Thorac Surg. 20(6):813–819. https://doi.org/10.1093/icvts/ivv034; PMid:25736285
2. Ismail NA, Elsaegh M, Dunning J. (2015). Novel Techniques in Video-assisted Thoracic Surgery (VATS) Lobectomy. Surg Technol Int. 26:206–209. Review. PMID: 26055011.
3. McElnay P et al. (2014). Adopting a standardized anterior approach significantly increases video-assisted thoracoscopic surgery lobectomy rates. Eur J Cardiothorac Surg. 1:100105. https://doi.org/10.1093/ejcts/ezt561; PMid:24335265. Epub 2013 Dec 11.
Eur J Cardiothorac Surg. 1:100105. https://doi.org/10.1093/ejcts/ezt561; PMid:24335265. Epub 2013 Dec 11.
4. Melfi FM, Fanucchi O, Davini F, Mussi A. (2014). VATS-based approach for robotic lobectomy. Thorac Surg Clin. 2:143–149. https://doi.org/10.1016/j.thorsurg.2014.02.003; PMid:24780417
5. Mercedes de la Torre et al. (2016). Uniportal VATS lobectomy. Minerva Chir. 71(1):46–60. Epub 2015 Nov 24. Review. PubMed PMID: 26606690.
6. Mollberg NM, Mulligan MS. (2014). Video-assisted thoracoscopic (VATS) lobectomy after induction therapy. Thorac Surg Clin. 4:465–470. https://doi.org/10.1016/j.thorsurg.2014.07.013; PMid:25441140
Фиброзный пульпит: формы, симптомы, методы лечения
Без лечения хроническая фиброзная форма пульпита может привести к потере зуба. Врачи клиники «Денталюкс-М» в Москве используют все возможности современной стоматологии, чтобы помочь вам избежать такого исхода.
СУТЬ ЭТОЙ ПАТОЛОГИИ
Кариозное разрушение эмали приводит к повреждению лежащего под ней дентина — твердой ткани, пронизанной системой канальцев, которые соединены с мягкой «сердцевиной» зуба. Это и есть пульпа, а состоит она из:
- нервов;
- кровеносных сосудов;
- лимфатических узлов;
- соединительной ткани.
Чем в большей степени разрушаются эмаль и дентин, тем выше вероятность перехода патологического процесса на мягкие ткани. Поэтому лучшая профилактика осложнений кариеса — своевременные визиты к врачу.
Вялотекущее хроническое воспаление, при котором в полости зуба идет образование гранулята с последующим склерозированием и разрастанием соединительной ткани, носит название фиброзного пульпита.
ПРИЧИНЫ И СИМПТОМЫ
В большинстве случаев предшественником этой формы становится острое воспаление «нерва» зуба, которое сопровождается выраженными болевыми ощущениями. Это бывает после вскрытия канала у пациентов с высокой сопротивляемостью организма, когда появляются пути для нормального оттока воспалительного экссудата.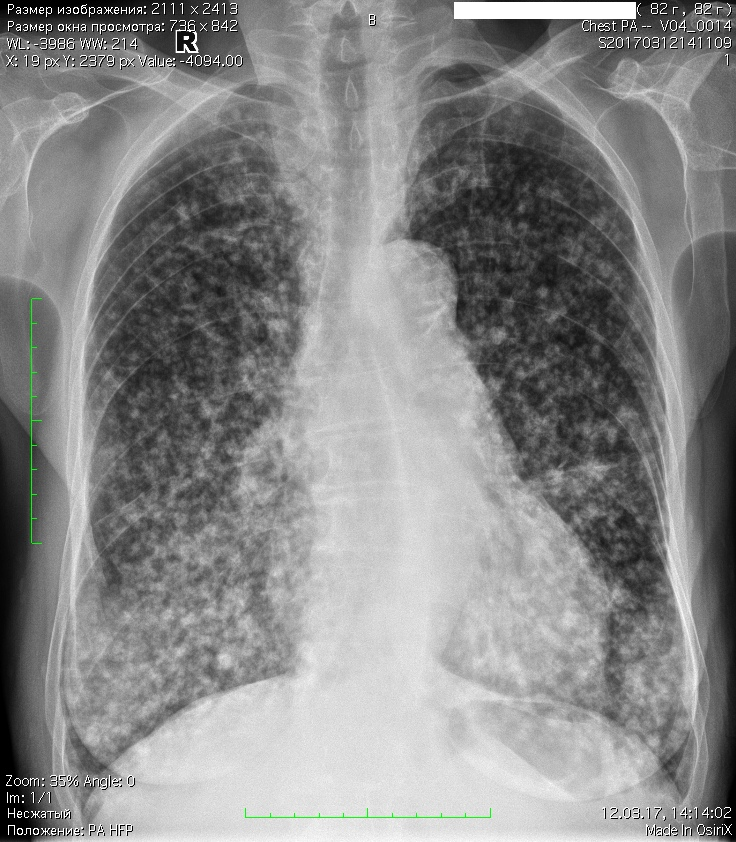
У детей младшего возраста и пациентов с низкой реактивностью организма эта болезнь может изначально приобретать хронический характер, без клинических проявлений острой стадии.
ТИПИЧНЫЕ СИМПТОМЫ:
- ноющие боли, усиливающиеся вечером и ночью;
- резкая продолжительная реакция на температурный раздражитель;
- чувство распирания и тяжести в зубе;
- острая боль при зондировании канала.
ТОЧНАЯ ДИАГНОСТИКА
Самое важное — четко дифференцировать фиброзный пульпит от других заболеваний. В частности, от глубокого кариеса его отличает продолжительная болевая реакция на внешнее раздражение, а также отсутствие самопроизвольных острых болей, отдающих в висок или челюсть.
Для гангренозной формы характерны сероватая окраска эмали, гнилостный запах, болезненность при зондировании устья каналов. При патологической гипертрофии мягких тканей зуба зуба (еще одно заболевание в классификации пульпитов) пациент жалуется на длительные боли, не связанные с раздражающими факторами, а врач во время осмотра видит разросшуюся кровоточивую пульпу.
Если вы воспользуетесь услугами нашей стоматологии, мы выполним точную дифференциальную диагностику, применив специальные методы исследования. После этого подберем оптимальный способ терапии.
СПОСОБЫ ЛЕЧЕНИЯ
При этой патологии наблюдается необратимое изменение мягких тканей зуба, последствия которого можно ликвидировать только с помощью частичного или полного их удаления. Консервативная терапия эффекта не даст, так как даже с помощью сильных лекарств невозможно вернуть пульпе прежнее состояние. Поэтому ее извлекают из зуба одним из двух способов.
-
Витальный метод
Эта стоматологическая операция представляет собой удаление «нерва» без его предварительного «умерщвления». Бывает:
- частичной (ампутация) — удаляется только пульпа коронковой части, без проникновения в каналы, способ применяют в основном в детской стоматологии;
- полной (экстирпация) — извлекается весь «нерв», в том числе из корневой части зуба.

-
Девитальный метод
При фиброзном пульпите этот способ лечения в последнее время используют редко, так как он более травматичен и менее физиологичен для организма. Эта методика предполагает предварительное умерщвление «нерва» специальными препаратами с последующей его экстирпацией. Девитальную ампутацию сегодня не применяют.
ЛЕЧЕБНЫЕ МАНИПУЛЯЦИИ
Все стоматологические операции в нашей клинике проводят под анестезией, поэтому пациент не чувствует боли. Вначале врач препарирует кариозную полость с помощью бормашины, затем обрабатывает антисептиками. После удаления пульпы одним из методов специалист готовит каналы к пломбированию.
На завершающей стадии освободившуюся и расширенную внутреннюю полость зуба пломбируют, после чего восстанавливают разрушенную часть коронки. В нашей клинике лечение фиброзного пульпита проводится под контролем рентгенографии, что помогает снизить риск осложнений.
Борьба с корнями муковисцидоза
В области муковисцидоза наконец-то происходят прорывы. В то время как последние заголовки CF рекламируют новое генетическое лечение, направленное на его первопричину, остается серьезная проблема: как нам избавиться от хронических инфекций легких, от которых страдают пациенты с CF? Ученый из Университета штата Мичиган пытается понять, как эти сложные инфекции вызывают такое ужасное заболевание.
Посредством гранта Национального института здравоохранения на сумму 2,7 миллиона долларов США MSU и Spectrum Health изучают повсеместно распространенные анаэробные бактерии, обнаруженные у всех пациентов с МВ, которые ученые часто отвергают как нефакторные.
«Хотя недавно одобренный препарат Трикафта не является лекарством, он, безусловно, продемонстрировал положительную пользу для здоровья людей, страдающих этим заболеванием; даже пациенты на Трикафте будут бороться с хроническими легочными инфекциями », — сказал Роберт Куинн, доцент кафедры биохимии и молекулярной биологии МГУ и исследователь Global Impact, который руководит грантом.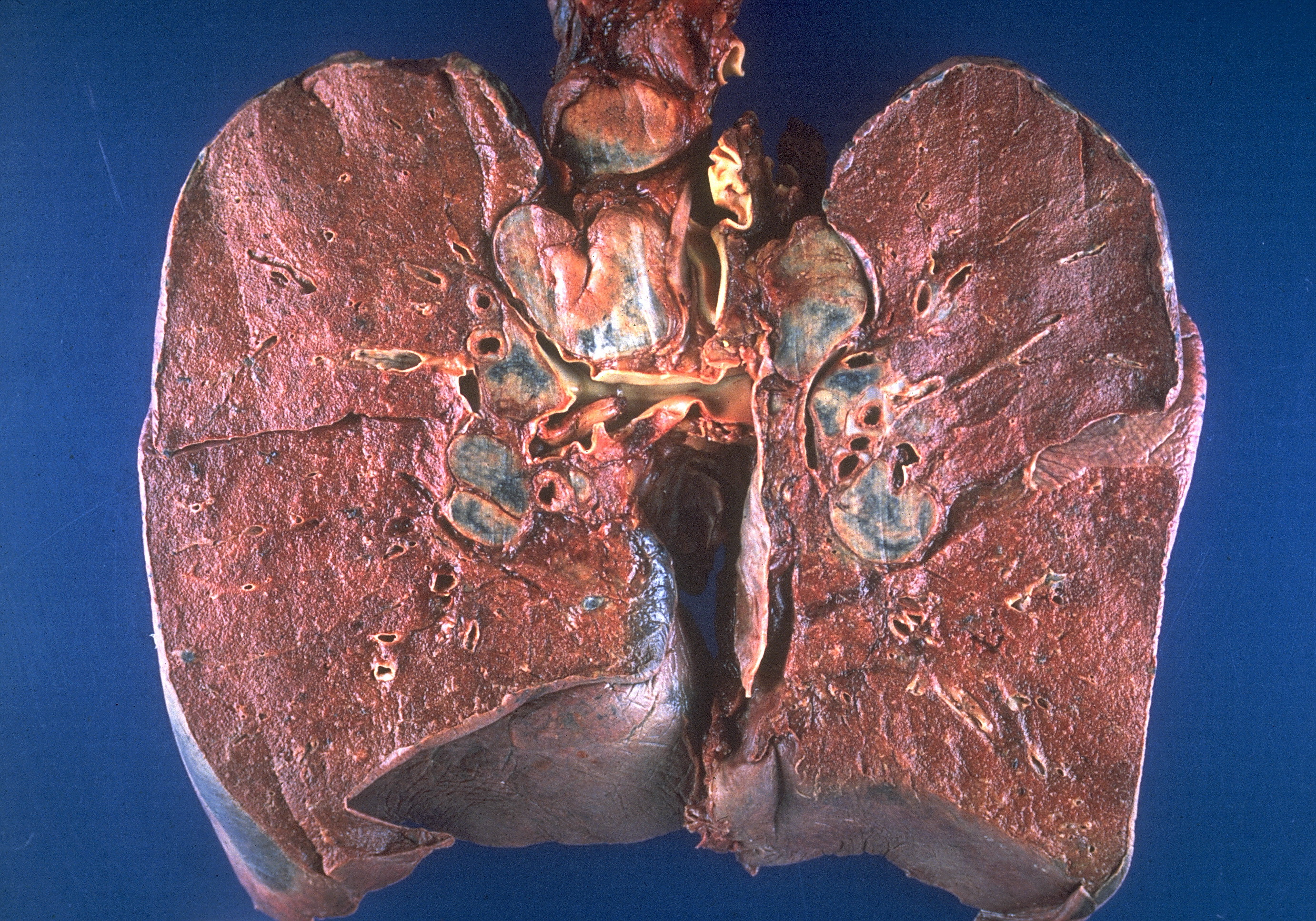 «Мы должны использовать двойной подход: лечение первопричины и лечение легочных инфекций, если мы хотим когда-либо искоренить болезнь.”
«Мы должны использовать двойной подход: лечение первопричины и лечение легочных инфекций, если мы хотим когда-либо искоренить болезнь.”
Муковисцидоз — это прогрессирующее опасное для жизни заболевание, при котором густая слизь накапливается в основном в легких, а также в других частях тела. Врачи лечат хроническую легочную инфекцию все более агрессивными антибиотиками. Хотя многие ученые не понимают эффективности лечения антибиотиками против инфекций МВ, это традиционный подход к большинству, если не всем, пациентам.
Команда Куинна сосредоточена на бактериях, которые размножаются в легких, поскольку сгущающаяся слизь перекрывает им доступ кислорода.Каким бы парадоксальным это ни казалось в легких, эти анаэробные бактерии живут без кислорода и часто присутствуют в легких, инфицированных CF, но мало что известно об их роли в качестве патогенов или участников CF.
КомандаКуинн сосредоточивает свое внимание на обострениях легких, обострениях болезни, которые требуют госпитализации, включая усиление тяжести симптомов, потерю жизненной емкости легких и агрессивное лечение антибиотиками. Во время этих обострений происходит обновление популяций бактерий; анаэробные бактерии переключают механизмы, чтобы процветать и доминировать.
«Многие врачи, лечащие пациентов, не знают об этих анаэробах», — сказал Куинн. «Есть еще много предположений о лечении CF. Назначаются антибиотики, обострения временно стихают, и пациента выписывают из больницы; но иногда они не улучшаются, и врачи не понимают, почему.
«Мы считаем, что врачи не лечили основную причину обострения — анаэробы», — сказал Куинн.
Сотрудничая со Spectrum Health, ученые смогут собрать множество образцов у пациентов, страдающих муковисцидозом, и изучить микробную динамику, которая вызывает заболевание.Они также будут использовать новую модель, разработанную в МГУ, которая имитирует легкое, инфицированное CF, чтобы они могли проверить свою гипотезу в более реалистичной среде.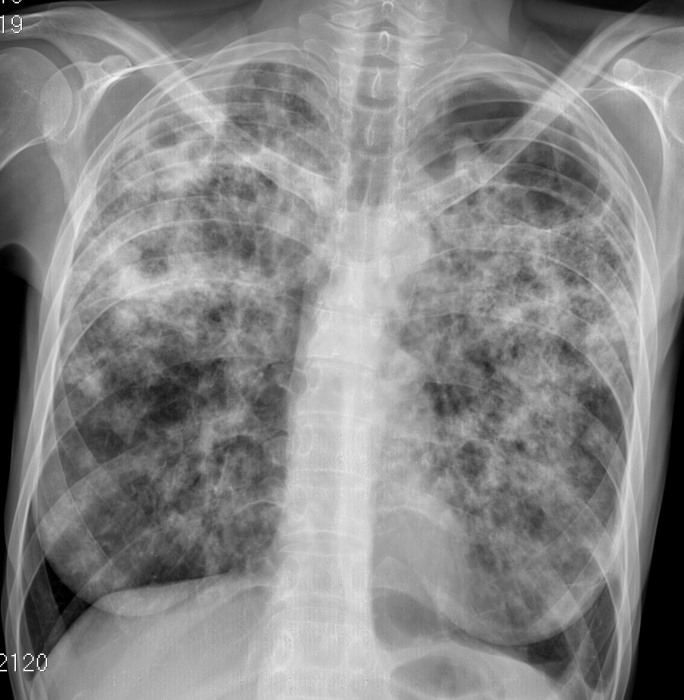
Кроме того, команда будет использовать передовые мультиомные методы, включая секвенирование микробиома, метаболомику и новые платформы анализа биоинформатических данных, по сути, используя подход больших данных для выявления ключей к излечению, сказал Куинн.
«Наше научное обоснование состоит в том, что лучшее понимание того, что вызывает микробные изменения во время этих обострений, приведет к более эффективной и целенаправленной терапии против патогенов», — сказал он.
Лэйн Кэмерон, Роберт Куинн
Этот контент был первоначально размещен Университетом штата Мичиган.
Борьба с муковисцидозом в корне
Исследования и технологии
ВОСТОК-ЛАНСИНГ, штат Мичиган, , 19 ноября 2019 г. — Наконец-то происходят прорывы в области муковисцидоза. В то время как последние заголовки CF рекламируют новое генетическое лечение, направленное на его первопричину, остается серьезная проблема: как нам избавиться от хронических инфекций легких, от которых страдают пациенты с CF? Ученый из Университета штата Мичиган пытается понять, как эти сложные инфекции вызывают такое ужасное заболевание.
Посредством гранта Национального института здравоохранения на сумму 2,7 миллиона долларов США MSU и Spectrum Health изучают повсеместно распространенные анаэробные бактерии, обнаруженные у всех пациентов с МВ, которые ученые часто отвергают как нефакторные.
«Хотя недавно одобренный препарат Трикафта не является лекарством, он, безусловно, продемонстрировал положительную пользу для здоровья людей, страдающих этим заболеванием; даже пациенты на Трикафте будут бороться с хроническими легочными инфекциями », — сказал Роберт Куинн, доцент кафедры биохимии и молекулярной биологии МГУ, ведущий грант.«Мы должны использовать двойной подход: лечить первопричину и лечить легочные инфекции, если мы хотим когда-либо искоренить болезнь».
Муковисцидоз — это прогрессирующее опасное для жизни заболевание, при котором густая слизь накапливается в основном в легких, а также в других частях тела. Врачи лечат хроническую легочную инфекцию все более агрессивными антибиотиками. Хотя многие ученые не понимают эффективности лечения антибиотиками против инфекций МВ, это традиционный подход к большинству, если не всем, пациентам.
«Исследование микробиома под руководством доктора Куинна чрезвычайно важно. У людей с муковисцидозом часто развиваются легочные инфекции », — сказал пульмонолог Spectrum Health Марк Макклелланд, доктор медицины. «Это исследование должно помочь нам лучше понять эти инфекции и позволить нам более эффективно лечить пациентов. При этом конечная цель — улучшить функцию легких и общее состояние здоровья ».
Команда Куинна сосредоточена на бактериях, которые размножаются в легких, поскольку сгущающаяся слизь перекрывает им доступ кислорода.Каким бы парадоксальным это ни казалось в легких, эти анаэробные бактерии живут без кислорода и часто присутствуют в легких, инфицированных CF, но мало что известно об их роли в качестве патогенов или участников CF.
КомандаКуинн сосредоточивает свое внимание на обострениях легких, обострениях болезни, которые требуют госпитализации, включая усиление тяжести симптомов, потерю жизненной емкости легких и агрессивное лечение антибиотиками. Во время этих обострений происходит обновление популяций бактерий; анаэробные бактерии переключают механизмы, чтобы процветать и доминировать.
«Многие врачи, лечащие пациентов, не знают об этих анаэробах», — сказал Куинн. «Есть еще много предположений о лечении CF. Назначаются антибиотики, обострения временно стихают, и пациента выписывают из больницы; но иногда они не улучшаются, и врачи не понимают, почему.
«Мы считаем, что врачи не лечили основную причину обострения — анаэробы», — сказал Куинн.
Сотрудничая со Spectrum Health, ученые смогут собрать множество образцов у пациентов, страдающих муковисцидозом, и изучить микробную динамику, которая вызывает заболевание. Они также будут использовать новую модель, разработанную в МГУ, которая имитирует легкое, инфицированное CF, чтобы они могли проверить свою гипотезу в более реалистичной среде.
Они также будут использовать новую модель, разработанную в МГУ, которая имитирует легкое, инфицированное CF, чтобы они могли проверить свою гипотезу в более реалистичной среде.
Кроме того, команда будет использовать передовые мультиомные методы, включая секвенирование микробиома, метаболомику и новые платформы анализа биоинформатических данных, по сути, используя подход больших данных для выявления ключей к излечению, сказал Куинн.
«Наше научное обоснование состоит в том, что лучшее понимание того, что вызывает микробные изменения во время этих обострений, приведет к более эффективной и целенаправленной терапии против патогенов», — сказал он.
###
Университет штата Мичиган работает над продвижением общего блага необычными способами в течение 160 лет. Один из ведущих исследовательских университетов в мире, МГУ фокусирует свои обширные ресурсы на поиске решений некоторых из наиболее актуальных мировых проблем, предоставляя при этом изменяющие жизнь возможности разнообразному и инклюзивному академическому сообществу с помощью более 200 программ обучения по 17 степеням. -дипломные колледжи.
Контакт : Лэйн Кэмерон, Университетская коммуникация: (517) 353-8819, (765) 748-4827, camer102 @ msu.edu; Роберт Куинн, биохимия и молекулярная биология: (517) 353-1426, [email protected]
Spectrum Health System, некоммерческая интегрированная система здравоохранения, привержена делу улучшения здоровья и благополучия наших сообществ. Мы выполняем нашу миссию каждый день с 31 000 сострадательных профессионалов, 4600 медицинскими экспертами, 3300 преданными добровольцами и планом медицинского страхования с более чем 1 миллионом участников. Наши талантливые врачи и лица, осуществляющие уход, имеют привилегию предлагать полный спектр услуг по уходу и оздоровлению нашим сообществам в 14 больницах, включая детскую больницу Хелен ДеВос, 150 амбулаторных пунктов и услуги телемедицины.Мы ищем решения для здравоохранения сегодня и завтра, которые разнообразят наши предложения. Наша система здравоохранения, находящаяся под местным управлением и базирующаяся в Гранд-Рапидсе, штат Мичиган, предоставила обществу 550 миллионов долларов в 2019 календарном году. Благодаря щедрости наших сообществ мы получили 37 миллионов долларов на благотворительность для поддержки исследований, научных исследований, инноваций и клинической помощи. Компания Spectrum Health была признана одной из 15 лучших систем здравоохранения страны по версии Truven Health Analytics®, входящей в состав IBM Watson HealthTM.
Контактное лицо:
Тим Хокинс
Связи со СМИ
Офис: 616.486.6091
Мобильный: 616.443.0361
Электронная почта: [email protected]
IPF могут иметь различные и сложные генетические корни
Генетические факторы могут влиять, по крайней мере, частично на риск идиопатического легочного фиброза (IPF), особенно при семейных формах заболевания, и обзор Медицинской школы Нанкинского университета, Китай, представил обновленный взгляд на генетические факторы риска ИЛФ.
Статья «Гены-кандидаты идиопатического фиброза легких: современные данные и исследования» была опубликована в журнале The Application of Clinical Genetics.
Считается, что на семейные IPF приходится менее 5 процентов всех случаев IPF, но более поздние оценки показывают, что цифры с большей вероятностью приближаются к 20 процентам. Единственная разница между спорадической и семейной IPF — это то, что болезнь, как правило, проявляется раньше у семейных пациентов.
Был идентифицирован ряд генов, которые могут быть связаны с развитием болезни.Сегодняшние подходы, использующие методы секвенирования следующего поколения для анализа последовательностей целых экзомов и целых геномов, а также полногеномные исследования ассоциаций (GWAS), вероятно, позволят выявить больше генов, которые могут повлиять на развитие или исход IPF.
Одна из теорий патологии IPF утверждает, что это заболевание влияет на стабильность альвеол. Идея состоит в том, что слой эпителиальных клеток, выстилающий альвеолы легких, является дисфункциональным. Однако является ли эта дисфункция следствием воспалительных реакций — как предполагает классическая гипотеза — или аномальной репарации альвеолярного эпителия, остается предметом разногласий.
Сообщается, что дефекты генетических факторов, влияющих на стабильность альвеол, чаще встречаются у пациентов с семейной ИЛФ. Такие гены, как SFTPC — , кодирующий белок SP-C, могут влиять на поверхностное натяжение на границе раздела воздух-вода в альвеолах легких. Эпителиальные клетки внутри альвеол выстланы поверхностно-активным веществом, состоящим из 10 процентов белка и 90 процентов липидов. Отсутствие этого защитного слоя вызывает коллапс альвеол. Было обнаружено, что несколько генов, кодирующих различные компоненты слоя сурфактанта, а также факторы, обрабатывающие эти компоненты, мутированы как в семейных, так и в спорадических IPF.
Наряду с SFTPC, у некоторых людей затрагивает связанный SFTPA2 ген . Этот ген, помимо того, что играет роль в стабильности альвеол, связан с профибротическим фактором TGF-β, и пациенты с мутированным SFTPA2 имеют более высокие уровни TGF-β.
Другой ген, названный ABCA3, , был идентифицирован при неонатальном респираторном дистресс-синдроме и интерстициальном заболевании легких у детей. Белок переносит липиды через плазматическую мембрану клеток, и исследователи полагают, что он может играть роль в метаболизме и транспорте сурфактанта.В этом гене было идентифицировано более 150 различных мутаций, некоторые из которых, как полагают, влияют на эффекты мутации в гене SPTPC . Недавние исследования также показали, что, помимо предположения о риске заболевания легких у детей, мутации в ABCA3 также могут лежать в основе некоторых случаев ИЛФ у взрослых.
Укорочение теломер — один из факторов, наиболее часто связанных с IPF. Теломеры — это участки ДНК на концах хромосом, защищающие их от истирания и слияния с другими хромосомами.Теломеры естественным образом укорачиваются с возрастом, что, возможно, объясняет увеличение показателей IPF у пожилых людей. Мутации в генах комплекса теломеразы — ферментативного механизма, пополняющего теломеры во время деления клеток — приводят к увеличению скорости разрушения теломер, и IPF является наиболее частым клиническим проявлением синдрома коротких теломер.
Белки TERT и TERC в комплексе теломеразы поражаются наиболее часто, и примерно у 10 процентов семейных и от 1 до 3 процентов спорадических пациентов с ИЛФ наблюдаются вариации в этих двух основных компонентах теломеразы.Тем не менее, связь коротких теломер-IPF не может быть объяснена только этими двумя генами, поскольку до 25 процентов спорадических и 40 процентов семейных случаев имеют укороченные теломеры, но менее половины этих пациентов имеют мутации в TERT или Гены TERC . Другие гены, связанные с теломерами, изучаются, и есть некоторые доказательства того, что ген DKC1, кодирующий другой компонент теломеразы, может участвовать в IPF. Тем не менее, др. Исследования предполагают, что PARN и, что более важно, RTEL1 вносят вклад в короткие теломеры и IPF.
A GWAS в 2011 году при скрининге пациентов с семейной интерстициальной пневмонией идентифицировал MUC5B как ген, наиболее сильно связанный с риском интерстициальной пневмонии. Более поздние исследования показали, что частота риска составляет 38 процентов среди пациентов с ИЛФ, 34 процента среди пациентов с семейной интерстициальной пневмонией и 9 процентов в контрольной группе. Ген кодирует компонент слизи дыхательных путей, и общие мутации приводят к увеличению выработки белка. Специфическая мутация в промоторной области гена, контролирующая экспрессию гена, в настоящее время является наиболее распространенным генетическим вариантом, предрасполагающим к ИЛФ.
Неизвестно, как высокие уровни белка MUC5B влияют на развитие IPF, но недавние исследования показали, что белок обнаруживается в альвеолярных эпителиальных клетках, которые обычно не экспрессируют факторы слизи. Исследователи предполагают, что повышенные уровни MUC5B могут быть связаны с нарушением очистки от слизи и восстановления альвеол, а также мешают механизмам иммунной защиты. Было высказано предположение, что этот генетический вариант может служить прогностическим биомаркером для развития IPF, но необходимы дополнительные исследования, чтобы прояснить роль этого белка в IPF.
Давняя гипотеза иммунного вовлечения в IPF могла быть поставлена под сомнение из-за недостаточной эффективности иммуномодулирующих препаратов, таких как азатиоприн, но, тем не менее, остаются доказательства дисфункциональных иммунных компонентов. Мутации в иммунных генах TLR часто связаны с IPF. Мутация в гене TOLLIP была связана со смертностью, и другие исследования показывают, что ELMOD2 — ген , экспрессируемый в альвеолярных макрофагах — может быть связан с семейной IPF.Однако из-за ряда противоречивых результатов ген ELMOD2 все еще исследуется в качестве гена-кандидата в IPF.
Другие исследования показали, что генетические вариации в локусе гена MHC, определяющие гистосовместимость тканей, вносят вклад в IPF, но эти утверждения все еще исследуются. Доказательства изменений в генах цитокинов, кодирующих различные сигнальные молекулы иммунной системы, также открыты для обсуждения. Одно интересное исследование показало, что ряд генов цитокинов не увеличивает риск заболевания, но способствует его тяжести.
Наконец, различные генетические факторы, связанные с такими несопоставимыми функциями, как адгезия клеток, целостность цитоскелета и митохондриальная дисфункция, также были предложены, чтобы играть роль в развитии болезни IPF.
Авторы заявили, что более полные списки вариантов генов, вносящих вклад в IPF, могут быть получены с помощью высокопроизводительного анализа и секвенирования следующего поколения. Однако для понимания патологических механизмов, которые могут привести к лучшему лечению, может быть более важным изучить взаимодействия между генами и факторами окружающей среды.
Паеонифлорин, основной активный компонент корней Paeonia lactiflora, ослабляет вызванный блеомицином фиброз легких у мышей, подавляя синтез коллагена I типа.
Наблюдать влияние пеонифлорина на активацию фибробластов 3T3, пролиферацию и выработку коллагена посредством IL-13 / Сигнальный путь STAT6. Штамм клеток 3T3 культивировали в бессывороточной среде в течение 12 ч, затем стимулировали пеонифлорином (200, 400, 600, 800 и 1000 мг / л) или rIL-13 (6,25, 12.5, 50, 100 и 200 мкг / л) в течение еще 24 часов. В то же время наблюдалась холостая контрольная группа для пеонифлорина или rIL-13. Пролиферацию клеток 3T3 анализировали с помощью набора для подсчета клеток-8 (CCK-8), и подходящую концентрацию (100 мкг / л) rIL-13 выбирали в соответствии с результатом пролиферации клеток. Затем клетки 3T3, культивированные в бессывороточной среде в течение 12 часов, стимулировали 100 мкг / л rIL-13 в течение 12 часов, а затем обрабатывали различными концентрациями пеонифлорина (200, 400, 600, 800 и 1000 мг / л. ) еще на 24 часа.Необработанные клетки 3T3 служили холостым контролем. Пролиферацию клеток измеряли с помощью CCK-8. Содержание гидроксипролина в супернатанте клеток определяли методом щелочного лизиса. Экспрессию белков IL-13Ralpha1, альфа-SMA и STAT6 определяли вестерн-блоттингом. Экспрессию мРНК Col-I, Col-III, IL-13Ralpha1 и STAT6 анализировали с помощью ОТ-ПЦР. Пеонифлорин ингибировал пролиферацию клеток 3T3 в зависимости от концентрации (r = -0,980, P <0,01), и между всеми группами была статистически значимая разница (F = 198.599, P <0,01). rIL-13 вызывал заметно зависимое от концентрации увеличение пролиферации клеток 3T3 (r = 0,538, P <0,05). Пеонифлорин (200, 400, 600, 800 и 1000 мг / л) ингибировал пролиферацию клеток 3T3, стимулированную rIL-13, в зависимости от концентрации (1,780 +/- 0,177, 1,636 +/- 0,073, 0,965 +/- 0,066 , 0,623 +/- 0,037, 0337 +/- 0,022, r = -0,971, P <0,01), и среди всех групп существовала значимая разница (F = 198,537, P <0,01). Более того, пеонифлорин также подавлял секрецию гидроксипролина из клеток 3T3, стимулированных rIL-13, в зависимости от концентрации (3.030 +/- 0,094, 2,976 +/- 0,047, 2,814 +/- 0,047, 2,652 +/- 0,124, 2,408 +/- 0,124, r = -0,916, P <0,01) со статистической значимостью среди всех групп (F = 13,642 , P <0,01). Дальнейшие исследования показали, что пеонифлорин снижает как экспрессию белков альфа-SMA, IL-13Ralpha1 и STAT6, так и экспрессию мРНК Col-I, Col-III, IL-13Ralpha1 и STAT6 в клетках 3T3, стимулированных rIL-13. Пеонифлорин подавляет активацию, пролиферацию фибробластов и выработку коллагена из фибробластов через сигнальный путь IL-13 / STAT6, который может быть одним из механизмов антипеченочного фиброза пеонифлорина при японском шистосомозе.
ПРАЙМ PubMed | Пеонифлорин, основной активный компонент корней Paeonia lactiflora, ослабляет вызванный блеомицином фиброз легких у мышей, подавляя синтез коллагена I типа
Citation
Ji, Yu, et al. «Пеонифлорин, основной активный компонент корней Paeonia Lactiflora, ослабляет вызванный блеомицином фиброз легких у мышей, подавляя синтез коллагена I типа». Журнал этнофармакологии, т. 149, нет. 3, 2013, стр.825-32.
Ji Y, Wang T, Wei ZF и др. Пеонифлорин, основной активный компонент корней Paeonia lactiflora, ослабляет вызванный блеомицином фиброз легких у мышей, подавляя синтез коллагена I типа. Дж. Этнофармакол . 2013; 149 (3): 825-32.
Цзи, Ю., Ван, Т., Вэй, З. Ф., Лу, Г. X., Цзян, С. Д., Ся, Ю. Ф., и Дай, Ю. (2013). Пеонифлорин, основной активный компонент корней Paeonia lactiflora, ослабляет вызванный блеомицином фиброз легких у мышей, подавляя синтез коллагена I типа. Журнал этнофармакологии , 149 (3), 825-32. https://doi.org/10.1016/j.jep.2013.08.017
Ji Y, et al. Пеонифлорин, основной активный компонент корней Paeonia Lactiflora, ослабляет вызванный блеомицином фиброз легких у мышей, подавляя синтез коллагена I типа. J Ethnopharmacol. , 7 октября 2013 г .; 149 (3): 825-32. PubMed PMID: 23973787.
TY — JOUR T1 — Пеонифлорин, основной активный компонент корней Paeonia lactiflora, ослабляет вызванный блеомицином фиброз легких у мышей, подавляя синтез коллагена I типа.AU — Джи, Ю, AU — Ван, Тин, AU — Вэй, Чжи-Фэн, AU — Лу, Го-Сюнь, AU — Цзян, Си-де, AU — Ся, Ю-Фэн, AU — Дай, Юэ, 1 год — 2013/08/22 / PY — 2013/03/21 / получено PY — 2013/07/01 / исправлено PY — 2013/08/06 / принято PY — 2013/8/27 / entrez PY — 2013/8/27 / pubmed PY — 2014/4/22 / medline KW — внеклеточный матрикс KW — Paeoniflorin KW — Легочный фиброз KW — путь TGF-β / Smad KW — коллаген I типа SP — 825 EP — 32 JF — журнал этнофармакологии JO — J Этнофармакол ВЛ — 149 ИС — 3 N2 — ЭТНОФАРМАКОЛОГИЧЕСКАЯ АКТУАЛЬНОСТЬ: В теории традиционной китайской медицины фиброз легких (ЛФ) относится к легочной артралгии, что означает застой крови в легочной ткани.Корни Paeonia lactiflora Pall обычно используются для облегчения симптомов этого заболевания, улучшая кровообращение и устраняя застой крови. Пэонифлорин, основной активный ингредиент P. lactiflora, может иметь потенциал против PF. ЦЕЛЬ ИССЛЕДОВАНИЯ: это исследование было направлено на изучение эффектов и лежащих в основе механизмов действия пеонифлорина на индуцированную блеомицином (BLM) ПФ у мышей. МАТЕРИАЛЫ И МЕТОДЫ: Модель PF была создана на мышах путем интратрахеальной инстилляции BLM. Пеонифлорин (25, 50, 100 мг / кг) и преднизон (6 мг / кг) в качестве положительного контроля вводили перорально в течение 21 дня подряд.Патогистологические изменения оценивали по окрашиванию гематоксилином и эозином и окрашиванию трихромом Массона. Содержание гидроксипролина определяли с помощью наборов. Содержание коллагена I типа, TGF-β1 и IFN-γ определяли с помощью ELISA. Уровни α-SMA, Smad4, Smad7 и фосфорилирование Smad2 / 3 определяли с помощью вестерн-блоттинга. Экспрессию мРНК MMP-1 и TIMP-1 определяли с помощью RT-PCR. Результаты. У мышей, получавших BLM, пеонифлорин (50 мг / кг) значительно продлевал периоды выживания, ослаблял инфильтрацию воспалительных клеток, интерстициальный фиброз и отложение внеклеточного матрикса в тканях легких.Он также снизил содержание гидроксипролина (маркер коллагенов), коллагена I типа и α-SMA (индикатор миофибробластов) в тканях легких мышей. Пеонифлорин подавлял экспрессию TGF-β1, Smad4 и фосфорилирование Smad2 / 3, в то время как повышал экспрессию Smad7 в тканях легких. Кроме того, пэонифлорин увеличивал содержание IFN-γ. Но это лишь незначительно повлияло на экспрессию мРНК MMP-1 и TIMP-1 в тканях легких мышей. ВЫВОДЫ. Пеонифлорин ослабляет ФП, подавляя синтез коллагена I типа, ингибируя активацию пути TGF-β / Smad и увеличивая экспрессию IFN-γ.СН — 1872-7573 UR — https://www.unboundmedicine.com/medline/citation/23973787/paeoniflorin_the_main_active_constituent_of_paeonia_lactiflora_roots_attenuates_bleomycin_induced_pulmonary_fibrosis_in_mice_the_syppressing_type_mice_by_syppressing_type L2 — https://linkinghub.elsevier.com/retrieve/pii/S0378-8741(13)00571-0 БД — ПРЕМЬЕР DP — Unbound Medicine ER —
Лечение защемления сосудов с сосуществующим фиброзом корней крестцового нерва
Цель исследования
Продемонстрировать декомпрессию крестцовых нервов из аберрантных сосудов и фиброзной ткани, расположенной на сплетении.
Дизайн
Видео-презентация двух кейсов.
Окружение
Третичный центр, специализирующийся на современной гинекологической хирургии и нейропельвеологии.
Пациенты или участники
Случай 1: Беременность 43 лет, 1 беременность. У 1 пациентки наблюдались дисменорея, диспареуния и боль в половых органах с дизурией. Гинекологическое обследование выявило глубокий инфильтративный эндометриоз с ректовагинальным узелком и частичной облитерацией кармана Дугласа.В анамнезе она перенесла лапароскопическую операцию по поводу эндометриоза с левой овариэктомией и лечилась внутрисосудистой эмболизацией спиральной спиралью по поводу синдрома застойного таза.
Случай 2: Беременность 41 года, 1 родство 1 пациентка обратилась с жалобой на хроническую боль в области таза и левостороннюю седалищную боль с хронической дизестезией в дерматоме седалищного нерва без двигательного дефицита нижних конечностей. Гинекологическое обследование выявило глубокий инфильтративный эндометриоз и полную облитерацию кармана Дугласа.В анамнезе она перенесла несколько лапароскопических и лапаротомических операций по поводу эндометриоза.
Вмешательства
Роботизированная лапароскопическая декомпрессия крестцового нерва и рассечение тупика с бритьем ректального узла (случай 1) и лапароскопическая декомпрессия крестцового нерва и рассечение тупика (случай 2).
Измерения и основные результаты
Пациенты были обследованы через 3 -е -е и 6 -е -е месяцы после операции. Оба пациента сообщают о значительном уменьшении боли с помощью визуальной аналоговой шкалы.
Заключение
Поскольку пояснично-крестцовое сплетение расположено над крестцовой костью, оно может быть легко сдавлено аномальной структурой (аномальные сосуды, фиброзная ткань, опухоль и т. Д.), Расположенной на сплетении. Глубокий инфильтративный эндометриоз может поражать забрюшинную ткань, вызывая фиброз. Аномальный сосуд, расположенный на крестцовом сплетении, может намного легче захватить корни при сосуществующем фиброзе. Через шесть месяцев наблюдения оценка по визуальной аналоговой шкале для случаев 1 и 2 снизилась с 10 до 4 и с 10 до 3 соответственно.Пациенты по-прежнему находятся под наблюдением.
Рекомендуемые статьи Цитирующие статьи (0)
Авторские права © 2020 Опубликовано Elsevier Inc.
Рекомендуемые статьи
Цитирующие статьи
Управление перифолликулярным фиброзом
При тщательном гистологическом наблюдении биопсий лысой кожи головы миниатюризация концевых волосков является отличительной чертой AGA и часто связана с перифолликулярным фиброзом. Было обнаружено, что миниатюризация волосяных фолликулов связана с отложением так называемого «коллагена или коллагена». соединительнотканные стримеры под фолликулом », а также 2–2.5-кратное увеличение фолликулярной дермальной оболочки, состоящей из плотно упакованных коллагеновых пучков.
Предыдущие сообщения показали, что лечение DHT и тестостероном вызывало повышение постоянной концентрации мРНК альфа-1 (I) -проколлагена в клетках остеобластоподобной остеосаркомы человека и что синтез коллагена у мышей стимулировался андрогеном. По этой причине перифолликулярный фиброз может быть еще одним патогенетическим механизмом AGA, а не простым феноменом, обычно наблюдаемым при AGA.
Тестостерон и ДГТ стимулируют транскрипцию и экспрессию белка гена проколлагена типа I в фолликулярных фиброблатах дермы. Это предполагает, что индукция синтеза проколлагена I типа тестостероном может быть частично ответственна за плотно упакованные пучки коллагена вокруг миниатюрных волосяных фолликулов, что приводит к перифолликулярному фиброзу, наблюдаемому при AGA.
Hibberts NA, Howell AE, Randall VA (1998) Клетки дермального сосочка лысеющего волосяного фолликула содержат более высокие уровни рецепторов андрогенов, чем те, которые получены из не облысевшей кожи головы.J Endocrinol 156: 59–65
Hibino T, Nishiyama T (2004) Роль TGF-beta2 в цикле человеческого волоса. J Dermatol Sci 35: 9–18
Хоффманн Р., Зейдл Т., Ниб М. и др. (2002) Изменения в профилях экспрессии генов в развивающихся В-клетках костного мозга мышей. Genome Res 12: 98–111
Хант Д.П., Моррис П.Н., Стерлинг Дж. И др. (2008) Высокообогащенная ниша клеток-предшественников с нейрональным и глиальным потенциалом внутри дермального сосочка волосяного фолликула взрослой кожи. Стволовые клетки 26: 163–72
Inui S, Fukuzato Y, Nakajima T et al.(2002) Андроген-индуцибельный TGF-бета1 из облысевших клеток дермального сосочка подавляет рост эпителиальных клеток: ключ к пониманию парадоксального воздействия андрогена на рост волос человека. FASEB J 16: 1967–9
Itahana K, Dimri G, Campisi J (2001) Регулирование клеточного старения с помощью p53. Eur J Biochem 268: 2784–91
Jacobs JJ, de Lange T (2004) Важная роль p16INK4a в p53-независимом теломер-управляемом старении. Curr Biol 14: 2302–8
Jahoda CA (2003) Движение клеток в дерме волосяного фолликула — больше, чем улица с двусторонним движением? J Invest Dermatol 121: ix – xi
Jahoda CA, Horne KA, Оливер RF (1984) Индукция роста волос путем имплантации культивированных клеток дермального сосочка.Nature 311: 560–2
Кауфман К.Д. (1996) Метаболизм андрогенов, влияющий на рост волос при андрогенетической алопеции. Дерматол Клин 14: 697–711
Kauser S, Westgate GE, Green MR et al. (2011) Фолликул человеческого волоса и эпидермальные меланоциты демонстрируют разительные различия в профиле старения, в котором участвует каталаза. J Invest Dermatol 131: 979–82
Коли К., Сахаринен Дж., Хюйтиайнен М. и др. (2001) Латентность, активация и связывающие белки TGF-бета. Microsc Res Tech 52: 354–62
Kwack MH, Kim MK, Kim JC et al.(2012) Dickkopf 1 способствует регрессии волосяных фолликулов. J Invest Dermatol 132: 1554–60
Квак М.Х., Сунг Ю.К., Чунг Э.Дж. и др. (2008) Дигидротестостерон-индуцируемый диккопф-1 из облысевших клеток дермального сосочка вызывает апоптоз в фолликулярных кератиноцитах. J Invest Dermatol 128: 262–9
Киприану Н., Исаакс Дж. Т. (1989) Экспрессия трансформирующего фактора роста-бета в вентральной части простаты крысы во время запрограммированной гибели клеток, вызванной кастрацией. Мол эндокринол 3: 1515–22
Lange CA, Gioeli D, Hammes SR et al.(2007) Интеграция быстрых сигнальных событий с действием рецепторов стероидных гормонов при раке груди и простаты. Энн Рев Физиол 69: 171–99
Махер П. (2005) Влияние стресса и старения на метаболизм глутатиона. Aging Res Rev 4: 288–314
Mathieu J, Zhou W, Xing Y et al. (2014) Факторы, индуцируемые гипоксией, играют разные и специфичные для стадии роли во время репрограммирования человеческих клеток до плюрипотентности. Стволовая клетка клетки 14: 592–605
Миранда Б.Х., Тобин Д.Д., Шарп Д.Т. и др.(2010) Промежуточные волосяные фолликулы: новая, более клинически значимая модель для исследований роста волос. Br J Dermatol 163: 287–95
Mohyeldin A, Garzon-Muvdi T, Quinones-Hinojosa A (2010) Кислород в биологии стволовых клеток: критический компонент ниши стволовых клеток. Стволовая клетка клетки 7: 150–6
Норвуд О.Т. (1975) Облысение по мужскому типу: классификация и частота. South Med J 68: 1359–65 Nyholt DR, Gillespie NA, Heath AC et al. (2003) Генетические основы облысения по мужскому типу. J Invest Dermatol 121: 1561–4
Оливер Р.Ф. (1966) Рост усов после удаления дермального сосочка и длины фолликула у крысы с капюшоном.J Embryol Exp Morphol 15: 331–47
Филпотт М.П., Сандерс Д., Вестгейт Г.Е. и др. (1994) Влияние инсулина и инсулиноподобных факторов роста на культивируемые волосяные фолликулы человека: IGF-I в физиологических концентрациях является важным регулятором роста волосяных фолликулов in vitro. J Invest Dermatol 102: 857–61
Pi M, Parrill AL, Quarles LD (2010) GPRC6A опосредует негеномные эффекты стероидов. J Biol Chem 285: 39953–64
Placencio VR, Sharif-Afshar AR, Li X et al. (2008) Передача сигналов стромального трансформирующего фактора роста-бета опосредует ответ простаты на удаление андрогенов за счет паракринной активности Wnt.Cancer Res 68: 4709–18
Randall VA (2007) Гормональная регуляция волосяных фолликулов демонстрирует биологический парадокс. Semin Cell Dev Biol 18: 274–85
Рэндалл В.А., Торнтон М.Дж., Хамада К. и др. (1991) Андрогены и волосяной фолликул. Культивируемые клетки дермального сосочка человека как модельная система. Ann NY Acad Sci 642: 355–75
Севери Г., Синклер Р., Хоппер Дж. Л. и др. (2003) Андрогенетическая алопеция у мужчин в возрасте 40-69 лет: распространенность и факторы риска. Br J Dermatol 149: 1207–13
Шин Х., Ю Х.Г., Инуи С. и др.(2013) Индукция трансформирующего фактора роста бета 1 андрогеном опосредуется активными формами кислорода в клетках дермального сосочка волосяного фолликула. BMB Rep 46: 460–4
Su LH, Chen TH (2010) Ассоциация андрогенетической алопеции с метаболическим синдромом у мужчин: исследование на уровне сообщества.

