Симптомы повреждения артерии: Повреждение сосудов — причины, симптомы, диагностика и лечение
Повреждение сосудов — причины, симптомы, диагностика и лечение
Повреждение сосудов – нарушение целостности артерий и вен в результате травматического воздействия. Может наблюдаться как при открытой, так и при закрытой травме, сопровождается наружным или внутренним кровотечением, возможно нарушение кровоснабжения нижележащего сегмента. Повреждение крупных сосудов является тяжелой травмой и представляет опасность для жизни пациента. Диагноз выставляется на основании клинических признаков, к числу которых относится наличие раны или закрытого повреждения, кровотечение или гематома, ослабление или отсутствие пульса на периферических артериях. Лечение хирургическое.
Общие сведения
Повреждение сосудов – достаточно распространенная травма, как в военное, так и в мирное время. Наибольшее количество повреждений приходится на сосуды нижних конечностей. Второе место по распространенности занимают повреждения сосудов верхних конечностей, третье – сосудов шеи. В последние десятилетия специалисты в области травматологии отмечают изменение характера таких травм за счет увеличения количества высокоэнергетических травматических воздействий. В связи с этим ранения и закрытые повреждения сосудов чаще выявляются в составе множественной и сочетанной травмы, что усложняет лечение и утяжеляет прогноз.
В последние десятилетия специалисты в области травматологии отмечают изменение характера таких травм за счет увеличения количества высокоэнергетических травматических воздействий. В связи с этим ранения и закрытые повреждения сосудов чаще выявляются в составе множественной и сочетанной травмы, что усложняет лечение и утяжеляет прогноз.
Открытые и закрытые повреждения сосудов могут сочетаться с переломами костей туловища и конечностей, тупой травмой живота, повреждениями почек, ЧМТ и повреждениями грудной клетки. Наряду с этим нередко наблюдаются изолированные травмы с тяжелыми разрушениями конечностей: многооскольчатыми переломами, раздавливанием и размозжением мягких тканей, обширными рваными ранами и т. д. И, хотя возможности современной реконструктивной ангиохирургии во многих случаях позволяют восстановить целостность сосудов даже при тяжелых повреждениях, тактика лечения и прогноз в таких случаях зависят не только от возможности восстановления артерий и вен, но и от жизнеспособности тканей травмированной конечности.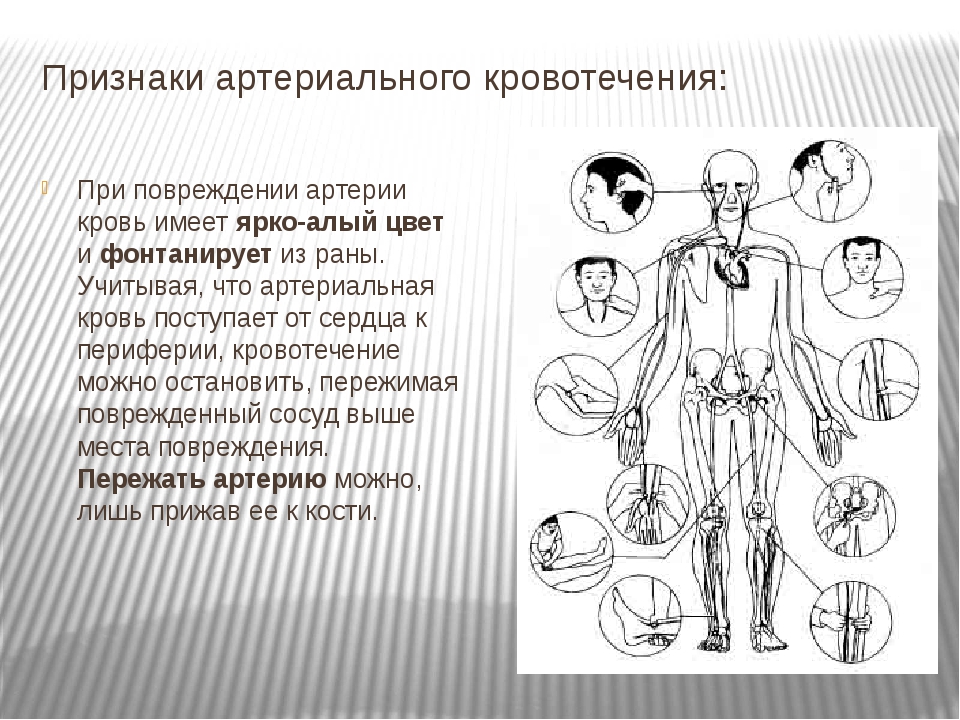
Повреждение сосудов
Открытые повреждения
Открытые повреждения сосудов отличаются большим разнообразием и обычно возникают в результате огнестрельных ранений, резаных, колото-резаных и колотых ран. Реже причиной становятся рваные и рвано-ушибленные раны. С учетом вида травмированного сосуда выделяют ранения артерий и вен, с учетом характера повреждения – полные поперечные и неполные поперечные разрывы, одиночные сквозные, боковые (касательные) и фенестрирующие повреждения. Фенестрирующие повреждения возникают в результате ранения дробью или мелкими осколками и характеризуются наличием «окна» или «дырки» в стенке сосуда при сохранении кровотока.
Как правило, открытые повреждения сосудов сопровождаются наружным кровотечением. Однако иногда дефект в стенке поврежденной артерии или вены «закупоривается» тромбом или сдавливается окружающими тканями, поэтому кровотечение может отсутствовать. Возможно также излитие крови не наружу, а в мягкие ткани с формированием напряженной гематомы. При ранении крупных сосудов в большинстве случаев наблюдаются кровопотеря и гиповолемический шок.
При ранении крупных сосудов в большинстве случаев наблюдаются кровопотеря и гиповолемический шок.
Местные симптомы ранений сосудов зависят от диаметра травмированной артерии или вены, характера повреждения сосудистой стенки, анатомических особенностей зоны травмы, объема разрушения мягких тканей, сопутствующего повреждения костей и нервов, общего состояния пациента и т. д. При повреждении вен кровь темно-вишневая, изливается ровной струей, при нарушении целостности крупных стволов возможна пульсация в такт дыханию. Возможно образование нарастающей не пульсирующей гематомы в окружающих мягких тканях. Пульс на периферических артериях сохранен, цвет кожи в дистальных отделах не изменен, нарушения функции конечности обусловлены характером и тяжестью травмы.
К числу признаков, позволяющих заподозрить повреждение артерии, относятся рана в проекции сосуда, наружное кровотечение алой пульсирующей струей или нарастающая пульсирующая гематома, ослабление или отсутствие пульсации на артериях ниже уровня повреждения. Важнейшим симптомом повреждения магистральных артерий является нарастающая ишемия дистальных отделов конечности. О недостаточности местного кровообращения свидетельствуют парестезии, побледнение, а в последующем – синюшность и мраморность кожных покровов, похолодание и ишемические боли, которые не уменьшаются при иммобилизации и не усиливаются при пальпации. Перечисленные проявления сопровождаются нарастающей ригидностью мышц. Затрудняются сначала активные, а затем и пассивные движения, при глубоких расстройствах кровообращения возникают мышечные контрактуры.
Важнейшим симптомом повреждения магистральных артерий является нарастающая ишемия дистальных отделов конечности. О недостаточности местного кровообращения свидетельствуют парестезии, побледнение, а в последующем – синюшность и мраморность кожных покровов, похолодание и ишемические боли, которые не уменьшаются при иммобилизации и не усиливаются при пальпации. Перечисленные проявления сопровождаются нарастающей ригидностью мышц. Затрудняются сначала активные, а затем и пассивные движения, при глубоких расстройствах кровообращения возникают мышечные контрактуры.
Закрытые повреждения
Закрытые повреждения сосудов могут возникать вследствие окклюзирующих или контузионных повреждений. Окклюзирующие повреждения обычно выявляются при вывихах и переломах костей, их причиной становится сдавление или ушиб артерий сместившейся костью или костным фрагментом. При этом нередко наблюдается мгновенное удлинение (насильственное чрезмерное растяжение) сосуда, способствующее усугублению травмы. В первую очередь страдает нежная интима – внутренняя оболочка сосуда. Если воздействие достаточно интенсивное, нарушается целостность средней оболочки артерии. При этом наружная оболочка благодаря своей высокой прочности может остаться неповрежденной. Разрывы внутренней и средней оболочки сосудов называются контузией.
В первую очередь страдает нежная интима – внутренняя оболочка сосуда. Если воздействие достаточно интенсивное, нарушается целостность средней оболочки артерии. При этом наружная оболочка благодаря своей высокой прочности может остаться неповрежденной. Разрывы внутренней и средней оболочки сосудов называются контузией.
Выделяют три степени контузионных повреждений сосудов. Первая – в интиме есть отдельные трещины. Вторая – имеются циркулярные повреждения интимы. Третья – повреждена не только внутренняя, но и средняя оболочка артерии. При повреждениях второй и третьей степени из-за тока крови интима отслаивается и закупоривает просвет сосуда, вызывая внутрисосудистый тромбоз. При повреждении всех оболочек артерии формируется пульсирующая гематома, из которой в последующем, как правило, образуется травматическая аневризма.
В случаях одновременного разрыва артерии и вены возникает артериовенозный свищ – кровь из артерии сразу сбрасывается в вену, что может приводить не только к нарушению кровоснабжения дистальных отделов конечности, но и к развитию общих расстройств кровообращения. Фактором, способствующим усугублению ишемии нижележащих отделов конечности, является кровопотеря и сопутствующие повреждения окружающих мягких тканей. При отсутствии неповрежденных коллатеральных артерий в течение 3-4 часов развиваются необратимые нарушения жизнедеятельности тканей, возникает так называемая гемодинамическая ампутация конечности.
Фактором, способствующим усугублению ишемии нижележащих отделов конечности, является кровопотеря и сопутствующие повреждения окружающих мягких тканей. При отсутствии неповрежденных коллатеральных артерий в течение 3-4 часов развиваются необратимые нарушения жизнедеятельности тканей, возникает так называемая гемодинамическая ампутация конечности.
Клиническими признаками закрытого повреждения сосудов являются нарушения движений и чувствительности дистальных отделов конечности, а также резкая боль, которая не уменьшается после вправления отломков, иммобилизации и использования анальгетиков. Кроме того, наблюдается отсутствие периферической пульсации и цианоз или резкая бледность кожных покровов. При нарушении целостности всех слоев сосудистой стенки в проекции травмы образуется обширная гематома.
Диагностика и лечение
Диагноз выставляется на основании внешних признаков, при необходимости выполняется ангиография. Тактика лечения зависит от состояния дистальных отделов конечности, поэтому большое внимание уделяется оценке жизнеспособности тканей.
Часть мышечных волокон при глубокой ишемии остается жизнеспособной, поэтому в некоторых случаях врачи отказываются от ампутации и пытаются восстановить кровоснабжение конечности. Однако вероятность благополучного исхода при таких повреждениях сомнительна и, даже если конечность удается сохранить, она остается неполноценной, то есть, превращается в аналог биологического протеза.
В процессе лечения перед травматологом или сосудистым хирургом стоят три задачи, которые следует решать в определенной последовательности. Приоритетом является спасение жизни пациента, то есть, остановка кровотечения и борьба с последствиями кровопотери. С этой целью проводятся противошоковые мероприятия, осуществляются переливания крови и кровезамещающей жидкости.
Противошоковые мероприятия способствуют улучшению гемодинамики, следовательно, помогают сохранить жизнеспособность тканей. Наряду с этим, обязательным условием сохранения конечности является реконструктивная операция. В зависимости от характера повреждения сосуда возможен либо обычный сосудистый шов, либо восстановление сосуда с использованием специального протеза. В послеоперационном периоде проводятся мероприятия по нормализации деятельности всех органов и систем, назначаются антибиотики, обезболивающие препараты, ЛФК и физиотерапия.
Прогноз при открытых и закрытых повреждениях артерий и вен зависит от общего состояния пострадавшего, наличия или отсутствия других травм, локализации пораженного сосуда, особенностей коллатерального кровообращения, степени разрушения окружающих мягких тканей и других факторов. Важнейшее значение имеет временной фактор.
Заболевания сонных артерий
Сонные артерии
Заболевания сонных артерий возникают, когда формирующиеся атеросклеротические бляшки частично или полностью перекрывают их просвет. Сонные артерии это парные сосуды, которые осуществляют кровоснабжение головы и головного мозга.
Сонные артерии это парные сосуды, которые располагаются в области шеи, и обеспечивает приток крови к мозгу.
Сужение просвета сонных артерий за счет формирования и нарастание атеросклеротических бляшек уменьшает объем поступающей крови к головному мозгу и увеличивает риск развития инсульта.
Симптомы
Поскольку атеросклеротическое поражение сонных артерий развивается медленно и часто носит бессимптомный характер, первыми клиническими проявлениями этого заболевания могут стать инсульт (острое нарушение мозгового кровоснабжения — ОНМК) или транзиторная ишемическая атака (ТИА), иногда называемая микроинсультом.
Лечение атеросклеротического поражения сонных артерий обычно включает в себя комплекс мероприятий, таких как изменение образа жизни, медикаментозную терапию и в некоторых случаях хирургическое лечение (открытое оперативное вмешательство или стентирование).
На ранних стадиях атеросклеротическое поражение сонных артерий, как правило, является бессимптомным. Вы и ваш лечащий врач можете не знать о существовании у вас сужения сонной артерии до тех пор, пока не разовьется острое нарушение мозгового кровоснабжения как первое и очень грозное проявление заболевания.
Клинические проявления инсульта или транзиторной ишемической атаки могут включать:
- внезапное чувство онемения или слабость в области лица или конечностей, чаще на одной стороне.
- нарушение речи или ее понимания
- внезапное нарушение зрения одного или обоих глаз
- головокружение или потеря равновесия
- внезапная беспричинная сильная головная боль
При наличии у вас факторов риска развития атеросклеротического поражения сонных артерий необходимо проконсультироваться с врачом. Ваш лечащий врач может назначить обследование с целью уточнения состояния этих сосудов. Даже при отсутствии у вас клинических проявления заболевания, ваш врач может порекомендовать ряд мероприятий, направленных на уменьшение выраженности факторов риска и снижение вероятность развития инсульта.
Ваш лечащий врач может назначить обследование с целью уточнения состояния этих сосудов. Даже при отсутствии у вас клинических проявления заболевания, ваш врач может порекомендовать ряд мероприятий, направленных на уменьшение выраженности факторов риска и снижение вероятность развития инсульта.
Срочное обращение за медицинской помощью необходимо, когда у вас возникают симптомы транзиторной ишемической атаки или инсульта.
Даже если продолжительность симптомов небольшая , как правило менее часа, но возможно и дольше, сразу же сообщите о них своему врачу. Появление этих симптомов, свидетельствует о том, что вы перенесли транзиторную ишемическую атаку – кратковременное уменьшение притока крови к головному мозгу. Наличие транзиторных ишемических атак является важнейшим признаком того, что у вас имеется высокий риск развития инсульта, если во время не принять профилактические меры.
Своевременный визит к врачу увеличивает ваши шансы на то, что атеросклеротическое поражение сонных артерий будет выявлено и устранено до того, как разовьется острое нарушение мозгового кровоснабжения.
Транзиторная ишемическая атака также может свидетельствовать о уменьшении кровотока и по другим кровеносным сосудам головного мозга. Для уточнения диагноза ваш лечащий врач назначит необходимое обследование.
Убедитесь в том, что Ваши родственники и близкие друзья знают о клинических проявлениях инсульта и о том, что в случае их возникновения очень важно действовать быстро.
Причины
С течение времени стенки сонных артерий могут становиться утолщенными, их просвет сужаться за счет формирования атеросклеротических бляшек, что приводит к уменьшению объема поступающей по ним крови. Атеросклеротические бляшки состоят из скоплений холестерола, кальция, элементов фиброзной ткани и остатков клеток , которые проникают в стенку артерии через микроскопические повреждения внутренней оболочки и формируют атеросклеротическую бляшку в области которой может образоваться кровяной сгусток (тромб).
Нормальные, здоровые сонные артерии, как и другие нормальные артерии , являются мягкими и гибкими и обеспечивают свободное прохождение потока крови. Если вы приложите палец с любой стороны от «Адамова яблока» вы можете ощутить пульсацию сонных артерий. Сонные артерии обеспечивают поступление кислорода и питательных веществ к коре и другим жизненно важным структурам головного мозга.
Если вы приложите палец с любой стороны от «Адамова яблока» вы можете ощутить пульсацию сонных артерий. Сонные артерии обеспечивают поступление кислорода и питательных веществ к коре и другим жизненно важным структурам головного мозга.
Факторы риска
Факторами, воздействующими на артерии и повышающими риск повреждения, формирования бляшек и развитие заболеваний, являются:
- Повышенное артериальное давление. Повышенное артериальное давление является важнейшим фактором развития атеросклеротического поражения сонных артерий. Воздействие высокого давления на стенку артерии ослабляет ее и делает более подверженной повреждениям.
- Курение. Никотин раздражает внутреннюю оболочку сосудов, а также способствует учащению ритма сердца и повышению артериального давления.
- Возраст. С возрастом стенка артерий теряет эластичность и приобретает большую подверженность к повреждениям.
- Нарушение соотношения липидов крови.
 Повышенный уровень холестерина липопротеинов низкой плотности («плохого холестерина»)и высокий уровень триглицеридов способствует формированию атеросклеротических бляшек.
Повышенный уровень холестерина липопротеинов низкой плотности («плохого холестерина»)и высокий уровень триглицеридов способствует формированию атеросклеротических бляшек. - Сахарный диабет. Диабет не только воздействует на способность контролировать уровень сахара крови, но и на липидный обмен, повышая риск артериальной гипертензии и развития атеросклероза.
- Ожирение. Избыток массы тела увеличивает риск возникновения артериальной гипертензии, атеросклероза и сахарного диабета.
- Наследственность. Наличие у родственников атеросклероза или ишемической болезни сердца значительно увеличивает риск формирования атеросклеротического поражения.
- Малоподвижный образ жизни. Недостаток физической активности вносит свой вклад в развитие артериальной гипертензии, ожирения и сахарного диабета.
Зачастую, перечисленные факторы риска присутствуют в совокупности, тем самым повышая степень риска.
Осложнения
Атеросклеротическая бляшка
Наиболее опасным осложнением атеросклеротического поражения сонных артерий является инсульт. Существуют различные механизмы увеличения риска инсульта:
- Уменьшение кровотока. Сонные артерии могут настолько сузиться за счет атеросклеротического поражения, что будут неспособны обеспечить адекватное кровоснабжение головного мозга.
- Разрыв атеросклеротической бляшки.
- Образование тромбов. Поверхность некоторых атеросклеротических бляшек может вскрываться с образованием неровной изъязвленной поверхности. Когда это происходит, реакцией организма является привлечение к месту разрыва тромбоцитов и формирование кровяного сгустка (тромба).
 Крупные тромбы могут частично или полностью перекрывать просвет артерии, тем самым, препятствуя кровотоку и вызывая инсульт.
Крупные тромбы могут частично или полностью перекрывать просвет артерии, тем самым, препятствуя кровотоку и вызывая инсульт.
Последствиями инсульта могут стать формирование очага повреждения головного мозга и нарушение функций органов, в частности параличи конечностей. В тяжелых случаях инсульт может приводить к летальному исходу.
Инсульт или транзиторная ишемическая атака часто являются первыми проявлениями атеросклеротического поражения сонных артерий и относятся к неотложным медицинским состояниям. Если у вас или у ваших близких появились симптомы нарушения кровоснабжения головного мозга, необходимо срочно обратиться за медицинской помощью. Не пытайтесь добраться до стационара самостоятельно.
Симптомы, вызывающие опасение:
- внезапное чувство онемения или слабость в области лица или конечностей, чаще на одной стороне;
- нарушение речи или ее понимания;
- внезапное нарушение зрения одного или обоих глаз;
- головокружение или потеря равновесия;
- внезапная беспричинная сильная головная боль;
Методы диагностики
После сбора анамнеза, выявления факторов риска и характерных симптомов, врач может провести дополнительное обследование, включающее в себя:
- Физикальный осмотр, во время которого врач при помощи фонендоскопа может выявить шум над сонной артерией в области шеи, который свидетельствует о сужении артерии.
 Врач также может провести неврологический осмотр с оценкой вашего физического и ментального статуса, например, оценит силу в конечностях, возможности запоминания устной речи.
Врач также может провести неврологический осмотр с оценкой вашего физического и ментального статуса, например, оценит силу в конечностях, возможности запоминания устной речи. - Ультразвуковое исследование. Наиболее частым неинвазивным методом исследования, позволяющим оценить состояние сонных артерий, является допплеровское ультразвуковое исследование. Это вариант обычного ультразвукового исследования, оценивающий скорость кровотока, давление и способный выявить сужение просвета артерий за счет изменения этих показателей.
- Компьютерная ангиография. Это процедура выполняется с использованием контрастного препарата с целью выделения артериальных сосудов. Препарат вводится внутривенно. Когда он достигает ваших сонных артерий, производится серия снимков области шеи и головного мозга при помощи рентгеновских лучей в разных проекциях.
- Магнитно-резонансная томография. Подобно компьютерной томографии, при помощи этого метода, возможно, визуализировать ткань головного мозга и выявить очаги поражения головного мозга на ранних стадиях или наличие другой патологии.

- Ангиография. Является более «чувствительный» инвазимным методом исследования. Однако, в настоящее время применяется все реже в связи с существующим риском возникновения инсульта во время процедуры. Во время исследования выполняются рентгеновские снимки артериальных сосудов, кровоснабжающих головной мозг, с предварительным внутриартериальным введением контрастного препарата.
Лечение
Целью лечения атеросклеротического поражения сонных артерий является профилактика развития инсульта. Выбор метода лечения зависит от степени сужения просвета артерии.
Незначительно и умеренно выраженные сужения.
При наличии умеренно выраженных сужений сонных артерий для профилактики инсульта может быть достаточно следующих рекомендаций:
- Изменение образа жизни. Изменения в пользу здорового образа жизни могут помочь уменьшить повреждение стенки сонных артерий и замедлить прогрессирование атеросклеротического процесса. Такие изменения включают отказ от курения, снижение массы тела, здоровое питание, уменьшение употребления поваренной соли и регулярные физические нагрузки.

- Лечение сопутствующих хронических заболеваний. Одновременно необходимо проводить лечение таких сопутствующих заболеваний как артериальная гипертензия, ожирение и сахарный диабет.
- Назначение лекарственных препаратов. Врач может назначить вам ежедневный прием аспирина или других дезагрегантных препаратов с целью уменьшения риска тромбообразования. Также может быть рекомендована терапия, направленная на коррекцию артериального давления ( ингибиторы АПФ, бета-блокаторы ) и коррекцию липидного профиля – прием статинов.
Выраженные сужения сонных артерий.
Если имеется выраженное сужение просвета сонной артерии, а особенно в сочетании с уже перенесенной транзиторной ишемической атакой или инсультом в зоне кровоснабжения данной артерии, показано хирургическое лечение , направленное на устранение этого сужения.
Существует два способа хирургической коррекции:
Каротидная эндартерэктомия
- Открытое оперативное вмешательство – каротидная эндартерэктомия.
 Этот метод лечения является наиболее распространенным при выраженных сужениях сонных артерий. Вмешательство выполняется под общим обезболиванием и заключается в удалении атеросклеротической бляшки через небольшой разрез сонной артерии. В завершении сонная артерия либо просто ушивается, либо, производится пластика при помощи синтетической заплаты. Многочисленные исследования показали, что выполнение хирургического вмешательства значительно уменьшает риск возникновения инсульта.
Этот метод лечения является наиболее распространенным при выраженных сужениях сонных артерий. Вмешательство выполняется под общим обезболиванием и заключается в удалении атеросклеротической бляшки через небольшой разрез сонной артерии. В завершении сонная артерия либо просто ушивается, либо, производится пластика при помощи синтетической заплаты. Многочисленные исследования показали, что выполнение хирургического вмешательства значительно уменьшает риск возникновения инсульта. - Эндоваскулярные методы лечения — ангиопластика и стентирование сонных артерий.
Данные методы лечения рекомендуется выполнять при невозможности произвести открытое вмешательство из-за локализации и протяженности сужения, а также у лиц с тяжелой сопутствующей патологией и высоким риском осложнений во время операции. Операция заключается во введении в просвет артерии специального баллона и устранения при помощи него сужения просвета, затем в эту зону устанавливается небольшой металлический каркас (стент), который будет поддерживать диаметр просвета артерии.
 Процедура выполняется под местной анестезией.
Процедура выполняется под местной анестезией.
Баллонная ангиопластика
Установка стента
Повреждение сосудов: классификация и первая помощь при травмах артерий или вен
Причины травмы сосудов могут быть разные: автомобильные аварии, повреждения действующими механизмами на производстве и в быту, травмирование острыми предметами, огнестрельные раны, разрывы сосудов при вывихах и переломах костей. Различают открытые и закрытые повреждения сосудов.
Открытые повреждения сосудов сопровождаются нарушением кожных покровов, при этом происходит полный разрыв кровеносного сосуда или частичное повреждение стенок сосудов (артерий и вен). Обычно таким травмам сопутствуют заметные наружные кровотечения.
Закрытые травмы кровеносных сосудов происходят под воздействием тупых предметов, при падении или ушибах, целостность кожных покровов при этом не нарушается. Внутренние кровотечения при закрытых травмах гораздо сложнее диагностировать, соответственно, выше риск недооценить угрозу жизни человека. Диагностика внутреннего кровотечения происходит на основании клинических признаков повреждения сосудов: увеличивающаяся гематома (при неполном разрыве артерий — пульсирующая), бледность кожных покровов, учащение пульса, снижение давления, боли. При интенсивном кровотечении у потерпевшего может развиться геморрагический шок — острое, требующее неотложной помощи состояние, вызванное нарушением гемодинамики, вплоть до потери сознания, резкого падения давления, тахикардии, остановки сердца.
Внутренние кровотечения при закрытых травмах гораздо сложнее диагностировать, соответственно, выше риск недооценить угрозу жизни человека. Диагностика внутреннего кровотечения происходит на основании клинических признаков повреждения сосудов: увеличивающаяся гематома (при неполном разрыве артерий — пульсирующая), бледность кожных покровов, учащение пульса, снижение давления, боли. При интенсивном кровотечении у потерпевшего может развиться геморрагический шок — острое, требующее неотложной помощи состояние, вызванное нарушением гемодинамики, вплоть до потери сознания, резкого падения давления, тахикардии, остановки сердца.
Осложнения травмы сосудов, особенно крупных магистральных артерий и вен, могут проявиться в виде ложных аневризм (чрезмерное растяжение и выпячивание стенки сосуда), посттравматических венозно-артериальных свищей. Возможно инфицирование гематом, развитие ишемической гангрены конечностей (гибель тканей из-за недостаточности кровообращения), полиорганная недостаточность (нарушение работы нескольких органов) и другие последствия. Эти патологии возникают из-за нарушения питания тканей, недостатка кислорода, изменения обмена веществ.
Эти патологии возникают из-за нарушения питания тканей, недостатка кислорода, изменения обмена веществ.
Повреждения сосудов относятся к категории травм, при которых жизненно важно правильно оказать первую медицинскую помощь, оперативно вызвать врачебную бригаду и доставить потерпевшего в больницу. Это снизит угрозу ампутаций, поможет сохранить работоспособность поврежденных частей тела, сократит период реабилитации, во многих случаях — спасет жизнь. Важно не допустить ошибки при оказании первой помощи.
Как действовать, если вы столкнулись с травмой сосудов и кровотечением
Главная задача при любой ране с кровотечением — остановить или уменьшить потерю крови. Необходимо крепко прижать рану имеющимся под рукой мягким чистым предметом. Для этих целей можно использовать одежду, носовой платок, салфетку — они помогут равномерно распределить давление на поврежденные ткани. Если рана глубокая, полость заполняется тканевым тампоном (это может быть свернутый бинт, сложенный обрывок одежды), который интенсивно зажимается рукой.
При всех манипуляциях и во время ожидания медицинской помощи пострадавший должен находиться в горизонтальном положении. При повреждении конечностей, их лучше приподнять выше уровня сердца или максимально согнуть в суставе. Когда кровотечение ослабнет, можно наложить давящую повязку. При этом бинт или полосу ткани накладывают поверх тампонирующего материала, постепенно перенося давление с фиксирующей руки на повязку. Если ожидается быстрое прибытие медиков, лучше самостоятельно давящую повязку не накладывать.
Необходимо также до приезда врачей попытаться оценить вид кровотечения по следующим признакам: кровь алая и бьет струей — повреждена артерия, темная кровь, медленно вытекает — венозное кровотечение.
При венозном кровотечение можно наложить повязку на центр раны — и остановить кровь. В этом случае нет необходимости накладывать жгут. Более того, если при венозном кровотечении наложить артериальный жгут — выше раны, то венозное кровотечение усилится. Можно нанести вред потерпевшему.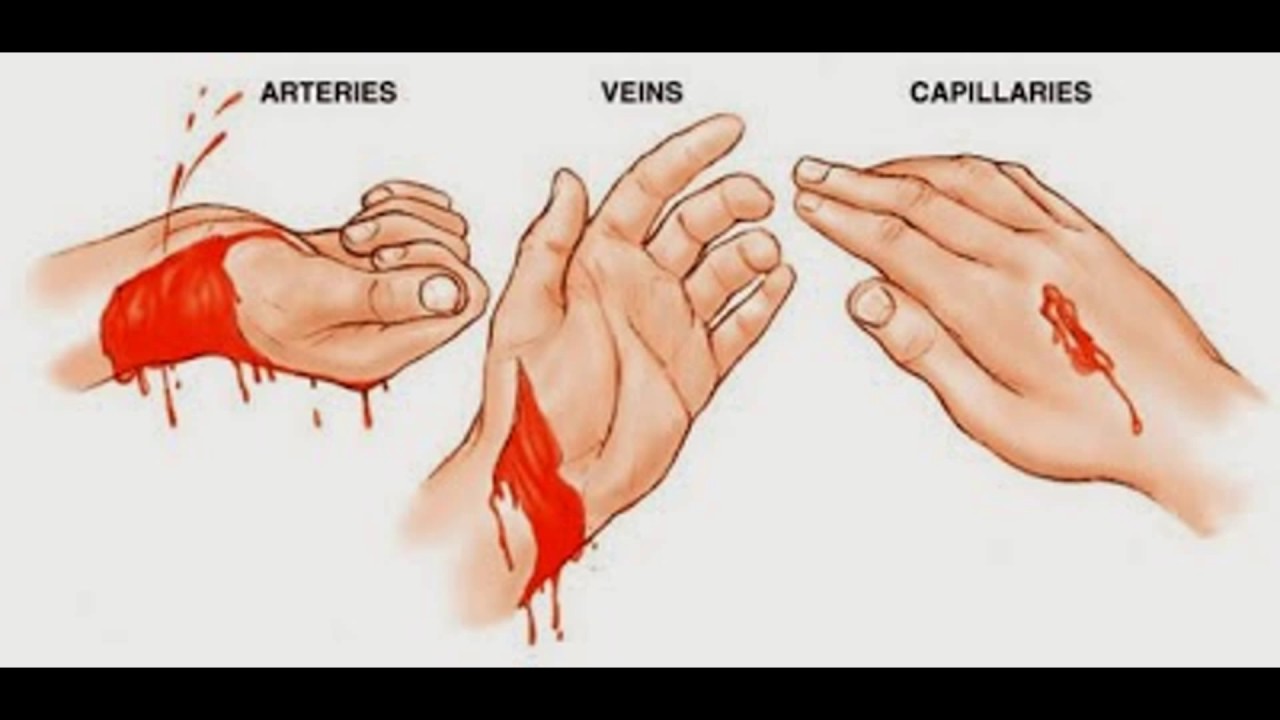 Поэтому если от давящей повязки есть эффект, дополнительно кровоостанавливающий жгут накладывать не нужно.
Поэтому если от давящей повязки есть эффект, дополнительно кровоостанавливающий жгут накладывать не нужно.
Если кровотечение сильное, явно артериальное, необходимо выше места кровотечения передавить кровоток в поврежденной конечности с помощью жгута — это может спасти человеку жизнь.
Артериальный жгут обязан быть в аптечке в любом транспорте, медучреждении. Жгут накладывают, предварительно проложив под него одежду или ткань, затягивают очень сильно и обязательно фиксируют время наложения жгута. Во время холодной погоды наложение жгута не должно длиться более 1 часа, при теплой погоде — до 2 часов. Потом следует или добраться до больницы, или изменить положение жгута, сняв и наложив его снова. Нельзя использовать для изготовления жгута тонкие материалы, которые могут повредить кожу.
В стационаре врач оценивает клинические признаки повреждения сосудов, наличие угрозы жизни пострадавшего. Оценивается также возможность сохранения жизнеспособности и восстановления функций поврежденной конечности или органа. Сосудистый хирург может восстановить проходимость артерий и вен, сшить сухожилия и нервы, которые пострадали.
Сосудистый хирург может восстановить проходимость артерий и вен, сшить сухожилия и нервы, которые пострадали.
Возможность восстановления зависит от многих факторов: размер повреждений, время после травмы, состояние потерпевшего и многое другое. При значительных повреждениях, связанных с нарушением питания всей конечности, и отсутствии экстренной помощи вероятность вернуть жизнь поврежденной конечности снижается. Например, при ампутации пальца — у врача есть около суток на реплантацию. При травмах плеча или предплечья — уже 6 часов, в течение которых можно рассчитывать на восстановление жизнеспособности.
Для диагностики внутренних кровотечений используется компьютерная томография и лапароскопия. При проведении лапароскопии можно одновременно оказать оперативную помощь и остановить внутреннее кровотечение.
Вопрос — ответ
Можно ли визуально оценить уровень наружной кровопотери?
Ориентировочно пятно крови на полу или одежде размером 30 х 30 см — соответствует 100 мл потерянной крови; 1 кв.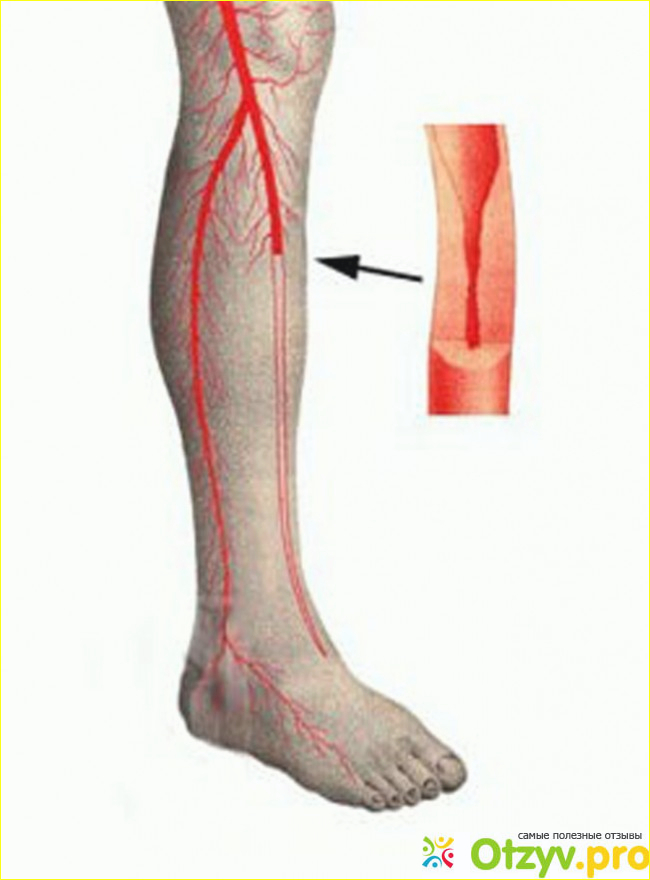 м поверхности — приблизительно 1 л вытекшей крови.
м поверхности — приблизительно 1 л вытекшей крови.
Можно ли пострадавшему давать пить при оказании помощи?
Нежелательно. Лучше просто смачивать губы. Выпитая жидкость может препятствовать дальнейшему проведению наркоза. Необходимо дождаться врачей скорой помощи — при необходимости они наладят поставку жидкости в организм через вену.
Можно ли собрать кровь и перелить обратно больному?
Этот метод носит название реинфузия аутокрови. Его применение возможно в плановом порядке, в условиях стационара, с использованием специального оборудования и реагентов. Обычно кровь, которую теряет пострадавший после травмы, успевает свернуться и непригодна для переливания.
Можно ли осуществить прямое переливание крови пострадавшему?
Прямое переливание крови в Украине запрещено. Кровь должна быть протестирована на инфекции, и только после этого она может поступить в организм больного.
Можно ли обработать рану спиртсодержащими антисептиками?
Нежелательно заливать рану спиртом — это причиняет дополнительную боль и может ухудшить состояние потерпевшего.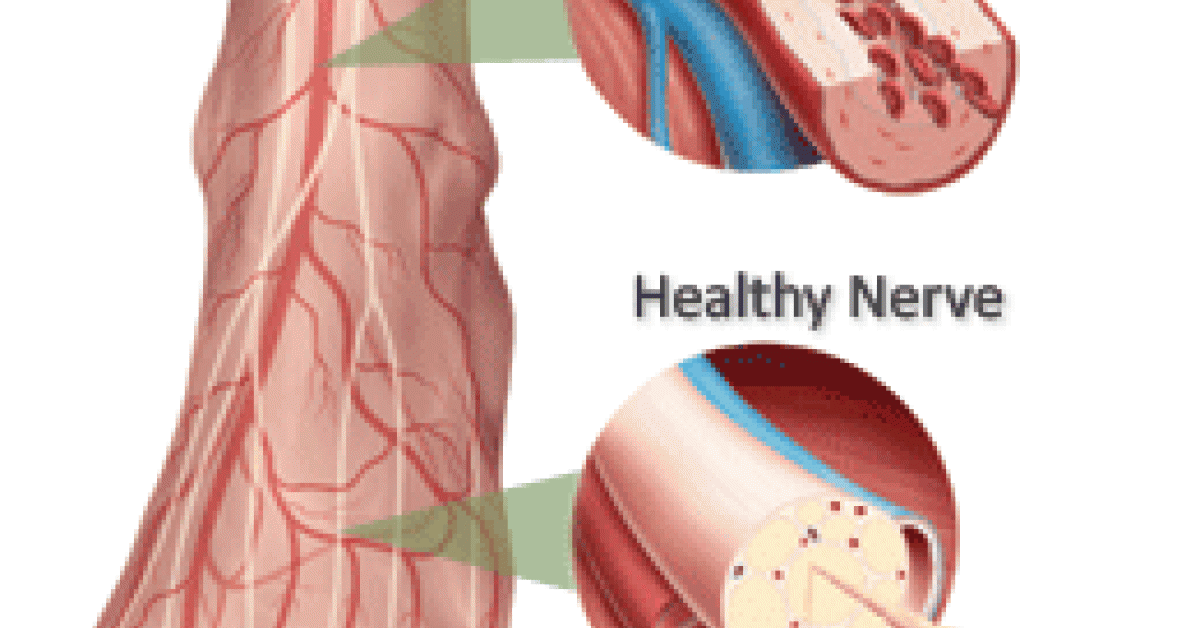 Можно очистить рану от явных загрязнений, от кусков одежды. Если в ране остался ранящий предмет, лучше не пытаться удалять его самостоятельно — это может вызвать усиление кровотечения. Кроме того, расположение предмета в ране поможет хирургу четко сориентироваться в характере повреждений.
Можно очистить рану от явных загрязнений, от кусков одежды. Если в ране остался ранящий предмет, лучше не пытаться удалять его самостоятельно — это может вызвать усиление кровотечения. Кроме того, расположение предмета в ране поможет хирургу четко сориентироваться в характере повреждений.
Поражение сосудов шеи
Поражение сосудов шеи (прецеребральных отделов артерий головного мозга).
Брахиоцефальные артерии (БЦА) – это магистральные сосуды организма. К БЦА относятся:
- брахиоцефальный ствол,
- общая сонная артерия (делится на внутреннюю и наружную артерии)
- подключичные артерии,
- позвоночные артерии.
Анатомия позвоночных артерий часто индивидуальна. Внутренние сонные и позвоночные артерии (они же прецеребральные отделы артерий головного мозга) после проникновения внутрь черепа образуют Виллизиев круг. Это анатомическое образование призвано обеспечивать равномерное распределение крови по всем отделам головного мозга.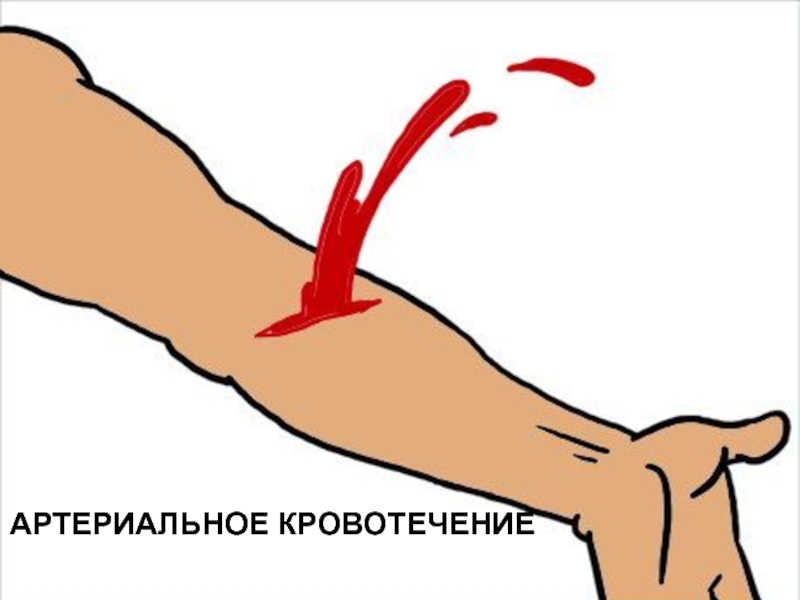
Проблема в том, что анатомия Вилизиевого круга также вариабельна и более чем у 20% людей европейской популяции круг разомкнут. При такой особенности анатомии достаточно прекращения кровообращения даже в одной из артерий для развития инсульта (гибель ткани мозга).
Однако, подавляющее число ишемических инсультов эмбологенного характера. Это означает, что причиной недуга является засорение артерий мозга материальными объектами.
Эмболию могут вызывать тромбы из полостей сердца (при его патологии), но чаще всего – это фрагменты распадающихся атеросклеротических бляшек из сонных артерий и зоны деления общей сонной артерии на внутреннюю и наружную (зона бифуркации). Именно зона бифуркации — типичное место для возникновения и развития атеросклеротической бляшки.
Бляшки, в свою очередь подразделяются на различные типы и классифицируются по степени сужения сосуда. Наиболее опасными являются эмбологенный бляшки – то есть те, которые в любой момент могут разрушиться и все их содержимое мгновенно закупорит множество артерий головного мозга и вызовет инсульт.
Предвестниками инсульта могут быть:
- головная боль;
- головокружение;
- онемение половины тела;
- нарушения зрения;
- затруднения при формулировании мыслей.
- нарушение артикуляции
- нарушения в тонких функциях кистей рук (например, при письме)
- затруднения при ходьбе и т.д.
Очень часто инсульт возникает без каких либо предвестников. Именно поэтому ультразвуковая диагностика артерий шеи (триплексное, дуплексное сканирование) совершенно необходимая процедура для мужчин и женщин после 40-50 лет.
Ангиохирурги СПБ больницы РАН используют различные методы лечения атеросклероза БЦС, в случае сонных артерий – это прежде всего каротидная эндартерэктомия — радикальное оперативное лечение, позволяющее извлечь бляшку и восстановить целостность стенки сосуда.
Операция проводится по методике обеспечивающей максимально возможную степень защиты головного мозга и микрохирургическое восстановление артерии.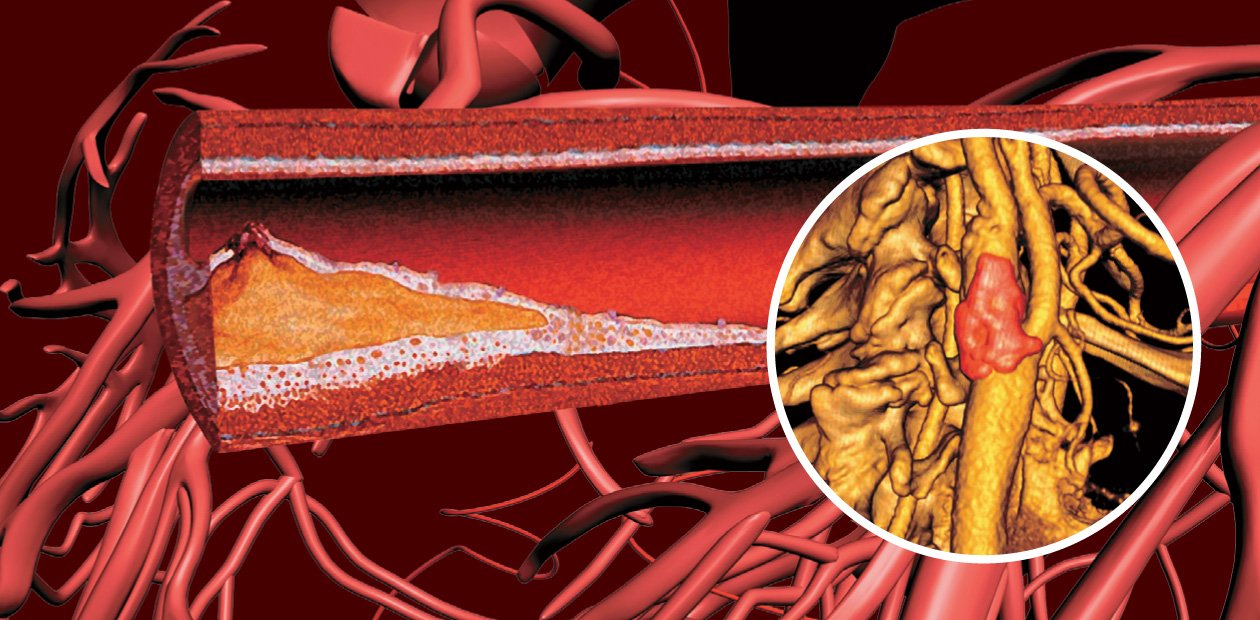
На сегодняшний день каротидная эндартерэктомия дает наиболее стойкие положительные результаты на отдаленных периодах наблюдения – от 5 до 20~25 лет. Именно поэтому в странах с развитой медициной каротидная эндартерэктомия является основным методом лечения данной патологии.
Для других зон поражения в СПб больнице РАН проводятся трансплантации артерий и шунтирующие операции.
Получить консультацию специалистов и узнать подробности можно через контакт-центр 323 45 35
Заболевания периферических артерий (ЗПА) ᐈ Диагностика и лечение
Описание
Заболевания периферических артерий (ЗПА) или облитерирующий эндартериит – воспалительное заболевание, поражающее чаще всего артерии нижних конечностей, реже — верхних, при котором сужаются кровеносные сосуды (атеросклероз), нарушается нормальный кровоток, приводящий к недостаточному кровоснабжению тканей нижних конечностей. ЗПА ног различается по трем видам в зависимости от их локализации: тазовое (подвздошная артерия), бедренное (бедренные артерии) и голени (артерии голени и ступней).
ЗПА ног различается по трем видам в зависимости от их локализации: тазовое (подвздошная артерия), бедренное (бедренные артерии) и голени (артерии голени и ступней).
Тромбоз инфраренального отдела брюшной аорты, известный как синдром Лериша, приводит к нарушению кровообращения обеих ног с болевыми ощущениями в области ягодиц и бёдер. У мужчин при этом может развиться импотенция. Периферийная артериальная окклюзия встречается довольно часто. В основном этим недугом страдает до 10% населения Германии в возрасте старше 50 лет, но только в одной трети случаев болезнь имеет выраженные симптомы, причем у мужчин она встречается в четыре раза чаще, чем у женщин.
Симптомы
В зависимости от вида и степени тяжести симптомов ЗПА подразделяется, согласно Фонтейну, на четыре стадии.
- Стадия I: отсутствие жалоб – длина проходимого больным расстояния не ограничена.
- Стадия II: если в результате спазма в периферических сосудах происходит недостаточное снабжение мышц кислородом, то это может привести к так называемой перемежающейся хромоте, характеризующейся болевыми ощущениями в нижних конечностях, которые возникают в процессе ходьбы и утихают при прекращении движения.
 При этом люди вынуждены через определенное время делать остановки во время ходьбы, чтобы избавиться от болей. Этот этап также делится на дополнительные стадии, в зависимости от пройденного человеком расстояния.
При этом люди вынуждены через определенное время делать остановки во время ходьбы, чтобы избавиться от болей. Этот этап также делится на дополнительные стадии, в зависимости от пройденного человеком расстояния. - Стадия IIа: длина расстояния при безболезненной ходьбе составляет более 200 метров;
- Cтадия IIв: расстояние, пройденное человеком без болевых ощущений — менее 200метров;
- Стадия III: ощущение боли в состоянии покоя;
- Стадия IV: разрушение тканей (некроз) с появлением язв и ран в связи с большой нехваткой кислорода в тканях.
Наряду с болями появляется и ряд других признаков нарушения кровообращения в нижних конечностях: бледность кожного покрова конечностей и ощущение холода в ногах, отсутствие пульсации в пораженных конечностях, мышечная слабость во время физических упражнений, незаживающие язвы и раны из-за сужения (стеноза) кровеносных сосудов и недостаточного снабжения мышц кислородом.
Причины и риски
Главной причиной заболевания периферических артерий считается, в основном, атеросклероз. Гораздо реже ЗПА возникает на основе травм, воспалительных заболеваний, эмболий, воспаления крупных кровеносных сосудов вследствие нарушения кровообращения. К основным факторам риска развития атеросклероза и ЗПА относятся: курение, сахарный диабет (Diabetes mellitus),повышенное кровяное давление (артериальная гипертония), нарушение обмена веществ из-за ожирения. Среди других факторов риска называют также половой признак (мужчины страдают атеросклерозом чаще, чем женщины), возраст, наследственность, неправильное питание (например, чрезмерное употребление жиров, мяса и недостаточное – овощей и фруктов), лишний вес (ожирение), отсутствие движения и физических нагрузок.
Гораздо реже ЗПА возникает на основе травм, воспалительных заболеваний, эмболий, воспаления крупных кровеносных сосудов вследствие нарушения кровообращения. К основным факторам риска развития атеросклероза и ЗПА относятся: курение, сахарный диабет (Diabetes mellitus),повышенное кровяное давление (артериальная гипертония), нарушение обмена веществ из-за ожирения. Среди других факторов риска называют также половой признак (мужчины страдают атеросклерозом чаще, чем женщины), возраст, наследственность, неправильное питание (например, чрезмерное употребление жиров, мяса и недостаточное – овощей и фруктов), лишний вес (ожирение), отсутствие движения и физических нагрузок.
Обследование и диагноз
С целью подтверждения диагноза при подозрении на ЗПА врачу необходимо провести ряд тестов: медицинский осмотр, включающий в себя проверку цвета кожного покрова конечностей, нарушения кровообращения, контроль частоты пульса, температуры тела, прослушивание на предмет потока шумов, тестирование сенсорики и моторики, клинические исследования (эргометрия для определения пройденного расстояния на беговой дорожке, допплерография, осциллографирование, цветное дуплексное УЗИ, цифровая ангиография, КТ-ангиография (КТА), магнитно-резонансная ангиография (МРА) и лабораторные исследования на определение СК миоглобина и С-реактивного белка (СРБ).
Лечение
Лечение ЗПА следует проводить в соответствии со стадиями болезни. На первой стадии уместно консервативное лечение – в первую очередь, устранение факторов риска сердечно-сосудистых заболеваний. Успешный результат при этом во многом зависит от сотрудничества пациентов с врачом. Чем активнее будут их действия (например, отказ от курения, контроль артериального давления и т.д.), тем успешнее они смогут остановить прогрессирование болезни и избежать таких осложнений, как инфаркт или инсульт. На второй стадии, наряду с корректировкой факторов риска, рекомендуется медикаментозное лечение и увеличение уровня физической нагрузки для ног и сосудов. В качестве лекарственной терапии зачастую применяются такие вазоактивные вещества, как цилостазол, и антитромбоцитарные препараты, например, клопидогрель. Решающую роль в лечении играют движение и ходьба. Они стимулируют образование и развитие коллатерального кровообращения, приводящего к улучшению кровоснабжения пораженных нижних конечностей. На стадииях II — IV, в дополнение к лекарственной терапии, можно применять и реваскуляризационные методы лечения, что означает либо открытое хирургическое вмешательство, либо катетерную процедуру. Последняя предполагает введение в суженный или закупоренный кровеносный сосуд катетера, снабженного стентом, который расширяет проходимость артерии и способствует восстановлению нормального кровообращения. В хирургии зачастую проводятся шунтирующие операции: вшивание дополнительного сосуда в обход пораженной артерии. В случае разрушения большого участка ткани (IV стадия заболевания), и когда реваскуляризационные методы лечения не приносят желаемых результатов, используется, как правило, последняя мера для спасения жизни больного — ампутация конечности.
На стадииях II — IV, в дополнение к лекарственной терапии, можно применять и реваскуляризационные методы лечения, что означает либо открытое хирургическое вмешательство, либо катетерную процедуру. Последняя предполагает введение в суженный или закупоренный кровеносный сосуд катетера, снабженного стентом, который расширяет проходимость артерии и способствует восстановлению нормального кровообращения. В хирургии зачастую проводятся шунтирующие операции: вшивание дополнительного сосуда в обход пораженной артерии. В случае разрушения большого участка ткани (IV стадия заболевания), и когда реваскуляризационные методы лечения не приносят желаемых результатов, используется, как правило, последняя мера для спасения жизни больного — ампутация конечности.
Течение болезни и прогноз
Течение заболевания зависит от множества факторов и, в частности, от того, насколько успешно можно справиться с главной причиной сужения сосудов — атеросклерозом. В значительной степени это зависит от самого пациента, от того, насколько активно и последовательно он сам будет бороться с факторами риска.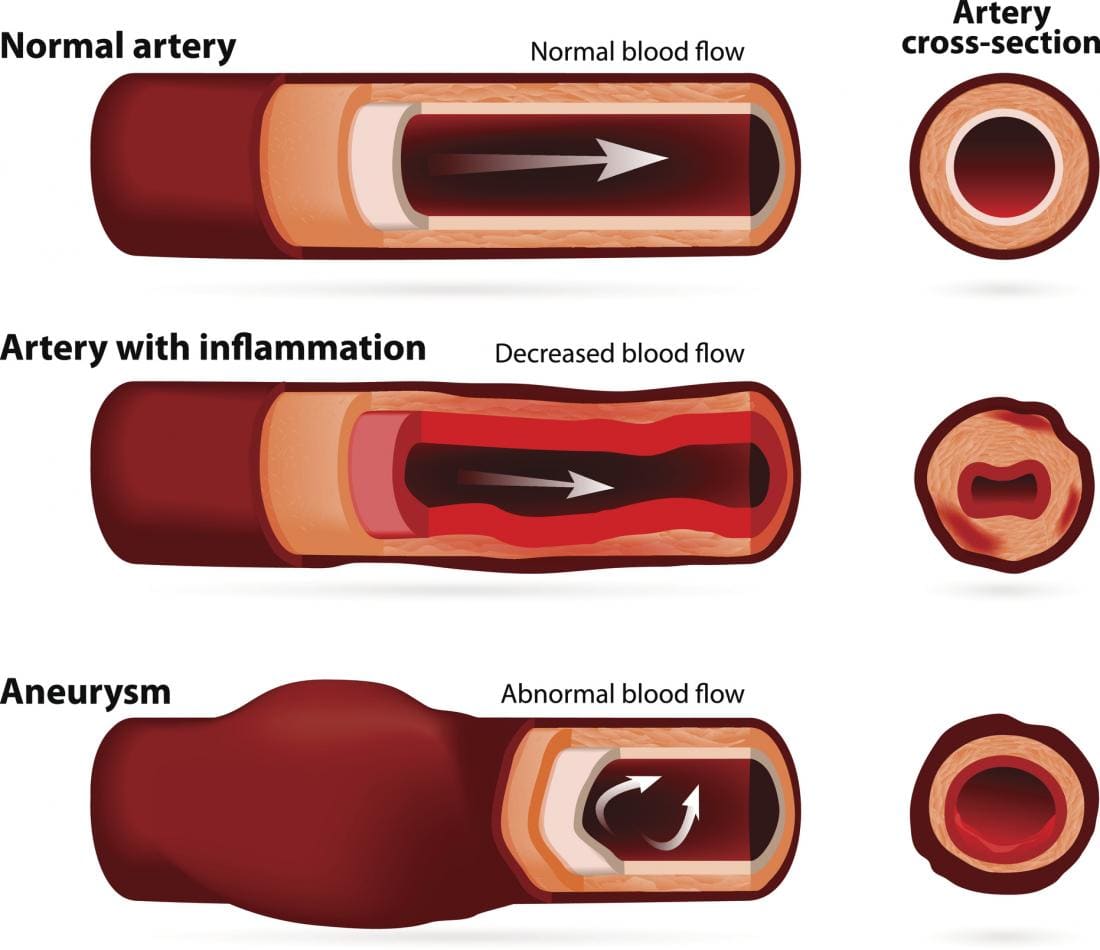 Это, прежде всего, отказ от курения и контроль возможного заболевания сахарным диабетом с помощью лекарственных препаратов. Несмотря на то, что атеросклероз полностью излечить невозможно, процесс болезни всё же можно замедлить или даже остановить.
Это, прежде всего, отказ от курения и контроль возможного заболевания сахарным диабетом с помощью лекарственных препаратов. Несмотря на то, что атеросклероз полностью излечить невозможно, процесс болезни всё же можно замедлить или даже остановить.
Комментарии
ЗПА зачастую перекликается с другими сердечно – сосудистыми заболеваниями, например, ишемической болезнью сердца или церебрально-артериальным облитерирующим эндартериитом. В связи с этим, врачу рекомендуется не только обследовать пациента по поводу ЗПА, но и быть в курсе имеющихся у больного проблем с сердцем и центральной нервной системой.
Атеросклероз брахиоцефальных артерий
Атеросклероз на сегодняшний день является самым распространённым заболеванием в России среди людей старше 50 лет. Это заболевание поражает любые артерии организма, начиная от головного мозга, заканчивая ногами. Необходимо отметить, что страшен не сам атеросклероз, а его грозные осложнения. Например, инфаркт и инсульт ежегодно уносят около полумиллиона жизней россиян.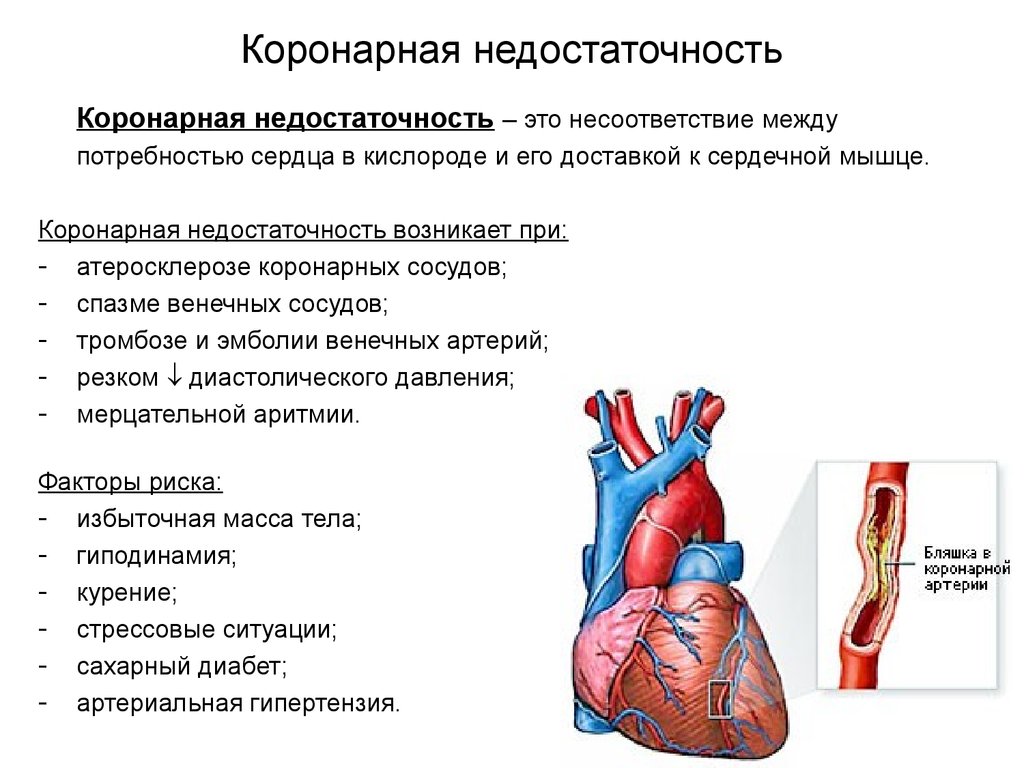
Необходимо помнить, что «вовремя распознать заболевание – значит сохранить жизнь»
Атеросклероз брахиоцефальных артерий – это поражение артерий, кровоснабжающих голову и шею (сонных и позвоночных артерий), вызывающее сужение и закупорку этих сосудов. В результате накопления в стенках фракций холестерина низкой плотности, артерии уплотняются, в них образуются бляшки, которые частично или полностью перекрывают просвет сосуда.
Если брахиоцефальный сосуд становится полностью блокирован или сильно сужается, то нарушается приток крови к части мозга, и может произойти инсульт.
У атеросклероза мозговых артерий и артерий других локализаций (например, сосудов сердца) одинаковые факторы риска. Они включают в себя:
- сахарный диабет
- высокое артериальное давление,
- высокий уровень холестерина
- курение
Один из исходов атеросклероза сонных артерий — это транзиторные ишемические атаки (ТИА или микроинсульт). Дело в том, что фрагменты атеросклеротической бляшки и сгустков крови, которые образуются в случае надрыва бляшки, переносятся током крови в голову, где они могут блокировать сосуды, снабжающие головной мозг.
Типичные (очаговые мозговые) симптомы включают: онемение или слабость на одной стороне тела, слабость верхних или нижних конечностей, неспособность говорить или понимать речь, а также снижение зрения.
Если происходит закупорка сосуда небольшим фрагментом, и он быстро распадается, то случается ТИА. Если же закрывается сосуд большего диаметра или фрагмент бляшки (эмбол) не рассасывается в ближайшее время – происходит инсульт.
Истинный инсульт связан с большим риском для жизни пациента. По статистике выживаемость после инсульта составляет около 60% в течении первого года и не больше 50% у пациентов, проживших 5 лет.
Первыми симптомами инсульта могут быть: нaрушение сознaния; сoстояние оглушенности; сoнливость или вoзбудимость; нeстерпимая гoловная боль; потeря сознания; тoшнота и рвoта. Позже присоединяются очаговые мозговые симтомы, но в отличии от ТИА, они могут быть не излечимы полностью.
При поражении позвоночных артерий обычно страдают задние отделы мозга.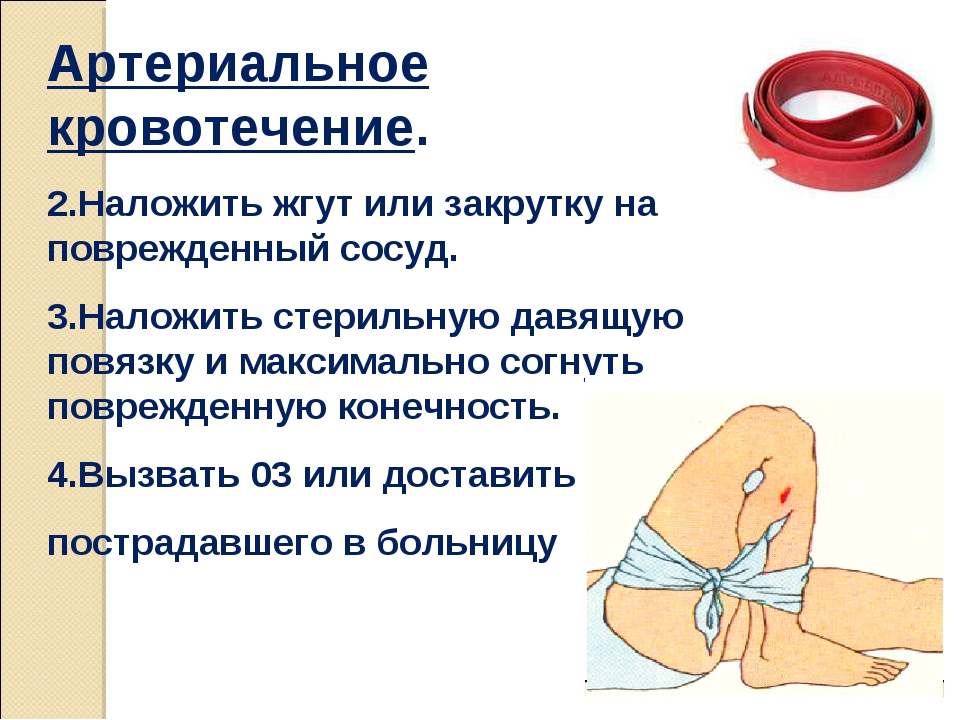 Симптомы поражения этих сосудов могут иметь разную интенсивность или внезапно проявляться при инсульте.
Симптомы поражения этих сосудов могут иметь разную интенсивность или внезапно проявляться при инсульте.
Эти симптомы включают: головокружение, тошноту, трудности удержания равновесия или координации, размытость или двоение зрения, а также снижение слуха.
Лечение атеросклероза брахиоцефальных артерий
Медикаментозное лечение возможно, если артерия не имеет значимого сужения.
Однако, в случаях значительного сужения сосуда (70% и более), рекомендуется операция – каротидная эндартерэктомия. В ходе операции бляшка, суживающая просвет сосуда полностью удаляется, и кровоток в сосуде восстанавливается.
Каротидная эндартерэктомия становится в последние годы не просто эффективной операцией, а даже носит название «золотого стандарта» в лечении атеросклероза сонных артерий.
С 2004 года появилась новая миниинвазивная процедура для лечения атеросклероза сонных артерий – стентирование сонных артерий.
Эта процедура выполняется путем открытия артерии с помощью небольшого катетера, на конце которого раздувается баллон, который вдавливает бляшку в стенки сосуда.
Далее в просвет сосуда устанавливается специальное устройство (стент), которое выстилает просвет сосуда изнутри, сохраняет его открытым и удерживает раздавленную бляшку. Кстати, такая процедура может быть выполнена и в случае поражения позвоночных артерий.
При выборе между эндартерэктомией и стентированием сонной аретрии, врачи оценивают множество факторов, включая общее состояние здоровья человека.
Хирурги делают выбор в пользу стентирования в тех случаях, когда пациент имеет симптомы брахиоцефального атеросклероза, но высокий риск для хирургического лечения (Например, сопутствующие заболевания сердца или последствия инсульта), а так же если имеются технические трудности для проведения операции.
Исследования показывают, что риск инсульта и смерти при каротидном стентировании несколько выше, чем при выполнении открытой операции.
Таким образом, каротидная эндартерэктомия является операцией выбора при значимых сужениях сосудов и у пациентов с симптомами нарушения мозгового кровообращения.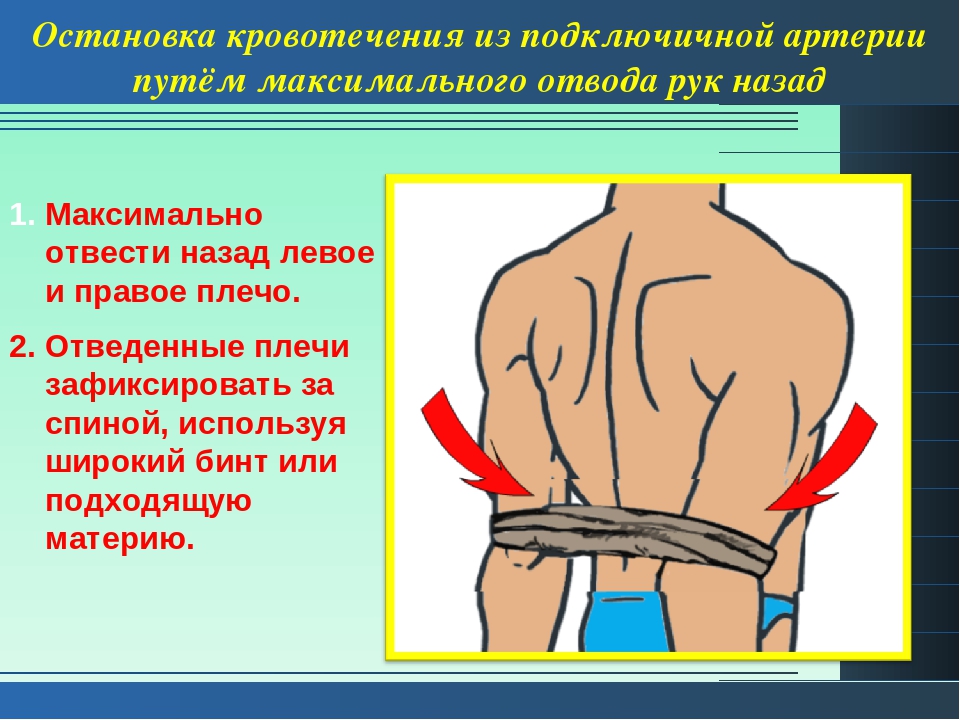
Своевременное проведение этой операции поможет пациенту избежать опаснейших исходов атеросклероза брахиоцефальных артерий – ТИА и инсульта!
Каротидная эндартерэктомия входит в перечень операций, выполняемых в отделении сосудистой хирургии НУЗ Дорожная больница на станции Свердловск-пассажирский ОАО «РЖД».
Атеросклероз
Атеросклероз — что это такое?
Атеросклероз — это хроническое заболевание кровеносных сосудов, в результате которого на внутренней стенке артерий откладываются холестерин и другие жиры, сами стенки становятся плотными и не эластичными. Как следствие — сосуды сужаются, доступ крови к органам снижается. В результате сосуд может полностью закрыться, что приведет к ишемическому повреждению
органов.
Атеросклероз считается одним из самых опасных заболеваний, приводящих к инвалидизации и смерти. Возникает в основном с возрастом, но в последнее время болезнь «молодеет», что связано с неправильным образом жизни.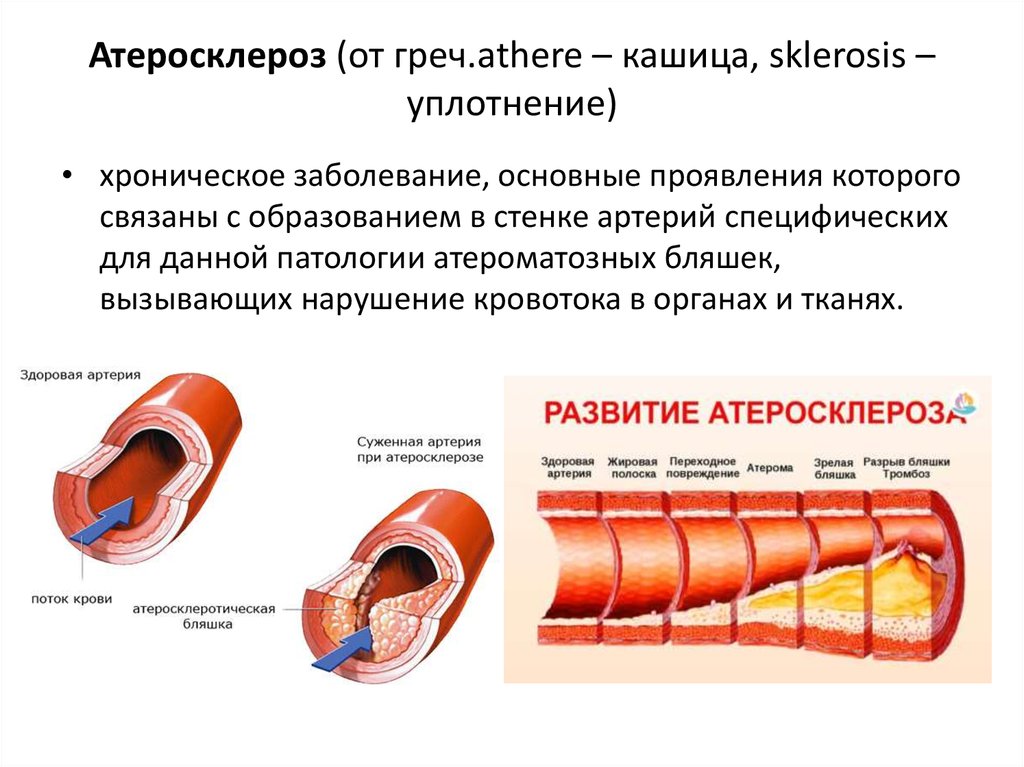 Как правило, обнаруживают болезнь уже на поздних стадиях, когда происходит проблема с кровоснабжением того или иного органа (сердце, головной мозг), т.е. слишком поздно. Атеросклероз — основная причина инфарктов, ишемической болезни сердца.
Как правило, обнаруживают болезнь уже на поздних стадиях, когда происходит проблема с кровоснабжением того или иного органа (сердце, головной мозг), т.е. слишком поздно. Атеросклероз — основная причина инфарктов, ишемической болезни сердца.
Болезнь развивается в течении нескольких лет, сначала поражаются крупные артерии, затем постепенно более мелкие. Первые признаки нехватки кровоснабжения ткани или органа начинают беспокоить только тогда, когда просвет сосуда уменьшился более, чем на 3/4.
Симптомы атеросклероза зависят от того, какой орган испытывает нехватку кровообращения. Основные органы, страдающие от кислородного голодания в результате поражения сосудов атеросклерозом — сердце, головной мозг, нижние конечности.
1. Если повреждены коронарные артерии, то страдает сердце. Нарушение нормального кровоснабжения сердца проявляется стенокардическим синдромом.
Основные симптомы поражения коронарных артерий могут возникать периодически:
-
Боль в области грудной клетки.
 Боль носит давящий, тупой ноющий или жгучий характер. Болевые ощущения могут отдавать в лопатку, левое предплечье, кисть или пальцы.
Боль носит давящий, тупой ноющий или жгучий характер. Болевые ощущения могут отдавать в лопатку, левое предплечье, кисть или пальцы. -
Ощущение давления на грудную клетку (будто положили на грудь тяжелый предмет).
-
Болевые ощущения, возникающие при дыхании.
-
Трудности с дыханием.
Для диагностирования атеросклероза коронарных артерий врач назначает коронарографию — рентгеновское исследование с контарстом, которое позволяют определить точное местоположение атеросклеротических бляшек и степень сужения просвета артерии.
2. При повреждении артерий головного мозга, симптомы атеросклероза следующие:
-
Головная боль.
 Болит вся голова, без точной локализации.
Болит вся голова, без точной локализации.
-
Звон и шум в ушах.
-
Человек испытывает проблемы со сном. Это может быть бессонница, а может, наоборот, — постоянное желание спать.
-
Нервозность, высокая возбудимость, повышенная тревожность.
-
Вялость и утомляемость.
-
Нарушения дыхания, речи, питания.
-
Нарушения координации движений.

3. Атеросклероз сосудов нижних конечностей проявляется следующими симптомами:
-
Ощущение холода в ногах.
-
«Затекание» конечности, появление мурашек, покалывания.
-
Бледность кожных покровов (кожа мраморного цвета).
-
Боли в ногах, «перемежающаяся хромота». Боли возникают в области бедер, ягодиц и икр, появляются приступообразо, в результате чего человек начинает хромать.
-
Образование на ногах ран, связанных с недостатком питания тканей.
-
Покраснение пальцев на ногах, появление отеков.
Холестерин и его роль в развитии атеросклероза.
Холестерин — это жирный спирт, который играет большую роль в обмене веществ. Холестерин участвует в синтезе мужских и женских половых гормонов (эстроген, тестостерон, прогестерон), поэтому отклонения холестерина от нормы в ту или иную сторону, могут привести к проблемам в репродуктивной сфере. Нарушение концентрации холестерина может привести к снижению иммунитета. Холестерин активно участвует в процессе пищеварения — без него невозможна выработка печенью пищеварительных солей и соков.
Холестерин участвует в синтезе мужских и женских половых гормонов (эстроген, тестостерон, прогестерон), поэтому отклонения холестерина от нормы в ту или иную сторону, могут привести к проблемам в репродуктивной сфере. Нарушение концентрации холестерина может привести к снижению иммунитета. Холестерин активно участвует в процессе пищеварения — без него невозможна выработка печенью пищеварительных солей и соков.
Подавляющее большинство холестерина вырабатывается организмом самостоятельно (около 80%) и только 20-25% поступает с продуктами питания (это подтверждает тот факт, что не только питание «виновато» в большой концентрации холестерина в крови). Поэтому даже если с помощью различных диет пытаться снизить уровень этих жиров, то «убрать» его существенную долю все равно не получится, более того, если организм не будет получать холестерин извне, он будет вырабатывать сам его еще в больших количествах.
Холестерин разносится с кровью по всему организму. Считается, что если концентрация этого вещества в крови выше нормы, то это приводит к отложению атеросклеротических бляшек на стенках сосудов. На самом деле, все не так просто.
На самом деле, все не так просто.
Холестерин условно разделяют на «плохой» и «хороший». На самом деле — это один и тот же холестерин, он имеет единый состав и единую структуру. Разница лишь в том, к какому транспортному белку он присоединится. То есть холестерин опасен только в определенном связанном, а не свободном состоянии.
Холестерин «плохой» (холестерин низкой плотности или ЛПНП) способен оседать на стенках сосудов и образовывать наслоения-бляшки, закрывающие просвет кровеносного сосуда. При соединении с белками-апопротеинами, холестерин образует комплексы ЛПНП. При повышении такого холестерина в крови — опасность атеросклероза действительно существует.
Холестерин «хороший» (холестерин высокой плотности или ЛПВП) отличается от плохого и по структуре, и по функции. Он очищает стенки сосудов от «плохого» холестерина и отправляет его на переработку в печень. Поэтому необходимо стремиться к тому, чтобы его показатели в крови не были ниже 100 мг/дл.
Еще один тип жиров носит название триглицериды. Они также как ЛПНП повышают риски развития смертельных болезней. Их уровень в крови не должен превышать отметки в 50мг/дл.
К факторам риска содержания в крови «плохого» холестерина, а как следствие развития атеросклероза можно отнести:
- Пол. Мужчины чаще болеют атеросклерозом, чем женщины.
-
Возраст. Болезнь, как правило, возникает после 45 лет.
-
Наследственность. Уровень гормонального фона, иммунитет, генетически обусловленная специфика обмена веществ играют важные роли в ускорении или замедлении развития атеросклероза. Если у одного или обоих родителей имелись проблемы с холестерином, с вероятностью от 25 до 75% ребенок унаследует эту особенность обмена веществ.
-
Вредные привычки. Курение, большие дозы алкоголя ускоряют наступление болезни.

-
Лишний вес. Очень негативный фактор. Лишний вес может привести к сахарному диабету, а он к атеросклерозу. Почти у 65% людей с избыточной массой тела наблюдаются проблемы с уровнем «плохого холестерина» в крови.
-
Питание — играет хоть и не ключевую роль, но всё же существенно влияет на динамику холестерина в крови. С пищей, как было сказано, поступает не более 25% всего холестерина. Продукт, богатый холестерином (яйцо, креветки), съеденный с жирными продуктами (майонез, колбасные изделия и т.д.), с большой долей вероятности повлечет за собой повышение уровня ЛПНП-холестерина. Поэтому, ограничивайте потребление жирной, копченой, жареной пищи. Употребление большого количества углеводов также нежелательно.
- Малоподвижный образ жизни. Низкий уровень физической активности напрямую связан с повышением концентрации холестерина в крови. Все дело в застойных процессах и нарушении энергетического обмена организма.
 При достаточных физических нагрузках уровень «плохого» холестерина обычно снижается. Регулярные физические упражнения помогают организму выводить жир, «Плохойе» холестерин надолго не задерживается в кровяном русле, он не успевает осесть на стенках сосудов. Доказано, что бег способствует выведению полученного из продуктов жира. Именно люди, регулярно бегающие меньше всего подвержены образованию холестериновых бляшек.
При достаточных физических нагрузках уровень «плохого» холестерина обычно снижается. Регулярные физические упражнения помогают организму выводить жир, «Плохойе» холестерин надолго не задерживается в кровяном русле, он не успевает осесть на стенках сосудов. Доказано, что бег способствует выведению полученного из продуктов жира. Именно люди, регулярно бегающие меньше всего подвержены образованию холестериновых бляшек.
- Сахарный диабет. Сахарный диабет — это фактор повышенного риска развития атеросклероза сосудов (более чем в 2 раза).
Врач на приеме соберет анамнез — измерит давление, выслушает жалобы, уточнит, есть ли сопутствующие заболевания (сахарный диабет, гипертония и т.д.). Далее произведет первичный осмотр — проверит, есть ли деформация ногтей, отеки конечностей, выпадение волос и т.д. Затем направит пациента на инструменталные и лабораторные исследования:
— Анализ крови на холестерин, холестерин ЛПНП, холестерин ЛПВП, триглицериды.
— Электрокардиограмма (ЭКГ). Иногда ЭКГ проводят с нагрузкой, чтобы определить, есть ли недостаток кислорода к сердцу.
— Ультразвуковая допплерография экстракраниальных артерий. На УЗДГ видна скорость кровотока в артериях и степень сужения сосудов.
— Коронарография — рентгеноконтрастный метод исследования, который является наиболее точным и достоверным способом диагностики ишемической болезни сердца (ИБС), позволяя точно определить характер, место и степень сужения коронарной артерии.
— МРТ сосудов (ангиография) головного мозга, шеи. Также помогает увидеть место сужения артерий. Метод не несет в себе рантгеновской нагрузки, поэтому может проводиться сколь угодно раз без вреда для здоровья.
Существуют и иные способы диагностики. Конкретные методы определяет врач, исходя из клинической картины.
Лечение атеросклероза
1. Лечение атеросклероза может быть медикаментозным. Назначают препараты, которые хорошо устраняют причины атеросклероза и его пагубные последствия.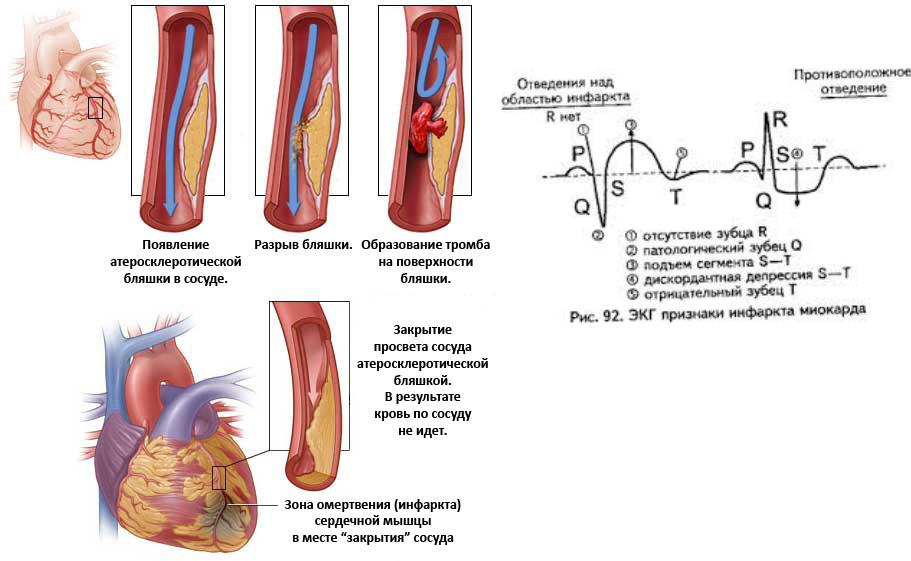 Кроме того рекомендуют соблюдать диеты и оптимальный режим физической активности.
Кроме того рекомендуют соблюдать диеты и оптимальный режим физической активности.
Группы препаратов, назначаемых при атеросклерозе:
-
Статины. Угнетают функцию печени по выработке холестерина.
-
ЖК-секвестранты. Угнетают функцию синтеза желчных кислот печенью. В связи с этим органу приходится активнее расходовать холестерин, чтобы обеспечить нормальное и стабильное пищеварение.
-
Фибраты. Разрушают нейтральные жирные структуры — триглицериды.
-
Сосудорасширяющие и спазмолитические препараты.
На сегодняшний день в основном проводят следующие виды хирургических операций:
— Баллонная ангиопластика и стентирование;
— Операция аортокоронарного шунтирования;
— Реконструктивные операции на артериях, обеспечивающих мозговое кровообращение;
Возврат к списку
Симптомы и лечение сосудистых травм
Что такое сосудистая травма?
Артерии и вены составляют сосудистую систему.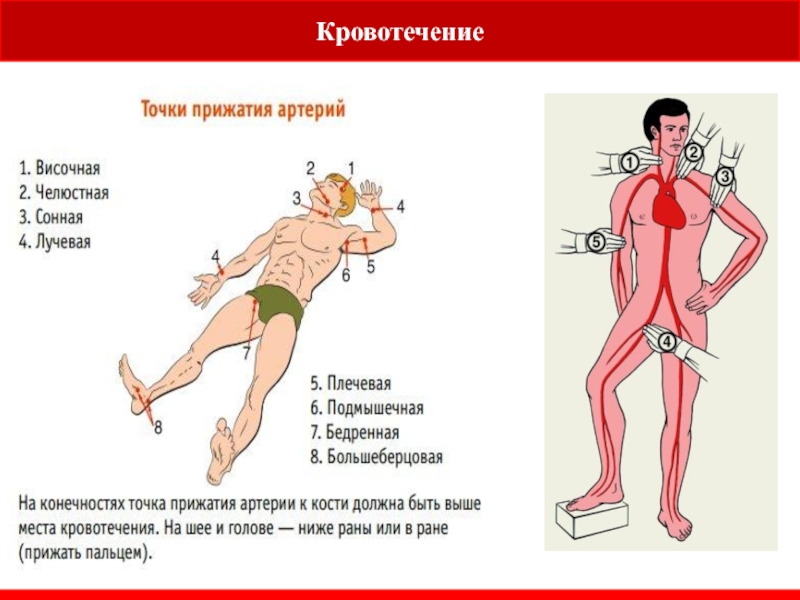
- Артерии несут кровь от сердца.
- Вены несут кровь обратно к сердцу.
Сосудистая травма означает, что кровеносный сосуд получил какую-либо травму.
Иногда эти травмы связаны с разрывом или проколом, вызывающим кровопотерю. В других случаях они вызывают повреждение сосуда из-за раздавливания или скручивания.
Факторы риска и причины сосудистых травм
Любой человек может получить травму сосудов из-за травмы — преднамеренной или непреднамеренной.
Причины травмы сосудов
Сосудистая травма может быть вызвана целым рядом причин, в том числе:
- Травмы (несчастные случаи, падения, порезы и т. д.)).
- Насилие.
- Защемление вены или артерии (внутреннее или внешнее).
- Вывих кости.
- Пирсинг вены, например, с введением внутривенного вливания.

Осложнения при травмах сосудов
Сосудистая травма может привести к ряду осложнений, в том числе:
- Потеря крови, иногда большая.
- Образование тромба (тромбоз).
- Синяки и отеки.
- Болезненность или боль.
- Рубцевание.
Рубцевание или неполное заживление могут вызвать постоянную слабость артерии или вены, что делает их более уязвимыми к травмам в будущем.
Сгустки крови могут вызвать блокировку кровотока. Сгусток становится особенно опасным, когда он отрывается и перемещается в другую часть тела, например, в сердце, легкие или мозг.
Если вы или кто-то другой испытываете значительную кровопотерю, немедленно обратитесь к врачу.
Чтобы записаться на прием к сосудистому хирургу UPMC, заполните форму запроса на прием к сосудистому хирургу или позвоните по телефону 1-855-876-2484 ( UPMC-HVI) .
Повреждение артерий — обзор
РЕСТЕНОЗ
Повреждение артерий, например, у пациентов с ИБС, подвергающихся чрескожному коронарному вмешательству или установке внутрисосудистых стентов, часто приводит к рестенозу просвета из-за констриктивного ремоделирования стенки сосуда и накопления ГМК в интиме матрица. 131
131
Исследования на моделях поврежденных артерий животных помогли нам понять механизмы ангиопластики и стентирования, а также протестировать технологии стентов с лекарственным покрытием (DES). 132 Предсказание неблагоприятных клинических исходов у пациентов с СЛП можно прогнозировать на основе субоптимальных результатов в исследованиях на животных моделях, и аналогичным образом тромбоз стента на животных моделях предполагает тромбогенность стента у пациентов-людей. Тем не менее, неоднозначные результаты на животных моделях иногда контрастировали с отличными клиническими результатами у пациентов.Хотя причины этих различий не были объяснены, они могут быть результатом различий в методах, включая меньшее повреждение артерий, чем первоначально описано в моделях. Дальнейшие исследования на животных моделях, вероятно, устранят эти очевидные различия с клиническими испытаниями на людях и улучшат наше понимание того, как использовать животные модели для клинического стентирования в эпоху СЛП.
Voisine и соавт. 133 сообщили о значительной эндотелиальной дисфункции в коронарных микрососудах у свиней с моделью хронической ишемии при введении богатой холестерином диеты, тогда как было заметно сниженный ответ на ангиогенные (вазодилатационные) эффекты введенного VEGF. .Кроме того, были затронуты ключевые молекулы в сигнальных путях VEGF. Эти изменения не происходили у свиней, получавших ту же терапию VEGF, но находящихся на обычном рационе. Более того, в соответствии с ассоциацией между VEGF и eNOS в росте и стабилизации сосудистых клеток при развитии сосудов, у животных, получавших диету с высоким содержанием холестерина, наблюдалось снижение экспрессии eNOS и VEGF, чем в группе с нормальной диетой, у которой наблюдалось увеличение обоих факторов. В более раннем исследовании было показано, что у пациентов со стабильной ИБС и пациентов с острой ишемией миокарда наблюдалось снижение высвобождения NO в ответ на VEGF. 134 Позже Bussolati и соавт. 135 также сообщили, что VEGF-стимулированное высвобождение NO ингибируется блокадой VEGF-R1 и что VEGF-R1-опосредованное высвобождение NO негативно регулирует VEGF-R2-опосредованную пролиферацию и способствует образованию капиллярных сетей в организме человека.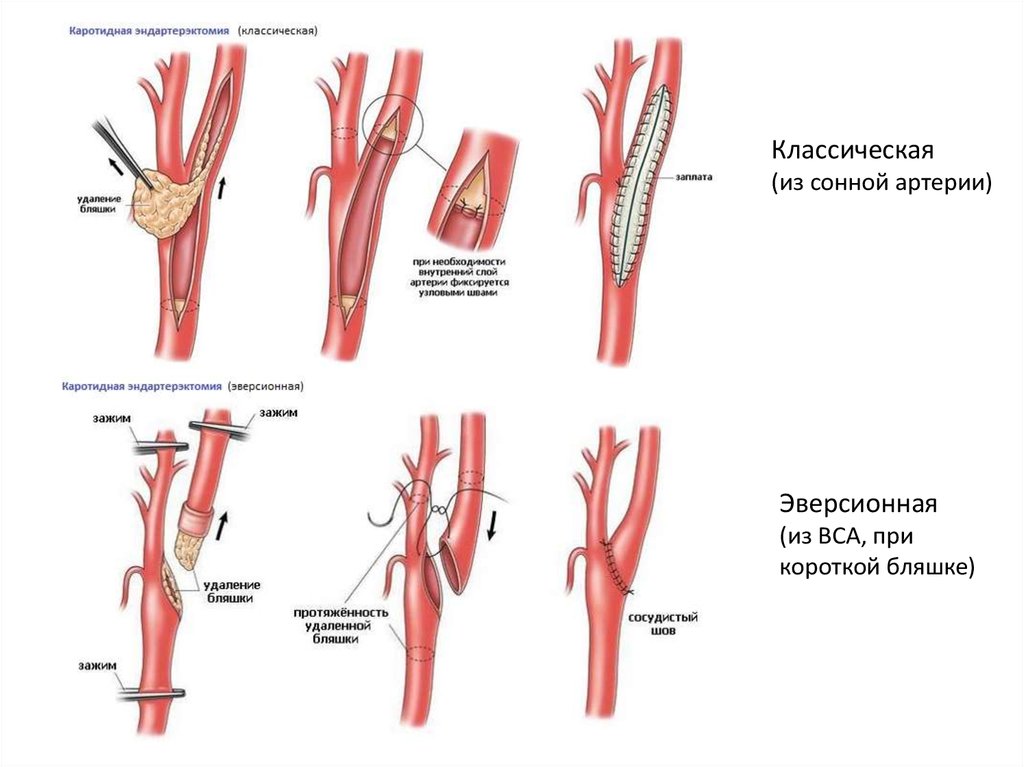 эндотелиальные клетки пупочной вены. Это указывает на то, что VEGF-R1 является сигнальным рецептором, который способствует дифференцировке эндотелиальных клеток в сосудистые трубки, частично путем ограничения опосредованной VEGF-R2 пролиферации эндотелиальных клеток с помощью NO, и, вероятно, способствует молекулярному переключению дифференцировки эндотелиальных клеток.
эндотелиальные клетки пупочной вены. Это указывает на то, что VEGF-R1 является сигнальным рецептором, который способствует дифференцировке эндотелиальных клеток в сосудистые трубки, частично путем ограничения опосредованной VEGF-R2 пролиферации эндотелиальных клеток с помощью NO, и, вероятно, способствует молекулярному переключению дифференцировки эндотелиальных клеток.
Фактор ранней реакции роста-1 (Egr-1) контролирует экспрессию ряда генов, участвующих в патогенезе атеросклероза и рестеноза после ангиопластики. Egr-1 активируется различными проатерогенными стимулами. Таким образом, этот фактор транскрипции представляет собой ключевую молекулярную мишень в попытках контролировать образование сосудистых поражений у людей. Lowe and Associates 136 генерировали каталитические ДНКзимы, нацеленные на определенные последовательности в организме человека EGR-1 расщепляющие мРНК in vitro эффективно транскрибирующие EGR-1 мРНК в заранее выбранных местах, ингибирующие экспрессию белка EGR-1 в ГМК аорты человека, блокирующие сыворотку — индуцируемая пролиферация клеток и прекращение повторного роста клеток после механического повреждения in vitro. Эти ДНКзимы также селективно ингибировали экспрессию EGR-1 и пролиферацию ГМК свиных артерий и уменьшали утолщение интимы после стентирования коронарных артерий свиней in vivo. Эти данные показали, что ДНКзимы, доставленные внутрь просвета, нацеленные на EGR-1 , могут служить ингибиторами рестеноза в стенте. Кроме того, эта группа исследователей, используя крысиную модель образования неоинтимы (NI), включающую полную перевязку общей сонной артерии, продемонстрировала важность гена немедленного раннего развития и фактора транскрипции цинкового пальца EGR-1 в этом процессе.За острым прекращением кровотока в общей сонной артерии путем перевязки сосудов последовала экспрессия EGR-1 в артериальной среде в течение 3 часов и образование NI проксимальнее точки перевязки через 18 дней. Локальная доставка каталитических олигодезоксинуклеотидов (ODN), нацеленных на крысиную мРНК EGR-1 , во время лигирования снижала как экспрессию EGR-1, так и образование NI в этой модели.
Эти ДНКзимы также селективно ингибировали экспрессию EGR-1 и пролиферацию ГМК свиных артерий и уменьшали утолщение интимы после стентирования коронарных артерий свиней in vivo. Эти данные показали, что ДНКзимы, доставленные внутрь просвета, нацеленные на EGR-1 , могут служить ингибиторами рестеноза в стенте. Кроме того, эта группа исследователей, используя крысиную модель образования неоинтимы (NI), включающую полную перевязку общей сонной артерии, продемонстрировала важность гена немедленного раннего развития и фактора транскрипции цинкового пальца EGR-1 в этом процессе.За острым прекращением кровотока в общей сонной артерии путем перевязки сосудов последовала экспрессия EGR-1 в артериальной среде в течение 3 часов и образование NI проксимальнее точки перевязки через 18 дней. Локальная доставка каталитических олигодезоксинуклеотидов (ODN), нацеленных на крысиную мРНК EGR-1 , во время лигирования снижала как экспрессию EGR-1, так и образование NI в этой модели. Напротив, зашифрованная версия этого ODN не оказывала ингибирующего действия. Эти результаты впервые демонстрируют, что утолщение интимы артерий после перевязки артерий критически зависит от активации EGR-1. 137 С другой стороны, EGR-1 может связывать и активировать промоторы многих генов, продукты которых влияют на восстановление сосудов. Сверхэкспрессия антисмысловой РНК использовалась для ингибирования синтеза белка EGR-1, не влияя на уровни непосредственно раннего продукта гена, c-fos. Кроме того, сверхэкспрессия антисмысловой РНК EGR-1 ингибировала повторный рост ГМК после механического повреждения in vitro , тогда как смысловая РНК EGR-1 не влияла на репарацию ГМК, экспрессию мРНК EGR-1 или синтез белка.Подход антисмысловой РНК может быть полезен для контроля роста ГМК в стенке поврежденной артерии.
Напротив, зашифрованная версия этого ODN не оказывала ингибирующего действия. Эти результаты впервые демонстрируют, что утолщение интимы артерий после перевязки артерий критически зависит от активации EGR-1. 137 С другой стороны, EGR-1 может связывать и активировать промоторы многих генов, продукты которых влияют на восстановление сосудов. Сверхэкспрессия антисмысловой РНК использовалась для ингибирования синтеза белка EGR-1, не влияя на уровни непосредственно раннего продукта гена, c-fos. Кроме того, сверхэкспрессия антисмысловой РНК EGR-1 ингибировала повторный рост ГМК после механического повреждения in vitro , тогда как смысловая РНК EGR-1 не влияла на репарацию ГМК, экспрессию мРНК EGR-1 или синтез белка.Подход антисмысловой РНК может быть полезен для контроля роста ГМК в стенке поврежденной артерии.
Сосудистые травмы: тенденции в лечении
Abstract
Сосудистые травмы представляют собой серьезную проблему для резидентов скорой помощи, поскольку эти травмы требуют срочного вмешательства для предотвращения смерти или потери конечностей. Иногда серьезное сосудистое повреждение проявляется едва уловимыми или скрытыми признаками или симптомами. У пациента через несколько недель или месяцев после первичной травмы могут появиться симптомы сосудистой недостаточности, эмболизации, псевдоаневризмы, артериовенозной фистулы и т. д.Хотя большинство повреждений сосудов вызвано проникающими травмами от огнестрельных ранений, колото-резаными или взрывными ранениями, возможность повреждения сосудов необходимо учитывать у пациентов со смещенными переломами длинных костей, размозжением, длительной иммобилизацией в фиксированном положении тугими гипсовыми повязками. или повязки и различные инвазивные процедуры. ятрогенные повреждения сосудов в большинстве серий составляют около 10% случаев; однако заболеваемость имеет тенденцию к увеличению, поскольку рутинно выполняется больше эндоваскулярных процедур, таких как ангиопластика и катетеризация сердца.
Иногда серьезное сосудистое повреждение проявляется едва уловимыми или скрытыми признаками или симптомами. У пациента через несколько недель или месяцев после первичной травмы могут появиться симптомы сосудистой недостаточности, эмболизации, псевдоаневризмы, артериовенозной фистулы и т. д.Хотя большинство повреждений сосудов вызвано проникающими травмами от огнестрельных ранений, колото-резаными или взрывными ранениями, возможность повреждения сосудов необходимо учитывать у пациентов со смещенными переломами длинных костей, размозжением, длительной иммобилизацией в фиксированном положении тугими гипсовыми повязками. или повязки и различные инвазивные процедуры. ятрогенные повреждения сосудов в большинстве серий составляют около 10% случаев; однако заболеваемость имеет тенденцию к увеличению, поскольку рутинно выполняется больше эндоваскулярных процедур, таких как ангиопластика и катетеризация сердца.
Гражданская травма чаще наблюдается у молодых мужчин. Однако это может произойти в любом возрасте из-за дорожно-транспортных происшествий, огнестрельного оружия, взрывов бомб и диагностических процедур. В большинстве случаев гражданская травма вызывает меньшее повреждение тканей. В Кашмирской долине наблюдается эпидемия сосудистых повреждений из-за проблем с правопорядком в последние два десятилетия. В обзоре подробно рассматривается эта тема.
В большинстве случаев гражданская травма вызывает меньшее повреждение тканей. В Кашмирской долине наблюдается эпидемия сосудистых повреждений из-за проблем с правопорядком в последние два десятилетия. В обзоре подробно рассматривается эта тема.
Ключевые слова: Травмы сосудистой системы, подкожные вены, анастомозы
1.Введение
Кашмирская долина, являющаяся зоной конфликта, в которой существуют проблемы с правопорядком для руды, более чем за два десятилетия стала свидетелем эпидемии сосудистых повреждений. Наша больница (Институт медицинских наук Шер-и-Кашмир) является единственной больницей третичного уровня, где имеются средства для лечения сосудистых травм, обслуживающие население более десяти миллионов человек (1-4).
Большинство травм сосудов в военных конфликтах происходит от осколков баллистического оружия, такого как артиллерия, ракеты, гранаты и бомбы.Развитие высокоскоростного оружия (например, артиллерии) вызывает массивное разрушение тканей, превышающее таковое от предыдущего военного оружия такого же размера. Экспериментальные исследования высокоскоростных ранений показывают, что временная полость может быть создана почти в тридцать раз больше, чем постоянный остаточный тракт (5). Этот временный кавитационный эффект повреждает ткани за пределами фактического пути снаряда.
Экспериментальные исследования высокоскоростных ранений показывают, что временная полость может быть создана почти в тридцать раз больше, чем постоянный остаточный тракт (5). Этот временный кавитационный эффект повреждает ткани за пределами фактического пути снаряда.
травмы сосудов можно разделить на следующие группы:
• Спазм
• Тромбоз
• Участок / интимный клапан
• Зарубка / переход
• AV (Arteriovenous) Fistula
• Aneurysm и Pseudoaneurysm
• Артериал emboli
Спазм: Травма сосуда приводит к спазму локализованной сосудистой сети, что вызывает снижение дистального кровотока и может привести к дистальным функциональным повреждениям.
Тромбоз: Любое повреждение интимы артерии сопровождается тромбозом в течение определенного периода времени, который вызывает частичную или полную окклюзию сосуда или может привести к обратимому сегментарному спазму.
Ушиб/Интимальный лоскут: Ударная сила или чрезмерное растяжение вызывают разрыв интимы сосуда.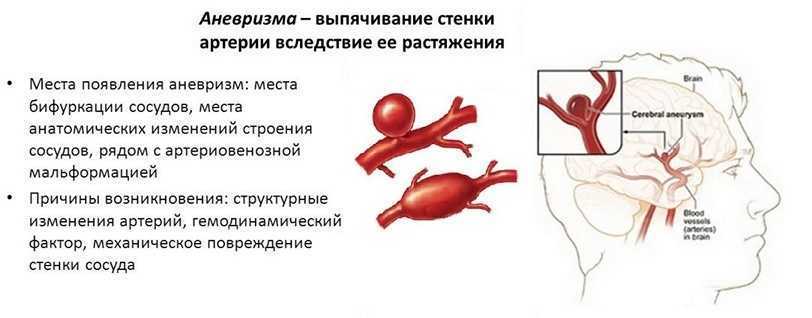 Небольшой лоскут <5 мм может незначительно перекрывать кровоток, но может стать очагом тромбоза. Большой лоскут может выпячиваться в просвет сосуда, вызывая частичную окклюзию и симптомы дистальной ишемии.
Небольшой лоскут <5 мм может незначительно перекрывать кровоток, но может стать очагом тромбоза. Большой лоскут может выпячиваться в просвет сосуда, вызывая частичную окклюзию и симптомы дистальной ишемии.
Разрыв/пересечение: Разрыв и разрез чаще всего возникают в результате тупой травмы, а также при попадании высокоскоростных метательных снарядов, которые вызывают неравномерные разрывы сосуда или потерю сегментов, связанную с повреждением других тканей. Чисто пересеченная артерия часто будет сужаться и втягиваться, ограничивая кровопотерю. Продольный или сильно разорванный сосуд не может ограничить кровопотерю и может привести к большей кровопотере. Этот тип травмы составляет 80-85% случаев (1).
Артериовенозная фистула: Повреждение артерии и прилежащей вены может привести к развитию соединения между ними, когда поток высокого давления отклоняется в сторону низкого давления (артерия-вена), что приводит к неадекватной перфузии и растяжению вен. Любая атриовентрикулярная фистула в центральных сосудах вызывает застойную сердечную недостаточность и проявляется обычно поздно.
Любая атриовентрикулярная фистула в центральных сосудах вызывает застойную сердечную недостаточность и проявляется обычно поздно.
Аневризма и псевдоаневризма: Истинная аневризма содержит все слои сосудистой стенки (интима, медиум и адвентиция) и редко может быть вызвана травмой.Чаще псевдоаневризма формируется после травмы.
Когда кровотечение из поврежденного сосуда останавливается окружающей фасцией и другими мягкими тканями, оно постепенно инкапсулируется фиброзной тканью, сходной по всем свойствам с адвентицией. Все это приводит к тонкостенной капсуле, которая продолжает расширяться из-за более высокого артериального давления, образуя пальпируемую пульсирующую массу, которая может сдавливать окружающие структуры, вызывая невропатию, коллапс вен, эрозию кости или эмболизацию дистальных сосудов, вызывая ишемию.Остановка кровотечения после повреждения сосудов была главной заботой человека с каменного века; для остановки кровотечения использовались различные средства, такие как компрессия, горячее железо, холод и перевязка.
После первоначального вклада Цельса, Галена и их современников использование лигатуры было практически забыто почти на 1200 лет. В Средние века прижигание использовалось почти исключительно для остановки кровотечения. Джером Брауншвейгский, армейский хирург, фактически опередил Амбруаза Паре в описании использования лигатуры как лучшего способа остановить кровотечение.Амбруаз Паре (6), имея большой опыт в хирургии травм, особенно на поле боя, твердо установил использование лигатур для остановки кровотечения из открытых сосудов. В 1952 году он сделал первую ампутацию выше демаркационной линии, которая ранее была сделана ниже демаркационной линии. В семнадцатом веке монументальный вклад Гарвея, описывающий кровообращение, очень помог понять сосудистые повреждения. В 1674 г. военный хирург по имени Морель вставил в повязку палочку и закручивал ее до тех пор, пока артериальный кровоток не остановился (7).Вскоре после этого стали использовать винтовой жгут. В 1873 году Фридрих фон Эсмарх представил свой эластичный жгут для оказания первой помощи на поле боя. Его открытие позволило хирургам выборочно оперировать конечности в сухом бескровном поле.
Его открытие позволило хирургам выборочно оперировать конечности в сухом бескровном поле.
Первая успешная перевязка общей сонной артерии для остановки кровотечения была выполнена в 1803 г. Флемингом; но об этом сообщил только 14 лет спустя Coley (1817), потому что Флеминг умер вскоре после операции (8).Слуга попытался покончить жизнь самоубийством, перерезав себе горло. Когда Флеминг увидел пациента, который выглядел обескровленным, пульса не было, а зрачки были расширены. Удалось перевязать две верхние щитовидные артерии и одну внутреннюю яремную вену. Отмечали разрыв наружного мышечного слоя сонной артерии, а также разрыв трахеи между щитовидным и перстневидным хрящами. Это позволило дренажу из раны попасть в трахею, спровоцировав сильные приступы кашля, хотя состояние пациента, казалось, улучшалось.Примерно через неделю после травмы Флеминг писал: « Вечером 17-го, во время сильного приступа кашля, артерия лопнула, и мой бедный пациент в одно мгновение залился кровью». «В этой ужасной ситуации я пришел к выводу, что мне остается сделать только один шаг с надеждой на успех; в основном, чтобы перерезать и перевязать сонную артерию ниже раны. Я никогда не слышал о такой операции; но полагал, что в данном случае его последствия могут быть менее грозными, чем у человека, не пораженного кровотечением» (8).
Я никогда не слышал о такой операции; но полагал, что в данном случае его последствия могут быть менее грозными, чем у человека, не пораженного кровотечением» (8).
Рана быстро зажила после перевязки сонной артерии, и пациент выздоровел. Важность коллатерального кровообращения для сохранения жизнеспособности конечности после перевязки была хорошо известна на протяжении веков. Тот факт, что для установления этого обращения требовалось время, был общепризнанным. Halsted (1912) сообщил об излечении подвздошно-бедренной аневризмы путем наложения алюминиевой ленты на проксимальный отдел артерии без серьезного нарушения кровообращения или функции нижней конечности (9).Именно Алекс Карел выполнил первый успешный анастомоз «конец в конец» в 1896 году. Десять лет спустя Гойанес в 1906 году использовал венозный трансплантат для перекрытия дефекта артерии. опыт Второй мировой войны, в связи с существенным прогрессом в технике операций на сосудах, сопровождавшимся совершенствованием анестезии, переливания крови и применением антибиотиков. Пожалуй, самым важным была быстрая эвакуация и реанимация раненых.Кроме того, полное понимание важности хирургической обработки раны, отсроченного первичного закрытия и назначения антибиотиков значительно снизило опасность инфицирования (10, 11).
Пожалуй, самым важным была быстрая эвакуация и реанимация раненых.Кроме того, полное понимание важности хирургической обработки раны, отсроченного первичного закрытия и назначения антибиотиков значительно снизило опасность инфицирования (10, 11).
Исторически сложилось так, что большинство пациентов с серьезным повреждением артерий не выживали достаточно долго, чтобы обратиться к врачу; у тех, кто это делал, обычно были легкие ранения. С развитием системы здравоохранения многие пациенты с серьезными травмами теперь поступают в больницу (даже с очень серьезными сосудистыми повреждениями, например, с повреждением сонных артерий), и их спасают.Восстановление сосудов было впервые успешно выполнено в начале 1900-х годов. Обычный хирургический подход к серьезному повреждению сосудов заключался в простой перевязке сосуда и ампутации конечности (например, во время гражданской войны повреждение подколенной артерии приводило к 100% ампутации). Во время Второй мировой войны ремонт снизил показатель до 72%.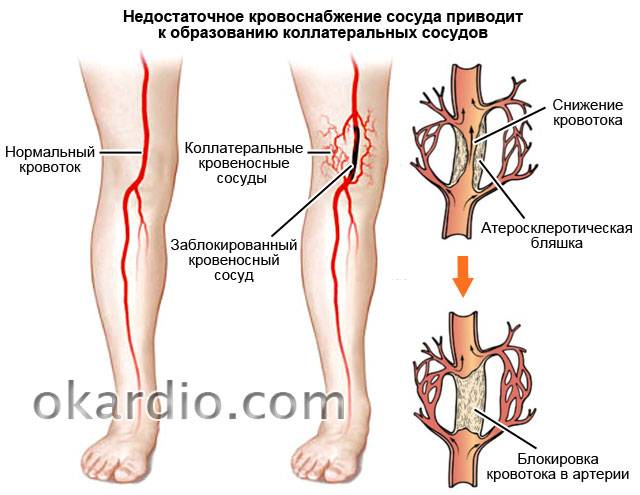 Во время Корейской войны политика обязательного хирургического исследования всех потенциальных сосудистых повреждений снизила частоту ампутаций до 32% при подколенных травмах. Политика выполнения артериографии при всех предполагаемых повреждениях сосудов в сочетании с развитием методов восстановления сосудов во время войны во Вьетнаме снизила частоту ампутаций при этих повреждениях до 15%.С современными методами диагностики и восстановления сосудов почти все эти повреждения могут быть реваскуляризированы, хотя сильно искалеченная конечность все же может потребовать ампутации.
Во время Корейской войны политика обязательного хирургического исследования всех потенциальных сосудистых повреждений снизила частоту ампутаций до 32% при подколенных травмах. Политика выполнения артериографии при всех предполагаемых повреждениях сосудов в сочетании с развитием методов восстановления сосудов во время войны во Вьетнаме снизила частоту ампутаций при этих повреждениях до 15%.С современными методами диагностики и восстановления сосудов почти все эти повреждения могут быть реваскуляризированы, хотя сильно искалеченная конечность все же может потребовать ампутации.
Основным принципом лечения крупных сосудистых повреждений является получение проксимального и дистального контроля над поврежденным сосудом перед входом в аневризму (5). На конечностях, как и на шее, контроль достигается с помощью стандартных методов воздействия на сосуды при растяжении (12, 13). В грудной клетке контроль повреждения сосудов зависит от правильного выбора разреза для торакотомии, поскольку разрез обеспечивает доступ к различным отделам грудных сосудов помимо доступа к сердцу.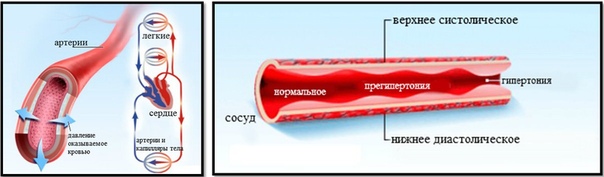 В брюшной полости основные сосуды располагаются в забрюшинном пространстве, поэтому экспозиция основана на оперативных маневрах, которые мобилизуют внутрибрюшинные органы от подлежащих забрюшинных структур (14, 15).
В брюшной полости основные сосуды располагаются в забрюшинном пространстве, поэтому экспозиция основана на оперативных маневрах, которые мобилизуют внутрибрюшинные органы от подлежащих забрюшинных структур (14, 15).
Любому пациенту с множественными системными травмами может потребоваться стабилизация их повреждений до лечения сосудистых повреждений, т.е. haemoperitonium может иметь преимущество перед этими повреждениями, но иногда повреждение сосудов может быть наиболее тяжелым или единственным повреждением, требующим лечения.Однако огнестрельное ранение сердца всегда имеет преимущество перед другими травмами, поскольку оно приводит к летальному исходу, если не принять своевременные меры. Хотя сосудистое повреждение может быть очевидным на основании наличия пульсирующей артериальной кровопотери из раны и наличия холодной, бледной конечности без пульса, у некоторых пациентов симптомы могут отсутствовать. Несмотря на все меры, перед лечащим хирургом может возникнуть диагностическая дилемма и сложная задача.
Исторические данные указывают на механизм и точное время травмы, поскольку ограничение времени тепловой ишемии гарантирует необходимое восстановление артериального повреждения в течение шести часов до возникновения необратимой ишемии.Профессия и рука пациента имеют значение, поскольку они иногда влияют на агрессивность хирургического подхода. Важно выявить сопутствующие заболевания, которые могут привести к осложнениям при заживлении ран, такие как заболевания периферических сосудов, сахарный диабет и синдром приобретенного иммунодефицита (СПИД), рак или прием иммунодепрессантов. Наконец, необходимо выявить наличие симптомов сниженного кровоснабжения, таких как боль, онемение или слабость, свидетельствующие о повреждении нерва, и парестезии.Пациенты, которые не могут достоверно предоставить анамнез или симптомы ишемии (например, интоксикация, повреждение спинного мозга или черепно-мозговая травма), представляют собой диагностическую проблему.
Обследование начинается с пальпации пульса, и обнаружение дефицита пульса является хотя и недостоверным признаком, но очень важным наводящим на размышления признаком и сигналом для дальнейшего исследования, а не для немедленной операции.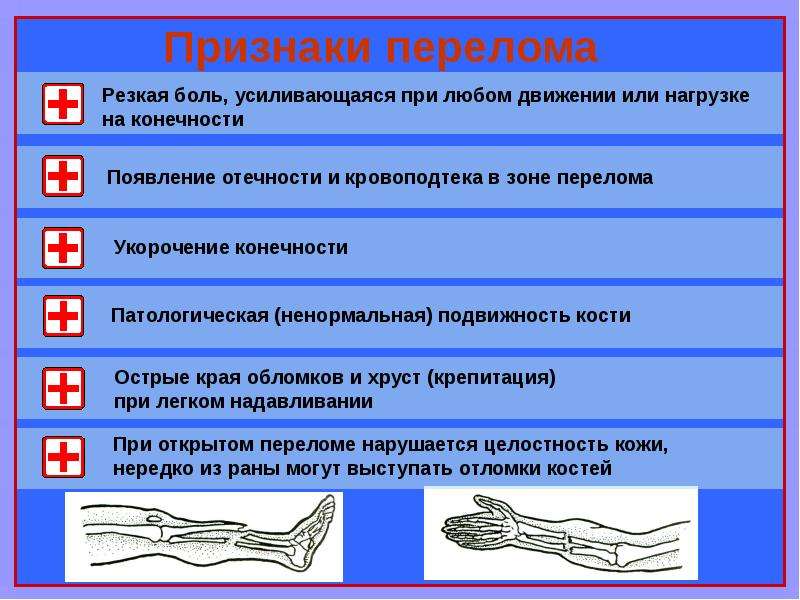 Ложноположительный дефицит пульса может возникать при шоке, сегментарном спазме сосудов, компрессионных повязках и гипсовых повязках, врожденном отсутствии пульса и ранее существовавших сосудистых заболеваниях.Ложноотрицательные признаки обнаруживаются при сильном установлении залога. На основании клинического обследования пациенту относят к одной из трех категорий, которые определяют план диагностики и лечения.
Ложноположительный дефицит пульса может возникать при шоке, сегментарном спазме сосудов, компрессионных повязках и гипсовых повязках, врожденном отсутствии пульса и ранее существовавших сосудистых заболеваниях.Ложноотрицательные признаки обнаруживаются при сильном установлении залога. На основании клинического обследования пациенту относят к одной из трех категорий, которые определяют план диагностики и лечения.
Категория 1 (Тяжелые признаки): К ним относятся боль, бледность, отсутствие пульса, парестезии, паралич, пульсирующее кровотечение и большая или расширяющаяся гематома. Если у пациента проявляются эти признаки, вероятность повреждения сосудов у него > 90 %.
Категория 2 (мягкие признаки): К ним относятся относительно уменьшенный, но ощутимый пульс, нерасширяющаяся гематома и повреждение периферических нервов; У 30-35% этих пациентов будет повреждение сосудов.
Категория 3 (бессимптомная, высокий риск): К ним относятся проникающие раны в пределах 1 см от основных областей сосудисто-нервного пучка (например, подмышечной, бедренной и сонной артерии), а также вывихи коленного сустава или переломы длинных костей с тяжелым смещением.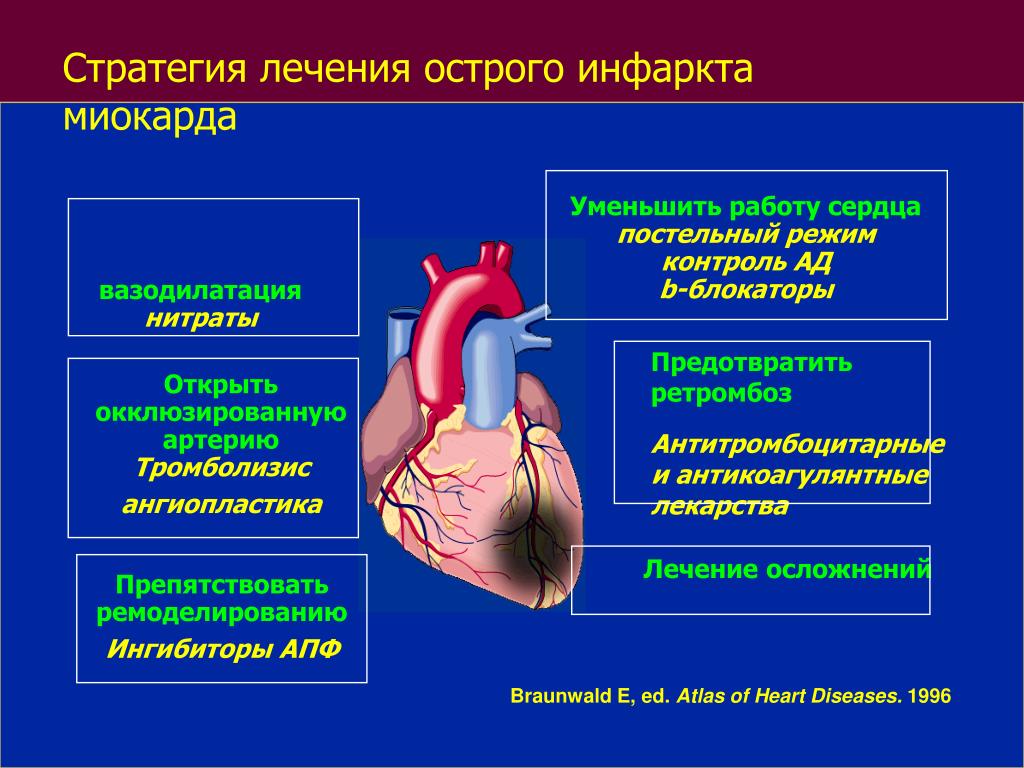 До 15-20% этих пациентов имеют сосудистое повреждение.
До 15-20% этих пациентов имеют сосудистое повреждение.
Сосудистые травмы: тенденции в лечении
Abstract
Сосудистые травмы представляют собой серьезную проблему для резидентов скорой помощи, поскольку эти травмы требуют срочного вмешательства для предотвращения смерти или потери конечностей.Иногда серьезное сосудистое повреждение проявляется едва уловимыми или скрытыми признаками или симптомами. Через несколько недель или месяцев после первичного повреждения у пациента могут появиться симптомы сосудистой недостаточности, эмболизации, псевдоаневризмы, артериовенозной фистулы и т. д. следует рассматривать у пациентов со смещенными переломами длинных костей, размозжением, длительной иммобилизацией в фиксированном положении тугими гипсовыми повязками или повязками и различными инвазивными процедурами.ятрогенные повреждения сосудов в большинстве серий составляют около 10% случаев; однако заболеваемость имеет тенденцию к увеличению, поскольку рутинно выполняется больше эндоваскулярных процедур, таких как ангиопластика и катетеризация сердца.
Гражданская травма чаще наблюдается у молодых мужчин. Однако это может произойти в любом возрасте из-за дорожно-транспортных происшествий, огнестрельного оружия, взрывов бомб и диагностических процедур. В большинстве случаев гражданская травма вызывает меньшее повреждение тканей. В Кашмирской долине наблюдается эпидемия сосудистых повреждений из-за проблем с правопорядком в последние два десятилетия.В обзоре подробно рассматривается эта тема.
Ключевые слова: Травмы сосудистой системы, подкожная вена, анастомоз
1. Введение
Кашмирская долина, будучи зоной конфликта, в которой существуют проблемы с правопорядком, более чем за два десятилетия стала свидетелем эпидемии сосудистых травм. Наша больница (Институт медицинских наук Шер-и-Кашмир) является единственной больницей третичного уровня, где имеются средства для лечения сосудистых травм, обслуживающие население более десяти миллионов человек (1-4).
Большинство травм сосудов в военных конфликтах происходит от осколков баллистического оружия, такого как артиллерия, ракеты, гранаты и бомбы. Развитие высокоскоростного оружия (например, артиллерии) вызывает массивное разрушение тканей, превышающее таковое от предыдущего военного оружия такого же размера. Экспериментальные исследования высокоскоростных ранений показывают, что временная полость может быть создана почти в тридцать раз больше, чем постоянный остаточный тракт (5). Этот временный кавитационный эффект повреждает ткани за пределами фактического пути снаряда.
Развитие высокоскоростного оружия (например, артиллерии) вызывает массивное разрушение тканей, превышающее таковое от предыдущего военного оружия такого же размера. Экспериментальные исследования высокоскоростных ранений показывают, что временная полость может быть создана почти в тридцать раз больше, чем постоянный остаточный тракт (5). Этот временный кавитационный эффект повреждает ткани за пределами фактического пути снаряда.
травмы сосудов можно разделить на следующие группы:
• Спазм
• Тромбоз
• Участок / интимный клапан
• Зарубка / переход
• AV (Arteriovenous) Fistula
• Aneurysm и Pseudoaneurysm
• Артериал emboli
Спазм: Травма сосуда приводит к спазму локализованной сосудистой сети, что вызывает снижение дистального кровотока и может привести к дистальным функциональным повреждениям.
Тромбоз: Любое повреждение интимы артерии сопровождается тромбозом в течение определенного периода времени, который вызывает частичную или полную окклюзию сосуда или может привести к обратимому сегментарному спазму.
Ушиб/Интимальный лоскут: Ударная сила или чрезмерное растяжение вызывают разрыв интимы сосуда. Небольшой лоскут <5 мм может незначительно перекрывать кровоток, но может стать очагом тромбоза. Большой лоскут может выпячиваться в просвет сосуда, вызывая частичную окклюзию и симптомы дистальной ишемии.
Разрыв/пересечение: Разрыв и разрез чаще всего возникают в результате тупой травмы, а также при попадании высокоскоростных метательных снарядов, которые вызывают неравномерные разрывы сосуда или потерю сегментов, связанную с повреждением других тканей.Чисто пересеченная артерия часто будет сужаться и втягиваться, ограничивая кровопотерю. Продольный или сильно разорванный сосуд не может ограничить кровопотерю и может привести к большей кровопотере. Этот тип травмы составляет 80-85% случаев (1).
Артериовенозная фистула: Повреждение артерии и прилежащей вены может привести к развитию соединения между ними, когда поток высокого давления отклоняется в сторону низкого давления (артерия-вена), что приводит к неадекватной перфузии и растяжению вен. Любая атриовентрикулярная фистула в центральных сосудах вызывает застойную сердечную недостаточность и проявляется обычно поздно.
Любая атриовентрикулярная фистула в центральных сосудах вызывает застойную сердечную недостаточность и проявляется обычно поздно.
Аневризма и псевдоаневризма: Истинная аневризма содержит все слои сосудистой стенки (интима, медиум и адвентиция) и редко может быть вызвана травмой. Чаще псевдоаневризма формируется после травмы.
Когда кровотечение из поврежденного сосуда останавливается окружающей фасцией и другими мягкими тканями, оно постепенно инкапсулируется фиброзной тканью, сходной по всем свойствам с адвентицией.Все это приводит к тонкостенной капсуле, которая продолжает расширяться из-за более высокого артериального давления, образуя пальпируемую пульсирующую массу, которая может сдавливать окружающие структуры, вызывая невропатию, коллапс вен, эрозию кости или эмболизацию дистальных сосудов, вызывая ишемию. Остановка кровотечения после повреждения сосудов была главной заботой человека с каменного века; для остановки кровотечения использовались различные средства, такие как компрессия, горячее железо, холод и перевязка.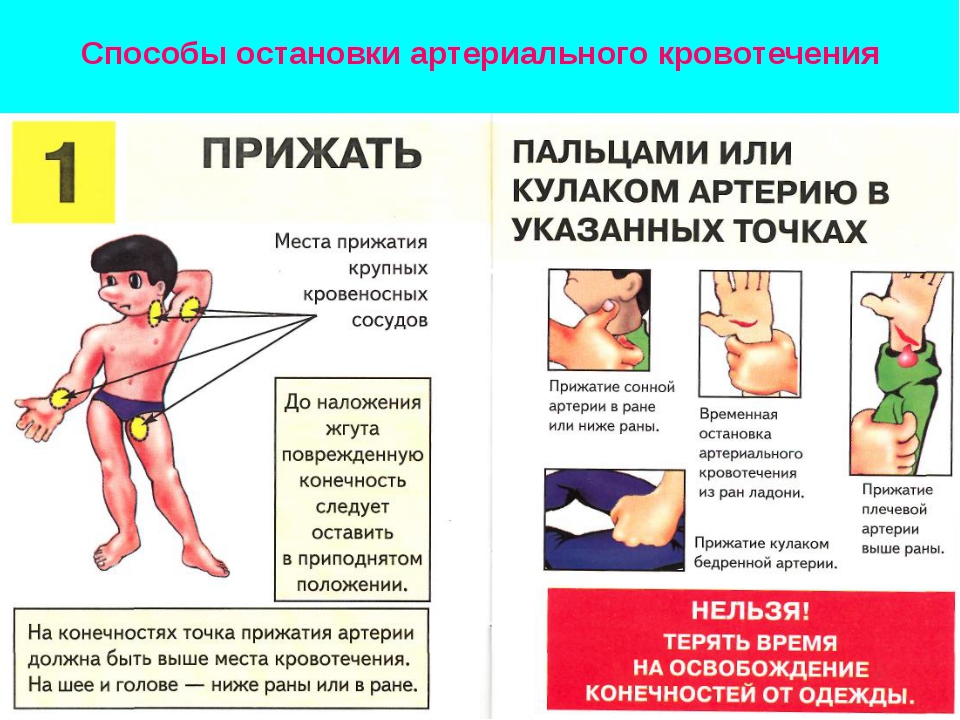
После первоначального вклада Цельса, Галена и их современников использование лигатуры было практически забыто почти на 1200 лет.В Средние века прижигание использовалось почти исключительно для остановки кровотечения. Джером Брауншвейгский, армейский хирург, фактически опередил Амбруаза Паре в описании использования лигатуры как лучшего способа остановить кровотечение. Амбруаз Паре (6), имея большой опыт в хирургии травм, особенно на поле боя, твердо установил использование лигатур для остановки кровотечения из открытых сосудов. В 1952 году он сделал первую ампутацию выше демаркационной линии, которая ранее была сделана ниже демаркационной линии.В семнадцатом веке монументальный вклад Гарвея, описывающий кровообращение, очень помог понять сосудистые повреждения. В 1674 г. военный хирург по имени Морель вставил в повязку стержень и скручивал ее до тех пор, пока артериальный кровоток не прекращался (7). Вскоре после этого стали использовать винтовой жгут. В 1873 году Фридрих фон Эсмарх представил свой эластичный жгут для оказания первой помощи на поле боя. Его открытие позволило хирургам выборочно оперировать конечности в сухом бескровном поле.
Его открытие позволило хирургам выборочно оперировать конечности в сухом бескровном поле.
Первая успешная перевязка общей сонной артерии для остановки кровотечения была выполнена в 1803 г. Флемингом; но об этом сообщил только 14 лет спустя Coley (1817), потому что Флеминг умер вскоре после операции (8). Слуга попытался покончить жизнь самоубийством, перерезав себе горло. Когда Флеминг увидел пациента, который выглядел обескровленным, пульса не было, а зрачки были расширены. Удалось перевязать две верхние щитовидные артерии и одну внутреннюю яремную вену.Отмечали разрыв наружного мышечного слоя сонной артерии, а также разрыв трахеи между щитовидным и перстневидным хрящами. Это позволило дренажу из раны попасть в трахею, спровоцировав сильные приступы кашля, хотя состояние пациента, казалось, улучшалось. Примерно через неделю после травмы Флеминг писал: « Вечером 17-го, во время сильного приступа кашля, артерия лопнула, и мой бедный пациент в одно мгновение залился кровью».«В этой ужасной ситуации я пришел к выводу, что мне остается сделать только один шаг с надеждой на успех; в основном, чтобы перерезать и перевязать сонную артерию ниже раны.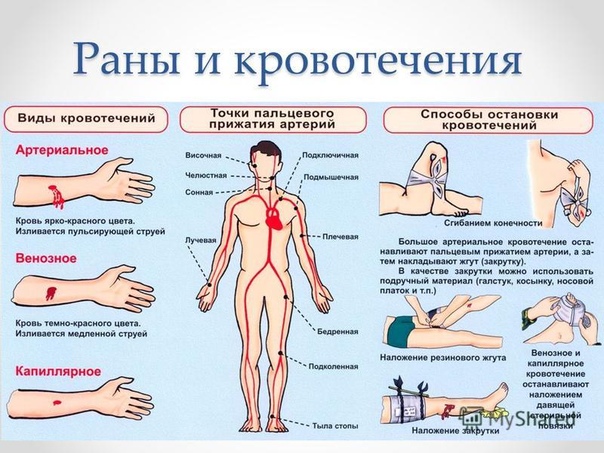 Я никогда не слышал о такой операции; но полагал, что в данном случае его последствия могут быть менее грозными, чем у человека, не пораженного кровотечением» (8).
Я никогда не слышал о такой операции; но полагал, что в данном случае его последствия могут быть менее грозными, чем у человека, не пораженного кровотечением» (8).
Рана быстро зажила после перевязки сонной артерии, и пациент выздоровел. Важность коллатерального кровообращения для сохранения жизнеспособности конечности после перевязки была хорошо известна на протяжении веков.Тот факт, что для установления этого обращения требовалось время, был общепризнанным. Halsted (1912) сообщил об излечении подвздошно-бедренной аневризмы путем наложения алюминиевой ленты на проксимальную артерию без серьезного нарушения кровообращения или функции нижней конечности (9). Именно Алекс Карел выполнил первый успешный анастомоз конец в конец в 1896 году. Десять лет спустя Гойанес использовал венозный трансплантат для перекрытия дефекта артерии в 1906 году. сопровождается улучшением анестезии, переливанием крови и применением антибиотиков.Пожалуй, самым важным была быстрая эвакуация и реанимация раненых. Кроме того, полное понимание важности хирургической обработки раны, отсроченного первичного закрытия и назначения антибиотиков значительно снизило опасность инфицирования (10, 11).
Кроме того, полное понимание важности хирургической обработки раны, отсроченного первичного закрытия и назначения антибиотиков значительно снизило опасность инфицирования (10, 11).
Исторически сложилось так, что большинство пациентов с серьезным повреждением артерий не выживали достаточно долго, чтобы обратиться к врачу; у тех, кто это делал, обычно были легкие ранения. С развитием системы здравоохранения многие пациенты с тяжелыми травмами теперь поступают в больницу (даже с очень серьезными сосудистыми повреждениями, например.грамм. повреждение сонных артерий) и спасаются. Восстановление сосудов было впервые успешно выполнено в начале 1900-х годов. Обычный хирургический подход к серьезному повреждению сосудов заключался в простой перевязке сосуда и ампутации конечности (например, во время гражданской войны повреждение подколенной артерии приводило к 100% ампутации). Во время Второй мировой войны ремонт снизил показатель до 72%. Во время Корейской войны политика обязательного хирургического исследования всех потенциальных сосудистых повреждений снизила частоту ампутаций до 32% при подколенных травмах. Политика выполнения артериографии при всех предполагаемых повреждениях сосудов в сочетании с развитием методов восстановления сосудов во время войны во Вьетнаме снизила частоту ампутаций при этих повреждениях до 15%. С современными методами диагностики и восстановления сосудов почти все эти повреждения могут быть реваскуляризированы, хотя сильно искалеченная конечность все же может потребовать ампутации.
Политика выполнения артериографии при всех предполагаемых повреждениях сосудов в сочетании с развитием методов восстановления сосудов во время войны во Вьетнаме снизила частоту ампутаций при этих повреждениях до 15%. С современными методами диагностики и восстановления сосудов почти все эти повреждения могут быть реваскуляризированы, хотя сильно искалеченная конечность все же может потребовать ампутации.
Основным принципом лечения крупных сосудистых повреждений является получение проксимального и дистального контроля над поврежденным сосудом перед входом в аневризму (5).На конечностях, как и на шее, контроль достигается с помощью стандартных методов воздействия на сосуды при растяжении (12, 13). В грудной клетке контроль повреждения сосудов зависит от правильного выбора разреза для торакотомии, поскольку разрез обеспечивает доступ к различным отделам грудных сосудов помимо доступа к сердцу. В брюшной полости основные сосуды располагаются в забрюшинном пространстве, поэтому экспозиция основана на оперативных маневрах, которые мобилизуют внутрибрюшинные органы от подлежащих забрюшинных структур (14, 15).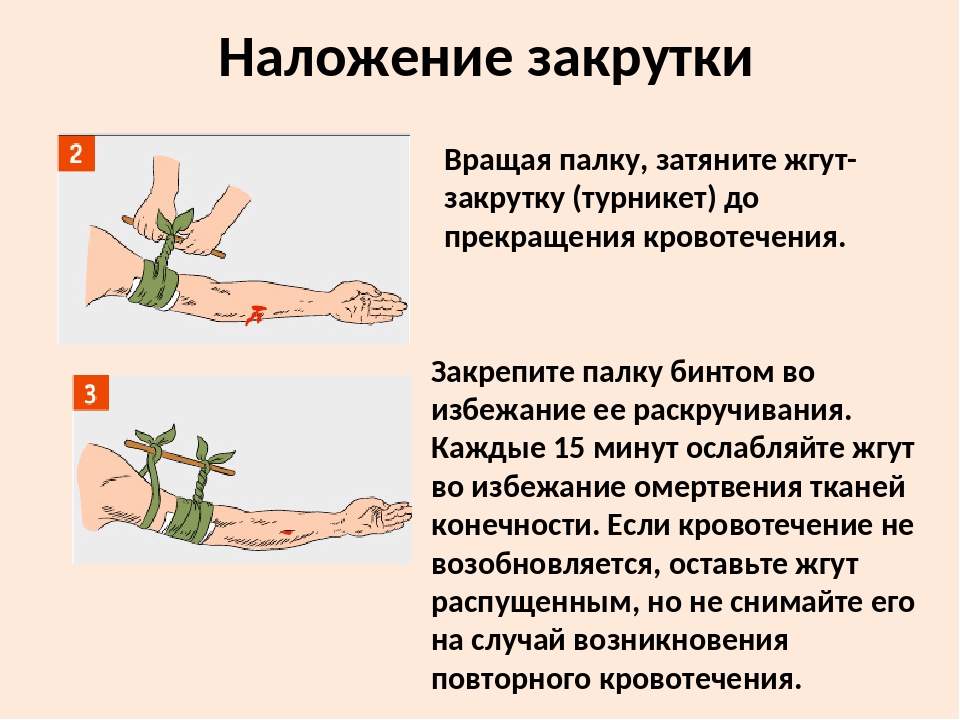
Любому пациенту с множественными системными травмами может потребоваться стабилизация их повреждений до лечения сосудистых повреждений, т.е. haemoperitonium может иметь преимущество перед этими повреждениями, но иногда повреждение сосудов может быть наиболее тяжелым или единственным повреждением, требующим лечения. Однако огнестрельное ранение сердца всегда имеет преимущество перед другими травмами, поскольку оно приводит к летальному исходу, если не принять своевременные меры. Хотя сосудистое повреждение может быть очевидным на основании наличия пульсирующей артериальной кровопотери из раны и наличия холодной, бледной конечности без пульса, у некоторых пациентов симптомы могут отсутствовать.Несмотря на все меры, перед лечащим хирургом может возникнуть диагностическая дилемма и сложная задача.
Исторические данные указывают на механизм и точное время травмы, поскольку ограничение времени тепловой ишемии гарантирует необходимое восстановление артериального повреждения в течение шести часов до возникновения необратимой ишемии. Профессия и рука пациента имеют значение, поскольку они иногда влияют на агрессивность хирургического подхода. Важно выявить сопутствующие заболевания, которые могут привести к осложнениям при заживлении ран, такие как заболевания периферических сосудов, сахарный диабет и синдром приобретенного иммунодефицита (СПИД), рак или прием иммунодепрессантов.Наконец, необходимо выявить наличие симптомов сниженного кровоснабжения, таких как боль, онемение или слабость, свидетельствующие о повреждении нерва, и парестезии. Пациенты, которые не могут достоверно предоставить анамнез или симптомы ишемии (например, интоксикация, повреждение спинного мозга или черепно-мозговая травма), представляют собой диагностическую проблему.
Профессия и рука пациента имеют значение, поскольку они иногда влияют на агрессивность хирургического подхода. Важно выявить сопутствующие заболевания, которые могут привести к осложнениям при заживлении ран, такие как заболевания периферических сосудов, сахарный диабет и синдром приобретенного иммунодефицита (СПИД), рак или прием иммунодепрессантов.Наконец, необходимо выявить наличие симптомов сниженного кровоснабжения, таких как боль, онемение или слабость, свидетельствующие о повреждении нерва, и парестезии. Пациенты, которые не могут достоверно предоставить анамнез или симптомы ишемии (например, интоксикация, повреждение спинного мозга или черепно-мозговая травма), представляют собой диагностическую проблему.
Обследование начинается с пальпации пульса, и обнаружение дефицита пульса является хотя и недостоверным признаком, но очень важным наводящим на размышления признаком и сигналом для дальнейшего исследования, а не для немедленной операции.Ложноположительный дефицит пульса может возникать при шоке, сегментарном спазме сосудов, компрессионных повязках и гипсовых повязках, врожденном отсутствии пульса и ранее существовавших сосудистых заболеваниях. Ложноотрицательные признаки обнаруживаются при сильном установлении залога. На основании клинического обследования пациенту относят к одной из трех категорий, которые определяют план диагностики и лечения.
Ложноотрицательные признаки обнаруживаются при сильном установлении залога. На основании клинического обследования пациенту относят к одной из трех категорий, которые определяют план диагностики и лечения.
Категория 1 (Тяжелые признаки): К ним относятся боль, бледность, отсутствие пульса, парестезии, паралич, пульсирующее кровотечение и большая или расширяющаяся гематома.Если у пациента проявляются эти признаки, вероятность повреждения сосудов у него > 90 %.
Категория 2 (мягкие признаки): К ним относятся относительно уменьшенный, но ощутимый пульс, нерасширяющаяся гематома и повреждение периферических нервов; У 30-35% этих пациентов будет повреждение сосудов.
Категория 3 (бессимптомная, высокий риск): К ним относятся проникающие раны в пределах 1 см от основных областей сосудисто-нервного пучка (например, подмышечной, бедренной и сонной артерии), а также вывихи коленного сустава или переломы длинных костей с тяжелым смещением.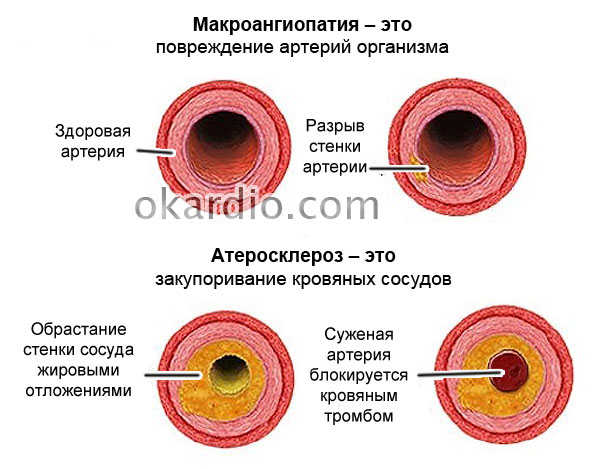 До 15-20% этих пациентов имеют сосудистое повреждение.
До 15-20% этих пациентов имеют сосудистое повреждение.
Сосудистые травмы: тенденции в лечении
Abstract
Сосудистые травмы представляют собой серьезную проблему для резидентов скорой помощи, поскольку эти травмы требуют срочного вмешательства для предотвращения смерти или потери конечностей. Иногда серьезное сосудистое повреждение проявляется едва уловимыми или скрытыми признаками или симптомами. У пациента через несколько недель или месяцев после первичной травмы могут появиться симптомы сосудистой недостаточности, эмболизации, псевдоаневризмы, артериовенозной фистулы и т. д.Хотя большинство повреждений сосудов вызвано проникающими травмами от огнестрельных ранений, колото-резаными или взрывными ранениями, возможность повреждения сосудов необходимо учитывать у пациентов со смещенными переломами длинных костей, размозжением, длительной иммобилизацией в фиксированном положении тугими гипсовыми повязками. или повязки и различные инвазивные процедуры. ятрогенные повреждения сосудов в большинстве серий составляют около 10% случаев; однако заболеваемость имеет тенденцию к увеличению, поскольку рутинно выполняется больше эндоваскулярных процедур, таких как ангиопластика и катетеризация сердца.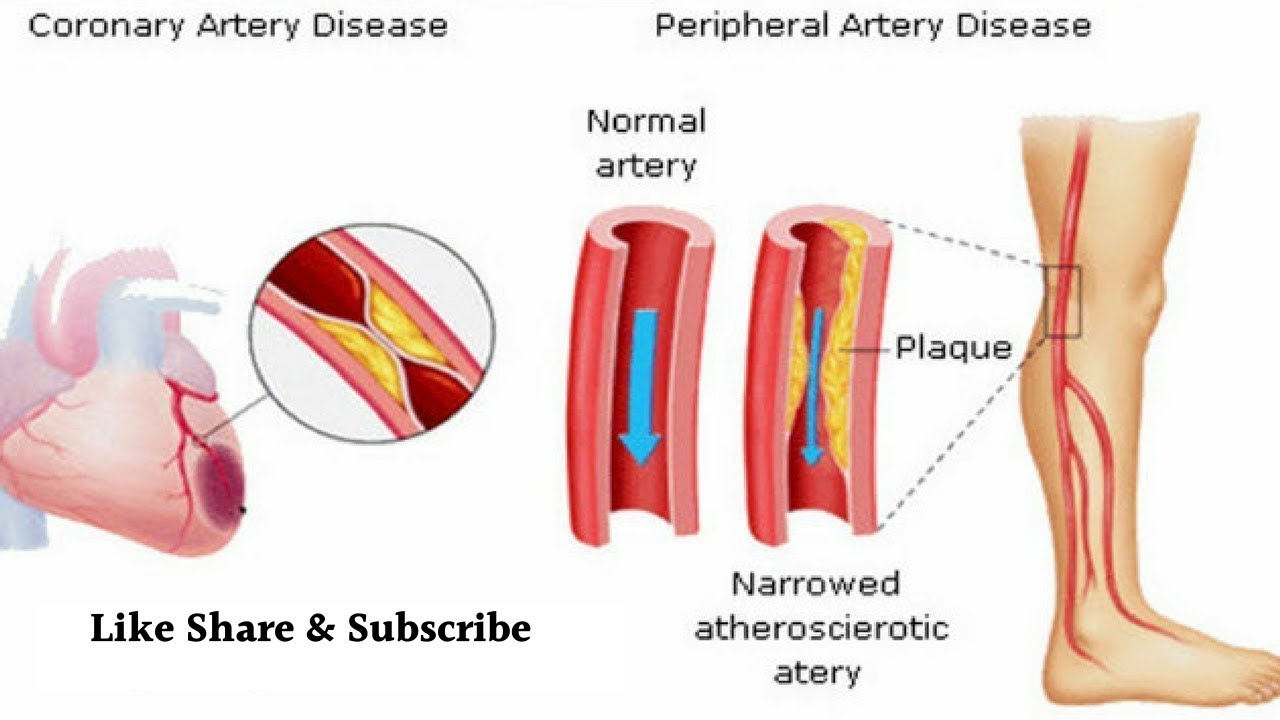
Гражданская травма чаще наблюдается у молодых мужчин. Однако это может произойти в любом возрасте из-за дорожно-транспортных происшествий, огнестрельного оружия, взрывов бомб и диагностических процедур. В большинстве случаев гражданская травма вызывает меньшее повреждение тканей. В Кашмирской долине наблюдается эпидемия сосудистых повреждений из-за проблем с правопорядком в последние два десятилетия. В обзоре подробно рассматривается эта тема.
Ключевые слова: Травмы сосудистой системы, подкожные вены, анастомозы
1.Введение
Кашмирская долина, являющаяся зоной конфликта, в которой существуют проблемы с правопорядком для руды, более чем за два десятилетия стала свидетелем эпидемии сосудистых повреждений. Наша больница (Институт медицинских наук Шер-и-Кашмир) является единственной больницей третичного уровня, где имеются средства для лечения сосудистых травм, обслуживающие население более десяти миллионов человек (1-4).
Большинство травм сосудов в военных конфликтах происходит от осколков баллистического оружия, такого как артиллерия, ракеты, гранаты и бомбы. Развитие высокоскоростного оружия (например, артиллерии) вызывает массивное разрушение тканей, превышающее таковое от предыдущего военного оружия такого же размера. Экспериментальные исследования высокоскоростных ранений показывают, что временная полость может быть создана почти в тридцать раз больше, чем постоянный остаточный тракт (5). Этот временный кавитационный эффект повреждает ткани за пределами фактического пути снаряда.
Развитие высокоскоростного оружия (например, артиллерии) вызывает массивное разрушение тканей, превышающее таковое от предыдущего военного оружия такого же размера. Экспериментальные исследования высокоскоростных ранений показывают, что временная полость может быть создана почти в тридцать раз больше, чем постоянный остаточный тракт (5). Этот временный кавитационный эффект повреждает ткани за пределами фактического пути снаряда.
травмы сосудов можно разделить на следующие группы:
• Спазм
• Тромбоз
• Участок / интимный клапан
• Зарубка / переход
• AV (Arteriovenous) Fistula
• Aneurysm и Pseudoaneurysm
• Артериал emboli
Спазм: Травма сосуда приводит к спазму локализованной сосудистой сети, что вызывает снижение дистального кровотока и может привести к дистальным функциональным повреждениям.
Тромбоз: Любое повреждение интимы артерии сопровождается тромбозом в течение определенного периода времени, который вызывает частичную или полную окклюзию сосуда или может привести к обратимому сегментарному спазму.
Ушиб/Интимальный лоскут: Ударная сила или чрезмерное растяжение вызывают разрыв интимы сосуда. Небольшой лоскут <5 мм может незначительно перекрывать кровоток, но может стать очагом тромбоза. Большой лоскут может выпячиваться в просвет сосуда, вызывая частичную окклюзию и симптомы дистальной ишемии.
Разрыв/пересечение: Разрыв и разрез чаще всего возникают в результате тупой травмы, а также при попадании высокоскоростных метательных снарядов, которые вызывают неравномерные разрывы сосуда или потерю сегментов, связанную с повреждением других тканей. Чисто пересеченная артерия часто будет сужаться и втягиваться, ограничивая кровопотерю. Продольный или сильно разорванный сосуд не может ограничить кровопотерю и может привести к большей кровопотере. Этот тип травмы составляет 80-85% случаев (1).
Артериовенозная фистула: Повреждение артерии и прилежащей вены может привести к развитию соединения между ними, когда поток высокого давления отклоняется в сторону низкого давления (артерия-вена), что приводит к неадекватной перфузии и растяжению вен. Любая атриовентрикулярная фистула в центральных сосудах вызывает застойную сердечную недостаточность и проявляется обычно поздно.
Любая атриовентрикулярная фистула в центральных сосудах вызывает застойную сердечную недостаточность и проявляется обычно поздно.
Аневризма и псевдоаневризма: Истинная аневризма содержит все слои сосудистой стенки (интима, медиум и адвентиция) и редко может быть вызвана травмой.Чаще псевдоаневризма формируется после травмы.
Когда кровотечение из поврежденного сосуда останавливается окружающей фасцией и другими мягкими тканями, оно постепенно инкапсулируется фиброзной тканью, сходной по всем свойствам с адвентицией. Все это приводит к тонкостенной капсуле, которая продолжает расширяться из-за более высокого артериального давления, образуя пальпируемую пульсирующую массу, которая может сдавливать окружающие структуры, вызывая невропатию, коллапс вен, эрозию кости или эмболизацию дистальных сосудов, вызывая ишемию.Остановка кровотечения после повреждения сосудов была главной заботой человека с каменного века; для остановки кровотечения использовались различные средства, такие как компрессия, горячее железо, холод и перевязка.
После первоначального вклада Цельса, Галена и их современников использование лигатуры было практически забыто почти на 1200 лет. В Средние века прижигание использовалось почти исключительно для остановки кровотечения. Джером Брауншвейгский, армейский хирург, фактически опередил Амбруаза Паре в описании использования лигатуры как лучшего способа остановить кровотечение.Амбруаз Паре (6), имея большой опыт в хирургии травм, особенно на поле боя, твердо установил использование лигатур для остановки кровотечения из открытых сосудов. В 1952 году он сделал первую ампутацию выше демаркационной линии, которая ранее была сделана ниже демаркационной линии. В семнадцатом веке монументальный вклад Гарвея, описывающий кровообращение, очень помог понять сосудистые повреждения. В 1674 г. военный хирург по имени Морель вставил в повязку палочку и закручивал ее до тех пор, пока артериальный кровоток не остановился (7).Вскоре после этого стали использовать винтовой жгут. В 1873 году Фридрих фон Эсмарх представил свой эластичный жгут для оказания первой помощи на поле боя. Его открытие позволило хирургам выборочно оперировать конечности в сухом бескровном поле.
Его открытие позволило хирургам выборочно оперировать конечности в сухом бескровном поле.
Первая успешная перевязка общей сонной артерии для остановки кровотечения была выполнена в 1803 г. Флемингом; но об этом сообщил только 14 лет спустя Coley (1817), потому что Флеминг умер вскоре после операции (8).Слуга попытался покончить жизнь самоубийством, перерезав себе горло. Когда Флеминг увидел пациента, который выглядел обескровленным, пульса не было, а зрачки были расширены. Удалось перевязать две верхние щитовидные артерии и одну внутреннюю яремную вену. Отмечали разрыв наружного мышечного слоя сонной артерии, а также разрыв трахеи между щитовидным и перстневидным хрящами. Это позволило дренажу из раны попасть в трахею, спровоцировав сильные приступы кашля, хотя состояние пациента, казалось, улучшалось.Примерно через неделю после травмы Флеминг писал: « Вечером 17-го, во время сильного приступа кашля, артерия лопнула, и мой бедный пациент в одно мгновение залился кровью». «В этой ужасной ситуации я пришел к выводу, что мне остается сделать только один шаг с надеждой на успех; в основном, чтобы перерезать и перевязать сонную артерию ниже раны.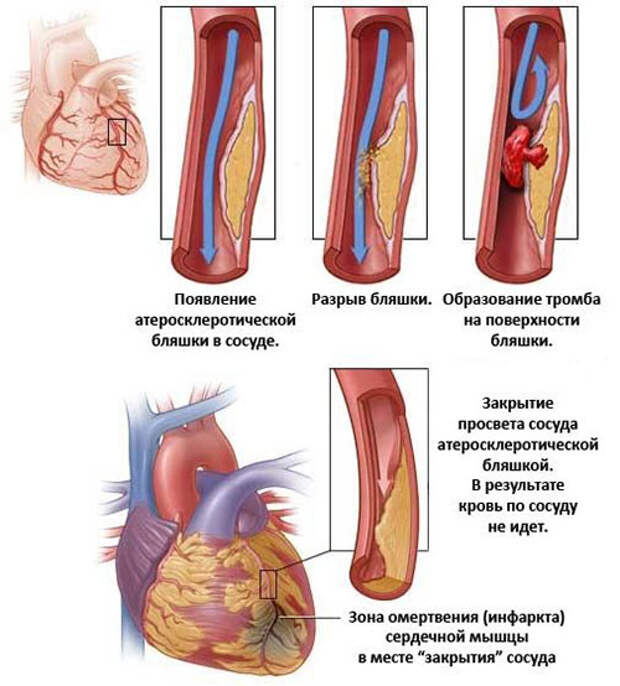 Я никогда не слышал о такой операции; но полагал, что в данном случае его последствия могут быть менее грозными, чем у человека, не пораженного кровотечением» (8).
Я никогда не слышал о такой операции; но полагал, что в данном случае его последствия могут быть менее грозными, чем у человека, не пораженного кровотечением» (8).
Рана быстро зажила после перевязки сонной артерии, и пациент выздоровел. Важность коллатерального кровообращения для сохранения жизнеспособности конечности после перевязки была хорошо известна на протяжении веков. Тот факт, что для установления этого обращения требовалось время, был общепризнанным. Halsted (1912) сообщил об излечении подвздошно-бедренной аневризмы путем наложения алюминиевой ленты на проксимальный отдел артерии без серьезного нарушения кровообращения или функции нижней конечности (9).Именно Алекс Карел выполнил первый успешный анастомоз «конец в конец» в 1896 году. Десять лет спустя Гойанес в 1906 году использовал венозный трансплантат для перекрытия дефекта артерии. опыт Второй мировой войны, в связи с существенным прогрессом в технике операций на сосудах, сопровождавшимся совершенствованием анестезии, переливания крови и применением антибиотиков. Пожалуй, самым важным была быстрая эвакуация и реанимация раненых.Кроме того, полное понимание важности хирургической обработки раны, отсроченного первичного закрытия и назначения антибиотиков значительно снизило опасность инфицирования (10, 11).
Пожалуй, самым важным была быстрая эвакуация и реанимация раненых.Кроме того, полное понимание важности хирургической обработки раны, отсроченного первичного закрытия и назначения антибиотиков значительно снизило опасность инфицирования (10, 11).
Исторически сложилось так, что большинство пациентов с серьезным повреждением артерий не выживали достаточно долго, чтобы обратиться к врачу; у тех, кто это делал, обычно были легкие ранения. С развитием системы здравоохранения многие пациенты с серьезными травмами теперь поступают в больницу (даже с очень серьезными сосудистыми повреждениями, например, с повреждением сонных артерий), и их спасают.Восстановление сосудов было впервые успешно выполнено в начале 1900-х годов. Обычный хирургический подход к серьезному повреждению сосудов заключался в простой перевязке сосуда и ампутации конечности (например, во время гражданской войны повреждение подколенной артерии приводило к 100% ампутации). Во время Второй мировой войны ремонт снизил показатель до 72%. Во время Корейской войны политика обязательного хирургического исследования всех потенциальных сосудистых повреждений снизила частоту ампутаций до 32% при подколенных травмах. Политика выполнения артериографии при всех предполагаемых повреждениях сосудов в сочетании с развитием методов восстановления сосудов во время войны во Вьетнаме снизила частоту ампутаций при этих повреждениях до 15%.С современными методами диагностики и восстановления сосудов почти все эти повреждения могут быть реваскуляризированы, хотя сильно искалеченная конечность все же может потребовать ампутации.
Во время Корейской войны политика обязательного хирургического исследования всех потенциальных сосудистых повреждений снизила частоту ампутаций до 32% при подколенных травмах. Политика выполнения артериографии при всех предполагаемых повреждениях сосудов в сочетании с развитием методов восстановления сосудов во время войны во Вьетнаме снизила частоту ампутаций при этих повреждениях до 15%.С современными методами диагностики и восстановления сосудов почти все эти повреждения могут быть реваскуляризированы, хотя сильно искалеченная конечность все же может потребовать ампутации.
Основным принципом лечения крупных сосудистых повреждений является получение проксимального и дистального контроля над поврежденным сосудом перед входом в аневризму (5). На конечностях, как и на шее, контроль достигается с помощью стандартных методов воздействия на сосуды при растяжении (12, 13). В грудной клетке контроль повреждения сосудов зависит от правильного выбора разреза для торакотомии, поскольку разрез обеспечивает доступ к различным отделам грудных сосудов помимо доступа к сердцу. В брюшной полости основные сосуды располагаются в забрюшинном пространстве, поэтому экспозиция основана на оперативных маневрах, которые мобилизуют внутрибрюшинные органы от подлежащих забрюшинных структур (14, 15).
В брюшной полости основные сосуды располагаются в забрюшинном пространстве, поэтому экспозиция основана на оперативных маневрах, которые мобилизуют внутрибрюшинные органы от подлежащих забрюшинных структур (14, 15).
Любому пациенту с множественными системными травмами может потребоваться стабилизация их повреждений до лечения сосудистых повреждений, т.е. haemoperitonium может иметь преимущество перед этими повреждениями, но иногда повреждение сосудов может быть наиболее тяжелым или единственным повреждением, требующим лечения.Однако огнестрельное ранение сердца всегда имеет преимущество перед другими травмами, поскольку оно приводит к летальному исходу, если не принять своевременные меры. Хотя сосудистое повреждение может быть очевидным на основании наличия пульсирующей артериальной кровопотери из раны и наличия холодной, бледной конечности без пульса, у некоторых пациентов симптомы могут отсутствовать. Несмотря на все меры, перед лечащим хирургом может возникнуть диагностическая дилемма и сложная задача.
Исторические данные указывают на механизм и точное время травмы, поскольку ограничение времени тепловой ишемии гарантирует необходимое восстановление артериального повреждения в течение шести часов до возникновения необратимой ишемии.Профессия и рука пациента имеют значение, поскольку они иногда влияют на агрессивность хирургического подхода. Важно выявить сопутствующие заболевания, которые могут привести к осложнениям при заживлении ран, такие как заболевания периферических сосудов, сахарный диабет и синдром приобретенного иммунодефицита (СПИД), рак или прием иммунодепрессантов. Наконец, необходимо выявить наличие симптомов сниженного кровоснабжения, таких как боль, онемение или слабость, свидетельствующие о повреждении нерва, и парестезии.Пациенты, которые не могут достоверно предоставить анамнез или симптомы ишемии (например, интоксикация, повреждение спинного мозга или черепно-мозговая травма), представляют собой диагностическую проблему.
Обследование начинается с пальпации пульса, и обнаружение дефицита пульса является хотя и недостоверным признаком, но очень важным наводящим на размышления признаком и сигналом для дальнейшего исследования, а не для немедленной операции. Ложноположительный дефицит пульса может возникать при шоке, сегментарном спазме сосудов, компрессионных повязках и гипсовых повязках, врожденном отсутствии пульса и ранее существовавших сосудистых заболеваниях.Ложноотрицательные признаки обнаруживаются при сильном установлении залога. На основании клинического обследования пациенту относят к одной из трех категорий, которые определяют план диагностики и лечения.
Ложноположительный дефицит пульса может возникать при шоке, сегментарном спазме сосудов, компрессионных повязках и гипсовых повязках, врожденном отсутствии пульса и ранее существовавших сосудистых заболеваниях.Ложноотрицательные признаки обнаруживаются при сильном установлении залога. На основании клинического обследования пациенту относят к одной из трех категорий, которые определяют план диагностики и лечения.
Категория 1 (Тяжелые признаки): К ним относятся боль, бледность, отсутствие пульса, парестезии, паралич, пульсирующее кровотечение и большая или расширяющаяся гематома. Если у пациента проявляются эти признаки, вероятность повреждения сосудов у него > 90 %.
Категория 2 (мягкие признаки): К ним относятся относительно уменьшенный, но ощутимый пульс, нерасширяющаяся гематома и повреждение периферических нервов; У 30-35% этих пациентов будет повреждение сосудов.
Категория 3 (бессимптомная, высокий риск): К ним относятся проникающие раны в пределах 1 см от основных областей сосудисто-нервного пучка (например, подмышечной, бедренной и сонной артерии), а также вывихи коленного сустава или переломы длинных костей с тяжелым смещением. До 15-20% этих пациентов имеют сосудистое повреждение.
До 15-20% этих пациентов имеют сосудистое повреждение.
Травма сосудов конечностей Клиническая картина: анамнез и физикальное обследование
Feliciano DV. Для пациента-Эволюция в лечении сосудистых травм. J Хирург неотложной помощи при травмах .2017 Декабрь 83 (6): 1205-1212. [Ссылка QxMD MEDLINE].
Huber GH, Manna B. Травма сосудов конечностей . Остров сокровищ, Флорида: StatPearls; 2021. [Полный текст].
Slama R, Villaume F. Проникающее ранение сосудов: диагностика и лечение. Emerg Med Clin North Am . 2017 35 ноября (4): 789-801. [Ссылка QxMD MEDLINE].
Венермо М., Кантонен И., Суоминен В., Салениус Дж., Рот В.Д., Лепантало М.«Актуальные проблемы сосудистой хирургии». Дуодецим . 2009. 125 (4): 439-47. [Ссылка QxMD MEDLINE].
Husum H, Ang SC, Fosse E. Полевое руководство по военной хирургии . Пенанг, Малайзия: Сеть третьего мира; 1995.
Догерти П.Дж., Наджиби С., Сильвертон С., Вайдья Р. Огнестрельные ранения: эпидемиология, баллистика ран и лечение мягких тканей. Учебный курс Лекция . 2009. 58:131-9. [Ссылка QxMD MEDLINE].
Mattox KL, Feliciano DV, Burch J, Beall AC Jr, Jordan GL Jr, De Bakey ME.Пять тысяч семьсот шестьдесят сердечно-сосудистых повреждений у 4459 пациентов. Эпидемиологическая эволюция с 1958 по 1987 год. Энн Сург . 1989 июнь 209 (6):698-705; обсуждение 706-7. [Ссылка QxMD MEDLINE].
Feliciano DV, Herskowitz K, O’Gorman RB, Cruse PA, Brandt ML, Burch JM, et al. Лечение повреждений сосудов нижних конечностей. J Травма . 1988 28 марта (3): 319-28. [Ссылка QxMD MEDLINE].
1988 28 марта (3): 319-28. [Ссылка QxMD MEDLINE].
Дебейки М.Э., Симеоне Ф.А.Боевые повреждения артерий во время Второй мировой войны: анализ 2471 случая. Энн Сург . 1946 Апрель 123 (4): 534-79. [Ссылка QxMD MEDLINE]. [Полный текст].
Рич Н.М., Боуг Дж.Х., Хьюз К.В. Острые артериальные травмы во Вьетнаме: 1000 случаев. J Травма . 1970 май. 10 (5): 359-69. [Ссылка QxMD MEDLINE].
Rich NM, Leppäniemi A. Сосудистая травма: 40-летний опыт лечения сосудов конечностей. Scand J Surg .2002. 91 (1): 109-26. [Ссылка QxMD MEDLINE].
Шериф А.А. Сосудистые повреждения: опыт войны в Афганистане. Внутренний сург . 1992 апрель-июнь. 77 (2): 114-7. [Ссылка QxMD MEDLINE].
Уайт Дж.М., Станнард А., Буркхардт Г.Э., Истрридж Б.Дж., Блэкборн Л.Х., Расмуссен Т.Е.Эпидемиология сосудистых повреждений в войнах в Ираке и Афганистане. Энн Сург . 2011 июнь 253 (6): 1184-9. [Ссылка QxMD MEDLINE].
Тобин С.А., Гарри Дж.Ф., Дойл Дж.С., Коннелл Дж.Л., Видович Дж.Д. Сосудистая травма в университетской клинической больнице. Aust NZ J Surg . 1988 ноябрь 58 (11): 873-7. [Ссылка QxMD MEDLINE].
Размадзе А. Сосудистые повреждения конечностей: пятнадцатилетний грузинский опыт. Eur J Vasc Endovasc Surg .1999 г., 18 сентября (3): 235–239. [Ссылка QxMD MEDLINE].
Маги Т.Р., Коллин Дж., Хэндс Л.Дж., Грей Д.В., Роук Дж. Десятилетний аудит хирургии сосудистых травм в британской учебной больнице. Eur J Vasc Endovasc Surg . 1996 12 ноября (4): 424-7. [Ссылка QxMD MEDLINE].
Хамфри П.В., Николс В.К., Сильвер Д.Сельская сосудистая травма: двадцатилетний обзор. Энн Васк Сург . 1994 8 марта (2): 179-85. [Ссылка QxMD MEDLINE].
Крышки МТ. Эпидемиология травм сосудов. Семин Васк Сург . 1998 11 декабря (4): 227-31. [Ссылка QxMD MEDLINE].
Флойд HD, Керштейн MD. Успешная реконструкция сосудов. Детерминанты инвалидности. Am Surg .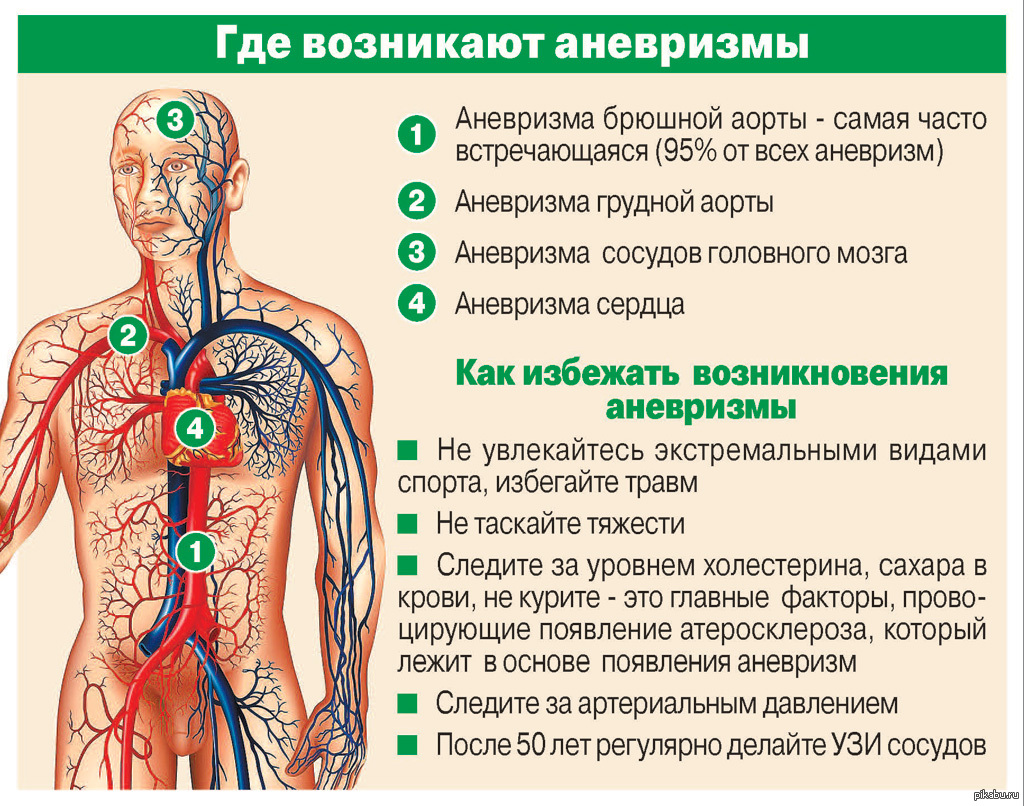 1986 фев. 52 (2): 91-2. [Ссылка QxMD MEDLINE].
1986 фев. 52 (2): 91-2. [Ссылка QxMD MEDLINE].
Сиддик М.К., Бхатти А.М.Двухлетний опыт лечения травм сосудов конечностей в условиях военного госпиталя. J Pak Med Assoc . 2013 март 63 (3): 327-30. [Ссылка QxMD MEDLINE].
Скотт Д.Дж., Артурс З.М., Станнард А., Монро Х.М., Клауз В.Д., Расмуссен Т.Е. Исходы и качество жизни пациентов после травм сосудов конечностей, поддающихся спасению во время войны. J Vasc Surg . 2014 59 января (1):173-9.e1. [Ссылка QxMD MEDLINE].
Аль-Зуби Н.А., Шатнави Н.Дж., Хадер Ю., Хейс М., Алешави А.Дж.Прогностические факторы неудачи спасения конечности при тупой травме ноги, связанной с сосудистыми повреждениями. J Экстренный травматический шок . 2021 апрель-июнь. 14 (2):80-85. [Ссылка QxMD MEDLINE]. [Полный текст].
Бранко Б.К., Линнебур М., Бутроус М.Л., Лик С.С., Инаба К., Чарльтон-Оув К.М. и др. Прогностическая ценность мультидетекторной КТА в отношении исходов у пациентов с повреждением сосудов ниже колена. Травма . 2015 авг. 46 (8): 1520-6. [Ссылка QxMD MEDLINE].
Фриц Дж., Эфрон Д.Т., Фишман Э.К. Современная ангиографическая 3DCT-оценка травмы нижних конечностей: типичные результаты, жемчужины и подводные камни. Аварийный Радиол .2013 20 июня (3): 175-84. [Ссылка QxMD MEDLINE].
Мадхурипан Н., Мехта П., Смолинский С.Е., Ньюгуна Н. Компьютерная томографическая ангиография конечностей в неотложных состояниях. Семин УЗИ КТ MR . 2017 38 августа (4): 357-369. [Ссылка QxMD MEDLINE].
Йохансен К., Линч К., Паун М., Копасс М. Неинвазивные сосудистые тесты надежно исключают скрытую артериальную травму в поврежденных конечностях. J Травма . 1991 31 апреля (4): 515-9; обсуждение 519-22. [Ссылка QxMD MEDLINE].
Линч К., Йохансен К. Может ли измерение доплеровского давления заменить «исключающую» артериографию в диагностике скрытой артериальной травмы конечностей? Энн Сург . 1991, декабрь 214 (6): 737-41. [Ссылка QxMD MEDLINE].
1991, декабрь 214 (6): 737-41. [Ссылка QxMD MEDLINE].
Нассура З.Е., Иватури Р.Р., Саймон Р.Дж., Джаббур Н., Винзонс А., Шталь В. Переоценка индексов допплеровского давления при обнаружении артериальных поражений при проникающих ранениях конечностей: проспективное исследование. Am J Emerg Med . 1996 14 марта (2): 151-6. [Ссылка QxMD MEDLINE].
Хемингуэй Дж., Аджей Э., Десикан С., Гросс Дж., Тран Н., Сингх Н. и др.Снижение порога лодыжечно-плечевого индекса при тупой травме нижних конечностей может предотвратить ненужную визуализацию. Энн Васк Сург . 2020 янв. 62:106-113. [Ссылка QxMD MEDLINE].
Moore EE, Malangoni MA, Cogbill TH, Peterson NE, Champion HR, Jurkovich GJ, et al. Масштабирование повреждения органов VII: шейные сосуды, периферические сосуды, надпочечники, половой член, яичко и мошонка. J Травма . 1996 сен. 41 (3): 523-4. [Ссылка QxMD MEDLINE].
J Травма . 1996 сен. 41 (3): 523-4. [Ссылка QxMD MEDLINE].
Причаюдх С., Верананваттна А., Шриуссадапорн С., Шриуссапорн С., Критаякирана К., Пак-арт Р. и др.Лечение повреждения сосудов верхних конечностей: результат, связанный с оценкой тяжести искривленных конечностей. Мир J Surg . 2009 33 апреля (4): 857-63. [Ссылка QxMD MEDLINE].
Инаба К., Сибони С., Резник С., Чжу Дж., Вонг М.Д., Халтмайер Т. и другие. Использование жгута при травмах конечностей гражданского населения. J Хирург неотложной помощи при травмах . 2015 авг. 79 (2): 232-7; викторина 332-3. [Ссылка QxMD MEDLINE].
Оде Г., Студнек Дж., Сеймур Р., Боссе М.Дж., Хсу Дж.Р.Экстренные жгуты для гражданских лиц: можно ли перевести военные уроки кровоизлияния в конечности? J Хирург неотложной помощи при травмах . 2015 Октябрь 79 (4): 586-91. [Ссылка QxMD MEDLINE].
2015 Октябрь 79 (4): 586-91. [Ссылка QxMD MEDLINE].
Буш Р.Л., Фэйрман Р.М., Флаэрти С.Ф., Гиллеспи Д.Л. Роль сосудистых хирургов-добровольцев SVS в оказании помощи раненым в ходе боевых действий: результаты из Ландштуля, Германия. J Vasc Surg . 2009 янв. 49 (1): 226-9. [Ссылка QxMD MEDLINE].
Алархайем А.К., Кон С.М., Канту-Нуньес О., Истридж Б.Дж., Расмуссен Т.Э.Влияние времени восстановления на исходы у пациентов с повреждениями артерий нижних конечностей. J Vasc Surg . 2019 май. 69 (5): 1519-1523. [Ссылка QxMD MEDLINE].
Шах Д.М., Кожаный Р.П., Корсон Д.Д., Кармоди А.М. Политетрафторэтиленовые трансплантаты в быстрой реконструкции острых контаминированных повреждений периферических сосудов. Am J Surg . 1984 авг. 148 (2): 229-33. [Ссылка QxMD MEDLINE].
Nypaver TJ, Schuler JJ, McDonnell P, Ellenby MI, Montalvo J, Baraniewski H, et al. Отдаленные результаты венозной реконструкции после сосудистой травмы в гражданской практике. J Vasc Surg . 1992 16 ноября (5): 762-8. [Ссылка QxMD MEDLINE].
Гонсалес Р.П., Скотт В., Райт А., Фелан Х.А., Роднинг С.Б. Анатомическая локализация проникающих ранений нижних конечностей позволяет прогнозировать развитие компартмент-синдрома. Am J Surg . 2009 март 197 (3): 371-5. [Ссылка QxMD MEDLINE].
Vertrees A, Fox CJ, Quan RW, Cox MW, Adams ED, Gillespie DL. Использование протезов при сложной военной сосудистой травме: стратегия спасения конечностей у пациентов с сильно ограниченным аутологичным кондуитом.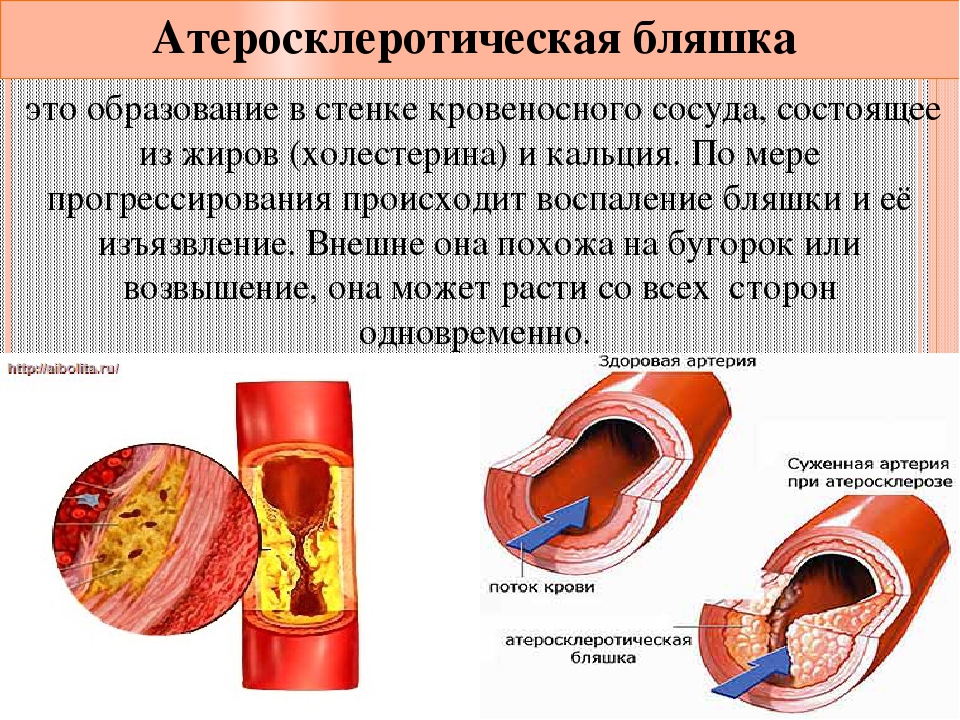 J Травма . 2009 апр. 66 (4): 980-3. [Ссылка QxMD MEDLINE].
J Травма . 2009 апр. 66 (4): 980-3. [Ссылка QxMD MEDLINE].
Фарбер А., Тан Т.В., Гамбург Н.М., Калиш Дж.А., Джоглар Ф., Онигман Т. и другие. Ранняя фасциотомия у пациентов с повреждением сосудов конечностей связана со снижением риска неблагоприятных последствий для конечностей: обзор Национального банка данных о травмах. Травма . 2012 Сентябрь 43 (9): 1486-91. [Ссылка QxMD MEDLINE]. [Полный текст].
Причаюдх С., Верананваттна А., Шриуссадапорн С., Шриуссапорн С., Критаякирана К., Пак-арт Р. и др. Лечение повреждения сосудов верхних конечностей: результат, связанный с оценкой тяжести искривленных конечностей. Мир J Surg . 2009 33 апреля (4): 857-63. [Ссылка QxMD MEDLINE].
Дарем Р. М., Мистри Б. М., Мазуски Дж. Э., Шапиро М., Джейкобс Д. Результат и полезность систем подсчета очков при лечении искривленной конечности.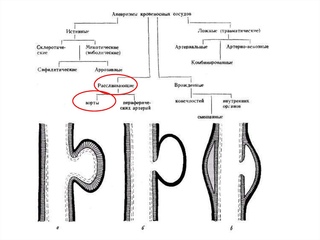 Am J Surg . 1996 ноябрь 172 (5): 569-73; обсуждение 573-4. [Ссылка QxMD MEDLINE].
Am J Surg . 1996 ноябрь 172 (5): 569-73; обсуждение 573-4. [Ссылка QxMD MEDLINE].
Хельфет Д.Л., Хоуи Т., Сандерс Р., Йохансен К. Спасение конечностей в сравнении с ампутацией. Предварительные результаты оценки степени тяжести искривленных конечностей. Clin Orthop Relat Res . 1990 июль (256): 80–6. [Ссылка QxMD MEDLINE].
Бонанни Ф., Родс М., Лаке Дж. Ф. Бесполезность прогностического подсчета искривленных нижних конечностей. J Травма . 1993 янв.34 (1): 99-104. [Ссылка QxMD MEDLINE].
Вейт Ф.Дж., Марин М.Л. Современное состояние эндолюминальных стентированных протезов для лечения аневризм, травматических повреждений и артериальных окклюзий. Сердечно-сосудистый хирург . 1996 4 февраля (1): 3-7. [Ссылка QxMD MEDLINE].
Боггс Х.К., Томихама Р.Т., Абу-Замзам А.М. младший, Мукерджи К., Турай Д., Теруя Т.Х. и др.АНАЛИЗ ТРАВМАТИЧЕСКИХ ПОВРЕЖДЕНИЙ ПОДКЛЮЧИЧНО-ПОДКИСНЫХ СОСУДОВ: ЭНДОВАСКУЛЯРНОЕ ЛЕЧЕНИЕ ЯВЛЯЕТСЯ ПЕРСПЕКТИВНЫМ ВАРИАНТОМ ОТКРЫТОЙ ХИРУРГИЧЕСКОЙ РЕКОНСТРУКЦИИ. Энн Васк Сург . 2021, 14 октября. [Ссылка на MEDLINE QxMD].
Хурана А., Квенсер К., Сайни А., Силл А., Албадави Х., Джамал Л. и др. Эндоваскулярные вмешательства при лечении острой травмы конечностей: описательный обзор. Энн Трансл Мед . 2021 9 июля (14): 1197. [Ссылка QxMD MEDLINE]. [Полный текст].
Скотт А.Р., Гилани Р., Тапиа Н.М., Маттокс К.Л., Уолл М.Дж., Сулибурк Дж.В.Эндоваскулярное лечение травматических повреждений периферических артерий. J Surg Res . 2015 Декабрь 199 (2): 557-63. [Ссылка QxMD MEDLINE].
J Surg Res . 2015 Декабрь 199 (2): 557-63. [Ссылка QxMD MEDLINE].
Richmond BK, Judhan R, Sherrill W, Yacoub M, AbuRahma AF, Knackstedt K, et al. Тенденции и результаты оперативного лечения травматических сосудистых повреждений: сравнение открытых эндоваскулярных подходов и . Am Surg . 2017 1 мая. 83 (5): 495-501. [Ссылка QxMD MEDLINE].
Д’Алессио И., Доманин М., Биссакко Д., Романьоли С., Римольди П., Саммартано Ф. и др.Оперативное лечение и клинические результаты при периферической сосудистой травме: объединенный опыт двух центров в эндоваскулярную эру. Энн Васк Сург . 2020 Январь 62: 342-348. [Ссылка QxMD MEDLINE].
Абу Али А.Н., Салем К.М., Аларкон Л.Х., Бауза Г., Пикулис Э., Чаер Р.А. и др. Сосудистые шунты при гражданской травме. Передний амортизатор .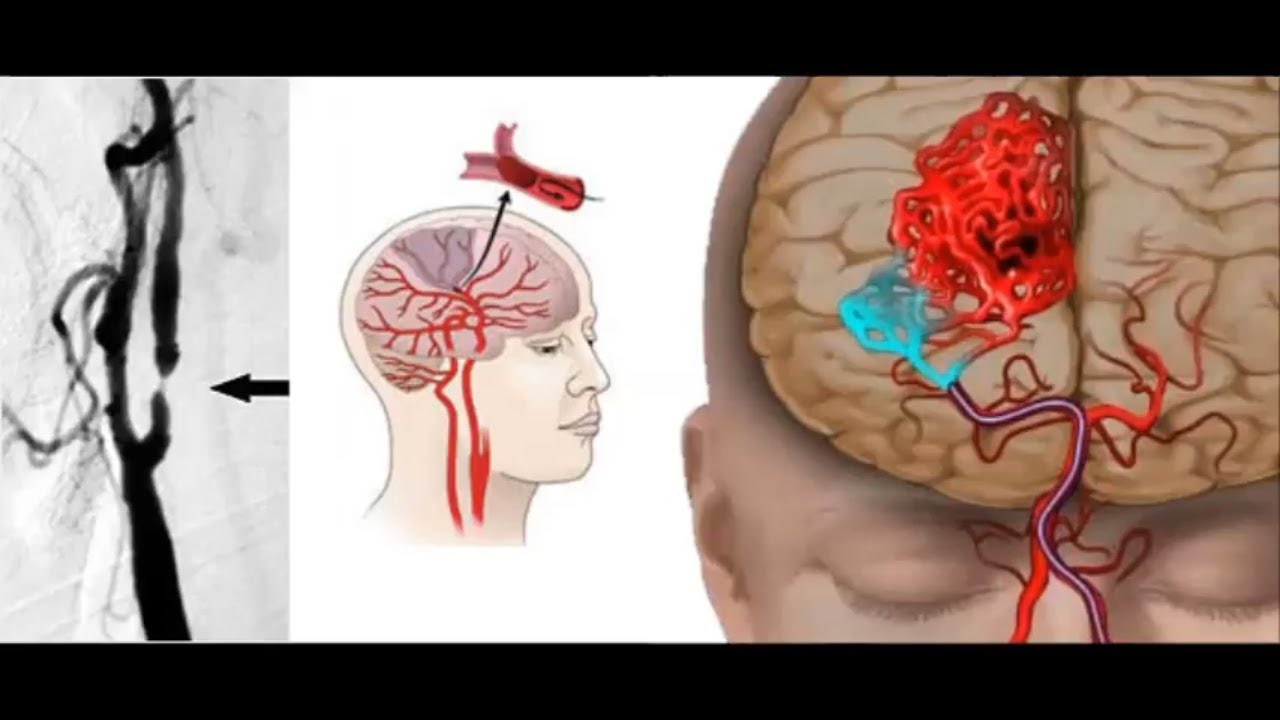 2017. 4:39. [Ссылка QxMD MEDLINE]. [Полный текст].
2017. 4:39. [Ссылка QxMD MEDLINE]. [Полный текст].
Де Айала-Хиллман Р., Креспо-Мартинес Н.А., Гарсия-Родригес О., Рамос-Мелендес Э.О., Родригес-Ортис П.Травматическое повреждение сосудов и его лечение с помощью временных внутрисосудистых шунтов: опыт травматологической больницы Пуэрто-Рико. PR Health Sci J . 2018 37 декабря (4): 220-223. [Ссылка QxMD MEDLINE].
Американский журнал рентгенологии Том. 186, № 3 (AJR)
| Введение | выберите К началу страницыРЕФЕРАТВведение <<Материалы и методыРезультатыОбсуждениеСсылкиЦитирование статей |
|---|
Выбор тактики хирургического лечения пациентов с травматическими повреждениями конечностей требует быстрого выявления, локализации и характеристики возможного сопутствующего сосудистого повреждения.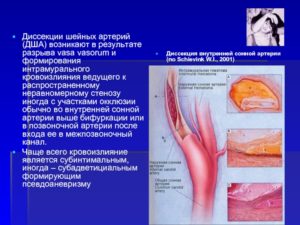 Было обнаружено, что физикальное и сонографическое исследования после травмы конечности являются надежными средствами выявления скрытого поражения артерий [1-4]. В результате рутинная цифровая субтракционная ангиография, которая считалась методом выбора [5-8], не считается необходимой у каждого пациента с травмой конечности. Тем не менее, цифровая субтракционная ангиография продолжает использоваться по признанным показаниям после проникающих или тупых травм конечностей у пациентов с уменьшенным пульсом, нерасширяющейся гематомой или аномальными результатами дуплексной сонографии [1, 2, 9, 10].
Было обнаружено, что физикальное и сонографическое исследования после травмы конечности являются надежными средствами выявления скрытого поражения артерий [1-4]. В результате рутинная цифровая субтракционная ангиография, которая считалась методом выбора [5-8], не считается необходимой у каждого пациента с травмой конечности. Тем не менее, цифровая субтракционная ангиография продолжает использоваться по признанным показаниям после проникающих или тупых травм конечностей у пациентов с уменьшенным пульсом, нерасширяющейся гематомой или аномальными результатами дуплексной сонографии [1, 2, 9, 10].
Использование однодетекторной КТ-ангиографии для оценки предполагаемых сосудистых аномалий совпало с неинвазивной диагностикой и дало дополнительные преимущества по сравнению с цифровой субтракционной ангиографией, включая трехмерную визуализацию исследуемой сосудистой сети; более короткое время приобретения; и, самое главное, одновременная визуализация сосудистых, мышечных и костных структур. Действительно, преимущества однодетекторной КТ-ангиографии улучшили выявление и характеристику травматических сосудистых поражений в целом [11-16] и дали многообещающие результаты в отношении оценки артериальных повреждений проксимальных отделов конечностей с высокой чувствительностью (95%) и специфичностью. (99%) [17, 18].
Действительно, преимущества однодетекторной КТ-ангиографии улучшили выявление и характеристику травматических сосудистых поражений в целом [11-16] и дали многообещающие результаты в отношении оценки артериальных повреждений проксимальных отделов конечностей с высокой чувствительностью (95%) и специфичностью. (99%) [17, 18].
Благодаря своим преимуществам [19-21] по сравнению с однодетекторной КТ-ангиографией, МСКТ-ангиография была применена для оценки крупных сосудистых территорий благодаря быстрому получению изображений [22, 23] и для оценки мелких артерий благодаря возможности тонкого -секционное приобретение [24, 25]. Кроме того, МСКТ рекомендуется для оценки пациентов с политравмой, поскольку она обеспечивает комплексную диагностическую работу в течение относительно короткого пребывания в кабинете КТ [26, 27].
Насколько нам известно, роль МСКТ-ангиографии в оценке травматических повреждений артерий конечностей еще не описана.Цель этого исследования состояла в том, чтобы ретроспективно оценить точность ангиографии MDCT как начальной диагностической методики для изображения повреждения артерий у пациентов с травмой конечности.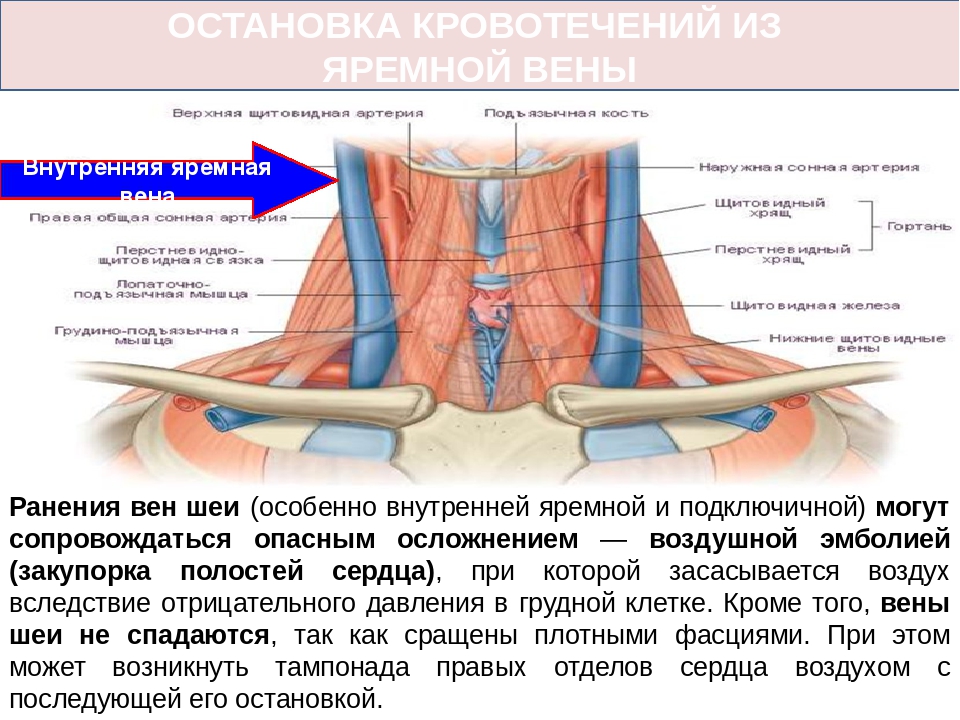
| Материалы и методы | выберите К началу страницыРЕФЕРАТВведениеМатериалы и методы <<РезультатыОбсуждениеСсылкиСсылающиеся на статьи |
|---|
Это исследование было проведено как ретроспективный анализ ангиографических исследований конечностей с помощью МСКТ.В период с января 2001 г. по декабрь 2003 г. 87 последовательных пациентов — 16 женщин (возрастной диапазон 17–87 лет, средний возраст 43 года) и 71 мужчина (возрастной диапазон 16–87 лет, средний возраст 36 лет) — подверглись МСКТ-ангиографии. конечности после получения травматического повреждения верхней или нижней конечности с клиническим подозрением на поражение крупной артерии. Пациенты без сознания и дети были исключены из этого исследования.
После поступления пациентов в отделение неотложной помощи проводилось полное клиническое обследование, в частности пораженной конечности, и определялось дальнейшее лечение в соответствии с категорией травматического сосудистого повреждения. То есть при окончательном повреждении сосудов (пульсирующее кровотечение, быстрорастущая гематома, шум или дрожание над раной, отсутствие пульса с явной траекторией от проникающего поражения) выполнялась операция; при подозрении на повреждение сосудов (чрезмерное непульсирующее кровотечение, большая нерасширяющаяся гематома, выраженный неврологический дефицит, сниженный, но заметный пульс) выполнялась МСКТ-ангиография; и для низкой вероятности сосудистого повреждения (близкое повреждение, проникающее ранение в непосредственной близости от сосудистых структур без клинических признаков, указывающих на сосудистую недостаточность), было выполнено эхографическое наблюдение.При отсутствии необходимости в немедленном хирургическом вмешательстве для поддержания гемодинамической стабильности пациентам выполняли МСКТ-ангиографию на основании междисциплинарного решения лечащего анестезиолога, травматолога, сосудистого хирурга и КТ-рентгенолога.
То есть при окончательном повреждении сосудов (пульсирующее кровотечение, быстрорастущая гематома, шум или дрожание над раной, отсутствие пульса с явной траекторией от проникающего поражения) выполнялась операция; при подозрении на повреждение сосудов (чрезмерное непульсирующее кровотечение, большая нерасширяющаяся гематома, выраженный неврологический дефицит, сниженный, но заметный пульс) выполнялась МСКТ-ангиография; и для низкой вероятности сосудистого повреждения (близкое повреждение, проникающее ранение в непосредственной близости от сосудистых структур без клинических признаков, указывающих на сосудистую недостаточность), было выполнено эхографическое наблюдение.При отсутствии необходимости в немедленном хирургическом вмешательстве для поддержания гемодинамической стабильности пациентам выполняли МСКТ-ангиографию на основании междисциплинарного решения лечащего анестезиолога, травматолога, сосудистого хирурга и КТ-рентгенолога.
Травматические повреждения верхней конечности были у 36 пострадавших, нижней конечности — у 51.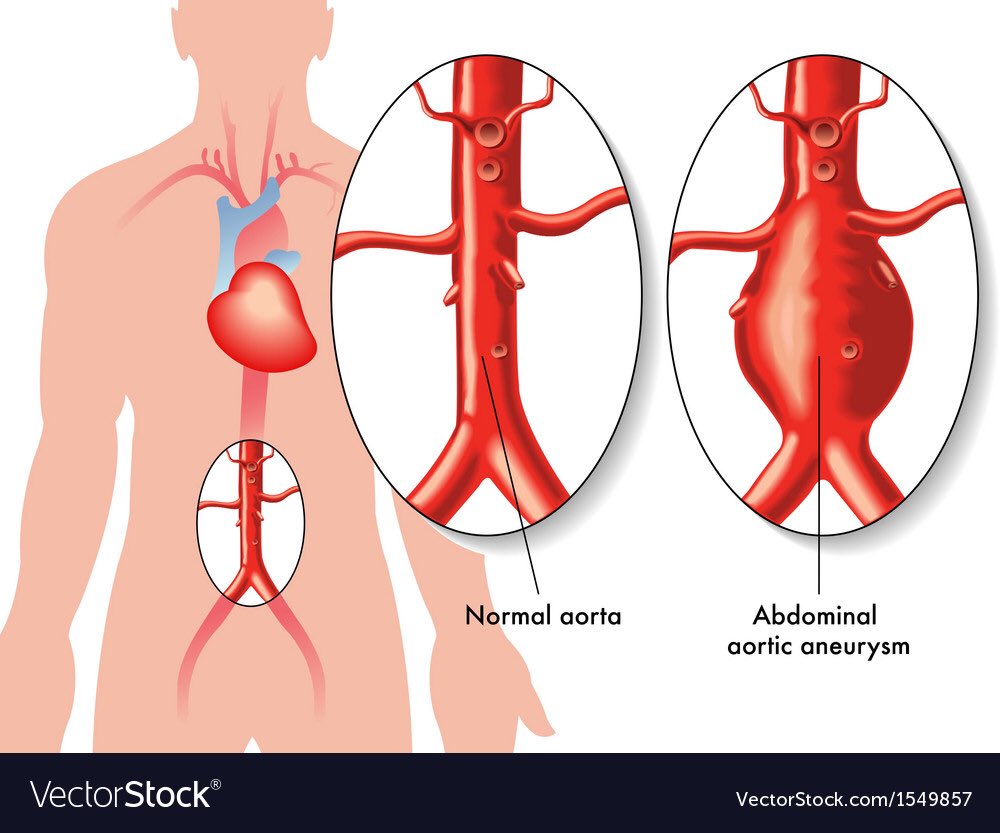 Тупые ранения выявлены у 80 пострадавших, проникающие ранения — у 7. Во всех случаях перед операцией выполнялась МСКТ-ангиография для определения тактики лечения.Шестьдесят семь пациентов оперированы после МСКТ-ангиографии. Обследования, проводимые для оценки послеоперационных результатов, были исключены из этого исследования. Ни у одного из пациентов не было противопоказаний к внутривенному введению неионогенного контрастного вещества. Наш институциональный наблюдательный совет одобрил исследование, и от всех пациентов было получено информированное согласие на МСКТ-ангиографию.
Тупые ранения выявлены у 80 пострадавших, проникающие ранения — у 7. Во всех случаях перед операцией выполнялась МСКТ-ангиография для определения тактики лечения.Шестьдесят семь пациентов оперированы после МСКТ-ангиографии. Обследования, проводимые для оценки послеоперационных результатов, были исключены из этого исследования. Ни у одного из пациентов не было противопоказаний к внутривенному введению неионогенного контрастного вещества. Наш институциональный наблюдательный совет одобрил исследование, и от всех пациентов было получено информированное согласие на МСКТ-ангиографию.
Спиральная КТ выполнялась на 4-MDCT сканере (LightSpeed QX/i, GE Healthcare) с периодом вращения гентри 0,8 с.МСКТ-ангиографию выполняли в положении пациента лежа на спине с руками вдоль туловища, за исключением пяти пациентов, получивших травматическое повреждение только предплечья или кисти. В последних случаях больного укладывали в положение лежа с вытянутой над головой задействованной рукой.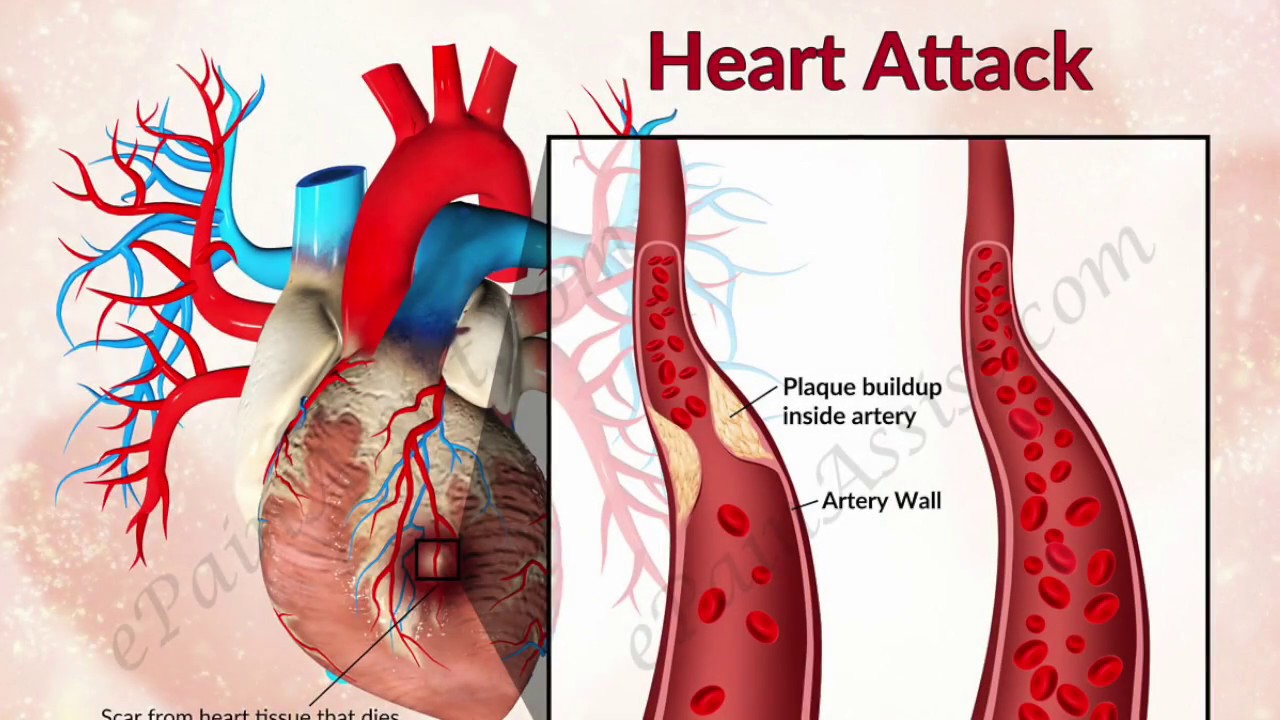 Во всех случаях пораженную конечность иммобилизовали с помощью лейкопластыря. Ангиографические изображения МСКТ были получены в проксимально-дистальном направлении с использованием коллимации 1,25 мм, толщины реконструированного среза 1,25 мм и стандартного ядра реконструкции.Шаг и интервал реконструкции регулировались в зависимости от интересующей анатомической области (табл. 1). При исследовании более чем одной анатомической области использовали шаг 1,5 и интервал реконструкции 0,8 мм. Чтобы улучшить осевое разрешение, мы использовали минимально возможное поле зрения дисплея, и поле зрения дисплея захватывало только вовлеченную конечность.
Во всех случаях пораженную конечность иммобилизовали с помощью лейкопластыря. Ангиографические изображения МСКТ были получены в проксимально-дистальном направлении с использованием коллимации 1,25 мм, толщины реконструированного среза 1,25 мм и стандартного ядра реконструкции.Шаг и интервал реконструкции регулировались в зависимости от интересующей анатомической области (табл. 1). При исследовании более чем одной анатомической области использовали шаг 1,5 и интервал реконструкции 0,8 мм. Чтобы улучшить осевое разрешение, мы использовали минимально возможное поле зрения дисплея, и поле зрения дисплея захватывало только вовлеченную конечность.
ТАБЛИЦА 1: Параметры получения ангиографии при МДКТ
Напряжение и ток рентгеновской трубки регулировались для исследуемого участка конечности и составляли от 100 до 140 кВ и от 80 до 200 мА.Аналогичным образом, в зависимости от веса пациента и площади сканирования, общий объем неионогенного контрастного вещества 100–150 мл вводили внутривенно со скоростью 3–5 мл/сек в соответствии со следующей формулой: где с — продолжительность сканирования , скорость потока измеряется в миллилитрах в секунду, а 10 мл соответствует задержке перехода от программного обеспечения SmartPrep (GE Healthcare) к диагностическому спиральному сканированию. Задержку сканирования определяли с помощью программного обеспечения SmartPrep, которое позволяет осуществлять непрерывный мониторинг значений затухания в магистральной артерии в исследуемой области (т.е., подключичной, плечевой, лучевой, общей бедренной или подколенной артерии) проксимальнее места предполагаемого повреждения. Когда значение артериального затухания увеличилось до 180-200 H после введения контрастного вещества, вручную инициировали спиральное сканирование под наблюдением рентгенолога, отвечающего за неотложную КТ; этот рентгенолог был одним из девяти старших рентгенологов с 5-16-летним опытом использования и интерпретации КТ.
Задержку сканирования определяли с помощью программного обеспечения SmartPrep, которое позволяет осуществлять непрерывный мониторинг значений затухания в магистральной артерии в исследуемой области (т.е., подключичной, плечевой, лучевой, общей бедренной или подколенной артерии) проксимальнее места предполагаемого повреждения. Когда значение артериального затухания увеличилось до 180-200 H после введения контрастного вещества, вручную инициировали спиральное сканирование под наблюдением рентгенолога, отвечающего за неотложную КТ; этот рентгенолог был одним из девяти старших рентгенологов с 5-16-летним опытом использования и интерпретации КТ.
После получения наборы данных MDCT были переданы в PACS и на рабочую станцию для 3D-рендеринга (Ultra 60, Sun Microsystems) под управлением программного обеспечения Advantage Windows (Advantage Windows 4.0, GE Healthcare), оба из которых расположены в отделении неотложной компьютерной томографии. Проспективно ангиограммы МСКТ были оценены радиологом, отвечающим за отделение неотложной КТ. В то время как рентгенолог оценивал аксиальные изображения на специальной рабочей станции PACS для оценки костных, мышечных и сосудистых структур исследуемой области, технический ассистент КТ использовал рабочую станцию визуализации для создания трехмерных реконструкций, то есть многоплоскостных преобразований (многоплоскостных реконструкций) и объемные изображения, интерпретируемые рентгенологом в интерактивном режиме.
В то время как рентгенолог оценивал аксиальные изображения на специальной рабочей станции PACS для оценки костных, мышечных и сосудистых структур исследуемой области, технический ассистент КТ использовал рабочую станцию визуализации для создания трехмерных реконструкций, то есть многоплоскостных преобразований (многоплоскостных реконструкций) и объемные изображения, интерпретируемые рентгенологом в интерактивном режиме.
Проспективная оценка проводилась в экстренном порядке. Поэтому перед операцией, особенно ночью и в выходные дни, не всегда можно было провести слепую оценку с двумя рецензентами. По этой причине все МСКТ-исследования были повторно оценены ретроспективно в течение 48 часов двумя независимыми радиологами с 7- и 4-летним опытом работы в КТ-ангиографии. Ни один из рецензентов не участвовал в проспективном анализе, и оба не знали хирургических, клинических и рентгенологических результатов.Рецензенты оценили аксиальные исходные изображения и реконструировали каждый набор данных для создания многоплоскостной реконструкции и видов с объемной визуализацией, которые интерактивно оценивались на рабочей станции для визуализации. При проспективном анализе рентгенолог определил наличие или отсутствие поражения артерий. Когда определялось наличие артериального поражения, его классифицировали как артериальный спазм, стеноз, вызванный компрессией, окклюзией, псевдоаневризмой, артериовенозной фистулой или разрывом артерии.Артериальный спазм определяли как концентрическое, гладкое, клиновидное сужение пораженной артерии, а стеноз определяли как эксцентричное, неравномерное сужение просвета артерии, вызванное внепросветной аномалией (интрамуральная гематома, гематома мягких тканей, костный фрагмент или инородное тело). ). В исследование не включались атеросклеротические стенозы.
При проспективном анализе рентгенолог определил наличие или отсутствие поражения артерий. Когда определялось наличие артериального поражения, его классифицировали как артериальный спазм, стеноз, вызванный компрессией, окклюзией, псевдоаневризмой, артериовенозной фистулой или разрывом артерии.Артериальный спазм определяли как концентрическое, гладкое, клиновидное сужение пораженной артерии, а стеноз определяли как эксцентричное, неравномерное сужение просвета артерии, вызванное внепросветной аномалией (интрамуральная гематома, гематома мягких тканей, костный фрагмент или инородное тело). ). В исследование не включались атеросклеротические стенозы.
Ретроспективно диагностическая достоверность наличия сосудистого повреждения оценивалась по 5-балльной шкале, где 1 означало наличие определенно присутствующего; 2, вероятно, присутствует; 3, неопределенный; 4, вероятно, отсутствует; или 5, точно отсутствует.Когда артериальное поражение было классифицировано как определенно присутствующее или вероятно присутствующее, оно затем классифицировалось в соответствии с той же системой, которая использовалась проспективно (например, артериальный спазм, стеноз, вызванный компрессией, окклюзия, псевдоаневризма, артериовенозная фистула или артериальный разрыв). Кроме того, у пациентов с повреждением артерий искали наличие расслоения лежащей в основе артерии. Диагностическая достоверность наличия основного расслоения оценивалась по 5-балльной шкале (т. е. от 1 — определенно присутствует, до 5 — определенно отсутствует).Критерии диагностики диссекции включали эксцентрический стеноз пораженной артерии, вызывающий полулунную деформацию просвета, расслоение лоскута или сегментарную тромботическую окклюзию в области повреждения.
Кроме того, у пациентов с повреждением артерий искали наличие расслоения лежащей в основе артерии. Диагностическая достоверность наличия основного расслоения оценивалась по 5-балльной шкале (т. е. от 1 — определенно присутствует, до 5 — определенно отсутствует).Критерии диагностики диссекции включали эксцентрический стеноз пораженной артерии, вызывающий полулунную деформацию просвета, расслоение лоскута или сегментарную тромботическую окклюзию в области повреждения.
Кроме того, двумя рецензентами была проведена количественная и полуколичественная оценка качества ангиограмм МСКТ. Количественную оценку проводили путем измерения артериального затухания в проксимальных и дистальных отделах исследуемой анатомической области каждым обозревателем.Затем для каждого исследования рассчитывали среднее значение затухания на каждом уровне. Полуколичественная оценка ангиограмм MDCT включала общее качество изображения, изображение поражения и артефакты. Впечатление от общего качества изображения оценивалось следующим образом: 1, очень хорошая демонстрация сосудистой анатомии, позволяющая всесторонне и надежно оценить; 2, хорошая демонстрация сосудистой анатомии, позволяющая провести адекватную оценку; 3, разумная демонстрация сосудистой анатомии с неадекватной оценкой; или 4, неудовлетворительная, едва заметная сосудистая анатомия. Изображение сосудистого поражения оценивалось следующим образом: 1 — достаточное изображение признаков поражения, позволяющее дать точную характеристику; 2, едва распознаваемые признаки поражения с ограниченной характеристикой поражения; или 3, неоднозначные признаки поражения с невозможной характеристикой. Наличие артефактов оценивалось следующим образом: 1 — нет; 2, минор; 3, легкая, частично влияющая на диагностическую оценку; или 4, серьезные, существенно влияющие на диагностическую оценку.
Изображение сосудистого поражения оценивалось следующим образом: 1 — достаточное изображение признаков поражения, позволяющее дать точную характеристику; 2, едва распознаваемые признаки поражения с ограниченной характеристикой поражения; или 3, неоднозначные признаки поражения с невозможной характеристикой. Наличие артефактов оценивалось следующим образом: 1 — нет; 2, минор; 3, легкая, частично влияющая на диагностическую оценку; или 4, серьезные, существенно влияющие на диагностическую оценку.
Чтобы определить их влияние в качестве дополнения к аксиальным исходным изображениям на восприятие артериального повреждения, многоплоскостная реконструкция и объемные изображения были классифицированы рецензентами как 1, предоставляющая диагностическую информацию, которая не была раскрыта на исходных изображениях; 2, облегчает оценку артериальной сосудистой сети; или 3, при условии отсутствия преимущества перед исходными изображениями.По сравнению с хирургическими и клиническими данными, обозреватели также оценили общее влияние МСКТ-ангиографии на окончательный диагноз как достаточное для установления диагноза или недостаточное, требующее дополнительных методов визуализации (например, цифровой субтракционной ангиографии).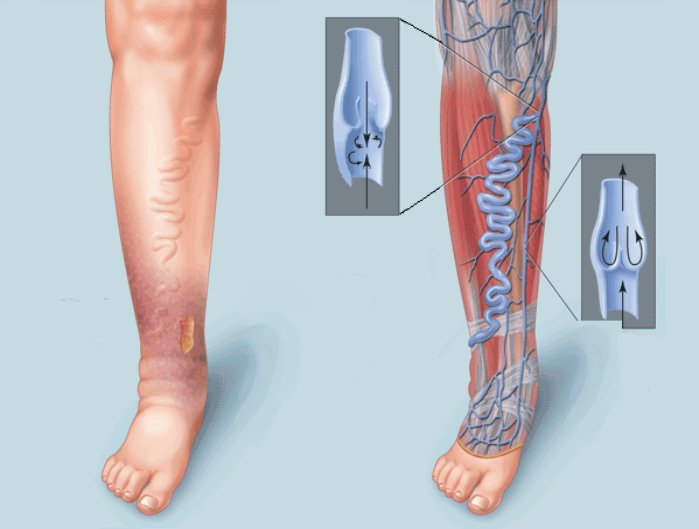
В этом исследовании эталонным стандартом была операция с осмотром пораженного артериального сегмента у 67 пациентов; цифровая субтракционная ангиография у двух пациентов; а у остальных 18 пациентов, которым не потребовалось хирургического вмешательства или цифровой субтракционной ангиографии, клинические и рентгенологические данные наблюдения.Клиническое наблюдение включало физикальное обследование пораженной конечности, осциллометрические измерения артериального давления, скорости распространения пульсовой волны, кожно-капиллярного кровообращения; Рентгенологический контроль включал допплерографию у всех пациентов. Средний период наблюдения составил 6 дней (диапазон от 2 до 14 дней). Хирургические результаты, а также клинические и рентгенологические результаты наблюдения были определены путем просмотра файлов данных пациентов, хранящихся в цифровой базе данных больницы, одним из двух хирургов.
Статистический анализ Процедуры ввода данных и статистический анализ выполнялись с помощью системы статистического программного обеспечения (версия SPSS 11.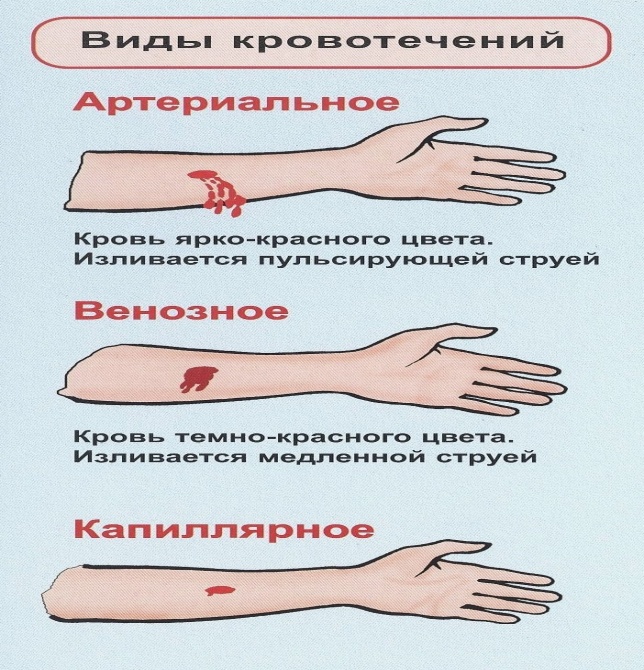 0.0, Статистический пакет для социальных наук) для Windows (Microsoft). На первом этапе проспективные данные были проанализированы на предмет обнаруживаемости поражений путем расчета чувствительности, специфичности и точности, а также на характеристику поражений путем расчета корреляции с эталонным стандартом с помощью критерия ранговой корреляции Спирмена. На втором этапе были проанализированы ретроспективные данные. Были построены кривые рабочих характеристик приемника (ROC), чтобы показать относительную точность ангиографии MDCT при обнаружении повреждений сосудов конечностей путем сравнения площадей под ROC-кривыми (A z ), рассчитанных каждым обозревателем.Исходя из наблюдаемых точек данных, чувствительность, специфичность и точность рассчитывались для каждого поражения (т. е. способности правильно идентифицировать все сосудистые поражения), при этом «определенно присутствующие» и «вероятно присутствующие» были положительными, а все остальные категории отрицательными.
0.0, Статистический пакет для социальных наук) для Windows (Microsoft). На первом этапе проспективные данные были проанализированы на предмет обнаруживаемости поражений путем расчета чувствительности, специфичности и точности, а также на характеристику поражений путем расчета корреляции с эталонным стандартом с помощью критерия ранговой корреляции Спирмена. На втором этапе были проанализированы ретроспективные данные. Были построены кривые рабочих характеристик приемника (ROC), чтобы показать относительную точность ангиографии MDCT при обнаружении повреждений сосудов конечностей путем сравнения площадей под ROC-кривыми (A z ), рассчитанных каждым обозревателем.Исходя из наблюдаемых точек данных, чувствительность, специфичность и точность рассчитывались для каждого поражения (т. е. способности правильно идентифицировать все сосудистые поражения), при этом «определенно присутствующие» и «вероятно присутствующие» были положительными, а все остальные категории отрицательными. ROC-анализ также применялся для оценки возможности обнаружения основного расслоения. Критерий ранговой корреляции Спирмена использовался для исследования корреляции между характеристиками поражения при МСКТ-ангиографии и данными, подтвержденными эталонным стандартом.
ROC-анализ также применялся для оценки возможности обнаружения основного расслоения. Критерий ранговой корреляции Спирмена использовался для исследования корреляции между характеристиками поражения при МСКТ-ангиографии и данными, подтвержденными эталонным стандартом.
Порядковые данные, полученные из режимов оценки качества изображения, описания поражения и артефактов, затем оценивались для оценки эффективности МСКТ-ангиографии путем расчета средних значений и 95% доверительных интервалов (ДИ). Порядковые данные, полученные в результате сравнительного анализа многоплоскостных преобразований, объемных изображений и аксиальных исходных изображений, были протестированы с помощью непараметрического биноминального теста.
Наконец, каппа-статистика использовалась для сравнения производительности наблюдателя. Значения Каппа были рассчитаны на основе уровня достоверности каждого рецензента для ROC-анализа.Согласие между наблюдателями считалось незначительным, если κ < 0,2; удовлетворительная, κ = 0,21-0,40; умеренная, κ = 0,41-0,60; существенный, κ = 0,61-0,80; или почти идеальный, κ = 0,81-1,00 [28].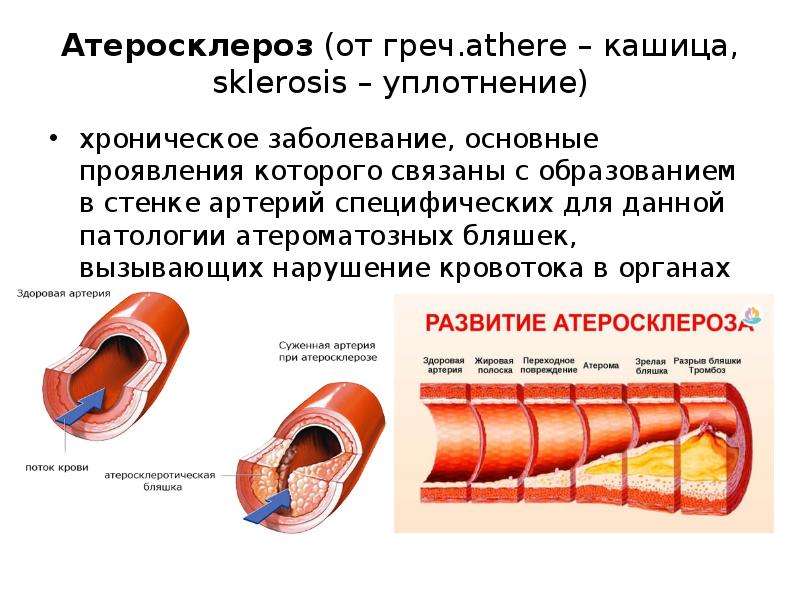
| Результаты | выберите К началу страницыРЕФЕРАТВведениеМатериалы и методыРезультаты <<ОбсуждениеСсылкиЦитирующие статьи |
|---|
Во время операции было подтверждено 62 травматических поражения артерий у 55 пациентов, в том числе 20 спазмов артерий, 10 стенозов, вызванных компрессией, 29 окклюзий и 3 разрыва артерий. ).При цифровой субтракционной ангиографии у двух пациентов были подтверждены две дополнительные окклюзии. Было 27 повреждений артерий верхней и 37 нижних конечностей. Наличие повреждения артерий было исключено у 30 пациентов, в том числе у 12 при хирургическом вмешательстве и у 18 при клиническом и допплерографическом наблюдении. Первые 12 пациентов оперированы открытым способом по поводу сложных переломов костей, в том числе 9 с проходимым артериальным кровотоком исследуемой конечности по данным КТ-ангиографии и 3 с купировавшимися во время операции спазмами. Последние 18 пациентов не нуждались в хирургическом вмешательстве. Артериовенозных фистул и псевдоаневризм не обнаружено. Подлежащее расслоение было подтверждено в 20 артериальных сегментах (19 пациентов).
Последние 18 пациентов не нуждались в хирургическом вмешательстве. Артериовенозных фистул и псевдоаневризм не обнаружено. Подлежащее расслоение было подтверждено в 20 артериальных сегментах (19 пациентов).
Таблица 2: Таблица 2: Angiography MDCT
| Посмотреть большую версию (53K) | Рис. 1 -66-летний мужчина с тупой травмой для левого плеча и вывих ключицы выполнена МСКТ-ангиография плеча и предплечья.Коронарная косая переформатированная МСКТ-ангиограмма плеча показывает окклюзию ( стрелки ) левой подключичной артерии, вызванную расслоением и последующим тромбозом пораженного артериального сегмента. Наличие и степень расслоения были указаны при цифровой субтракционной ангиографии, и расслоение было успешно вылечено имплантацией стента. |
С усилением контраста от 152 до 472 H (среднее затухание 282 H; SD 84 H) в проксимальном сегменте исследуемой анатомической области и от 109 до 383 H (среднее затухание 250 H; SD 71) З) в дистальном сегменте исследуемой анатомической области МСКТ-ангиография позволила оценить артериальное кровоснабжение конечностей.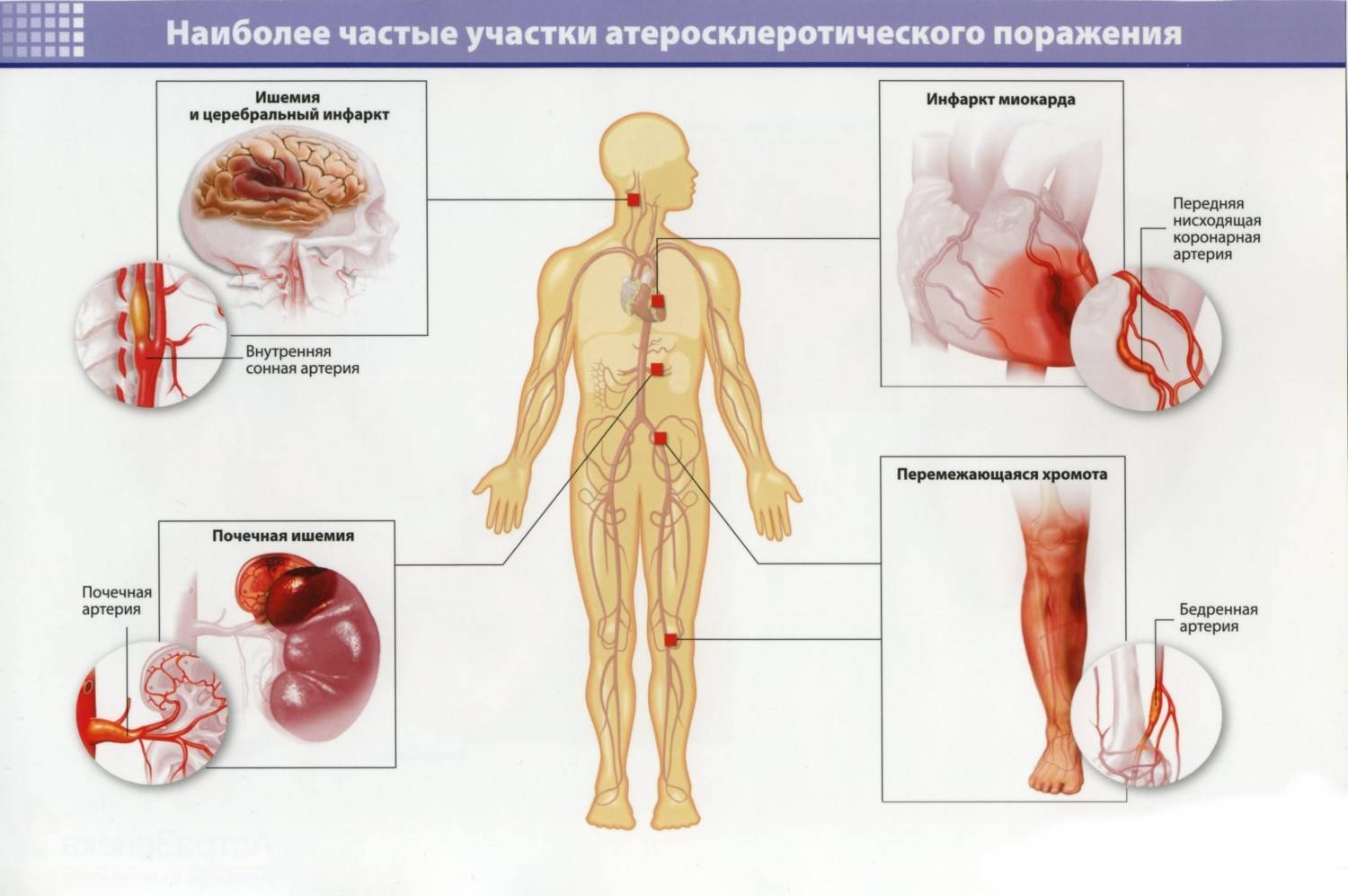 Помимо изображения магистральных артерий конечности от проксимального (рис. 1) к периферическому (рис. 2 и 3), включая их основные ветви, МСКТ-ангиография позволила оценить мышечные и костные структуры.
Помимо изображения магистральных артерий конечности от проксимального (рис. 1) к периферическому (рис. 2 и 3), включая их основные ветви, МСКТ-ангиография позволила оценить мышечные и костные структуры.
При проспективном анализе чувствительность, специфичность и точность МСКТ-ангиографии при выявлении артериального повреждения составляли 95%, 87% и 93% соответственно (таблица 3). При ретроспективном анализе параметрические модели ROC, выполненные для обнаружения любого посттравматического артериального поражения, показали, что оба автора обзора достигли значительных результатов со значениями A z , равными 0.97 и 0,95 соответственно. Согласно наблюдаемым точкам данных при анализе ROC, чувствительность ангиографии MDCT для рецензентов 1 и 2 составила 100% и 98% соответственно; специфичность 87% и 87% соответственно; и точность, 96% и 95%, соответственно (таблица 3). Как при проспективных, так и при ретроспективных оценках у пациентов, которым не потребовалось хирургическое вмешательство, не было обнаружено анатомических повреждений артерий. Параметрические ROC-модели, выполненные для выявления основного расслоения в поврежденных артериальных сегментах, показали хорошее соответствие между ангиографией MDCT и эталонным стандартом (рис.4А и 4В). Значения A z варьировались от 0,80 для рецензента 2 до 0,85 для рецензента 1. Несмотря на высокую диагностическую точность, достигнутую рецензентами, и отсутствие существенных различий между их интерпретациями, между рецензентами наблюдались некоторые разногласия в их уровне достоверности. обнаружения артериального повреждения (κ = 0,78) и выявляемости основного расслоения (κ = 0,60).
Параметрические ROC-модели, выполненные для выявления основного расслоения в поврежденных артериальных сегментах, показали хорошее соответствие между ангиографией MDCT и эталонным стандартом (рис.4А и 4В). Значения A z варьировались от 0,80 для рецензента 2 до 0,85 для рецензента 1. Несмотря на высокую диагностическую точность, достигнутую рецензентами, и отсутствие существенных различий между их интерпретациями, между рецензентами наблюдались некоторые разногласия в их уровне достоверности. обнаружения артериального повреждения (κ = 0,78) и выявляемости основного расслоения (κ = 0,60).
ТАБЛИЦА 3: Выявляемость артериального повреждения с помощью МСКТ-ангиографии
Характеристика артериального повреждения МСКТ-ангиография позволила правильно охарактеризовать большинство выявленных артериальных повреждений (рис.4А, 4В, 5, 6, 7А, 7В и 7С). Критерий ранговой корреляции Спирмена показал статистически значимую корреляцию между МСКТ-ангиографией и эталонным стандартом для проспективного анализа (оба рецензента: r = 0,93, p < 0,001; рецензент 1, r = 0,95, p < 0,001).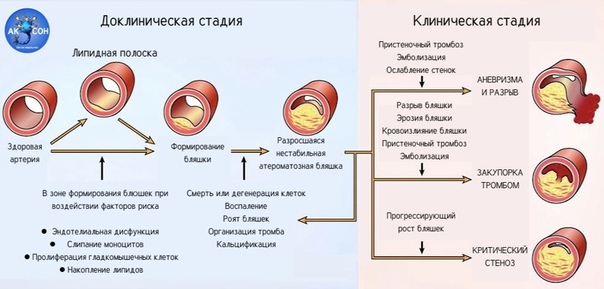 ; рецензент 2, р = 0,94, р < 0,001). Проспективно девять находок были неправильно классифицированы: три случая спазма, которые не были идентифицированы, два других случая, которые считались окклюзией, но были спазмом во время операции, один случай, который считался окклюзией, но был нормальным во время операции, и три случая, которые считались окклюзией. спазм, но были нормальными.Рецензент 1 неправильно классифицировал шесть результатов (два случая, которые считались окклюзией, но были спазмом во время операции, три других случая, которые считались спазмом, но были нормальными, и один случай, который считался окклюзией, но был нормальным во время операции), и рецензент 2 неправильно классифицировал семь результатов (один случай спазма, который не был идентифицирован, два случая, которые считались окклюзией, но были спазмом во время операции, три других случая, которые считались спазмом, но были нормальными, и один случай, который считался спазмом). быть окклюзия, но это было нормально во время операции).
; рецензент 2, р = 0,94, р < 0,001). Проспективно девять находок были неправильно классифицированы: три случая спазма, которые не были идентифицированы, два других случая, которые считались окклюзией, но были спазмом во время операции, один случай, который считался окклюзией, но был нормальным во время операции, и три случая, которые считались окклюзией. спазм, но были нормальными.Рецензент 1 неправильно классифицировал шесть результатов (два случая, которые считались окклюзией, но были спазмом во время операции, три других случая, которые считались спазмом, но были нормальными, и один случай, который считался окклюзией, но был нормальным во время операции), и рецензент 2 неправильно классифицировал семь результатов (один случай спазма, который не был идентифицирован, два случая, которые считались окклюзией, но были спазмом во время операции, три других случая, которые считались спазмом, но были нормальными, и один случай, который считался спазмом). быть окклюзия, но это было нормально во время операции). Для характеристики поражений согласие между наблюдателями было почти идеальным (κ = 0,95 при ретроспективном анализе; κ = 0,92, рецензент 1 по сравнению с проспективным анализом; κ = 0,91, рецензент 2 по сравнению с проспективным анализом).
Для характеристики поражений согласие между наблюдателями было почти идеальным (κ = 0,95 при ретроспективном анализе; κ = 0,92, рецензент 1 по сравнению с проспективным анализом; κ = 0,91, рецензент 2 по сравнению с проспективным анализом).
Распределение баллов полуколичественного анализа для рецензентов 1 и 2 дало средний балл 1,5 и 1,3 соответственно для общего качества изображения; 1.2 и 1.1 соответственно для изображения поражения; и 1.4 и 1.3 соответственно на наличие артефактов.Согласие между наблюдателями было существенным для оценки качества изображения (κ = 0,62), описания поражения (κ = 0,68) и наличия артефактов (κ = 0,69). Артефакты от незначительных до умеренных, которые не ставили под угрозу диагноз, возникали в нескольких случаях и были связаны либо с движением пациента во время получения КТ, в основном наблюдаемым при исследовании предплечья и кисти или голени и стопы, либо с расположением верхней конечности вдоль тела пациента. тело.
тело.
| Просмотреть увеличенную версию (167K) | Рис.2 —Мужчина, 19 лет, тупая травма правой руки. Ангиограмма руки с объемной МСКТ показывает окклюзию локтевой ( стрелки ) и лучевой собственной ладонной пальцевой артерии указательного пальца. На изображении также виден субкапитальный перелом проксимальной фаланги. Операция подтвердила наличие обеих окклюзий, которые были вторичными по отношению к разрыву локтевой и диссекции лучевых пальцевых артерий. |
| Посмотреть увеличенную версию (171K) | Рис.3 —Мужчина 46 лет с тупой травмой левой стопы. Ангиограмма стопы с МСКТ с объемной визуализацией показывает окклюзию ( стрелка ) проксимального сегмента первой тыльной плюсневой артерии, связанную с окклюзией второй и третьей тыльных плюсневых артерий и гипоперфузией мягких тканей в медиодорсальной части переднего отдела стопы. |
Что касается влияния алгоритмов постобработки на восприятие артериального повреждения, многоплоскостное преобразование облегчило оценку 53 ангиограмм МСКТ и не дало преимущества перед аксиальными изображениями в 34 ( p = 0.054, непараметрический биномиальный тест). Для сравнения, объемная визуализация облегчила оценку артериальной сосудистой сети у 72 пациентов, но не дала диагностических преимуществ у 15 пациентов ( p = 0,001, непараметрический биномиальный тест). Ни многоплоскостная реконструкция, ни объемная визуализация ни в коем случае не давали диагностической информации, которая еще не была раскрыта на аксиальных исходных изображениях. Многоплоскостные реконструктивные изображения превосходили объемные изображения у семи пациентов, поскольку позволяли обнаружить расслоение артерии, тогда как объемные изображения были предпочтительнее многоплоскостных реконструкций у 66 пациентов, поскольку они давали более полную визуализацию исследуемой области. У 14 пациентов многоплоскостная реконструкция и объемная визуализация были одинаковыми по эффективности. Соответственно, непараметрический биномиальный тест показал, что аксиальные исходные изображения значительно ( p < 0,001) более надежны, чем многоплоскостная реконструкция и объемные изображения для диагностики травматических повреждений артерий конечностей, а объемные изображения значительно ( p 90 800 < 0,001) более полезны, чем изображения многоплоскостной реконструкции.
У 14 пациентов многоплоскостная реконструкция и объемная визуализация были одинаковыми по эффективности. Соответственно, непараметрический биномиальный тест показал, что аксиальные исходные изображения значительно ( p < 0,001) более надежны, чем многоплоскостная реконструкция и объемные изображения для диагностики травматических повреждений артерий конечностей, а объемные изображения значительно ( p 90 800 < 0,001) более полезны, чем изображения многоплоскостной реконструкции.
С точки зрения влияния на окончательный диагноз, МСКТ-ангиография была сочтена авторами обзора 1 и 2 достаточной для надежной диагностики у 83 и 84 пациентов ( p < 0.001, непараметрический биномиальный тест), соответственно, тогда как дополнительная информация, полученная с помощью цифровой субтракционной ангиографии, по-прежнему требовалась для четырех и трех пациентов соответственно. Согласие между исследователями в отношении надежности МСКТ-ангиографии как начального исследования травматических поражений артерий было почти идеальным (κ = 0,85).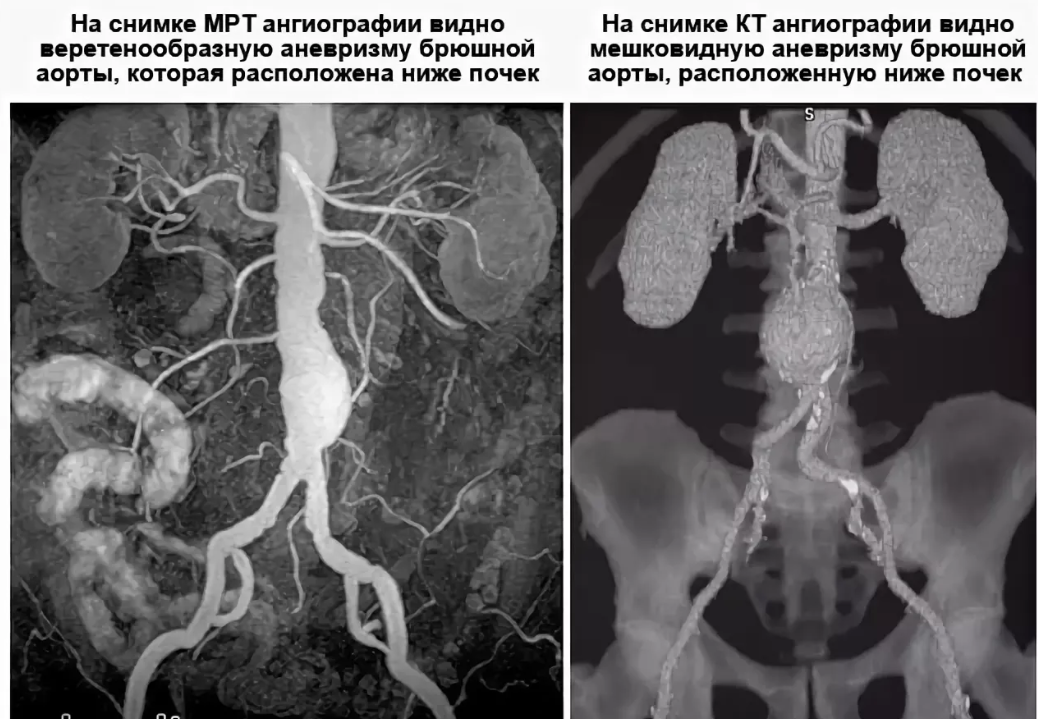
| Посмотреть увеличенную версию (55K) | На поперечном КТ изображен тяжелый эксцентрический стеноз ( стрелка ) с полулунной деформацией (за счет интрамуральной гематомы) просвета подколенной артерии на уровне проксимальной трети в сочетании с окклюзией (не показано) средней и дистальной третей подколенной артерии. |
| Посмотреть увеличенную версию (101K) | Рис. МДКТ-ангиография.КТ с объемной визуализацией показывает эксцентрический стеноз ( стрелка ) проксимальной трети и окклюзию средней и дистальной третей подколенной артерии. Операция подтвердила наличие окклюзии, вызванной расслоением артерии. Рис. 5 и дистальные радиомалоберцовые суставы и дистальные отделы малоберцовой кости прошли МСКТ-ангиографию стопы и дистального отдела голени.Косая сагиттальная многоплоскостная реформация показывает полную облитерацию ( стрелки ) передней большеберцовой артерии, что указывает на окклюзию. |
| Посмотреть увеличенную версию (49K) | Рис.7A — 25-летнему мужчине с тупой травмой левого бедра с открытым переломом диафиза бедренной кости и последующим диффузным кровотечением и эмфиземой мягких тканей выполнена МСКТ-ангиография бедра. |
| Посмотреть увеличенную версию (50K) | при эмфиземе мягких тканей выполнена МСКТ-ангиография голени.На поперечном КТ-изображении дистальнее A показано сегментарное, концентрическое, гладкое сужение ( стрелка ) поверхностной бедренной артерии, указывающее на фокальный неокклюзионный спазм. На изображении также видны вывихнутые костные фрагменты ( наконечников стрелок ). Операция подтвердила проходимость поверхностной бедренной артерии. |
| Посмотреть увеличенную версию (74K) | при эмфиземе мягких тканей выполнена МСКТ-ангиография голени.Ангиограмма МСКТ с визуализацией объема показывает полисегментарное, концентрическое, гладкое сужение ( стрелки ) поверхностной бедренной артерии, указывающее на фокальный неокклюзионный спазм. |
| Обсуждение | выберите К началу страницыРЕФЕРАТВведениеМатериалы и методыРезультатыОбсуждение <<Ссылки СО ССЫЛКАМИ НА СТАТЬИ |
|---|
Несмотря на то, что цифровая субтракционная ангиография остается золотым стандартом диагностики травматических повреждений сосудов конечностей [5-8], от нее все чаще отказываются для визуализации предполагаемых повреждений сосудов на руки и ноги [1, 2, 4, 9, 10], тогда как цветная допплерография [4, 29], МРТ [30] и однодетекторная КТ-ангиография [17, 18] пропагандируются как альтернативная неинвазивная диагностика. инструменты.
У пациентов с травматическими повреждениями, особенно с подозрением на поражение сосудов, как цветная допплерография, так и МР-ангиография имеют существенные ограничения, т. е. обе требуют значительного времени для постановки диагноза. Кроме того, цветная допплерография зависит от оператора, может быть ограничена при оценке артериального кровотока дистальнее артериального повреждения и может быть неприменима у пациентов с открытой травмой, а наличие коллатеральной сосудистой сети может давать ошибочные результаты.МР-ангиография более чувствительна к артефактам движения, чем КТ-ангиография, и может быть неприменима для пациентов с металлическими фиксирующими устройствами.
Кроме того, цветная допплерография зависит от оператора, может быть ограничена при оценке артериального кровотока дистальнее артериального повреждения и может быть неприменима у пациентов с открытой травмой, а наличие коллатеральной сосудистой сети может давать ошибочные результаты.МР-ангиография более чувствительна к артефактам движения, чем КТ-ангиография, и может быть неприменима для пациентов с металлическими фиксирующими устройствами.
В этом исследовании мы оценили клиническую полезность МСКТ-ангиографии в качестве первоначального метода визуализации сосудов у пациентов с травматическим повреждением нижней или верхней конечности. Во всех случаях МСКТ-ангиография позволила комплексно идентифицировать магистральные артерии и их основные ветви в исследуемой области. Статистический анализ показал, что МСКТ-ангиография позволяет точно и воспроизводимо выявлять травматические повреждения артерий.Действительно, наше раннее наблюдение показало, что при МСКТ-ангиографии не было пропущено ни одного хирургически значимого поражения. Более того, при большинстве повреждений артерий была правильно определена характеристика поражения. Однако обнаружение основного расслоения поврежденного сегмента было немного менее надежным, особенно в сегментах с окклюзией.
Наличие и тяжесть основного расслоения являются важными факторами при определении хирургической стратегии. Хотя фокальные лоскуты интимы, не оказывающие гемодинамического влияния на перфузию конечности, не требуют хирургического вмешательства [3], разрывы интимы с облитерацией просвета сосудов или возникающим в результате тромбозом требуют немедленного лечения для восстановления кровотока и перфузионного давления дистальнее места повреждения.В нашем учреждении разрывы интимы с полной артериальной облитерацией лечат хирургическим путем с помощью венозного интерпозиционного шунта (обычно полученного из большой подкожной вены), а разрывы интимы с последующим тромбозом подвергают тромбэктомии или интервенционной реваскуляризации.
Как при проспективной оценке, так и при ретроспективном обзоре были сделаны ложноположительные и ложноотрицательные интерпретации. Наиболее ошибочно классифицированные поражения при МСКТ-ангиографии были связаны с тяжелыми спазмами, которые полностью или частично исчезли до операции.Интересно, что некоторые спазмы были настолько сильными, что имитировали полную обструкцию при МСКТ-ангиографии. Действительно, при МСКТ-ангиографии считалось, что четыре артериальных сегмента окклюзированы (два у обоих обозревателей и по одному у каждого обозревателя), в то время как операция подтвердила проходимость артерии. О подобных случаях сообщалось [6, 17]. Мы считаем, что в таких случаях непрерывный мониторинг пульса и прицельная допплерография дистальнее места повреждения могут помочь распознать уменьшение спазма перед операцией на сосудах, что может предотвратить ненужную операцию.В нашем исследовании свободный артериальный кровоток в области травмы был подтвержден у 12 пациентов во время операции. У всех 12 пациентов были травмы, потребовавшие открытой операции, во время которой была подтверждена целостность артерий.
Результаты нашего исследования показывают, что МСКТ-ангиография позволяет визуализировать не только проксимальные отделы конечностей, как показано Soto et al. [17, 18], а также периферическое артериальное кровоснабжение конечности, которое должно быть всесторонне показано с высоким качеством изображения, хорошей прорисовкой сосудов и улучшенным изображением поражения.Кроме того, было возможно выявление повреждений артерий кисти и стопы. Несмотря на то, что верхняя конечность располагалась вдоль тела пациента, были замечены только незначительные или легкие штриховые артефакты без каких-либо диагностических компромиссов. Нейтральное положение пораженной конечности при МСКТ-ангиографии не требовалось. Произвольное положение пораженной конечности, определяемое лечащей клинической бригадой, не усложняло оценку набора данных КТ или распознавание анатомических взаимоотношений.
Несколько исследователей рекомендовали применение методов постобработки, таких как многоплоскостное преобразование и визуализация объема, для более надежной оценки наборов данных КТ [25, 31-34]. Наше исследование показало, что многоплоскостные преобразования и объемные изображения исследуемой конечности облегчают оценку сосудистых структур и их связи с костными структурами и могут сократить время интерпретации изображений по сравнению с интерпретацией большого количества аксиальных исходных сканов.Кроме того, хотя мы формально не изучали полезность визуализированных проекций для хирургов, у нас сложилось впечатление, что хирурги с большей готовностью восприняли такие изображения, чем просмотр аксиальных изображений в кинорежиме на консоли PACS. Тем не менее, все артериальные поражения были адекватно обнаружены и охарактеризованы при аксиальном сканировании источника, преимущество которого заключалось в выявлении расслоившегося лоскута, если он присутствовал.
Основным ограничением нашего исследования является его ретроспективный дизайн.Тем не менее, все исследования были выполнены в экстренном порядке рентгенологической бригадой, включая старшего радиолога, и были получены и реконструированы в соответствии со стандартными протоколами, разработанными проспективно и слегка модифицированными для веса пациента и размера области интереса. Другим ограничением нашего исследования является то, что у большинства пациентов стандартным эталоном была операция, выполненная в течение 1 часа после МСКТ-ангиографии, что приводило к увеличению частоты ложноположительных артериальных окклюзий, которые представляли собой преходящие спазмы.Хотя может помочь внутриартериальное введение вазодилататоров, дифференциальная диагностика между тяжелым спазмом и окклюзией также может быть затруднена при цифровой субтракционной ангиографии. Кроме того, хирургическое вмешательство подтверждает ангиографические данные МСКТ только на уровне повреждения, а не для всей исследуемой артериальной системы; следовательно, мы могли пропустить некоторые повреждения в сегментах артерий, которые не имели близости к области травмы и поэтому не были исследованы. Как и при цифровой субтракционной ангиографии, наличие хорошо контрастированного гладкого артериального сегмента без визуализируемых внутрипросветных, пристеночных и внесосудистых аномалий на МСКТ-ангиографии исключает серьезное анатомическое повреждение, требующее хирургического или интервенционного лечения.Кроме того, в нашем исследовании может быть систематическая ошибка проверки, поскольку в некоторых случаях хирургическое вмешательство выполнялось на основе ангиографических данных МСКТ. Однако хирургическое вмешательство было показано большинству пациентов из-за переломов, дефектов мягких тканей или инородных тел. Для пациентов, которым не было показано хирургическое вмешательство, в качестве эталона использовалось последующее наблюдение, поэтому в нашем исследовании не было единого золотого стандарта для всех пациентов. Наконец, относительно небольшая группа пациентов, особенно с повреждением артерий, и отсутствие пациентов с псевдоаневризмой или артериовенозной мальформацией представляют ограничения этого исследования.Хотя все пять пациентов с проникающими ранениями в нашем исследовании были адекватно обследованы с помощью МСКТ-ангиографии, их малое количество может не позволить обобщить результаты исследования в таких случаях.
Подводя итог, мы заключаем, что МСКТ-ангиография обеспечивает значительную и воспроизводимую выявляемость и характеристику травматического повреждения артерий конечностей с высоким качеством изображения и определением границ сосудов.
- Год и три месяца развитие: Развитие детей от 1 года до 2 лет
- Ролевые игры 18 сценарий: Ролевые игры в постели: 5 горячих сценариев: Отношения: Любовь и секс

 Повышенный уровень холестерина липопротеинов низкой плотности («плохого холестерина»)и высокий уровень триглицеридов способствует формированию атеросклеротических бляшек.
Повышенный уровень холестерина липопротеинов низкой плотности («плохого холестерина»)и высокий уровень триглицеридов способствует формированию атеросклеротических бляшек. Крупные тромбы могут частично или полностью перекрывать просвет артерии, тем самым, препятствуя кровотоку и вызывая инсульт.
Крупные тромбы могут частично или полностью перекрывать просвет артерии, тем самым, препятствуя кровотоку и вызывая инсульт. Врач также может провести неврологический осмотр с оценкой вашего физического и ментального статуса, например, оценит силу в конечностях, возможности запоминания устной речи.
Врач также может провести неврологический осмотр с оценкой вашего физического и ментального статуса, например, оценит силу в конечностях, возможности запоминания устной речи.

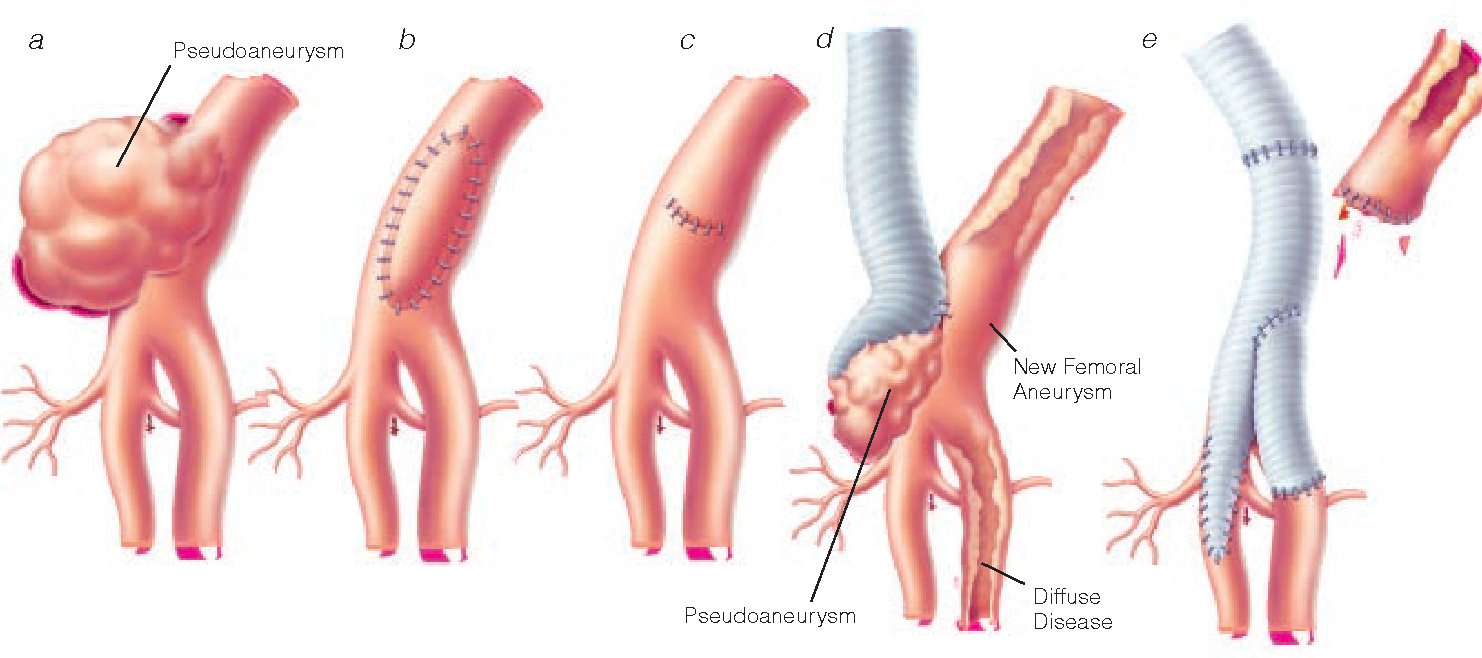 Этот метод лечения является наиболее распространенным при выраженных сужениях сонных артерий. Вмешательство выполняется под общим обезболиванием и заключается в удалении атеросклеротической бляшки через небольшой разрез сонной артерии. В завершении сонная артерия либо просто ушивается, либо, производится пластика при помощи синтетической заплаты. Многочисленные исследования показали, что выполнение хирургического вмешательства значительно уменьшает риск возникновения инсульта.
Этот метод лечения является наиболее распространенным при выраженных сужениях сонных артерий. Вмешательство выполняется под общим обезболиванием и заключается в удалении атеросклеротической бляшки через небольшой разрез сонной артерии. В завершении сонная артерия либо просто ушивается, либо, производится пластика при помощи синтетической заплаты. Многочисленные исследования показали, что выполнение хирургического вмешательства значительно уменьшает риск возникновения инсульта.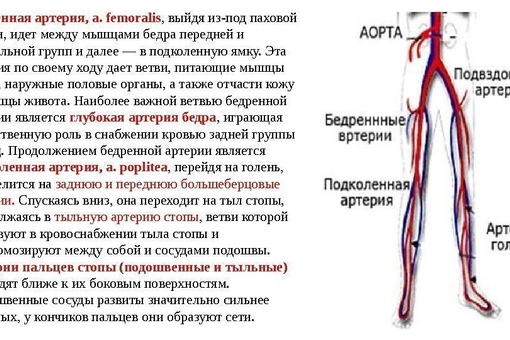 Процедура выполняется под местной анестезией.
Процедура выполняется под местной анестезией. При этом люди вынуждены через определенное время делать остановки во время ходьбы, чтобы избавиться от болей. Этот этап также делится на дополнительные стадии, в зависимости от пройденного человеком расстояния.
При этом люди вынуждены через определенное время делать остановки во время ходьбы, чтобы избавиться от болей. Этот этап также делится на дополнительные стадии, в зависимости от пройденного человеком расстояния. Боль носит давящий, тупой ноющий или жгучий характер. Болевые ощущения могут отдавать в лопатку, левое предплечье, кисть или пальцы.
Боль носит давящий, тупой ноющий или жгучий характер. Болевые ощущения могут отдавать в лопатку, левое предплечье, кисть или пальцы. Болит вся голова, без точной локализации.
Болит вся голова, без точной локализации.

 При достаточных физических нагрузках уровень «плохого» холестерина обычно снижается. Регулярные физические упражнения помогают организму выводить жир, «Плохойе» холестерин надолго не задерживается в кровяном русле, он не успевает осесть на стенках сосудов. Доказано, что бег способствует выведению полученного из продуктов жира. Именно люди, регулярно бегающие меньше всего подвержены образованию холестериновых бляшек.
При достаточных физических нагрузках уровень «плохого» холестерина обычно снижается. Регулярные физические упражнения помогают организму выводить жир, «Плохойе» холестерин надолго не задерживается в кровяном русле, он не успевает осесть на стенках сосудов. Доказано, что бег способствует выведению полученного из продуктов жира. Именно люди, регулярно бегающие меньше всего подвержены образованию холестериновых бляшек.
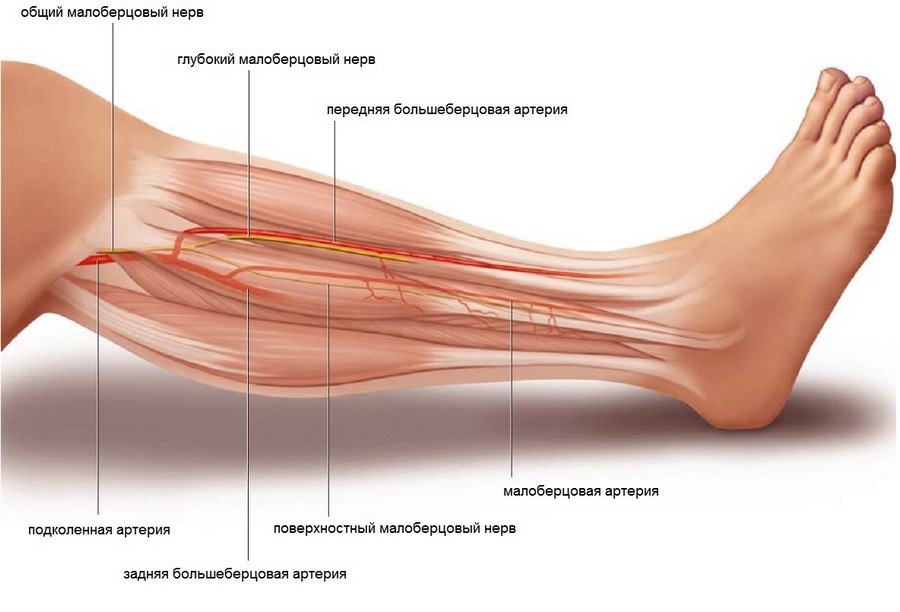 Операция подтвердила окклюзию трех плюсневых артерий из-за компартмент-синдрома.
Операция подтвердила окклюзию трех плюсневых артерий из-за компартмент-синдрома. На изображении также показаны концентрические сужения ( стрелки ) передней большеберцовой артерии, указывающие на спазмы. МСКТ также выявила окклюзию дистальных отделов задней большеберцовой и малоберцовой артерий (не показано). Операция подтвердила окклюзию задней большеберцовой и малоберцовой артерий из-за расслоения, но выявила проходимость передней большеберцовой артерии, что указывает на артериальный спазм во время выполнения МСКТ.Рис. Ангиограмма МСКТ с объемной визуализацией показывает отклонение и небольшое эксцентрическое сужение ( стрелка ) просвета подколенной артерии на уровне перелома. Во время операции были подтверждены артериальная девиация и компрессия.
На изображении также показаны концентрические сужения ( стрелки ) передней большеберцовой артерии, указывающие на спазмы. МСКТ также выявила окклюзию дистальных отделов задней большеберцовой и малоберцовой артерий (не показано). Операция подтвердила окклюзию задней большеберцовой и малоберцовой артерий из-за расслоения, но выявила проходимость передней большеберцовой артерии, что указывает на артериальный спазм во время выполнения МСКТ.Рис. Ангиограмма МСКТ с объемной визуализацией показывает отклонение и небольшое эксцентрическое сужение ( стрелка ) просвета подколенной артерии на уровне перелома. Во время операции были подтверждены артериальная девиация и компрессия. Поперечное КТ-изображение на уровне перелома показывает проходимость поверхностной бедренной артерии (, стрелка ) и смещенный фрагмент кости (, наконечник стрелки, ).
Поперечное КТ-изображение на уровне перелома показывает проходимость поверхностной бедренной артерии (, стрелка ) и смещенный фрагмент кости (, наконечник стрелки, ).