Воспаление надкостницы чем лечить: что это такое, симптомы, лечение.
Периостит челюсти – что это|Симптомы и лечение периостита зуба
Периостит — это воспаление надкостницы, которое чаще всего развивается в результате других заболеваний. Обычно воспалительный процесс начинается в одном слое надкостницы, а по мере развития болезни распространяется и на остальные. Кость и надкостница тесно связаны друг с другом, поэтому существует вероятность развития осложнения в виде остеопериостита — распространения воспаления в том числе на костную ткань.
Неосложненные формы периостита лечат врачи-стоматологи. Кроме лечения этого заболевания, важно обратить внимание и на терапию основной патологии, которая стала причиной воспаления.
Причины периостита
Причиной периостита челюсти может стать травма, а также воспалительное заболевание в полости рта — пульпит, периодонтит, острый гингивит и пр. Более редкими причинами считаются ревматические заболевания, патологии вен, специфические инфекции, аллергические реакции, хронические соматические заболевания.
Классическим вариантом развития болезни является осложненный пульпитом кариес. Воспаление распространяется на околозубные ткани, появляется периодонтит — воспаление околозубных тканей. При отсутствии лечения поражается и надкостница. В этом случае речь идет об одонтогенном периостите — болезни, появившейся на фоне заболевания зуба.
Виды и симптомы периостита
Периостит может быть острым и хроническим, асептическим и инфекционным. В зависимости от характера протекания болезни выделяют несколько видов болезни, каждый из которых сопровождается типичными проявлениями. Заболевание может поражать любые кости, но чаще появляется в области нижней челюсти.
Простой
Простой периостит зуба — это асептический воспалительный процесс, развивающийся на фоне ушиба или перелома, а также в связи с очагами воспаления вблизи надкостницы, например, в мышцах. Болезнь сопровождается умеренной отечностью мягких тканей.
Фиброзный периостит формируется при длительном воспалительном процессе, начинается постепенно, протекает в хронической форме. Время от времени могут возникать обострения. Эта форма болезни предполагает образование новой ткани на поверхности челюсти.
СерозныйСерозная форма болезни сопровождается образованием инфильтрата — в очаге воспаления появляется серозный экссудат. При отсутствии лечения острого периостита этого вида воспаления существует вероятность развития гнойных процессов, характеризующихся более тяжелым течением.
Гнойный
Гнойный периостит может быть следствием попадания инфекции, например, при травмах, сопровождающихся повреждением надкостницы, распространении воспалительного процесса из других очагов (флегмоны).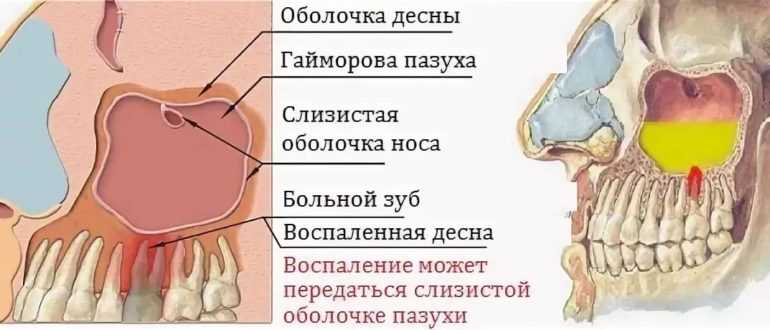
Также выделяют острейший периостит с преобладанием гнилостных процессов. Надкостница набухает, распадается, а гнойное содержимое попадает непосредственно к кости, распространяется в мягких тканях, что приводит к флегмоне челюсти. Это опасное осложнение может стать причиной тяжелых последствий и даже летального исхода.
По происхождению выделяют следующие виды периостита:
- Одонтогенный, или воспалительный: развивается при прогрессировании воспаления в надкостнице и полости рта. Обычно появляется как результат невылеченных стоматологических заболеваний, чаще всего – кариеса и его осложнений (пульпита, периодонтита).

- Гематогенный: связан с попаданием инфекции в надкостницу через кровеносную систему. Вероятная причина – наличие очагов инфекции близко к челюстям – тонзиллита (воспаления миндалин) или синусита (воспаления околоносовых пазух).
- Лимфогенный: такой вид воспаления подразумевает попадание инфекции в надкостницу с током лимфы. Здесь, как и в случае с гематогенным периоститом, роль могут играть воспалительные заболевания верхних дыхательных путей, лимфатических узлов и пр.
- Травматический: в этом случае воспаление развивается на фоне травм челюсти и других повреждений надкостницы.
- Аллергический: такая форма заболевания встречается очень редко, связана она с аллергическими реакциями в виде воспаления.
Симптомы периостита зависят от формы болезни, общего состояния здоровья, наличия или отсутствия хронических патологий, возраста и пр. К типичным признакам относят следующие:
- покраснение слизистых оболочек десны, отечность;
- болезненность, усиливающаяся при надавливании, жевании, приеме горячих напитков;
- повышение температуры тела;
- асимметрия лица, отек щеки;
- увеличение подчелюстных, заушных, иногда шейных лимфатических узлов и пр.

Стоит отметить, что гнойная форма болезни протекает быстрее, сопровождается симптомами общей интоксикации, более высокой температурой, иррадиацией боли в висок, ухо. Многие отмечают характерную пульсацию в очаге воспаления.
Методы диагностики
Часто осмотра стоматолога достаточно для обнаружения периостита, однако важно оценить состояние околозубных тканей, костей челюсти, определить границы воспаления. Для этого проводится рентгенография. Периостит на рентгене определить легко — врач увидит степень и распространенность поражения и примет решение о подходящей тактике лечения.
В ряде случаев проводят лабораторные исследования, это особенно актуально при общем плохом самочувствии.
Методы лечения
Гнойное воспаление надкостницы челюсти требует хирургического вмешательства. Операция включает в себя три этапа:
1. Обезболивание. Перед введением анестетика область инъекции также может быть обезболена с помощью аппликационного препарата.
2. Периостомия. Врач выполняет небольшой разрез мягких тканей, обычно по складке между щекой и десной, захватывая надкостницу. Это необходимо для выведения гнойного содержимого очага воспаления, а также промывания образованной полости антисептиками.
3. Установка дренажа. Дренирование предусматривает введение резинового, реже марлевого лоскута внутрь разреза. Это помогает предупредить преждевременное зарастание тканей и отток гнойного экссудата еще в течение нескольких дней.
Специалист назначит растворы для полоскания полости рта, а также расскажет, как часто нужно являться на прием для замены дренажа. Обычно наложение швов не предполагается, впоследствии рана затягивается самостоятельно. Такой метод позволяет сохранить зуб, если специалист принимает такое решение на основании данных осмотра и рентгеновского снимка.
Серозная форма заболевания может подлежать консервативной терапии. Могут использоваться антибактериальная терапия, физиотерапевтические методы, полоскания и пр.
Могут использоваться антибактериальная терапия, физиотерапевтические методы, полоскания и пр.
Лечение периостита у детей тоже часто требует хирургического вмешательства. Однако подход строго индивидуален. Врач учитывает возраст ребенка, стадию развития болезни, общее состояние маленького пациента. Обычно лечение занимает до 10 дней.
Острый гнойный процесс требует установки дренажа. Чтобы вывести гной из тканей, врач выполняет небольшой разрез под местным обезболиванием и вставляет в него специальную резинку для предотвращения зарастания раны. За несколько дней гной выводится, а состояние ребенка улучшается.
В течение всего периода дренирования важно принимать назначенные медикаменты. Специалист выпишет антибиотики, если это необходимо, и порекомендует проводить полоскание рта антисептиками.
После очищения полости от гнойного содержимого пораженный зуб обычно подлежит удалению, его редко удается сохранить. Консервативное лечение целесообразно только при отсутствии гнойного процесса и отека.
Лечением некоторых форм периостита успешно занимаются стоматологи- хирурги сети клиник «СТОМА». Наличие современной аппаратуры, качественных инструментов и препаратов позволяет нам в некоторых клинических случаях оказать помощь пациентам с острым состоянием и предупреждать возможные осложнения. Записаться на прием вы можете по телефону или через специальную форму на сайте.
Список литературы
- Скрипников П. Н., Эйхгорн Т. Ю., Коломиец С. В., Митько М. С. Особенности первичной реплантации зубов при хронических периодонтитах в стадии обострения и острых периоститах челюстей // Мир медицины и биологии. – 2009. − № 3. – С. 679.
- Гандылян К. С., Карпов С. М., Романенко И. П., Караков К. Г., Зеленский В. А., Порфириадис М. П., Хачатурян Э. Э., Доменюк Д. А., Чалая Е. Н. Острые одонтогенные воспалительные заболевания, варианты течения различных клинических форм // Медицинский Вестник Северного Кавказа. – 2015. – Т. 10, № 4. – С. 395−397.

- Романенко И. С., Конев С. С., Гандылян К. С., Карпова Е. Н., Баландина А. В., Апагуни А. Э. Клиническая характеристика различных вариантов течения острых одонтогенных воспалительных заболеваний // Российский стоматологический журнал. – 2015. – № 19(6). – С. 30–33.
Воспаление надкостницы при беге: причины, лечение, профилактика
Содержание:
- Что такое надкостница
- Воспаление надкостницы или шинсплинт
- Почему болит надкостница при беге
- Кто чаще сталкивается с воспалением надкостницы голени
- Что делать, если болит надкостница
- Видео о проблемах с надкостницей
Боли в надкостнице — проблема начинающих и слишком амбициозных спортсменов. Мало кто знает, но пики запроса «болит надкостница» в поисковиках приходятся на апрель-май и сентябрь-октябрь. Как раз на начало бегового сезона и период крупных марафонов.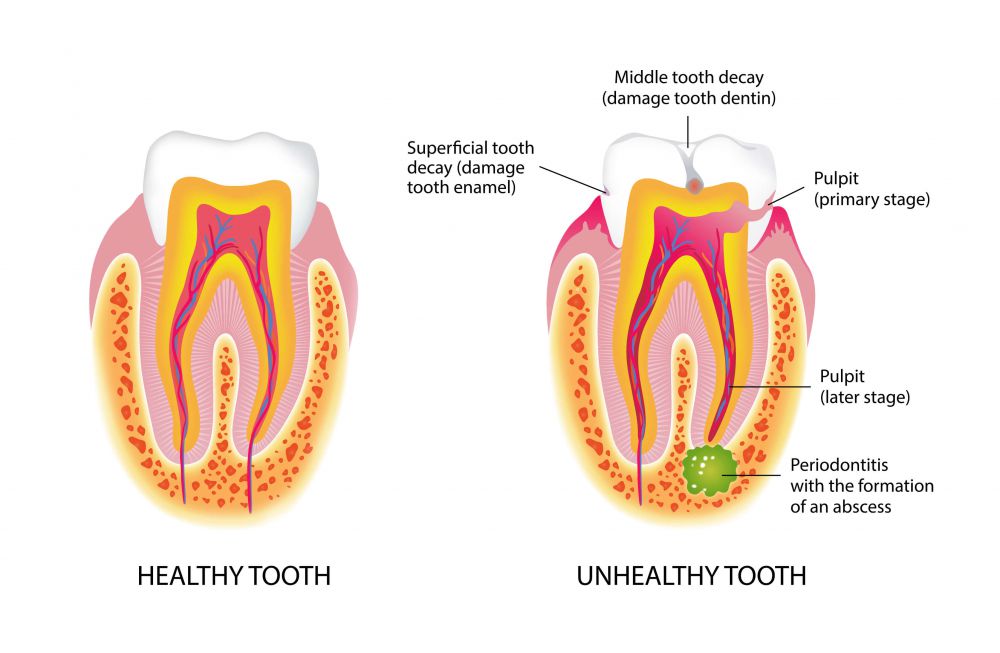 Это не совпадение, в этой закономерности и кроются основные причины болей в надкостнице. В статье кратко и понятно рассказываем, что такое надкостница, почему она болит и как этого избежать.
Это не совпадение, в этой закономерности и кроются основные причины болей в надкостнице. В статье кратко и понятно рассказываем, что такое надкостница, почему она болит и как этого избежать.
Что такое надкостница
Надкостница — это соединительная ткань, которая обволакивает кости снаружи. Она есть у всех костей в организме, соединяет кость с мышцами, участвует в кровоснабжении и росте кости в толщину. Надкостница производит молодые клетки костной ткани — остеобласты, с помощью которых происходит регенерация кости.
Воспаление надкостницы или шинсплинт
Воспаление надкостницы — частая проблема бегунов, особенно начинающих. Боль возникает в области передней и внутренней поверхности большеберцовой кости. Иногда локализуется в одной точке, но чаще распространяется по всей голени.
Воспаление надкостницы относится к группе заболеваний шинсплинт (Shin splints — «расколотая голень»). Помимо воспаления надкостницы, в группу шинсплинт входят другие заболевания области голени: воспаления мышц и связок, стрессовый перелом. Основная причина заболеваний группы шинсплинт — силишком большая физическая нагрузка.
Основная причина заболеваний группы шинсплинт — силишком большая физическая нагрузка.
Фото: jspodiatry.com
Симптомы на ранней стадии:
- Боль незначительная, концентрируется во внутренней части голени, чаще на границе голени и икроножных мышц
- Боль возникает в начале и в конце тренировки, ощущается при надавливании
Симптомы в запущенном состоянии:
- Ноющая боль и ощущение жжения во время ходьбы и в состоянии покоя
- Боль может распространиться по всей голени и отдавать в стопу или бедро
- Голень отекает и краснеет
- Повышается температура тела
Почему болит надкостница при беге
Раньше за причину шинсплинта принимали микроразрывы мягких тканей в месте прикрепления к надкостнице. Последние исследования показали, что при таких болях повреждаются сами кости, в очагах боли плотность кости становится ниже. После курса лечения боли пропадают, плотность костной ткани приходит в норму.
В большинстве случаев боль в надкостнице возникает из-за перегрузки. Проще говоря, если бегаете слишком много или слишком быстро. Дополнением к этому могут быть слабые мышцы, избыточный вес, неправильная обувь, нарушения пронации, техника бега. Самые распространенные ошибки: «втыкание» при приземлении и бег на носочках. Некоторые специально бегают на носочках, потому что кто-то там посоветовал.
При каждом приземлении во время бега голень немного изгибается под нагрузкой. При правильной работе мышц большая часть ударной нагрузки гасится за счет удлинения мышцы. Часть удара приходятся на связки и сухожилия. Если бегать слишком много, мышцы «забиваются», становятся менее эластичными. В таком состоянии они не могут поглотить ударную нагрузку, она передается на связки и надкостницу, что приводит к микротравмам и воспалениям.
Когда нагрузки дозированные, опорно-двигательный аппарат адаптируется: мышцы, кости и надкостница становятся крепче и переносят большие нагрузки. Если поднимать нагрузку резко, организм не успевает адаптироваться, ткань становится менее плотной — это ведет к воспалениям, трещинам и усталостным переломам.
Причины проблем с надкостницей:
- неправильная техника бега (постановка стопы)
- слишком высокая интенсивность или большой объем тренировок
- «забитость» мышц голени, которая вытекает из предыдущей причины
- плохая разминка и заминка
- мышечный дисбаланс и слабые мышцы-стабилизаторы
- некачественные или изношенные кроссовки
- бег по пересеченной местности без предварительной подготовки
Фото: lzf/Gettyimages
Кто чаще сталкивается с воспалением надкостницы голени
С болями в надкостнице чаще сталкиваются бегуны, футболисты, баскетболисты, танцоры, военные. Такой травме подвержены, чаще всего, менее опытные спортсмены и новички. У женщин эта травма встречается в 2-3 раза чаще, чем у мужчин.
Кроме того, в группе риска люди с:
- слабыми мышцами
- избыточным весом
- нарушениями работы стопы (гиперпронация, плоскостопие)
- слабыми костями (причины могут разные)
Что делать, если болит надкостница
- Перестаньте тренироваться.
 На ранних стадиях проблема с надкостницей может решиться простым отдыхом. Исключите ударную нагрузку на ноги, чтобы поврежденные ткани успели восстановиться. Если нет возможности полностью прекратить занятия — тренируйтесь без ударной нагрузки на ноги. Перейдите на более щадящий режим: замените бег на плавание или велосипед.
На ранних стадиях проблема с надкостницей может решиться простым отдыхом. Исключите ударную нагрузку на ноги, чтобы поврежденные ткани успели восстановиться. Если нет возможности полностью прекратить занятия — тренируйтесь без ударной нагрузки на ноги. Перейдите на более щадящий режим: замените бег на плавание или велосипед. - Обратитесь к врачу. Подойдет ортопед-травматолог или врач спортивной медицины. Выявить проблему можно с помощью осмотра или дополнительных исследований: рентген или МРТ. Не пытайтесь самостоятельно ставить диагноз и подбирать лечение. Доверяйте свое здоровье специалистам.
Как лечить надкостницу
Восстановление надкостницы может занять от 2-3 недель до нескольких месяцев в зависимости от запущенности травмы. Поставить точный диагноз и назначить необходимое лечение может только специалист.
При воспалении надкостницы обычно назначают:
- лечение по принципу RICE (отдых, лед, давящая повязка и приподнятое положение ноги)
- нестероидные противовоспалительные средства
- мази с «охлаждающим эффектом»
- массаж мышц голени
Профилактика болей в надкостнице
Укрепляйте мышцы.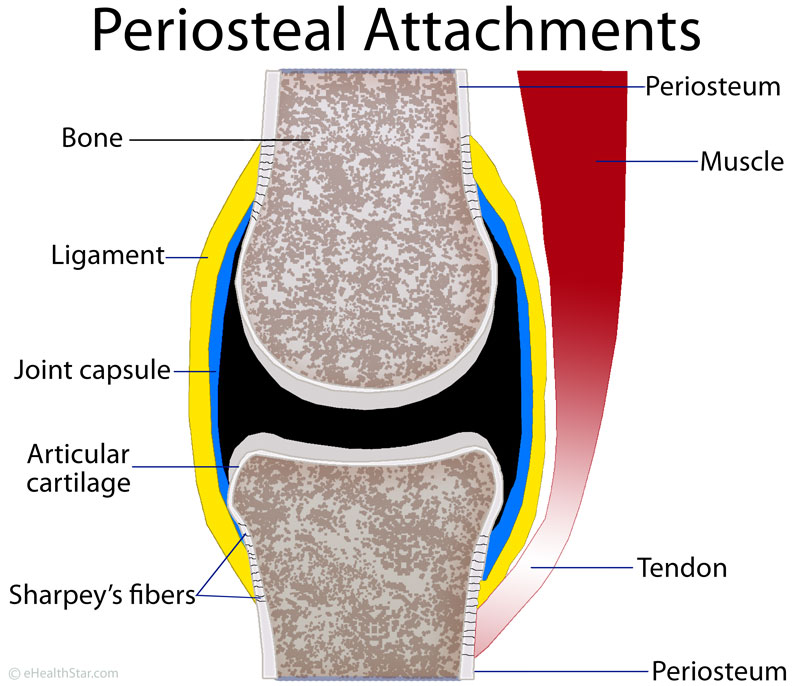 Большинство беговых травм случается из-за слабых мышц, которые не могут «переварить» беговые объемы. Регулярно делайте силовые упражнения, особенно на мышцы-стабилизаторы, укрепляйте голень и стопы. Чем тренированней и сильнее мышцы, тем меньшая нагрузка приходится на кости, связки и суставы. Вот почему у новичков проблемы с надкостницей встречаются чаще, чем у опытных спортсменов.
Большинство беговых травм случается из-за слабых мышц, которые не могут «переварить» беговые объемы. Регулярно делайте силовые упражнения, особенно на мышцы-стабилизаторы, укрепляйте голень и стопы. Чем тренированней и сильнее мышцы, тем меньшая нагрузка приходится на кости, связки и суставы. Вот почему у новичков проблемы с надкостницей встречаются чаще, чем у опытных спортсменов.
Наращивайте объемы постепенно. Перегруз на тренировках — одна из основных причин проблем со здоровьем у спортсменов. Порой кажется, что вы готовы бежать быстрее и дольше — но это не значит, что организм готов к высоким нагрузкам. Чтобы не заработать травму, наращивайте объем тренировок не более, чем на 10% в неделю.
Следите за техникой бега. Учитесь бегать легче и делать шаги чаще, правильно ставьте стопу при приземлении. Качество бега можно определить по каденсу. Если он низкий — ваш бег неэкономичный. Каденс 150 и ниже у новичков говорит о неправильной технике бега. Длинные шаги увеличивают ударную нагрузку на ноги, которая приводит к травмам голеностопа.
Длинные шаги увеличивают ударную нагрузку на ноги, которая приводит к травмам голеностопа.
Подберите кроссовки. Исправить анатомические особенности стопы не получится, но погасить ударную нагрузку можно, правильно подобрав кроссовки. Почти у каждого спортивного бренда есть модели кроссовок для людей с плоскостопием и гиперпронацией. Не забывайте, что у кроссовок есть ресурс, после которого их нужно менять. Обычно это 800-1200 км, максимум 1500 км. После такого пробега пена стаптывается, перестает амортизировать, что может привести к травмам.
Видео о проблемах с надкостницей
youtube.com/embed/W5Jk9XczRU4?feature=oembed&wmode=opaque» frameborder=»0″ allow=»accelerometer; autoplay; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»>
Занимайтесь спортом, двигайтесь и путешествуйте! Если нашли ошибку или хотите обсудить статью – пишите в комментариях. Мы всегда рады общению.
Подписывайтесь на нас в Telegram, ЯндексДзен и Вконтакте
Периостит:Причины,Симптомы,Лечение | doc.ua
Причины
Причиной острого периостита могут быть ранее проявленные периодонтиты, хронический гайморит, пародонтит, кисты челюстей или характерные опухоли. Такая патология может развиваться из-за удаления зуба (альвеолит).
Эту форму заболевания разделяют на две характерные стадии:
- серозная – обнаруживается у 41% пациентов и проявляется в виде воспалительного процесса на надкостнице с сопровождением острого хронического периодонтита;
- гнойная – встречается у 59% пациентов. При этой стадии наблюдается отечность и разрушение надкостницы. Между костью и надкостницей скапливается изначально серозный, а потом уже и гнойный экссудат. Из-за этого образования нарушается кровоснабжение, что сопровождается глубокими патологическими изменениями. Также может наблюдаться проникновение гноя в гаверсовы каналы и в костномозговые пространства.
Воспалительный процесс при остром периостите или флюсе зуба может быть разнообразен и зависеть от возраста и пола пациента, от начала локализации воспалительного процесса, от состояния иммунной системы и прочего.
Замечено, что зубной флюс может проявляться вследствие переохлаждения, физического или эмоционального перенапряжения, перегрева.
Симптомы
Боль в зубе может быть различного характера: ноющего, утихающего, пульсирующего, постоянного, а также может иррадировать на часть головы. Эта боль может сопровождаться жалобами – невозможностью полного открытия рта, болью при жевании, глотании, движении языком. Локализация отека при флюсе на десне располагается в области расположения больного зуба.
Если провести осмотр ротового пространства, то флюс можно заметить за счет его характерного красного цвета, а также возвышения над десной, отека слизистой оболочки. В зависимости от процесса воспаления может образовываться подслизистый или поднадкостничный абсцесс. В некоторых случаях может произойти самопроизвольное разрешение патологического процесса – прорыв гноя из-под десневых участков. Такое обычно может происходить на шестые, седьмые сутки. Но также возможна необходимость удаления флюса при серьезных формах.
Наблюдается у большинства больных и увеличение, болезненность лимфатических узлов или некоторые симптомы интоксикации в виде слабости, плохого аппетита, недомогания, нарушения сна. Часто такое может сопровождаться у особ пожилого или старческого возраста при наличии характерных заболеваний (сахарный диабет, болезни сердечно-сосудистой системы, пищеварительного тракта).
Периостит челюсти может протекать по-разному, но многое зависит от расположения причинного зуба. Таким образом, патология характеризуется воспалительным процессом и отеком на губе или крыльях носа. Но если причинный зуб расположен вверху, то отек может распространяться и на область возле глаз, углы рта, щечную область. Иногда возможно даже частичное задевание лицевого нерва, а может доходить и до ушной раковины. В случае развития периостита на нижней десне отек образуется в районе нижней губы, подбородка.
Диагностика
Диагноз может быть определен из лабораторного исследования взятой крови у человека. В частности, для характерного воспаления отмечается небольшое повышение лейкоцитов (10–11*109/л), увеличение нейтрофилов (75–78%). Можно провести и рентгенографический анализ челюстей.
В частности, для характерного воспаления отмечается небольшое повышение лейкоцитов (10–11*109/л), увеличение нейтрофилов (75–78%). Можно провести и рентгенографический анализ челюстей.
Стоит знать и то, что клинические проявления периостита могут быть признаком и других острых болезней воспалительного характера. Таковыми могут быть острый остеомиелит, воспаление челюстных кист, хронический сиалоаденит, злокачественные или доброкачественные образования в виде опухолей.
Острый флюс отличается от хронического непосредственным воспалением очага и характерным проявлением воспалительной реакции. Если имеет место периодонтит, то воспаление проявляется в корне воспаленного зуба, а при периостите – проникает в надкостницу. Обычно периостит не проявляет свой воспалительный процесс в слюнные железы. Но порой наблюдается и выделение мутной слюны, такое может быть при острой форме, когда нагнаиваются кисты челюстей или встречаются характерные опухоли (доброкачественные, злокачественные). В таких случаях поможет рентгенография, которая определит патологический очаг.
В таких случаях поможет рентгенография, которая определит патологический очаг.
При симптомах флюса необходимо проводить лечение (если воспаление не проходит). Стоит знать и то, что если проведено адекватное лечение вместе с хирургическим вмешательством, осуществлено дренирование и проведена необходимая противовоспалительная терапия, но нет ощутимого эффекта, не исключается возникновение опухоли злокачественного характера. При этом оставлять этот аспект нельзя без внимания и стоит использовать методы для обнаружения образования.
Лечение
При наличии периостита необходимо проводить комплексное лечение. Оно непосредственно может включать хирургическое вмешательство с целью своевременного и целесообразного удаления патологии. Часто флюс, лечение которого осуществляется народными методами, проходит сам по себе.
При хирургическом вмешательстве могут оставлять однокорневые зубы, которые хорошо поддаются пломбированию. А вот насчет многокорневых зубов вопрос неоднозначен, так как их можно удалять, а можно и нет. Но, если удаление зуба может быть связано с травмой при операции (дистопированный или ретинированный зуб), то его удаление обычно откладывают, пока не утихнут воспалительные реакции – примерно 7–10 дней. Хирургическое лечение проводится с использованием местных обезболивающих средств. Иногда необходимо одновременно вскрыть абсцесс и удалить зуб, тогда первым образом проводится вскрытие абсцесса, а потом устранение зуба. Абсцесс вскрывают путем разрезания скальпелем в необходимом месте воспаления. При этом по возможности врач не должен делать разрез близко к десневому краю, так как в дальнейшем это может развить некроз десны в поврежденном месте. Обычно рассекают слизистую оболочку до самой кости, так как это способствует полноценному вскрытию гнойного очага. Через этот надрез вводят специальную полоску для осуществления дренирования.
Но, если удаление зуба может быть связано с травмой при операции (дистопированный или ретинированный зуб), то его удаление обычно откладывают, пока не утихнут воспалительные реакции – примерно 7–10 дней. Хирургическое лечение проводится с использованием местных обезболивающих средств. Иногда необходимо одновременно вскрыть абсцесс и удалить зуб, тогда первым образом проводится вскрытие абсцесса, а потом устранение зуба. Абсцесс вскрывают путем разрезания скальпелем в необходимом месте воспаления. При этом по возможности врач не должен делать разрез близко к десневому краю, так как в дальнейшем это может развить некроз десны в поврежденном месте. Обычно рассекают слизистую оболочку до самой кости, так как это способствует полноценному вскрытию гнойного очага. Через этот надрез вводят специальную полоску для осуществления дренирования.
В зависимости от расположения очага производятся надрезы в той или иной области. К примеру, если абсцесс образовался на нижней челюсти, то надрез делают в параллельном или перпендикулярном направлении десны. Важно то, что надрез необходимо сделать удобным образом, чтобы вставить полоску для дренирования.
Важно то, что надрез необходимо сделать удобным образом, чтобы вставить полоску для дренирования.
Вскрывая воспалительные очаги, врач должен быть осторожным, чтобы не повредить уздечки верхней или нижней губы, так как это может привести к их укорачиванию или рубцеванию. Иногда бывают такие случаи, что пересечение уздечки неизбежно, тогда проводят два разреза – справа и слева от нее.
Дальнейшее лечение больного в постоперационном периоде основано на соблюдении главных правил с соблюдением терапии гнойных ран. В частности, пораженное место необходимо ополаскивать разнообразными антисептиками, которые необходимо чередовать. Перевязка раны производится до тех пор, пока не выйдет весь гной. Также в период лечения назначают болеутоляющие и антибактериальные средства, витамины, десенсибилизирующие и сульфаниламидные препараты. После вскрытия абсцесса на следующий день могут назначить ГНЛ-терапию, УВЧ-терапию или флюктуризацию.
При этом заболевании важно соблюдать все рекомендации врача стоматолога/ челюстно-лицевого хирурга, так как периостит относится к довольно серьезным патологиям, и поэтому его лечение проводится при стационарном или амбулаторном режиме.
Осложнения
Частые осложнения – распространение и прогрессирование воспалительного процесса. Это обычно случается из-за несвоевременного удаления зуба, недостаточного вскрытия или неправильного дренирования гнойного очага.
Воспаление, переломы и восстановление костей
1. Миранда М.А., Мун М.С. Стратегия лечения несращений и неправильных сращений. В: Стэннард Дж. П., Шмидт А. Х., Крегор П. Дж., редакторы. Хирургическое лечение ортопедической травмы. Нью-Йорк: Тиме; 2007. С. 77–100. [Google Scholar]
2. Hak DJ, Fitzpatrick D, Bishop JA, Marsh JL, Tilp S, Schnettler R, Simpson H, Alt V. Отсроченные союзы и несращения: эпидемиология, клинические проблемы и финансовые аспекты. Рана. 2014; 45 (Приложение 2): S3–7. [PubMed] [Академия Google]
3. Национальный фонд остеопороза. Что такое остеопороз? [Google Scholar]
4. Джахангир А.А., Нанли Р.М., Мехта С., Шаран А., стипендиаты TWHP. Костно-пластические заменители в ортопедической хирургии. ААОС сейчас. 2008; 2:1–5. [Google Scholar]
ААОС сейчас. 2008; 2:1–5. [Google Scholar]
5. Департамент исследований и науки AAoOS. Ежегодная заболеваемость общими скелетно-мышечными процедурами и лечением. 2014. [Google Scholar]
6. Маунциарис П.М., Спайсер П.П., Каспер Ф.К., Микос А.Г. Использование и модулирование воспаления в стратегиях регенерации кости. Tissue Eng Часть B Ред. 2011; 17:393–402. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Marsell R, Einhorn TA. Биология заживления переломов. Рана. 2011;42:551–5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Nich C, Takakubo Y, Pajarinen J, Ainola M, Salem A, Sillat T, Rao AJ, Raska M, Tamaki Y, Takagi M, Konttinen YT, Goodman SB, Галло Дж. Макрофаги-ключевые клетки в ответ на остатки износа при замене суставов. J Biomed Mater Res A. 2013;101:3033–45. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Моссер Д.М., Эдвардс Дж.П. Изучение полного спектра активации макрофагов. Нат Рев Иммунол. 2008; 8: 958–69. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Мантовани А., Бисвас С.К., Гальдьеро М.Р., Сика А., Локати М. Пластичность и поляризация макрофагов при восстановлении и ремоделировании тканей. Джей Патол. 2013; 229:176–85. [PubMed] [Google Scholar]
Мантовани А., Бисвас С.К., Гальдьеро М.Р., Сика А., Локати М. Пластичность и поляризация макрофагов при восстановлении и ремоделировании тканей. Джей Патол. 2013; 229:176–85. [PubMed] [Google Scholar]
11. Каваи Т., Акира С. Толл-подобные рецепторы и их взаимодействие с другими врожденными рецепторами при инфекциях и иммунитете. Иммунитет. 2011; 34: 637–50. [PubMed] [Академия Google]
12. Ortega-Gomez A, Perretti M, Soehnlein O. Разрешение воспаления: интегрированный взгляд. EMBO Мол Мед. 2013;5:661–74. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Kumagai K, Vasanji A, Drazba JA, Butler RS, Muschler GF. Циркулирующие клетки с остеогенным потенциалом физиологически мобилизуются в место заживления перелома в модели парабиотических мышей. J Ортоп Res. 2008; 26: 165–75. [PubMed] [Google Scholar]
14. Фонг Э.Л., Чан К.К., Гудман С.Б. Самонаведение стволовых клеток при травмах опорно-двигательного аппарата. Биоматериалы. 2011;32:395–409. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15. Osta B, Benedetti G, Miossec P. Классические и парадоксальные эффекты TNF-α на гомеостаз костей. Фронт Иммунол. 2014;5:1–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Osta B, Benedetti G, Miossec P. Классические и парадоксальные эффекты TNF-α на гомеостаз костей. Фронт Иммунол. 2014;5:1–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
16. Джанноудис П.В., Эйнхорн Т.А., Марш Д. Заживление переломов: алмазная концепция. Рана. 2007; 38 (Приложение 4): S3–6. [PubMed] [Google Scholar]
17. Jagodzinski M, Krettek C. Влияние механической стабильности на заживление переломов — обновление. Рана. 2007; 38 (Приложение 1): S3–10. [PubMed] [Академия Google]
18. Claes L, Recknagel S, Ignatius A. Заживление переломов в норме и при воспалении. Нат Рев Ревматол. 2012; 8: 133–43. [PubMed] [Google Scholar]
19. МакКиббин Б. Биология заживления переломов длинных костей. J Bone Joint Surg Br. 1978; 60-Б: 150–62. [PubMed] [Google Scholar]
20. Перрен С.М. Физические и биологические аспекты заживления переломов с особым упором на внутреннюю фиксацию. Clin Orthop Relat Relat Res. 1979: 175–96. [PubMed] [Академия Google]
21. Шапиро Ф. Восстановление кортикальной кости. Связь лакунарно-каналикулярной системы и межклеточных щелевых контактов с процессом репарации. J Bone Joint Surg Am. 1988; 70: 1067–81. [PubMed] [Google Scholar]
Шапиро Ф. Восстановление кортикальной кости. Связь лакунарно-каналикулярной системы и межклеточных щелевых контактов с процессом репарации. J Bone Joint Surg Am. 1988; 70: 1067–81. [PubMed] [Google Scholar]
22. Перрен С.М. Эволюция внутренней фиксации переломов длинных костей. Научная основа биологической внутренней фиксации: выбор нового баланса между стабильностью и биологией. J Bone Joint Surg Br. 2002; 84: 1093–110. [PubMed] [Google Scholar]
23. Harwood PJ, Newman JB, Michael ALR. Обновленная информация о заживлении переломов и несращении. Ортопедическая травма. 2010;24:9–23. [Google Scholar]
24. Gerstenfeld LC, Cullinane DM, Barnes GL, Graves DT, Einhorn TA. Заживление переломов как процесс постнатального развития: молекулярные, пространственные и временные аспекты его регуляции. Джей Селл Биохим. 2003; 88: 873–84. [PubMed] [Google Scholar]
25. Uhthoff HK, Rahn BA. Особенности заживления метафизарных переломов. Clin Orthop Relat Relat Res. 1981: 295–303. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
26. Аспенберг П., Сандберг О. Переломы дистального отдела лучевой кости срастаются путем формирования прямой костной ткани Per Aspenberg и Olof Sandberg. Акта Ортоп. 2013;84:297–300. [Бесплатная статья PMC] [PubMed] [Google Scholar]
27. Chen WT, Han da C, Zhang PX, Han N, Kou YH, Yin XF, Jiang BG. Особый характер заживления при стабильных метафизарных переломах. Акта Ортоп. 2015; 86: 238–42. [Бесплатная статья PMC] [PubMed] [Google Scholar]
28. Claes L, Reusch M, Gockelmann M, Ohnmacht M, Wehner T, Amling M, Beil FT, Ignatius A. Метафизарное заживление переломов следует тем же биомеханическим правилам, что и диафизарное заживление . J Ортоп Res. 2011;29:425–32. [PubMed] [Академия Google]
29. Колар П., Шмидт-Блик К., Шелл Х., Габер Т., Тобен Д., Шмидмайер Г., Перка С., Буттгерайт Ф., Дуда Г.Н. Ранняя гематома перелома и ее потенциальная роль в заживлении перелома. Tissue Eng, часть B, ред. 2010; 16: 427–34. [PubMed] [Google Scholar]
30. Grundnes O, Reikeras O. Важность гематомы для заживления переломов у крыс. Акта Ортоп Сканд. 1993; 64: 340–2. [PubMed] [Google Scholar]
Grundnes O, Reikeras O. Важность гематомы для заживления переломов у крыс. Акта Ортоп Сканд. 1993; 64: 340–2. [PubMed] [Google Scholar]
31. Park SH, Silva M, Bahk WJ, McKellop H, Lieberman JR. Влияние многократного орошения и хирургической обработки на заживление переломов в модели на животных. J Ортоп Res. 2002;20:1197–204. [PubMed] [Google Scholar]
32. Gerstenfeld LC, Cho TJ, Kon T, Aizawa T, Cruceta J, Graves BD, Einhorn TA. Нарушение образования внутримембранной кости во время восстановления кости в отсутствие передачи сигналов фактора некроза опухоли-альфа. Клетки Ткани Органы. 2001; 169: 285–94. [PubMed] [Google Scholar]
33. Gerstenfeld LC, Cho TJ, Kon T, Aizawa T, Tsay A, Fitch J, Barnes GL, Graves DT, Einhorn TA. Нарушение заживления переломов при отсутствии передачи сигналов ФНО-альфа: роль ФНО-альфа в резорбции эндохондрального хряща. Джей Боун Шахтер Рез. 2003; 18: 1584–9.2. [PubMed] [Google Scholar]
34. Yang X, Ricciardi BF, Hernandez-Soria A, Shi Y, Pleshko Camacho N, Bostrom MP.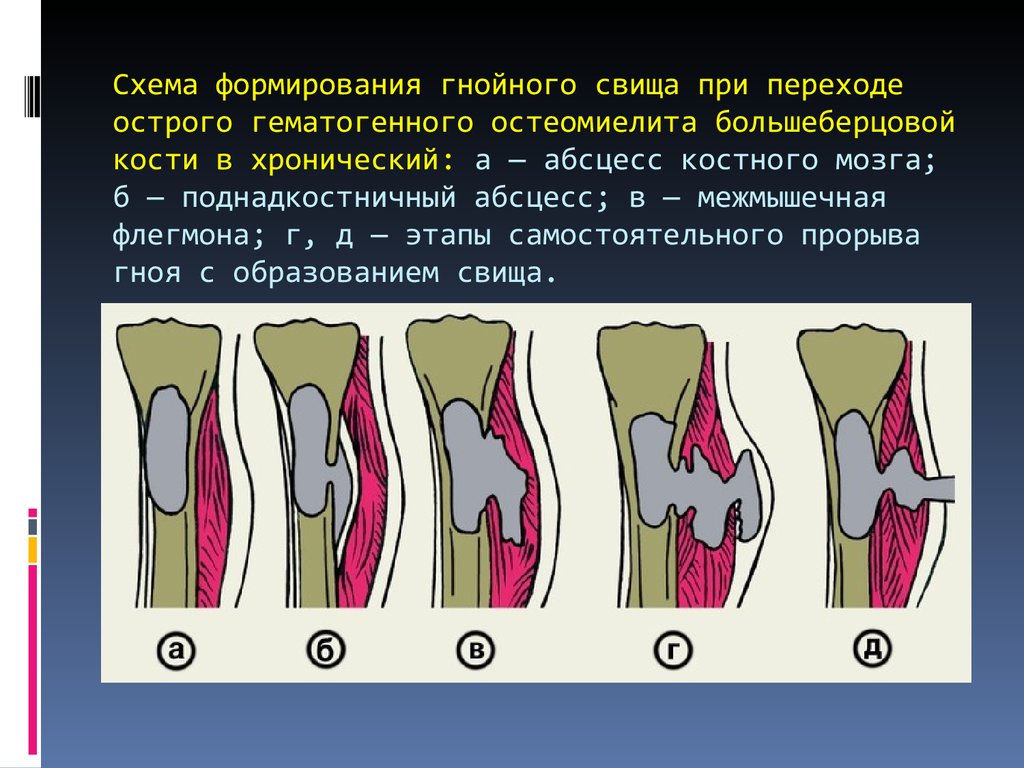 Минерализация и созревание костной мозоли задерживаются во время заживления переломов у мышей с нокаутом интерлейкина-6. Кость. 2007;41:928–36. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Минерализация и созревание костной мозоли задерживаются во время заживления переломов у мышей с нокаутом интерлейкина-6. Кость. 2007;41:928–36. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Glass GE, Chan JK, Freidin A, Feldmann M, Horwood NJ, Nanchahal J. TNF-альфа способствует заживлению переломов, усиливая рекрутирование и дифференцировку мышечных волокон. стромальные клетки. Proc Natl Acad Sci U S A. 2011;108:1585–9.0. [Бесплатная статья PMC] [PubMed] [Google Scholar]
36. Bastian O, Pillay J, Alblas J, Leenen L, Koenderman L, Blokhuis T. Системное воспаление и заживление переломов. Дж. Лейкок Биол. 2011; 89: 669–73. [PubMed] [Google Scholar]
37. Xing Z, Lu C, Hu D, Yu YY, Wang X, Colnot C, Nakamura M, Wu Y, Miclau T, Marcucio RS. Множественные роли CCR2 во время заживления переломов. Dis Model Mech. 2010;3:451–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
38. Херст С.М., Уилкинсон Т.С., Маклафлин Р.М., Джонс С., Хориучи С., Ямамото Н. , Роуз-Джон С., Фуллер Г.М., Топли Н., Джонс С.А. IL-6 и его растворимый рецептор организуют временное переключение в характере рекрутирования лейкоцитов, наблюдаемом при остром воспалении. Иммунитет. 2001; 14: 705–14. [PubMed] [Академия Google]
, Роуз-Джон С., Фуллер Г.М., Топли Н., Джонс С.А. IL-6 и его растворимый рецептор организуют временное переключение в характере рекрутирования лейкоцитов, наблюдаемом при остром воспалении. Иммунитет. 2001; 14: 705–14. [PubMed] [Академия Google]
39. Александр К.А., Чанг М.К., Мэйлин Э.Р., Колер Т., Мюллер Р., Ву А.С., Ван Ройен Н., Свит М.Дж., Хьюм Д.А., Раггатт Л.Дж., Петтит А.Р. Костные макрофаги способствуют заживлению внутримембранной кости in vivo в модели повреждения большеберцовой кости у мышей. Джей Боун Шахтер Рез. 2011;26:1517–32. [PubMed] [Google Scholar]
40. Raggatt LJ, Wullschleger ME, Alexander KA, Wu AC, Millard SM, Kaur S, Maugham ML, Gregory LS, Steck R, Pettit AR. Заживление перелома посредством образования периостальной мозоли требует наличия макрофагов как для инициации, так и для прогрессирования ранней эндохондральной оссификации. Ам Джей Патол. 2014;184:3192–204. [PubMed] [Google Scholar]
41. Pettit AR, Chang MK, Hume DA, Raggatt LJ. Костные макрофаги: новый взгляд на связь во время костной динамики. Кость. 2008;43:976–82. [PubMed] [Google Scholar]
Кость. 2008;43:976–82. [PubMed] [Google Scholar]
42. Kon T, Cho TJ, Aizawa T, Yamazaki M, Nooh N, Graves D, Gerstenfeld LC, Einhorn TA. Экспрессия остеопротегерина, активатора рецептора лиганда NF-kappaB (лиганд остеопротегерина) и родственных провоспалительных цитокинов при заживлении переломов. Джей Боун Шахтер Рез. 2001;16:1004–14. [PubMed] [Академия Google]
43. Билби Р., Джонс Э., МакГонагл Д. Роль мезенхимальных стволовых клеток в поддержании и восстановлении кости. Рана. 2007; 38 (Приложение 1): S26–32. [PubMed] [Google Scholar]
44. Ву А.С., Раггатт Л.Дж., Александр К.А., Петтит А.Р. Раскрытие вклада макрофагов в восстановление кости. Представитель Bonekey 2013; 2:373. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Xu L, Li G. Циркулирующие мезенхимальные стволовые клетки и их клиническое значение. J Ортоп перевод. 2014; 2:1–7. [Академия Google]
46. Циридис Э., Упадхьяй Н., Джанноудис П. Молекулярные аспекты заживления переломов: какие молекулы важны? Рана. 2007; 38 (Приложение 1): S11–25. [PubMed] [Google Scholar]
2007; 38 (Приложение 1): S11–25. [PubMed] [Google Scholar]
47. Schindeler A, McDonald MM, Bokko P, Little DG. Ремоделирование кости при восстановлении переломов: клеточная картина. Semin Cell Dev Biol. 2008; 19: 459–66. [PubMed] [Google Scholar]
48. Grundnes O, Reikeras O. Кровоток и механические свойства заживающей кости. Бедренные остеотомии изучали на крысах. Акта Ортоп Сканд. 1992;63:487–91. [PubMed] [Google Scholar]
49. Мельник М., Хенке Т., Клаес Л., Аугат П. Реваскуляризация при заживлении переломов с повреждением мягких тканей. Arch Orthop Trauma Surg. 2008; 128:1159–65. [PubMed] [Google Scholar]
50. Керамарис Н.К., Калори Г.М., Николау В.С., Шемитч Э.Х., Джанноудис П.В. Васкуляризация переломов и заживление костей: систематический обзор роли VEGF. Рана. 2008; 39 (Приложение 2): S45–57. [PubMed] [Google Scholar]
51. Томпсон З., Миклау Т., Ху Д., Хелмс Дж. А. Модель внутримембранозной оссификации при заживлении переломов. J Ортоп Res. 2002;20:1091–8. [PubMed] [Google Scholar]
2002;20:1091–8. [PubMed] [Google Scholar]
52. Мализос К.Н., Папатеодору Л.К. Лечебный потенциал молекулярных аспектов надкостницы. Рана. 2005; 36 (Приложение 3): S13–9. [PubMed] [Google Scholar]
53. Гастон М.С., Симпсон А.Х. Ингибирование заживления переломов. J Bone Joint Surg Br. 2007; 89: 1553–60. [PubMed] [Google Scholar]
54. Komatsu DE, Warden SJ. Контроль заживления переломов и его терапевтическое воздействие: улучшение природы. Джей Селл Биохим. 2010;109:302–11. [PubMed] [Академия Google]
55. Serhan CN, Savill J. Разрешение воспаления: начало программирует конец. Нат Иммунол. 2005; 6: 1191–7. [PubMed] [Google Scholar]
56. O’Keefe RJ, Mao J. Инженерия и регенерация костной ткани: от открытия до клиники — обзор. Tissue Eng, часть B, ред. 2011; 17: 389–92. [Бесплатная статья PMC] [PubMed] [Google Scholar]
57. Mountziaris PM, Mikos AG. Модуляция воспалительной реакции для усиления регенерации костной ткани. Tissue Eng Часть B Ред. 2008; 14:179–86. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2008; 14:179–86. [Бесплатная статья PMC] [PubMed] [Google Scholar]
58. Уотерс Р.В., Гамрадт С.К., Аснис П., Викери Б.Х., Авнур З., Хилл Э., Бостром М. Системные кортикостероиды ингибируют заживление кости в модели остеотомии локтевой кости у кролика. Акта Ортоп Сканд. 2000;71:316–21. [PubMed] [Google Scholar]
59. Arron JR, Choi Y. Кость против иммунной системы. Природа. 2000; 408: 535–6. [PubMed] [Google Scholar]
60. Арболея Л., Кастаньеда С. Остеоиммунология: изучение взаимосвязи между иммунной системой и костной тканью. Реуматол клин. 2013;9: 303–315. [PubMed] [Google Scholar]
61. Такаянаги Х. Остеоиммунология: общие механизмы и взаимодействие между иммунной и костной системами. Нат Рев Иммунол. 2007; 7: 292–304. [PubMed] [Google Scholar]
62. Уолш М.С., Ким Н., Кадоно Ю., Ро Дж., Ли С.Ю., Лоренцо Дж., Чой Ю. Остеоиммунология: взаимодействие между иммунной системой и костным метаболизмом. Анну Рев Иммунол. 2006; 24:33–63. [PubMed] [Google Scholar]
63. Konnecke I, Serra A, El Khassawna T, Schlundt C, Schell H, Hauser A, Ellinghaus A, Volk HD, Radbruch A, Duda GN, Schmidt-Bleek K. T and B клетки участвуют в восстановлении кости, инфильтрируя костную мозоль перелома в виде двух волн. Кость. 2014;64:155–65. [PubMed] [Академия Google]
Konnecke I, Serra A, El Khassawna T, Schlundt C, Schell H, Hauser A, Ellinghaus A, Volk HD, Radbruch A, Duda GN, Schmidt-Bleek K. T and B клетки участвуют в восстановлении кости, инфильтрируя костную мозоль перелома в виде двух волн. Кость. 2014;64:155–65. [PubMed] [Академия Google]
64. Criscitiello C, Viale G, Gelao L, Esposito A, De Laurentiis M, De Placido S, Santangelo M, Goldhirsch A, Curigliano G. Перекрестные помехи между костной нишей и иммунной системой: остеоиммунологическая сигнализация как потенциальная мишень для лечения рака . Лечение рака, ред. 2015; 41:61–8. [PubMed] [Google Scholar]
65. Greenblatt MB, Shim JH. Остеоиммунология: краткое введение. Иммунная сеть. 2013;13:111–5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
66. Ковач Т.К., Диге А.С., Лобо П.И., Куи В. Взаимодействие между МСК и иммунными клетками: последствия для заживления костей. Дж. Иммунол Рез. 2015;2015:752510. [Бесплатная статья PMC] [PubMed] [Google Scholar]
67. Ши С., Памер Э.Г. Рекрутирование моноцитов при инфекции и воспалении. Нат Рев Иммунол. 2011; 11: 762–74. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Ши С., Памер Э.Г. Рекрутирование моноцитов при инфекции и воспалении. Нат Рев Иммунол. 2011; 11: 762–74. [Бесплатная статья PMC] [PubMed] [Google Scholar]
68. Браун Б.Н., Ратнер Б.Д., Гудман С.Б., Амар С., Бадылак С.Ф. Поляризация макрофагов: возможность улучшить результаты в биоматериалах и регенеративной медицине. Биоматериалы. 2012; 33:3792–802. [Бесплатная статья PMC] [PubMed] [Google Scholar]
69. Martinez FO, Sica A, Mantovani A, Locati M. Активация макрофагов и поляризация. Фронт биосай. 2008; 13: 453–61. [PubMed] [Академия Google]
70. Spiller KL, Nassiri S, Witherel CE, Anfang RR, Ng J, Nakazawa KR, Yu T, Vunjak-Novakovic G. Последовательная доставка иммуномодулирующих цитокинов для облегчения перехода M1-M2 макрофагов и усиления васкуляризации костные каркасы. Биоматериалы. 2015; 37: 194–207. [Бесплатная статья PMC] [PubMed] [Google Scholar]
71. da Silva Meirelles L, Chagastelles PC, Nardi NB. Мезенхимальные стволовые клетки присутствуют практически во всех постнатальных органах и тканях. Дж. Клеточные науки. 2006; 119:2204–13. [PubMed] [Академия Google]
Дж. Клеточные науки. 2006; 119:2204–13. [PubMed] [Академия Google]
72. Харада С., Родан Г.А. Контроль функции остеобластов и регуляция костной массы. Природа. 2003; 423:349–55. [PubMed] [Google Scholar]
73. Nakashima K, Zhou X, Kunkel G, Zhang Z, Deng JM, Behringer RR, de Crombrugghe B. Новый транскрипционный фактор osterix, содержащий цинковые пальцы, необходим для дифференцировки остеобластов и формирования кости. . Клетка. 2002; 108:17–29. [PubMed] [Google Scholar]
74. Мари П.Дж., Кассем М. Остеобласты при остеопорозе: прошлые, возникающие и будущие анаболические цели. Евр Дж Эндокринол. 2011; 165:1–10. [PubMed] [Академия Google]
75. Беллидо Т. Ремоделирование кости, управляемое остеоцитами. Кальциф ткани Int. 2014;94:25–34. [Бесплатная статья PMC] [PubMed] [Google Scholar]
76. Boyle WJ, Simonet WS, Lacey DL. Дифференцировка и активация остеокластов. Природа. 2003; 423:337–42. [PubMed] [Google Scholar]
77. Хосла С. Миниобзор: система OPG/RANKL/RANK. Эндокринология. 2001; 142:5050–5. [PubMed] [Google Scholar]
Эндокринология. 2001; 142:5050–5. [PubMed] [Google Scholar]
78. Ясуда Х., Сима Н., Накагава Н., Ямагути К., Киносаки М., Мочизуки С., Томоясу А., Яно К., Гото М., Мураками А., Цуда Э., Моринага Т., Хигасио К., Udagawa N, Takahashi N, Suda T. Фактор дифференцировки остеокластов является лигандом для фактора, ингибирующего остеопротегерин/остеокластогенез, и идентичен TRANCE/RANKL. Proc Natl Acad Sci U S A. 1998;95:3597–602. [Бесплатная статья PMC] [PubMed] [Google Scholar]
79. Такаянаги Х., Огасавара К., Хида С., Тиба Т., Мурата С., Сато К., Такаока А., Йокочи Т., Ода Х., Танака К., Накамура К., Танигучи Опосредованная Т-клетками регуляция остеокластогенеза путем передачи сигналов между RANKL и IFN-gamma. Природа. 2000;408:600–5. [PubMed] [Google Scholar]
80. Такаянаги Х. Воспалительная деструкция кости и остеоиммунология. J Периодонтальная Рез. 2005; 40: 287–93. [PubMed] [Академия Google]
81. Lee SK, Lorenzo J. Цитокины, регулирующие образование и функцию остеокластов. Курр Опин Ревматол. 2006;18:411–8. [PubMed] [Google Scholar]
Курр Опин Ревматол. 2006;18:411–8. [PubMed] [Google Scholar]
82. Такаянаги Х. Остеоиммунология и влияние иммунной системы на кость. Нат Рев Ревматол. 2009; 5: 667–76. [PubMed] [Google Scholar]
83. Aliprantis AO, Ueki Y, Sulyanto R, Park A, Sigrist KS, Sharma SM, Ostrowski MC, Olsen BR, Glimcher LH. NFATc1 у мышей репрессирует остеопротегерин во время остеокластогенеза и отделяет системную остеопению от воспаления при херувизме. Джей Клин Инвест. 2008; 118: 3775–89.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
84. Локсли Р.М., Киллин Н., Ленардо М.Дж. Надсемейства рецепторов TNF и TNF: интеграция биологии млекопитающих. Клетка. 2001; 104: 487–501. [PubMed] [Google Scholar]
85. Такахаши Н., Манди Г.Р., Рудман Г.Д. Рекомбинантный гамма-интерферон человека ингибирует образование клеток, подобных остеокластам человека. Дж Иммунол. 1986; 137:3544–9. [PubMed] [Google Scholar]
86. Чанг М.К., Раггатт Л.Дж., Александр К.А., Куливаба Дж.С., Фаззалари Н. Л., Шредер К., Мэйлин Э.Р., Риполл В.М., Хьюм Д.А., Петтит А.Р. Макрофаги костной ткани внедряются в ткани, выстилающие костную ткань человека и мыши, и регулируют функцию остеобластов in vitro и in vivo. Дж Иммунол. 2008; 181:1232–44. [PubMed] [Академия Google]
Л., Шредер К., Мэйлин Э.Р., Риполл В.М., Хьюм Д.А., Петтит А.Р. Макрофаги костной ткани внедряются в ткани, выстилающие костную ткань человека и мыши, и регулируют функцию остеобластов in vitro и in vivo. Дж Иммунол. 2008; 181:1232–44. [PubMed] [Академия Google]
87. Hoch AI, Binder BY, Genetos DC, Leach JK. Зависимая от дифференцировки секреция проангиогенных факторов мезенхимальными стволовыми клетками. ПЛОС Один. 2012;7:e35579. [Бесплатная статья PMC] [PubMed] [Google Scholar]
88. Porter JR, Ruckh TT, Popat KC. Инженерия костной ткани: обзор биомиметики костей и стратегий доставки лекарств. Биотехнологическая прог. 2009; 25:1539–60. [PubMed] [Google Scholar]
89. Антон К., Банерджи Д., Глод Дж. Связанные с макрофагами мезенхимальные стволовые клетки принимают активированный, мигрирующий, провоспалительный фенотип с повышенной секрецией IL-6 и CXCL10. ПЛОС Один. 2012;7:e35036. [Бесплатная статья PMC] [PubMed] [Google Scholar]
90. Freytes DO, Kang JW, Marcos-Campos I, Vunjak-Novakovic G. Макрофаги модулируют жизнеспособность и рост мезенхимальных стволовых клеток человека. Джей Селл Биохим. 2013;114:220–9. [PubMed] [Google Scholar]
Макрофаги модулируют жизнеспособность и рост мезенхимальных стволовых клеток человека. Джей Селл Биохим. 2013;114:220–9. [PubMed] [Google Scholar]
91. Шампанское CM, Takebe J, Offenbacher S, Cooper LF. Клеточные линии макрофагов продуцируют остеоиндуктивные сигналы, которые включают костный морфогенетический белок-2. Кость. 2002; 30: 26–31. [PubMed] [Google Scholar]
92. Fromigue O, Marie PJ, Lomri A. Костный морфогенетический белок-2 и трансформирующий фактор роста-бета2 взаимодействуют, модулируя пролиферацию и дифференцировку стромальных клеток костного мозга человека. Джей Селл Биохим. 1998;68:411–26. [PubMed] [Google Scholar]
93. Блом А.Б., ван Лент П.Л., Холтуйсен А.Е., Ван дер Краан П.М., Рот Дж., Ван Ройен Н., ван ден Берг В.Б. Макрофаги синовиальной оболочки опосредуют образование остеофитов во время экспериментального остеоартрита. Хрящевой остеоартрит. 2004; 12: 627–35. [PubMed] [Google Scholar]
94. Ви Л., Бахт Г.С., Уэтстоун Х., Нг А., Вей К. , Пун Р., Милваганам С., Гринпас М., Алман Б.А. Макрофаги способствуют дифференцировке остеобластов in vivo: последствия для восстановления переломов и гомеостаза кости. Джей Боун Шахтер Рез. 2015;30:1090–102. [PubMed] [Google Scholar]
, Пун Р., Милваганам С., Гринпас М., Алман Б.А. Макрофаги способствуют дифференцировке остеобластов in vivo: последствия для восстановления переломов и гомеостаза кости. Джей Боун Шахтер Рез. 2015;30:1090–102. [PubMed] [Google Scholar]
95. Николаиду В., Вонг М.М., Редпат А.Н., Эрсек А., Бабан Д.Ф., Уильямс Л.М., Коуп А.П., Хорвуд Н.Дж. Моноциты индуцируют активацию STAT3 в мезенхимальных стволовых клетках человека, способствуя образованию остеобластов. ПЛОС Один. 2012;7:e39871. [Бесплатная статья PMC] [PubMed] [Google Scholar]
96. Guihard P, Boutet MA, Brounais-Le Royer B, Gamblin AL, Amiaud J, Renaud A, Berreur M, Redini F, Heymann D, Layrolle P, Blanchard F. Онкостатин m, воспалительный цитокин, продуцируемый макрофагами, поддерживает внутримембранозное заживление кости в мышиной модели повреждения большеберцовой кости. Ам Джей Патол. 2015; 185:765–75. [PubMed] [Академия Google]
97. Chen Z, Wu C, Gu W, Klein T, Crawford R, Xiao Y. Остеогенная дифференцировка МСК костного мозга бета-трикальцийфосфатом, стимулирующим макрофаги через сигнальный путь BMP2. Биоматериалы. 2014; 35:1507–18. [PubMed] [Google Scholar]
Биоматериалы. 2014; 35:1507–18. [PubMed] [Google Scholar]
98. Лоренцо Дж. Взаимодействие между иммунными и костными клетками: новое понимание со многими остающимися вопросами. Джей Клин Инвест. 2000; 106: 749–52. [Бесплатная статья PMC] [PubMed] [Google Scholar]
99. Gilbert L, He X, Farmer P, Boden S, Kozlowski M, Rubin J, Nanes MS. Ингибирование дифференцировки остеобластов фактором некроза опухоли-альфа. Эндокринология. 2000;141:3956–64. [PubMed] [Google Scholar]
100. Cavagis A, Takamori E, Granjeiro J, Oliveira R, Ferreira C, Peppelenbosch M, Zambuzzi W. TNF-альфа способствует ослаблению фосфорилирования Y397FAK и Y416Src в остеобластах. Оральный Дис. 2014;20:780–6. [PubMed] [Google Scholar]
101. Ding J, Ghali O, Lencel P, Broux O, Chauveau C, Devedjian JC, Hardouin P, Magne D. TNF-альфа и IL-1бета ингибируют экспрессию RUNX2 и коллагена, но увеличивают щелочную реакцию. активность фосфатазы и минерализация в мезенхимальных стволовых клетках человека. Жизнь наук. 2009 г.;84:499–504. [PubMed] [Google Scholar]
Жизнь наук. 2009 г.;84:499–504. [PubMed] [Google Scholar]
102. Guo R, Yamashita M, Zhang Q, Zhou Q, Chen D, Reynolds DG, Awad HA, Yanoso L, Zhao L, Schwarz EM, Zhang YE, Boyce BF, Xing L. Убиквитинлигаза Smurf1 опосредует вызванную фактором некроза опухоли системную потерю костной массы, способствуя протеасомной деградации костных морфогенетических сигнальных белков. Дж. Биол. Хим. 2008; 283:23084–92. [Бесплатная статья PMC] [PubMed] [Google Scholar]
103. Lange J, Sapozhnikova A, Lu C, Hu D, Li X, Miclau T, 3rd, Marcucio RS. Действие ИЛ-1бета при заживлении переломов. J Ортоп Res. 2010; 28: 778–84. [Бесплатная статья PMC] [PubMed] [Google Scholar]
104. Miller RR, Cappola AR, Shardell MD, Hawkes WG, Yu-Yahiro JA, Hebel JR, Magaziner J. Стойкие изменения интерлейкина-6 и функции нижних конечностей после перелома бедра. J Gerontol A Biol Sci Med Sci. 2006;61:1053–1058. [PubMed] [Google Scholar]
105. Caparbo VF, Prada F, Silva CA, Regio PL, Pereira RM. Сыворотка крови детей с полиартикулярным ювенильным идиопатическим артритом (пЮИА) ингибирует дифференцировку, минерализацию и может усиливать апоптоз остеобластов человека «in vitro» Clin Rheumatol. 2009 г.;28:71–7. [PubMed] [Google Scholar]
2009 г.;28:71–7. [PubMed] [Google Scholar]
106. Hofbauer LC, Lacey DL, Dunstan CR, Spelsberg TC, Riggs BL, Khosla S. Интерлейкин-1бета и фактор некроза опухоли-альфа, но не интерлейкин-6, стимулируют экспрессию гена лиганда остеопротегерина. в остеобластных клетках человека. Кость. 1999; 25: 255–9. [PubMed] [Google Scholar]
107. Lam J, Takeshita S, Barker JE, Kanagawa O, Ross FP, Teitelbaum SL. TNF-альфа индуцирует остеокластогенез путем прямой стимуляции макрофагов, подвергающихся воздействию пермиссивных уровней лиганда RANK. Джей Клин Инвест. 2000; 106:1481–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
108. Jimi E, Nakamura I, Duong LT, Ikebe T, Takahashi N, Rodan GA, Suda T. Интерлейкин 1 индуцирует многоядерную и костно-резорбтивную активность остеокластов в отсутствие остеобластов/стромальных клеток. Разрешение ячейки опыта. 1999; 247:84–93. [PubMed] [Google Scholar]
109. Tan SD, Kuijpers-Jagtman AM, Semeins CM, Bronckers AL, Maltha JC, Von den Hoff JW, Everts V, Klein-Nulend J. Напряжение сдвига жидкости ингибирует TNF-альфа-индуцированный апоптоз остеоцитов. . Джей Дент Рез. 2006; 85: 905–9. [PubMed] [Академия Google]
Напряжение сдвига жидкости ингибирует TNF-альфа-индуцированный апоптоз остеоцитов. . Джей Дент Рез. 2006; 85: 905–9. [PubMed] [Академия Google]
110. Мори Г., Д’Амелио П., Фаччо Р., Брунетти Г. Взаимодействие между костью и иммунной системой. Клин Дев Иммунол. 2013;2013:720504. [Бесплатная статья PMC] [PubMed] [Google Scholar]
111. Girasole G, Jilka RL, Passeri G, Boswell S, Boder G, Williams DC, Manolagas SC. 17 бета-эстрадиол ингибирует продукцию интерлейкина-6 стромальными клетками костного мозга и остеобластами in vitro: потенциальный механизм антиостеопоротического действия эстрогенов. Джей Клин Инвест. 1992; 89: 883–9.1. [Бесплатная статья PMC] [PubMed] [Google Scholar]
112. Grogaard B, Gerdin B, Reikeras O. Полиморфноядерные лейкоциты: играют ли они роль в заживлении переломов? Arch Orthop Trauma Surg. 1990; 109: 268–71. [PubMed] [Google Scholar]
113. Тобен Д., Шредер И., Эль Хассауна Т., Мехта М., Хоффманн Дж. Э., Фриш Дж. Т., Шелл Х., Лиенау Дж. , Серра А., Радбрух А., Дуда Г. Н. Заживление переломов ускоряется при отсутствии адаптивной иммунной системы. Джей Боун Шахтер Рез. 2011;26:113–24. [PubMed] [Академия Google]
, Серра А., Радбрух А., Дуда Г. Н. Заживление переломов ускоряется при отсутствии адаптивной иммунной системы. Джей Боун Шахтер Рез. 2011;26:113–24. [PubMed] [Академия Google]
114. Мартин П., Д’Суза Д., Мартин Дж., Гроуз Р., Купер Л., Маки Р., МакКерчер С.Р. Заживление ран в ПУ. 1 нулевая мышь — восстановление тканей не зависит от воспалительных клеток. Карр Биол. 2003; 13:1122–8. [PubMed] [Google Scholar]
115. Kim J, Hematti P. Макрофаги, образованные мезенхимальными стволовыми клетками: новый тип альтернативно активированных макрофагов. эксп Гематол. 2009; 37:1445–53. [Бесплатная статья PMC] [PubMed] [Google Scholar]
116. Arai F, Hirao A, Ohmura M, Sato H, Matsuoka S, Takubo K, Ito K, Koh GY, Suda T. Передача сигналов Tie2/ангиопоэтин-1 регулирует покоя гемопоэтических стволовых клеток в костномозговой нише. Клетка. 2004;118:149–61. [PubMed] [Google Scholar]
117. Кальви Л.М., Адамс Г.Б., Вайбрехт К.В., Вебер Дж.М., Олсон Д.П., Найт М.С., Мартин Р.П.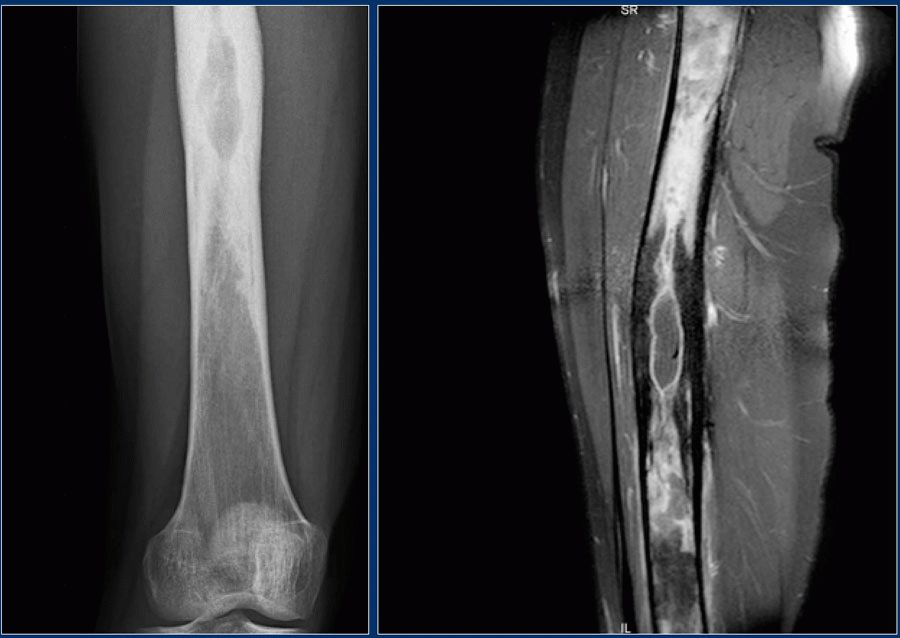 , Шипани Э., Дивиети П., Брингхерст Ф.Р., Милнер Л.А., Кроненберг Х.М., Скадден Д.Т. Остеобластические клетки регулируют нишу гемопоэтических стволовых клеток. Природа. 2003; 425:841–6. [PubMed] [Google Scholar]
, Шипани Э., Дивиети П., Брингхерст Ф.Р., Милнер Л.А., Кроненберг Х.М., Скадден Д.Т. Остеобластические клетки регулируют нишу гемопоэтических стволовых клеток. Природа. 2003; 425:841–6. [PubMed] [Google Scholar]
118. Коллет О., Дар А., Шивтиель С., Калинкович А., Лапид К., Штейнберг Ю., Тесио М., Самстейн Р. М., Гойхберг П., Шпигель А., Элсон А., Лапидот Т. Остеокласты разрушают эндосталь. компоненты и способствуют мобилизации гемопоэтических клеток-предшественников. Нат Мед. 2006; 12: 657–64. [PubMed] [Академия Google]
119. Рао М., Супакорндей Т., Шмидт А.П., Линк Д.С. Остеокласты незаменимы для мобилизации гемопоэтических предшественников с помощью гранулоцитарного колониестимулирующего фактора у мышей. эксп Гематол. 2015;43:110–4. е1–2. [Бесплатная статья PMC] [PubMed] [Google Scholar]
120. Charles JF, Aliprantis AO. Остеокласты: больше, чем «пожиратели костей» Trends Mol Med. 2014;20:449–59. [Бесплатная статья PMC] [PubMed] [Google Scholar]
121. Cho DI, Kim MR, Jeong HY, Jeong HC, Jeong MH, Yoon SH, Kim YS, Ahn Y. Мезенхимальные стволовые клетки реципрокно регулируют баланс M1/M2. в макрофагах костного мозга мышей. Эксп Мол Мед. 2014;46:e70. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Мезенхимальные стволовые клетки реципрокно регулируют баланс M1/M2. в макрофагах костного мозга мышей. Эксп Мол Мед. 2014;46:e70. [Бесплатная статья PMC] [PubMed] [Google Scholar]
122. Ren G, Zhang L, Zhao X, Xu G, Zhang Y, Roberts AI, Zhao RC, Shi Y. Иммуносупрессия, опосредованная мезенхимальными стволовыми клетками, происходит за счет согласованного действия хемокинов и оксида азота. Клеточная стволовая клетка. 2008; 2: 141–50. [PubMed] [Google Scholar]
123. Nakajima H, Uchida K, Guerrero AR, Watanabe S, Sugita D, Takeura N, Yoshida A, Long G, Wright KT, Johnson WE, Baba H. Трансплантация мезенхимальных стволовых клеток способствует альтернативный путь активации макрофагов и функционального восстановления после травмы спинного мозга. J Нейротравма. 2012;29: 1614–25. [Бесплатная статья PMC] [PubMed] [Google Scholar]
124. Maggini J, Mirkin G, Bognanni I, Holmberg J, Piazzon IM, Nepomnaschy I, Costa H, Canones C, Raiden S, Vermeulen M, Geffner JR. Мезенхимальные стромальные клетки, полученные из костного мозга мышей, превращают активированные макрофаги в регулирующий профиль. PloS Один. 2010:5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
PloS Один. 2010:5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
125. Prockop DJ. Краткий обзор: две петли отрицательной обратной связи помещают мезенхимальные стволовые/стромальные клетки в центр ранних регуляторов воспаления. Стволовые клетки. 2013;31:2042–2046. [PubMed] [Академия Google]
126. Гомес-Баррена Э., Россет П., Лозано Д., Становичи Дж., Эрмталлер С., Гербхард Ф. Заживление переломов костей: клеточная терапия при отсроченных сращениях и несращениях. Кость. 2015;70:93–101. [PubMed] [Google Scholar]
127. Гудман С.Б., Гибон Э., Паджаринен Дж., Лин Т.Х., Кини М., Рен П.Г., Нич С., Яо З., Эгашира К., Ян Ф., Конттинен Ю.Т. Новые биологические стратегии лечения перипротезного остеолиза ортопедических имплантатов для замены суставов, вызванного частицами износа. Интерфейс JR Soc. 2014:11. [Бесплатная статья PMC] [PubMed] [Google Scholar]
128. Кордова Л.А., Трише В., Эскриу В., Россе П., Амио Дж., Батталья С., Шарье С., Берреур М., Брион Р., Гуин Ф. , Лайролл П., Пассути Н., Хейманн Д. Ингибирование остеолиза и увеличение кости образование после местного введения siRNA-таргетинга RANK в модели остеолиза, индуцированного полиэтиленовыми частицами. Акта Биоматер. 2015;13:150–158. [PubMed] [Google Scholar]
, Лайролл П., Пассути Н., Хейманн Д. Ингибирование остеолиза и увеличение кости образование после местного введения siRNA-таргетинга RANK в модели остеолиза, индуцированного полиэтиленовыми частицами. Акта Биоматер. 2015;13:150–158. [PubMed] [Google Scholar]
129. Хейманн Д. Бисфосфонаты и заболевания костей: прошлое, настоящее и будущее. Курр Фарм Дез. 2010;16:2948–2949. [Бесплатная статья PMC] [PubMed] [Google Scholar]
130. Нарди А., Вентура Л., Коцци Л., Тонини Г., Зеннаро Р., Чели М., Рамаззина Э. Костная анаболическая терапия. Старение Clin Exp Res. 2013;25:121–124. [PubMed] [Google Scholar]
131. Andrews EB, Gilsenan AW, Midkiff K, Sherrill B, Wu Y, Mann BH, Masica D. Постмаркетинговое исследование остеосаркомы и терипаратида у взрослых в США: дизайн исследования и первые результаты 7 лет. Джей Боун Шахтер Рез. 2012;27:2429–2437. [Бесплатная статья PMC] [PubMed] [Google Scholar]
132. Allen MR. Бисфосфонаты и остеонекроз челюсти: переход от постели к скамье.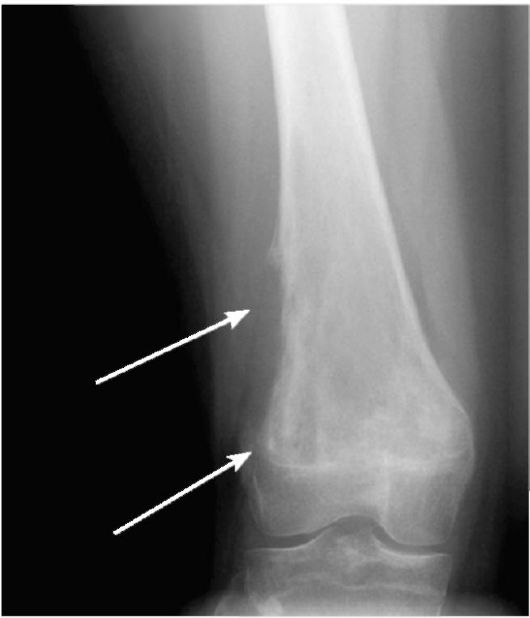 Клетки Ткани Органы. 2009 г.;189:289–294. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Клетки Ткани Органы. 2009 г.;189:289–294. [Бесплатная статья PMC] [PubMed] [Google Scholar]
133. Carvalho NNC, Voss LA, Almeida MOP, Salgado CL, Bandeira F. Атипичные переломы бедренной кости при длительном применении бисфосфонатов: краткосрочные ответы на стронция ранелат и терипаратид. J Clin Endocrinol Metab. 2011;96:2675–2680. [PubMed] [Google Scholar]
134. Саймон Л.С. Остеопороз. Реум Дис Клин Норт Ам. 2007; 33: 149–76. [PubMed] [Google Scholar]
135. Симпсон А.Х., Мюррей И.Р. Модели остеопоротических переломов. Curr Osteoporos Rep. 2015; 13:9–15. [PubMed] [Google Scholar]
136. Silverman SL, Siris E, Kendler DL, Belazi D, Brown JP, Gold DT, Lewiecki EM, Papaioannou A, Simonelli C, Ferreira I, Balasubramanian A, Dakin P, Ho P, Siddhanti S, Stolshek B, Recknor C. Стойкость в течение 12 месяцев с деносумабом у женщин в постменопаузе с остеопорозом: промежуточные результаты проспективного обсервационного исследования. Остеопорос Инт. 2015;26:361–72. [Бесплатная статья PMC] [PubMed] [Google Scholar]
137. Pietschmann P, Mechcheriakova D, Meshcheryakova A, Foger-Samwald U, Ellinger I. Иммунология остеопороза: мини-обзор. Геронтология. 2015 [Бесплатная статья PMC] [PubMed] [Google Scholar]
Pietschmann P, Mechcheriakova D, Meshcheryakova A, Foger-Samwald U, Ellinger I. Иммунология остеопороза: мини-обзор. Геронтология. 2015 [Бесплатная статья PMC] [PubMed] [Google Scholar]
138. Франчески С., Бонафе М., Валенсен С., Оливьери Ф., Де Лука М., Оттавиани Э., Де Бенедиктис Г. Воспалительное старение. Эволюционный взгляд на иммуностарение. Энн Н.Ю. Академия наук. 2000; 908: 244–54. [PubMed] [Google Scholar]
139. Lencel P, Magne D. Воспаление: движущая сила остеопороза? Мед Гипотезы. 2011;76:317–21. [PubMed] [Google Scholar]
140. Topini C, Topini D, Cerica G, Nardocci F, Topini G. Остеопороз и риск переломов, анализ популяции, поступившей в реабилитацию после острого состояния. Clin Cases Miner Bone Metab. 2014;11:129–31. [Бесплатная статья PMC] [PubMed] [Google Scholar]
141. Perren SM. Заживление переломов: заживление переломов понимается как результат увлекательного каскада физических и биологических взаимодействий. Часть I. Попытка объединить наблюдения 30-летнего исследования АО. Acta Chir Orthop Traumatol Cech. 2014; 81: 355–64. [PubMed] [Google Scholar]
Acta Chir Orthop Traumatol Cech. 2014; 81: 355–64. [PubMed] [Google Scholar]
142. Доносо О., Пино А.М., Зейтц Г., Оссес Н., Родригес Дж. П. Связанное с остеопорозом изменение сигнального статуса BMP-2 в МСК человека в адипогенных условиях. Джей Селл Биохим. 2015 [PubMed] [Академия Google]
143. Coughlan T, Dockery F. Остеопороз и риск переломов у пожилых людей. Клин Мед. 2014; 14:187–91. [Бесплатная статья PMC] [PubMed] [Google Scholar]
144. Ибрагим Н., Хамис М.Ф., Мод Юнох М.Ф., Абдулла С., Мохамед Н., Шуид А.Н. Целенаправленная доставка ловастатина и токотриенола к месту перелома способствует заживлению перелома в модели остеопороза: микрокомпьютерная томография и биомеханическая оценка. ПЛОС Один. 2014;9:e115595. [Бесплатная статья PMC] [PubMed] [Google Scholar]
145. Николау В.С., Эфстатопулос Н., Контакис Г., Канакарис Н.К., Яннудис П.В. Влияние остеопороза на время заживления переломов бедренной кости. Рана. 2009 г.;40:663–8. [PubMed] [Google Scholar]
146. Пантели М., Поунтос И., Джонс Э., Джанноудис П.В. Биологический и молекулярный профиль несращенной ткани перелома: современные данные. J Cell Mol Med. 2015;19:685–713. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Пантели М., Поунтос И., Джонс Э., Джанноудис П.В. Биологический и молекулярный профиль несращенной ткани перелома: современные данные. J Cell Mol Med. 2015;19:685–713. [Бесплатная статья PMC] [PubMed] [Google Scholar]
147. Copuroglu C, Calori GM, Giannoudis PV. Перелом несросшийся: кто в группе риска? Рана. 2013;44:1379–82. [PubMed] [Google Scholar]
148. Беренс А., ван Дерсен Дж. М., Рудольф К. Л., Шумахер Б. Влияние повреждения генома и старения на функцию стволовых клеток. Nat Cell Biol. 2014;16:201–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
149. Iwakura T, Miwa M, Sakai Y, Niikura T, Lee SY, Oe K, Hasegawa T, Kuroda R, Fujioka H, Doita M, Kurosaka M. Гипертрофическая незаращенная ткань человека содержит мезенхимальные клетки-предшественники с многолинейной способностью in vitro . J Ортоп Res. 2009; 27: 208–15. [PubMed] [Google Scholar]
150. Kloen P, Doty SB, Gordon E, Rubel IF, Goumans MJ, Helfet DL. Экспрессия и активация сигнальных компонентов BMP в несращениях переломов у человека. J Bone Joint Surg Am. 2002; 84-А: 1909–18. [PubMed] [Академия Google]
J Bone Joint Surg Am. 2002; 84-А: 1909–18. [PubMed] [Академия Google]
151. Qu G, фон Шредер HP. Остеогенный потенциал ткани псевдоартроза и кости несращений ладьевидной кости человека. J Hand Surg Eur Vol. 2008; 33: 449–56. [PubMed] [Google Scholar]
152. Fernandez-Bances I, Perez-Basterrechea M, Perez-Lopez S, Nunez Batalla D, Fernandez Rodriguez MA, Alvarez-Viejo M, Ferrero-Gutierrez A, Menendez-Menendez Y, Garcia -Gala JM, Escudero D, Paz Aparicio J, Carnero Lopez S, Lopez Fernandez P, Gonzalez Suarez D, Otero Hernandez J. Восстановление псевдоартроза длинных костей с помощью аутологичных мононуклеарных клеток костного мозга в сочетании с аллогенным костным трансплантатом. Цитотерапия. 2013;15:571–57. [PubMed] [Академия Google]
153. Hisatome T, Yasunaga Y, Yanada S, Tabata Y, Ikada Y, Ochi M. Неоваскуляризация и регенерация кости путем имплантации аутологичных мононуклеарных клеток костного мозга. Биоматериалы. 2005; 26:4550–6. [PubMed] [Google Scholar]
154. Seita J, Weissman IL. Гемопоэтические стволовые клетки: самообновление против дифференцировки. Wiley Interdiscip Rev Syst Biol Med. 2010;2:640–53. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Seita J, Weissman IL. Гемопоэтические стволовые клетки: самообновление против дифференцировки. Wiley Interdiscip Rev Syst Biol Med. 2010;2:640–53. [Бесплатная статья PMC] [PubMed] [Google Scholar]
155. Hernigou P, Poignard A, Manicom O, Mathieu G, Rouard H. Использование чрескожной аутологичной трансплантации костного мозга при несращении и аваскулярном некрозе кости. J Bone Joint Surg Br. 2005;87:896–902. [PubMed] [Google Scholar]
156. Паттерсон Т.Е., Кумагаи К., Гриффит Л., Мюшлер Г.Ф. Клеточные стратегии для улучшения восстановления переломов. J Bone Joint Surg Am. 2008; 90 (Приложение 1): 111–9. [PubMed] [Google Scholar]
157. Lin TH, Tamaki Y, Pajarinen J, Waters HA, Woo DK, Yao Z, Goodman SB. Хроническое воспаление при перипротезном остеолизе, индуцированном биоматериалом: NF-kappaB в качестве терапевтической мишени. Акта Биоматер. 2014; 10:1–10. [Бесплатная статья PMC] [PubMed] [Google Scholar]
158. Бранемарк Р., Бранемарк П.И., Ридевик Б., Майерс Р. Р. Остеоинтеграция в скелетной реконструкции и реабилитации: обзор. J Rehabil Res Dev. 2001; 38: 175–81. [PubMed] [Google Scholar]
Р. Остеоинтеграция в скелетной реконструкции и реабилитации: обзор. J Rehabil Res Dev. 2001; 38: 175–81. [PubMed] [Google Scholar]
159. Андерсон Дж.М., Родригес А., Чанг Д.Т. Реакция инородного тела на биоматериалы. Семин Иммунол. 2008; 20:86–100. [Бесплатная статья PMC] [PubMed] [Google Scholar]
160. Trindade R, Albrektsson T, Tengvall P, Wennerberg A. Реакция инородного тела на биоматериалы: о механизмах наращивания и разрушения остеоинтеграции. Clin Implant Dent Relat Res. 2014 в печати. [PubMed] [Академия Google]
161. Albrektsson T, Dahlin C, Jemt T, Sennerby L, Turri A, Wennerberg A. Является ли потеря маргинальной кости вокруг оральных имплантатов результатом спровоцированной реакции на инородное тело? Clin Implant Dent Relat Res. 2014;16:155–65. [PubMed] [Google Scholar]
162. Sundfeldt M, Carlsson LV, Johansson CB, Thomsen P, Gretzer C. Асептическое расшатывание, не только вопрос износа: обзор различных теорий. Акта Ортоп. 2006; 77: 177–97. [PubMed] [Google Scholar]
163. Albrektsson T, Dahl E, Enbom L, Engevall S, Engquist B, Eriksson AR, Feldmann G, Freiberg N, Glantz PO, Kjellman O, et al. Остеоинтегрированные оральные имплантаты. Шведское многоцентровое исследование 8139последовательно установленные имплантаты Nobelpharma. J Пародонтол. 1988; 59: 287–96. [PubMed] [Google Scholar]
Albrektsson T, Dahl E, Enbom L, Engevall S, Engquist B, Eriksson AR, Feldmann G, Freiberg N, Glantz PO, Kjellman O, et al. Остеоинтегрированные оральные имплантаты. Шведское многоцентровое исследование 8139последовательно установленные имплантаты Nobelpharma. J Пародонтол. 1988; 59: 287–96. [PubMed] [Google Scholar]
164. Papaspyridakos P, Mokti M, Chen CJ, Benic GI, Gallucci GO, Chronopoulos V. Показатели выживаемости имплантатов и протезов с фиксированными на имплантатах полными зубными протезами на беззубой нижней челюсти по крайней мере через 5 лет: систематический обзор. Clin Implant Dent Relat Res. 2014;16:705–717. [PubMed] [Google Scholar]
165. Zwartele RE, Witjes S, Doets HC, Stijnen T, Poll RG. Тотальное бесцементное эндопротезирование тазобедренного сустава при ревматоидном артрите: систематический обзор литературы. Arch Orthop Trauma Surg. 2012; 132:535–46. [Бесплатная статья PMC] [PubMed] [Google Scholar]
166. Галло Дж., Раска М., Конттинен Ю.Т., Нич С. , Гудман С.Б. Сенсоры врожденного иммунитета, участвующие в патофизиологии заболеваний суставов: краткий обзор. Имплантаты J Long Term Eff Med. 2014; 24: 297–317. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Гудман С.Б. Сенсоры врожденного иммунитета, участвующие в патофизиологии заболеваний суставов: краткий обзор. Имплантаты J Long Term Eff Med. 2014; 24: 297–317. [Бесплатная статья PMC] [PubMed] [Google Scholar]
167. Gallo J, Vaculova J, Goodman SB, Konttinen YT, Thyssen JP. Вклад анализа тканей человека в понимание механизмов расшатывания и остеолиза при полной замене тазобедренного сустава. Акта Биоматер. 2014;10:2354–66. [Бесплатная статья PMC] [PubMed] [Google Scholar]
168. Паджаринен Дж., Ямсен Э., Конттинен Ю.Т., Гудман С.Б. Врожденные иммунные реакции при септическом и асептическом остеолизе вокруг тазобедренных имплантатов. Имплантаты J Long Term Eff Med. 2014; 24: 283–96. [Бесплатная статья PMC] [PubMed] [Google Scholar]
169. Zhang X, Morham SG, Langenbach R, Young DA, Xing L, Boyce BF, Puzas EJ, Rosier RN, O’Keefe RJ, Schwarz EM. Доказательства прямой роли циклооксигеназы 2 в остеолизе, вызванном износом имплантатов. Джей Боун Шахтер Рез. 2001; 16: 660–70. [PubMed] [Академия Google]
[PubMed] [Академия Google]
170. Чайлдс Л.М., Гоутер Дж.Дж., О’Киф Р.Дж., Шварц Э.М. Эффективность этанерцепта при остеолизе, вызванном износом. Джей Боун Шахтер Рез. 2001; 16: 338–47. [PubMed] [Google Scholar]
171. Gibon E, Ma T, Ren PG, Fritton K, Biswal S, Yao Z, Smith L, Goodman SB. Селективное ингибирование оси лиганд-рецептор MCP-1-CCR2 снижает системный перенос макрофагов в присутствии частиц сверхвысокомолекулярного полиэтилена. J Ортоп Res. 2012;30:547–53. [Бесплатная статья PMC] [PubMed] [Google Scholar]
172. Keeney M, Waters H, Barcay K, Jiang X, Yao Z, Pajarinen J, Egashira K, Goodman SB, Yang F. Доставка мутантного белка MCP-1 из послойное покрытие ортопедических имплантатов для модуляции воспалительной реакции. Биоматериалы. 2013; 34:10287–95. [Бесплатная статья PMC] [PubMed] [Google Scholar]
173. Lin TH, Sato T, Barcay KR, Waters H, Loi F, Zhang R, Pajarinen J, Egashira K, Yao Z, Goodman SB. Олигодезоксинуклеотид-приманка NF-kappaB усиливал остеогенез в мезенхимальных стволовых клетках, подвергшихся воздействию полиэтиленовой частицы. Tissue Eng Часть A. 2015; 21: 875–83. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Tissue Eng Часть A. 2015; 21: 875–83. [Бесплатная статья PMC] [PubMed] [Google Scholar]
174. Beane OS, Fonseca VC, Cooper LL, Koren G, Darling EM. Влияние старения на регенеративные свойства костномозговых, мышечных и жировых мезенхимальных стволовых/стромальных клеток. ПЛОС Один. 2014;9:e115963. [Бесплатная статья PMC] [PubMed] [Google Scholar]
175. Rao AJ, Nich C, Dhulipala LS, Gibon E, Valladares R, Zwingenberger S, Smith RL, Goodman SB. Локальный эффект доставки IL-4 на остеолиз, вызванный частицами полиэтилена, в своде черепа мышей. J Biomed Mater Res A. 2013; 101:1926–34. [Бесплатная статья PMC] [PubMed] [Google Scholar]
176. Pajarinen J, Kouri VP, Jamsen E, Li TF, Mandelin J, Konttinen YT. Реакция макрофагов на частицы титана определяется поляризацией макрофагов. Акта Биоматер. 2013;9: 9229–40. [PubMed] [Google Scholar]
177. Паджаринен Дж., Тамаки Ю., Антониос Дж. К., Лин Т. Х., Сато Т., Яо З., Такаги М., Конттинен Ю. Т., Гудман С. Б. Модуляция поляризации мышиных макрофагов in vitro с использованием доставки IL-4 осмотическими насосами.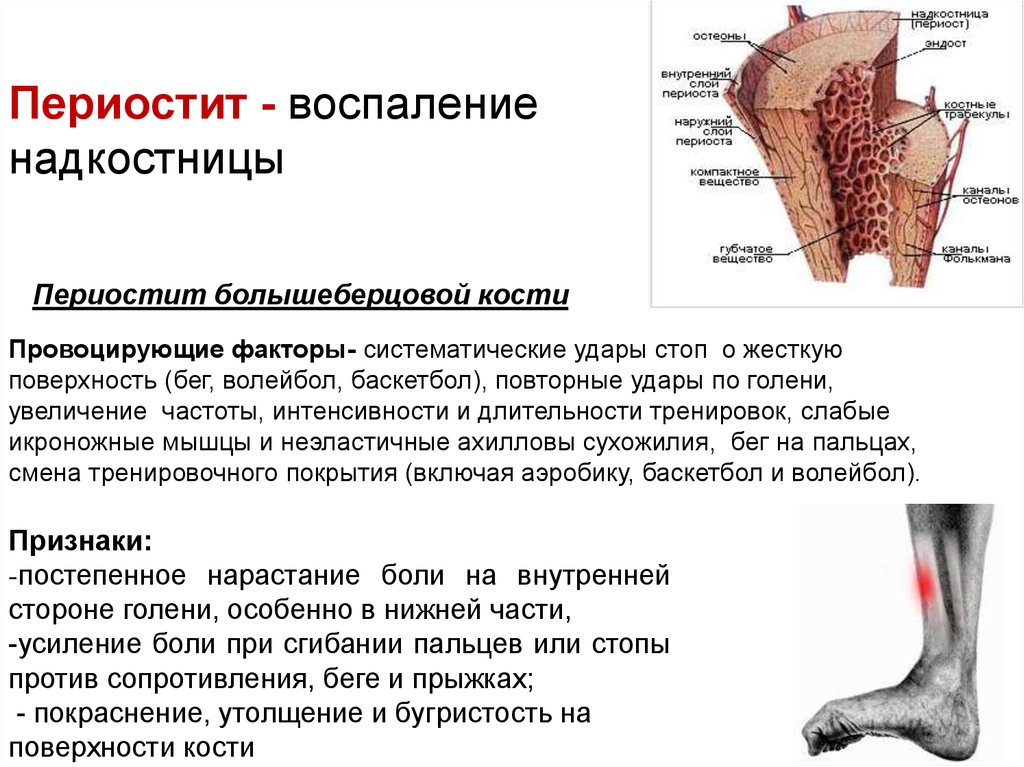 J Biomed Mater Res A. 2015;103:1339–45. [PMC free article] [PubMed] [Google Scholar]
J Biomed Mater Res A. 2015;103:1339–45. [PMC free article] [PubMed] [Google Scholar]
178. Pirris SM, Nottmeier EW, Kimes S, O’Brien M, Rahmathulla G. Ретроспективное исследование методов костной пластики гребня подвздошной кости с реконструкцией аллотрансплантатом: знают ли пациенты вообще какой гребень подвздошной кости был взят? Клиническая статья J Neurosurge Spine. 2014;21:595–600. [PubMed] [Google Scholar]
179. Grayson WL, Frohlich M, Yeager K, Bhumiratana S, Chan ME, Cannizzaro C, Wan LQ, Liu XS, Guo XE, Vunjak-Novakovic G. Разработка трансплантатов человеческой кости анатомической формы. Proc Natl Acad Sci U S A. 2010;107:3299–304. [Бесплатная статья PMC] [PubMed] [Google Scholar]
180. Jing W, Smith AA, Liu B, Li J, Hunter DJ, Dhamdhere G, Salmon B, Jiang J, Cheng D, Johnson CA, Chen S, Lee К., Сингх Г., Хелмс Дж.А. Реинжиниринг аутологичных костных трансплантатов с помощью активатора стволовых клеток WNT3A. Биоматериалы. 2015;47:29–40. [PubMed] [Google Scholar]
181. Kanczler JM, Oreffo RO. Остеогенез и ангиогенез: потенциал инженерии кости. Eur Cell Mater. 2008; 15:100–14. [PubMed] [Google Scholar]
Kanczler JM, Oreffo RO. Остеогенез и ангиогенез: потенциал инженерии кости. Eur Cell Mater. 2008; 15:100–14. [PubMed] [Google Scholar]
182. Wang M, Zhang G, Wang Y, Liu T, Zhang Y, An Y, Li Y. Взаимодействие мезенхимальных стволовых клеток и макрофагов способствует восстановлению сердечной мышцы. Int J Biochem Cell Biol. 2015;58:53–61. [PubMed] [Google Scholar]
183. Spiller KL, Anfang RR, Spiller KJ, Ng J, Nakazawa KR, Daulton JW, Vunjak-Novakovic G. Роль фенотипа макрофагов в васкуляризации каркасов тканевой инженерии. Биоматериалы. 2014; 35:4477–4488. [Бесплатная статья PMC] [PubMed] [Google Scholar]
184. Spiller KL, Vunjak-Novakovic G. Клинический перевод контролируемых систем доставки белков для тканевой инженерии. Препарат Делив Трансл Рез. 2015;5:101–15. [Бесплатная статья PMC] [PubMed] [Google Scholar]
185. Wernike E, Montjovent MO, Liu Y, Wismeijer D, Hunziker EB, Siebenrock KA, Hofstetter W, Klenke FM. VEGF, включенный в кальций-фосфатную керамику, способствует васкуляризации и формированию кости in vivo. Eur Cell Mater. 2010;19:30–40. [PubMed] [Академия Google]
Eur Cell Mater. 2010;19:30–40. [PubMed] [Академия Google]
186. Аро Х.Т., Говендер С., Патель А.Д., Эрнигу П., Перера де Грегорио А., Попеску Г.И., Голден Дж.Д., Кристенсен Дж., Валентин А. Рекомбинантный морфогенетический белок кости человека-2: рандомизированное исследование при открытых переломах большеберцовой кости, обработанных рассверленным фиксация ногтей. J Bone Joint Surg Am. 2011; 93:801–8. [PubMed] [Google Scholar]
187. Das A, Tanner S, Barker DA, Green D, Botchwey EA. Доставка препаратов, нацеленных на рецептор S1P, через биоразлагаемые полимерные каркасы усиливает регенерацию кости при черепном дефекте критического размера. J Biomed Mater Res A. 2014;102:1210–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
188. Каплан Дж.М., Юд М.Е., Лоди Т.А. Иммуномодулирующая активность мезенхимальных стволовых клеток. Curr Stem Cell Res Ther. 2011; 6: 297–316. [PubMed] [Google Scholar]
189. Микита Дж., Дюбурдье-Кассаньо Н., Делоар М.С., Векрис А. , Биран М., Раффард Г., Броше Б., Канрон М.Х., Франкони Дж.М., Буазио С., Петри К.Г. Измененные паттерны активации M1/M2 моноцитов в экспериментальной крысиной модели рассеянного склероза с тяжелым рецидивом. Улучшение клинического состояния при введении активированных М2 моноцитов. Мульт Склер. 2011;17:2–15. [PubMed] [Академия Google]
, Биран М., Раффард Г., Броше Б., Канрон М.Х., Франкони Дж.М., Буазио С., Петри К.Г. Измененные паттерны активации M1/M2 моноцитов в экспериментальной крысиной модели рассеянного склероза с тяжелым рецидивом. Улучшение клинического состояния при введении активированных М2 моноцитов. Мульт Склер. 2011;17:2–15. [PubMed] [Академия Google]
Периостальная реакция
<-Склеротические поражения костей | Обызвествления мягких тканей->
Надкостница представляет собой мембрану толщиной в несколько слоев клеток, которая покрывает почти всю кость. Практически единственными частями, не покрытыми этой мембраной, являются части, покрытые хрящом. Помимо того, что он покрывает кость и делится с костью частью своего кровоснабжения, он также производит кость, когда его стимулируют соответствующим образом. Что нужно, чтобы это произошло? Практически все, что ломается, рвется, растягивается, воспаляется или даже касается надкостницы. Таким образом, когда какой-то анонимный процесс стимулирует это реактивное образование костей, в конечном итоге мы видим доказательства этого в некоторых исследованиях изображений.
Когда мы обнаружим эту реактивную новую кость, что нам с ней делать? В лучшем случае можно было бы увидеть картину периостальной реакции и затем поставить точный гистологический диагноз. Увы, это не тот мир. Мы не можем поставить точный гистологический диагноз. Но подождите — будет еще хуже! Мы даже не можем точно сказать, является ли основной процесс доброкачественным или злокачественным! Как оказалось, все, что мы можем сделать, это с некоторой уверенностью сказать, является ли процесс доброкачественным или агрессивным. Почему это? Что ж, надкостница — довольно разношерстная ткань, и она одинаково реагирует на всех желающих. Основным фактором, определяющим внешний вид новообразования кости, является скорость роста аномального процесса, и он имеет мало общего с какими-либо внутренними свойствами надкостницы. Следовательно, любые различия в характере периостальной реакции должны возникать в самом патологическом процессе, а не в надкостнице. Опять же, свидетельство скорости, с которой растут эти процессы, является главным, на что мы обращаем внимание при оценке периостальной реакции. Знание этой скорости поможет нам разделить эти процессы на две большие категории.
Знание этой скорости поможет нам разделить эти процессы на две большие категории.
При медленно растущих процессах у надкостницы достаточно времени, чтобы отреагировать на процесс. То есть он может производить новую кость так же быстро, как растет поражение. Следовательно, можно было бы ожидать увидеть твердую, непрерывную периостальную новую кость вдоль края пораженной кости.
солидная периостальная реакция вдоль кортикального слоя кости
рисунок по Ragsdale, et al. 1981
Однако при быстро растущих процессах надкостница не может образовывать новую кость так же быстро, как растет поражение. Таким образом, вместо сплошного образования новой кости мы видим прерывистый рисунок. Этот прерывистый паттерн может проявляться по-разному, в зависимости от того, насколько неуклонно растет поражение. Если поражение растет неравномерно, скачкообразно, то надкостница может успеть образовать тонкую оболочку кальцифицированной новой кости до того, как поражение снова начнет расти во время следующего всплеска роста. Это может привести к образованию одной или нескольких концентрических оболочек новой кости над очагом поражения. Этот паттерн иногда называют пластинчатой или «луковистой» периостальной реакцией.
Это может привести к образованию одной или нескольких концентрических оболочек новой кости над очагом поражения. Этот паттерн иногда называют пластинчатой или «луковистой» периостальной реакцией.
пластинчатая периостальная реакция
рисунок по Ragsdale, et al. 1981
Если поражение растет быстро, но неуклонно, надкостница не успевает отложить даже тонкую костную оболочку, и картина может выглядеть совсем иначе . В таких случаях крошечные волокна, соединяющие надкостницу с костью (волокна Шарпея), вытягиваются перпендикулярно кости. Когда эти волокна окостеневают, они производят периостальную реакцию, иногда называемую «солнечными вспышками» или «волосами на концах», в зависимости от того, какая часть кости вовлечена в процесс.
«солнечные лучи» и «волосы на концах» периостальная реакция
рисунок по Ragsdale, et al. 1981
Остеосаркома дистального отдела бедренной кости, демонстрирующая плотное опухолевое образование кости и солнечные лучи периостальной реакции.
Другая модель, наблюдаемая в быстрорастущих процессах, называется треугольником Кодмана. Это немного неправильное название, так как на самом деле не существует полного треугольника. Когда процесс растет слишком быстро, чтобы надкостница могла отреагировать даже тонкими оболочками новой кости, иногда окостеневают только края приподнятой надкостницы. Когда эта небольшая часть окостенения видна на рентгенограмме по касательной, она образует небольшой угол с поверхностью кости, но не полный треугольник. Таким образом, когда процесс растет слишком быстро, чтобы даже волокна Шарпея могли окостенеть, можно увидеть только мягкотканную массу, отходящую от кости, возможно, с небольшими треугольниками Кодмана по краям.
треугольник Кодмана
фигура по Рэгсдейлу и др. 1981
Таааааак…… какое значение имеют все эти паттерны? Что ж, обычно мы можем разделить поражения на одну из двух категорий: доброкачественные и агрессивные процессы. Если мы видим твердую картину периостальной реакции, мы можем быть достаточно уверены, что имеем дело с доброкачественным процессом. Насколько уверенно? По моим оценкам, в обычной повседневной практике вы можете быть уверены в этом правиле примерно на 90–95 % (9).), но ваш пробег может отличаться. Как и со многими правилами в медицине, с использованием этого правила связаны некоторые предостережения. Основное предостережение с этим правилом заключается в том, что доброкачественные процессы и злокачественные процессы могут сосуществовать. Обычно это может проявляться, когда есть перелом или инфекция в той же области, что и опухоль. В этом случае вы можете увидеть довольно сложную картину периостальной реакции, которая демонстрирует некоторые элементы, которые выглядят доброкачественными, а некоторые — очень агрессивными.
Насколько уверенно? По моим оценкам, в обычной повседневной практике вы можете быть уверены в этом правиле примерно на 90–95 % (9).), но ваш пробег может отличаться. Как и со многими правилами в медицине, с использованием этого правила связаны некоторые предостережения. Основное предостережение с этим правилом заключается в том, что доброкачественные процессы и злокачественные процессы могут сосуществовать. Обычно это может проявляться, когда есть перелом или инфекция в той же области, что и опухоль. В этом случае вы можете увидеть довольно сложную картину периостальной реакции, которая демонстрирует некоторые элементы, которые выглядят доброкачественными, а некоторые — очень агрессивными.
сложный паттерн периостальной реакции
рисунок по Ragsdale, et al. 1981
Следует отметить, что подобные сложные паттерны могут вводить в заблуждение, и их следует интерпретировать с осторожностью. Однако в целом, чем агрессивнее характер периостальной реакции, тем выше вероятность того, что вы имеете дело со злокачественным новообразованием.
Вот неполный список причин солидной и агрессивной периостальной реакции:
Причины солидной периостальной реакции
- инфекция
- доброкачественные новообразования
- остеоид-остеома
- эозинофильная гранулема
- гипертрофическая легочная остеоартропатия
- тромбоз глубоких вен нижних конечностей
Причины агрессивной периостальной реакции
- остеомиелит
- злокачественные новообразования
- остеосаркома
- хондросаркома
- фибросаркома
- лимфома
- лейкемия
- метастазы
Ссылки
- Ragsdale BD, Madewell JE, Sweet DE. Рентгенологический и патологоанатомический анализ солитарных поражений костей. Часть II: Периостальные реакции. Radiol Clin N Am 1981;19:749-783.
Переломы костей — канал Better Health
Сломанная кость или перелом кости возникает, когда сила, воздействующая на кость, превышает силу, которую кость может выдержать. Это нарушает структуру и прочность кости и приводит к боли, потере функции, а иногда и к кровотечениям и травмам в области поражения.
Это нарушает структуру и прочность кости и приводит к боли, потере функции, а иногда и к кровотечениям и травмам в области поражения.
Наш скелет состоит из костей. Кости представляют собой тип соединительной ткани, укрепленной кальцием и костными клетками. Кости имеют более мягкий центр, называемый костным мозгом, где образуются клетки крови. Основными функциями нашего скелета являются поддержка нашего тела, обеспечение движения и защита наших внутренних органов.
Существуют различные типы переломов костей. Некоторые из них более серьезны, чем другие, в зависимости от силы и направления силы, конкретной пораженной кости, а также возраста и общего состояния здоровья человека. Общие переломы костей включают запястье, лодыжку и бедро. Переломы шейки бедра чаще всего случаются у пожилых людей.
Сломанные кости заживают от четырех до восьми недель, в зависимости от возраста и состояния здоровья человека и типа перелома.
Причины переломов костей
Причины переломов костей могут включать:
- Травматические происшествия, такие как спортивные травмы, автомобильные аварии и падения
- Такие состояния, как остеопороз и некоторые виды рака, которые вызывают более легкое незначительные травмы и падения могут стать серьезными.

Симптомы переломов костей
Переломы отличаются от других повреждений скелета, таких как вывихи, хотя в некоторых случаях их трудно отличить друг от друга. Иногда у человека может быть несколько видов травм. Если вы сомневаетесь, относитесь к травме как к перелому.
Симптомы перелома зависят от конкретной кости и тяжести травмы, но могут включать:
- Боль
- Отек
- Кровоподтеки
- Деформация
- Невозможность пользоваться конечностью.
Типы переломов костей
Различные типы переломов включают:
- Закрытый (простой) перелом – сломанная кость не пронзила кожу
- Открытый (сложный) перелом – сломанная кость выступает сквозь кожу, или рана ведет к месту перелома. Инфекция и внешнее кровотечение более вероятны
- Перелом зеленой ветки – небольшая тонкая трещина в кости. Это может произойти у детей, потому что их кости более гибкие, чем у взрослых
- Волосяной перелом – наиболее распространенной формой является стрессовый перелом, часто возникающий в стопе или голени в результате повторного стресса при таких действиях, как бег трусцой или бег
- Сложный перелом – повреждаются структуры, окружающие перелом.
 Могут быть повреждения вен, артерий или нервов, а также может быть повреждение выстилки кости (надкостницы)
Могут быть повреждения вен, артерий или нервов, а также может быть повреждение выстилки кости (надкостницы) - Оскольчатый перелом – кость раздроблена на мелкие осколки. Этот тип осложненного перелома срастается медленнее
- Отрывной перелом – мышцы прикрепляются к кости с помощью сухожилий, типа соединительной ткани. Мощные мышечные сокращения могут вырвать сухожилие и вырвать кусочки кости. Этот тип перелома чаще встречается в коленном и плечевом суставах.
- Компрессионный перелом – происходит при столкновении двух костей. Кости позвоночника, называемые позвонками, могут иметь такой тип перелома. Пожилые люди, особенно с остеопорозом, подвержены более высокому риску.
Не все переломы руки или ноги человека. Травма головы, грудной клетки, позвоночника или таза может привести к перелому костей, таких как череп и ребра. Эти переломы дополнительно осложняются основной структурой тела, которую обычно защищает кость. Некоторые из этих переломов может быть очень трудно лечить, используя только принципы оказания первой помощи, поскольку они могут представлять собой опасные для жизни травмы. Всегда обращайтесь за неотложной помощью, если вы подозреваете этот тип перелома.
Всегда обращайтесь за неотложной помощью, если вы подозреваете этот тип перелома.
Осложнения переломов костей
Другие проблемы, вызванные переломом кости, могут включать:
- Кровопотеря – кости имеют обильное кровоснабжение. Тяжелый перелом может привести к потере большого количества крови
- Травмы органов, тканей или окружающих структур – например, мозг может быть поврежден при переломе черепа. Органы грудной клетки могут быть повреждены при переломе ребра
- Задержка роста кости – если длинная кость ребенка ломается вблизи сустава, где находятся пластинки роста.
Первая помощь при переломах костей
Хорошая первая помощь при переломах всегда важна. Перемещение сломанных костей может усилить боль и кровотечение, а также повредить ткани вокруг травмы. Это может привести к осложнениям при восстановлении и заживлении травмы в дальнейшем.
Первая помощь при переломах заключается в иммобилизации (ограничении движения) поврежденного участка. Для этого можно использовать шпильки. Контролируйте любое внешнее кровотечение. Сложные переломы, при которых конечность сильно деформирована, могут нуждаться в повторном выравнивании перед шинированием — это должны делать только фельдшеры или медицинский персонал.
Для этого можно использовать шпильки. Контролируйте любое внешнее кровотечение. Сложные переломы, при которых конечность сильно деформирована, могут нуждаться в повторном выравнивании перед шинированием — это должны делать только фельдшеры или медицинский персонал.
Переломы головы или тела, такие как череп, ребра и таз, являются серьезными и должны лечиться парамедиками.
Если вы подозреваете перелом кости, вам следует:
- Удерживать пострадавшего неподвижно – не перемещать его, если нет непосредственной опасности, особенно если вы подозреваете перелом черепа, позвоночника, ребер, таза или бедра
- Сначала займитесь кровоточащими ранами. Остановите кровотечение, плотно прижав рану чистой повязкой. Если кость выступает, надавите на края раны
- Если кровотечение остановлено, накройте рану чистой повязкой
- Никогда не пытайтесь выпрямить сломанные кости
- При переломе конечности обеспечьте поддержку и комфорт, например подложите подушку под голень или предплечье.
 Однако не причиняйте дополнительной боли или ненужного движения сломанной кости
Однако не причиняйте дополнительной боли или ненужного движения сломанной кости - Наложите шину, чтобы поддержать конечность. Шины не обязательно должны быть изготовлены профессионалами. Такие предметы, как деревянные доски и сложенные журналы, могут помочь при некоторых переломах. Вы должны иммобилизовать конечность выше и ниже места перелома
- Используйте повязку для поддержки перелома руки или ключицы
- Приподнимите место перелома, если это возможно, и приложите холодный компресс, чтобы уменьшить отек и боль им потребуется операция
- В экстренных случаях звоните по номеру три нуля (000), чтобы вызвать скорую помощь.
Диагностика и лечение переломов костей
Врачи могут диагностировать переломы костей с помощью рентгена. Они также могут использовать КТ (компьютерную томографию) и МРТ (магнитно-резонансную томографию).
Сломанные кости срастаются сами по себе. Целью лечения является правильное расположение фрагментов кости. Кость должна полностью восстановиться в силе, движении и чувствительности. При некоторых сложных переломах может потребоваться хирургическое вмешательство или хирургическое вытяжение (или и то, и другое).
Кость должна полностью восстановиться в силе, движении и чувствительности. При некоторых сложных переломах может потребоваться хирургическое вмешательство или хирургическое вытяжение (или и то, и другое).
В зависимости от того, где находится перелом и насколько он серьезен, лечение может включать:
- Шины — для остановки движения сломанной конечности
- Брекеты — для поддержки кости
- Гипсовая повязка — для поддержки и иммобилизации кости
- Вытяжение – менее распространенный вариант
- Металлические стержни или пластины, вставленные хирургическим путем – для фиксации фрагментов кости вместе
- Обезболивающее.
Операция при переломах костей
Гипсовая повязка – один из наиболее распространенных способов иммобилизации конечности. Этот слепок сделан из препарата гипса, который затвердевает при добавлении воды. В зависимости от локализации и тяжести перелома операционные процедуры могут включать:
- Закрытые или простые переломы – два конца сломанной кости совмещаются и удерживаются на месте.
 Конечность тщательно бинтуют, затем накладывают влажный пластырь. Иногда, после высыхания гипса, гипс разделяется на две части, и обе половины повторно перевязываются снаружи. Это позволяет избежать любого отека, который может возникнуть
Конечность тщательно бинтуют, затем накладывают влажный пластырь. Иногда, после высыхания гипса, гипс разделяется на две части, и обе половины повторно перевязываются снаружи. Это позволяет избежать любого отека, который может возникнуть - Открытые или сложные переломы – они тщательно очищаются в операционной для удаления осколков перед установкой, потому что сломанная кость, подвергшаяся воздействию открытого воздуха, может инфицироваться
- Длинные кости – длинные кости, такие как бедренная кость, трудно выровнять. У взрослых их часто лечат внутренним гвоздем. Ребенку может потребоваться вытяжение в течение нескольких дней, прежде чем наложить гипс на кость. Как только два конца кости начинают проявлять признаки заживления, ногу и тазобедренный сустав иммобилизуют в гипсе. В других случаях штифты вставляются выше и ниже перелома и закрепляются на внешней раме или «фиксаторе». Это делается под общим наркозом.
Сразу после операции по поводу перелома кости
После операции врач проверит, есть ли у вас полное ощущение в этой области. Например, если у вас сломана рука в гипсе, вас могут попросить пошевелить пальцами. Они также проверят вашу конечность на покалывание, бледность (бледный цвет) или прохладу. Эти тесты проверяют, влияет ли шина на нервы и кровоснабжение вашей конечности. Поврежденную часть держат как можно неподвижнее в первые несколько дней.
Например, если у вас сломана рука в гипсе, вас могут попросить пошевелить пальцами. Они также проверят вашу конечность на покалывание, бледность (бледный цвет) или прохладу. Эти тесты проверяют, влияет ли шина на нервы и кровоснабжение вашей конечности. Поврежденную часть держат как можно неподвижнее в первые несколько дней.
Медсестры предложат вам обезболивающее. Они определят разницу между болью при переломе и любой болью, которая может быть вызвана шиной, тракцией, гипсовой повязкой, неправильным положением конечности или отеком конечности.
Процесс заживления переломов костей
Сгустки крови, которые образуются на концах сломанных костей, являются началом процесса заживления. В течение примерно пяти недель тело соединяет две части кости вместе с комбинацией волокнистых клеток и хрящей.
Эта временная кость (мозоль) не такая прочная, как настоящая кость. Он может легко сломаться, пока его медленно не заменит настоящая кость. По этой причине врач может снять гипсовую повязку или шину через несколько недель, но вам все равно необходимо бережно относиться к кости в течение как минимум еще одного месяца.
Другие методы лечения переломов костей
Некоторые кости, такие как ключица или кости пальцев ног, иммобилизуют с помощью повязки или шины (вместо гипса) и дают им отдохнуть в течение примерно двух месяцев.
Осложнения переломов костей
Возможные осложнения переломов костей могут включать:
- Неправильное положение конечности
- Инфекция
- Неправильно подобранная гипсовая повязка (например, слишком тугая или слишком свободная).
Самопомощь после перелома кости
Следуйте советам врача, но общие рекомендации включают:
- До тех пор, пока гипсовая повязка не схватится должным образом, избегайте прямого нагревания, например, грелки.
- Максимально дайте конечности покой.
- Используйте приемы, показанные вам медсестрами, для ходьбы или управления повседневными делами. Например, вы рискуете получить дополнительную травму, если неправильно используете костыли.
- Избегайте подъема или вождения автомобиля до заживления перелома.

- Если кожа под гипсовой повязкой зудит, не просовывайте ничего между гипсовой повязкой и конечностью (например, вешалкой или карандашом). Вместо этого используйте фен, чтобы надуть холодный воздух на гипс.
- Не мочите гипс, так как влажный гипс становится мягким и не обеспечивает необходимой поддержки. Влажный пластырь также может раздражать кожу. Принимая душ, заверните повязку в полиэтиленовый пакет и приклейте ее непосредственно к коже, чтобы обеспечить водонепроницаемость.
- Немедленно обратитесь к врачу, если у вас отек, посинение или потеря подвижности пальцев рук или ног, покалывание, онемение или усиление боли.
Долгосрочная перспектива после перелома кости
В большинстве случаев гипс снимают через несколько недель, но вы должны обращаться с конечностью с осторожностью по крайней мере в течение следующего месяца или около того. Переломы ног заживают несколько месяцев. Более слабая временная кость (мозоль) все еще заменяется настоящей костью и может быть легко повреждена.
Ваш врач может сделать дополнительные рентгеновские снимки, чтобы проверить процесс заживления кости.
В отличие от кожи, сломанные кости заживают без образования рубцовой ткани. Но обездвиженные мышцы имеют свойство ослабевать и увядать. Вам может понадобиться реабилитация, в том числе укрепляющие упражнения, на короткое время.
Где получить помощь
- Ваш врач
- Отделение неотложной помощи больницы
- В экстренных случаях всегда звоните три нуля (000)
Что следует помнить
- Перелом – это перелом или трещина в кости.
- Перелом происходит, когда сила, воздействующая на кость, превышает силу, которую кость может выдержать структурно.
- Наиболее распространенными местами переломов костей являются запястье, лодыжка и бедро.
- Лечение включает иммобилизацию кости гипсовой повязкой или хирургическое введение металлических стержней или пластин для удержания фрагментов кости вместе.



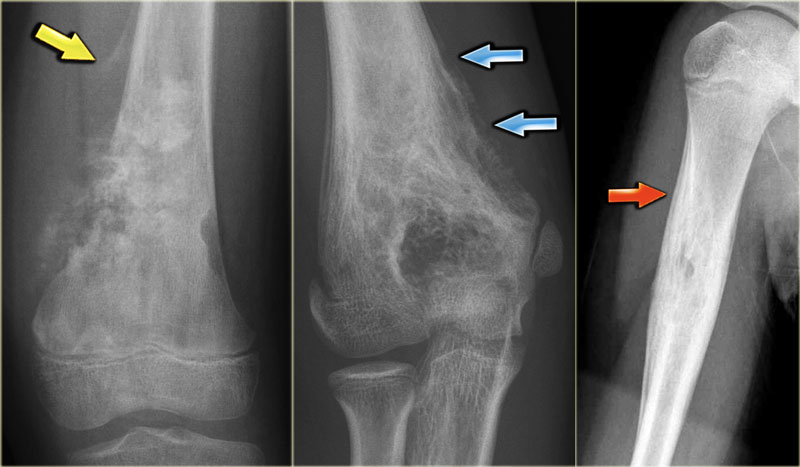

 На ранних стадиях проблема с надкостницей может решиться простым отдыхом. Исключите ударную нагрузку на ноги, чтобы поврежденные ткани успели восстановиться. Если нет возможности полностью прекратить занятия — тренируйтесь без ударной нагрузки на ноги. Перейдите на более щадящий режим: замените бег на плавание или велосипед.
На ранних стадиях проблема с надкостницей может решиться простым отдыхом. Исключите ударную нагрузку на ноги, чтобы поврежденные ткани успели восстановиться. Если нет возможности полностью прекратить занятия — тренируйтесь без ударной нагрузки на ноги. Перейдите на более щадящий режим: замените бег на плавание или велосипед.